文档内容
2011 年福建省中考化学真题及答案
(满分:100分;考试时间:60分钟)
友情提示:请把所有答案填写(涂)到答题卡上!请不要错位、越界答题!
相对原子质量:H—1C—12O—16Fe—56
部分碱和盐的溶解性表(室温)
OH- NO- Cl- SO2- CO2-
3 4 3
NH+ 溶、挥 溶 溶 溶 溶
4
K+ 溶 溶 溶 溶 溶
Na+ 溶 溶 溶 溶 溶
Ba2+ 溶 溶 溶 不 不
Ca2+ 微 溶 溶 微 不
Mg2+ 不 溶 溶 溶 微
Al3+ 不 溶 溶 溶 —
Cu2+ 不 溶 溶 溶 —
一、选择题(本题共30分)
每小题的四个选项中只有一项符合题目要求,请在答题卡填涂此项的字母。
1.下列物质属于单质的是
A.S B.PO C.NaHCO D.CO(NH)
2 5 3 2 2
2.下列物质充分混合后能形成溶液的是
3.化学反应前后可能发生改变的是
A.分子的数目 B.原子的数目 C.物质的总质量 D.元素的种类
4.中国环保网5月6日报道,我省今年第一季度23个城市中有18个出现酸雨,其中一个城
市雨水的pH达到3.58,你认为导致酸雨的原因可能是
A.乱扔垃圾 B.使用含磷洗衣粉
C.生活污水的任意排放 D.煤燃烧产生的气体
5.下列没有发生化学变化的是
A.雕像受腐蚀 B.铜插入硝酸银溶液后 C.镁条燃烧 D.水流过沙砾池
6.下列说法错误的是
A.氧气具有可燃性 B.活性炭有强吸附性
C.氢氧化钠有强烈的腐蚀性 D.水果、蔬菜富含人体所需的维生素
7.粗盐提纯中,蒸发时不需要用到的仪器是8.下列化学反应属于置换反应的是
A.2HO 2H↑+O↑ B.Zn+HSO ═ZnSO+H↑
2 2 2 2 4 4 2
C.KOH+HCl═KCl+HO D.CO+Ca(OH)═HO+CaCO↓
2 2 2 2 3
9.下列操作正确的是
A.胶头滴管的使用 B.试管夹套入试管 C.熄灭酒精灯 D.液体药品的取用
10.下列混合液中滴入Ba(OH)2溶液,立即产生白色沉淀的是
A.Mg(NO ) HCl NaCl B.CuCl NHNO KCl
3 2 2 4 3
C.AlCl HNO CaCl D.NaCO KOH NaNO
3 3 2 2 3 3
二、填空与简答(本题共36分)
11.按要求填空:
(1)下列是某同学书写的错误化学式,请加以改正。
锰(MN)改为 ;硫酸钾(KSO)改为 。
4
(2)用化学符号表示:2个水分子 ;甲烷 。
12.今年5月1日起,我国提出“在室内公共场所禁止吸烟”,相应场所
应该张贴右图的 标志,香烟的烟气中含有 等几百种有毒
物质(只要求填写一种物质)。
13.请从“a熟石灰b食盐c石墨d酚酞溶液e石蕊溶液”中选择合适的物质填空。
(1)常用于改良酸性土壤的物质是 ;(2)可以作润滑剂的物质是 ;
(3)可用于腌渍鱼、蔬菜等食品的物质是 ;(4)碱性溶液能使 显红色。
14.右图火三角中还缺少的燃烧条件是 ;在实验室里如果洒落
的 酒 精 ( CHOH ) 在 桌 面 上 燃 烧 起 来 , 可 以 用
2 5
灭 火 。 请 你 写 出 酒 精 燃 烧 的 化 学 方 程 式
。
15.2011年3月11日,日本福岛第一核电站因地震发生核泄漏。
(1)核泄漏中含有碘—131粒子,其原子结构示意图如右图所示,该
原子的核电荷数为 ,电子层数为 层;碘属于
元素(填“金属”或“非金属”)。(2)核电站机组冷却产生的核污水从裂缝渗入海里,
东电公司采用“水玻璃”封住渗漏层,“水玻璃”的
主要成分是硅酸钠(Na2SiO3)。
①硅酸钠中硅元素的化合价是 价。②二氧化硅
与氢氧化钠反应生成硅酸钠和水,请写出该反应的化
学方程式 ,其反应原理与初中学
过的 和氢氧化钠反应相似。
三、实验与探究(本题共24分)
16.回答下列问题:
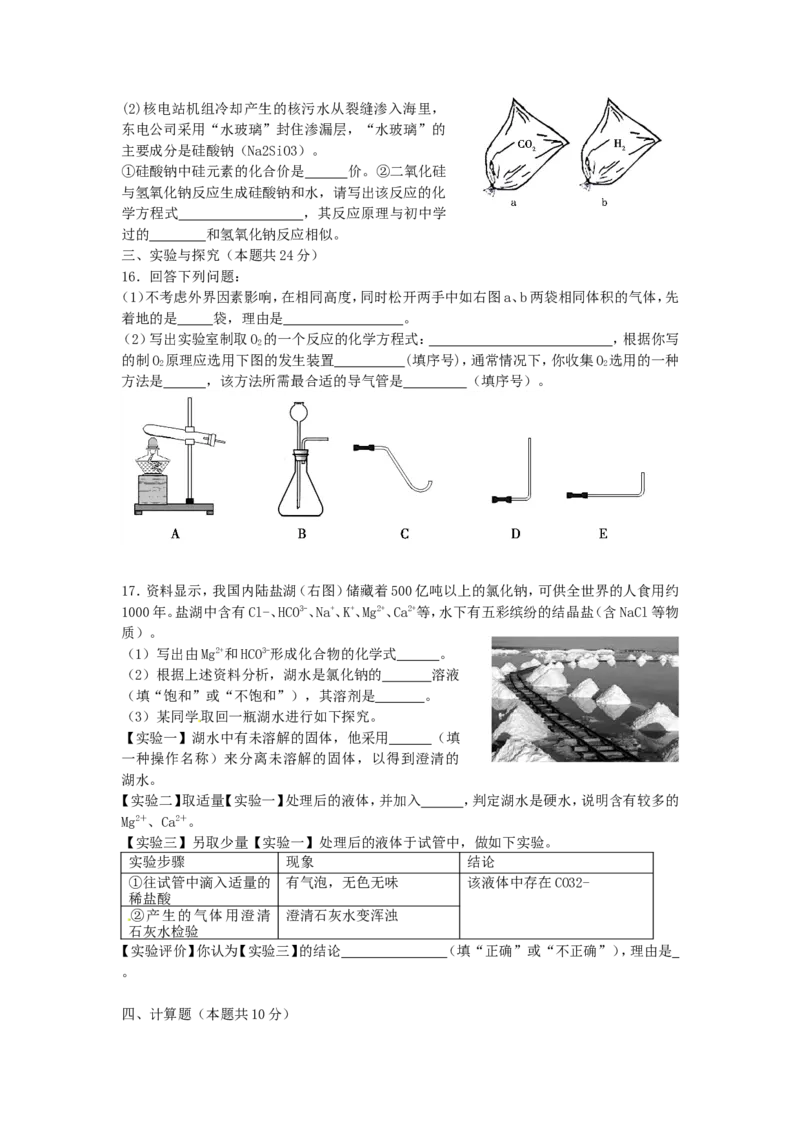
(1)不考虑外界因素影响,在相同高度,同时松开两手中如右图a、b两袋相同体积的气体,先
着地的是 袋,理由是 。
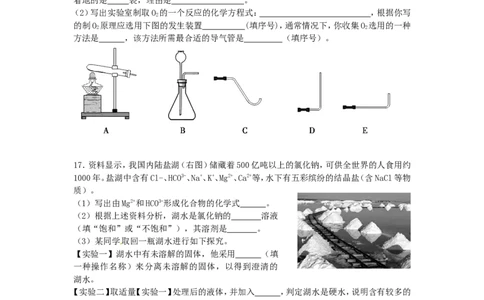
(2)写出实验室制取O 的一个反应的化学方程式: ,根据你写
2
的制O 原理应选用下图的发生装置 (填序号),通常情况下,你收集O 选用的一种
2 2
方法是 ,该方法所需最合适的导气管是 (填序号)。
17.资料显示,我国内陆盐湖(右图)储藏着500亿吨以上的氯化钠,可供全世界的人食用约
1000年。盐湖中含有Cl-、HCO3-、Na+、K+、Mg2+、Ca2+等,水下有五彩缤纷的结晶盐(含NaCl等物
质)。
(1)写出由Mg2+和HCO3-形成化合物的化学式 。
(2)根据上述资料分析,湖水是氯化钠的 溶液
(填“饱和”或“不饱和”),其溶剂是 。
(3)某同学取回一瓶湖水进行如下探究。
【实验一】湖水中有未溶解的固体,他采用 (填
一种操作名称)来分离未溶解的固体,以得到澄清的
湖水。
【实验二】取适量【实验一】处理后的液体,并加入 ,判定湖水是硬水,说明含有较多的
Mg2+、Ca2+。
【实验三】另取少量【实验一】处理后的液体于试管中,做如下实验。
实验步骤 现象 结论
①往试管中滴入适量的 有气泡,无色无味 该液体中存在CO32-
稀盐酸
②产生的气体用澄清 澄清石灰水变浑浊
石灰水检验
【实验评价】你认为【实验三】的结论 (填“正确”或“不正确”),理由是
。
四、计算题(本题共10分)18.某炼铁厂在高温条件下利用一氧化碳还原赤铁矿(主要成分是FeO)。现有100t的赤铁
2 3
矿,理论上可炼得纯铁56t。(反应的化学方程式:3CO+FeO 2Fe+3CO)
2 3 2
计算:
(1)CO中碳元素和氧元素的质量比 ;
(2)求赤铁矿中FeO 的质量分数。
2 3参考答案
总说明:
1.本答案供评卷时参考,若出现其它合理答案,请参照评分标准给分。
2.书写化学方程式时,化学式写错不给分;化学式正确但其它出现错误(包括未配平、未注明
反应条件、未标出或标错“↑”、“↓”)的扣1分。
3.化学专用名词中出现错别字的扣1分,元素符号错误的不得分。
4.凡试题中未指明写物质的名称或化学式的,只要正确均给分。
一、选择题(本题共30分,每小题3分)
题目 1 2 3 4 5 6 7 8 9 10
答案 A B A D D A C B C D
二.填空与简答(本题共36分,每个化学方程式3分)
11.(共8分,每空2分)(1)Mn ;KSO(2)2HO ;CH
2 4 2 4
12.(共4分,每空2分)B ;一氧化碳(其他合理答案均可得分)
13.(共8分,每空2分)(1)a(2)c(3) b(4)d (填写物质的名称也可得分)
14.(共7分,化学方程式3分,其余每空2分)可燃物与空气(或氧气)接触;湿抹布(水除外,
其他合理答案均可给分);CHOH + 3O 2CO + 3HO
2 5 2 2 2
15.(共9分)(1)53; 5 ;非金属 (每空1分,共3分)
(2)①+4②SiO + 2NaOH═NaSiO + HO ;二氧化碳 (其他合理答案也可得分 )
2 2 3 2
【第1空1分,最后1空2分,共6分】
三、实验与探究(本题共24分)
16.(共12分)
(1)a;二氧化碳(或CO)的密度比氢气(或空气)大 (第1空1分,共3分)
2
(2)2HO 2HO+O↑(或2KMnO KMnO + MnO + O↑或
2 2 2 2 4 2 4 2 2
2KClO 2KCl +3O↑);B(或A);排水法(或向上排空气法);C(或D)
3 2
【化学方程式3分,其余每空2分,第1空与第2空、第3空与第4空对应才可得分,共9分】
17.(共12分,最后两空各1分,其余每空2分)
(1)Mg(HCO ) (2)饱和 ;水
3 2
(3)过滤 ;肥皂水搅拌,不起泡(或起泡较少) ;不正确 ;Mg2+、Ca2+不能与CO2―同时存在水
3
溶液中
四、计算题(本题共10分)
18.(1)3∶4 (或12∶16)(2分)
(2)解:设100t赤铁矿中含FeO 的质量为X
2 3
3CO + FeO 2Fe + 3CO
2 3 2
160 2×56
X 56t ……………(2分)
……………(2分)X=80t ……………(2分)
赤铁矿中Fe2O3的质量分数为: ……………(2分)
答:赤铁矿中Fe2O3 的质量分数是80%。
(说明:若计算过程中不带单位扣1分)