文档内容
2008年全国普通高等学校招生统一考试
上海化学试卷解析
1..(08上海卷)食品检验是保证食品安全的重要措施,下列不属于食品安全检测指标的
是( )
A.淀粉的含量 B.二氧化硫的含量
C.亚硝酸盐的含量 D.甲醛的含量
解析:选项B、C、D都是有毒物质,是食品安全检测的指标。
答案:A
2..(08上海卷)化学科学需要借助化学专用语言来描述,下列有关化学用语正确的是(
)
O C O
解析:CO的中的C最外层上只有4个电子正确的电子式为: 。
2
答案:B
3..(08上海卷)植物及其废弃物可以制取乙醇燃料,下列关于乙醇燃料的说法错误的是
( )
A.它是一种再生能源 B.乙醇易燃烧,污染小
C.乙醇只能在实验室内作燃料 D.粮食作物是制乙醇的重要原料
解析:乙醇不仅在实验室内可作燃料,而且还可作还可作内燃机等的燃料。
答案:C
4..(08上海卷)下列化学式既能表示物质的组成,又能表示物质的一个分子的是(
)
A.NaOH B.SiO C.Fe D.CH
2 3 8
解析:NaOH是离子晶体,SiO是原子晶体,Fe为金属晶体,它们均只表示物质的组成,不
2
能表示物质的一个分子。
答案:D
5..(08上海卷)下列关于化学学习和研究的说法错误的是( )
A.化学模型有助于解释一些化学现象
B.质量守恒定律是大量实验事实的总结
C.化学家提出的假设都能被实验证实
D.化学基本原理的应用是有一定条件的
解析:化学家提出的假设只要是正确的,随着科学的发展可能被实验证实,也可能不能证
实。
答案:C
6..(08上海卷)下列物质中,只有氧化性、只有还原性,既有氧化性又有还原性的顺序
排列的一组是( )
A.F、K、HCl B.Cl、Al、H C.NO、Na、Br D.O、SO、HO
2 2 2 2 2 2 2 2
解析:元素具有最高价时只有氧化性,注意F没有最高化合价,元素具有最低化合价时只
2
第1页 | 共14页有还原性,而处于中间价态时既具有氧化性又具有还原性。
答案:A
7..(08上海卷)下列各化合物的命名中正确的是( )
解析:选项A应命名为1、3-丁二烯;选项B应命名为2-丁醇;选项C应命名为邻甲基苯酚
。
答案:D
8..(08上海卷)在一定的条件下,完全分解下列某化合物2g,产生氧气1.6g,此化合物
是( )
解析:此题主要考查摩尔质量。选项A中m(16
2g 2g
O)= ×16g·mol-1=1.78g;选项B中m(16O)= ×16g·mol-1=1.
2 18g·mol-1 2 20g·mol-1
2g
6g;选项中m(18O)= ×18g·mol-1=1.8g;选项中m(18O)=2g/22g·mol-1×
2 20g·mol-1 2
18g·mol-1=1.64g。
答案:B
9..(08上海卷)设N为阿伏加德罗常数,下列说法正确的是( )
A
A.23gNa在氧气中完全燃烧失电子数为0.5N
A
B.1L2mol·L-1的MgCl溶液中含Mg2+数为2N
2 A
C.标准状况下,11.2LSO所含分子数为0.5N
3 A
D.室温下,8g甲烷含有共价键数为2N
A
解析:选项A中n(Na)=1mol,转移的电子数为N;选项B中n(MgCl)=2mol,但Mg2+部分水
A 2
解,所
以溶液中含Mg2+数小于2N;选项C中SO在标准状况下为液体。
A 3
答案:D
10..(08上海卷)由图的装置中,干燥烧瓶内盛有某种气体,烧杯和滴定管内盛放某种液
体。挤压滴管的胶头,下列
与实验事实不相符的是( )
A.CO(NaHCO溶液)/无色喷泉 B.NH(HO含酚酞)/红色喷泉
2 3 3 2
C.HS(CuSO溶液)/黑色喷泉 D.HCl(AgNO溶液)/白色喷泉
2 4 3
解析:选项A中NaHCO与CO不反应,烧瓶内的压强不变,不能形成喷泉;选项B中NH易溶于
3 2 3
水,形成NH·HO,NH·HO NH+OH-,溶液呈碱性,嫩形成红色喷泉;选项C中
3 2 3 2 4
HS+CuSO===HSO+CuS↓,CuS为黑色沉淀,能形成黑色喷泉;选项D中HCl+AgNO==
2 4 2 4 3
=HNO+AgCl↓,AgCl为白色沉淀,能形成白色喷泉。
3
答案:A
11..(08上海卷)常温下,某溶液中由水电离出来的c(H+)=1.0×10-
13mol·L-1,该溶液可能是( )
①二氧化硫 ②氯化铵水溶液 ③硝酸钠水溶液 ④氢氧化钠水溶液
A.①④ B.①② C.②③ D.③④
解析:某溶液中由水电离出来的c(H+)=1.0×10-
第2页 | 共14页13mol·L-1,说明溶液既可能呈酸性,也有可能呈碱性。①SO+HO HSO,HSO
2 2 2 3 2 3
HSO-+H+,HSO-
3 3
SO2-+H+,溶液呈酸性;④NaOH===Na++OH-,溶液呈碱性。
3
答案:A
12..(08上海卷)取一张用饱和的NaCl溶液浸湿的pH试纸,两根铅笔芯作电极,接通直流
电源,一段时间
后,发现a电极与试纸接触处出现一个双色同心圆,内圈为白色,外圈呈浅红色。则下
列
说法错误的是( )
A.b电极是阴极 B.a电极与电源的正极相连
C.电解过程中水是氧化剂 D.b电极附近溶液的pH变小
解析:a电极与试纸接触处出现一个双色同心圆,内圈为白色,外圈呈浅红色,说明a极负
极产生了Cl,所以a极与电源的正极相连,即a为阳极,电极反应式为:2Cl--2e-
2
===Cl↑,b为阴极,2HO-4e- ===H↑+2OH-,所以b极附近的pH增大。
2 2 2
答案:D
13..(08上海卷)已知在热的碱性溶液中,NaClO发生如下反应:3NaClO 2NaCl+Na
ClO。在相同条件下NaClO也能发生类似的反应,其最终产物是( )
3 2
A.NaCl、NaClO B.NaCl、NaClO C.NaClO、NaClO D.NaClO、NaClO
3 3 3 4
解析:在已知反应中氯元素的化合价:+1→+5和+1→-1,既然NaClO也有类似的反应
2
,即氯元素的化合价既有升高,也有降低,选项A中均降低;选项B、C与题意相符;
选项D化合价均升高,但选项C中NaClO不是最终产物。
答案:B
14..(08上海卷)某酸性溶液中只有Na+、CHCOO-、H+、OH-四种离子。则下列描述正确
3
的是( )
A.该溶液由pH=3的CHCOOH与pH=11的NaOH溶液等体积混合而成
3
B.该溶液由等物质的量浓度、等体积的NaOH溶液和CHCOOH溶液混合而成
3
C.加入适量的NaOH,溶液中离子浓度为c(CHCOO-)>c(Na+)>c(OH-)>c(H+)
3
D.加入适量氨水,c(CHCOO-)一定大于c(Na+)、c(NH+)之和
3 4
解析:此题的关键应注意题中的“酸性”两个字,选项B溶液NaOH与CHCOOH恰好完全反应
3
,所以溶液呈碱性;选项C中当加入NaOH后溶液仍然呈酸性,则c(H+)>c(OH-),不
成立,当恰好完全反应,溶液呈碱性,则c(Na+)>C(CHCOO-),当碱过量时,必定c
3
(Na+)>C(CHCOO-),所以在任何情况下溶液的离子关系都不能成立;选项D中加入
3
氨水,由电荷守恒得:c(CHCOO-)+c(OH-)=c(Na+)+c(NH+)+c(H+),当溶液仍呈
3 4
酸性即c(OH-)<c(H+),则c(CHCOO-)>c(NH+)+c(Na+);当溶液呈中性时,c(H+)
3 4
=c(OH-),则c(CHCOO-)=c(NH+)+c(Na+);当溶液呈碱性时,c(H+)<c(OH-),
3 4
则c(CHCOO-)<c(NH+)+c(Na+),所以c(CHCOO-)一不定大于c(Na+)、c(NH+)之和
3 4 3 4
。
答案:A
15..(08上海卷)已知气体的摩尔质量越小,扩散速度越快。右图所示为气体扩散速度的
实验,两种气体扩散相遇时形成白色烟环。下列关于甲、乙的判断正
确的是( )
A.甲是浓氨水,乙是浓硫酸
B.甲是浓盐酸,乙是浓氨水
第3页 | 共14页C.甲是浓氨水,乙是浓盐酸 D.甲是浓硝酸,乙是浓氨水
解析:根据题意NH的摩尔质量小于HCl和HNO,所以NH应甲处产生,HCl和HNO气体应在乙
3 3 3 3
处产生。
答案:C
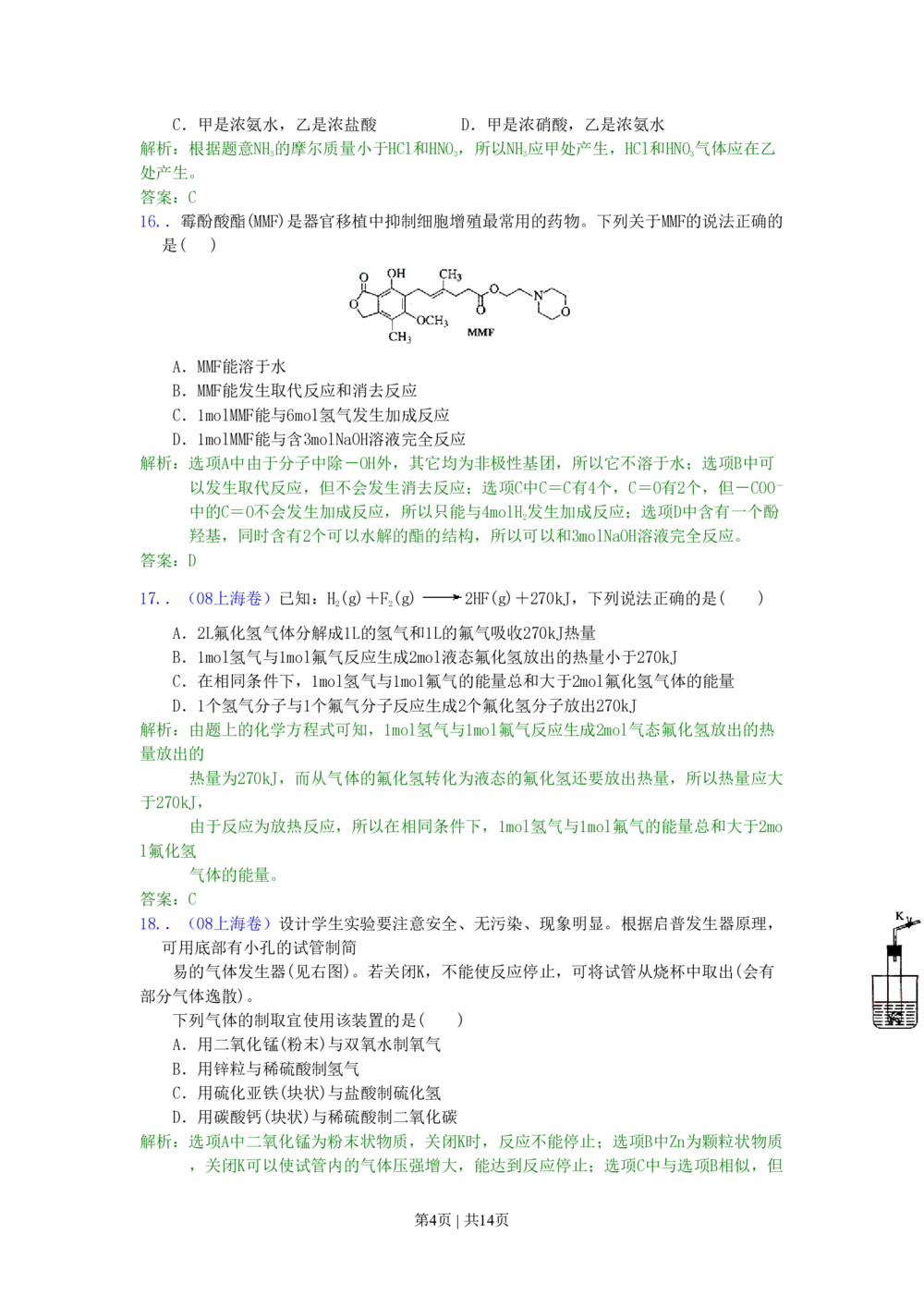
16..霉酚酸酯(MMF)是器官移植中抑制细胞增殖最常用的药物。下列关于MMF的说法正确的
是( )
A.MMF能溶于水
B.MMF能发生取代反应和消去反应
C.1molMMF能与6mol氢气发生加成反应
D.1molMMF能与含3molNaOH溶液完全反应
解析:选项A中由于分子中除-OH外,其它均为非极性基团,所以它不溶于水;选项B中可
以发生取代反应,但不会发生消去反应;选项C中C=C有4个,C=O有2个,但-COO-
中的C=O不会发生加成反应,所以只能与4molH发生加成反应;选项D中含有一个酚
2
羟基,同时含有2个可以水解的酯的结构,所以可以和3molNaOH溶液完全反应。
答案:D
17..(08上海卷)已知:H(g)+F(g) 2HF(g)+270kJ,下列说法正确的是( )
2 2
A.2L氟化氢气体分解成1L的氢气和1L的氟气吸收270kJ热量
B.1mol氢气与1mol氟气反应生成2mol液态氟化氢放出的热量小于270kJ
C.在相同条件下,1mol氢气与1mol氟气的能量总和大于2mol氟化氢气体的能量
D.1个氢气分子与1个氟气分子反应生成2个氟化氢分子放出270kJ
解析:由题上的化学方程式可知,1mol氢气与1mol氟气反应生成2mol气态氟化氢放出的热
量放出的
热量为270kJ,而从气体的氟化氢转化为液态的氟化氢还要放出热量,所以热量应大
于270kJ,
由于反应为放热反应,所以在相同条件下,1mol氢气与1mol氟气的能量总和大于2mo
l氟化氢
气体的能量。
答案:C
18..(08上海卷)设计学生实验要注意安全、无污染、现象明显。根据启普发生器原理,
可用底部有小孔的试管制简
易的气体发生器(见右图)。若关闭K,不能使反应停止,可将试管从烧杯中取出(会有
部分气体逸散)。
下列气体的制取宜使用该装置的是( )
A.用二氧化锰(粉末)与双氧水制氧气
B.用锌粒与稀硫酸制氢气
C.用硫化亚铁(块状)与盐酸制硫化氢
D.用碳酸钙(块状)与稀硫酸制二氧化碳
解析:选项A中二氧化锰为粉末状物质,关闭K时,反应不能停止;选项B中Zn为颗粒状物质
,关闭K可以使试管内的气体压强增大,能达到反应停止;选项C中与选项B相似,但
第4页 | 共14页HS有毒,对空气造成污染;选项D中CaCO与HSO反应生成CaSO,由于CaSO微溶于
2 3 2 4 4 4
水,附在CaCO表面,使反应停止,达不到制取CO的目的。
3 2
答案:B
19..(08上海卷)研究发现,空气中少量的NO能参与硫酸型酸雨的形成,反应过程如下
2
:
①SO+NO SO+NO ②SO+HO HSO ③2NO+O 2NO
2 2 5 3 3 2 2 4 2 2
NO在上述过程中的作用,与HSO在下述变化中的作用相似的是( )
2 2 4
A.潮湿的氯气通过盛有浓HSO的洗气瓶B.硫化氢通入浓HSO
2 4 2 4
C.浓HSO滴入萤石中,加热
2 4
D.加入少量的HSO使乙酸乙酯水解
2 4
解析:在反应①中NO起氧化剂的作用,从反应①、③看NO起催化作用,选项A中浓硫酸起
2 2
吸水剂的作用;选项B中浓硫酸起氧化剂作用;选项C中浓硫酸起酸性作用;选项D中
浓硫酸起催化剂作用。
答案:B、D
20..(08上海卷)下列离子方程式书写正确的是( )
A.AgNO溶液滴入少量的NaS溶液 2Ag++S2- AgS↓
3 2 2
B.过量的CO通入Ca(ClO)溶液中 ClO-+CO+HO HCO-+HClO
2 2 2 2 3
C.向NaCO溶液中加入过量CHCOOH溶液 CO2-+2H+ CO↑+HO
2 3 3 3 2 2
D.向Ba(OH)溶液中加入少量的NaHSO溶液 2HSO-+Ba2++2OH-
2 3 3
BaSO↓+SO2-+2HO
3 3 2
解析:选项C中CHCOOH为弱酸,在离子方程式中不能改写;选项D中一个NaHSO中只含有一
3 3
个HSO-,所以离子方程式中为:HSO-+Ba2++OH-===BaSO↓+HO。
3 3 3 2
答案:A、B
21..(08上海卷)等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时
间t产生气体体积V的数据,根据数据绘制得到图1,则曲线a、b、c、d所对应的实验组
别可能是( )
A.4-3-2-1 B.1-2-3-4 C.3-4-2-1 D.1-2-4-3
解析:化学反应速率与温度、浓度和固体物质的表面积的大小有关,实验1的盐酸的浓度最
小,反应的温度最低,所以化学反应速率最慢;由于实验3的反应温度比实验2的反
应温度高,所以反应速率实验3大于实验2;而实验4和实验3虽然浓度相同,但反应
的温度不同,物质的状态也不相同,所以不能比较。
答案:A、C
第5页 | 共14页22..(08上海卷)在石灰窑中烧制生石灰,1molCaCO完全分解所需要的能量,可燃烧0.4
3
53mol碳来提供。设空气中O体积分数为0.21,N为0.79,则石灰窑产生的气体中CO的
2 2 2
体积分数可能是( )
A.0.43 B.0.46 C.0.49 D.0.52
点燃 高温
解析: C+O CO CaCO CaO+CO↑
2 2 3 2
0.453mol 0.453mol 0.453mol 1mol 1mol
0.79 × 0.453
产生的CO的总量为:1.453mol,消耗0.453molO含有的N为 =1.70mo
2 2 2 0.21
1.453mol
l,所以气体中的CO的体积分数为: =0.46。
2 1.453mol+1.70mol
答案:A、B
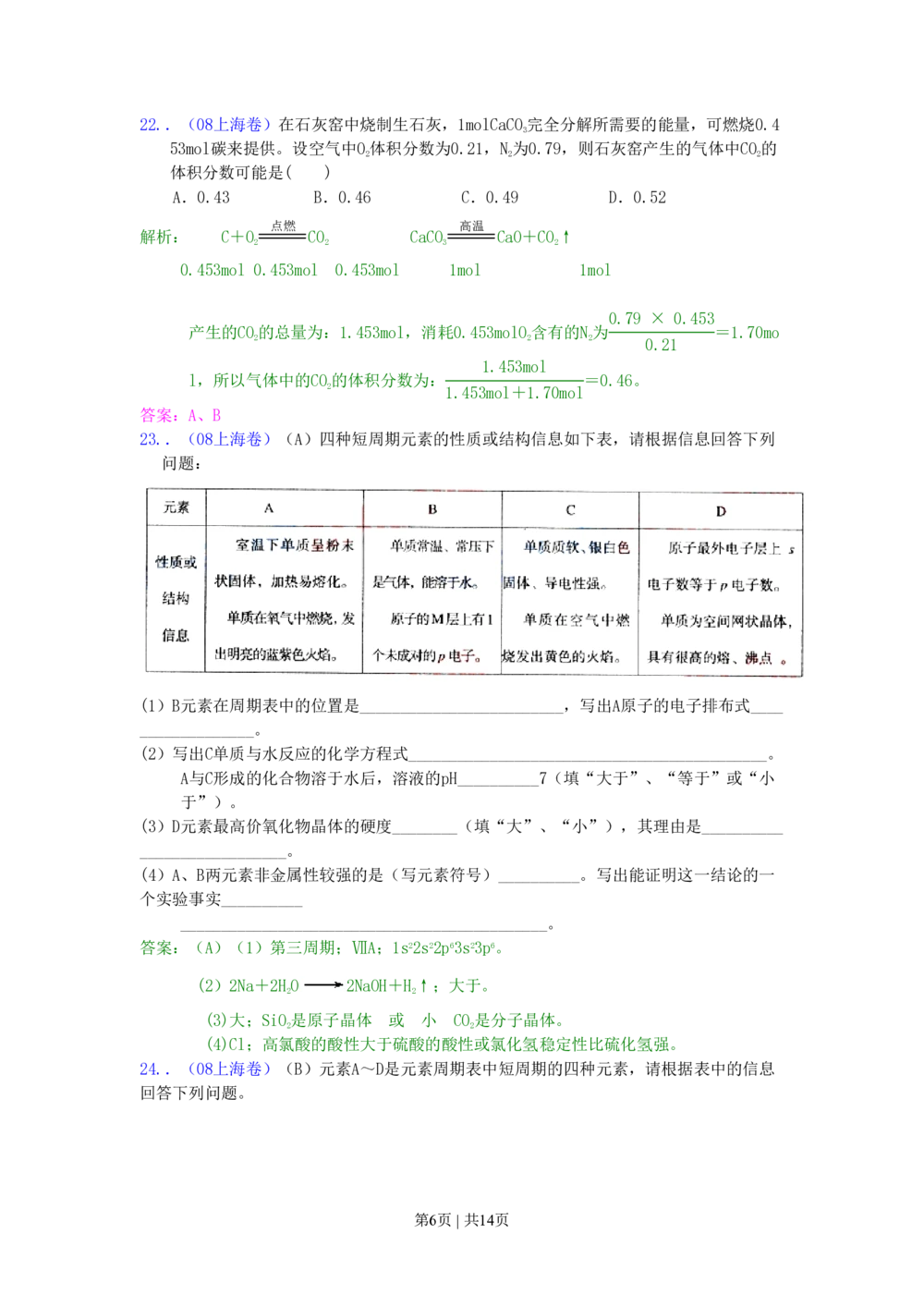
23..(08上海卷)(A)四种短周期元素的性质或结构信息如下表,请根据信息回答下列
问题:
(1)B元素在周期表中的位置是_________________________,写出A原子的电子排布式____
______________。
(2)写出C单质与水反应的化学方程式____________________________________________。
A与C形成的化合物溶于水后,溶液的pH__________7(填“大于”、“等于”或“小
于”)。
(3)D元素最高价氧化物晶体的硬度________(填“大”、“小”),其理由是__________
__________________。
(4)A、B两元素非金属性较强的是(写元素符号)__________。写出能证明这一结论的一
个实验事实__________
_____________________________________________。
答案:(A)(1)第三周期;ⅦA;1s22s22p63s23p6。
(2)2Na+2HO 2NaOH+H↑;大于。
2 2
(3)大;SiO是原子晶体 或 小 CO是分子晶体。
2 2
(4)Cl;高氯酸的酸性大于硫酸的酸性或氯化氢稳定性比硫化氢强。
24..(08上海卷)(B)元素A~D是元素周期表中短周期的四种元素,请根据表中的信息
回答下列问题。
第6页 | 共14页(1)上表中与A属于同一周期的元素是_____________,写出D离子的电子排布式__________
____________。
(2)D和C形成的化合物属于_________晶体。写出C单质与水反应的化学方程式___________
______________。
(3)对元素B的单质或化合物描述正确的是_________。
a、B元素的最高正价为+6 b、常温、常压下单质难溶于水
c、单质分子中含有18个电子 d、在一定条件下镁条能与单质B反应
(4)A和D两元素金属性较强的是(写元素符号)_____。写出能证明该结论的一个实验事实
________________。
答案:(B)(1)Mg;1s22s22s6。
(2)离子;2F+2HO 4HF+O.
2 2 2
(3)b;d(B是氧气或氮气)。
(4)Na;钠与水反应比镁与水反应激烈或氢氧化钠的碱性比氢氧化镁强。
25..(08上海卷)某反应体系的物质有:NaOH、AuO、NaSO、NaSO、AuO、HO。
2 3 2 4 6 2 2 3 2 2
(1)请将AuO之外谁反应物与生成物分别填入以下空格内。
2 3
(2)反应中,被还原的元素是_______,还原剂是____________。
(3)将氧化剂与还原剂填入空格中,并标出电子转移的方向和数目。
(4)纺织工业中常用氯气作漂白剂,NaSO可作为漂白后布匹“脱氯剂”,NaSO和Cl反
2 2 3 2 2 3 2
应的产物是HSO、NaCl和HCl,则还原剂与氧化剂物质的量之比为__________。
2 4
解析:因为AuO为反应物,则AuO必定为生成物,在AuO中Au的化合价为+3,AuO中Au的
2 3 2 2 3 2
化合价为+1,即Au在反应中化合价降低,则另一种元素的化合价必定升高,在NaS
2 2
O中S的化合价为+2,NaSO中S的化合价为2.5价,所以NaSO为反应物,NaSO为
3 2 4 6 2 2 3 2 4 6
生成物,根据化合价的升降总数相等,在NaSO前配2,由S守恒,可知NaSO前配4
2 4 6 2 2 3
,AuO和AuO前分别配1,再根据Na+守恒,则生成物中必定为NaOH,且配平系数为4
2 3 2
,则HO为反应物,在其前面配2,配平后的化学方程式为:AuO+4NaSO+2HO===A
2 2 3 2 2 3 2
uO+2NaSO+4NaOH。
2 2 4 6
答案:(1)AuO、NaSO、HO、NaSO、AuO、NaOH。
2 3 2 2 3 2 2 4 6 2
+ 3
(2) A u;NaSO。
2 2 3
(3)
第7页 | 共14页(4)1∶4。
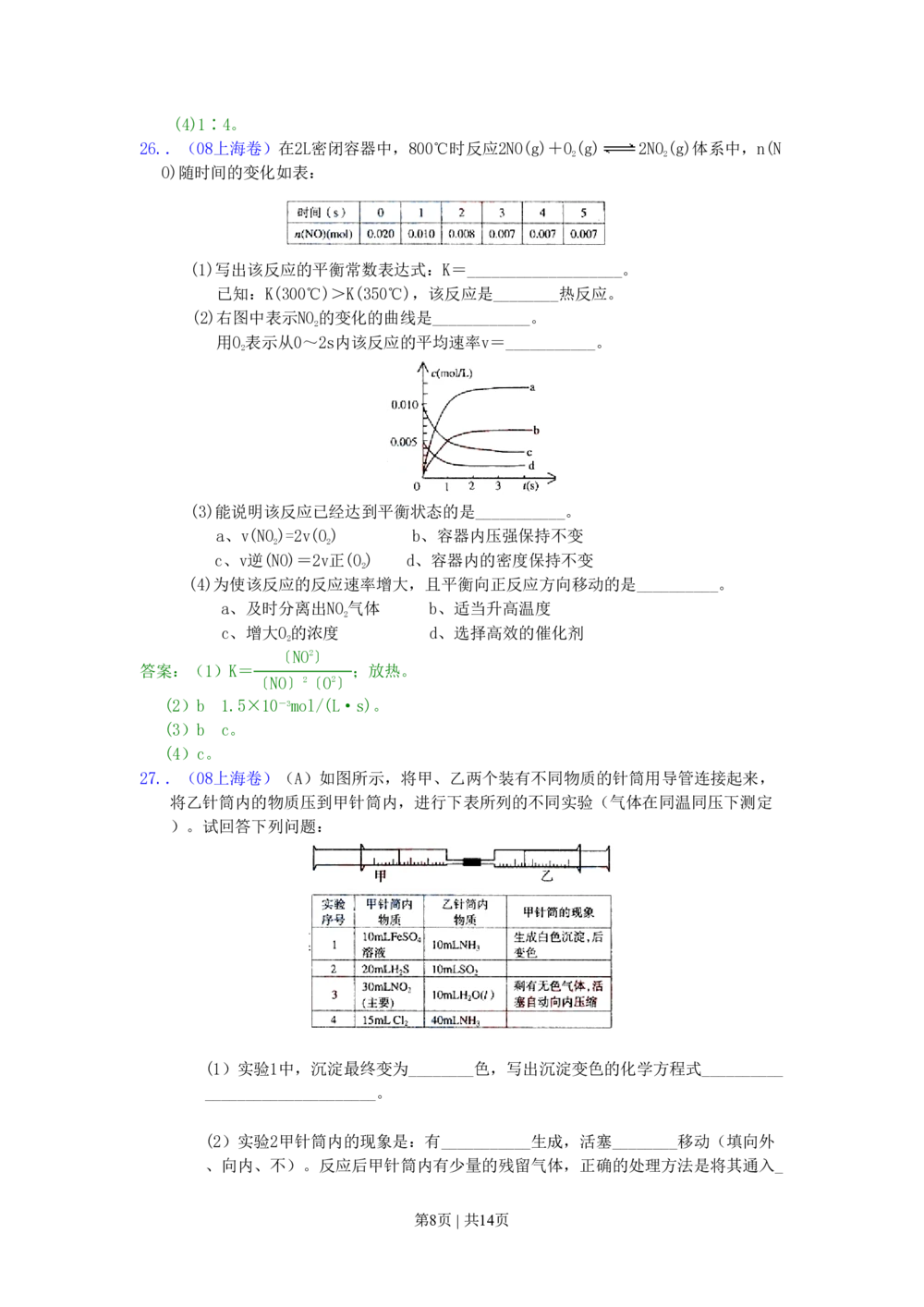
26..(08上海卷)在2L密闭容器中,800℃时反应2NO(g)+O(g) 2NO(g)体系中,n(N
2 2
O)随时间的变化如表:
(1)写出该反应的平衡常数表达式:K=___________________。
已知:K(300℃)>K(350℃),该反应是________热反应。
(2)右图中表示NO的变化的曲线是____________。
2
用O表示从0~2s内该反应的平均速率v=___________。
2
(3)能说明该反应已经达到平衡状态的是___________。
a、v(NO)=2v(O) b、容器内压强保持不变
2 2
c、v逆(NO)=2v正(O) d、容器内的密度保持不变
2
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是__________。
a、及时分离出NO气体 b、适当升高温度
2
c、增大O的浓度 d、选择高效的催化剂
2
〔NO2〕
答案:(1)K= ;放热。
〔NO〕2〔O2〕
(2)b 1.5×10-3mol/(L·s)。
(3)b c。
(4)c。
27..(08上海卷)(A)如图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,
将乙针筒内的物质压到甲针筒内,进行下表所列的不同实验(气体在同温同压下测定
)。试回答下列问题:
(1)实验1中,沉淀最终变为________色,写出沉淀变色的化学方程式__________
_____________________。
(2)实验2甲针筒内的现象是:有___________生成,活塞________移动(填向外
、向内、不)。反应后甲针筒内有少量的残留气体,正确的处理方法是将其通入_
第8页 | 共14页__________溶液中。
(3)实验3中,甲中的3mL气体是NO和NO的混合气体,那么甲中最后剩余的无色
2 2 4
气体是_______,写出NO与HO反应的化学方程式为___________________________
2 2
____。
(4)实验4中,已知:3Cl+2NH N+6HCl。甲针筒出活塞有移动,针筒内
2 3 2
有白烟产生外,气体的颜色变为____________。最后针筒内剩余气体的体积约为_
_______mL。
解析:(1)NH+HO NH·HO,FeSO+2NH·HO===Fe(OH)↓+(NH)SO,
3 2 3 2 4 3 2 2 4 2 4
4Fe(OH)+O+2HO===4Fe(OH),Fe(OH)为红褐色。
2 2 2 3 3
(2)HS+SO===3S+2HO,S为黄色固体,反应后针筒内的压强降低,所以针筒
2 2 2
内的活塞向内压缩,反应后甲针筒内剩余的少量气体不管是SO还是HS或其混合
2 2
物均可用NaOH溶液吸收。
(3)3NO+HO===2NHO+NO,NO 2NO,所以最后剩余的气体为NO。
2 2 3 2 4 2
(4)由方程式可知,随着反应的进行,Cl的量逐渐减少,最终完全反应。
2
3Cl+2NH===N+6HCl
2 3 2
15mL 10mL 5mL 30mL
剩余的NH为30mL,由NH+HCl===NHCl可知,生成的HCl与剩余的NH恰好完全反
3 3 4 3
应生成NHCl,所以最后剩余的气体为5mL。
4
答案:(1)红褐色;4Fe(OH)+O+2HO 4Fe(OH)↓。
2 2 2 3
(2)黄色固体;向内;NaOH。
(3)NO;3NO+HO 2HNO+NO。
2 2 3
(4)黄绿色变为无色;5。
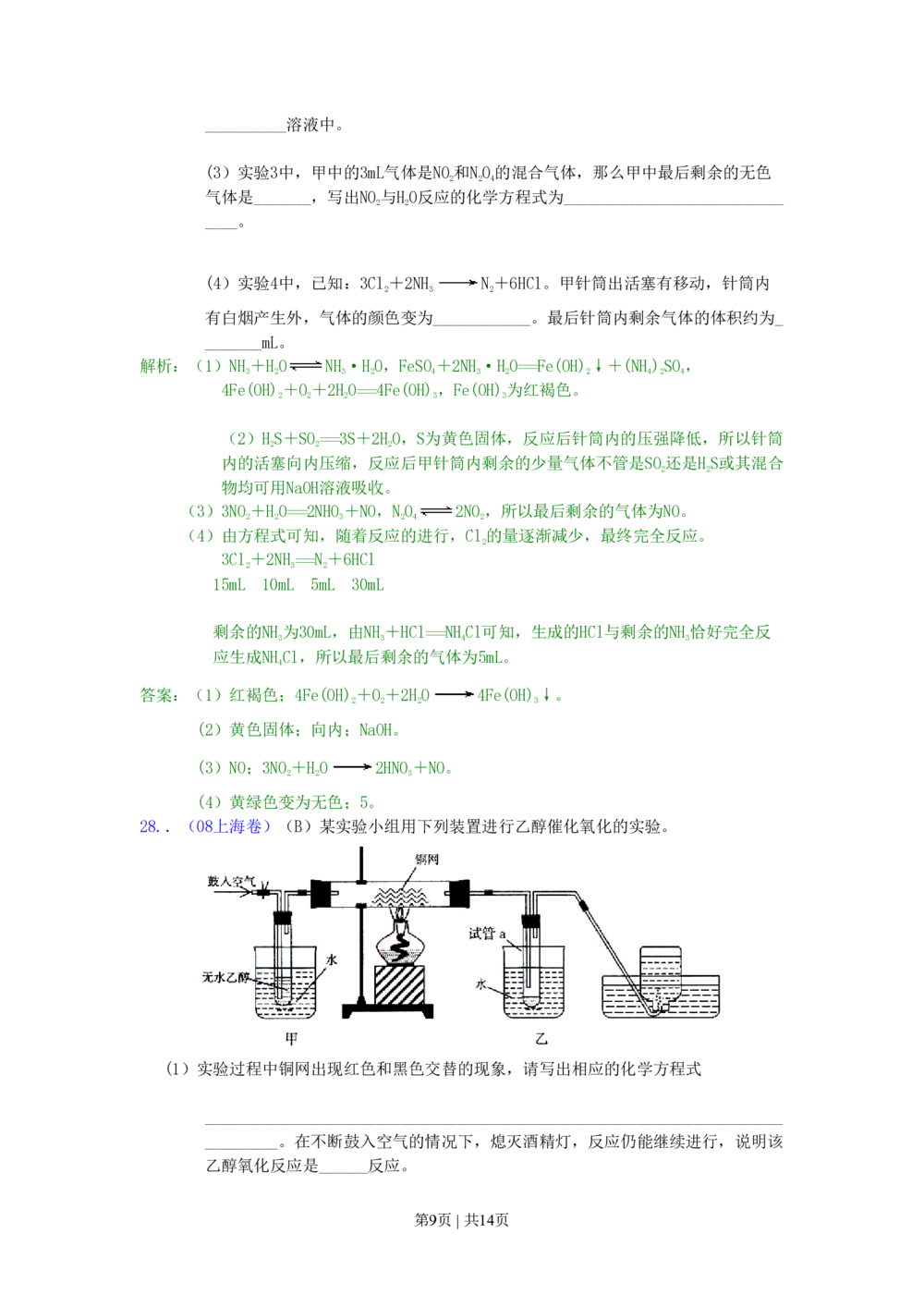
28..(08上海卷)(B)某实验小组用下列装置进行乙醇催化氧化的实验。
(1)实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学方程式
_______________________________________________________________________
_________。在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该
乙醇氧化反应是______反应。
第9页 | 共14页(2)甲和乙两个水浴作用不相同。甲的作用是_____________;乙的作用是______________
_____。
(3)反应进行一段时间后,干燥管a中能收集到不同的物质,它们是___________
_________________。集气瓶中收集到的气体的主要成分是___________________
__。
(4)若试管a中收集到的液体用紫色石蕊试纸,试纸显红色,说明液体中还有___
_________。要除去该物质,可先在混合液中加入_________(填写字母)。
a、氯化钠溶液 b、苯 c、碳酸氢钠溶液 d、四氯化碳
然后再通过___________(填实验操作名称)即可除去。
△
解析:(1)实验过程中铜网出现红色和黑色交替的现象,是因为2Cu+O 2CuO;
2
△
CHCHOH+CuO CHCHO+Cu+HO,熄灭酒精灯后,反应仍能进行,说明此
3 2 2
反应为放热反应。
(2)甲水浴的作用是加热乙醇,便于乙醇的挥发;乙水浴的作用是冷却,便于乙醛的收集
。
(3)经过反应后并冷却,a中收集到的物质有易挥发的乙醇,反应生成的乙醛和
水以及乙醛进一步氧化得到的乙酸。集气瓶中收集到的气体主要为氮气。
(4)试管a中收集到的液体用紫色石蕊试纸,试纸显红色,说明a中收集到的液体呈
酸性,这是由于CHCHO进一步氧化生成了CHCOOH,可以用NaHCO除去,然后经过
3 3 3
蒸馏即可得到乙醛。
△ △
答案:(1)2Cu+O 2CuO;CHCHOH+CuO CHCHO+Cu+HO;放热。
2 3 2 2
(2)加热;冷却。
(3)乙醛;乙醇;水;氮气。
(4)乙酸;c;蒸馏。
29..(08上海卷)明矾石是制取钾肥和氢氧化铝的重要原料,明矾石的组成和明矾相似,
此外还含有氧化铝和少量氧化铁杂质。具体实验步骤如下图所示:
根据上述图示,完成下列填空:
(1)明矾石焙烧后用稀氨水浸出。配制500mL稀氨水(每升含有39.20g氨)需要取
浓氨水(每升含有251.28g氨)__________mL,用规格为_______mL量筒量取。
第10页 | 共14页(2)氨水浸出后得到固体混合体系,过滤,滤液中除K+、SO2-外,还有大量的NH
4 4
+。检验NH+的方法是____________________________________________________
4
___。
(3)写出沉淀物中所有物质的化学式________________________________________。
(4)滤液I的成分是水和______________。
(5)为测定混合肥料KSO、(NH)SO中钾的含量,请完善下列步骤:
2 4 4 2 4
①称取钾氮肥试样并溶于水,加入足量______溶液,产生白色沉淀。
②___________、__________、_________(依次填写实验操作名称)。
③冷却、称重。
(6)若试样为mg,沉淀的物质的量为nmol,则试样中KSO的物质的量为:_______
2 4
____mol(用含有m、n的代数式表示)。
解析:(1)根据稀释前后溶质的质量不变得:0.5L×39.2g/L=v×251.28g/L,v=0.078L
=78mL。为了减少误差,最好选用与氨水的实际体积稍大一点的量筒即可。
(2)NH+的检验方法是:先将NH+中加入强碱,使之转化为NH,然后检验NH即可。
4 4 3 3
(3)Al3++3NH·HO===Al(OH)↓+3NH+,根据题意明矾石中含有AlO、FeO
3 2 3 4 2 3 2 3
,所以沉淀物为Al(OH)、AlO和FeO。
3 2 3 2 3
(4)由于明矾石的组成与明矾相似,所以滤液的成分中含有KSO和反应后生成
2 4
的(NH)SO以及水。
4 2 4
(5)混合肥料中含有KSO和(NH)SO,要产生白色沉淀,加入的溶液为BaCl
2 4 4 2 4 2
或Ba(NO)溶液,以后的操作为:先将混合液过滤,然后洗涤,最后干燥,冷却
3 2
后称量。
(6)根据题意有:174n(KSO)+132N[(NH)SO]=mg……①,再由SO2-守恒得
2 4 4 2 4 4
m-132n
:n(KSO)+n[(NH)SO]=nmol……②,n(KSO)= mol。
2 4 4 2 4 2 4 42
答案:(1)78;100。
(2)取滤液少许,加入NaOH,加热,生成的气体能使湿润的红色石蕊试纸变蓝。
(3)Al(OH);AlO;FeO.
3 2 3 2 3
(4)KSO;(NH)SO。
2 4 4 2 4
(5)BaCl;过滤;洗涤;干燥。
2
m-132n
(6) mol。
42
30..(08上海卷)近年来,由于石油价格的不断上涨,以煤为原料制备一些化工产品的前
景又被看好。下图是以煤为原料生产聚乙烯(PVC)和人造羊毛的合成线路。
第11页 | 共14页请回答下列问题:
(1)写出反应类型:反应①______________,反应②__________________。
(2)写出结构简式:PVC________________,C______________________。
(3)写出A D的化学方程式_______________________________。
(4)与D互为同分异构体且可发生碱性水解的物质有________种(不包括环状化合
物),写出其中一种的结构简式_______________________________________。
解析:煤干馏得到焦炭,在电炉中CaO与C反应生成CaC,再与水反应生成乙炔,所以A为乙
2
炔,则B为CH=CHCl,PVC为聚氯乙烯,乙炔与HCN发生加成反应生成CH=CH-CN,由
2 2
人造羊毛的结构简式可以看出,D的结构简式为CH=CHOOCCH,则E为CHCOOH。
2 3 3
答案:(1)加成反应;加聚反应。
(2) ;HC=HC-CN。
2
催化 剂
(3)HC CH+CHCOOH HC=CH-OOCCH。
3 2 3
(4)4;CH=CHCOOCH。
2 3
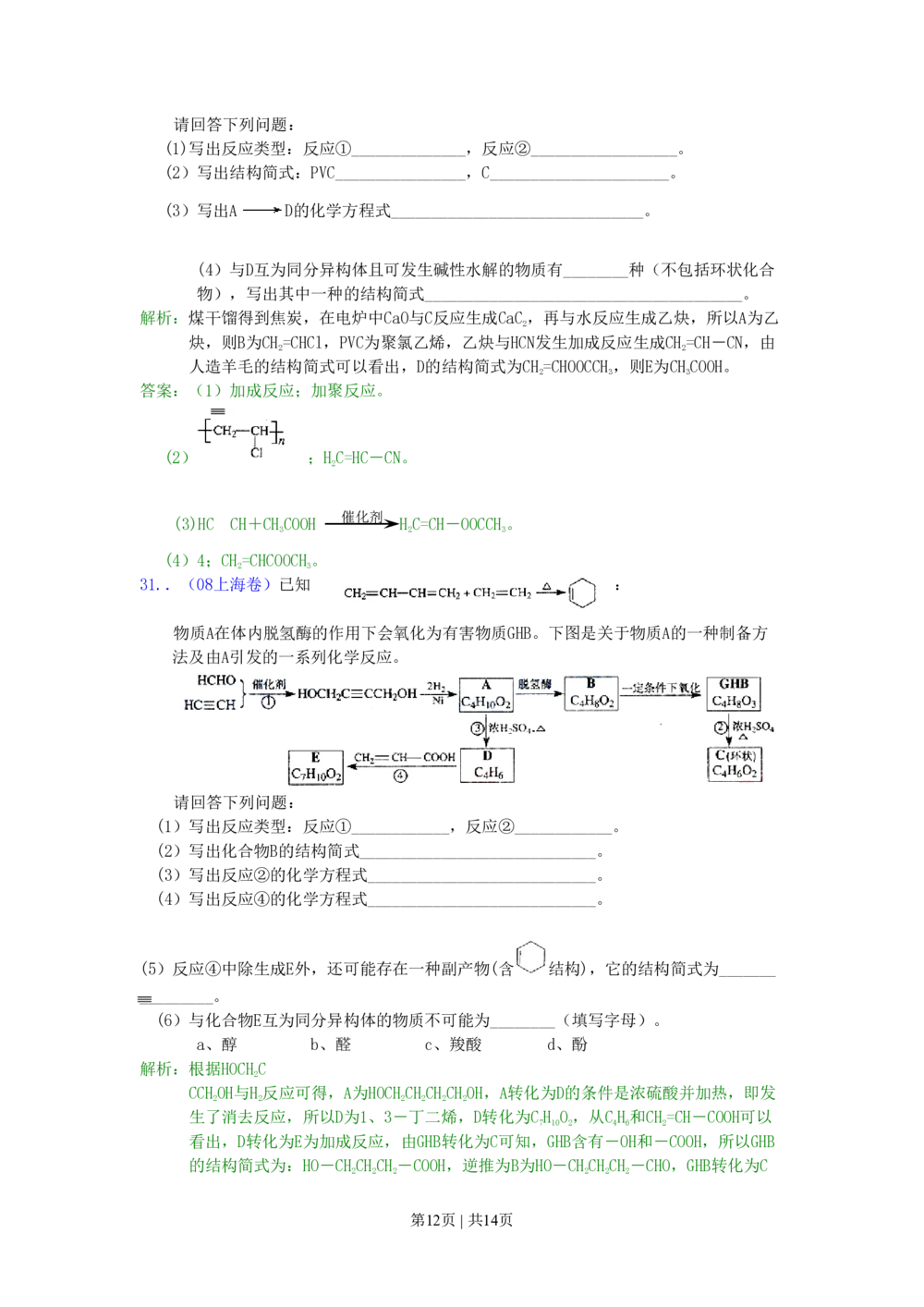
31..(08上海卷)已知 :
物质A在体内脱氢酶的作用下会氧化为有害物质GHB。下图是关于物质A的一种制备方
法及由A引发的一系列化学反应。
请回答下列问题:
(1)写出反应类型:反应①____________,反应②____________。
(2)写出化合物B的结构简式_____________________________。
(3)写出反应②的化学方程式____________________________。
(4)写出反应④的化学方程式____________________________。
(5)反应④中除生成E外,还可能存在一种副产物(含 结构),它的结构简式为_______
_________。
(6)与化合物E互为同分异构体的物质不可能为________(填写字母)。
a、醇 b、醛 c、羧酸 d、酚
解析:根据HOCHC
2
CCHOH与H反应可得,A为HOCHCHCHCHOH,A转化为D的条件是浓硫酸并加热,即发
2 2 2 2 2 2
生了消去反应,所以D为1、3-丁二烯,D转化为CH O,从CH和CH=CH-COOH可以
7 10 2 4 6 2
看出,D转化为E为加成反应,由GHB转化为C可知,GHB含有-OH和-COOH,所以GHB
的结构简式为:HO-CHCHCH-COOH,逆推为B为HO-CHCHCH-CHO,GHB转化为C
2 2 2 2 2 2
第12页 | 共14页是分子内发生酯化反应生成内酯。
答案:(1)加成反应;消去反应。
(2)HOCHCHCHCHO。
2 2 2
(3)
。
(4)
。
(5)
。
(6)d。
32..(08上海卷)生态溶液涉及农家肥料的综合利用,某种肥料经发酵得到一种含有甲烷
、二氧化碳、氮气的混合气体。2.016L(标准状况)该气体通过盛有红色CuO粉末的硬
△
质玻璃管,发生的反应为:CH+4CuO CO+2HO+
4 2 2
4Cu。当甲烷完全反应后,硬质玻璃管的质量减轻4.8g。将反应后产生的气体通过过量
的澄清石灰水,充分吸收,生成沉淀8.5g。
(1)原混合气体中甲烷的物质的量是____________。
(2)原混合气体中氮气的体积分数为多少?(写出计算过程)
4.8g
解析:由于硬质玻璃管减少的质量为CuO中的氧的质量,所以n(CuO)= =0.3mol,由
16g/mol
方程式可知反应的CH的物质的量为0.075mol。生成的CO也为0.075mol,将气体通过
4 2
澄清的石灰水生成8.5g沉淀,所以n(CO)=0.085mol,原混合气体中的n(CO)=0.01mo
2 2
2.016L
l,而气体的总物质的量为: =0.09mol,所以n(N)=0.005mol,N的体积
22.4L/mol 2 2
0.005mol
分数为: ×100%=5.56%。
0.09mol
答案:(1)0.075mol。
(2)5.56%。
33..(08上海卷)小苏打、胃舒、平达喜都是常用的中和胃酸的药物。
(1)小苏打片每片含0.5gNaHCO,2片小苏打片和胃酸完全中和,被中和的H+是__________
3
_mol。
(2)胃舒平每片含0.245gAl(OH)。中和胃酸时,6片小苏打片相当于胃舒平_____片。
3
(3)达喜的化学成分是铝和镁的碱式盐。
①取该碱式盐3.01g,加入2.0mol·L-1盐酸使其溶解,当加入盐酸42.5mL时,
开始产生CO,加入盐酸至45.0mL时正好反应完全,计算该碱式盐样品中氢氧根
2
与碳酸根的物质的量之比。
第13页 | 共14页②在上述碱式盐溶于盐酸后的溶液中加入过量的氢氧化钠,过滤,沉淀物进行
干燥后重1.74g,若该碱式盐中氢元素的质量分数为0.040,试推测该碱式盐的
化学式。
1g
解析:(1)2片小苏打所含NaHCO的质量为1g,其物质的量为 =0.012mol,
3 84g/mol
由HCO-+H+===CO↑+HO,可知n(H+)=0.012mol。
3 2 2
3g
(2)6片小苏打的物质的量为: =0036mol,即中和的H+为0.036mol,而每
84g/mol
0.245g
片的Al(OH)的物质的量为 =0.0031mol,由Al(OH)+3H+
3 78g/mol 3
0.012
===Al3++3HO,所以Al(OH)的片数为: =3.8片。
2 3 0.0031
(3)①碱式盐中加入HCl,首先是碱式盐中的OH-和CO2-与H+反应生成HO和HCO
3 2 3
-,所以n(HCO-)=2.0mol·L-1×0.0025L=0.005mol,即n(CO2-)=0.005mol
3 3
,H+与CO2-与HCl反应的H+的总物质的量为:2.0mol·L-1×0.0425L=0.085mo
3
l,所以n(OH-)=0.08mol,它们的物质的量之比为:16∶1。
1.74g
②能与过量的NaOH溶液反应产生沉淀的只有Mg2+,所以n[Mg(OH)]= =0
2 58g/mol
.03mol,若碱式盐中不含结晶水,则氢元素的质量分数为:0.08mol×1g/mol
0.08g
=0.08g,氢元素的质量分数为: =0.027<0.04,说明碱式盐中含有结晶
3.01g
水,根据题意有:m(Al)+m(HO)+0.03mol×24g/mol+0.005mol×60g/mol+
2
2
× m(H2O)+0.08mol × 1g/mol
18
0.08mol×17g/mol=3.01g, =0.04,所以m(H
3.01g
O)=0.36g,n(HO)=002mol,m(Al)=0.27g,n(Al)=001mol,所以n(Al3+)∶n(M
2 2
g2+)∶n(OH-)∶n(CO2-)∶n(HO)=0.01mol∶0.03mol∶0.08mol∶0.005mol∶
3 2
0.02mol=2∶6∶16∶1∶4,即碱式盐的化学式为:AlMg(OH) CO·4HO。
2 6 16 3 2
答案:(1)0.012mol。
(2)3.8。
(3)n(OH-)∶n(CO2-)=16∶1。
3
(4)AlMg(OH) CO·4HO。
2 6 16 3 2
第14页 | 共14页