文档内容
高三化学
考生注意:
1.本试卷分选择题和非选择题两部分。满分100分,考试时间75分钟。
2.答题前,考生务必用直径0.5毫米黑色墨水签字笔将密封线内项目填写清楚。
3.考生作答时,请将答案答在答题卡上。选择题每小题选出答案后,用2B铅笔把答题卡上对应题
目的答案标号涂黑;非选择题请用直径0.5毫米黑色墨水签字笔在答题卡上各题的答题区域内
作答,超出答题区域书写的答案无效,在试题卷、草稿纸上作答无效。
4.本卷命题范围:人教版必修第一、二册,选择性必修1第一章。
5.可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 Na 23
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合
题目要求的。
1.下列做法不能体现“绿色化学”思想的是
A.将废旧塑料裂解为化工原料
B.研发新能源汽车,降低汽油、柴油消耗
C.减少一次性筷子、纸杯和塑料袋的使用
D.乙烯、Ca(OH) 、Cl 制备 (环氧乙烷)
2 2
2.下列说法正确的是
A.MgO属于两性氧化物
B.Fe O 中的铁元素呈现两种价态
3 4
C.CO 和SiO 二者物理性质相似
2 2
D.用FeCl 溶液和NaOH溶液制备Fe(OH) 胶体
3 3
3.下列鉴别或检验能达到实验目的的是
A.用硝酸酸化的BaCl 溶液检验Na SO 是否被氧化 B.用酸性KMnO 检验乙烯中是否含有SO
2 2 3 4 2
C.用石灰水鉴别Na CO 与NaHCO D.用水检验溴蒸气和NO 气体
2 3 3 2
4.下列有关化学用语表示错误的是
A.H O的空间结构:V形
2
C.Cl-的结构示意图:
D.Fe (SO ) 溶于水的电离方程式:Fe (SO ) =2Fe3++3SO2−
2 4 3 2 4 3 4
5.下列反应的离子方程式书写正确的是
【高三第3次质量检测·化学 第1页(共6页)】 H-G
学科网(北京)股份有限公司A.少量Cl 通入NaI溶液中:Cl +I−=I +Cl−
2 2 2
B.用氢氟酸雕刻玻璃:SiO +4H++4F−=SiF ↑+2H O
2 4 2
C.NO 通入水中::2NO +H O=2H++2NO−
2 2 2 3
D.过量CO 通入饱和碳酸钠溶液中:2Na++CO2−+CO +H O=2NaHCO ↓
2 3 2 2 3
6.下列根据实验目的设计的装置连接中正确的是
浓硫酸
a b C d e f g
A.用碱石灰和浓氨水制备收集N H :连接a→d→e→e
3
B.用MnO 和浓盐酸制备收集Cl :连接b→f→c→e→d
2 2
C.用铜和稀硝酸制备收集NO:连接b→c→e
D.用铜和浓硫酸制备收集SO :连接a→c→e→d
2
7 . 在 298K 、 100kPa 时 , 已 知 :
1
2C(s)+O (g)=2CO(g) ΔH ,H (g)+ O (g)=H O(l) ΔH ,C(s)+H O(g)=CO(g)+H (g) ΔH
2 1 2 2 2 2 2 2 2 3
。下列关于ΔH 、ΔH 、ΔH 的关系正确的是
1 2 3
A.ΔH −2ΔH −2ΔH =0 B.ΔH −2ΔH −2ΔH <0
1 2 3 1 2 3
C.ΔH −2ΔH −2ΔH >0 D.无法确定
1 2 3
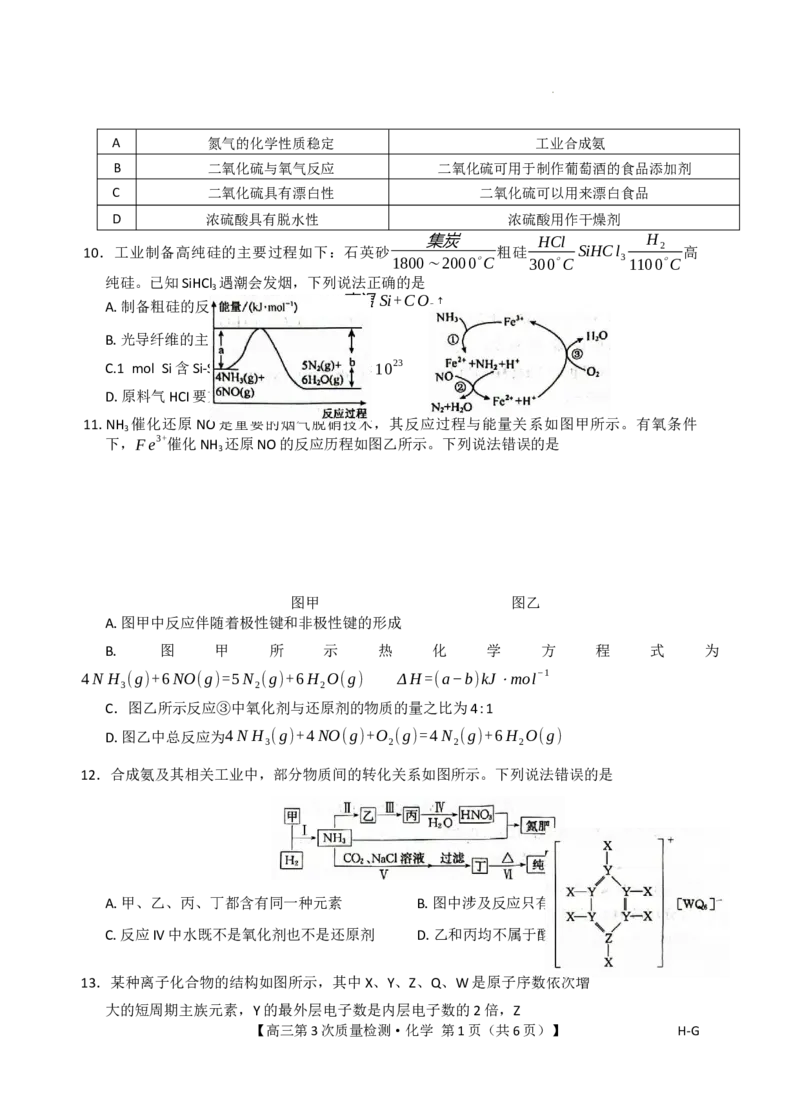
8.多相催化反应是在催化剂表面通过吸附、解吸过程进行的。如图为在某温度下,CH OH与H O
3 2
在铜基催化剂上的反应机理和能量与反应过程之间的关系(各物质均为气态):
下列说法错误的是
A.反应II过程中热效应ΔH<0
B.1 mol CH OH(g)和1 molH O(g)的总能量小于1molCO (g)和3molH (g)的总能量
3 2 2 2
C.选择优良的催化剂可以降低反应活化能,但不能改变反应的ΔH
D.CO(g)在反应过程中,先生成后消耗,故可认为CO(g)是催化剂
9.下表中物质性质和用途均正确且具有因果关系的是
选项 物质性质 用途
【高三第3次质量检测·化学 第1页(共6页)】 H-G
学科网(北京)股份有限公司A 氮气的化学性质稳定 工业合成氨
B 二氧化硫与氧气反应 二氧化硫可用于制作葡萄酒的食品添加剂
C 二氧化硫具有漂白性 二氧化硫可以用来漂白食品
D 浓硫酸具有脱水性 浓硫酸用作干燥剂
集炭 HCl H
10.工业制备高纯硅的主要过程如下:石英砂 粗硅 SiHCl 2 高
1800∼2000∘C 300∘C 3 1100∘C
纯硅。已知SiHCl 遇潮会发烟,下列说法正确的是
3
SiO +C高温Si+CO ↑
A.制备粗硅的反应方程式为 2 2
→
B.光导纤维的主要成分为高纯硅
C.1 mol Si含Si-Si键的数目约为4×6.02×1023
D.原料气HCI要充分干燥,去除水蒸气
11.NH 催化还原NO是重要的烟气脱硝技术,其反应过程与能量关系如图甲所示。有氧条件
3
下,Fe3+催化NH 还原NO的反应历程如图乙所示。下列说法错误的是
3
图甲 图乙
A.图甲中反应伴随着极性键和非极性键的形成
B. 图 甲 所 示 热 化 学 方 程 式 为
4N H (g)+6NO(g)=5N (g)+6H O(g) ΔH=(a−b)kJ⋅mol−1
3 2 2
C.图乙所示反应③中氧化剂与还原剂的物质的量之比为4:1
D.图乙中总反应为4N H (g)+4NO(g)+O (g)=4N (g)+6H O(g)
3 2 2 2
12.合成氨及其相关工业中,部分物质间的转化关系如图所示。下列说法错误的是
A.甲、乙、丙、丁都含有同一种元素 B.图中涉及反应只有反应I属于氮的固定
C.反应IV中水既不是氧化剂也不是还原剂 D.乙和丙均不属于酸性氧化物
13.某种离子化合物的结构如图所示,其中X、Y、Z、Q、W是原子序数依次增
大的短周期主族元素,Y的最外层电子数是内层电子数的2倍,Z
【高三第3次质量检测·化学 第1页(共6页)】 H-G
学科网(北京)股份有限公司与W 同主族,Q是元素周期表中电负性最大的元素。下列说法
错误的是
A.非金属性:Z>W
B.氢化物沸点:Z>Y
C.ZQ 分子中各原子最外层均达到8电子稳定结构
3
D.X、Z、Q三种元素能形成离子化合物
14.氧族元素碲( Te)被誉为“国防与尖端技术的维生素”。工业上常用铜阳极泥(主要成分是
52
Cu Te、含Ag、Au等杂质)为原料提取碲并回收贵金属,其工艺流程如图所示:
2
已知:TeO 微溶于水,易与较浓的强酸、强碱反应。下列说法错误的是
2
A.Te的最外层电子数为6
B . “ 酸 浸 1” 过 程 中 , Cu Te转 化 为 TeO , 反 应 的 化 学 方 程 式 为
2 2
Cu Te+2O +2H SO =2CuSO +TeO +2H O
2 2 2 4 4 2 2
C.“还原”过程中,反应的化学方程式为TeCl +2SO +4H O=2H SO +Te↓+4HCl
4 2 2 2 4
D.TeO2溶于浓NaOH溶液的离子方程式为TeO +2OH−=TeO2−+H O
2 4 2
二、非选择题:本题共4小题,共58分。
15.(14分)废旧三元锂电池正极材料(LiNi Co Mn O )中富含Li、Ni、Co、Mn等有价金
x 1−x−y y 2
属,将其回收的工艺流程如图所示:
已知:①浸出液中c(Li+ )=0.14mol⋅L−1;
②少量的Ni2+和Co2+与氨水反应生成的[∋(N H ) ] 2+ 比[Co(N H ) ] 2+ 更稳定。
3 6 3 6
回答下列问题:
(1)Fe在元素周期表中的位置为 。
(2)正极材料表示为LiMO (M代表Co、Ni、Mn,化合价均为+3)。
2
①“酸浸”时LiNiO 反应的化学方程式为 。
2
②“酸浸”时温度不宜过高的原因是 。
(3)浸出液中先加入氨水后加入(NH ) C O ,生成CoC O 沉淀而没有NiC O 沉淀生成的原
4 2 2 4 2 4 2 4
因是
。
【高三第3次质量检测·化学 第1页(共6页)】 H-G
学科网(北京)股份有限公司(4)气体X的电子式为 。
(5)一定量2NiCO ·Ni(OH) 与足量盐酸反应,消耗HCI的物质的量与生成CO 的物质的量之
3 2 2
比为
。
(6)现有10L浸出液,回收得到44.03gLi CO ,则Li+的回收率为 。
2 3
16.(14分)以黄铁矿(主要成分为,FeS ,,还有少量CuS、SiO )为原料,制备硫酸、亚硫酸氢钠
2 2
和硫酸亚铁晶体(FeSO ⋅7H O,溶解度随温度升高而增大)的部分工艺流程如下:
4 2
回答下列问题:
(1)“焙烧”后得到的固体主要成分为Fe O ,写出Fe O 与稀硫酸反应的离子方程式:
2 3 2 3
。
(2)“焙烧”产生的 SO 会污染环境,可用足量氨水吸收,写出反应的离子方程式:
2
。
(3)实验室用制得的浓硫酸和铜制备SO 的化学方程式为 。
2
(4)试剂X是 (填化学式)。
(5)设计实验,检验“还原”得到的溶液是否达到实验目的: 。
(6)从“还原”得到的溶液中获得硫酸亚铁晶体的操作: 、 、过滤、洗涤、干燥。
(7)工业上以SO 和纯碱为原料制备无水 NaHSO 的主要流程如图所示,下列说法错误的是
2 3
(填字母)。
A.“吸收”过程中有气体生成 B.“结晶”后母液中含有NaHCO
3
C.“气流干燥”时温度不宜过高 D.“中和”后溶液中含Na SO 和NaHCO
2 3 3
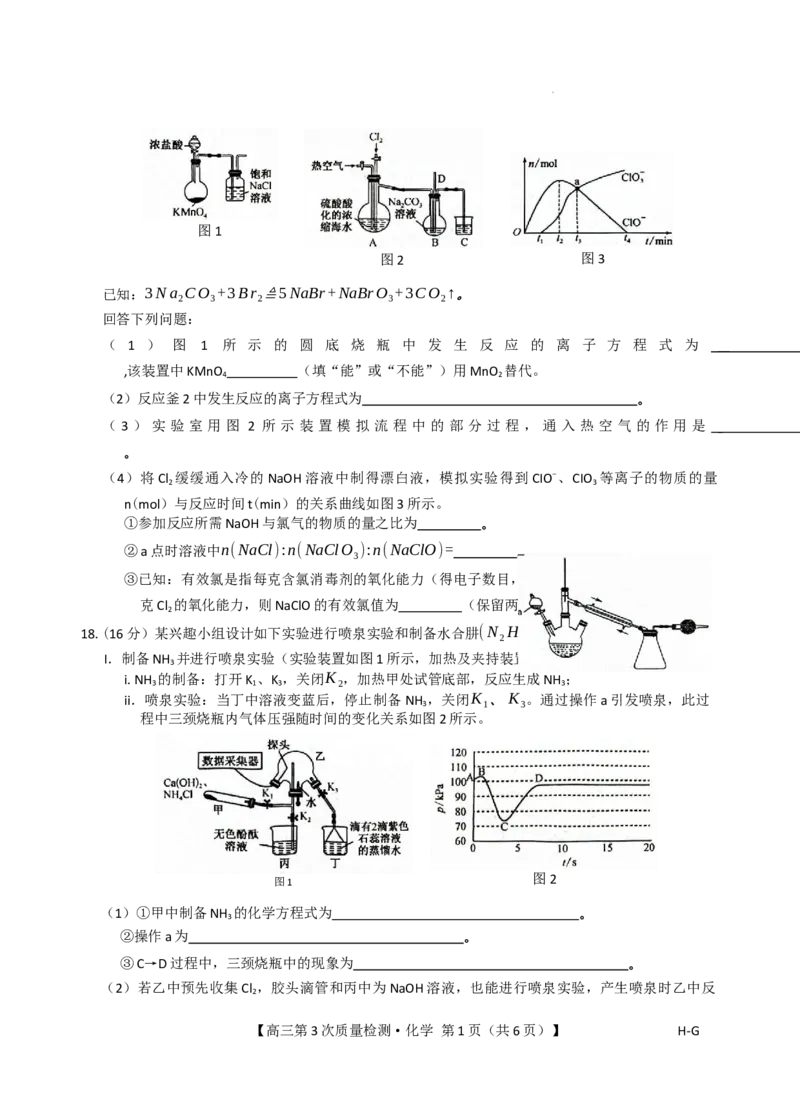
17.(14分)工业上以浓缩海水(含较高浓度的Br)为原料提取溴的部分流程及实验装置图如下:
【高三第3次质量检测·化学 第1页(共6页)】 H H - - G G
学科网(北京)股份有限公司图1
图2 图3
已知:3Na CO +3Br ≜5NaBr+NaBrO +3CO ↑。
2 3 2 3 2
回答下列问题:
( 1 ) 图 1 所 示 的 圆 底 烧 瓶 中 发 生 反 应 的 离 子 方 程 式 为
,该装置中KMnO (填“能”或“不能”)用MnO 替代。
4 2
(2)反应釜2中发生反应的离子方程式为 。
( 3 ) 实 验 室 用 图 2 所 示 装 置 模 拟 流 程 中 的 部 分 过 程 , 通 入 热 空 气 的 作 用 是
。
(4)将Cl 缓缓通入冷的NaOH溶液中制得漂白液,模拟实验得到CIO-、CIO 等离子的物质的量
2 3
n(mol)与反应时间t(min)的关系曲线如图3所示。
①参加反应所需NaOH与氯气的物质的量之比为 。
②a点时溶液中n(NaCl):n(NaClO ):n(NaClO)= 。
3
③已知:有效氯是指每克含氯消毒剂的氧化能力(得电子数目,氯元素转化为CI)相当于多少
克Cl 的氧化能力,则NaClO的有效氯值为 (保留两位有效数字)。
2
18.(16分)某兴趣小组设计如下实验进行喷泉实验和制备水合肼(N H ⋅H O)。回答下列问题:
2 4 2
I.制备NH 并进行喷泉实验(实验装置如图1所示,加热及夹持装置已省略)。
3
i.NH 的制备:打开K 、K ,关闭K ,加热甲处试管底部,反应生成NH ;
3 1 3 2 3
ii.喷泉实验:当丁中溶液变蓝后,停止制备 NH ,关闭K 、K 。通过操作a引发喷泉,此过
3 1 3
程中三颈烧瓶内气体压强随时间的变化关系如图2所示。
图1
图2
(1)①甲中制备NH 的化学方程式为 。
3
②操作a为 。
③C→D过程中,三颈烧瓶中的现象为 。
(2)若乙中预先收集Cl ,胶头滴管和丙中为NaOH溶液,也能进行喷泉实验,产生喷泉时乙中反
2
【高三第3次质量检测·化学 第1页(共6页)】 H-G
学科网(北京)股份有限公司应的离子方程式为 。
II.制备水合肼。
以NaClO溶液与含NaOH的CO(NH ) (沸点:196.6℃)溶液为
2 2
原料,利用图 3装置(部分仪器已省略)制备N H ⋅H O
2 4 2
(熔点:
-51.7℃,沸点:118.5℃,常温下为易溶于水的碱性液体,具
有较强的还原性)。
(3)三颈烧瓶中合成N H ⋅H O的化学方程式是 图3
2 4 2
(产物中还有两种盐),N H 溶于水显碱性,为二元弱碱,N H 与硫酸反
2 4 2 4
应生成酸式盐的化学式为 。
(4)从三颈烧瓶所得溶液中获得N H ⋅H O的操作是 (填字母)。
2 4 2
A.过滤 B.蒸发浓缩、冷却结晶 C.蒸馏
(5)图3中冷凝管能否改用球形冷凝管并说明理由: 。
(6)样品中N H ⋅H O含量的测定:称取样品1.500g,加入适量NaHCO 固体,配成250mL溶
2 4 2 3
液,每次取25.00mL溶液,滴入几滴淀粉溶液,用0.1000mol·L-1的标准I 溶液滴定,达滴定终
2
点时平均消耗标准 I 溶液的体积为 36.00mL,则样品中 N H ⋅H O的质量分数为
2 2 4 2
(已知:
N H ⋅H O+2I =N ↑+4HI+H O)。
2 4 2 2 2 2
【高三第3次质量检测·化学 第1页(共6页)】 H-G
学科网(北京)股份有限公司