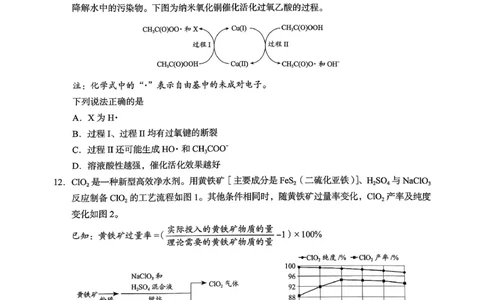
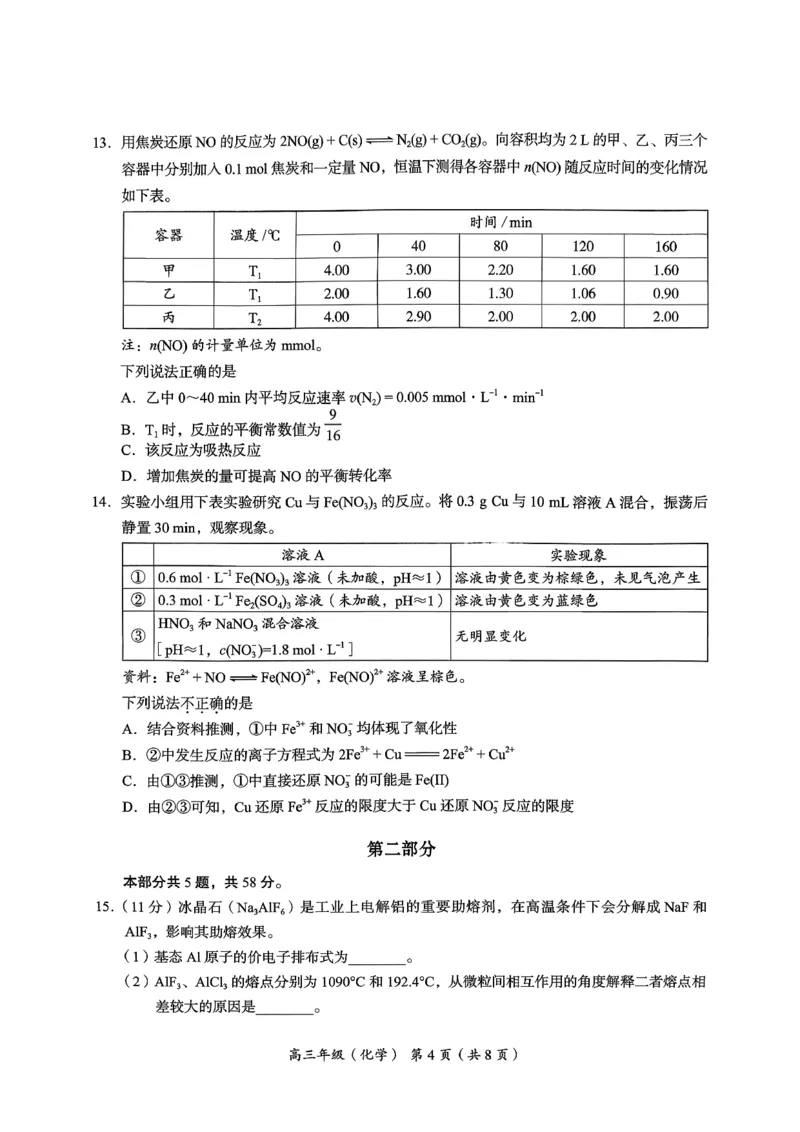
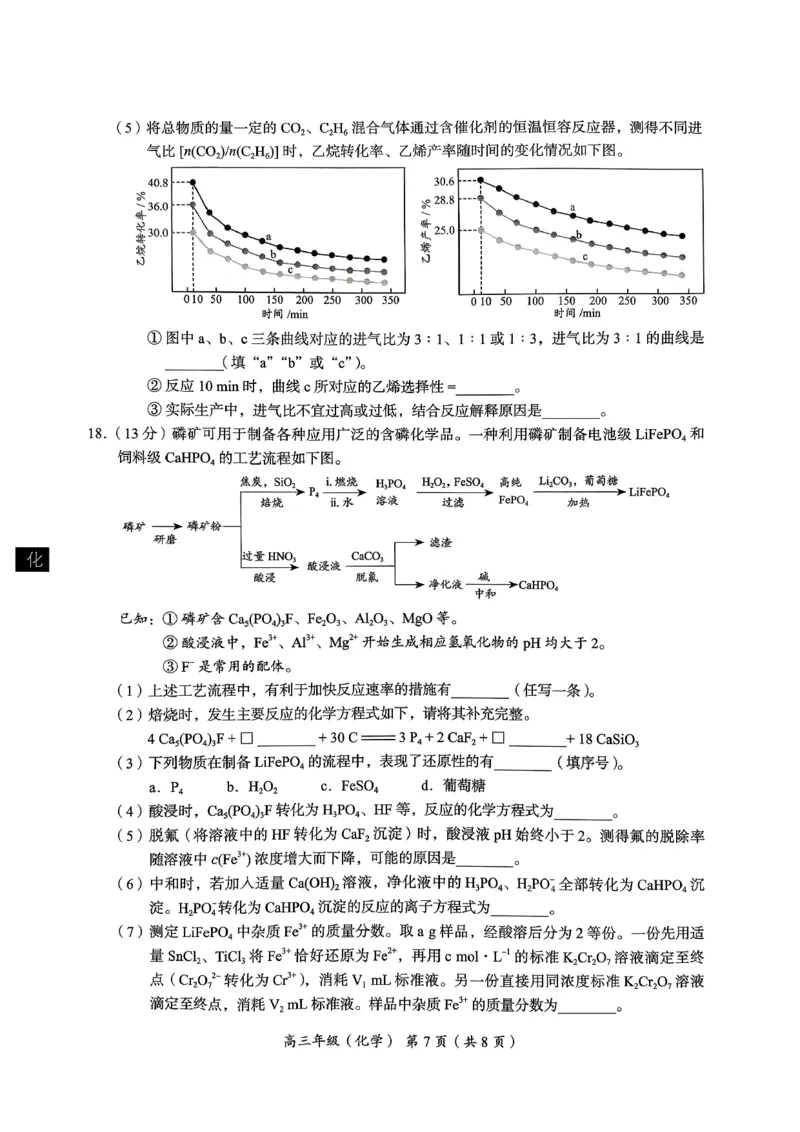
文档内容
{#{QQABAQKQgggIAIIAAQgCUQGQCgEYkBECAAgGwFAQMAABARFABAA=}#}{#{QQABAQKQgggIAIIAAQgCUQGQCgEYkBECAAgGwFAQMAABARFABAA=}#}{#{QQABAQKQgggIAIIAAQgCUQGQCgEYkBECAAgGwFAQMAABARFABAA=}#}{#{QQABAQKQgggIAIIAAQgCUQGQCgEYkBECAAgGwFAQMAABARFABAA=}#}{#{QQABAQKQgggIAIIAAQgCUQGQCgEYkBECAAgGwFAQMAABARFABAA=}#}{#{QQABAQKQgggIAIIAAQgCUQGQCgEYkBECAAgGwFAQMAABARFABAA=}#}{#{QQABAQKQgggIAIIAAQgCUQGQCgEYkBECAAgGwFAQMAABARFABAA=}#}{#{QQABAQKQgggIAIIAAQgCUQGQCgEYkBECAAgGwFAQMAABARFABAA=}#}海淀区 2025-2026 学年第一学期期中练习
高三化学参考答案
第一部分(共14题,每小题3分,共42分)
题号 1 2 3 4 5 6 7
答案 B C B D A C A
题号 8 9 10 11 12 13 14
答案 D C B C A B D
第二部分(共5题,共58分)
15.(11分)
(1) 3s23p1
(2) AlF 3熔化时破坏的是离子键,AlCl 3熔化时主要破坏分子间作用力,离子键比分子间
作用力更强,因此AlF 3熔点远高于AlCl
3
(3) ① II
② <
③ 正四面体 sp3
(4) ① 黑球
② 图2所示小立方体平移后无法完全重合(或不能无隙并置)
4
③
3�1030
−
��·� ×
16.(12分)
(1)cd
△
(2)① NH 4 ++OH-====NH 3↑ +H 2 O
② H
3
BO 3中B原子提供空轨道,NH 3中N原子提供孤电子对
③ b
一定条件
(3)① 6H++5CH
3
OH+6NO
3
- =======3N
2
+5CO
2
+13H
2
O
② II反应步骤少;消耗O 2和CH
3
OH的量较少
③ 0.75
17.(9分)
MeOx
1
{#{QQABAQKQgggIAIIAAQgCUQGQCgEYkBECAAgGwFAQMAABARFABAA=}#}(1)2C
2
H
6
+O
2
====== 2C
2
H
4
+2H
2
O
(2)锰基载氧体的氧活性过高,氧化性强,可能将乙烷(或乙烯)氧化为其他产物如 CO、
CO 2等
(3)共价晶体
(4)+177.7kJ·mol−1
(5)① a
② 83.3%
③ 进气比3:1时乙烯选择性小,CO 2比例大,对反应iv的促进作用大于对反应i的促
进;进气比1:3时,反应v发生使得乙烯产率小
18.(13分)
(1)研磨、焙烧、加热、提高HNO 3的浓度
(2)4Ca
5
(PO
4
)
3
F+18SiO
2
+30C=== 3P
4
+2CaF
2
+30CO+18CaSiO
3
(3)acd
(4)Ca
5
(PO
4
)
3
F+10HNO
3
====3H
3
PO
4
+HF+5Ca(NO
3
)
2
(5)随溶液中的Fe3+浓度增大,Fe3+与F-结合生成较稳定的配离子,消耗F-,Ca2+难与F-
形成沉淀
(6)H
2
PO
4
- +OH-+Ca2+====CaHPO 4↓+H
2
O
(7)2[56×6c(V
1
-V
2
)×10-3]/a
19.(13分)
(1)排除O
2
对KI与SO
2
反应的干扰
(2)Na SO +H SO ====Na SO +SO ↑+H O
2 3 2 4 2 4 2 2
(3)① 溶液未变蓝 BaCl 2溶液
一定条件
② 3SO +2H O======2SO2-+S↓+4H+
2 2 4
(4)KI能促进SO 2发生歧化反应,只加盐酸时SO 2的歧化反应难以发生,盐酸和KI同时存在
可以加快歧化反应
(5)① I
2
+SO
2
+2H
2
O====2I-+SO
4
2- +4H+
② <
③ 相同浓度的Cl-还原性弱于I-,反应i难以发生;Cl-的离子半径小于I-,结合能力弱,
不易形成中间产物
2
{#{QQABAQKQgggIAIIAAQgCUQGQCgEYkBECAAgGwFAQMAABARFABAA=}#}