文档内容
银川一中2026 届高三年级第三次月考 4.室温下,下列各组离子在指定溶液中一定能大量共存的是
A.无色透明的水溶液:
化 学 试 卷
B.使甲基橙变红的溶液:
注意事项: C.常温下 的溶液:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.作答时,务必将答案写在答题卡上。写在本试卷及草稿纸上无效。
D. 的溶液:
3.考试结束后,将本试卷和答题卡一并交回。
5.下列实验事实对应的结论不正确的是
可能用到的相对原子量:H-1 C-12 N-14 O-16 Na-23 S-32 Fe-56
一、选择题:(本题共14小题,每小题3分,共42分。每小题只有一项符合题目要求。) 实验事实 结论
1.化学与生产、生活、科技等密切相关,下列说法正确的是
向 溶液中滴加几滴溴水并振荡,产生淡黄
A 氧化性:
A. “真金不怕火炼”是指真金的熔点高 色沉淀
B. “华为麒麟980”手机中芯片的主要成分是二氧化硅
测量 和 两种饱和溶液的 ,前者 , 溶解度:
B
C. “釜底抽薪”是利用了除去氧化还原反应中还原剂的原理
后者
D. “百炼成钢”的化学含义是使用还原剂降低生铁中碳的含量
C 将 滴入酸性 溶液中,溶液褪色 具有还原性
2.下列化学用语或图示表达不正确的是
表面积相同的镁条和铝条与等浓度盐酸反应的剧烈程度:镁条>铝
A. 基态铬原子的价层电子排布式: D 金属性:
条
B. 过氧化钠的电子式:
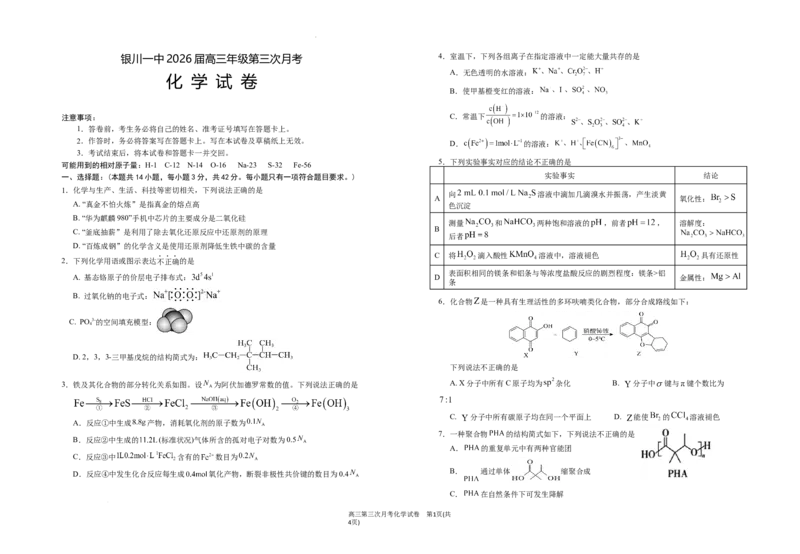
6.化合物 是一种具有生理活性的多环呋喃类化合物,部分合成路线如下:
C. PO 3-的空间填充模型:
4
D. 2,3,3-三甲基戊烷的结构简式为:
下列说法不正确的是
3.铁及其化合物的部分转化关系如图。设 为阿伏加德罗常数的值。下列说法正确的是 A. X分子中所有C原子均为 杂化 B. 分子中 键与 键个数比为
C. 分子中所有碳原子均在同一个平面上 D. 能使 的 溶液褪色
A.反应①中生成 产物,消耗氧化剂的原子数为
7.一种聚合物 的结构简式如下,下列说法不正确的是
B.反应②中生成的 (标准状况)气体所含的孤对电子对数为0.5
A. 的重复单元中有两种官能团
C.反应③中 含有的 数目为
B. 通过单体 缩聚合成
D.反应④中发生化合反应每生成 氧化产物,断裂非极性共价键的数目为0.4
C. 在自然条件下可发生降解
高三第三次月考化学试卷 第1页(共
学科网(北京)股份有限公司 4页)高三第三次月考化学试卷 第1页(共
4页)
D. 中存在手性碳原子
8.下列过程中,对应反应方程式正确的是
A.NaHS溶液中滴入 溶液:
B.AgCl溶于浓氨水:
注:消毒效率指全部 发生消毒反应时所能转移的电子数。
C.酸性 溶液氧化 :
A. “保存” 的离子方程式是
D.含氟牙膏防治龋齿的原理:
B. 作杀菌消毒剂利用了它的强氧化性
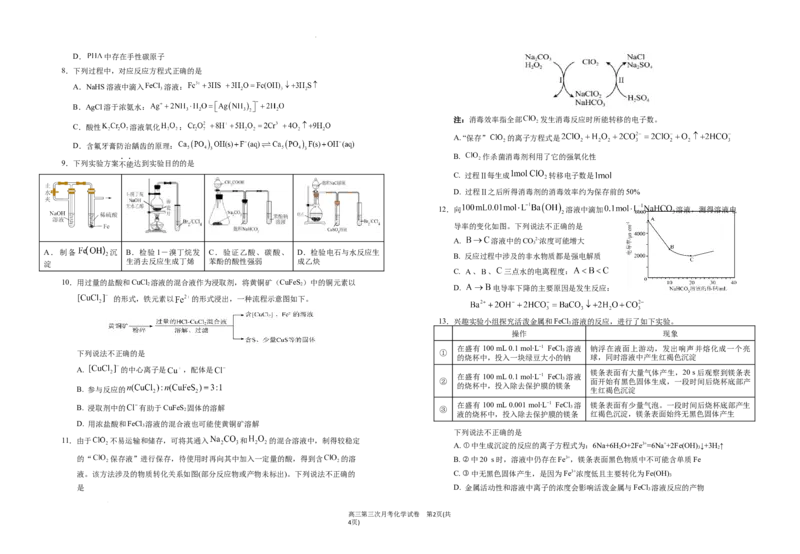
9.下列实验方案不能达到实验目的的是
C. 过程Ⅱ每生成 转移电子数是
D. 过程Ⅱ之后所得消毒剂的消毒效率约为保存前的50%
12.向 溶液中滴加 溶液,测得溶液电
导率的变化如图。下列说法不正确的是
A. 溶液中的CO2-浓度可能增大
3
A.制备 沉 B.检验1-溴丁烷发 C.验证乙酸、碳酸、 D.检验电石与水反应生
B. 反应过程中涉及的非水物质都是强电解质
生消去反应生成丁烯 苯酚的酸性强弱 成乙炔
淀
C. 、 、 三点水的电离程度:
10.用过量的盐酸和CuCl 溶液的混合液作为浸取剂,将黄铜矿(CuFeS)中的铜元素以
2 2
D. 电导率下降的主要原因是发生反应:
的形式,铁元素以 的形式浸出,一种流程示意图如下。
13.兴趣实验小组探究活泼金属和FeCl 溶液的反应,进行了如下实验。
3
操作 现象
在盛有100 mL 0.1 mol∙L−1 FeCl 溶液 钠浮在液面上游动,发出响声并熔化成一个亮
下列说法不正确的是 ① 3
的烧杯中,投入一块绿豆大小的钠 球,同时溶液中产生红褐色沉淀
A. 的中心离子是 ,配体是
镁条表面有大量气体产生,20 s后观察到镁条表
在盛有100 mL 0.1 mol∙L−1 FeCl 溶液
② 3 面开始有黑色固体生成,一段时间后烧杯底部产
的烧杯中,投入除去保护膜的镁条
B. 参与反应的 生红褐色沉淀
在盛有100 mL 0.001 mol∙L−1 FeCl 溶 镁条表面有少量气泡。一段时间后烧杯底部产生
B. 浸取剂中的 有助于CuFeS 2 固体的溶解 ③ 3
液的烧杯中,投入除去保护膜的镁条 红褐色沉淀,镁条表面始终无黑色固体产生
D. 用浓盐酸和FeCl 溶液的混合液也可能使黄铜矿溶解
3
下列说法不正确的是
11.由于 不易运输和储存,可将其通入 和 的混合溶液中,制得较稳定
A. ①中生成沉淀的反应的离子方程式为:6Na+6HO+2Fe3+=6Na++2Fe(OH) ↓+3H ↑
2 3 2
的“ 保存液”进行保存,待使用时再向其中加入一定量的酸,得到含 的溶 B. ②中20 s时,溶液中仍存在Fe3+,镁条表面黑色物质中不可能含单质Fe
液。该方法涉及的物质转化关系如图(部分反应物或产物未标出)。下列说法不正确的 C. ③中无黑色固体产生,是因为Fe3+浓度低且主要转化为Fe(OH)
3
是 D. 金属活动性和溶液中离子的浓度会影响活泼金属与FeCl 溶液反应的产物
3
高三第三次月考化学试卷 第2页(共
学科网(北京)股份有限公司 4页)高三第三次月考化学试卷 第2页(共
4页)
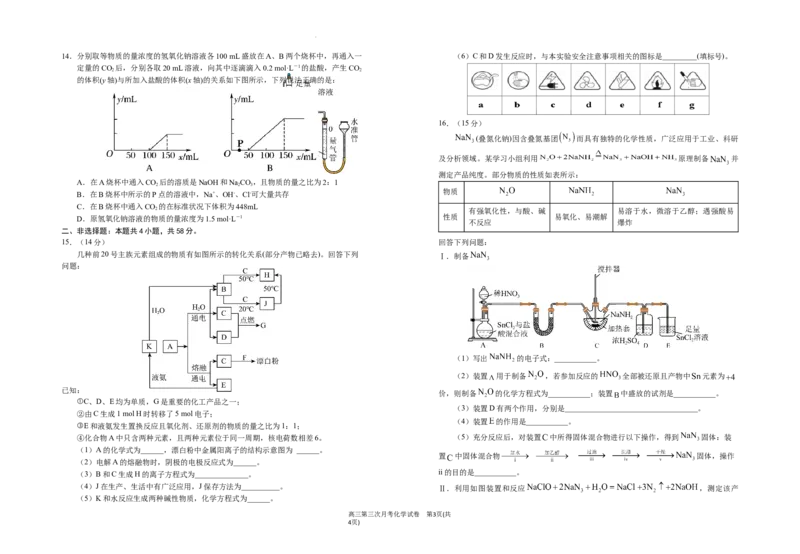
14.分别取等物质的量浓度的氢氧化钠溶液各100 mL盛放在A、B两个烧杯中,再通入一 (6)C和D发生反应时,与本实验安全注意事项相关的图标是_________(填标号)。
定量的CO 后,分别各取20 mL溶液,向其中逐滴滴入0.2 mol·L-1的盐酸,产生CO
2 2
的体积(y轴)与所加入盐酸的体积(x轴)的关系如下图所示,下列说法正确的是:
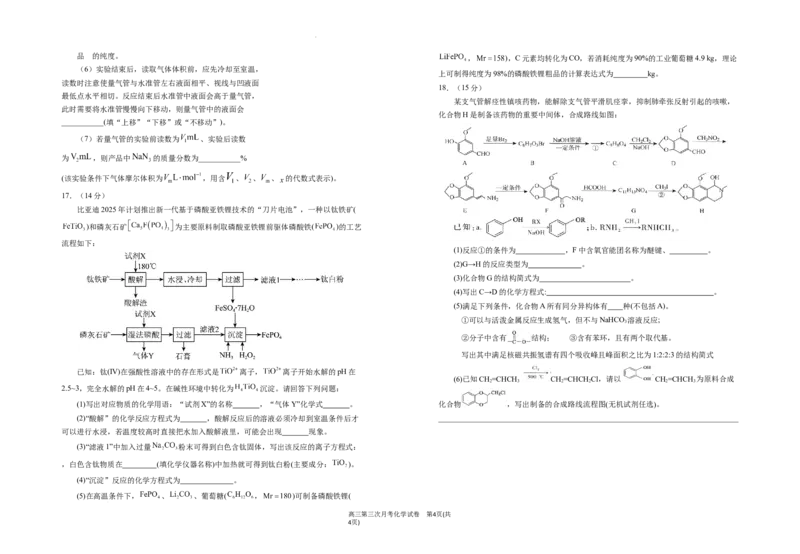
16.(15分)
(叠氮化钠)因含叠氮基团 而具有独特的化学性质,广泛应用于工业、科研
及分析领域。某学习小组利用 原理制备 并
测定产品纯度。部分物质的性质如表所示:
A.在A烧杯中通入CO 后的溶质是NaOH和NaCO,且物质的量之比为2:1
2 2 3
物质
B.在B烧杯中所示的P点的溶液中,Na+、OH-、Cl-可大量共存
C.在B烧杯中通入CO 的在标准状况下体积为448mL
2 有强氧化性,与酸、碱 易溶于水,微溶于乙醇;遇强酸易
D.原氢氧化钠溶液的物质的量浓度为1.5 mol·L-1 性质 易氧化、易潮解
不反应 爆炸
二、非选择题:本题共4小题,共58分。
15.(14分) 回答下列问题:
几种前20号主族元素组成的物质有如图所示的转化关系(部分产物已略去)。回答下列 Ⅰ.制备
问题:
(1)写出 的电子式:___________。
(2)装置 用于制备 ,若参加反应的 全部被还原且产物中 元素为
已知:
价,则制备 的化学方程式为___________;装置 中盛放的试剂是___________。
①C、D、E均为单质,G是重要的化工产品之一;
(3)装置D有两个作用,分别是___________________________________。
②由C生成1 mol H时转移了5 mol电子;
(4)装置 的作用是___________。
③E和液氨发生置换反应且氧化剂、还原剂的物质的量之比为1:1;
④化合物A中只含两种元素,且两种元素位于同一周期,核电荷数相差6。 (5)充分反应后,对装置 中所得固体混合物进行以下操作,得到 固体:装
(1)A的化学式为______,漂白粉中金属阳离子的结构示意图为 ______。
置 中固体混合物 固体,操作
(2)电解A的熔融物时,阴极的电极反应式为______。
(3)B和C生成H的离子方程式为______________。 ii的目的是___________。
(4)J在生产、生活中有广泛应用,J保存方法为__________。 Ⅱ.利用如图装置和反应 ,测定该产
(5)K和水反应生成两种碱性物质,化学方程式为______。
高三第三次月考化学试卷 第3页(共
学科网(北京)股份有限公司 4页)高三第三次月考化学试卷 第3页(共
4页)
品 的纯度。
, ),C元素均转化为CO,若消耗纯度为90%的工业葡萄糖4.9 kg,理论
(6)实验结束后,读取气体体积前,应先冷却至室温,
上可制得纯度为98%的磷酸铁锂粗品的计算表达式为 kg。
读数时注意使量气管与水准管左右液面相平、视线与凹液面
18.(15分)
最低点水平相切。反应结束后水准管中液面会高于量气管,
某支气管解痉性镇咳药物,能解除支气管平滑肌痉挛,抑制肺牵张反射引起的咳嗽,
此时需要将水准管慢慢向下移动,则量气管中的液面会
化合物H是制备该药物的重要中间体,合成路线如图:
___________(填“上移”“下移”或“不移动”)。
(7)若量气管的实验前读数为 、实验后读数
为 ,则产品中 的质量分数为___________%
(该实验条件下气体摩尔体积为 ,用含 、 、 、 的代数式表示)。
17.(14分)
比亚迪2025年计划推出新一代基于磷酸亚铁锂技术的“刀片电池”,一种以钛铁矿(
)和磷灰石矿 为主要原料制取磷酸亚铁锂前驱体磷酸铁( )的工艺
流程如下:
(1)反应①的条件为 ,F中含氧官能团名称为醚键、 。
(2)G→H的反应类型为 。
(3)化合物G的结构简式为 。
(4)写出C→D的化学方程式: 。
(5)满足下列条件,化合物A所有同分异构体有 种(不包括A)。
①可以与活泼金属反应生成氢气,但不与NaHCO 溶液反应;
3
②分子中含有 结构; ③含有苯环,且有两个取代基。
写出其中满足核磁共振氢谱有四个吸收峰且峰面积之比为1:2:2:3的结构简式
已知:钛(IV)在强酸性溶液中的存在形式是 离子, 离子开始水解的pH在
(6)已知CH=CHCH CH=CHCHCl,请以 CH=CHCH 为原料合成
2 3 2 2 2 3
2.5~3,完全水解的pH在4~5。在碱性环境中转化为 沉淀。请回答下列问题:
(1)写出对应物质的化学用语:“试剂X”的名称 ,“气体Y”化学式 。 化合物 ,写出制备的合成路线流程图(无机试剂任选)。
(2)“酸解”的化学反应方程式为 ,酸解反应后的溶液必须冷却到室温条件后才 _______________________________________________________________________________
可以进行水浸,若温度较高时直接把水加入酸解液里,可能会出现 现象。
(3)“滤液1”中加入过量 粉末可得到白色含钛固体,写出该反应的离子方程式:
,白色含钛物质在 (填化学仪器名称)中加热就可得到钛白粉(主要成分: )。
(4)“沉淀”反应的化学方程式为 。
(5)在高温条件下, 、 、葡萄糖( , )可制备磷酸铁锂(
高三第三次月考化学试卷 第4页(共
学科网(北京)股份有限公司 4页)