文档内容
2024 年 1 月“七省联考”考前化学猜想卷
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用
橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 F19 Na 23 Cl 35.5 Mn 55 Fe 56 Cu 64 Ag
108 Cs 133 Ba 137
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1.化学与生产生活、社会发展息息相关,下列说法不正确的是
A.铬是硬度最高的金属,常添加在不锈钢中以增强其耐腐蚀性
B.飞船返回舱表层材料中的玻璃纤维属于天然有机高分子
C.卡塔尔光伏电站实现了将光能转化为电能,用到的材料主要为硅单质
D.在合金中加入适量稀土金属可改善合金的性能,因而稀土元素又被称为“冶金工业的维生素”
2.下列化学用语表达正确的是
A. 用系统命名法命名为3−甲基丁酸
B.空间填充模型 既可以表示甲烷分子,也可以表示四氯化碳分子
C. 分子中,碳原子与氧原子之间形成的共价键类型为 键
D.基态铍原子最外层电子的电子云轮廓图:
3.金粉溶于过氧化氢-浓盐酸可以安全环保的制备氯金酸( ),其化学方程式为
。设 为阿伏加德罗常数的值,下列说法正确的是
A.消耗1molAu,反应转移的电子数为
B.消耗2molHCl生成的 分子数为
C.消耗85g ,产物中形成的配位键数目为
D.2mol液态水中含有的氢键数目为
4.下列叙述对应的离子方程式正确的是
A.向饱和NaOH溶液中通入过量 析出白色晶体:B.白色沉淀CuCl溶于 - 溶液得到深蓝色溶液:
C.向 溶液中滴入酸化的 溶液产生白色沉淀:
D.向 溶液中滴入 溶液产生黑色沉淀和气泡:
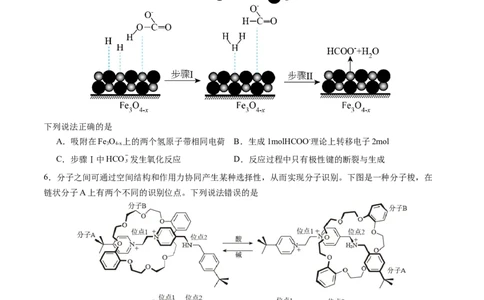
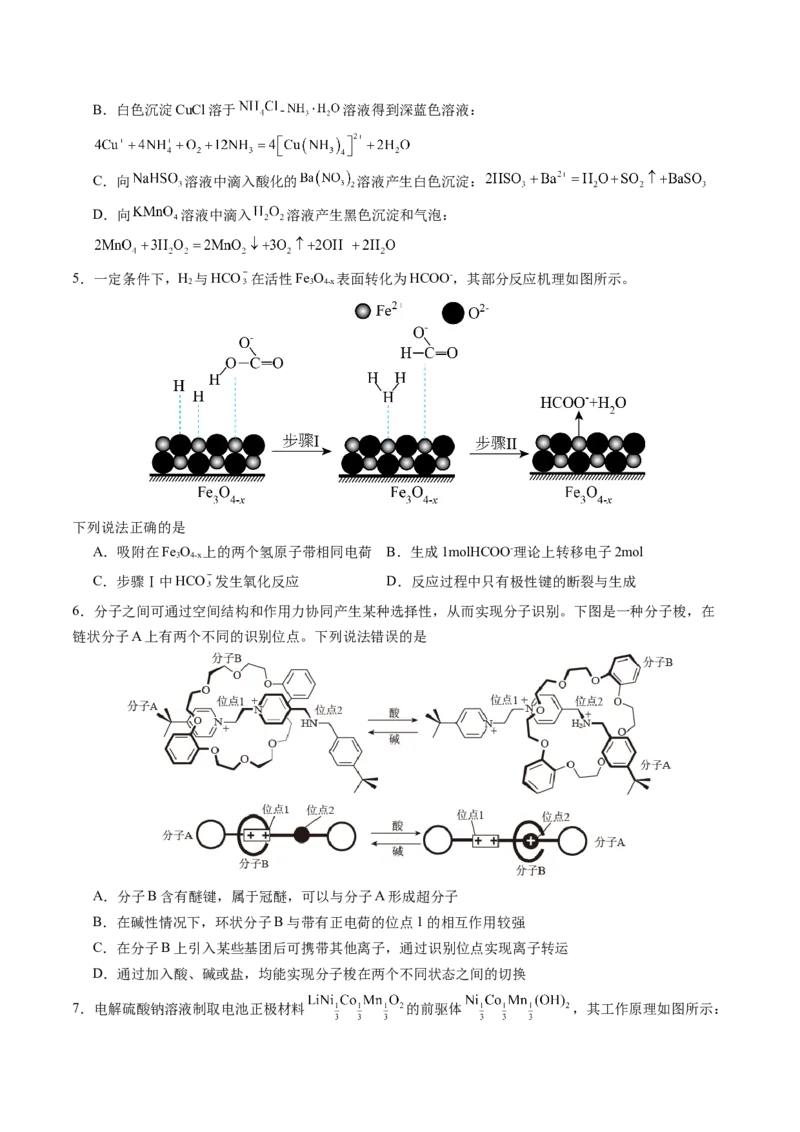
5.一定条件下,H 与HCO 在活性Fe O 表面转化为HCOO-,其部分反应机理如图所示。
2 3 4-x
下列说法正确的是
A.吸附在Fe O 上的两个氢原子带相同电荷 B.生成1molHCOO-理论上转移电子2mol
3 4-x
C.步骤Ⅰ中HCO 发生氧化反应 D.反应过程中只有极性键的断裂与生成
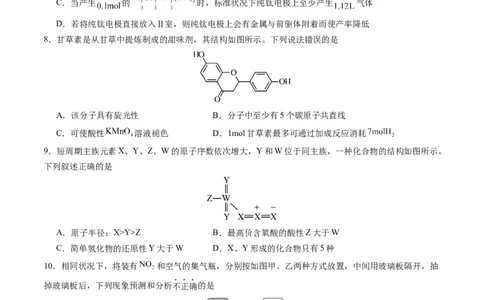
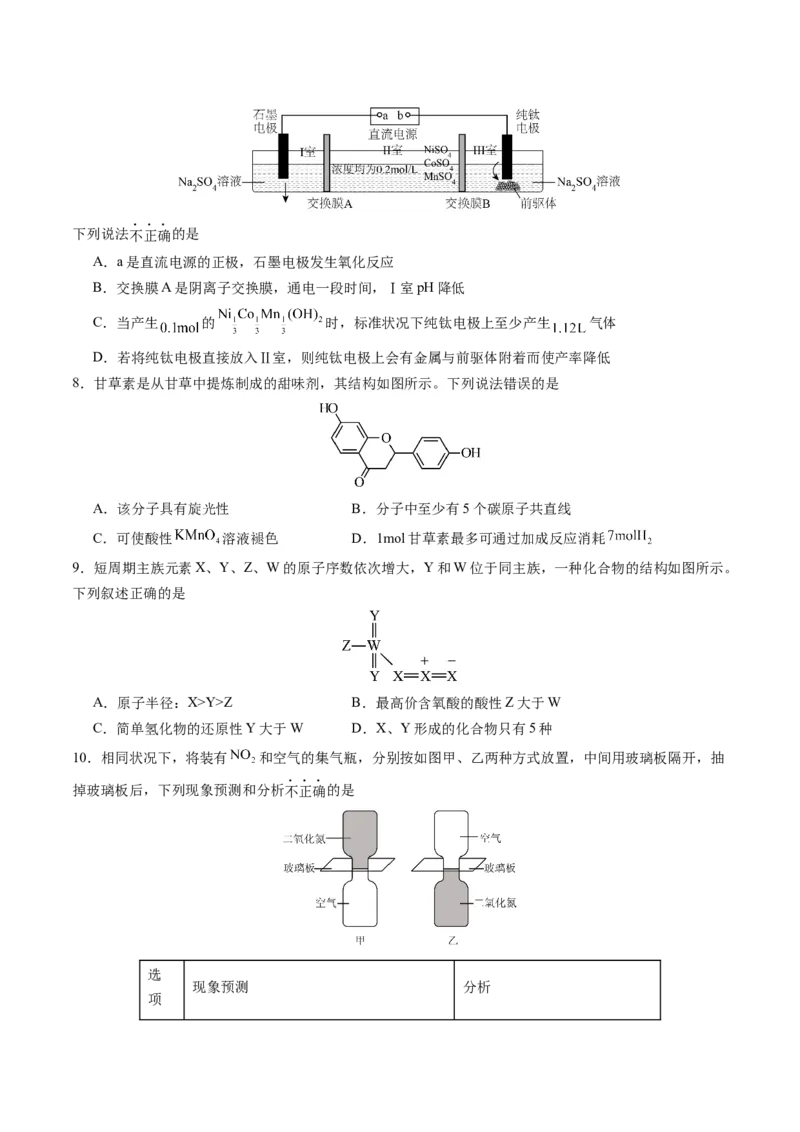
6.分子之间可通过空间结构和作用力协同产生某种选择性,从而实现分子识别。下图是一种分子梭,在
链状分子A上有两个不同的识别位点。下列说法错误的是
A.分子B含有醚键,属于冠醚,可以与分子A形成超分子
B.在碱性情况下,环状分子B与带有正电荷的位点1的相互作用较强
C.在分子B上引入某些基团后可携带其他离子,通过识别位点实现离子转运
D.通过加入酸、碱或盐,均能实现分子梭在两个不同状态之间的切换
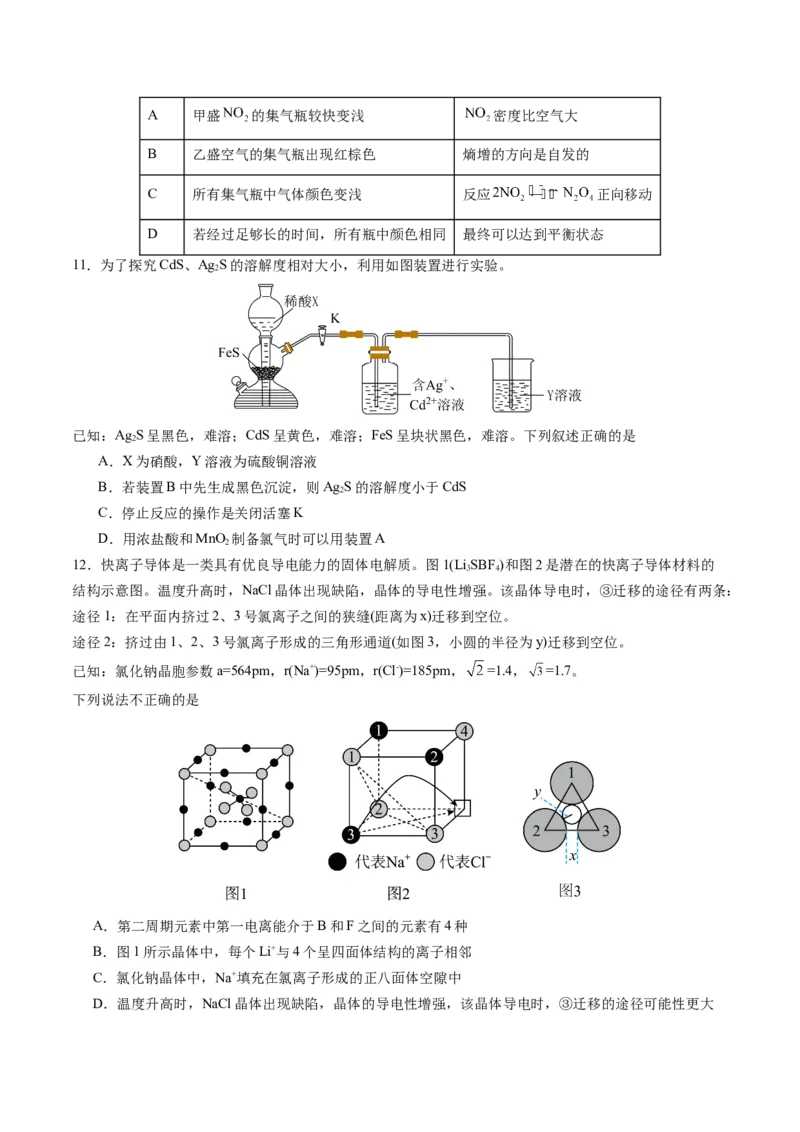
7.电解硫酸钠溶液制取电池正极材料 的前驱体 ,其工作原理如图所示:下列说法不正确的是
A.a是直流电源的正极,石墨电极发生氧化反应
B.交换膜A是阴离子交换膜,通电一段时间,Ⅰ室pH降低
C.当产生 的 时,标准状况下纯钛电极上至少产生 气体
D.若将纯钛电极直接放入Ⅱ室,则纯钛电极上会有金属与前驱体附着而使产率降低
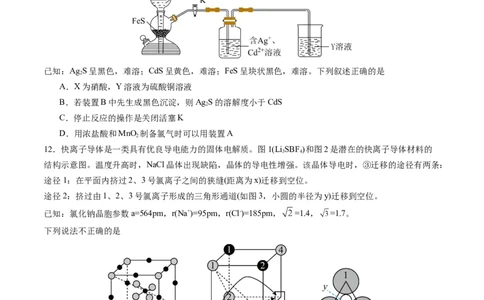
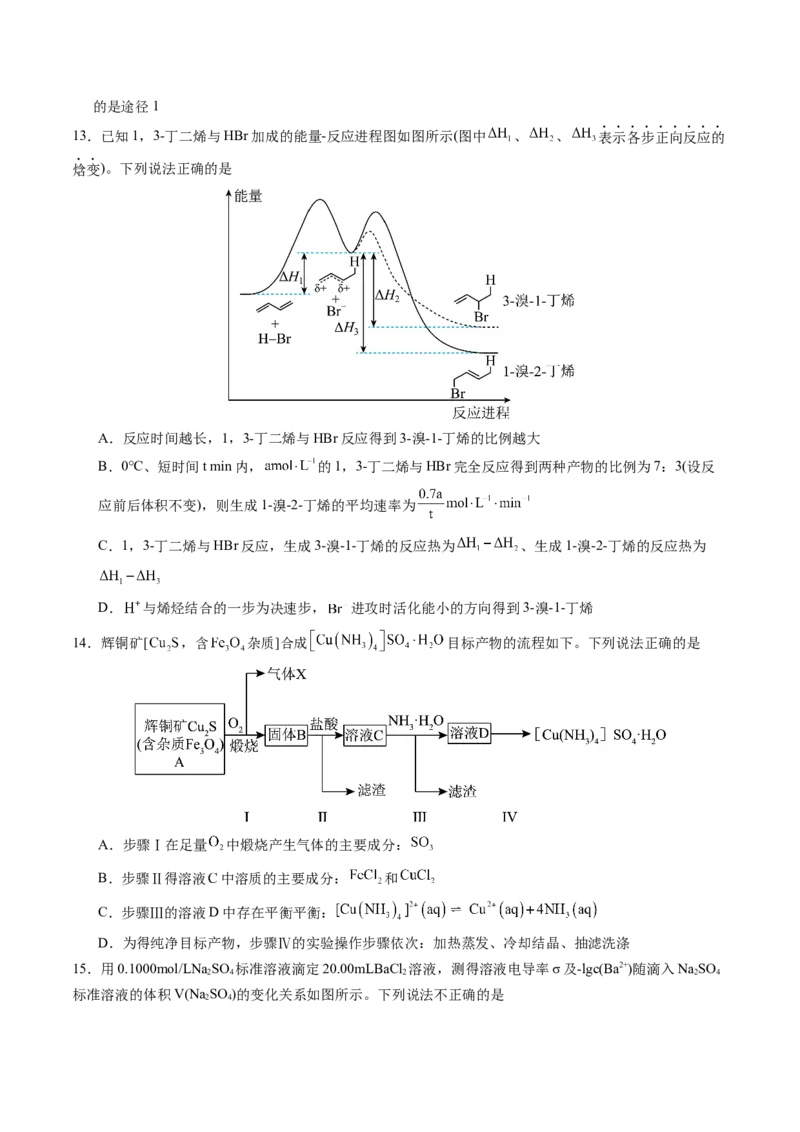
8.甘草素是从甘草中提炼制成的甜味剂,其结构如图所示。下列说法错误的是
A.该分子具有旋光性 B.分子中至少有5个碳原子共直线
C.可使酸性 溶液褪色 D.1mol甘草素最多可通过加成反应消耗
9.短周期主族元素X、Y、Z、W的原子序数依次增大,Y和W位于同主族,一种化合物的结构如图所示。
下列叙述正确的是
A.原子半径:X>Y>Z B.最高价含氧酸的酸性Z大于W
C.简单氢化物的还原性Y大于W D.X、Y形成的化合物只有5种
10.相同状况下,将装有 和空气的集气瓶,分别按如图甲、乙两种方式放置,中间用玻璃板隔开,抽
掉玻璃板后,下列现象预测和分析不正确的是
选
现象预测 分析
项A 甲盛 的集气瓶较快变浅 密度比空气大
B 乙盛空气的集气瓶出现红棕色 熵增的方向是自发的
C 所有集气瓶中气体颜色变浅 反应 正向移动
D 若经过足够长的时间,所有瓶中颜色相同 最终可以达到平衡状态
11.为了探究CdS、Ag S的溶解度相对大小,利用如图装置进行实验。
2
已知:Ag S呈黑色,难溶;CdS呈黄色,难溶;FeS呈块状黑色,难溶。下列叙述正确的是
2
A.X为硝酸,Y溶液为硫酸铜溶液
B.若装置B中先生成黑色沉淀,则Ag S的溶解度小于CdS
2
C.停止反应的操作是关闭活塞K
D.用浓盐酸和MnO 制备氯气时可以用装置A
2
12.快离子导体是一类具有优良导电能力的固体电解质。图1(Li SBF )和图2是潜在的快离子导体材料的
3 4
结构示意图。温度升高时,NaCl晶体出现缺陷,晶体的导电性增强。该晶体导电时,③迁移的途径有两条:
途径1:在平面内挤过2、3号氯离子之间的狭缝(距离为x)迁移到空位。
途径2:挤过由1、2、3号氯离子形成的三角形通道(如图3,小圆的半径为y)迁移到空位。
已知:氯化钠晶胞参数a=564pm,r(Na+)=95pm,r(Cl-)=185pm, =1.4, =1.7。
下列说法不正确的是
A.第二周期元素中第一电离能介于B和F之间的元素有4种
B.图1所示晶体中,每个Li+与4个呈四面体结构的离子相邻
C.氯化钠晶体中,Na+填充在氯离子形成的正八面体空隙中
D.温度升高时,NaCl晶体出现缺陷,晶体的导电性增强,该晶体导电时,③迁移的途径可能性更大的是途径1
13.已知1,3-丁二烯与HBr加成的能量-反应进程图如图所示(图中 、 、 表示各步正向反应的
焓变)。下列说法正确的是
A.反应时间越长,1,3-丁二烯与HBr反应得到3-溴-1-丁烯的比例越大
B.0℃、短时间t min内, 的1,3-丁二烯与HBr完全反应得到两种产物的比例为7:3(设反
应前后体积不变),则生成1-溴-2-丁烯的平均速率为
C.1,3-丁二烯与HBr反应,生成3-溴-1-丁烯的反应热为 、生成1-溴-2-丁烯的反应热为
D. 与烯烃结合的一步为决速步, 进攻时活化能小的方向得到3-溴-1-丁烯
14.辉铜矿[ ,含 杂质]合成 目标产物的流程如下。下列说法正确的是
A.步骤Ⅰ在足量 中煅烧产生气体的主要成分:
B.步骤Ⅱ得溶液 中溶质的主要成分: 和
C.步骤Ⅲ的溶液D中存在平衡平衡:
D.为得纯净目标产物,步骤Ⅳ的实验操作步骤依次:加热蒸发、冷却结晶、抽滤洗涤
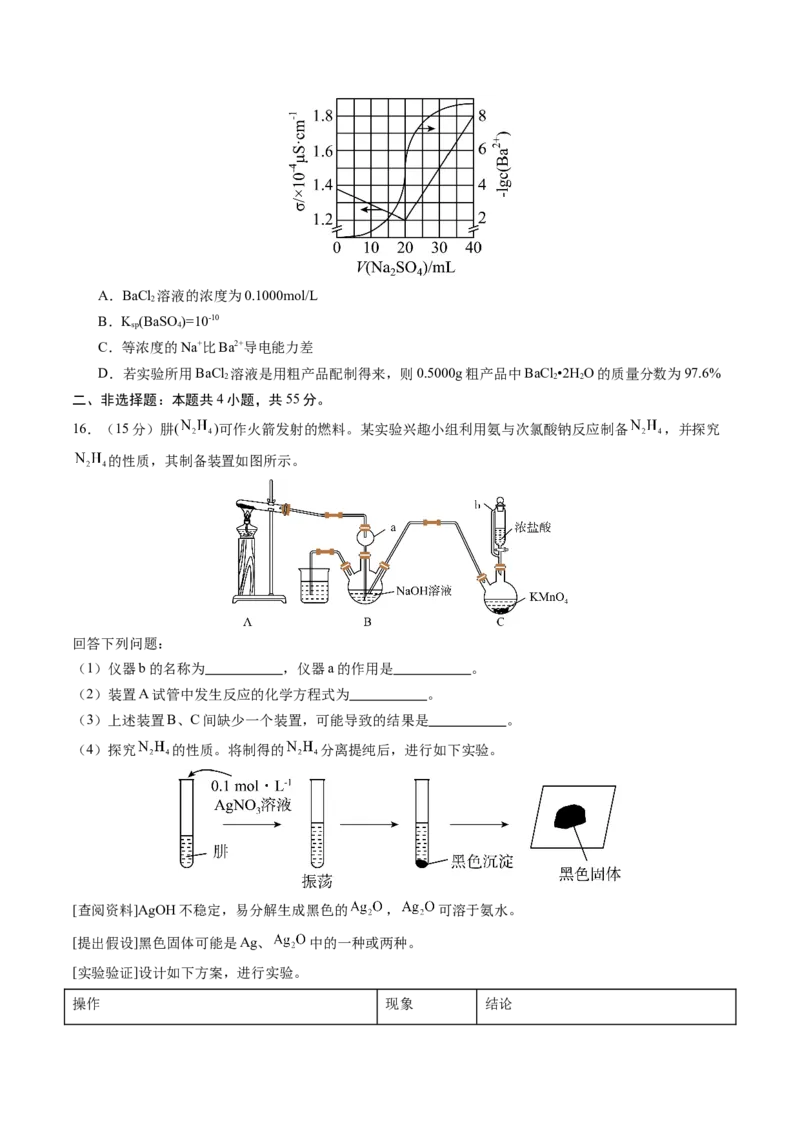
15.用0.1000mol/LNa SO 标准溶液滴定20.00mLBaCl 溶液,测得溶液电导率σ及-lgc(Ba2+)随滴入NaSO
2 4 2 2 4
标准溶液的体积V(Na SO )的变化关系如图所示。下列说法不正确的是
2 4A.BaCl 溶液的浓度为0.1000mol/L
2
B.K (BaSO)=10-10
sp 4
C.等浓度的Na+比Ba2+导电能力差
D.若实验所用BaCl 溶液是用粗产品配制得来,则0.5000g粗产品中BaCl •2H O的质量分数为97.6%
2 2 2
二、非选择题:本题共4小题,共55分。
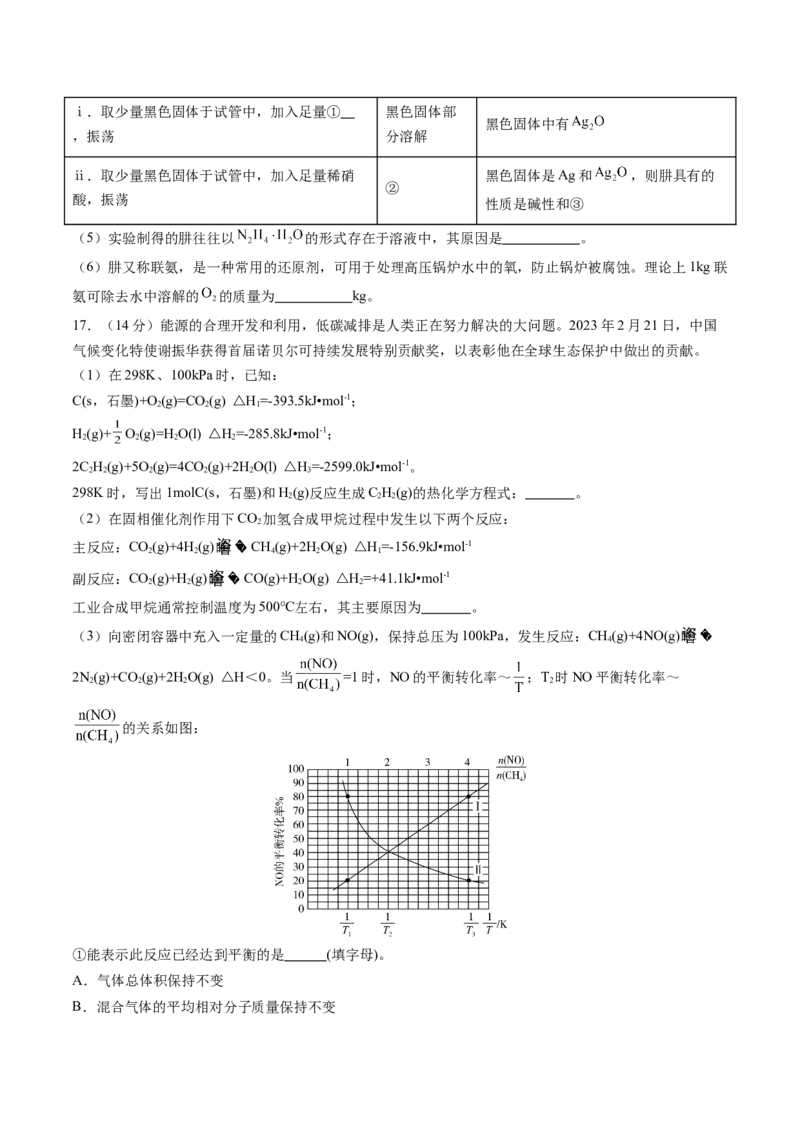
16.(15分)肼( )可作火箭发射的燃料。某实验兴趣小组利用氨与次氯酸钠反应制备 ,并探究
的性质,其制备装置如图所示。
回答下列问题:
(1)仪器b的名称为 ,仪器a的作用是 。
(2)装置A试管中发生反应的化学方程式为 。
(3)上述装置B、C间缺少一个装置,可能导致的结果是 。
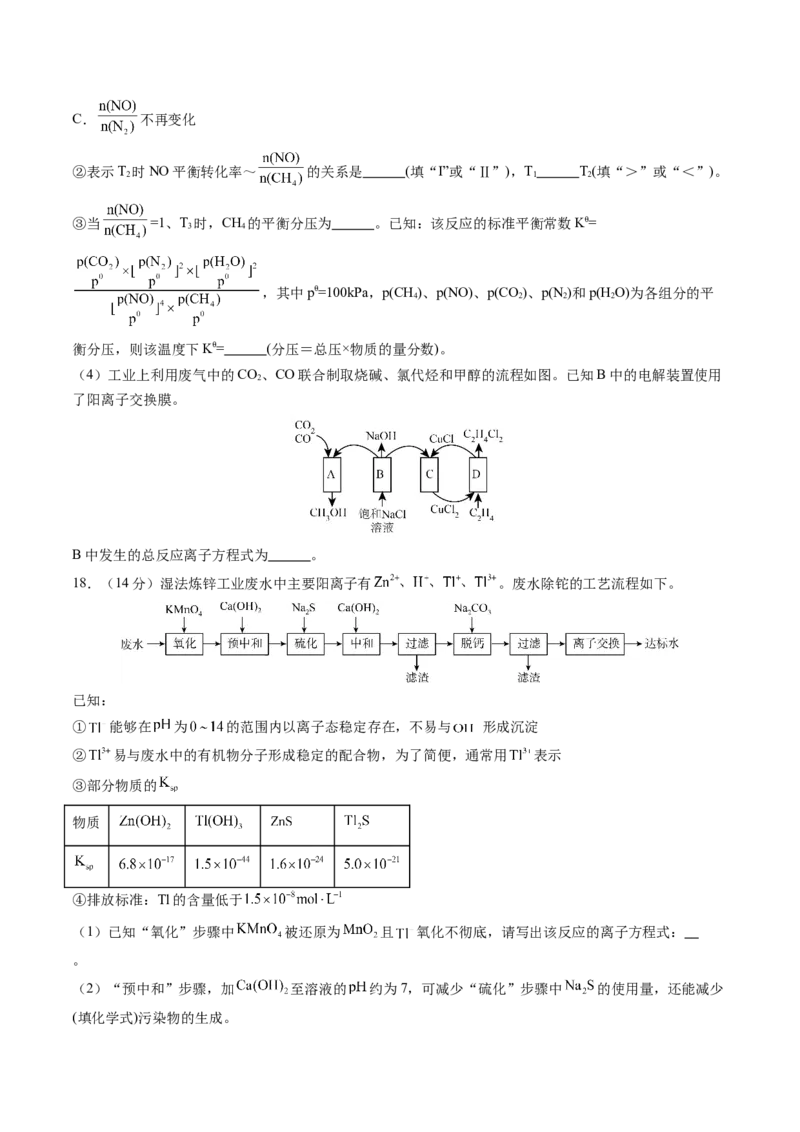
(4)探究 的性质。将制得的 分离提纯后,进行如下实验。
[查阅资料]AgOH不稳定,易分解生成黑色的 , 可溶于氨水。
[提出假设]黑色固体可能是Ag、 中的一种或两种。
[实验验证]设计如下方案,进行实验。
操作 现象 结论ⅰ.取少量黑色固体于试管中,加入足量① 黑色固体部
黑色固体中有
,振荡 分溶解
ⅱ.取少量黑色固体于试管中,加入足量稀硝 黑色固体是Ag和 ,则肼具有的
②
酸,振荡 性质是碱性和③
(5)实验制得的肼往往以 的形式存在于溶液中,其原因是 。
(6)肼又称联氨,是一种常用的还原剂,可用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论上1kg联
氨可除去水中溶解的 的质量为 kg。
17.(14分)能源的合理开发和利用,低碳减排是人类正在努力解决的大问题。2023年2月21日,中国
气候变化特使谢振华获得首届诺贝尔可持续发展特别贡献奖,以表彰他在全球生态保护中做出的贡献。
(1)在298K、100kPa时,已知:
C(s,石墨)+O (g)=CO (g) △H=-393.5kJ•mol-1;
2 2 1
H(g)+ O(g)=HO(l) △H=-285.8kJ•mol-1;
2 2 2 2
2C H(g)+5O(g)=4CO (g)+2HO(l) △H=-2599.0kJ•mol-1。
2 2 2 2 2 3
298K时,写出1molC(s,石墨)和H(g)反应生成C H(g)的热化学方程式: 。
2 2 2
(2)在固相催化剂作用下CO 加氢合成甲烷过程中发生以下两个反应:
2
主反应:CO(g)+4H(g) CH(g)+2HO(g) △H=-156.9kJ•mol-1
2 2 4 2 1
副反应:CO(g)+H(g) CO(g)+HO(g) △H=+41.1kJ•mol-1
2 2 2 2
工业合成甲烷通常控制温度为500℃左右,其主要原因为 。
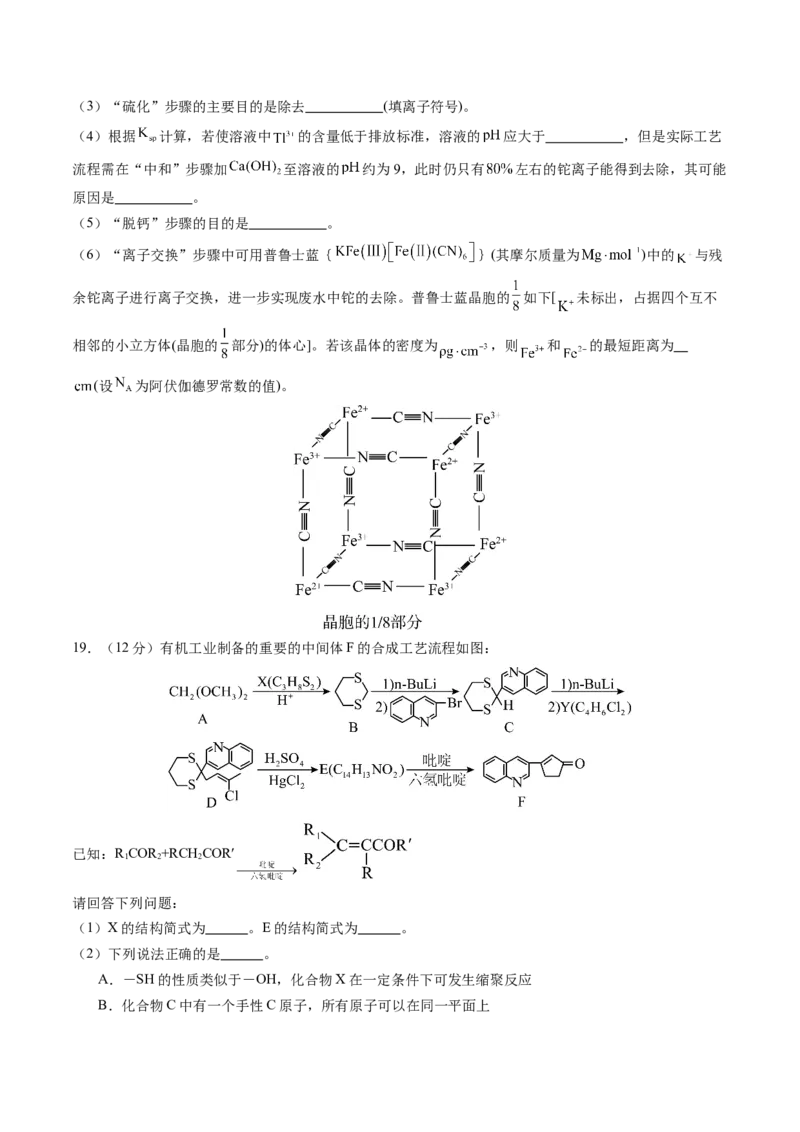
(3)向密闭容器中充入一定量的CH(g)和NO(g),保持总压为100kPa,发生反应:CH(g)+4NO(g)
4 4
2N(g)+CO (g)+2HO(g) △H<0。当 =1时,NO的平衡转化率~ ;T 时NO平衡转化率~
2 2 2 2
的关系如图:
①能表示此反应已经达到平衡的是 (填字母)。
A.气体总体积保持不变
B.混合气体的平均相对分子质量保持不变C. 不再变化
②表示T 时NO平衡转化率~ 的关系是 (填“I”或“Ⅱ”),T T(填“>”或“<”)。
2 1 2
③当 =1、T 时,CH 的平衡分压为 。已知:该反应的标准平衡常数Kθ=
3 4
,其中pθ=100kPa,p(CH)、p(NO)、p(CO)、p(N )和p(H O)为各组分的平
4 2 2 2
衡分压,则该温度下Kθ= (分压=总压×物质的量分数)。
(4)工业上利用废气中的CO、CO联合制取烧碱、氯代烃和甲醇的流程如图。已知B中的电解装置使用
2
了阳离子交换膜。
B中发生的总反应离子方程式为 。
18.(14分)湿法炼锌工业废水中主要阳离子有 。废水除铊的工艺流程如下。
已知:
① 能够在 为 的范围内以离子态稳定存在,不易与 形成沉淀
② 易与废水中的有机物分子形成稳定的配合物,为了简便,通常用 表示
③部分物质的
物质
④排放标准:Tl的含量低于
(1)已知“氧化”步骤中 被还原为 且 氧化不彻底,请写出该反应的离子方程式:
。
(2)“预中和”步骤,加 至溶液的 约为7,可减少“硫化”步骤中 的使用量,还能减少
(填化学式)污染物的生成。(3)“硫化”步骤的主要目的是除去 (填离子符号)。
(4)根据 计算,若使溶液中 的含量低于排放标准,溶液的 应大于 ,但是实际工艺
流程需在“中和”步骤加 至溶液的 约为9,此时仍只有 左右的铊离子能得到去除,其可能
原因是 。
(5)“脱钙”步骤的目的是 。
(6)“离子交换”步骤中可用普鲁士蓝{ }(其摩尔质量为 )中的 与残
余铊离子进行离子交换,进一步实现废水中铊的去除。普鲁士蓝晶胞的 如下[ 未标出,占据四个互不
相邻的小立方体(晶胞的 部分)的体心]。若该晶体的密度为 ,则 和 的最短距离为
(设 为阿伏伽德罗常数的值)。
19.(12分)有机工业制备的重要的中间体F的合成工艺流程如图:
已知:R COR +RCH COR′
1 2 2
请回答下列问题:
(1)X的结构简式为 。E的结构简式为 。
(2)下列说法正确的是 。
A.-SH的性质类似于-OH,化合物X在一定条件下可发生缩聚反应
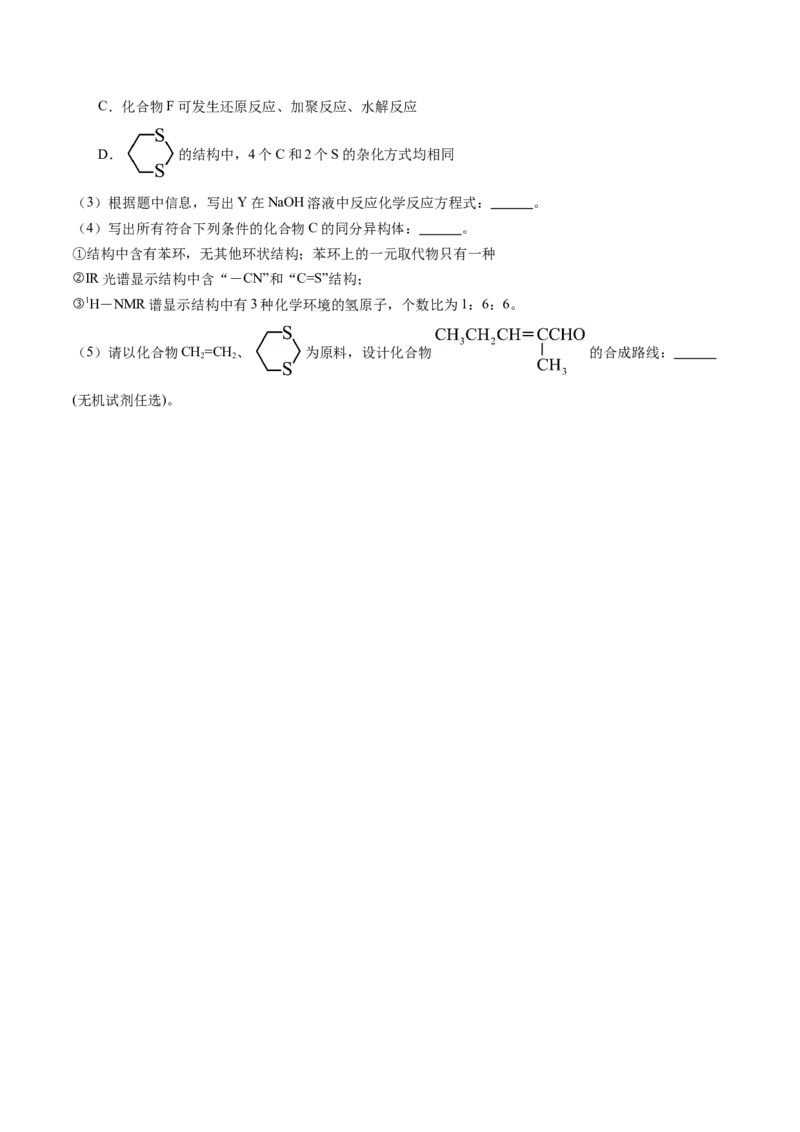
B.化合物C中有一个手性C原子,所有原子可以在同一平面上C.化合物F可发生还原反应、加聚反应、水解反应
D. 的结构中,4个C和2个S的杂化方式均相同
(3)根据题中信息,写出Y在NaOH溶液中反应化学反应方程式: 。
(4)写出所有符合下列条件的化合物C的同分异构体: 。
①结构中含有苯环,无其他环状结构;苯环上的一元取代物只有一种
②IR光谱显示结构中含“-CN”和“C=S”结构;
③1H-NMR谱显示结构中有3种化学环境的氢原子,个数比为1:6:6。
(5)请以化合物CH=CH 、 为原料,设计化合物 的合成路线:
2 2
(无机试剂任选)。