文档内容
衡阳市八中 2024 届高三第五次月考
化学试题
注意事项:本试卷满分为100分,时量为75分钟
可能用到的相对原子质量:H-1 C-12 O-16 Mn-55
一、选择题(本题共14小题,每小题3分,共42分)
1.化学与科技、生活有密切的关系。下列叙述正确的是( )
A.第三代核电“华龙一号”落户福建,核反应属于化学反应
B.城市内的光化学烟雾污染与氮、碳及硫的氧化物都有关
C.“84”消毒液沾到皮肤上应立即用大量水清洗,并涂抹维生素C
D.运动员“战袍”内层添加石墨烯片用于保暖,石墨烯和碳纳米管互为同位素
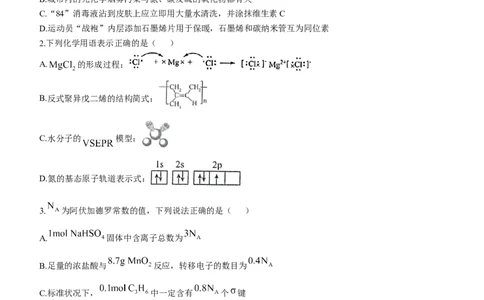
2.下列化学用语表示正确的是( )
A. 的形成过程:
B.反式聚异戊二烯的结构简式:
C.水分子的 模型:
D.氮的基态原子轨道表示式:
3. 为阿伏加德罗常数的值,下列说法正确的是( )
A. 固体中含离子总数为
B.足量的浓盐酸与 反应,转移电子的数目为
C.标准状况下, 中一定含有 个 键
D.将 固体完全溶于水,溶液中阴离子的数目大于
4.用化学沉淀法去除粗盐中杂质离子( 、 、 )的实验中,不需要用到的实验装置是( )A. B. C. D.
5.已知反应: ,该反应可用于提纯炔烃。下列
说法不正确的是( )
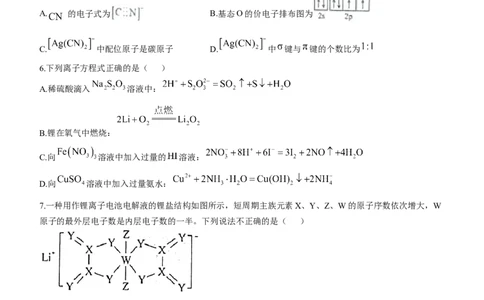
A. 的电子式为 B.基态O的价电子排布图为
C. 中配位原子是碳原子 D. 中 键与 键的个数比为
6.下列离子方程式正确的是( )
A.稀硫酸滴入 溶液中:
B.锂在氧气中燃烧:
C.向 溶液中加入过量的 溶液:
D.向 溶液中加入过量氨水:
7.一种用作锂离子电池电解液的锂盐结构如图所示,短周期主族元素X、Y、Z、W的原子序数依次增大,W
原子的最外层电子数是内层电子数的一半。下列说法不正确的是( )
A.简单氢化物的沸点: B. 中, 的化合价为
C.原子半径: D.W的最高价氧化物对应的水化物是中强酸
8.下列表格中的实验操作、现象和结论均正确且具有对应关系的是( )
选项 实验操作 现象 结论
将红热的炭放入浓硫酸中产生的气体通入澄清的
A 石灰水变浑浊
石灰水 炭被氧化成
原溶液中一定不含有
向某溶液中滴加 溶液,再将湿润的红色石
B 试纸不变蓝
蕊试纸放在反应容器口取涂改液与 溶液混合加热充分反应,取上层 涂改液中存在含氯化合
C 出现白色沉淀
清液,先加硝酸酸化,再加入硝酸银溶液 物
D 用玻璃棒蘸取某溶液置于酒精灯的外焰中灼烧 火焰呈黄色 该溶液中含有 元素
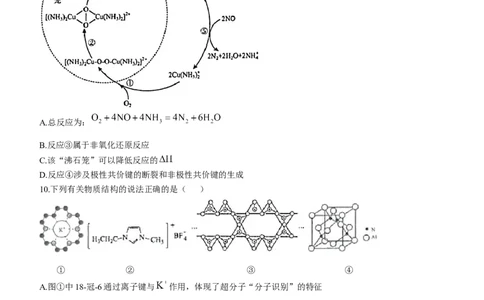
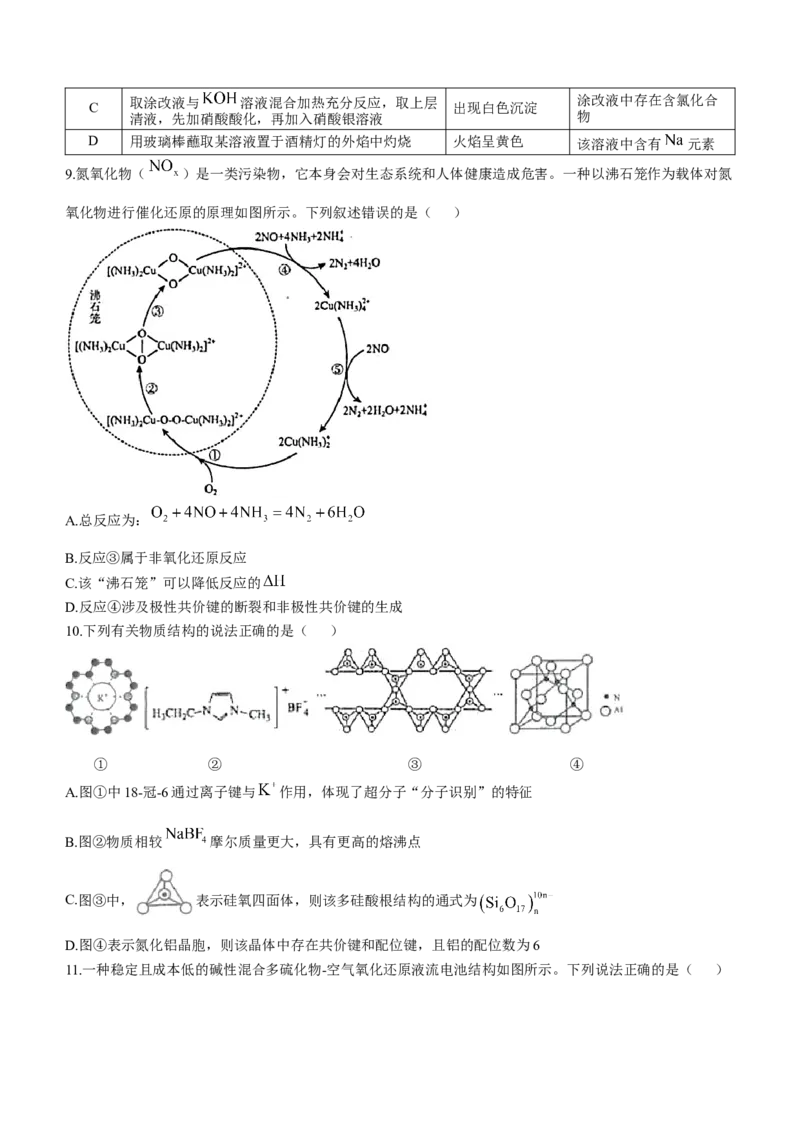
9.氮氧化物( )是一类污染物,它本身会对生态系统和人体健康造成危害。一种以沸石笼作为载体对氮
氧化物进行催化还原的原理如图所示。下列叙述错误的是( )
A.总反应为:
B.反应③属于非氧化还原反应
C.该“沸石笼”可以降低反应的
D.反应④涉及极性共价键的断裂和非极性共价键的生成
10.下列有关物质结构的说法正确的是( )
① ② ③ ④
A.图①中18-冠-6通过离子键与 作用,体现了超分子“分子识别”的特征
B.图②物质相较 摩尔质量更大,具有更高的熔沸点
C.图③中, 表示硅氧四面体,则该多硅酸根结构的通式为
D.图④表示氮化铝晶胞,则该晶体中存在共价键和配位键,且铝的配位数为6
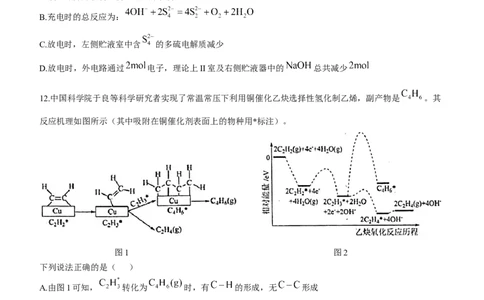
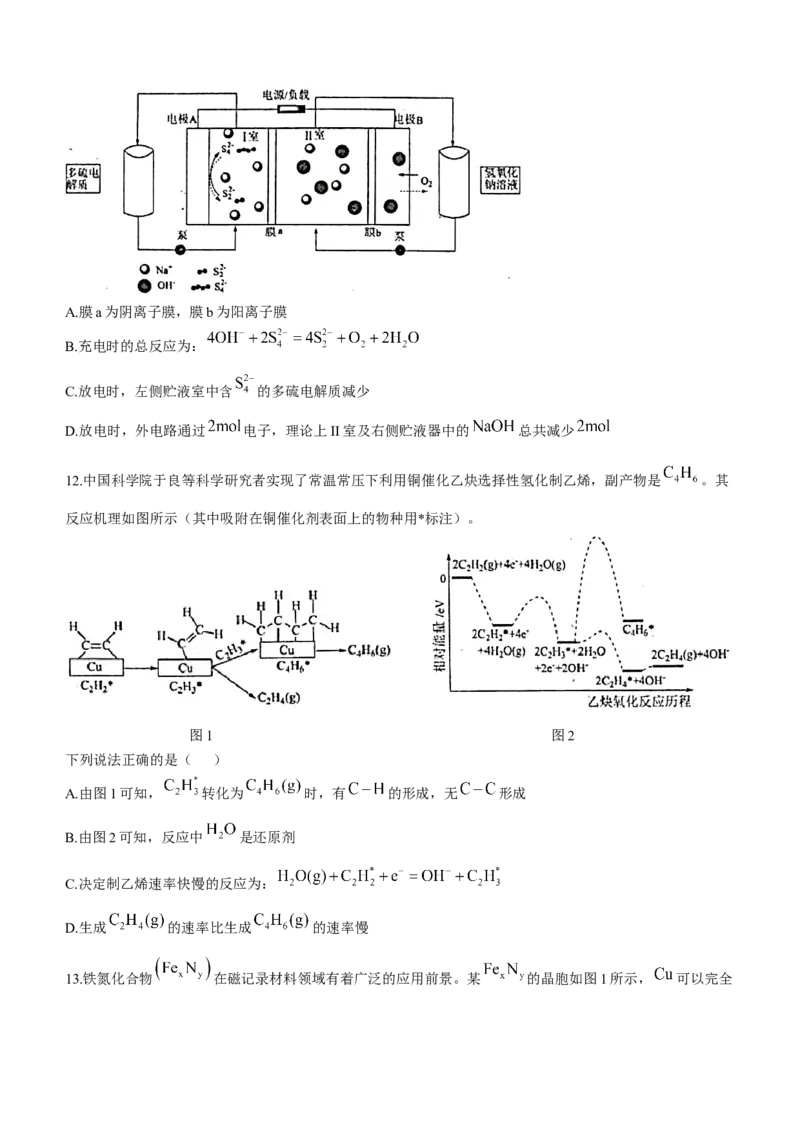
11.一种稳定且成本低的碱性混合多硫化物-空气氧化还原液流电池结构如图所示。下列说法正确的是( )A.膜a为阴离子膜,膜b为阳离子膜
B.充电时的总反应为:
C.放电时,左侧贮液室中含 的多硫电解质减少
D.放电时,外电路通过 电子,理论上II室及右侧贮液器中的 总共减少
12.中国科学院于良等科学研究者实现了常温常压下利用铜催化乙炔选择性氢化制乙烯,副产物是 。其
反应机理如图所示(其中吸附在铜催化剂表面上的物种用*标注)。
图1 图2
下列说法正确的是( )
A.由图1可知, 转化为 时,有 的形成,无 形成
B.由图2可知,反应中 是还原剂
C.决定制乙烯速率快慢的反应为:
D.生成 的速率比生成 的速率慢
13.铁氮化合物 在磁记录材料领域有着广泛的应用前景。某 的晶胞如图1所示, 可以完全替代该晶体中a位置 或者b位置 ,形成 替代型产物 。 转化为两种 替代型
产物的能量变化如图2所示,下列有关说法不正确的是( )
图1 图2
A. 元素位于元素周期表中的 区
B.图1中氮原子的配位数为6
C.更稳定的 替代型产物的化学式为
D.当a位置 位于体心时,b位置 位于棱上
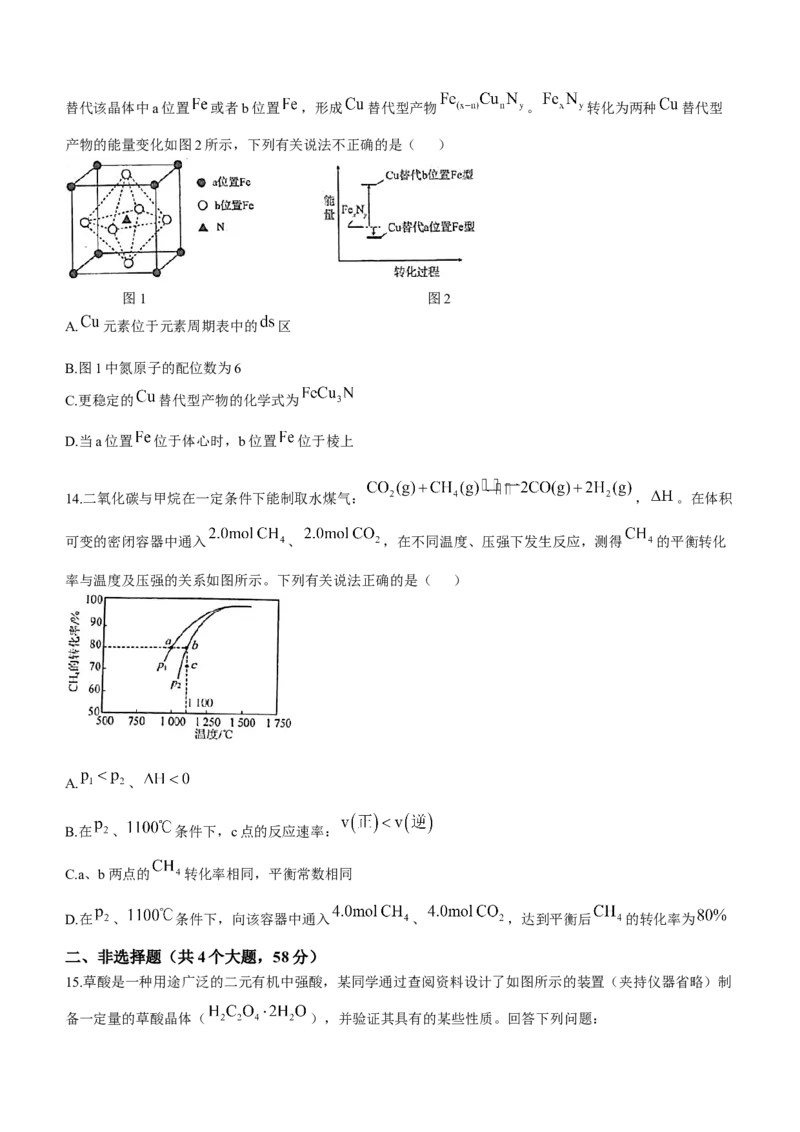
14.二氧化碳与甲烷在一定条件下能制取水煤气: , 。在体积
可变的密闭容器中通入 、 ,在不同温度、压强下发生反应,测得 的平衡转化
率与温度及压强的关系如图所示。下列有关说法正确的是( )
A. 、
B.在 、 条件下,c点的反应速率:
C.a、b两点的 转化率相同,平衡常数相同
D.在 、 条件下,向该容器中通入 、 ,达到平衡后 的转化率为
二、非选择题(共4个大题,58分)
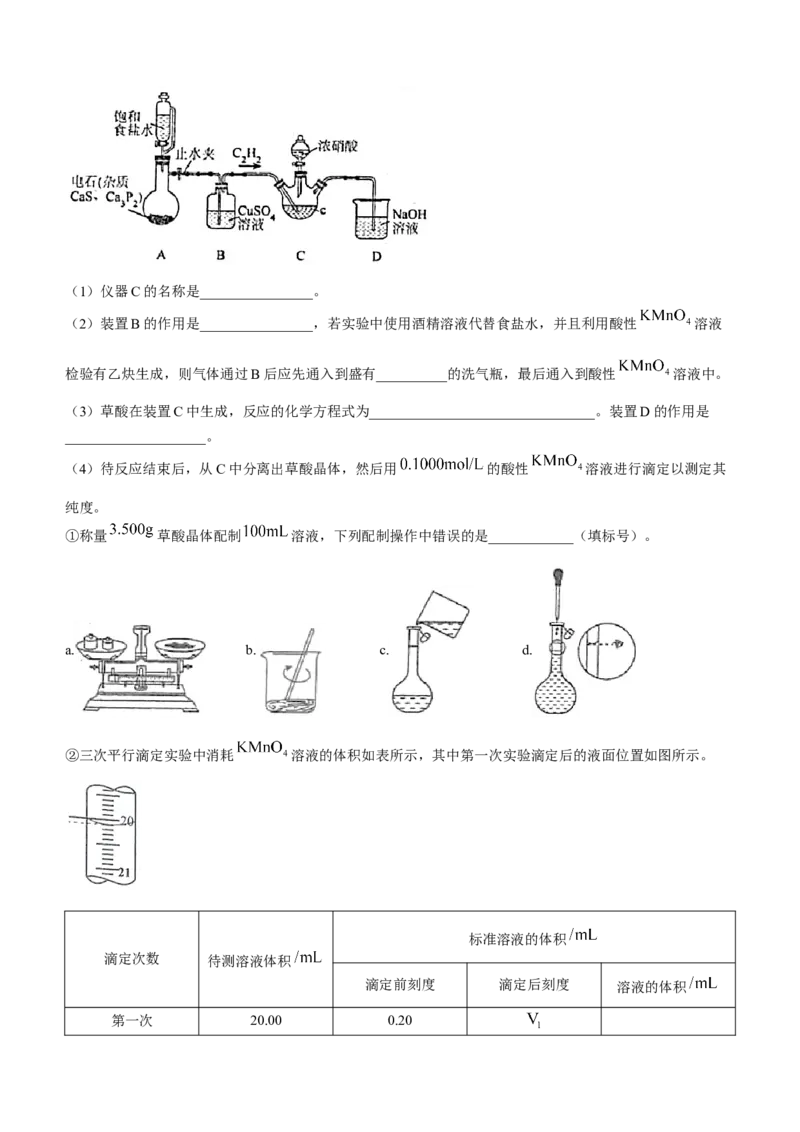
15.草酸是一种用途广泛的二元有机中强酸,某同学通过查阅资料设计了如图所示的装置(夹持仪器省略)制
备一定量的草酸晶体( ),并验证其具有的某些性质。回答下列问题:(1)仪器C的名称是________________。
(2)装置B的作用是________________,若实验中使用酒精溶液代替食盐水,并且利用酸性 溶液
检验有乙炔生成,则气体通过B后应先通入到盛有__________的洗气瓶,最后通入到酸性 溶液中。
(3)草酸在装置C中生成,反应的化学方程式为________________________________。装置D的作用是
____________________。
(4)待反应结束后,从C中分离出草酸晶体,然后用 的酸性 溶液进行滴定以测定其
纯度。
①称量 草酸晶体配制 溶液,下列配制操作中错误的是____________(填标号)。
a. b. c. d.
②三次平行滴定实验中消耗 溶液的体积如表所示,其中第一次实验滴定后的液面位置如图所示。
标准溶液的体积
滴定次数 待测溶液体积
滴定前刻度 滴定后刻度 溶液的体积
第一次 20.00 0.20第二次 20.00 2.56 28.40
第三次 20.00 0.22 20.32
则 __________ ,样品中草酸晶体的质量分数为_______________ (保留一位小数)。
16.从衣食住行到探索浩瀚宇宙,都有氮及其化合物的参与,但同时有毒含氮化合物的排放,也对环境产生污
染。如何实现环境保护与资源利用的和谐统一,已成为我们的重要研究课题。
(1)工业上利用 和 可以合成 , 又可以进一步制备火箭燃料肼 。已知:
①
②
③
写出气态肼在气态四氧化二氮中燃烧生成氮气和气态水的热化学方程式:____________________________。
(2) 的水溶液呈弱碱性,室温下其电离常数 ,则 的 水溶液 等
于______________(忽略 的二级电离和 的电离, )。
(3)利用测压法在刚性密闭容器中研究 时 的分解反应,现将一定量
的 充入该密闭容器中,测得体系的总压强随时间的变化如表所示:
反应时间/min 0 10 20 30 40
压强 15.00 14.02 13.20 12.50 12.50
① 时, _______________ 。
② 时 反应的平衡常数 ________________( 为以物质的量分数
表示的平衡常数)。若升高温度, 减小,则 ___________0(填“大于”“小于”或“等于”)。
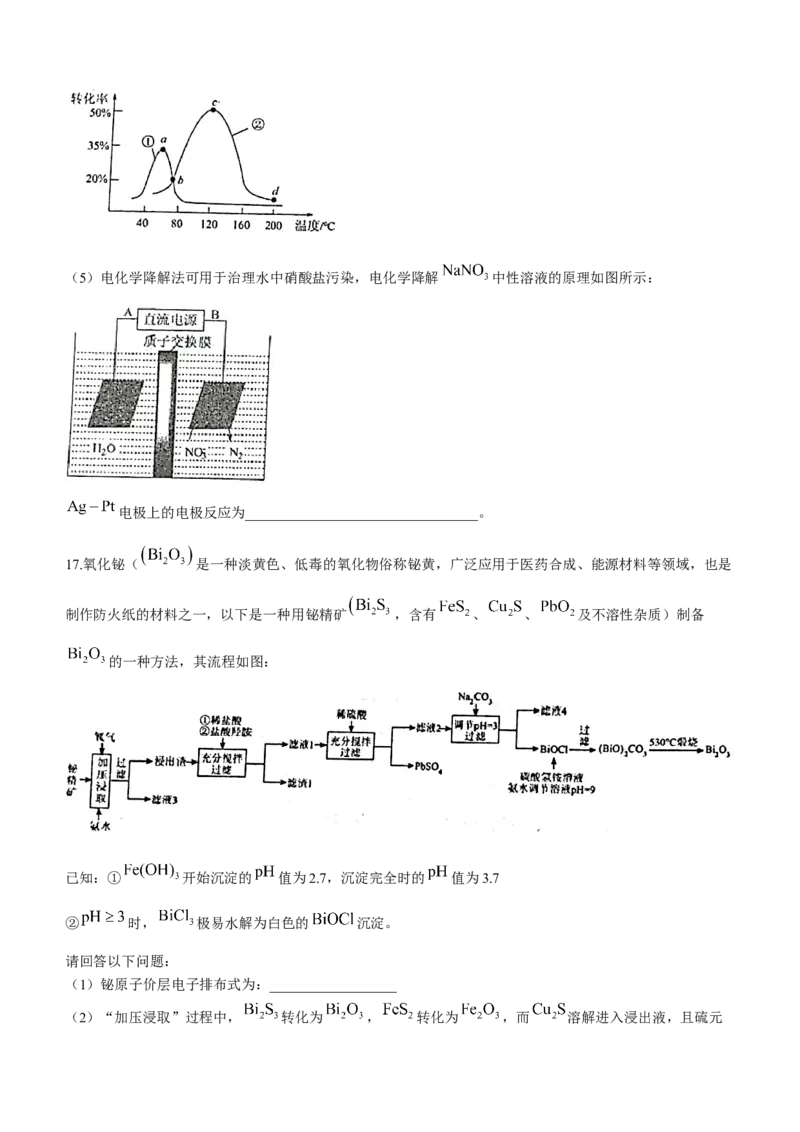
(4)将等物质的量的 和 分别充入盛有催化剂①和②的体积相同的刚性容器,进行反应
,经过相同时间测得 的转化率如图所示,图中cd
段转化率下降的可能原因是__________________________。(5)电化学降解法可用于治理水中硝酸盐污染,电化学降解 中性溶液的原理如图所示:
电极上的电极反应为_________________________________。
17.氧化铋( 是一种淡黄色、低毒的氧化物俗称铋黄,广泛应用于医药合成、能源材料等领域,也是
制作防火纸的材料之一,以下是一种用铋精矿 ,含有 、 、 及不溶性杂质)制备
的一种方法,其流程如图:
已知:① 开始沉淀的 值为2.7,沉淀完全时的 值为3.7
② 时, 极易水解为白色的 沉淀。
请回答以下问题:
(1)铋原子价层电子排布式为:__________________
(2)“加压浸取”过程中, 转化为 , 转化为 ,而 溶解进入浸出液,且硫元素转化为 ,请写出 在此过程中发生反应的离子方程式:____________________________________。
(3)实验室灼烧 时用到的硅酸盐制品有____________、____________、酒精灯、玻璃棒。
(4)根据流程分析,盐酸羟胺 在流程中的作用是:①______________;②______________。
(5)流程中生成 的化学方程式为:____________________________________。
(6)实际生产过程中温度保持在 左右 产率较高,请分析温度过低或过高时 产
率较低的原因______________________________________。
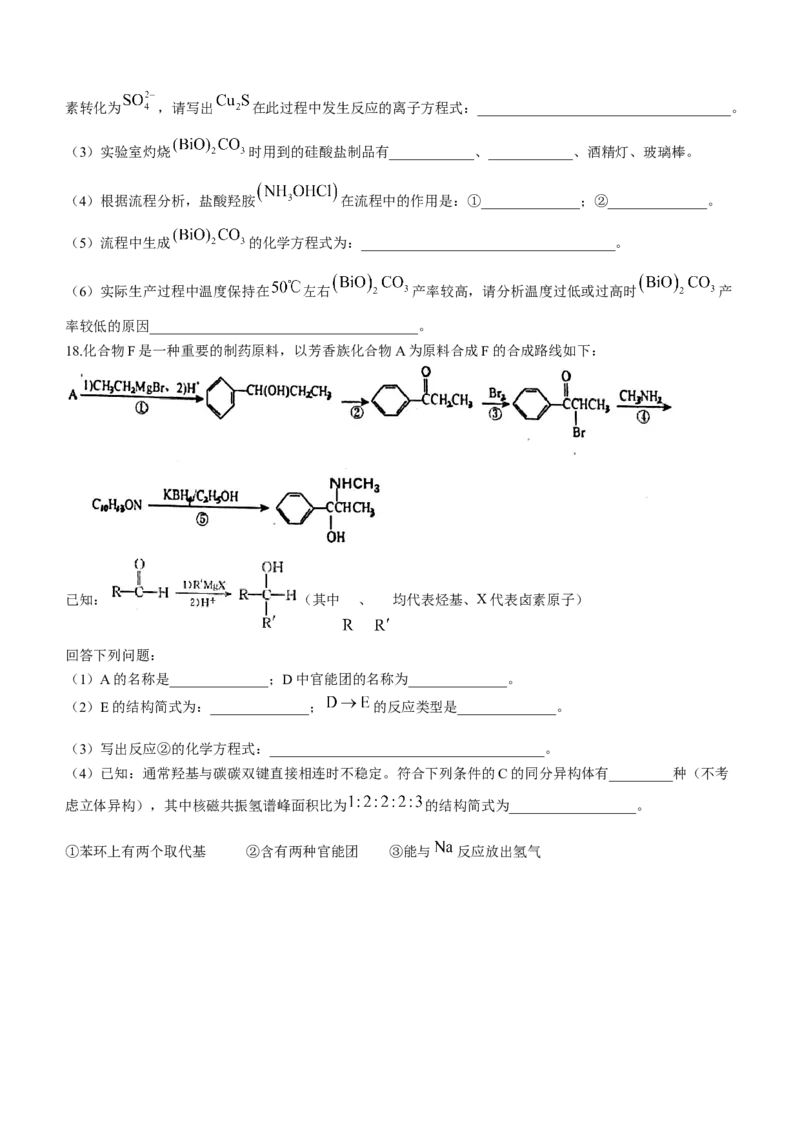
18.化合物F是一种重要的制药原料,以芳香族化合物A为原料合成F的合成路线如下:
已知: (其中 、 均代表烃基、X代表卤素原子)
回答下列问题:
(1)A的名称是______________;D中官能团的名称为______________。
(2)E的结构简式为:______________; 的反应类型是______________。
(3)写出反应②的化学方程式:_______________________________________。
(4)已知:通常羟基与碳碳双键直接相连时不稳定。符合下列条件的C的同分异构体有_________种(不考
虑立体异构),其中核磁共振氢谱峰面积比为 的结构简式为__________________。
①苯环上有两个取代基 ②含有两种官能团 ③能与 反应放出氢气