文档内容
1
雅礼中学 2025 届高三月考试卷(四)
化 学
时量:75分钟 满分:100分
可能用到的相对原子质量:H~1 C~12 O~16 S~32 Fe~56 Cu~64 Ba~137
第Ⅰ卷(选择题 共42分)
一、选择题(本题共14小题,每小题3分,共42分,每小题只有一个选项符合题意。)
1.中国传统文化对人类文明贡献巨大,我国古代人民在那时候就已经广泛应用化学知识,书中充分
记载了古代化学研究成果。下列关于古代化学的应用和记载,对其说明不合理的是( )
A.我国古代人民常用明矾除去铜器上的铜锈 [Cu (OH) CO]
2 2 3
B.杜康用高粱酿酒的原理是通过蒸馏法将高粱中的乙醇分离出来
C.《肘后备急方》中“青蒿一握,以水二升渍,绞取汁”,该提取过程属于物理变化
D.《抱朴子》记载“丹砂(HgS)烧之成水银,积变又还成丹砂”,该过程为氧化还原反应
2.设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.2 g HO和DO的混合物中,含有的电子总数为N
2 2 A
B.常温常压下,0.5 mol O 与11.2 L O 所含分子数均为0.5N
3 2 A
C.常温常压下,104 g苯乙烯(C H—CH===CH )中总共含有σ键数目为9N
6 5 2 A
D.56 g Fe与一定量稀硝酸充分反应后,若Fe完全溶解,则此时转移电子数可能为2.5N
A
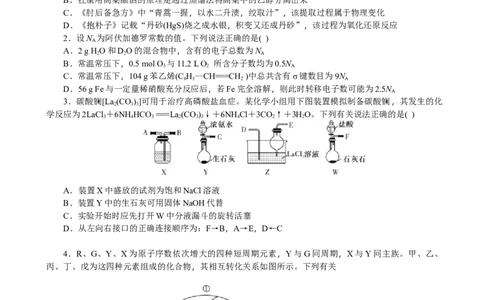
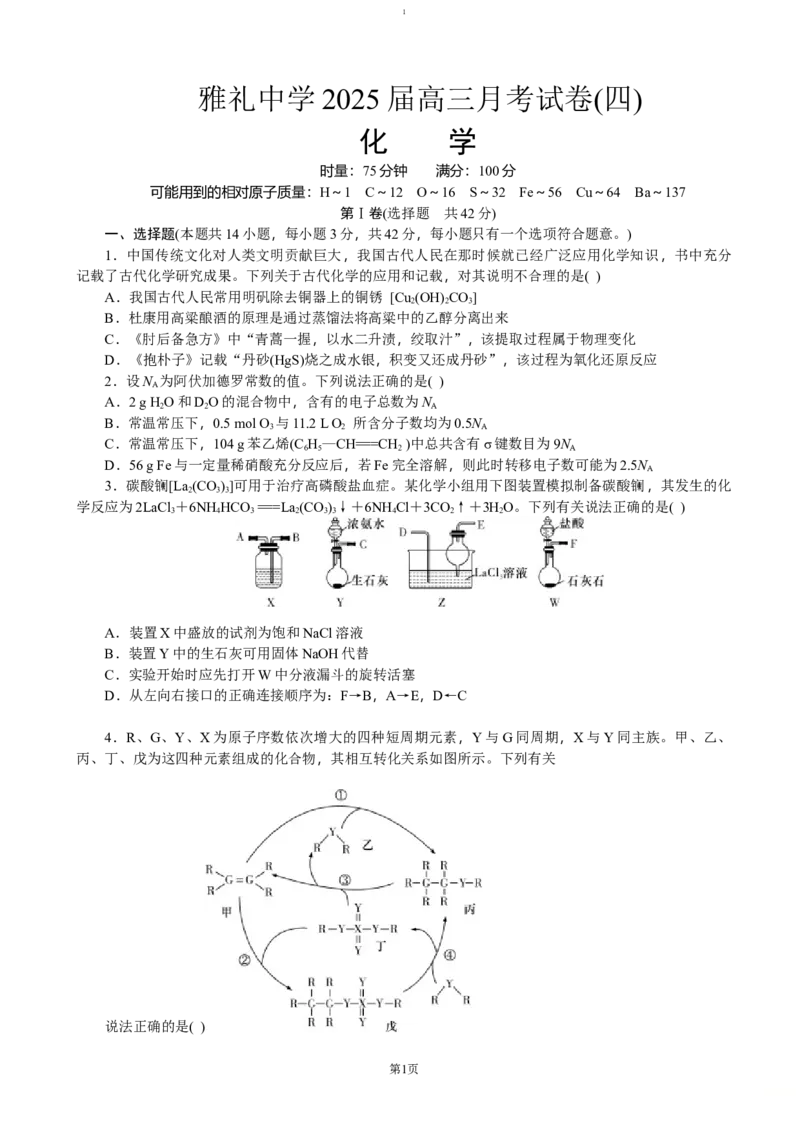
3.碳酸镧[La (CO)]可用于治疗高磷酸盐血症。某化学小组用下图装置模拟制备碳酸镧,其发生的化
2 3 3
学反应为2LaCl+6NH HCO ===La(CO)↓+6NH Cl+3CO↑+3HO。下列有关说法正确的是( )
3 4 3 2 3 3 4 2 2
A.装置X中盛放的试剂为饱和NaCl溶液
B.装置Y中的生石灰可用固体NaOH代替
C.实验开始时应先打开W中分液漏斗的旋转活塞
D.从左向右接口的正确连接顺序为:F→B,A→E,D←C
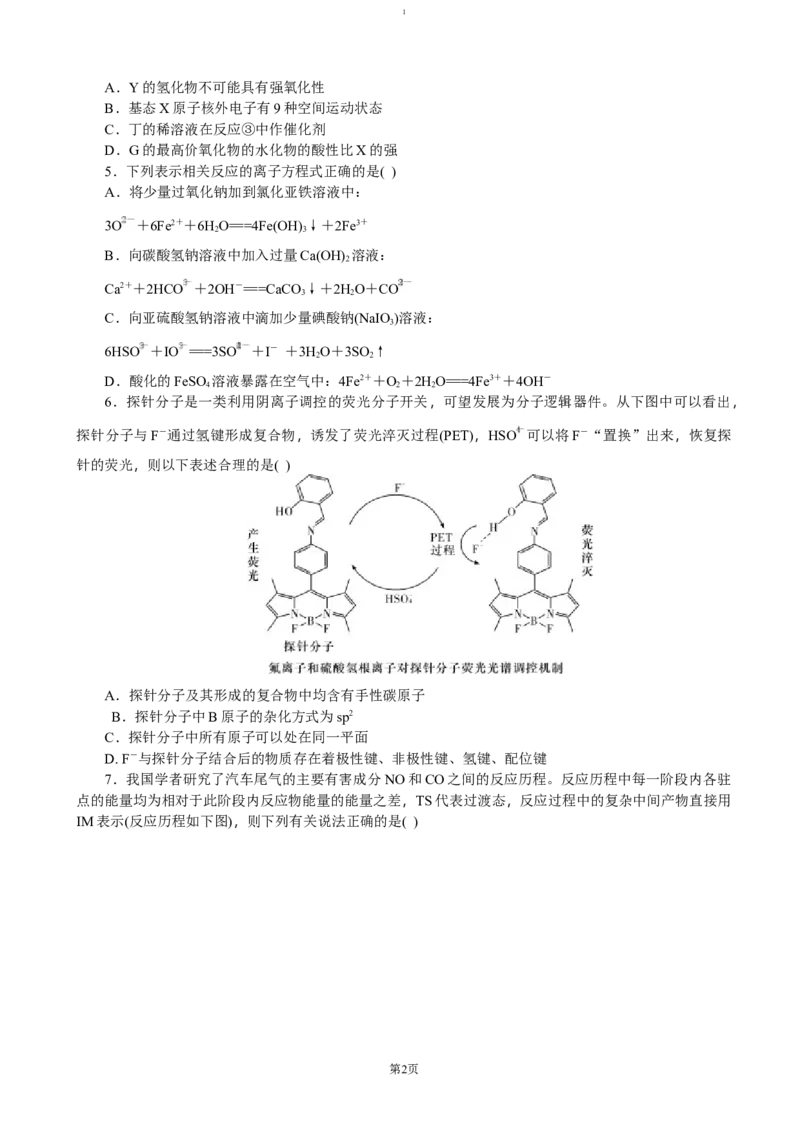
4.R、G、Y、X为原子序数依次增大的四种短周期元素,Y与G同周期,X与Y同主族。甲、乙、
丙、丁、戊为这四种元素组成的化合物,其相互转化关系如图所示。下列有关
说法正确的是( )
第1页1
A.Y的氢化物不可能具有强氧化性
B.基态X原子核外电子有9种空间运动状态
C.丁的稀溶液在反应③中作催化剂
D.G的最高价氧化物的水化物的酸性比X的强
5.下列表示相关反应的离子方程式正确的是( )
A.将少量过氧化钠加到氯化亚铁溶液中:
3O +6Fe2++6HO===4Fe(OH) ↓+2Fe3+
2 3
B.向碳酸氢钠溶液中加入过量Ca(OH) 溶液:
2
Ca2++2HCO +2OH-===CaCO ↓+2HO+CO
3 2
C.向亚硫酸氢钠溶液中滴加少量碘酸钠(NaIO )溶液:
3
6HSO +IO ===3SO +I- +3HO+3SO ↑
2 2
D.酸化的FeSO 溶液暴露在空气中:4Fe2++O+2HO===4Fe3++4OH-
4 2 2
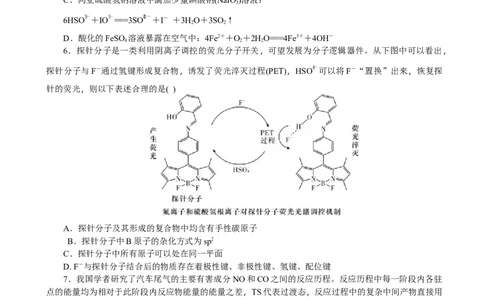
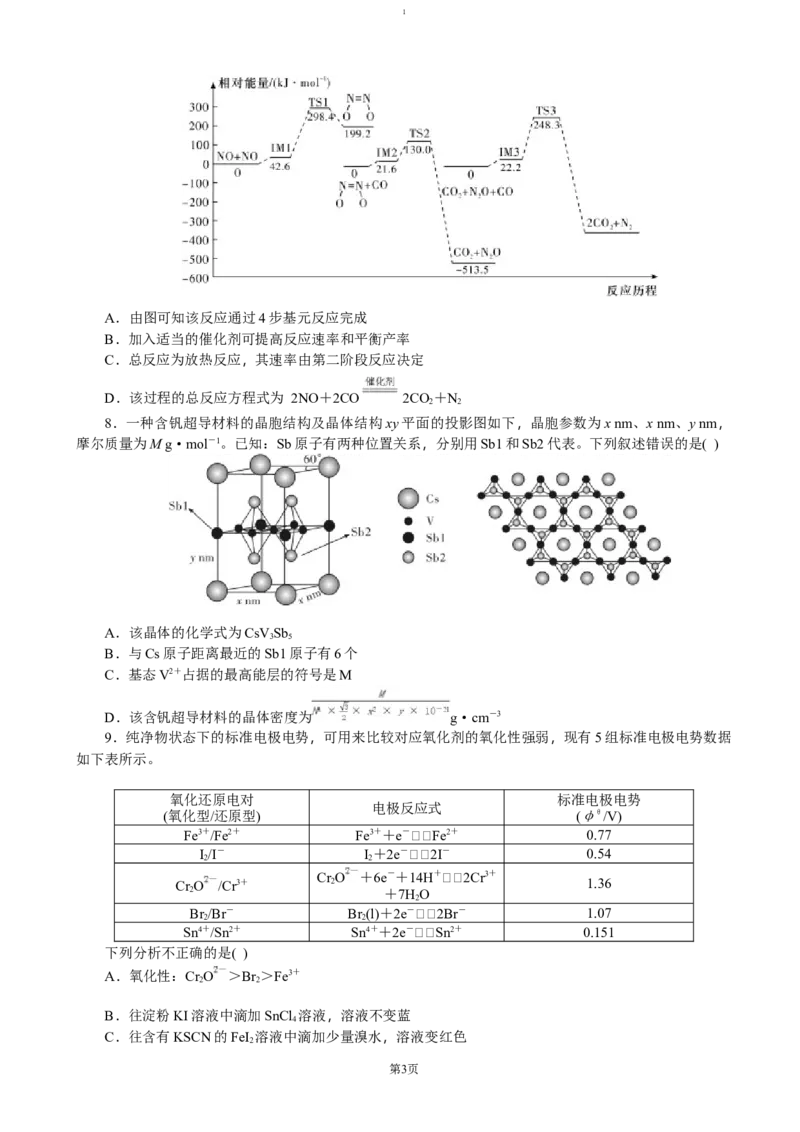
6.探针分子是一类利用阴离子调控的荧光分子开关,可望发展为分子逻辑器件。从下图中可以看出,
探针分子与F-通过氢键形成复合物,诱发了荧光淬灭过程(PET),HSO 可以将F-“置换”出来,恢复探
针的荧光,则以下表述合理的是( )
A.探针分子及其形成的复合物中均含有手性碳原子
B.探针分子中B原子的杂化方式为sp2
C.探针分子中所有原子可以处在同一平面
D. F-与探针分子结合后的物质存在着极性键、非极性键、氢键、配位键
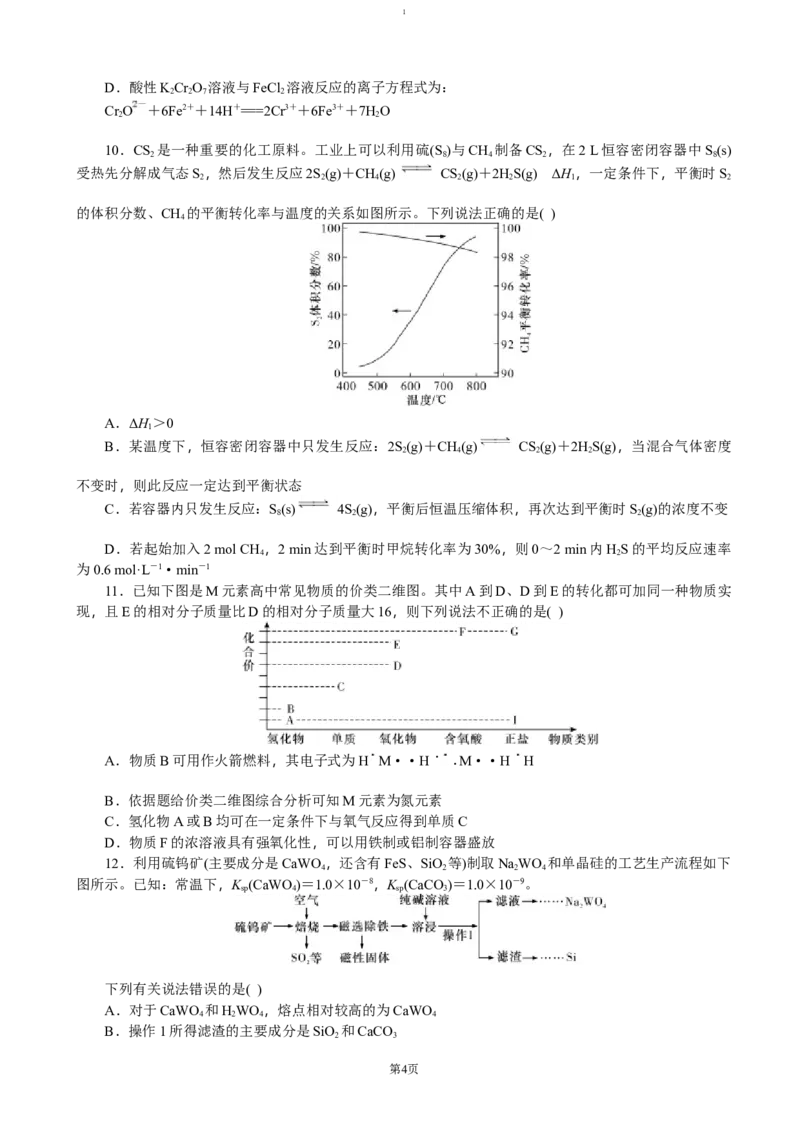
7.我国学者研究了汽车尾气的主要有害成分NO和CO之间的反应历程。反应历程中每一阶段内各驻
点的能量均为相对于此阶段内反应物能量的能量之差,TS代表过渡态,反应过程中的复杂中间产物直接用
IM表示(反应历程如下图),则下列有关说法正确的是( )
第2页1
A.由图可知该反应通过4步基元反应完成
B.加入适当的催化剂可提高反应速率和平衡产率
C.总反应为放热反应,其速率由第二阶段反应决定
D.该过程的总反应方程式为 2NO+2CO 2CO+N
2 2
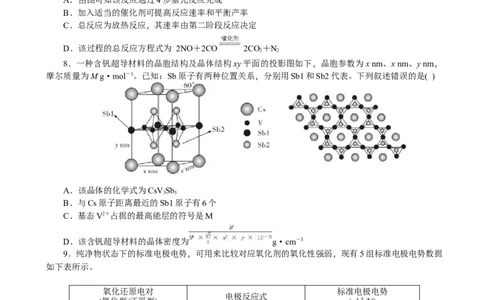
8.一种含钒超导材料的晶胞结构及晶体结构xy平面的投影图如下,晶胞参数为x nm、x nm、y nm,
摩尔质量为M g·mol-1。已知:Sb原子有两种位置关系,分别用Sb1和Sb2代表。下列叙述错误的是( )
A.该晶体的化学式为CsV Sb
3 5
B.与Cs原子距离最近的Sb1原子有6个
C.基态V2+占据的最高能层的符号是M
D.该含钒超导材料的晶体密度为 g·cm-3
9.纯净物状态下的标准电极电势,可用来比较对应氧化剂的氧化性强弱,现有5组标准电极电势数据
如下表所示。
氧化还原电对 标准电极电势
电极反应式
(氧化型/还原型) (φθ/V)
Fe3+/Fe2+ Fe3++e-Fe2+ 0.77
I/I- I+2e-2I- 0.54
2 2
Cr O +6e-+14H+2Cr3+
Cr O /Cr3+ 2 1.36
2 +7HO
2
Br /Br- Br (l)+2e-2Br- 1.07
2 2
Sn4+/Sn2+ Sn4++2e-Sn2+ 0.151
下列分析不正确的是( )
A.氧化性:Cr O >Br >Fe3+
2 2
B.往淀粉KI溶液中滴加SnCl 溶液,溶液不变蓝
4
C.往含有KSCN的FeI 溶液中滴加少量溴水,溶液变红色
2
第3页1
D.酸性KCr O 溶液与FeCl 溶液反应的离子方程式为:
2 2 7 2
Cr O +6Fe2++14H+===2Cr3++6Fe3++7HO
2 2
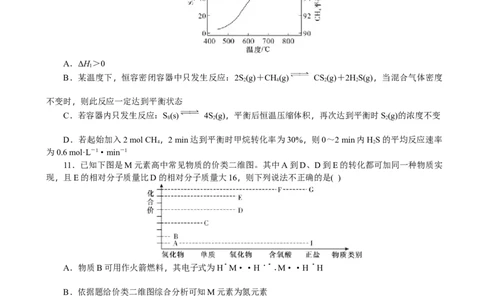
10.CS 是一种重要的化工原料。工业上可以利用硫(S )与CH 制备CS ,在2 L恒容密闭容器中S(s)
2 8 4 2 8
受热先分解成气态S,然后发生反应2S(g)+CH(g) CS(g)+2HS(g) ΔH,一定条件下,平衡时S
2 2 4 2 2 1 2
的体积分数、CH 的平衡转化率与温度的关系如图所示。下列说法正确的是( )
4
A.ΔH>0
1
B.某温度下,恒容密闭容器中只发生反应:2S(g)+CH(g) CS(g)+2HS(g),当混合气体密度
2 4 2 2
不变时,则此反应一定达到平衡状态
C.若容器内只发生反应:S(s) 4S(g),平衡后恒温压缩体积,再次达到平衡时S(g)的浓度不变
8 2 2
D.若起始加入2 mol CH ,2 min达到平衡时甲烷转化率为30%,则0~2 min内HS的平均反应速率
4 2
为0.6 mol·L-1·min-1
11.已知下图是M元素高中常见物质的价类二维图。其中A到D、D到E的转化都可加同一种物质实
现,且E的相对分子质量比D的相对分子质量大16,则下列说法不正确的是( )
A.物质B可用作火箭燃料,其电子式为H M··H · M··H H
·
B.依据题给价类二维图综合分析可知M元素为氮元素
C.氢化物A或B均可在一定条件下与氧气反应得到单质C
D.物质F的浓溶液具有强氧化性,可以用铁制或铝制容器盛放
12.利用硫钨矿(主要成分是CaWO ,还含有FeS、SiO 等)制取NaWO 和单晶硅的工艺生产流程如下
4 2 2 4
图所示。已知:常温下,K (CaWO )=1.0×10-8,K (CaCO)=1.0×10-9。
sp 4 sp 3
下列有关说法错误的是( )
A.对于CaWO 和HWO,熔点相对较高的为CaWO
4 2 4 4
B.操作1所得滤渣的主要成分是SiO 和CaCO
2 3
第4页1
C.“溶浸”时,通常可以用烧碱溶液代替纯碱溶液
D.“焙烧”时发生反应的化学方程式为3FeS+5O Fe O+3SO
2 3 4 2
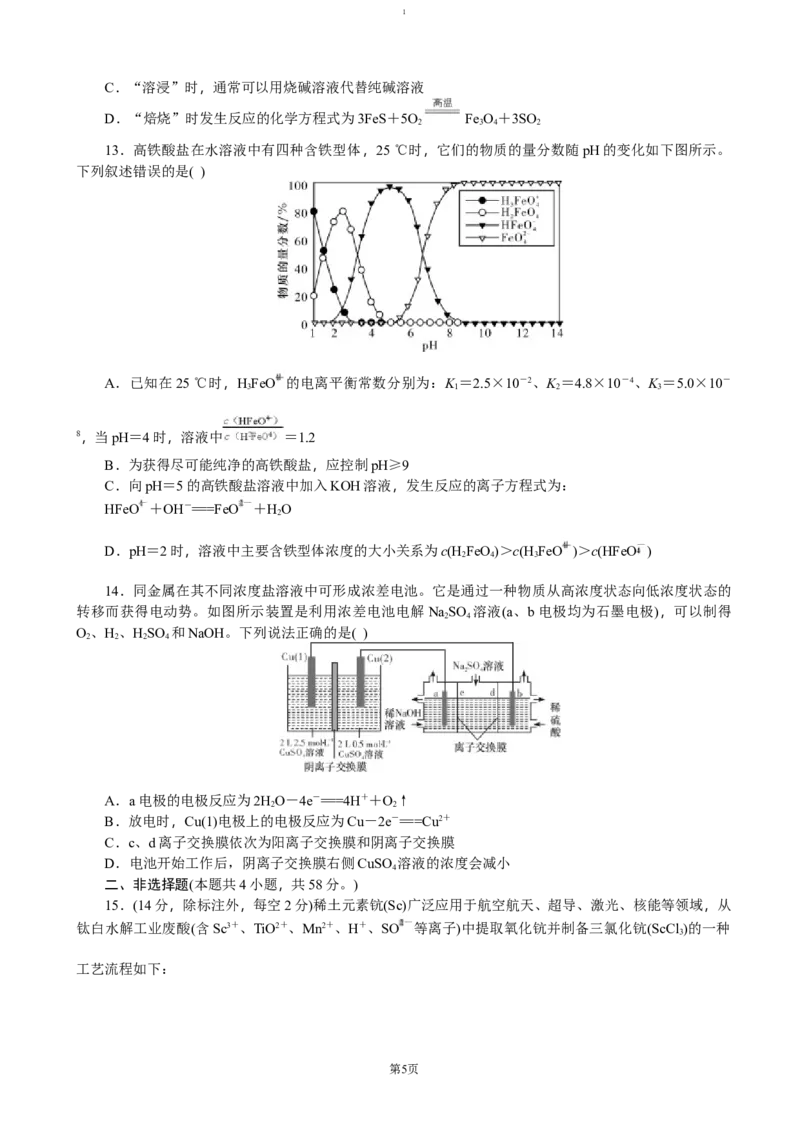
13.高铁酸盐在水溶液中有四种含铁型体,25 ℃时,它们的物质的量分数随pH的变化如下图所示。
下列叙述错误的是( )
A.已知在25 ℃时,HFeO 的电离平衡常数分别为:K =2.5×10-2、K =4.8×10-4、K =5.0×10-
3 1 2 3
8,当pH=4时,溶液中 =1.2
B.为获得尽可能纯净的高铁酸盐,应控制pH≥9
C.向pH=5的高铁酸盐溶液中加入KOH溶液,发生反应的离子方程式为:
HFeO +OH-===FeO +HO
2
D.pH=2时,溶液中主要含铁型体浓度的大小关系为c(H FeO)>c(H FeO )>c(HFeO )
2 4 3
14.同金属在其不同浓度盐溶液中可形成浓差电池。它是通过一种物质从高浓度状态向低浓度状态的
转移而获得电动势。如图所示装置是利用浓差电池电解NaSO 溶液(a、b电极均为石墨电极),可以制得
2 4
O、H、HSO 和NaOH。下列说法正确的是( )
2 2 2 4
A.a电极的电极反应为2HO-4e-===4H++O↑
2 2
B.放电时,Cu(1)电极上的电极反应为Cu-2e-===Cu2+
C.c、d离子交换膜依次为阳离子交换膜和阴离子交换膜
D.电池开始工作后,阴离子交换膜右侧CuSO 溶液的浓度会减小
4
二、非选择题(本题共4小题,共58分。)
15.(14分,除标注外,每空2分)稀土元素钪(Sc)广泛应用于航空航天、超导、激光、核能等领域,从
钛白水解工业废酸(含Sc3+、TiO2+、Mn2+、H+、SO 等离子)中提取氧化钪并制备三氯化钪(ScCl )的一种
3
工艺流程如下:
第5页1
已知:Ag CrO 为砖红色固体;K (AgCl)=2.0×10-10,K (Ag CrO)=2.0 ×10-12。
2 4 sp sp 2 4
请回答下列问题:
(1)萃取和反萃取操作都需使用到的主要玻璃仪器为________和__________。
(2)在钛白水解工业废酸中,加入HO 是为了使TiO2+转化为[TiO(OH)(HO) ]+,若该离子中Ti元素的
2 2 2 2 4
化合价为+4,则除OH-和HO外的其余氧元素价态为_____价。
2
(3)若温度对钪、钛的萃取率影响情况见下表,一般合适的萃取温度为 10~15 ℃,其理由是
______________________________________________。
T/℃ 5 10 15 25 30
钪的萃取率/% 91.3 96 97.1 97.3 98.0
钛的萃取率/% 0.94 0.95 2.10 3.01 4.20
(4)在“反萃取”步骤中,强碱性条件下双氧水可以氧化Mn2+生成MnO ,该反应的离子方程式为
2
___________________________________________________________。
(5)上述工艺流程在“灼烧”步骤中可得到 Sc O ,已知在后续的“加热氯化”步骤中可得到一种使灼
2 3
热 氧 化 铜 由 黑 变 红 的 气 体 , 请 依 题 写 出 此 时 由 Sc O 制 备 ScCl 的 化 学 方 程 式 :
2 3 3
_____________________________________________。
(6)现取制得的 ScCl 粗产品(只含难溶 Sc O 杂质)溶于水,配成溶液,采用KCrO 为指示剂,用
3 2 3 2 4
AgNO 标准溶液滴定,若在滴定时盛装标准溶液的滴定管未润洗,则导致测得粗产品中ScCl 含量__偏高
3 3
__(填“偏高”“偏低”或“无影响”);当达到滴定终点,溶液中Cl-恰好沉淀完全[假设此时c(Cl-)=
1.0×10-5 mol·L-1]时,此时溶液中CrO 的浓度为_____________________mol·L-1。
16.(16分,每空2分)(1)将CO 富集、活化、转化为具有高附加值的化学品对实现“碳中和”有重要
2
意义。CO 性质稳定,使其活化是实现转化的重要前提。
2
①使用过渡金属作催化剂,提供空轨道接受_______(填“C”或“O”)原子的孤电子对,破坏CO 的结构
2
使其活化。
②采用电化学、光化学等手段,使 CO _______________ (填“提供”或“接受”)电子转化为
2
CHOH。
3
(2)二氧化碳催化加氢制取二甲醚(DME)有利于减少温室气体二氧化碳,制取过程发生如下反应:
反应Ⅰ.CO (g)+3H(g) CHOH(g)+HO(g) ΔH
2 2 3 2 1
反应Ⅱ.2CH OH(g) CHOCH (g)+HO(g) ΔH=-23.4 kJ·mol-1
3 3 3 2 2
反应Ⅲ.CO (g)+H(g) CO(g)+HO(g) ΔH=+41.17 kJ·mol-1
2 2 2 3
回答下列问题:
①T℃时,向恒压容器中充入0.2 mol CO(g)和0.6 mol H(g),若在该条件下只发生反应Ⅰ,达平衡时,
1 2 2
放出4 kJ能量;若向相同容器中充入0.4 mol CH OH(g)和0.4 mol H O(g),达平衡时,吸收11.8 kJ能量,
3 2
则反应Ⅰ的ΔH=________________kJ·mol-1。
1
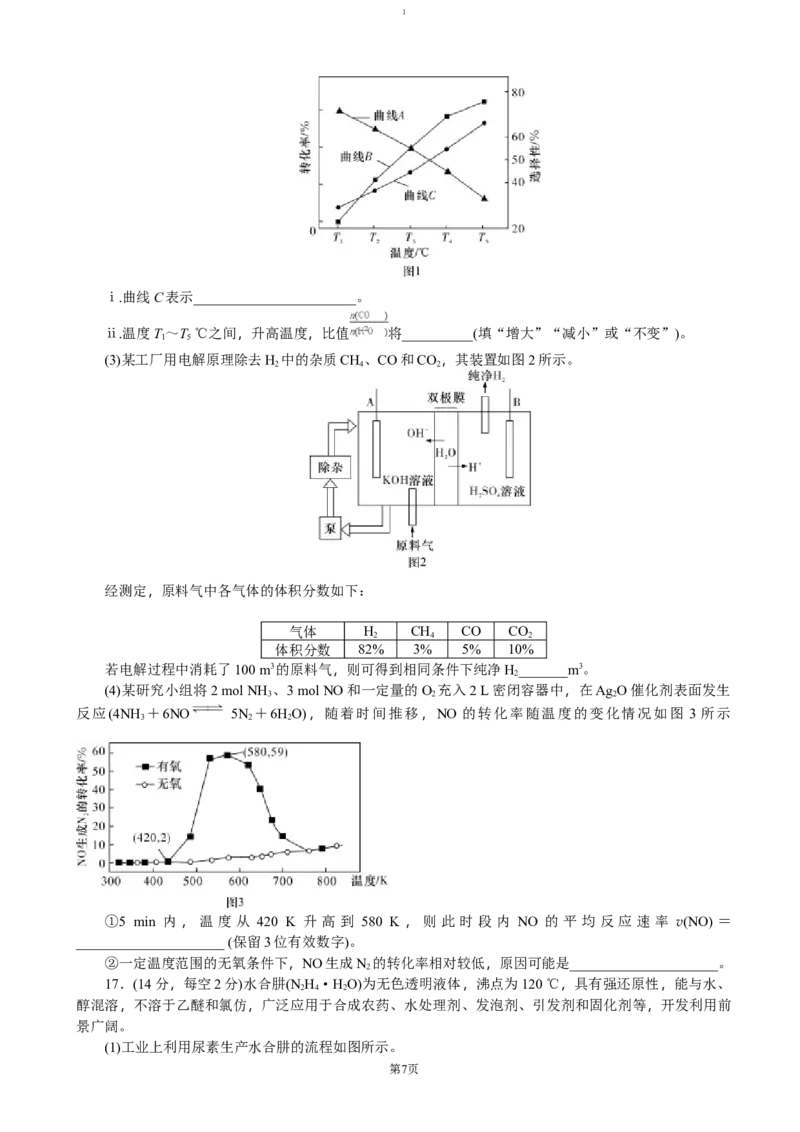
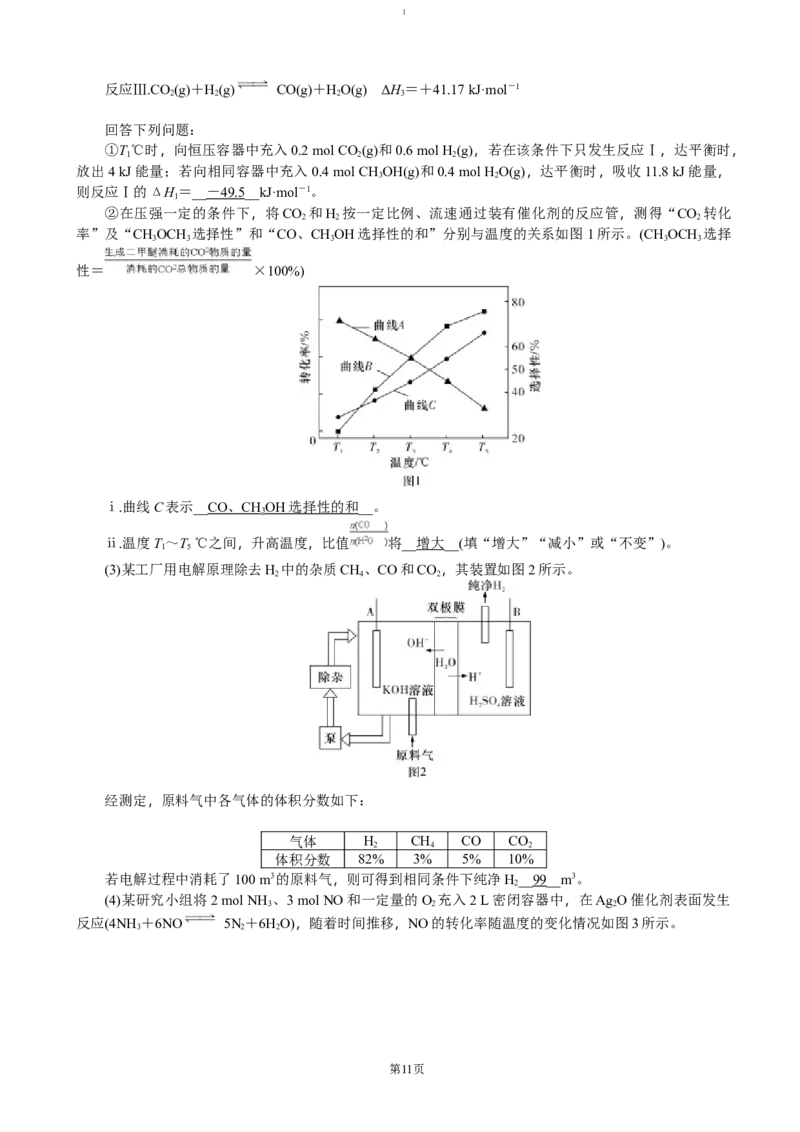
②在压强一定的条件下,将CO 和H 按一定比例、流速通过装有催化剂的反应管,测得“CO 转化
2 2 2
率”及“CHOCH 选择性”和“CO、CHOH选择性的和”分别与温度的关系如图1所示。(CHOCH 选择
3 3 3 3 3
性= ×100%)
第6页1
ⅰ.曲线C表示_______________________。
ⅱ.温度T~T ℃之间,升高温度,比值 将__________(填“增大”“减小”或“不变”)。
1 5
(3)某工厂用电解原理除去H 中的杂质CH、CO和CO,其装置如图2所示。
2 4 2
经测定,原料气中各气体的体积分数如下:
气体 H CH CO CO
2 4 2
体积分数 82% 3% 5% 10%
若电解过程中消耗了100 m3的原料气,则可得到相同条件下纯净H_______m3。
2
(4)某研究小组将2 mol NH 、3 mol NO和一定量的O 充入2 L密闭容器中,在Ag O催化剂表面发生
3 2 2
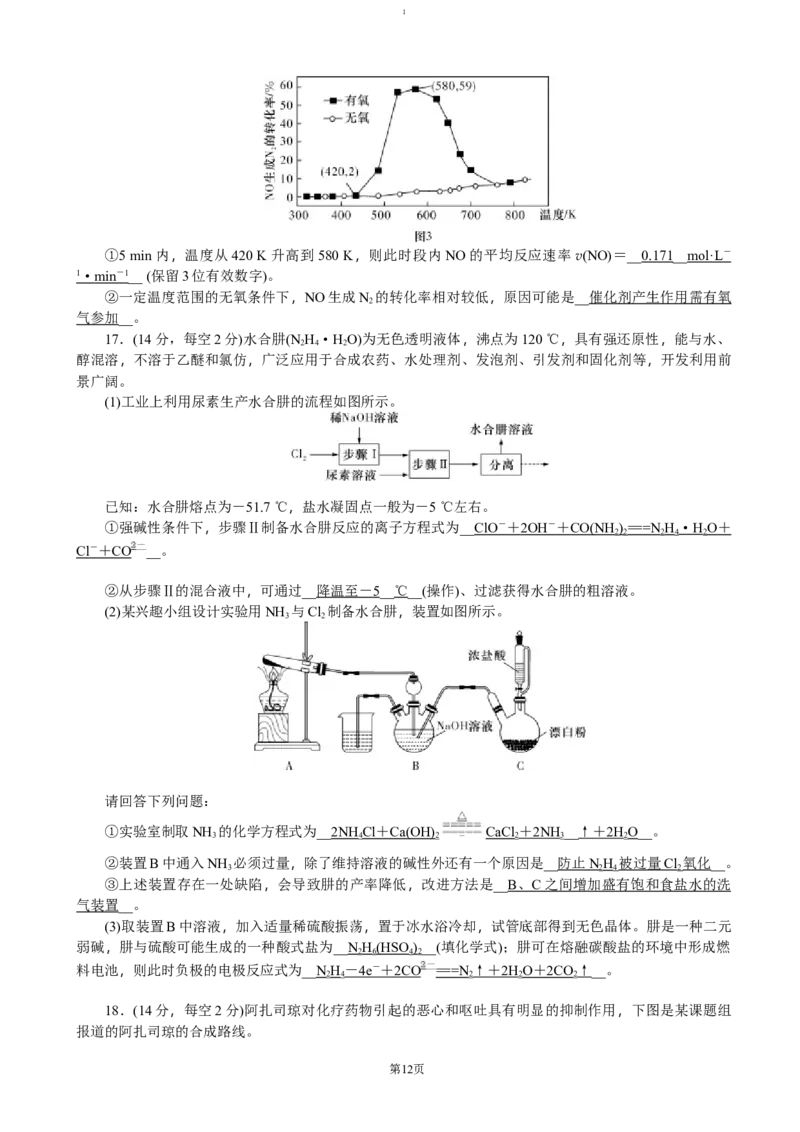
反应(4NH +6NO 5N +6HO),随着时间推移,NO 的转化率随温度的变化情况如图 3 所示
3 2 2
①5 min 内 , 温 度 从 420 K 升 高 到 580 K , 则 此 时 段 内 NO 的 平 均 反 应 速 率 v(NO) =
_____________________ (保留3位有效数字)。
②一定温度范围的无氧条件下,NO生成N 的转化率相对较低,原因可能是_____________________。
2
17.(14分,每空2分)水合肼(N H·HO)为无色透明液体,沸点为120 ℃,具有强还原性,能与水、
2 4 2
醇混溶,不溶于乙醚和氯仿,广泛应用于合成农药、水处理剂、发泡剂、引发剂和固化剂等,开发利用前
景广阔。
(1)工业上利用尿素生产水合肼的流程如图所示。
第7页1
已知:水合肼熔点为-51.7 ℃,盐水凝固点一般为-5 ℃左右。
①强碱性条件下,步骤Ⅱ制备水合肼反应的离子方程式为__________________________________。
②从步骤Ⅱ的混合液中,可通过___________________(操作)、过滤获得水合肼的粗溶液。
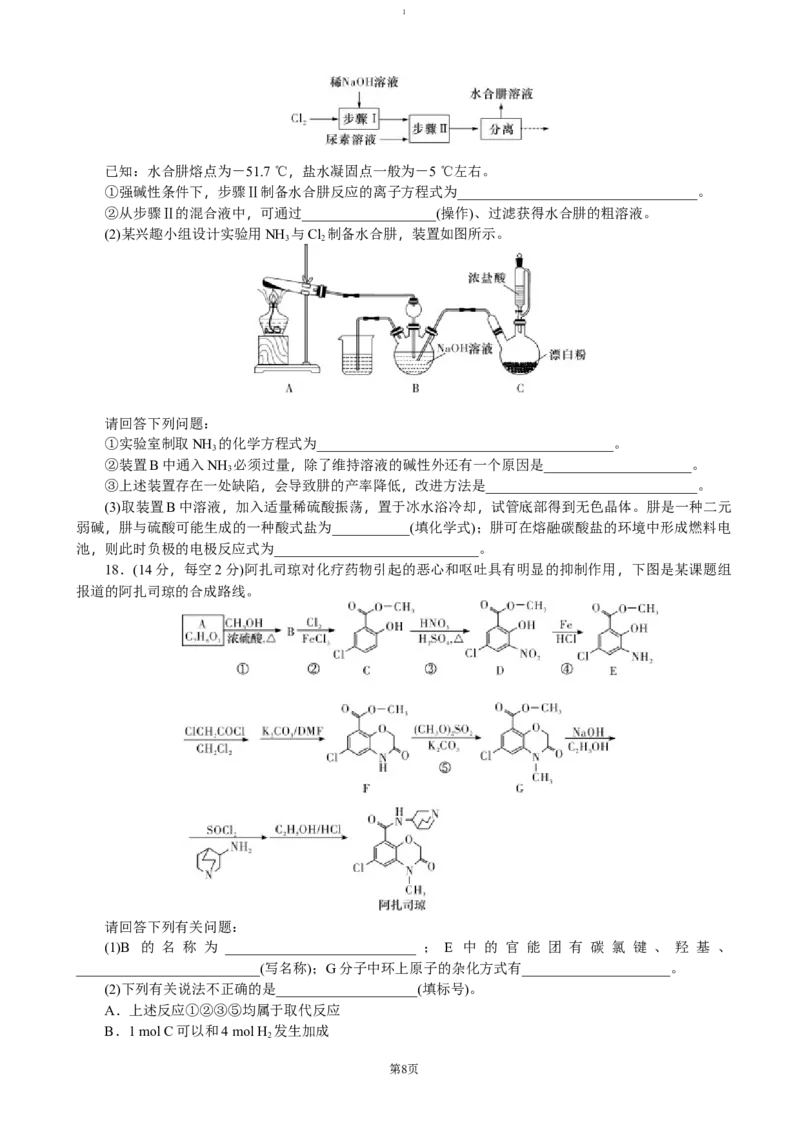
(2)某兴趣小组设计实验用NH 与Cl 制备水合肼,装置如图所示。
3 2
请回答下列问题:
①实验室制取NH 的化学方程式为__________________________________________。
3
②装置B中通入NH 必须过量,除了维持溶液的碱性外还有一个原因是_____________________。
3
③上述装置存在一处缺陷,会导致肼的产率降低,改进方法是______________________________。
(3)取装置B中溶液,加入适量稀硫酸振荡,置于冰水浴冷却,试管底部得到无色晶体。肼是一种二元
弱碱,肼与硫酸可能生成的一种酸式盐为___________(填化学式);肼可在熔融碳酸盐的环境中形成燃料电
池,则此时负极的电极反应式为_____________________________。
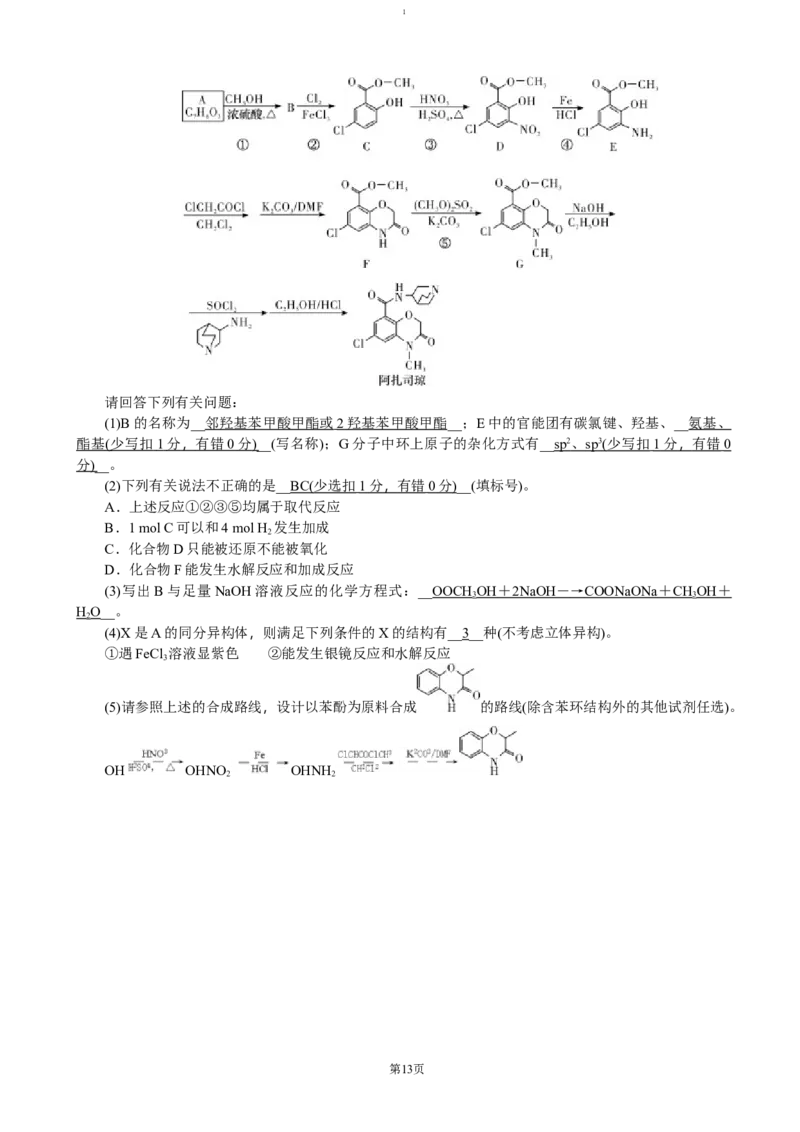
18.(14分,每空2分)阿扎司琼对化疗药物引起的恶心和呕吐具有明显的抑制作用,下图是某课题组
报道的阿扎司琼的合成路线。
请回答下列有关问题:
(1)B 的 名 称 为 ___________________________ ; E 中 的 官 能 团 有 碳 氯 键 、 羟 基 、
__________________________(写名称);G分子中环上原子的杂化方式有_____________________。
(2)下列有关说法不正确的是____________________(填标号)。
A.上述反应①②③⑤均属于取代反应
B.1 mol C可以和4 mol H 发生加成
2
第8页1
C.化合物D只能被还原不能被氧化
D.化合物F能发生水解反应和加成反应
(3)写出B与足量NaOH溶液反应的化学方程式:_________________________________。
(4)X是A的同分异构体,则满足下列条件的X的结构有____种(不考虑立体异构)。
①遇FeCl 溶液显紫色 ②能发生银镜反应和水解反应
3
(5)请参照上述的合成路线,设计以苯酚为原料合成 的路线(除含苯环结构外的其他试剂任选)。
第9页1
化学试题(雅礼版)-
雅礼中学 2025 届高三月考试卷(四)
化 学
一、选择题(本题共14小题,每小题3分,共42分,每小题只有一个选项符合题意。)
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14
答案 B D B B C D D B C C A C A C
第Ⅱ卷(非选择题 共58分)
二、非选择题(本题共4小题,共58分。)
15.(14分,除标注外,每空2分)
(1)萃取和反萃取操作都需使用到的主要玻璃仪器为__ 烧杯 ( 1 分 )__和__ ( 梨形 ) 分液漏斗 (1 分 )( 此两空顺
序可对调 )__。
(2)在钛白水解工业废酸中,加入HO 是为了使TiO2+转化为[TiO(OH)(HO) ]+,若该离子中Ti元素的
2 2 2 2 4
化合价为+4,则除OH-和HO外的其余氧元素价态为__ - 1__价。
2
(3)若温度对钪、钛的萃取率影响情况见下表,一般合适的萃取温度为10~15 ℃,其理由是__温度为
10 ~ 15 __ ℃ 时 , 钪的萃取率较高而且钛的萃取率较低 __。
T/℃ 5 10 15 25 30
钪的萃取率/% 91.3 96 97.1 97.3 98.0
钛的萃取率/% 0.94 0.95 2.10 3.01 4.20
(4)在“反萃取”步骤中,强碱性条件下双氧水可以氧化Mn2+生成MnO ,该反应的离子方程式为
2
__ Mn 2 + + H O + 2OH - __ == =MnO __ ↓ + 2H O__。
2 2 2 2
(5)上述工艺流程在“灼烧”步骤中可得到 Sc O ,已知在后续的“加热氯化”步骤中可得到一种使灼
2 3
热氧化铜由黑变红的气体,请依题写出此时由Sc O 制备ScCl 的化学方程式:__Sc O + 3C + 3C l
2 3 3 2 3 2
2ScCl + 3CO __。
3
(6)现取制得的 ScCl 粗产品(只含难溶 Sc O 杂质)溶于水,配成溶液,采用KCrO 为指示剂,用
3 2 3 2 4
AgNO 标准溶液滴定,若在滴定时盛装标准溶液的滴定管未润洗,则导致测得粗产品中ScCl 含量__偏高
3 3
__(填“偏高”“偏低”或“无影响”);当达到滴定终点,溶液中Cl-恰好沉淀完全[假设此时c(Cl-)=
1.0×10-5 mol·L-1]时,此时溶液中CrO 的浓度为__ 5.0 × 10 - 3 或 __0.005__mol·L-1。
16.(16分,每空2分)(1)将CO 富集、活化、转化为具有高附加值的化学品对实现“碳中和”有重要
2
意义。CO 性质稳定,使其活化是实现转化的重要前提。
2
①使用过渡金属作催化剂,提供空轨道接受__O__(填“C”或“O”)原子的孤电子对,破坏CO 的结构
2
使其活化。
②采用电化学、光化学等手段,使CO __接受__ (填“提供”或“接受”)电子转化为CHOH。
2 3
(2)二氧化碳催化加氢制取二甲醚(DME)有利于减少温室气体二氧化碳,制取过程发生如下反应:
反应Ⅰ.CO (g)+3H(g) CH OH(g)+HO(g) ΔH
2 2 3 2 1
反应Ⅱ.2CH OH(g) CHOCH (g)+HO(g) ΔH=-23.4 kJ·mol-1
3 3 3 2 2
第10页1
反应Ⅲ.CO (g)+H(g) CO(g)+HO(g) ΔH=+41.17 kJ·mol-1
2 2 2 3
回答下列问题:
①T℃时,向恒压容器中充入0.2 mol CO(g)和0.6 mol H(g),若在该条件下只发生反应Ⅰ,达平衡时,
1 2 2
放出4 kJ能量;若向相同容器中充入0.4 mol CH OH(g)和0.4 mol H O(g),达平衡时,吸收11.8 kJ能量,
3 2
则反应Ⅰ的ΔH=__ - 49. 5__kJ·mol-1。
1
②在压强一定的条件下,将CO 和H 按一定比例、流速通过装有催化剂的反应管,测得“CO 转化
2 2 2
率”及“CHOCH 选择性”和“CO、CHOH选择性的和”分别与温度的关系如图1所示。(CHOCH 选择
3 3 3 3 3
性= ×100%)
ⅰ.曲线C表示__ CO 、 CH OH 选择性的和 __。
3
ⅱ.温度T~T ℃之间,升高温度,比值 将__增大__(填“增大”“减小”或“不变”)。
1 5
(3)某工厂用电解原理除去H 中的杂质CH、CO和CO,其装置如图2所示。
2 4 2
经测定,原料气中各气体的体积分数如下:
气体 H CH CO CO
2 4 2
体积分数 82% 3% 5% 10%
若电解过程中消耗了100 m3的原料气,则可得到相同条件下纯净H__99__m3。
2
(4)某研究小组将2 mol NH 、3 mol NO和一定量的O 充入2 L密闭容器中,在Ag O催化剂表面发生
3 2 2
反应(4NH +6NO 5N+6HO),随着时间推移,NO的转化率随温度的变化情况如图3所示。
3 2 2
第11页1
①5 min内,温度从420 K升高到580 K,则此时段内NO的平均反应速率v(NO)=__0.171__ mol·L -
1 · min - 1 __ (保留3位有效数字)。
②一定温度范围的无氧条件下,NO生成N 的转化率相对较低,原因可能是__催化剂产生作用需有氧
2
气参加__。
17.(14分,每空2分)水合肼(N H·HO)为无色透明液体,沸点为120 ℃,具有强还原性,能与水、
2 4 2
醇混溶,不溶于乙醚和氯仿,广泛应用于合成农药、水处理剂、发泡剂、引发剂和固化剂等,开发利用前
景广阔。
(1)工业上利用尿素生产水合肼的流程如图所示。
已知:水合肼熔点为-51.7 ℃,盐水凝固点一般为-5 ℃左右。
①强碱性条件下,步骤Ⅱ制备水合肼反应的离子方程式为__ ClO - + 2OH - + CO(NH ) == =N H · H O +
2 2 2 4 2
Cl - + CO __。
②从步骤Ⅱ的混合液中,可通过__ 降温至- 5__℃__(操作)、过滤获得水合肼的粗溶液。
(2)某兴趣小组设计实验用NH 与Cl 制备水合肼,装置如图所示。
3 2
请回答下列问题:
①实验室制取NH 的化学方程式为__2NH Cl + Ca(OH) CaCl + 2NH __ ↑ + 2H O__。
3 4 2 2 3 2
②装置B中通入NH 必须过量,除了维持溶液的碱性外还有一个原因是__ 防止 N H 被过量 C l 氧化__。
3 2 4 2
③上述装置存在一处缺陷,会导致肼的产率降低,改进方法是__ B 、 C 之间增加盛有饱和食盐水的洗
气装置__。
(3)取装置B中溶液,加入适量稀硫酸振荡,置于冰水浴冷却,试管底部得到无色晶体。肼是一种二元
弱碱,肼与硫酸可能生成的一种酸式盐为__NH(HSO )__(填化学式);肼可在熔融碳酸盐的环境中形成燃
2 6 4 2
料电池,则此时负极的电极反应式为__NH - 4 e - + 2CO == =N ↑ + 2H O + 2CO ↑__。
2 4 2 2 2
18.(14分,每空2分)阿扎司琼对化疗药物引起的恶心和呕吐具有明显的抑制作用,下图是某课题组
报道的阿扎司琼的合成路线。
第12页1
请回答下列有关问题:
(1)B的名称为__ 邻羟基苯甲酸甲酯或 2 羟基苯甲酸甲酯 __;E中的官能团有碳氯键、羟基、__氨基、
酯基 ( 少写扣 1 分 , 有错 0 分 )__(写名称);G分子中环上原子的杂化方式有__ sp 2 、 sp 3 ( 少写扣 1 分 , 有错 0
分 )__。
(2)下列有关说法不正确的是__ BC( 少选扣 1 分 , 有错 0 分 ) __(填标号)。
A.上述反应①②③⑤均属于取代反应
B.1 mol C可以和4 mol H 发生加成
2
C.化合物D只能被还原不能被氧化
D.化合物F能发生水解反应和加成反应
(3)写出B与足量NaOH溶液反应的化学方程式:__OOCH OH + 2NaOH ― → COONaONa + CH OH +
3 3
HO__。
2
(4)X是A的同分异构体,则满足下列条件的X的结构有__3__种(不考虑立体异构)。
①遇FeCl 溶液显紫色 ②能发生银镜反应和水解反应
3
(5)请参照上述的合成路线,设计以苯酚为原料合成 的路线(除含苯环结构外的其他试剂任选)。
OH OHNO OHNH
2 2
第13页