文档内容
2025-2026 学年高一化学上学期第一次月考卷
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考证
号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.测试范围:必修一第1章-第2章第一节(人教版2019)。
5.难度系数:0.65
6.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:O-16 Na-23
第Ⅰ卷(选择题 共 48 分)
一、选择题:本题共16个小题,每小题3分,共48分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
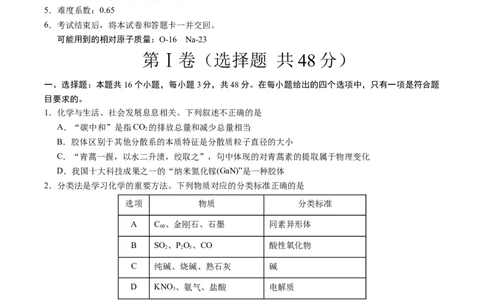
1.化学与生活、社会发展息息相关。下列叙述不正确的是
A.“碳中和”是指CO 的排放总量和减少总量相当
2
B.胶体区别于其他分散系的本质特征是分散质粒子直径的大小
C.“青蒿一握,以水二升渍,绞取之”,句中体现的对青蒿素的提取属于物理变化
D.我国十大科技成果之一的“纳米氮化镓(GaN)”是一种胶体
2.分类法是学习化学的重要方法。下列物质对应的分类标准正确的是
选项 物质 分类标准
A C 、金刚石、石墨 同素异形体
60
B SO 、PO、CO 酸性氧化物
2 2 5
C 纯碱、烧碱、熟石灰 碱
D KNO、氨气、盐酸 电解质
3
A.A B.B C.C D.D
3.下列转化中,必须加入氧化剂才能实现的是
A.Na→ NaOH B.HC →CO C. D.
2
4.下列物质中不能发生丁达尔效应的是
A.有色玻璃 B.烧碱溶液 C.雾霾 D. 胶体
5.下列反应不属于四种基本反应类型,但属于氧化还原反应的是
A. B.
1 / 6
学科网(北京)股份有限公司C. D.
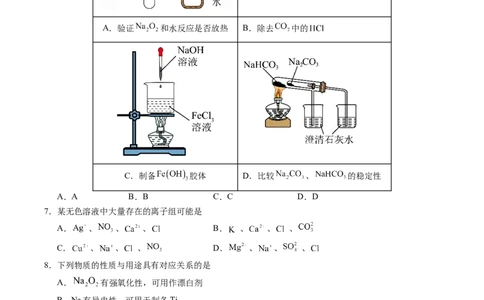
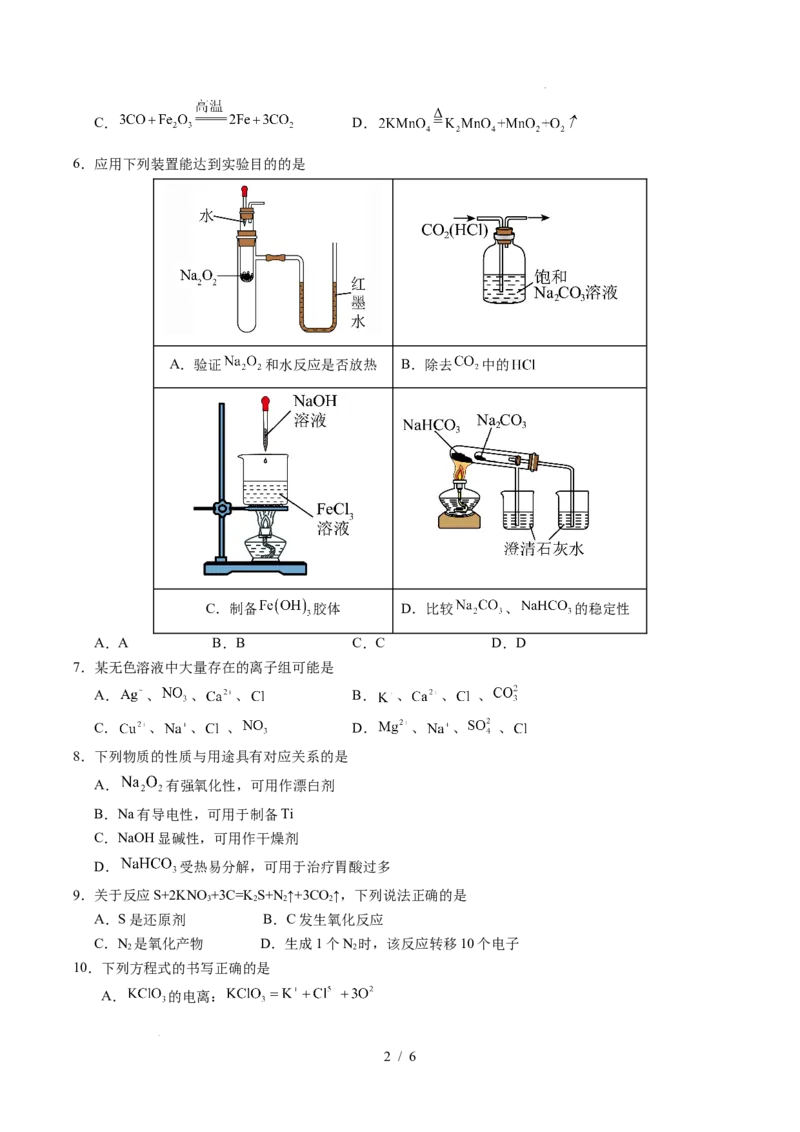
6.应用下列装置能达到实验目的的是
A.验证 和水反应是否放热 B.除去 中的
C.制备 胶体 D.比较 、 的稳定性
A.A B.B C.C D.D
7.某无色溶液中大量存在的离子组可能是
A. 、 、 、 B. 、 、 、
C. 、 、 、 D. 、 、 、
8.下列物质的性质与用途具有对应关系的是
A. 有强氧化性,可用作漂白剂
B.Na有导电性,可用于制备Ti
C.NaOH显碱性,可用作干燥剂
D. 受热易分解,可用于治疗胃酸过多
9.关于反应S+2KNO +3C=K S+N↑+3CO ↑,下列说法正确的是
3 2 2 2
A.S是还原剂 B.C发生氧化反应
C.N 是氧化产物 D.生成1个N 时,该反应转移10个电子
2 2
10.下列方程式的书写正确的是
A. 的电离:
2 / 6
学科网(北京)股份有限公司B.金属钠投入硫酸铜溶液中:
C.用小苏打治疗胃酸过多:
D.硫酸氢钠溶液和过量氢氧化钡溶液反应的离子方程式:
11.下列表示氧化还原反应中电子转移的方向和数目正确的是
A. B.
C. D.
12.下列关于钠及其化合物的说法正确的是
A.将金属钠在燃烧匙中点燃,可得到淡黄色固体NaO
2
B.NaO、NaO 均能与HO、CO 反应生成O,它们都可用作供氧剂
2 2 2 2 2 2
C.NaCO、NaHCO 溶液均能与Ca(OH) 溶液反应产生白色沉淀
2 3 3 2
D.将稀盐酸滴加到NaCO 和NaOH的混合溶液中,立即产生气泡
2 3
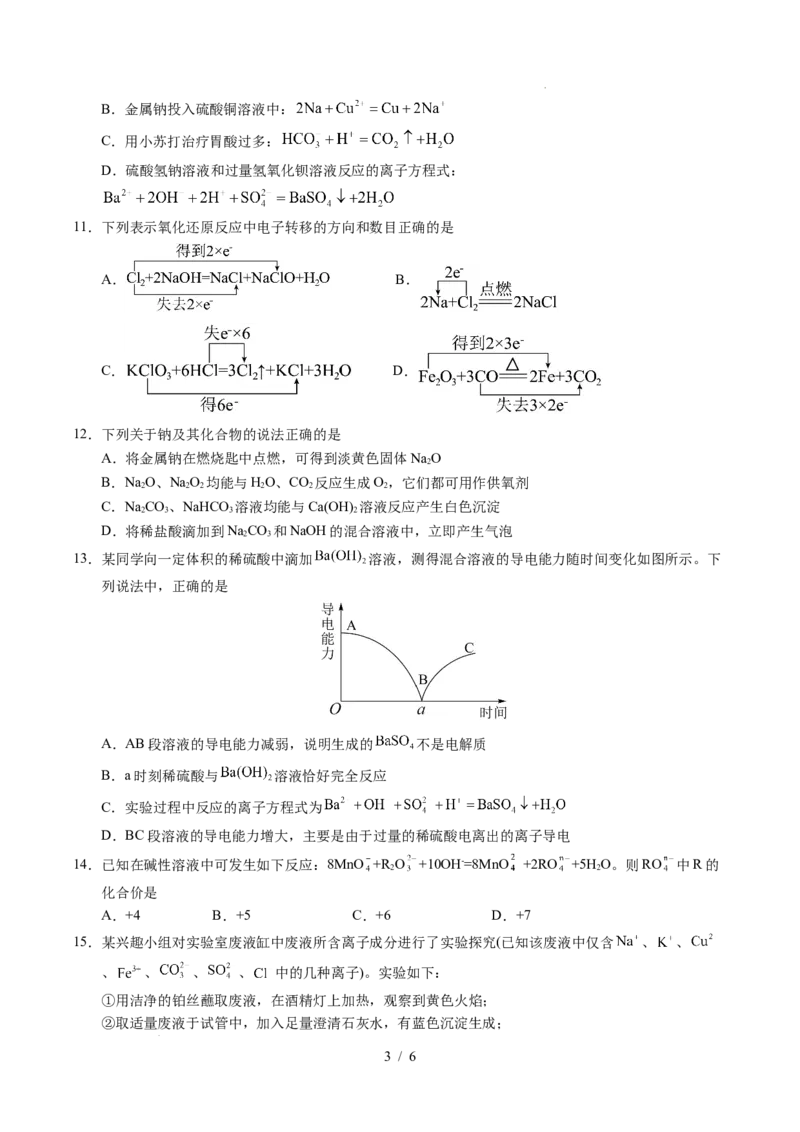
13.某同学向一定体积的稀硫酸中滴加 溶液,测得混合溶液的导电能力随时间变化如图所示。下
列说法中,正确的是
A.AB段溶液的导电能力减弱,说明生成的 不是电解质
B.a时刻稀硫酸与 溶液恰好完全反应
C.实验过程中反应的离子方程式为
D.BC段溶液的导电能力增大,主要是由于过量的稀硫酸电离出的离子导电
14.已知在碱性溶液中可发生如下反应:8MnO +R O +10OH-=8MnO +2RO +5H O。则RO 中R的
2 2
化合价是
A.+4 B.+5 C.+6 D.+7
15.某兴趣小组对实验室废液缸中废液所含离子成分进行了实验探究(已知该废液中仅含 、 、
、 、 、 、 中的几种离子)。实验如下:
①用洁净的铂丝蘸取废液,在酒精灯上加热,观察到黄色火焰;
②取适量废液于试管中,加入足量澄清石灰水,有蓝色沉淀生成;
3 / 6
学科网(北京)股份有限公司③另取适量废液于试管中,加入足量 溶液,有白色沉淀生成,过滤得滤液 。
根据以上实验判断,下列推断正确的是
A.根据实验①可得出废液中含有 ,不含
B.根据实验②可得出,溶液中肯定不含 、
C.实验③中白色沉淀为 和
D.若向滤液 中加入 溶液产生白色沉淀,证明原废液中有
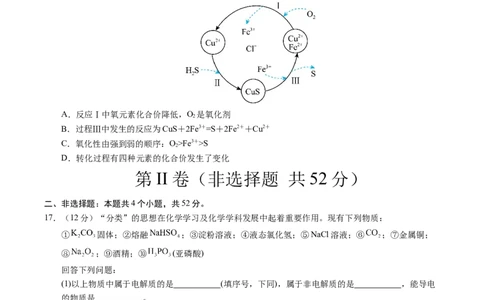
16.硫化氢(H S)是一种有毒、有害的不良气体。处理某废气中的HS,是将废气与空气混合通入FeCl 、
2 2 2
CuCl 、FeCl 的混合液中,其转化的流程如图所示。下列说法错误的是
2 3
A.反应Ⅰ中氧元素化合价降低,O 是氧化剂
2
B.过程Ⅲ中发生的反应为CuS+2Fe3+=S+2Fe2++Cu2+
C.氧化性由强到弱的顺序:O>Fe3+>S
2
D.转化过程有四种元素的化合价发生了变化
第 II 卷(非选择题 共 52 分)
二、非选择题:本题共4个小题,共52分。
17.(12分)“分类”的思想在化学学习及化学学科发展中起着重要作用。现有下列物质:
① 固体;②熔融 ;③淀粉溶液;④液态氯化氢;⑤NaCl溶液;⑥ ;⑦金属铜;
⑧ ;⑨酒精;⑩ (亚磷酸)
回答下列问题:
(1)以上物质中属于电解质的是 (填序号,下同),属于非电解质的是 ,能导电
的物质是 。
(2)物质②的电离方程式为 。
(3)③所属分散系为 ,如果③⑤混合,可利用 (填“滤纸”或“半透膜”)进行
分离。
(4)已知⑩与足量KOH溶液反应的化学方程式为 , 属于(填
“正盐”或“酸式盐”) 。
18.(12分) 、 、 、 四种不同化合物的水溶液中所含阳离子: 、 、 、 ,阴离
子: 、 、 、 (离子在物质中不能重复出现)。常温下分别取四种物质的水溶液进行
如下实验:
4 / 6
学科网(北京)股份有限公司①A的溶液显黄色,B的溶液显碱性;
②向C的溶液中滴加稀盐酸,一段时间后有无色无味的气体逸出。
回答下列问题:
(1)写出下列物质的化学式:B ,D 。
(2)向C的溶液中滴入少量稀盐酸,反应的离子方程式为 。
(3)A溶液和B溶液混合的实验现象是 。
(4)在烧杯中加入40mL蒸馏水,加热至沸腾后,向沸水中逐滴加入5~6滴A的饱和溶液,继续煮沸至
液体呈 色,停止加热,得到分散系M,得到分散系M的化学方程式为 ,分散系M
中分散质粒子的直径范围为 。
19.(14分)钠的化合物在生产生活中具有广泛应用。
I.我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献。联合制碱法的主要过程如
下图所示(部分物质已略去)。
(1)“侯氏制碱法”誉满全球,其中的“碱”为 (填化学式)。
(2)①~③所涉及的操作方法中,包含过滤的是 (填序号)。
(3)上述联合制碱法流程中可以循环使用的中一种物质是 (填化学式)。
(4)下列试剂可以鉴别 溶液和 溶液的是___________。
A. B. 溶液 C. 溶液 D.稀盐酸
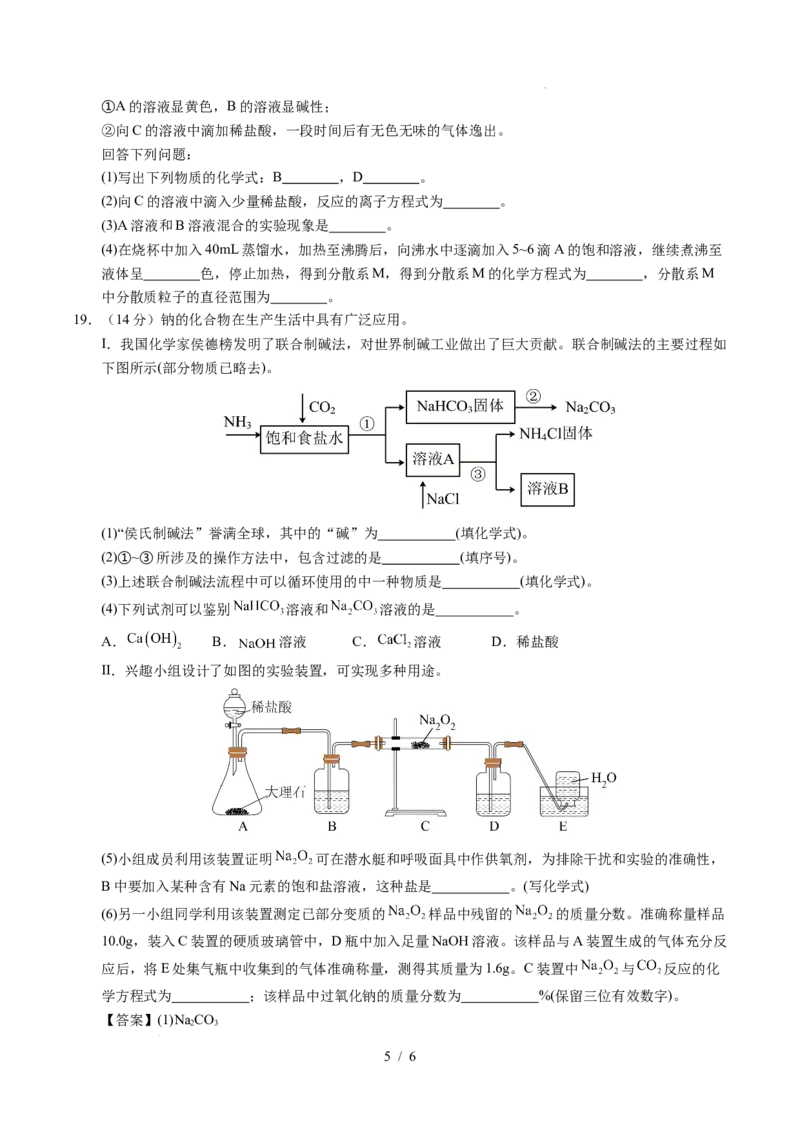
II.兴趣小组设计了如图的实验装置,可实现多种用途。
(5)小组成员利用该装置证明 可在潜水艇和呼吸面具中作供氧剂,为排除干扰和实验的准确性,
B中要加入某种含有Na元素的饱和盐溶液,这种盐是 。(写化学式)
(6)另一小组同学利用该装置测定已部分变质的 样品中残留的 的质量分数。准确称量样品
10.0g,装入C装置的硬质玻璃管中,D瓶中加入足量NaOH溶液。该样品与A装置生成的气体充分反
应后,将E处集气瓶中收集到的气体准确称量,测得其质量为1.6g。C装置中 与 反应的化
学方程式为 ;该样品中过氧化钠的质量分数为 %(保留三位有效数字)。
【答案】(1)Na CO
2 3
5 / 6
学科网(北京)股份有限公司(2)①③
(3)CO
2
(4)CD
(5)NaHCO
3
(6) 78.0%
20.(14分)氧化还原反应原理在研究物质性质及物质转化方面具有重要的意义。
Ⅰ. 易溶于水,外观和食盐相似,有咸味,人误食会中毒。
(1)人体正常的血红蛋白中含有 ,若误食亚硝酸盐(如 ),则导致血红蛋白中的 转化为
而使人体中毒,服用维生素C可解毒。 转化为 时, 在反应中被 (填“氧化”
或“还原”);服用维生素C可使血红蛋白中的 转变成 ,说明维生素C作 (填“氧化”
或“还原”)剂。
(2)已知 能发生反应: ,淀粉遇碘会变蓝色。则鉴别
固体和 固体,无须选用的物质为 (填标号)。
①水②碘化钾淀粉试纸③食醋④白酒
(3)某厂废液中含有2%~5%的 ,直接排放会造成污染,下列试剂能使 转化为不引起二
次污染的 的是 (填标号)。
A. B. C.
Ⅱ.铁有不同价态, 既有氧化性又有还原性,铁钉在氯气中被锈蚀成棕褐色含 的物质,而在
稀硫酸中生成浅绿色溶液(含 )。
(4)实验室常向煮沸的蒸馏水中滴加饱和 溶液制备 胶体,证明有胶体生成的最常用的实验
操作和现象是 。
(5)高铁酸钠( )是一种新型饮用水消毒剂。工业上常用 、 、 制备,配平
反应: 。
_______ _______ _______ _______ _______ _______
(6)已知反应: , 。则 、
、 氧化性强弱关系为 。
6 / 6
学科网(北京)股份有限公司