文档内容
`
山西大学附中
2025~2026 学年第一学期高三 9 月模块诊断(总第三次)
化 学 试 题
考查时间:75分钟 考查内容:有机化学、化学反应原理 命题人:张光明
一、选择题(每题3分,共48分)
1.高分子材料在生产生活中应用广泛。下列说法错误的是( )
A.芦苇可用于制造黏胶纤维,其主要成分为纤维素
B.淀粉是相对分子质量可达几十万的天然高分子物质
C.北京冬奥会火炬“飞扬”使用的碳纤维属于有机高分子材料
D.大豆蛋白纤维是一种再生纤维
2.下列说法错误的是( )
A.同温同压下,H (g)+Cl (g)=2HCl(g)在光照和点燃条件下的ΔH相同
2 2
B.已知25℃、101kPa条件下:4Al(s)3O (g)=2Al O (s) H 2834.9kJmol1,
2 2 3 1
4Al(s)2O (g)=2Al O (s) H 3119.1kJmol1,则可推出O 比O 稳定
3 2 3 2 3 2
C.甲烷的燃烧热ΔH=-890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为CH (g)+
4
2O (g)=CO (g)+2H O(l) ΔH=-890.3kJ·mol-1
2 2 2
D.已知500℃、30MPa下,将0.5molN (g)和1.5molH (g)置于密闭的容器中充分反应
2 2
生成NH (g),当N 的转化率为40%时,放热18.48kJ,则热化学方程式为N (g)+3H (g)
3 2 2 2
2NH (g) ΔH=-92.4kJ·mol-1
3
3.在一密闭容器中,反应aA(g)+bB(s) cC(g)+dD(g)达到平衡后,保持温度不变,将
容器缩小为原来的一半,当达到新的平衡时,A的浓度是原来的1.6倍,则下列说法正确
的是( )
A.a>c+d B.平衡向逆反应方向移动
C.物质A的转化率减小 D.物质D的浓度减小
4.金银花中能提取出有很高的药用价值的绿原酸(如图),下列说法错误的是( )
A.1mol绿原酸最多与5molH 发生加成反应
2
B.1mol绿原酸与浓溴水反应,最多消耗4molBr
2
C.绿原酸能发生取代、加成、消去和氧化反应
D.1mol绿原酸最多与4molNaOH反应
高三化学试题8第 1 页 共 8 页
{#{QQABAYKtpggw0gTACDwqR0UsCQsQsIOgJaoEBQAUqAQKSQNIBCA=}#}`
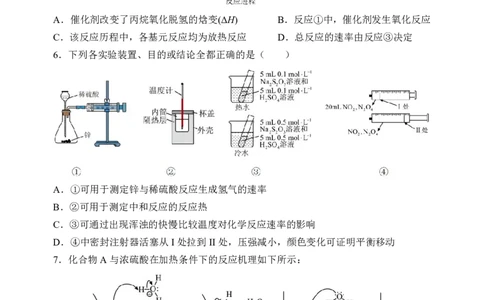
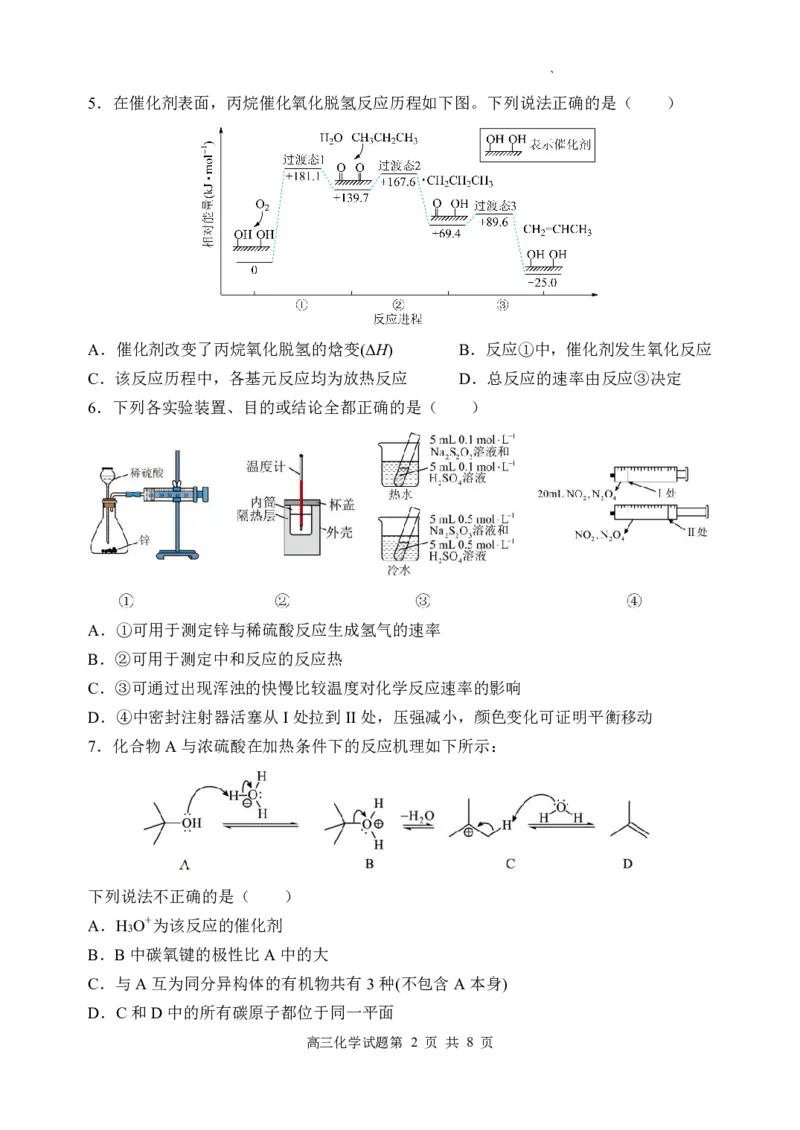
5.在催化剂表面,丙烷催化氧化脱氢反应历程如下图。下列说法正确的是( )
A.催化剂改变了丙烷氧化脱氢的焓变(ΔH) B.反应①中,催化剂发生氧化反应
C.该反应历程中,各基元反应均为放热反应 D.总反应的速率由反应③决定
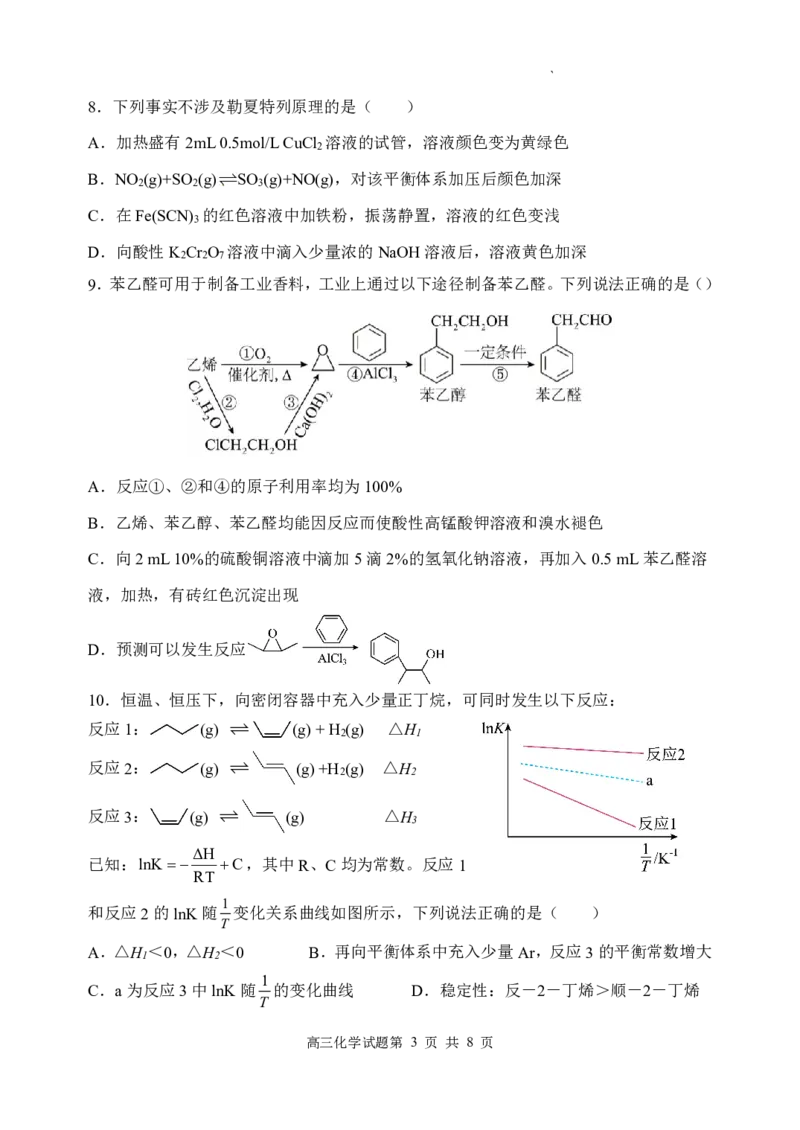
6.下列各实验装置、目的或结论全都正确的是( )
A.①可用于测定锌与稀硫酸反应生成氢气的速率
B.②可用于测定中和反应的反应热
C.③可通过出现浑浊的快慢比较温度对化学反应速率的影响
D.④中密封注射器活塞从I处拉到II处,压强减小,颜色变化可证明平衡移动
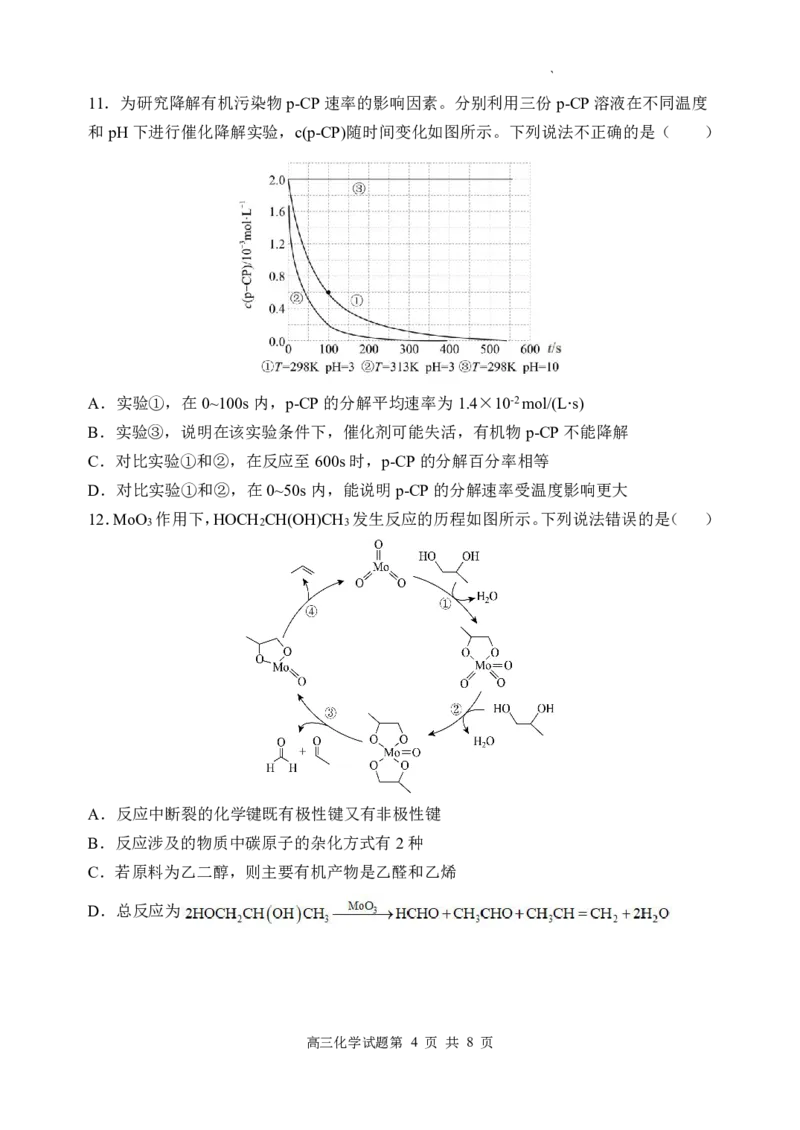
7.化合物A与浓硫酸在加热条件下的反应机理如下所示:
下列说法不正确的是( )
A.H O+为该反应的催化剂
3
B.B中碳氧键的极性比A中的大
C.与A互为同分异构体的有机物共有3种(不包含A本身)
D.C和D中的所有碳原子都位于同一平面
高三化学试题8第 2 页 共 8 页
{#{QQABAYKtpggw0gTACDwqR0UsCQsQsIOgJaoEBQAUqAQKSQNIBCA=}#}`
8.下列事实不涉及勒夏特列原理的是( )
A.加热盛有2mL0.5mol/LCuCl 溶液的试管,溶液颜色变为黄绿色
2
B.NO (g)+SO (g) SO (g)+NO(g),对该平衡体系加压后颜色加深
2 2 3
C.在Fe(SCN) 的红色溶液中加铁粉,振荡静置,溶液的红色变浅
3
D.向酸性K Cr O 溶液中滴入少量浓的NaOH溶液后,溶液黄色加深
2 2 7
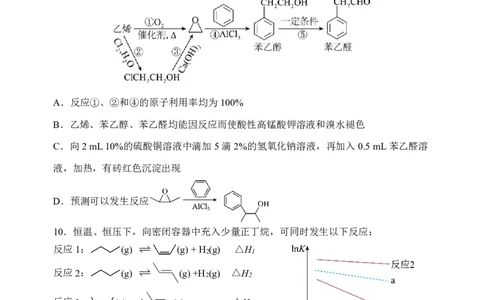
9.苯乙醛可用于制备工业香料,工业上通过以下途径制备苯乙醛。下列说法正确的是()
A.反应①、②和④的原子利用率均为100%
B.乙烯、苯乙醇、苯乙醛均能因反应而使酸性高锰酸钾溶液和溴水褪色
C.向2mL10%的硫酸铜溶液中滴加5滴2%的氢氧化钠溶液,再加入0.5mL苯乙醛溶
液,加热,有砖红色沉淀出现
D.预测可以发生反应
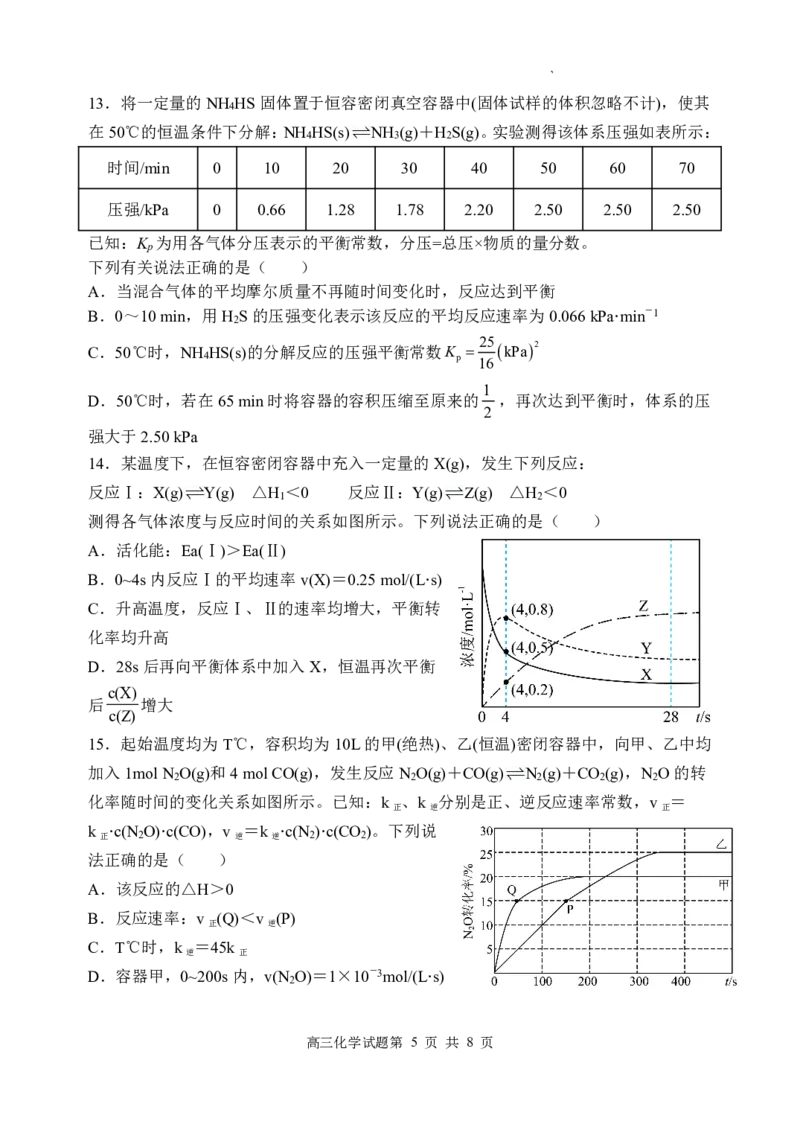
10.恒温、恒压下,向密闭容器中充入少量正丁烷,可同时发生以下反应:
反应1: (g) (g)+H (g) △H
2 1
反应2: (g) (g)+H (g) △H
2 2
反应3: (g) (g) △H
3
ΔH
已知:lnK C,其中R、C均为常数。反应1
RT
1
和反应2的lnK随 变化关系曲线如图所示,下列说法正确的是( )
T
A.△H <0,△H <0 B.再向平衡体系中充入少量Ar,反应3的平衡常数增大
1 2
1
C.a为反应3中lnK随 的变化曲线 D.稳定性:反-2-丁烯>顺-2-丁烯
T
高三化学试题8第 3 页 共 8 页
{#{QQABAYKtpggw0gTACDwqR0UsCQsQsIOgJaoEBQAUqAQKSQNIBCA=}#}`
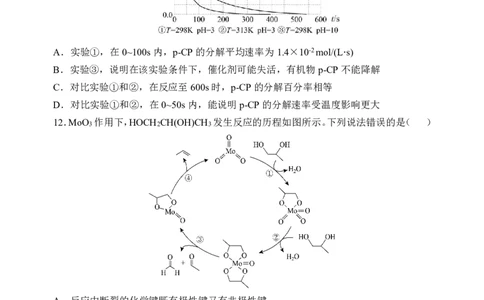
11.为研究降解有机污染物p-CP速率的影响因素。分别利用三份p-CP溶液在不同温度
和pH下进行催化降解实验,c(p-CP)随时间变化如图所示。下列说法不正确的是( )
A.实验①,在0~100s内,p-CP的分解平均速率为1.4×10-2mol/(L·s)
B.实验③,说明在该实验条件下,催化剂可能失活,有机物p-CP不能降解
C.对比实验①和②,在反应至600s时,p-CP的分解百分率相等
D.对比实验①和②,在0~50s内,能说明p-CP的分解速率受温度影响更大
12.MoO 作用下,HOCH CH(OH)CH 发生反应的历程如图所示。下列说法错误的是( )
3 2 3
A.反应中断裂的化学键既有极性键又有非极性键
B.反应涉及的物质中碳原子的杂化方式有2种
C.若原料为乙二醇,则主要有机产物是乙醛和乙烯
D.总反应为
高三化学试题8第 4 页 共 8 页
{#{QQABAYKtpggw0gTACDwqR0UsCQsQsIOgJaoEBQAUqAQKSQNIBCA=}#}`
13.将一定量的NH HS固体置于恒容密闭真空容器中(固体试样的体积忽略不计),使其
4
在50℃的恒温条件下分解:NH HS(s) NH (g)+H S(g)。实验测得该体系压强如表所示:
4 3 2
时间/min 0 10 20 30 40 50 60 70
压强/kPa 0 0.66 1.28 1.78 2.20 2.50 2.50 2.50
已知:K 为用各气体分压表示的平衡常数,分压=总压×物质的量分数。
p
下列有关说法正确的是( )
A.当混合气体的平均摩尔质量不再随时间变化时,反应达到平衡
B.0~10min,用H S的压强变化表示该反应的平均反应速率为0.066kPa·min-1
2
25
C.50℃时,NH HS(s)的分解反应的压强平衡常数K kPa2
4 p 16
1
D.50℃时,若在65min时将容器的容积压缩至原来的 ,再次达到平衡时,体系的压
2
强大于2.50kPa
14.某温度下,在恒容密闭容器中充入一定量的X(g),发生下列反应:
反应Ⅰ:X(g) Y(g) △H <0 反应Ⅱ:Y(g) Z(g) △H <0
1 2
测得各气体浓度与反应时间的关系如图所示。下列说法正确的是( )
A.活化能:Ea(Ⅰ)>Ea(Ⅱ)
B.0~4s内反应Ⅰ的平均速率v(X)=0.25mol/(L·s)
C.升高温度,反应Ⅰ、Ⅱ的速率均增大,平衡转
化率均升高
D.28s后再向平衡体系中加入X,恒温再次平衡
c(X)
后 增大
c(Z)
15.起始温度均为T℃,容积均为10L的甲(绝热)、乙(恒温)密闭容器中,向甲、乙中均
加入1molN O(g)和4molCO(g),发生反应N O(g)+CO(g) N (g)+CO (g),N O的转
2 2 2 2 2
化率随时间的变化关系如图所示。已知:k 、k 分别是正、逆反应速率常数,v =
正 逆 正
k ·c(N O)·c(CO),v =k ·c(N )·c(CO )。下列说
正 2 逆 逆 2 2
法正确的是( )
A.该反应的△H>0
B.反应速率:v (Q)<v (P)
正 逆
C.T℃时,k =45k
逆 正
D.容器甲,0~200s内,v(N O)=1×10-3mol/(L·s)
2
高三化学试题8第 5 页 共 8 页
{#{QQABAYKtpggw0gTACDwqR0UsCQsQsIOgJaoEBQAUqAQKSQNIBCA=}#}`
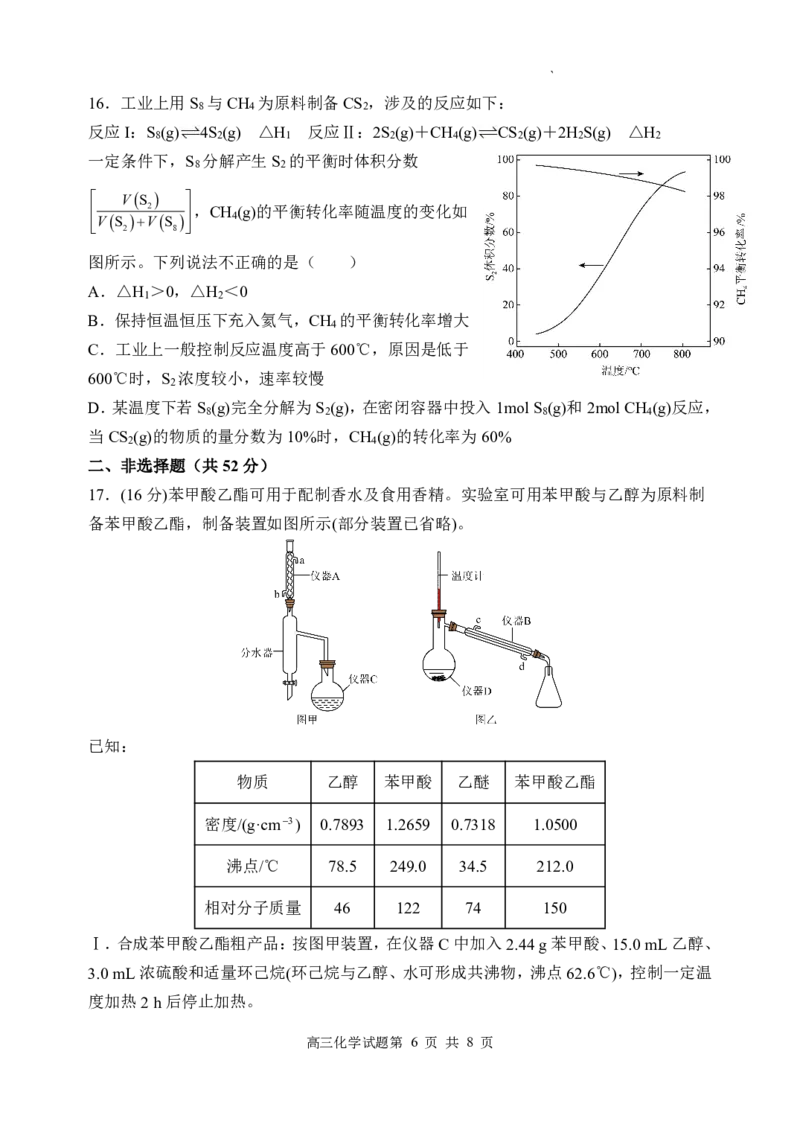
16.工业上用S 与CH 为原料制备CS ,涉及的反应如下:
8 4 2
反应I:S (g) 4S (g) △H 反应Ⅱ:2S (g)+CH (g) CS (g)+2H S(g) △H
8 2 1 2 4 2 2 2
一定条件下,S 分解产生S 的平衡时体积分数
8 2
VS
2 ,,CHCH (g)的平衡转化率随温度的变化如
VS
2
VS
8
4 4
图所示。下列说法不正确的是( )
A.△H >0,△H <0
1 2
B.保持恒温恒压下充入氦气,CH 的平衡转化率增大
4
C.工业上一般控制反应温度高于600℃,原因是低于
600℃时,S 浓度较小,速率较慢
2
D.某温度下若S (g)完全分解为S (g),在密闭容器中投入1molS (g)和2molCH (g)反应,
8 2 8 4
当CS (g)的物质的量分数为10%时,CH (g)的转化率为60%
2 4
二、非选择题(共52分)
17.(16分)苯甲酸乙酯可用于配制香水及食用香精。实验室可用苯甲酸与乙醇为原料制
备苯甲酸乙酯,制备装置如图所示(部分装置已省略)。
已知:
物质 乙醇 苯甲酸 乙醚 苯甲酸乙酯
密度/(g·cm3) 0.7893 1.2659 0.7318 1.0500
沸点/℃ 78.5 249.0 34.5 212.0
相对分子质量 46 122 74 150
Ⅰ.合成苯甲酸乙酯粗产品:按图甲装置,在仪器C中加入2.44g苯甲酸、15.0mL乙醇、
3.0mL浓硫酸和适量环己烷(环己烷与乙醇、水可形成共沸物,沸点62.6℃),控制一定温
度加热2h后停止加热。
高三化学试题8第 6 页 共 8 页
{#{QQABAYKtpggw0gTACDwqR0UsCQsQsIOgJaoEBQAUqAQKSQNIBCA=}#}`
(1)仪器A作用是 。
(2)本实验中制取苯甲酸乙酯的化学方程式为 。
(3)实验时加入环己烷的目的是 。
(4)分水器的“分水”原理是冷凝液在分水器中分层,上层有机层从支管处流回烧瓶,下层
水层从分水器下口放出,反应结束的标志是 。
Ⅱ.粗产品的精制:将仪器C中的反应液倒入盛有水的烧杯中,滴加饱和Na CO 溶液至
2 3
溶液呈中性,用分液漏斗分出有机层,再用乙醚萃取水层中的残留产品,将二者合并转
移至图乙的仪器D中,加入沸石和无水氯化钙,加热蒸馏,制得产品2.4mL。
(5)仪器D的名称是 。
(6)加入饱和Na CO 溶液的目的是为了除去 。
2 3
(7)采用图乙装置进行蒸馏操作,收集 ℃左右的馏分。
实际产量
(8)该实验中苯甲酸乙酯的产率是 (产率 100%)。
理论产量
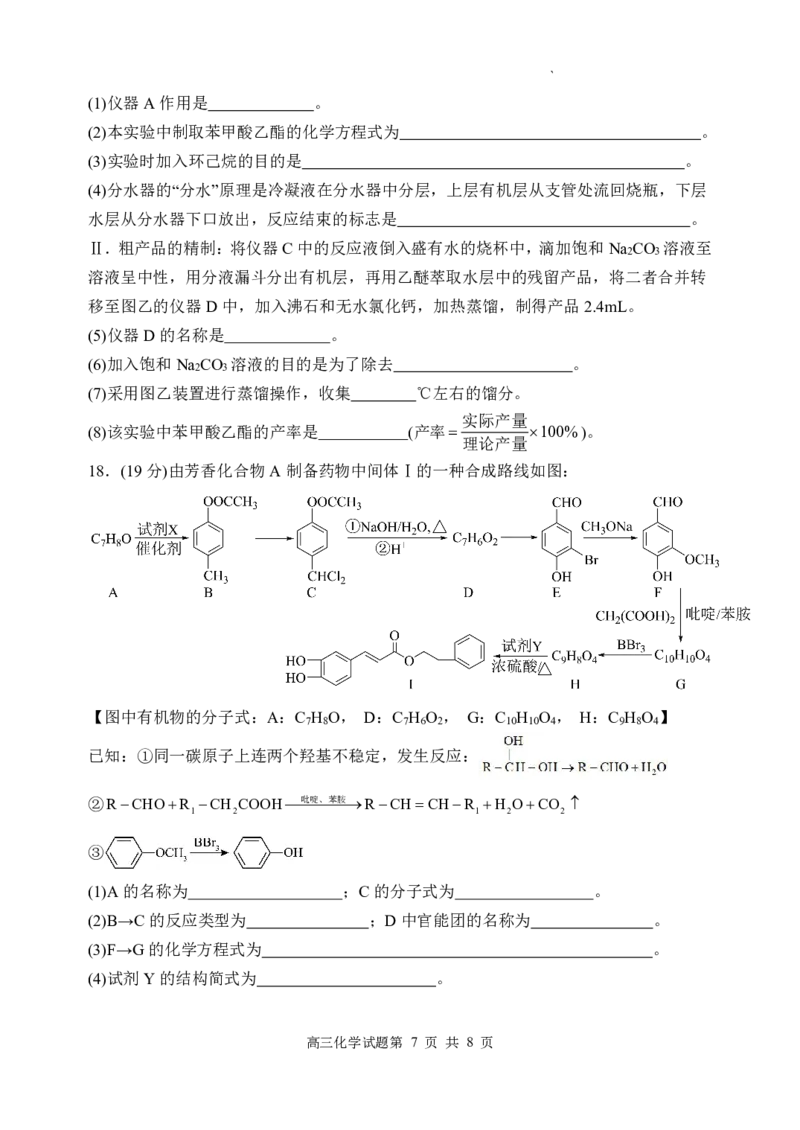
18.(19分)由芳香化合物A制备药物中间体Ⅰ的一种合成路线如图:
【图中有机物的分子式:A:C H O, D:C H O , G:C H O , H:C H O 】
7 8 7 6 2 10 10 4 9 8 4
已知:①同一碳原子上连两个羟基不稳定,发生反应:
②RCHOR CH COOH吡啶、苯胺RCHCHR H OCO
1 2 1 2 2
③
(1)A的名称为 ;C的分子式为 。
(2)B→C的反应类型为 ;D中官能团的名称为 。
(3)F→G的化学方程式为 。
(4)试剂Y的结构简式为 。
高三化学试题8第 7 页 共 8 页
{#{QQABAYKtpggw0gTACDwqR0UsCQsQsIOgJaoEBQAUqAQKSQNIBCA=}#}`
(5)同时满足下列条件的G的同分异构体有 种(不含立体异构)。
①苯环上只有两个取代基 ②只有一种官能团且能与NaHCO 溶液反应放出气体
3
其中核磁共振氢谱显示有3组峰,且峰面积之比为2:2:1的同分异构体的一种结构简式
为 。
(6) 参照上述合成路线,设计由CH CH CHCl 制备CH CH CH=CHCH 的合成路线
3 2 2 3 2 3
(有机溶剂及无机试剂任选)。
19.(17分)CO 催化加氢制备甲醇可以减少CO 的排放,有利于实现碳中和。在一定条
2 2
件下,CO 和H 可发生如下反应:
2 2
Ⅰ.CO (g)+3H (g) CH OH(g)+H O(g) △H K
2 2 3 2 1 1
Ⅱ.CO(g)+2H (g) CH OH(g) △H =+45.5kJ·mol-1 K
2 3 2 2
Ⅲ.CO (g)+H (g) CO(g)+H O(g) △H =-85.5kJ·mol-1 K
2 2 2 3 3
(1)反应热△H
1
= kJmol1。反应Ⅰ和反应Ⅱ的平衡常数分别为K
1
=24、K
2
=3,
则反应Ⅲ的平衡常数K = 。
3
(2)研究反应Ⅰ的速率方程,实验数据如下:
实验 c(CO )/mol·L-1 c(H )/mol·L-1 初始速率/mol·L-1·min-1
2 2
1 0.5 1.0 0.05
2 1.0 1.0 0.10
3 1.0 2.0 0.80
已知速率方程的表达式为v=k·cm(CO )·cn(H ),根据表格数据,计算m= ,n= 。
2 2
(3) 现向恒温恒压(10MPa)的密闭容器中充入1molCO 、2.5molH 和2.5molHe,假定只
2 2
发生反应Ⅰ,一段时间后达到平衡,CO 的平衡转化率为50%。回答下列问题:
2
①下列叙述能说明反应达到平衡状态的是 。
A. 容器内气体的压强不再发生改变 B.CO 的体积分数不再变化
2
C.3molH—H断裂的同时,断裂2molO—H D. 混合气体的密度不再变化
②在恒温恒压下,与未充入稀有气体He相比,采取充入稀有气体He,反应物的平衡转
化率如何改变并解释其原因 。
③反应Ⅰ的平衡常数K = MPa-2(分压=总压×物质的量分数)
p
(4)一定条件下,向体积为1L的恒容密闭容器中通入1.0molCO 和3.0molH ,发生反应
2 2
I、Ⅱ、Ⅲ,达到平衡时,容器中n(CH OH)为0.15mol,n(CO)为0.07mol,n(H O)为0.22mol,
3 2
则反应I的平衡常数为 L2mol2(用计算式表示,无需化简)。
高三化学试题8第 8 页 共 8 页
{#{QQABAYKtpggw0gTACDwqR0UsCQsQsIOgJaoEBQAUqAQKSQNIBCA=}#}