文档内容
参照机密级管理★启用前
河南省 2025 年高考综合改革适应性演练
化 学
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如
需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。
写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Si 28
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1.我国传统手工艺品是劳动人民的智慧结晶,并随着时代发展不断创新。下列手工艺品中主
要成分为无机物的是( )
A.云锦 B.牡丹瓷 C.麦秆画 D.油纸伞
2.下列化学用语或图示正确的是( )
2
A.CaO的电子式:Ca2 : O :
B.Li的结构示意 图:
C.中子数为38的镓原子:38Ga
31
D. 的化学名称:2乙基戊烷
化学试题第1页(共10页)
学科网(北京)股份有限公司3.W是一种短周期金属元素的单质,V是无色气体。它们之间的转化关系如图所示(略去部分
生成物和反应条件)。下列说法错误的是( )
A.气体V可通过排水法收集
B.X与水反应能生成气体V
C.Y易溶于水,溶液显碱性
D.电解Z的水溶液可得到W
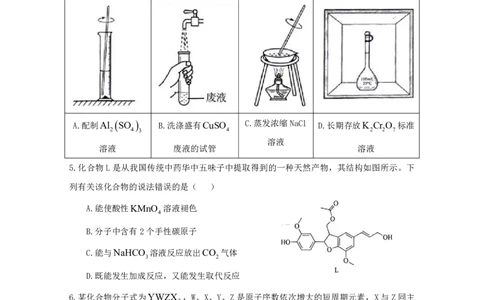
4.下列图示中,操作规范的是( )
A.配制Al SO B.洗涤盛有CuSO C.蒸发浓缩NaCl D.长期存放K Cr O 标准
2 4 3 4 2 2 7
溶液
溶液 废液的试管 溶液
5.化合物L是从我国传统中药华中五味子中提取得到的一种天然产物,其结构如图所示。下
列有关该化合物的说法错误的是( )
A.能使酸性KMnO 溶液褪色
4
B.分子中含有2个手性碳原子
C.能与NaHCO 溶液反应放出CO 气体
3 2
D.既能发生加成反应,又能发生取代反应
6.某化合物分子式为YWZX ,W、X、Y、Z是原子序数依次增大的短周期元素,X与Z同主
2
族,W与X质子数之和等于Z的质子数,Y最外层电子数是其内层电子总数的一半。下列说法
正确的是( )
A.电负性:W Y B.WX 的空间结构为直线形
2
C.最简单氢化物的沸点:XZ D.Y的第一电离能高于同周期相邻元素
化学试题第2页(共10页)
学科网(北京)股份有限公司7.对于下列过程中发生的化学反应,相应离子方程式正确的是( )
A.向浓硝酸中加入少量氧化亚铜:Cu O2H CuCu2 H O
2 2
Δ
B.以热氢氧化钠溶液洗涤附着在试管内壁的少量硫: 3S6OH 2S2SO23H O
3 2
C.醋酸铵的水解:NH H O NH H OH
4 2 3 2
D.向碘酸钾溶液中滴加双氧水:H O 2IO 6H I 2O 4H O
2 2 3 2 2 2
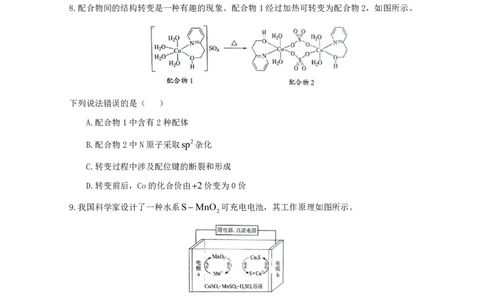
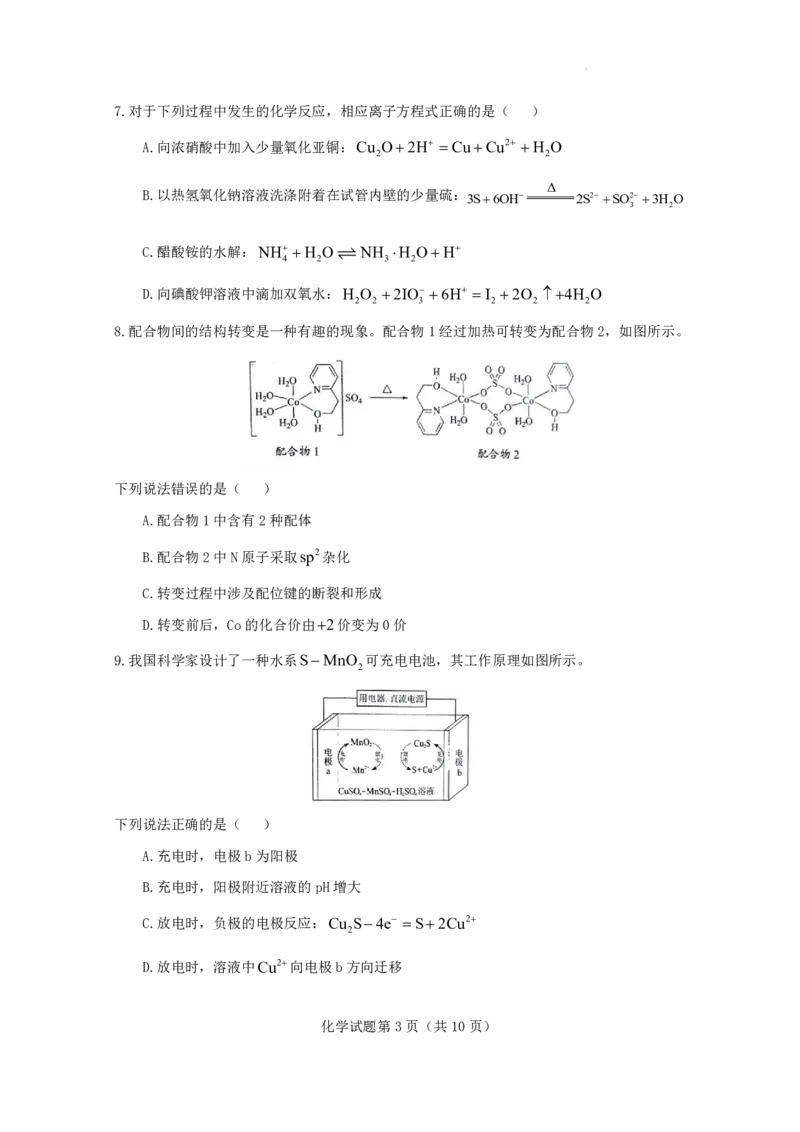
8.配合物间的结构转变是一种有趣的现象。配合物1经过加热可转变为配合物2,如图所示。
下列说法错误的是( )
A.配合物1中含有2种配体
B.配合物2中N原子采取sp2杂化
C.转变过程中涉及配位键的断裂和形成
D.转变前后,Co的化合价由2价变为0价
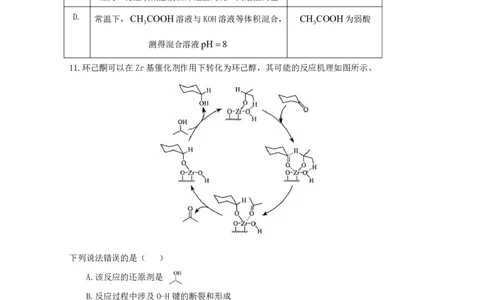
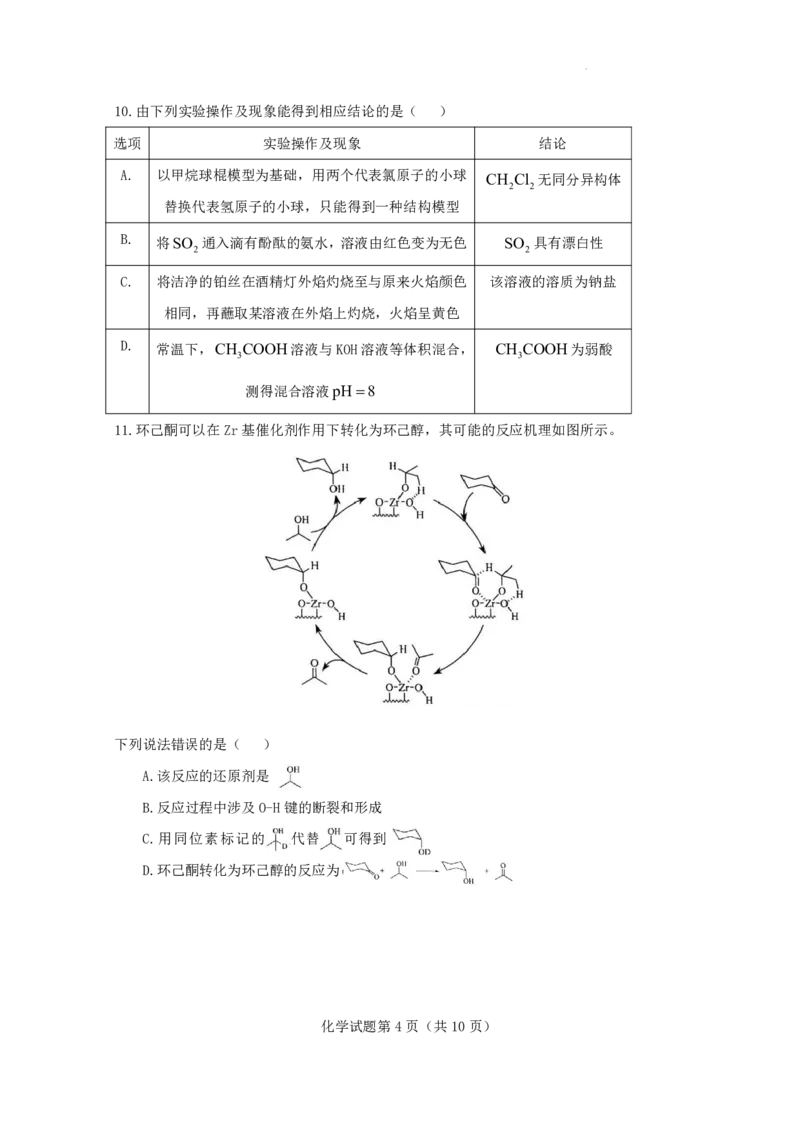
9.我国科学家设计了一种水系SMnO 可充电电池,其工作原理如图所示。
2
下列说法正确的是( )
A.充电时,电极b为阳极
B.充电时,阳极附近溶液的pH增大
C.放电时,负极的电极反应:Cu S4e S2Cu2
2
D.放电时,溶液中Cu2向电极b方向迁移
化学试题第3页(共10页)
学科网(北京)股份有限公司10.由下列实验操作及现象能得到相应结论的是( )
选项 实验操作及现象 结论
A. 以甲烷球棍模型为基础,用两个代表氯原子的小球
CH Cl 无同分异构体
2 2
替换代表氢原子的小球,只能得到一种结构模型
B.
将SO 通入滴有酚酞的氨水,溶液由红色变为无色 SO 具有漂白性
2 2
C. 将洁净的铂丝在酒精灯外焰灼烧至与原来火焰颜色 该溶液的溶质为钠盐
相同,再蘸取某溶液在外焰上灼烧,火焰呈黄色
D.
常温下,CH COOH溶液与KOH溶液等体积混合, CH COOH为弱酸
3 3
测得混合溶液pH8
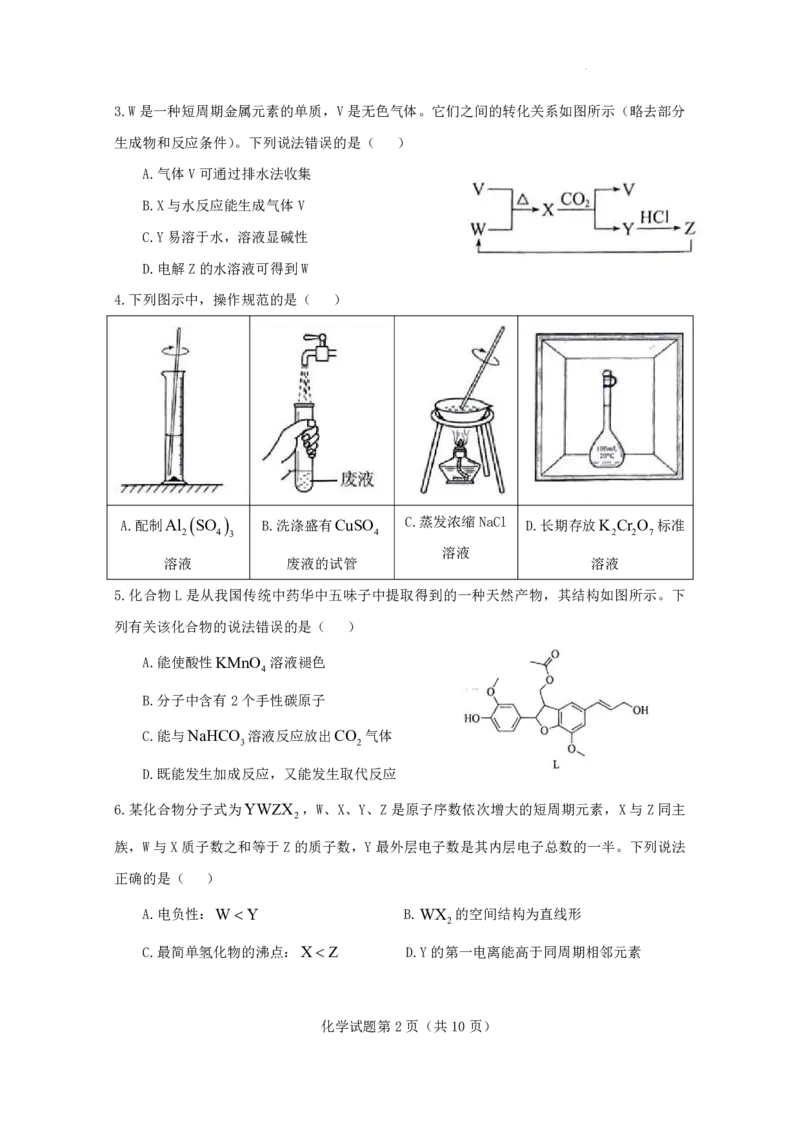
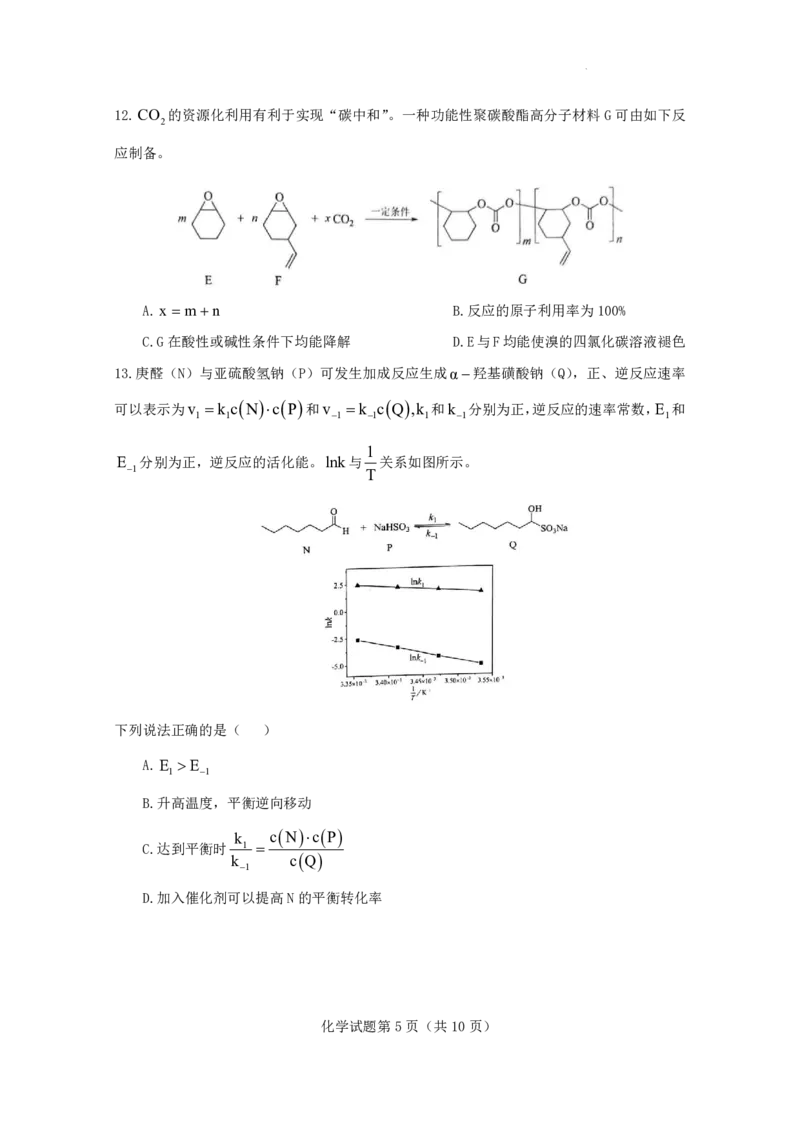
11.环己酮可以在Zr基催化剂作用下转化为环己醇,其可能的反应机理如图所示。
下列说法错误的是( )
A.该反应的还原剂是
B.反应过程中涉及O-H键的断裂和形成
C.用同位素标记的 代替 可得到
D.环己酮转化为环己醇的反应为
化学试题第4页(共10页)
学科网(北京)股份有限公司12.CO 的资源化利用有利于实现“碳中和”。一种功能性聚碳酸酯高分子材料G可由如下反
2
应制备。
A.x mn B.反应的原子利用率为100%
C.G在酸性或碱性条件下均能降解 D.E与F均能使溴的四氯化碳溶液褪色
13.庚醛(N)与亚硫酸氢钠(P)可发生加成反应生成α羟基磺酸钠(Q),正、逆反应速率
可以表示为v k c N c P 和v k c Q ,k 和k 分别为正,逆反应的速率常数,E 和
1 1 1 1 1 1 1
1
E 分别为正,逆反应的活化能。lnk与 关系如图所示。
1
T
下列说法正确的是( )
A.E E
1 1
B.升高温度,平衡逆向移动
k c
N
c
P
C.达到平衡时 1
k c Q
1
D.加入催化剂可以提高N的平衡转化率
化学试题第5页(共10页)
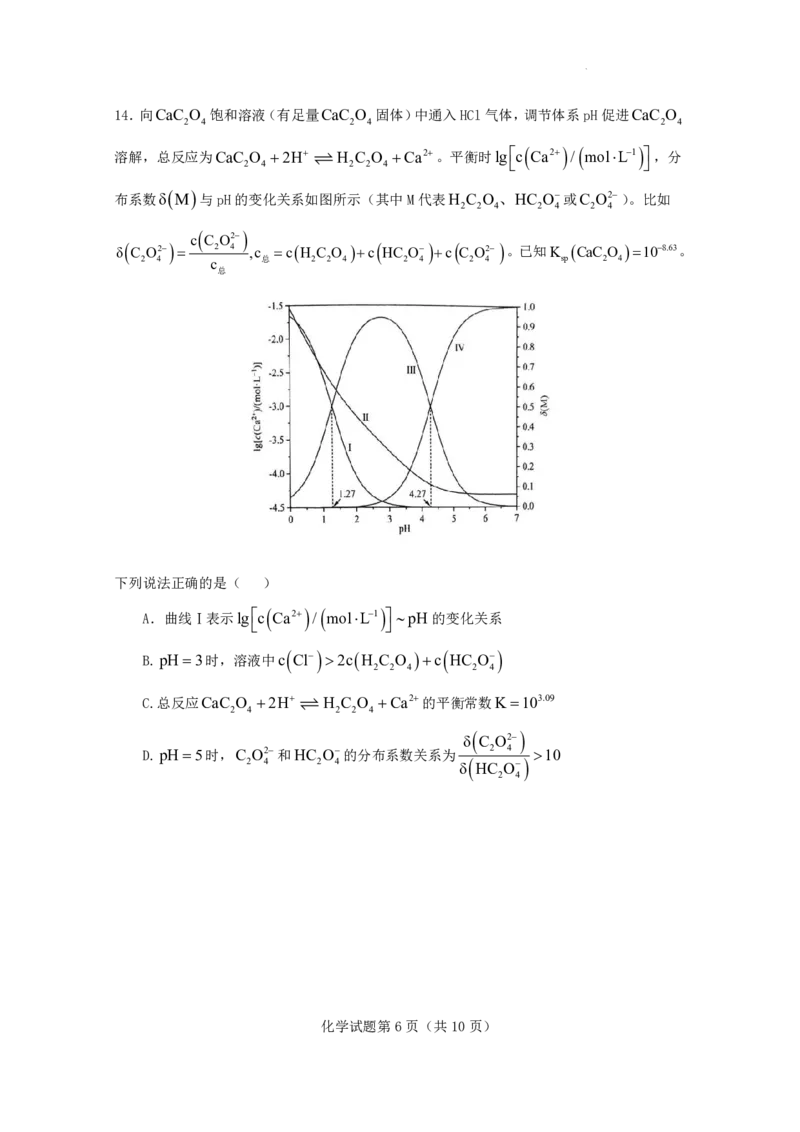
学科网(北京)股份有限公司14.向CaC O 饱和溶液(有足量CaC O 固体)中通入HCl气体,调节体系pH促进CaC O
2 4 2 4 2 4
溶解,总反应为CaC O 2H H C O Ca2。平衡时lgc Ca2 / molL1 ,分
2 4 2 2 4
布系数δ M 与pH的变化关系如图所示(其中M代表H C O 、HC O或C O2)。比如
2 2 4 2 4 2 4
c
C
O2
δ C O2 2 4 ,c cH C O c HC O c C O2 。已知K CaC O 108.63。
2 4 c 总 2 2 4 2 4 2 4 sp 2 4
总
下列说法正确的是( )
A.曲线Ⅰ表示lgc Ca2 / molL1 pH 的变化关系
B.pH3时,溶液中c Cl 2c H C O c HC O
2 2 4 2 4
C.总反应CaC O 2H H C O Ca2的平衡常数K103.09
2 4 2 2 4
δ
C
O2
D.pH5时,C O2和HC O的分布系数关系为 2 4 10
2 4 2 4
δ
HC
O
2 4
化学试题第6页(共10页)
学科网(北京)股份有限公司二、非选择题:本题共4小题,共58分。
15.( 14 分 ) 一 种 利 用 钛 白 粉 副 产 品 [ 主 要 成 分 为 FeSO 7H O , 含 有 少 量
4 2
Fe SO 、TiOSO 、MgSO 、MnSO 等]和农药盐渣(主要成分为Na PO 、Na SO
2 4 3 4 4 4 3 4 2 3
等)制备电池级磷酸铁的工艺流程如下。
一定条件下,一些金属氟化物的K 如下表。
sp
氟化物 FeF MgF MnF
2 2 2
K 2.3106 5.11011 5.2103
sp
回答下列问题:
(1)“除钳”中产生的少量气体是____________(填化学式);铁粉的作用之一是提高体
系的pH,使得TiO2水解以TiO xH O沉淀形式除去,其另一个作用是____________。
2 2
(2)“除杂1”中除去的离子是____________(填化学式)。
(3)“氧化1”中若H O 加入速度过快,会导致H O 用量增大,原因是____________。
2 2 2 2
本步骤不能使用稀盐酸代替H SO 溶液,原因是____________。
2 4
(4)滤渣3的主要成分是MnO xH O,生成该物质的离子方程式为____________。
2 2
(5)“氧化2”的目的是减少____________气体的排放(填化学式)。
(6)“沉铁”中如果体系酸性过强,会导致FePO 2H O 产量降低,原因是____________。
4 2
化学试题第7页(共10页)
学科网(北京)股份有限公司16.(14分)
某实验小组利用EDTA标准溶液滴定Ca2,从而间接测定Na CO 、NaFCO 混合溶液
2 3 3
中CO2和HCO的总浓度。已知EDTA与Ca2按物质的量之比1:1反应。
3 3
主要实验步骤如下:
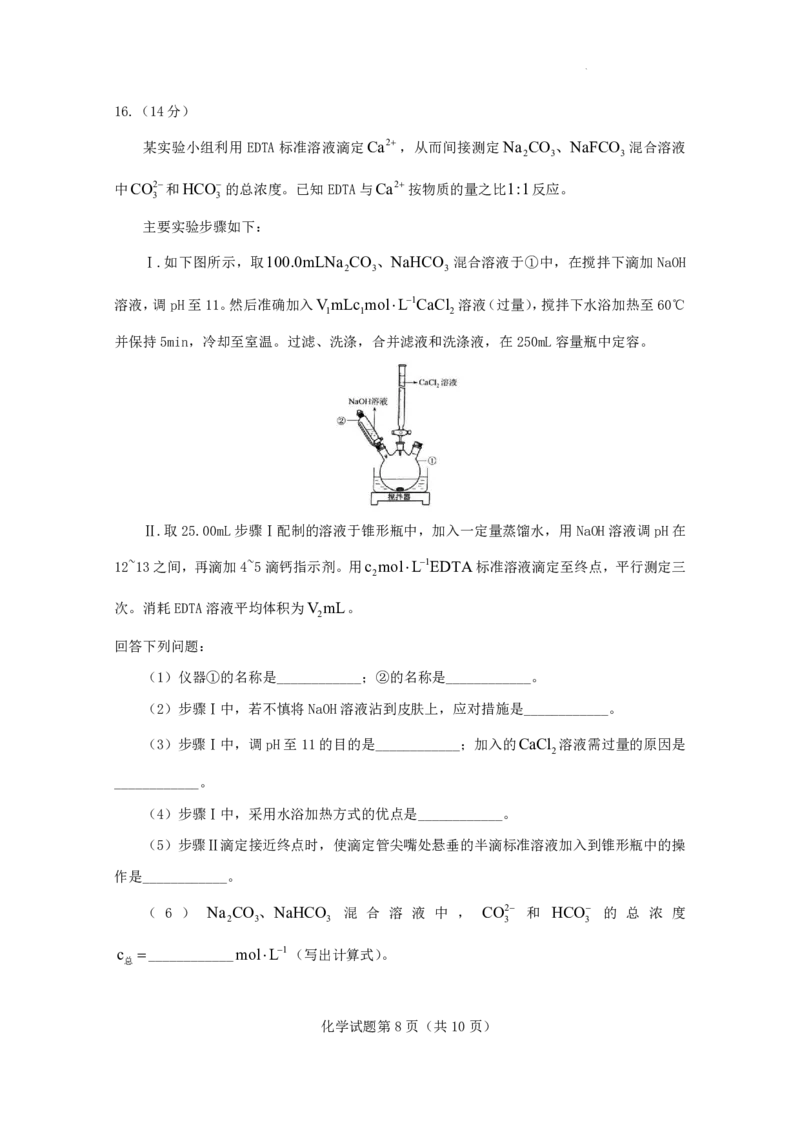
Ⅰ.如下图所示,取100.0mLNa CO 、NaHCO 混合溶液于①中,在搅拌下滴加NaOH
2 3 3
溶液,调pH至11。然后准确加入VmLc molL1CaCl 溶液(过量),搅拌下水浴加热至60℃
1 1 2
并保持5min,冷却至室温。过滤、洗涤,合并滤液和洗涤液,在250mL容量瓶中定容。
Ⅱ.取25.00mL步骤Ⅰ配制的溶液于锥形瓶中,加入一定量蒸馏水,用NaOH溶液调pH在
12~13之间,再滴加4~5滴钙指示剂。用c molL1EDTA标准溶液滴定至终点,平行测定三
2
次。消耗EDTA溶液平均体积为V mL。
2
回答下列问题:
(1)仪器①的名称是____________;②的名称是____________。
(2)步骤Ⅰ中,若不慎将NaOH溶液沾到皮肤上,应对措施是____________。
(3)步骤Ⅰ中,调pH至11的目的是____________;加入的CaCl 溶液需过量的原因是
2
____________。
(4)步骤Ⅰ中,采用水浴加热方式的优点是____________。
(5)步骤Ⅱ滴定接近终点时,使滴定管尖嘴处悬垂的半滴标准溶液加入到锥形瓶中的操
作是____________。
( 6 ) Na CO 、NaHCO 混 合 溶 液 中 , CO2 和 HCO 的 总 浓 度
2 3 3 3 3
c ____________molL1(写出计算式)。
总
化学试题第8页(共10页)
学科网(北京)股份有限公司17.(15分)
硅是电子工业中应用最为广泛的半导体材料,少量磷的掺入可提高硅的导电性能。Zn高
温还原SiCl (沸点27.6℃)是生产多晶硅的一种方法。
4
回答下列问题:
(1)基态Zn原子的价电子排布式为____________,SiCl 晶体的类型为____________。
4
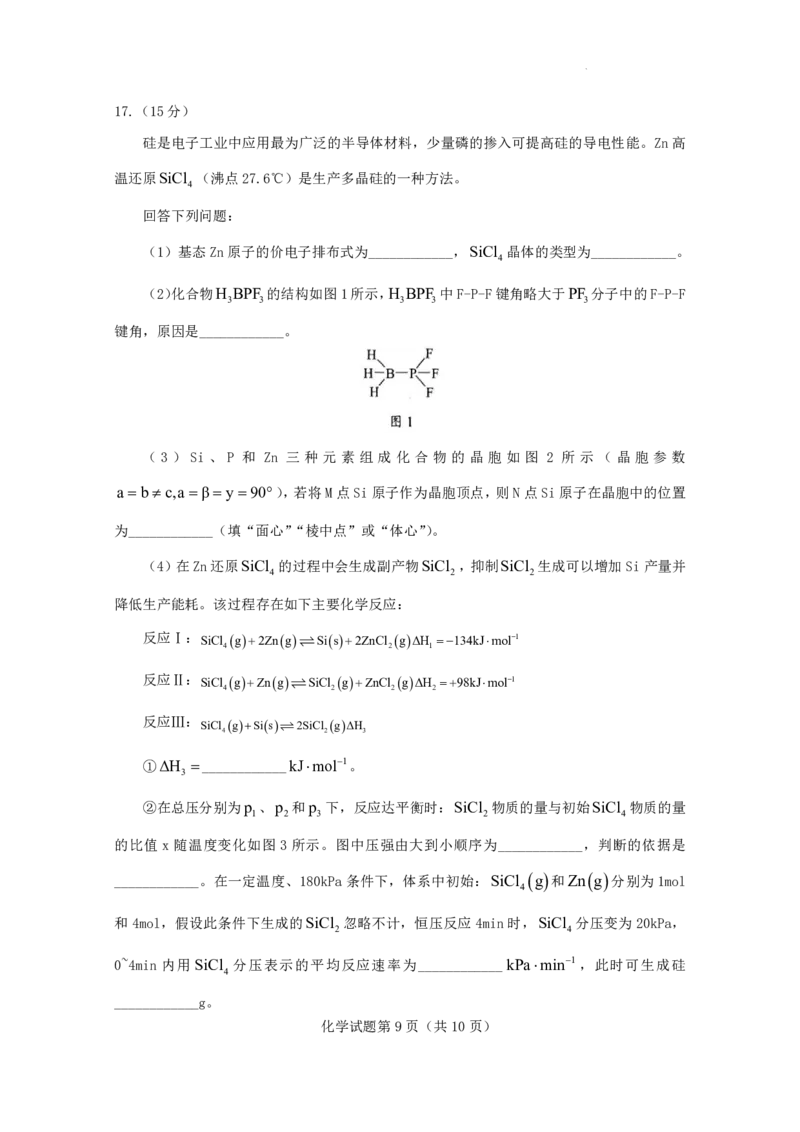
(2)化合物H BPF 的结构如图1所示,H BPF 中F-P-F键角略大于PF 分子中的F-P-F
3 3 3 3 3
键角,原因是____________。
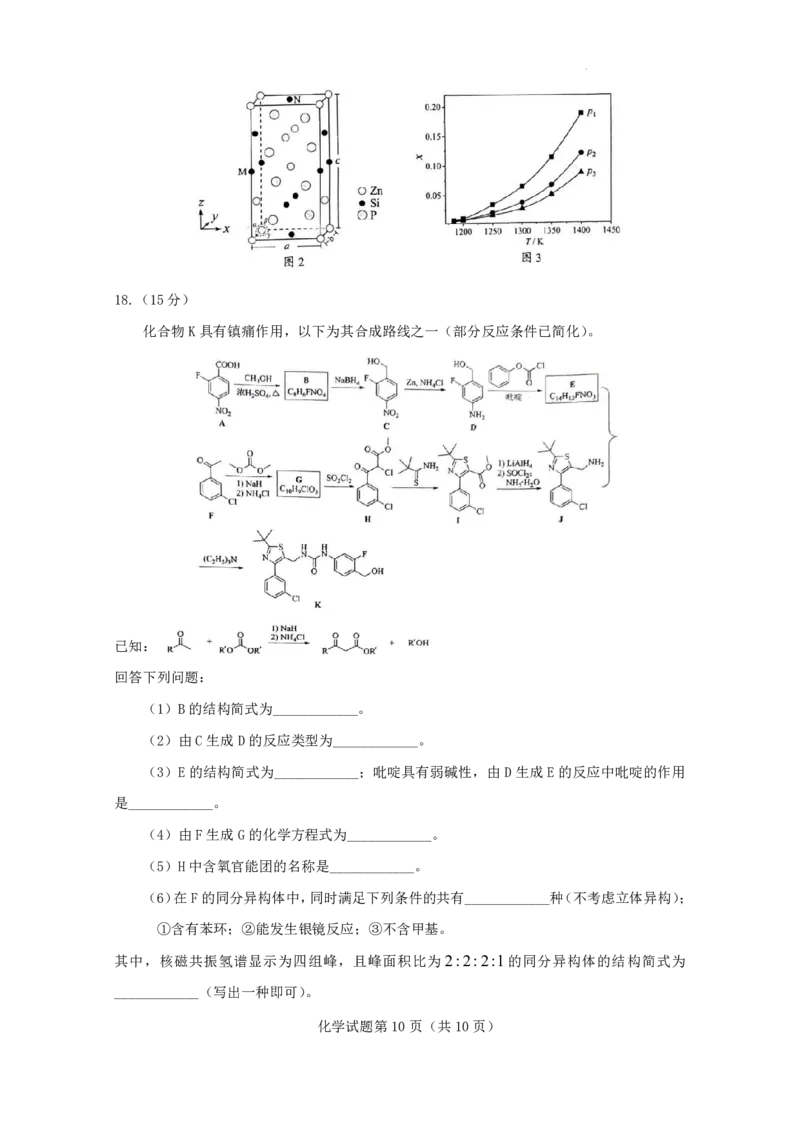
( 3 ) Si 、 P 和 Zn 三 种 元 素 组 成 化 合 物 的 晶 胞 如 图 2 所 示 ( 晶 胞 参 数
a bc,a β y90),若将M点Si原子作为晶胞顶点,则N点Si原子在晶胞中的位置
为____________(填“面心”“棱中点”或“体心”)。
(4)在Zn还原SiCl 的过程中会生成副产物SiCl ,抑制SiCl 生成可以增加Si产量并
4 2 2
降低生产能耗。该过程存在如下主要化学反应:
反应Ⅰ: SiCl g2Zng Sis2ZnCl gΔH 134kJmol1
4 2 1
反应Ⅱ: SiCl gZng SiCl gZnCl gΔH 98kJmol1
4 2 2 2
反应Ⅲ: SiCl gSis2SiCl gΔH
4 2 3
①ΔH ____________kJmol1。
3
②在总压分别为p 、p 和p 下,反应达平衡时:SiCl 物质的量与初始SiCl 物质的量
1 2 3 2 4
的比值 x 随温度变化如图 3 所示。图中压强由大到小顺序为____________,判断的依据是
____________。在一定温度、180kPa条件下,体系中初始:SiCl g 和Zn g 分别为1mol
4
和4mol,假设此条件下生成的SiCl 忽略不计,恒压反应4min时,SiCl 分压变为20kPa,
2 4
0~4min 内用SiCl 分压表示的平均反应速率为____________kPamin1,此时可生成硅
4
____________g。
化学试题第9页(共10页)
学科网(北京)股份有限公司18.(15分)
化合物K具有镇痛作用,以下为其合成路线之一(部分反应条件已简化)。
已知:
回答下列问题:
(1)B的结构简式为____________。
(2)由C生成D的反应类型为____________。
(3)E的结构简式为____________;吡啶具有弱碱性,由D生成E的反应中吡啶的作用
是____________。
(4)由F生成G的化学方程式为____________。
(5)H中含氧官能团的名称是____________。
(6)在F的同分异构体中,同时满足下列条件的共有____________种(不考虑立体异构);
①含有苯环;②能发生银镜反应;③不含甲基。
其中,核磁共振氢谱显示为四组峰,且峰面积比为2:2:2:1的同分异构体的结构简式为
____________(写出一种即可)。
化学试题第10页(共10页)
学科网(北京)股份有限公司