文档内容
2025/2026 学年度第一学期
联盟校第一次联考高三年级化学试题
(总分 100 份 考试时间 75 分
钟) 注意事项:
1. 本试卷中所有试题必须作答在答题纸上规定的位置,否则不给分。
2.答题前,务必将自己的姓名、准考证号用 0.5 毫米黑色墨水签字笔填写在试卷及
答题纸上。
3.作答非选择题时必须用黑色字迹 0.5 毫米签字笔书写在答题纸的指定位置上,作
答选择题必须用 2B 铅笔在答题纸上将对应题目的选项涂黑。如需改动,请用橡皮
擦干净后,再选涂其它答案,请保持答题纸清洁,不折叠、不破损。
一、单项选择题:共 14 小题,每题 3 分,共 42 分。每题只有一个选项最符合题意。
1. 我国承诺 2060 年前实现碳中和:碳中和是指通过植树造林、节能减排等形式,
抵消自身产生的二氧化碳排放量,实现二氧化碳“零排放”。下列不利于实现“碳中和
”的是 ( )
A. 植树造林 B. 节能减排 C. 焚烧秸秆 D. 风力发电
2. 反应 可用于石油开采。下列说法正确的是
( )
A.NH Cl 中只含有离子键 B.NH 的电子式为
4 3
C.Na+ 和 Cl-具有相同的电子层结构 D. 基态 N 原子的核外电子排布式:1s22s22p3
3. 对 Na、Mg、Al 有关性质的叙述,错误的是 ( )
A. 金属性:Na>Mg>Al B. 第一电离能:NaMg>Al
4.下列从含 Br 的稀溶液中提取 Br 的实验操作或原理能达到目的的是 ( )
2 2
A.用装置甲吹出 Br 蒸气并吸收 B.用装置乙制取 Cl
2 2
C.用装置丙制取 Br D.用装置丁蒸馏回收 Br
2 2
阅读下列材料,完成 5~7 题:N 是合成氨的重要原料。NH 可在 O 中燃烧生成 N ;NH 广泛用于硝酸、侯
2 3 2 2 3
氏制碱等工业;NH 也是其他含氮化合物的生产原料。金属钠与液氨缓慢反应放出
3
气体,同时生成 NaNH ,NaNH 遇水转化为 NaOH。Cu(OH) 溶于氨水得到深蓝色
2 2 2
[Cu(NH ) ](OH) 溶液,加入稀硫酸又转化为蓝色[Cu(H O) ]SO 溶液。氨水可用于
3 4 2 2 4 4
吸收废气中的 SO ,废水中的氨氮可用 NaClO 溶液将其氧化为 N 而除去。
2 2
5. 在指定条件下,下列选项中的物质间转化可以实现的是 ( )
A.NH NO HNO
3 3
B.NH N NO
3 2 2
C.过量氨水吸收废气中的 SO 生成(NH ) SO
2 4 2 3
D.将 CO 通入氨化的 NaCl 饱和溶液中可析出纯碱
2
6. 下列化学反应表示不正确的是 ( )
A. 合成氨反应:
B. 液氨与金属钠反应:2Na+2NH =2NaNH +H ↑
3 2 2
C. 氨水溶解 Cu(OH) :Cu(OH) +4NH ·H O=[Cu(NH ) ]2++2OH-+4H O
2 2 3 2 3 4 2
D. 常温,pH为 4 的氨氮废水与NaClO反应:3ClO-+2NH ·H O=N ↑+3Cl-+5H O
3 2 2 2
7. 下列有关物质性质的比较中,正确的是 ( )
A. 热稳定性:NH >H O B. 溶解度:NaHCO >NH HCO
3 2 3 4 3
C. 与氨形成配位键的能力:H+ >Cu2+ D. 与 H+ 结合的能力:OH- >
8. CCTV 报道,解放军总后勤部提出要让每个野外作业的战士都吃上热饭菜,其中
一种方法是利用原电池原理,将食盐颗粒、炭屑、铁屑装入食品包装的夹层中密封
起来,使用时撕开一口子,加入适量水振荡,就会产生热量加热食品。以下叙述正
确的是 ( )
A. 铁作负极,发生氧化反应 B. 碳作负极,发生还原反应
C.铁作正极,发生还原反应 D. 碳作正极,发生氧化反应
9. 在指定条件下,下列选项所示的物质间转化能实现的是 ( )
A.
B.
C.
D.10. 氧化亚铜常用于制船底防污漆。用 CuO 与 Cu 高温烧结可制取 Cu O,已知反应:
2
则 的 等于 ( )
A. B. C. D.
11.下列物质性质与应用对应关系正确的是 ( )
A.漂白粉在空气中不稳定,可用于漂白纸张
B.医用酒精能使蛋白质变性,可用于消毒杀菌
C.二氧化硅不与强酸反应,可用石英器皿盛放氢氟酸
D.铜的金属活泼性比铁的弱,可在铁闸上装若干铜块以减缓其腐蚀
12. 某抗凝血作用的药物 Z 可用下列反应合成。下列说法正确的是 ( )
A.X 与 NaHCO 溶液反应可以生成
3
B.1mol Y 与 NaOH 溶液反应,最多消耗 2mol NaOH
C.Z 与足量的氢气加成后的产物分子中含有 2 个手性碳原子
D.X、Y、Z 均易溶于水
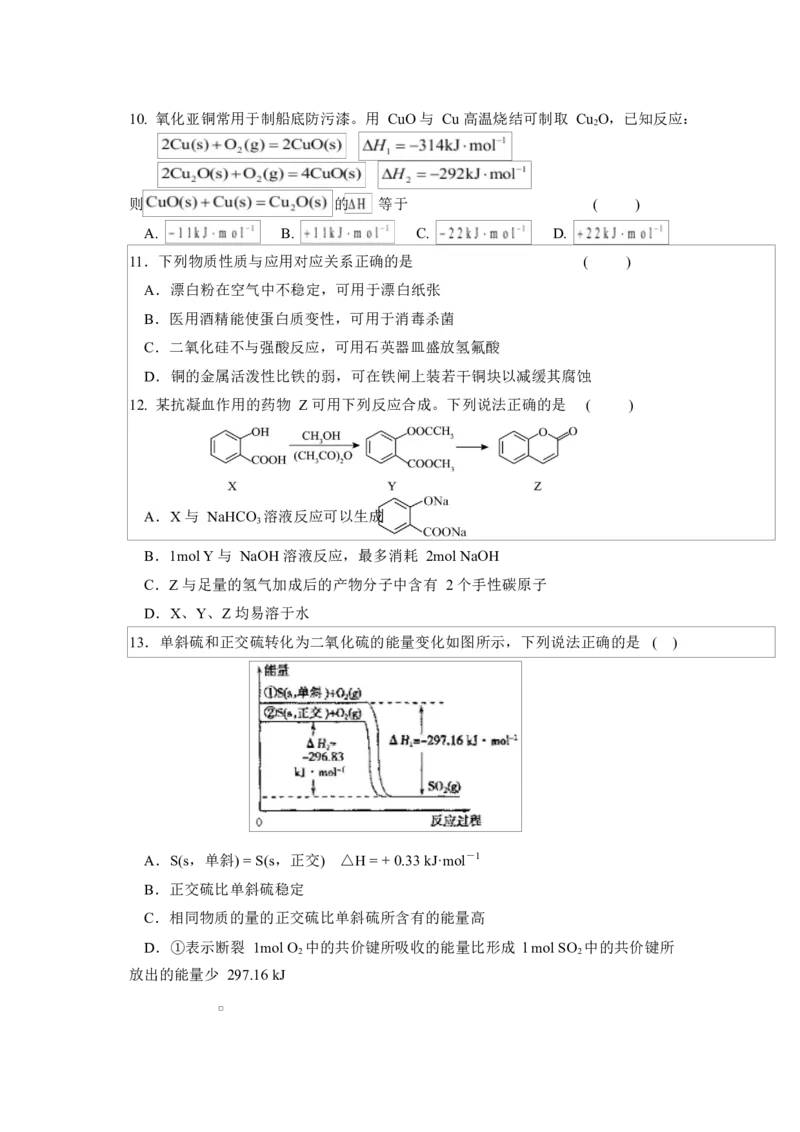
13.单斜硫和正交硫转化为二氧化硫的能量变化如图所示,下列说法正确的是 ( )
A.S(s,单斜) = S(s,正交) △H = + 0.33 kJ·mol-1
B.正交硫比单斜硫稳定
C.相同物质的量的正交硫比单斜硫所含有的能量高
D.①表示断裂 1mol O 中的共价键所吸收的能量比形成 l mol SO 中的共价键所
2 2
放出的能量少 297.16 kJ14. 室温下,下列实验探究方案能达到探究目的的是 ( )
选项 探究方案 探究目的
向 探究 与
A 溶液中滴入硫 氧
酸酸化的
溶液,观 化性强弱
察溶液颜色变
化
用 pH 计分别 探究键的极
B 测定等体积的 性对羧
溶液和
酸酸性的影响
溶
液
的
p
H
向 20%蔗糖溶液中加入少量稀硫酸,加热,再加入
C 蔗糖未水解
银氨溶液,未出现银镜
向甲、乙两支试管中分别加入
探究反应物浓度对
D
水解平衡的影响
溶液,向甲试管中加入少量 晶体,振荡、静置,
对比观察溶液颜色变化
二、非选择题:本题共 4 小题,共 58 分。
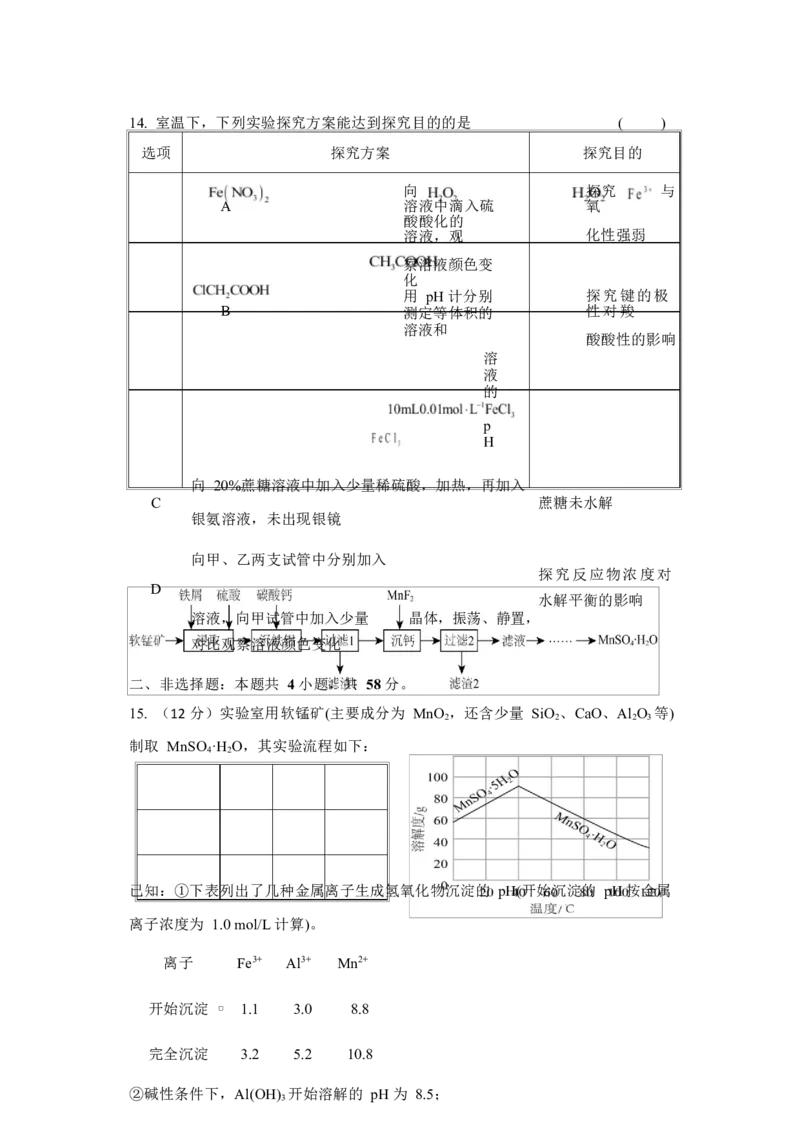
15. (12 分)实验室用软锰矿(主要成分为 MnO ,还含少量 SiO 、CaO、Al O 等)
2 2 2 3
制取 MnSO ·H O,其实验流程如下:
4 2
已知:①下表列出了几种金属离子生成氢氧化物沉淀的 pH(开始沉淀的 pH 按金属
离子浓度为 1.0 mol/L 计算)。
离子 Fe3+ Al3+ Mn2+
开始沉淀 1.1 3.0 8.8
完全沉淀 3.2 5.2 10.8
②碱性条件下,Al(OH) 开始溶解的 pH 为 8.5;
3③硫酸锰晶体的溶解度随温度的变化如所示。(1)"浸取"在题图所示的装置中进行。
①Al O 与硫酸反应的化学方程式为_________________________________;铁屑
2 3
被 MnO 氧化为 Fe3+,该反应的离子方程式为_______________________________。
2
②保持温度、反应物和溶剂的量不变,提高锰元素浸取率的操作有______________
。
(2)"沉铁铝”需控制溶液的 pH 范围为_______________________。
(3)检验“过滤 1”的滤被中是否存在 Fe3+的操作是__________________________。
(4)请补充由“过滤 2”的滤液制备 MnSO ·H O 的实验方案,将所得滤液_______
4 2
__________________________________________________,用无水乙醇洗涤 2~3 次,
干燥,密封包装。
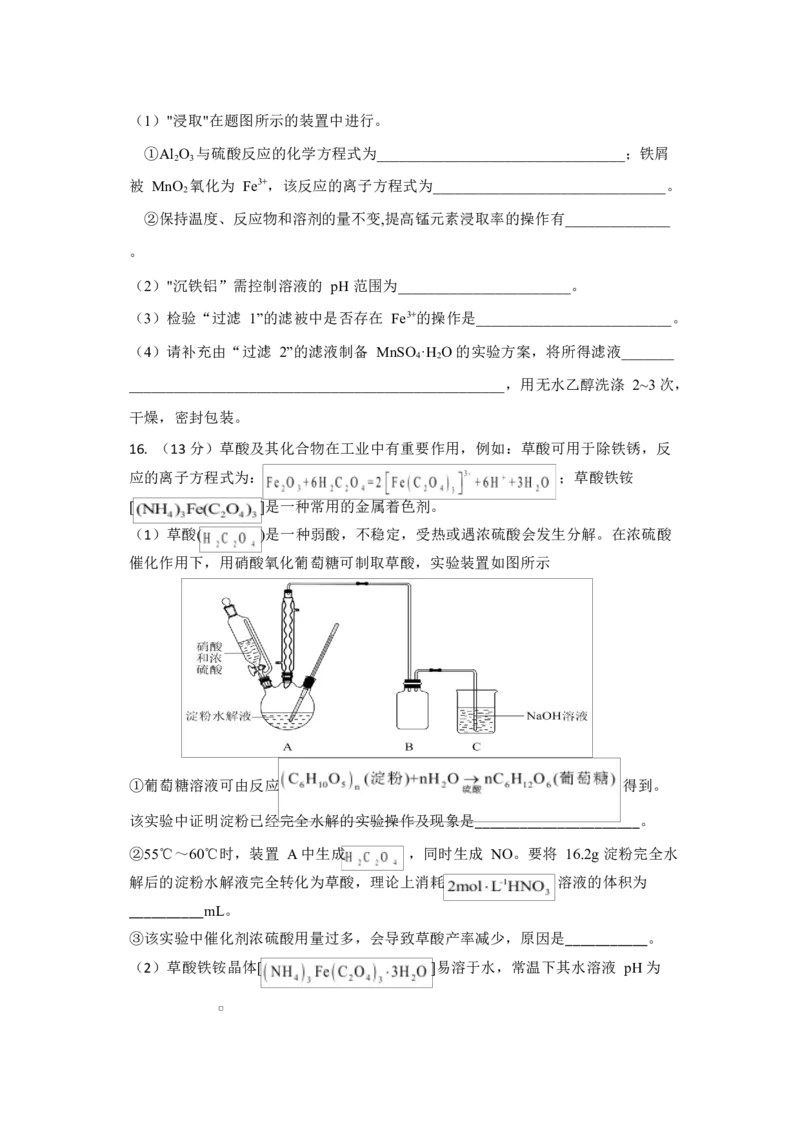
16. (13 分)草酸及其化合物在工业中有重要作用,例如:草酸可用于除铁锈,反
应的离子方程式为: ;草酸铁铵
[ ]是一种常用的金属着色剂。
(1)草酸( )是一种弱酸,不稳定,受热或遇浓硫酸会发生分解。在浓硫酸
催化作用下,用硝酸氧化葡萄糖可制取草酸,实验装置如图所示
①葡萄糖溶液可由反应 得到。
该实验中证明淀粉已经完全水解的实验操作及现象是______________________。
②55℃~60℃时,装置 A 中生成 ,同时生成 NO。要将 16.2g 淀粉完全水
解后的淀粉水解液完全转化为草酸,理论上消耗 溶液的体积为
__________mL。
③该实验中催化剂浓硫酸用量过多,会导致草酸产率减少,原因是___________。
(2)草酸铁铵晶体[ ]易溶于水,常温下其水溶液 pH 为4.0~5.0。设计以 、草酸溶液和氨水为原料,制备草酸铁铵晶体的实验方案:
______________________________________________________________________
_____________________________________________________________________。
(3)制得的草酸铁铵晶体中往往会混有少量草酸,为测定
(M=428g/mol)的含量,进行下列实验:称取样品 9.46g,
加稀硫酸溶解后,配成 100mL 溶液。取 20.00mL 配制的溶液,用浓度为 0.2000mol/L
的 KMnO 溶液滴定至终点时消耗 KMnO 溶液 28.00mL。已知:
4 4
(未配平)。通过计算,确定样品中
的质量分数___________(写出计算过程)。
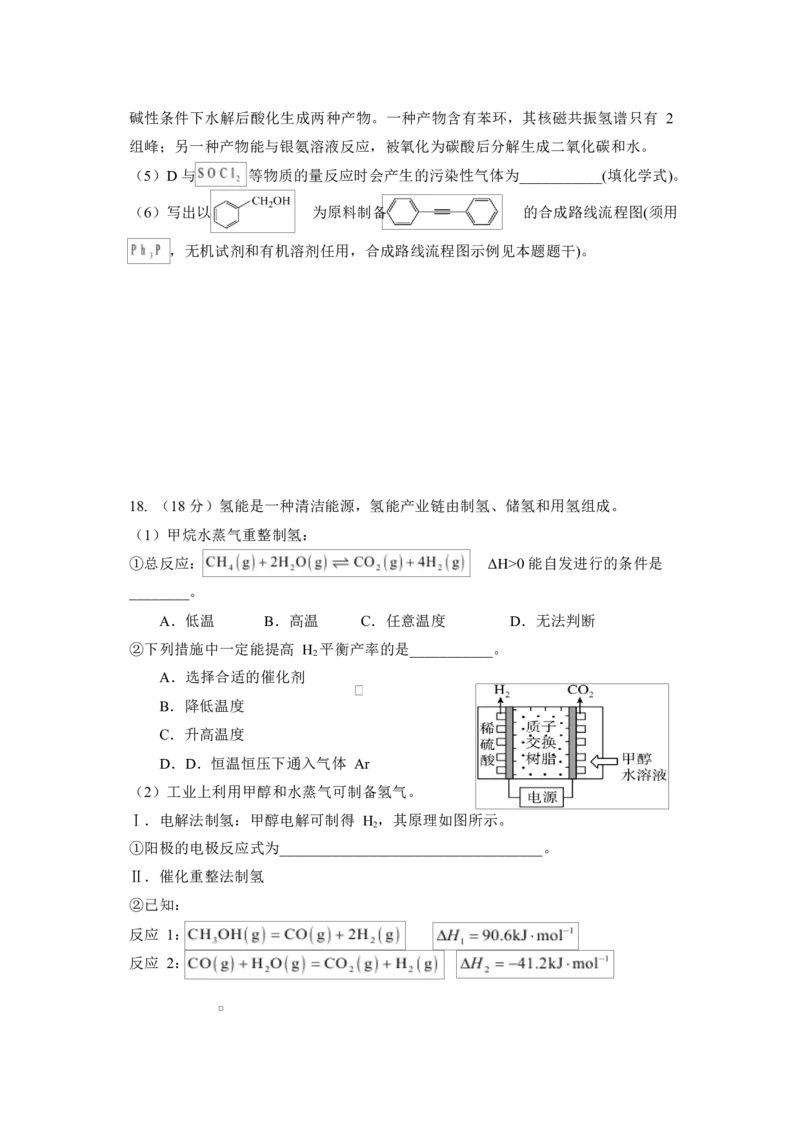
17. (15 分)本维莫德(G)是治疗湿疹的非激素类外用药,其合成路线如下:
其中,-Ph 为苯基( )。
(1)室温下,在水中 A 的溶解度比 B 的___________(填“大”或“小”或“无差别”)。
(2)X 的分子式为 ,常用作甲基化试剂,其结构简式为_________________
。
(3)Y 的分子式为 ,B→C 的反应类型为_________________。
(4)B 的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式_______。碱性条件下水解后酸化生成两种产物。一种产物含有苯环,其核磁共振氢谱只有 2
组峰;另一种产物能与银氨溶液反应,被氧化为碳酸后分解生成二氧化碳和水。
(5)D 与 等物质的量反应时会产生的污染性气体为___________(填化学式)。
(6)写出以 为原料制备 的合成路线流程图(须用
,无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
18. (18 分)氢能是一种清洁能源,氢能产业链由制氢、储氢和用氢组成。
(1)甲烷水蒸气重整制氢:
①总反应: ΔH>0 能自发进行的条件是
________。
A.低温 B.高温 C.任意温度 D.无法判断
②下列措施中一定能提高 H 平衡产率的是___________。
2
A.选择合适的催化剂
B.降低温度
C.升高温度
D.D.恒温恒压下通入气体 Ar
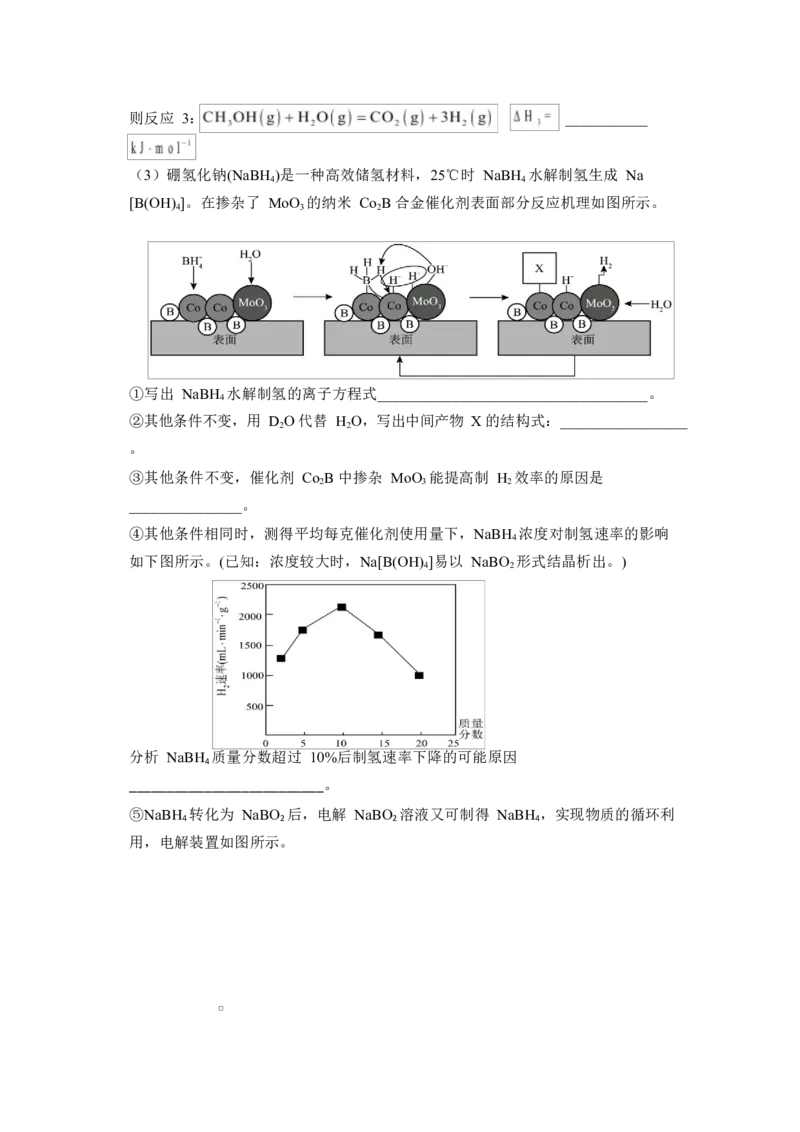
(2)工业上利用甲醇和水蒸气可制备氢气。
Ⅰ.电解法制氢:甲醇电解可制得 H ,其原理如图所示。
2
①阳极的电极反应式为___________________________________。
Ⅱ.催化重整法制氢
②已知:
反应 1:
反应 2:则反应 3: ___________
(3)硼氢化钠(NaBH )是一种高效储氢材料,25℃时 NaBH 水解制氢生成 Na
4 4
[B(OH) ]。在掺杂了 MoO 的纳米 Co B 合金催化剂表面部分反应机理如图所示。
4 3 2
①写出 NaBH 水解制氢的离子方程式____________________________________。
4
②其他条件不变,用 D O 代替 H O,写出中间产物 X 的结构式:_________________
2 2
。
③其他条件不变,催化剂 Co B 中掺杂 MoO 能提高制 H 效率的原因是
2 3 2
_______________。
④其他条件相同时,测得平均每克催化剂使用量下,NaBH 浓度对制氢速率的影响
4
如下图所示。(已知:浓度较大时,Na[B(OH) ]易以 NaBO 形式结晶析出。)
4 2
分析 NaBH 质量分数超过 10%后制氢速率下降的可能原因
4
__________________________。
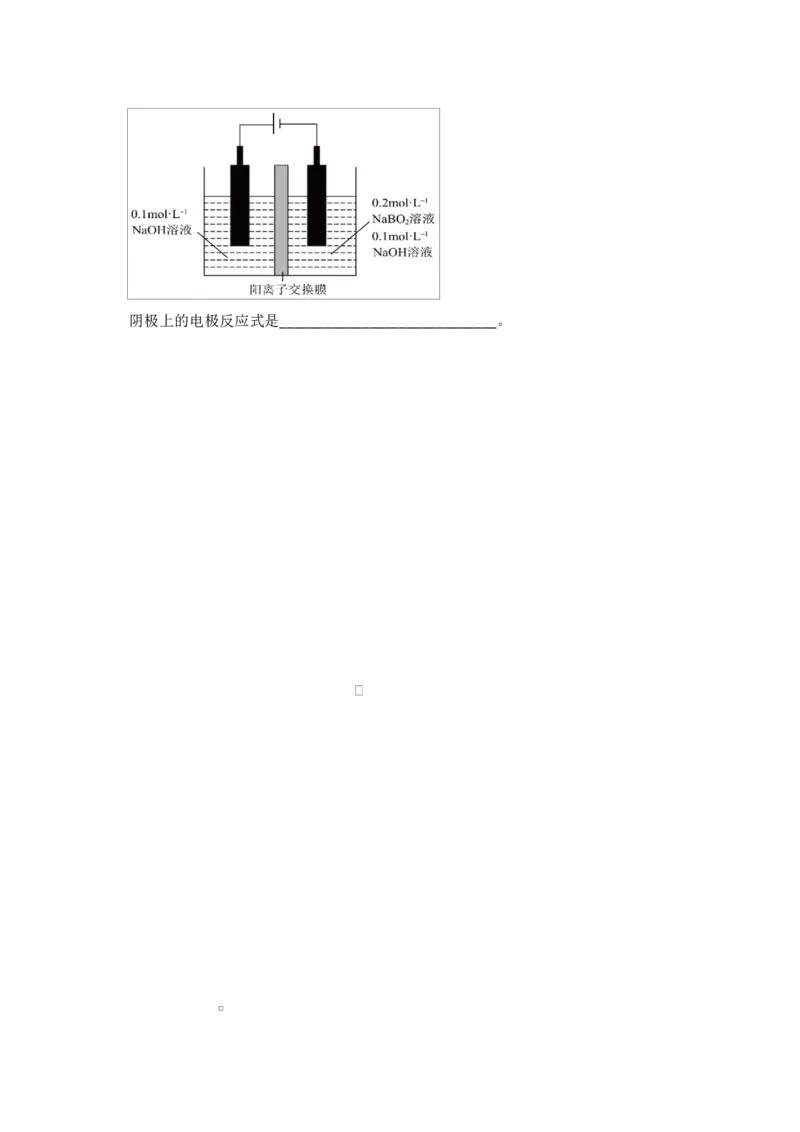
⑤NaBH 转化为 NaBO 后,电解 NaBO 溶液又可制得 NaBH ,实现物质的循环利
4 2 2 4
用,电解装置如图所示。阴极上的电极反应式是_____________________________。