文档内容
专题40 化学反应与能量变化
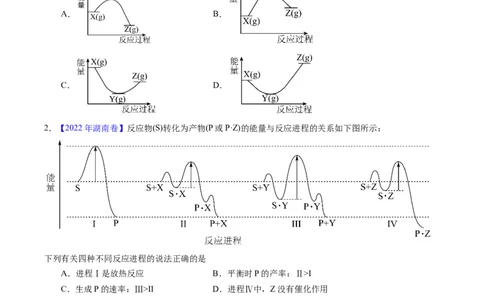
1.【2022年上海卷】反应 , ,已知 ,下列图象正确的是
A. B.
C. D.
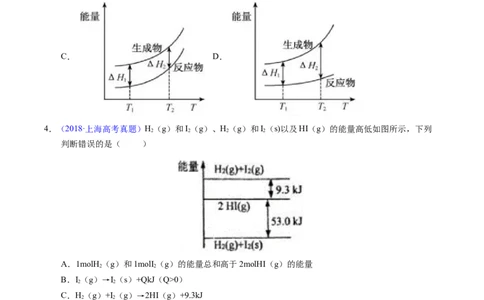
2.【2022年湖南卷】反应物(S)转化为产物(P或P·Z)的能量与反应进程的关系如下图所示:
下列有关四种不同反应进程的说法正确的是
A.进程Ⅰ是放热反应 B.平衡时P的产率:Ⅱ>Ⅰ
C.生成P的速率:Ⅲ>Ⅱ D.进程Ⅳ中,Z没有催化作用
3.(2021.1·浙江真题)在298.15 K、100 kPa条件下,N(g) +3H (g)=2NH (g) ΔH=-92.4 kJ·mol-1,N (g)
2 2 3 2
、H(g)和NH (g)的比热容分别为29.1、28.9和35.6J·K-1·mol-1。一定压强下,1 mol反应中,反应物
2 3
[N (g) +3H (g)]、生成物[2NH (g)]的能量随温度T的变化示意图合理的是
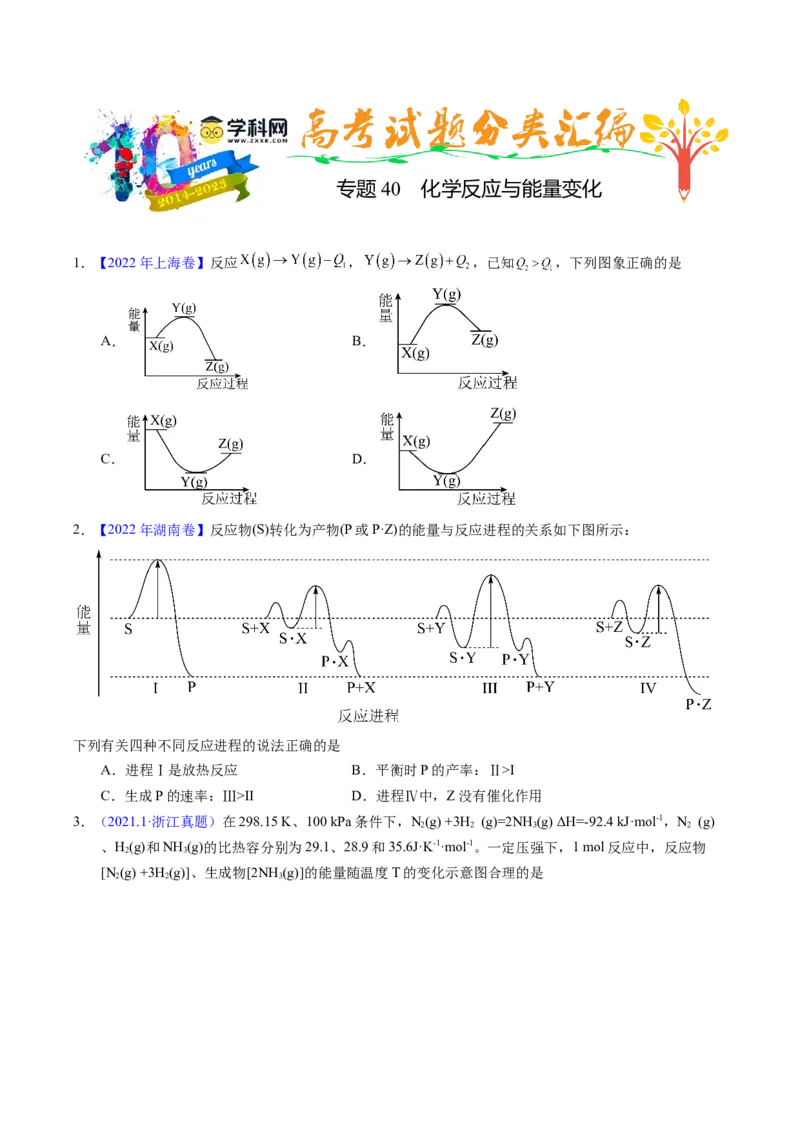
2 2 3A. B.
C. D.
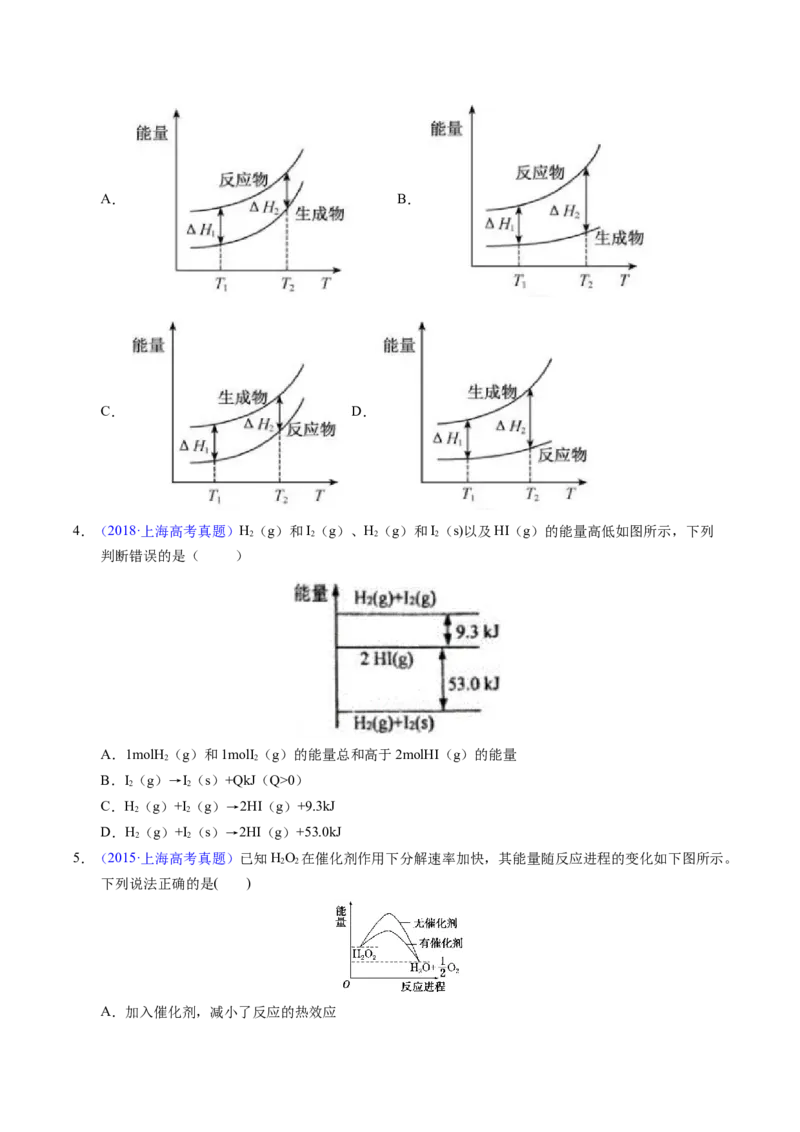
4.(2018·上海高考真题)H(g)和I(g)、H(g)和I(s)以及HI(g)的能量高低如图所示,下列
2 2 2 2
判断错误的是( )
A.1molH (g)和1molI (g)的能量总和高于2molHI(g)的能量
2 2
B.I(g)→I(s)+QkJ(Q>0)
2 2
C.H(g)+I (g)→2HI(g)+9.3kJ
2 2
D.H(g)+I (s)→2HI(g)+53.0kJ
2 2
5.(2015·上海高考真题)已知HO 在催化剂作用下分解速率加快,其能量随反应进程的变化如下图所示。
2 2
下列说法正确的是( )
A.加入催化剂,减小了反应的热效应B.加入催化剂,可提高HO 的平衡转化率
2 2
C.HO 分解的热化学方程式:HO===HO+1/2 O ΔH>0
2 2 2 2 2 2
D.反应物的总能量高于生成物的总能量
6.(2013·北京高考真题)下列设备工作时,将化学能转化为热能的是( )
A. 硅太阳能电池 B. 锂离子电池
C. 太阳能集热器 D. 燃气灶
7.(2018·上海高考真题)下列物质溶于水,溶液温度降低的是( )
A.浓硫酸 B.NaOH C.NaCl D.NH Cl
4
8.(2011·上海高考真题)根据碘与氢气反应的热化学方程式:
①I(g)+H(g) 2HI(g) △H=-9.48 k.J·mol-1
2 2
②I(s)+H((g) 2HI(g)△H=+26.48k.J·mol-1
2 2
下列判断正确的是
A.254gI(g)中通入2gH(g),反应放热9.48kJ
2
B.1mol固态碘与1mol气态碘所含的能量相差17.00kJ
C.反应②的反应物总能量比反应①的反应物总能量低
D.反应①的生成物比反应②的生成物稳定
9.(2017·浙江高考真题)下列物质放入水中,会显著放热的是
A.食盐 B.蔗糖 C.酒精 D.生石灰
10.(2016·浙江高考真题)下列说法正确的是
A.煤是无机化合物,天然气和石油是有机化合物
B.利用化石燃料燃烧放出的热量使水分解产生氢气,是氢能开发的研究方向
C.化学电源放电、植物光合作用都能发生化学变化,并伴随能量的转化
D.若化学过程中断开化学键放出的能量大于形成化学键所吸收的能量,则反应放热
11.(2016·浙江高考真题)2A(g) B(g) ΔH (ΔH <0); 2A(g) B(l) ΔH ;下列能量变化示
1 1 2
意图正确的是A. B.
C. D.
12.(2009·上海高考真题)右图是一个一次性加热杯的示意图。当水袋破裂时,水与固体碎块混和,杯内
食物温度逐渐上升。制造此加热杯可选用的固体碎块是
A.硝酸铵 B.生石灰
C.氯化镁 D.食盐
13.(2008·四川高考真题)下列关于热化学反应的描述中正确的是
A.HCl和NaOH反应的中和热ΔH=-57.3kJ/mol,则HSO 和Ca(OH) 反应的中和热ΔH=2×(-
2 4 2
57.3)kJ/mol
B.CO(g)的燃烧热是283.0kJ/mol,则2CO(g) =2CO(g)+O(g)反应的ΔH=+2×283.0kJ/mol
2 2
C.需要加热才能发生的反应一定是吸热反应
D.1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
14.(2014·上海高考真题)1,3-丁二烯和2-丁炔分别与氢气反应的热化学方程式如下:
CH=CH-CH=CH(g)+2H(g)→CH CHCHCH(g) ∆H=-236.6kJ/mol
2 2 2 3 2 2 3
CH-C≡C-CH(g)+2H(g)→CH CHCHCH(g) ∆H=-272.7kJ/mol
3 3 2 3 2 2 3
由此不能判断
A.1,3-丁二烯和2-丁炔稳定性的相对大小
B.1,3-丁二烯和2-丁炔分子储存能量的相对高低
C.1,3-丁二烯和2-丁炔相互转化的热效应
D.一个碳碳叁键的键能与两个碳碳双键的键能之和的大小
15.(2020·浙江高考真题)在一定温度下,某反应达到了化学平衡,其反应过程对应的能量变化如图。下
列说法正确的是A.E 为逆反应活化能,E为正反应活化能
a
B.该反应为放热反应,ΔH=E’-E
a a
C.所有活化分子的平均能量高于或等于所有分子的平均能量
D.温度升高,逆反应速率加快幅度大于正反应加快幅度,使平衡逆移
16.(2007·上海高考真题)已知正丁烷、异丁烷燃烧的热化学方程式分别为:CHCHCHCH(g)
3 2 2 3
+6.5O (g)→4CO (g)+5HO(l) △H=-2878kJ ·mol-1
2 2 2
(CH)CHCH (g)+6.5O (g) →4CO (g)+5HO(l) △H=-2869kJ· mol-1,下列说法正确的是
3 2 3 2 2 2
A.正丁烷分子储存的能量大于异丁烷分子
B.正丁烷的稳定性大于异丁烷
C.异丁烷转化为正丁烷的过程是一个放热过程
D.异丁烷分子中的碳氢键比正丁烷的多
17.(2008·上海高考真题)已知:H(g)+F(g) 2HF(g)+270kJ,下列说法正确的是( )
2 2
A.2L氟化氢气体分解成1L的氢气和1L的氟气吸收270kJ热量
B.1mol氢气与1mol氟气反应生成2mol液态氟化氢放出的热量小于270kJ
C.在相同条件下,1mol氢气与1mol氟气的能量总和大于2mol氟化氢气体的能量
D.1个氢气分子与1个氟气分子反应生成2个氟化氢分子放出270kJ
18.(2013·上海高考真题)将盛有NH HCO 粉末的小烧杯放入盛有少量醋酸的大烧杯中。然后向小烧杯
4 3
中加入盐酸,反应剧烈,醋酸逐渐凝固。由此可见
A.NH HCO 和盐酸的反应是放热反应
4 3
B.该反应中,热能转化为产物内部的能量
C.反应物的总能量高于生成物的总能量
D.反应的热化学方程式为:NH HCO +HCl→NHCl+CO ↑+H O-Q
4 3 4 2 2
19.(2009·天津高考真题)已知:2CO(g)+O(g)=2CO (g) ΔH=--566 kJ/mol
2 2
NaO(s)+CO(g)=Na CO(s)+ 1/2O (g)ΔH= --226 kJ/mol
2 2 2 2 3 2
根据以上热化学方程式判断,下列说法正确的是( )
A.CO的燃烧热为283 kJ
B.上图可表示由CO生成CO 的反应过程和能量关系
2C.2NaO(s)+2CO(s)=2Na CO(s)+O(g)ΔH< --452 kJ/mol
2 2 2 2 3 2
D.CO(g)与NaO(s)反应放出509 kJ热量时,电子转移数为2×6.02×1023
2 2
20.(2012·上海高考真题)工业生产水煤气的反应为:C(s)+HO(g)→CO(g)+H (g)-131.4 kJ。下列判断正
2 2
确的是
A.反应物能量总和大于生成物能量总和
B.CO(g)+H(g)→C(s)+H O(g)+131.4kJ
2 2
C.水煤气反应中生成1 mol H (g)吸收131.4 KJ热量
2
D.水煤气反应中生成1体积CO(g)吸收131.4 KJ热量
21.(2016·海南高考真题)由反应物X转化为Y和Z的能量变化如图所示。下列说法正确的是
A.由 反应的ΔH=E −E
5 2
B.由 反应的ΔH<0
C.降低压强有利于提高Y的产率
D.升高温度有利于提高Z的产率
22.(2009·上海高考真题)下列对化学反应的认识错误的是 ( )
A.会引起化学键的变化 B.会产生新的物质
C.必然引起物质状态的变化 D.必然伴随着能量的变化
23.(2011·上海高考真题)据报道,科学家开发出了利用太阳能分解水的新型催化剂。下列有关水分解过
程的能量变化示意图正确的是
A. B.
C. D.