文档内容
专题60 酸碱中和滴定及曲线
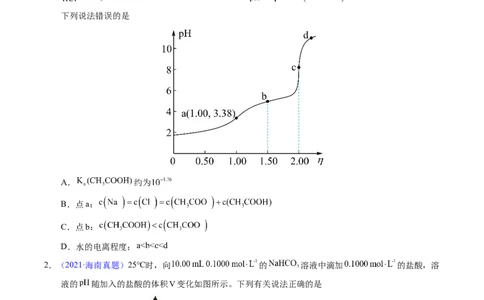
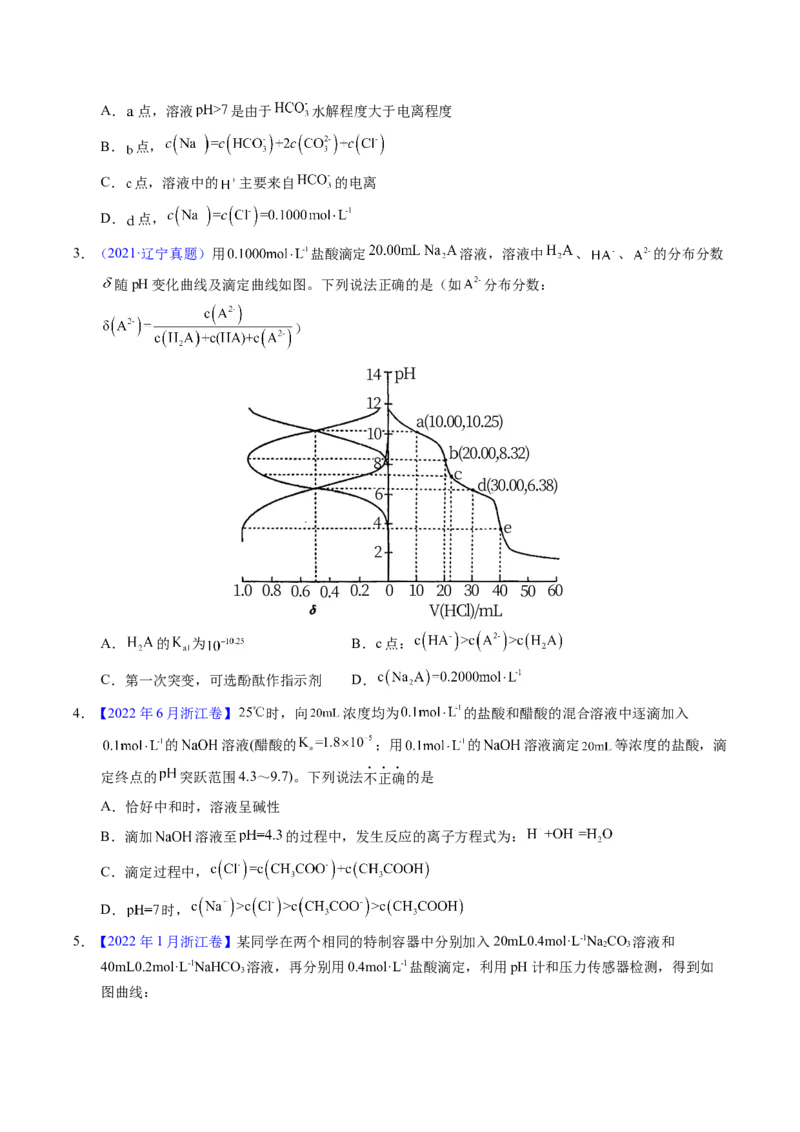
1.【2023年湖北卷】常温下,用浓度为 的 标准溶液滴定浓度均为 的
和 的混合溶液,滴定过程中溶液的 随 ( )的变化曲线如图所示。
下列说法错误的是
A. 约为
B.点a:
C.点b:
D.水的电离程度:
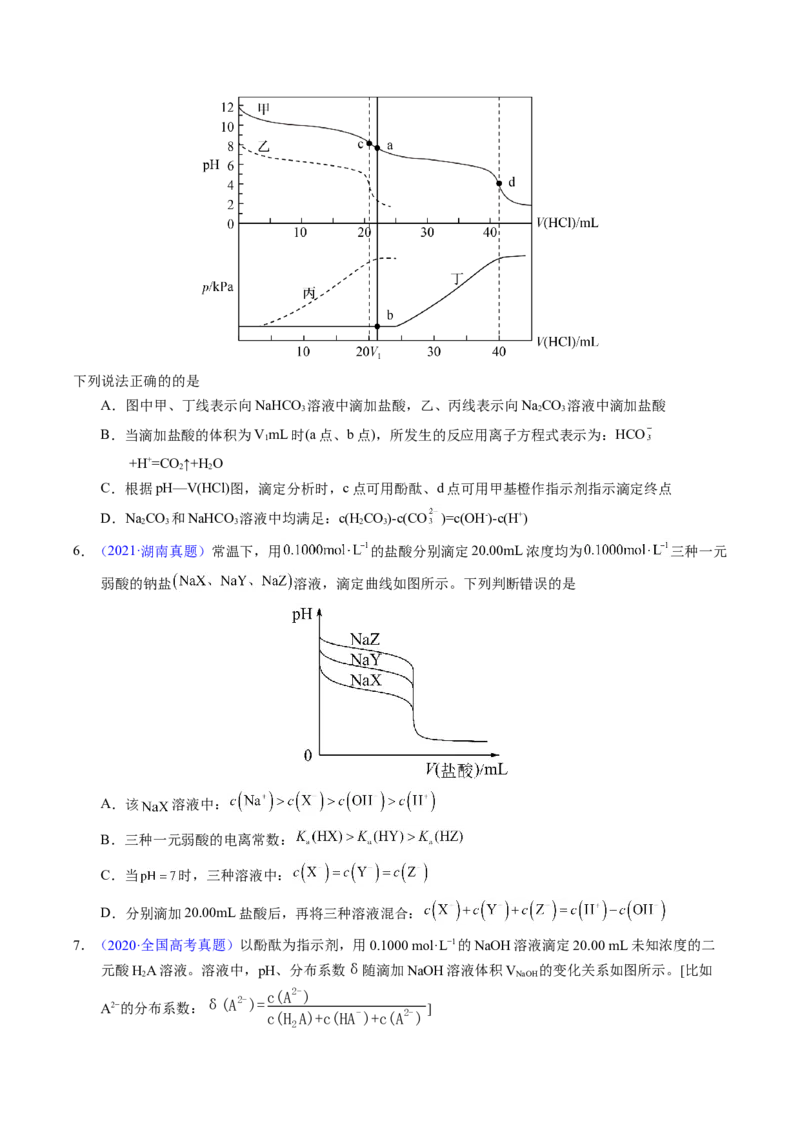
2.(2021·海南真题)25℃时,向 的 溶液中滴加 的盐酸,溶
液的 随加入的盐酸的体积 变化如图所示。下列有关说法正确的是A. 点,溶液 是由于 水解程度大于电离程度
B. 点,
C. 点,溶液中的 主要来自 的电离
D. 点,
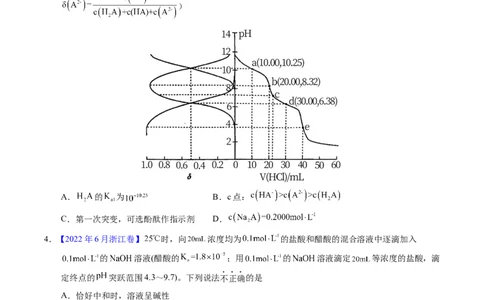
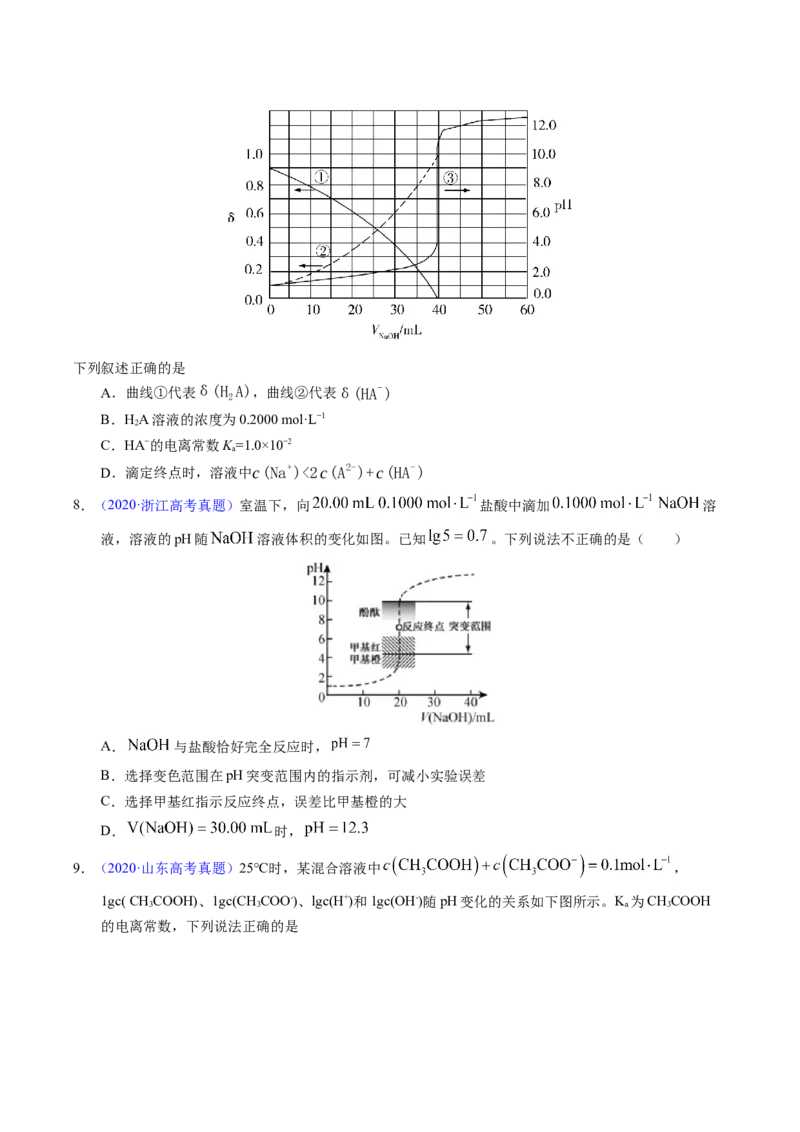
3.(2021·辽宁真题)用 盐酸滴定 溶液,溶液中 、 、 的分布分数
随pH变化曲线及滴定曲线如图。下列说法正确的是(如 分布分数:
)
A. 的 为 B.c点:
C.第一次突变,可选酚酞作指示剂 D.
4.【2022年6月浙江卷】 时,向 浓度均为 的盐酸和醋酸的混合溶液中逐滴加入
的 溶液(醋酸的 ;用 的 溶液滴定 等浓度的盐酸,滴
定终点的 突跃范围4.3~9.7)。下列说法不正确的是
A.恰好中和时,溶液呈碱性
B.滴加 溶液至 的过程中,发生反应的离子方程式为:
C.滴定过程中,
D. 时,
5.【2022年1月浙江卷】某同学在两个相同的特制容器中分别加入20mL0.4mol·L-1NaCO 溶液和
2 3
40mL0.2mol·L-1NaHCO 溶液,再分别用0.4mol·L-1盐酸滴定,利用pH计和压力传感器检测,得到如
3
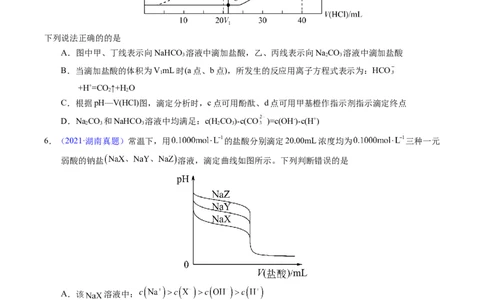
图曲线:下列说法正确的的是
A.图中甲、丁线表示向NaHCO 溶液中滴加盐酸,乙、丙线表示向NaCO 溶液中滴加盐酸
3 2 3
B.当滴加盐酸的体积为VmL时(a点、b点),所发生的反应用离子方程式表示为:HCO
1
+H+=CO ↑+H O
2 2
C.根据pH—V(HCl)图,滴定分析时,c点可用酚酞、d点可用甲基橙作指示剂指示滴定终点
D.NaCO 和NaHCO 溶液中均满足:c(HCO)-c(CO )=c(OH-)-c(H+)
2 3 3 2 3
6.(2021·湖南真题)常温下,用 的盐酸分别滴定20.00mL浓度均为 三种一元
弱酸的钠盐 溶液,滴定曲线如图所示。下列判断错误的是
A.该 溶液中:
B.三种一元弱酸的电离常数:
C.当 时,三种溶液中:
D.分别滴加20.00mL盐酸后,再将三种溶液混合:
7.(2020·全国高考真题)以酚酞为指示剂,用0.1000 mol·L−1的NaOH溶液滴定20.00 mL未知浓度的二
元酸HA溶液。溶液中,pH、分布系数δ随滴加NaOH溶液体积V 的变化关系如图所示。[比如
2 NaOH
c(A2-)
A2−的分布系数:δ(A2-)=
]
c(H A)+c(HA-)+c(A2-)
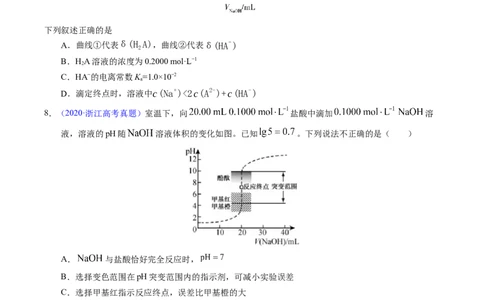
2下列叙述正确的是
A.曲线①代表δ(H A),曲线②代表δ(HA-)
2
B.HA溶液的浓度为0.2000 mol·L−1
2
C.HA−的电离常数K=1.0×10−2
a
D.滴定终点时,溶液中c(Na+)<2c(A2-)+c(HA-)
8.(2020·浙江高考真题)室温下,向 盐酸中滴加 溶
液,溶液的pH随 溶液体积的变化如图。已知 。下列说法不正确的是( )
A. 与盐酸恰好完全反应时,
B.选择变色范围在pH突变范围内的指示剂,可减小实验误差
C.选择甲基红指示反应终点,误差比甲基橙的大
D. 时,
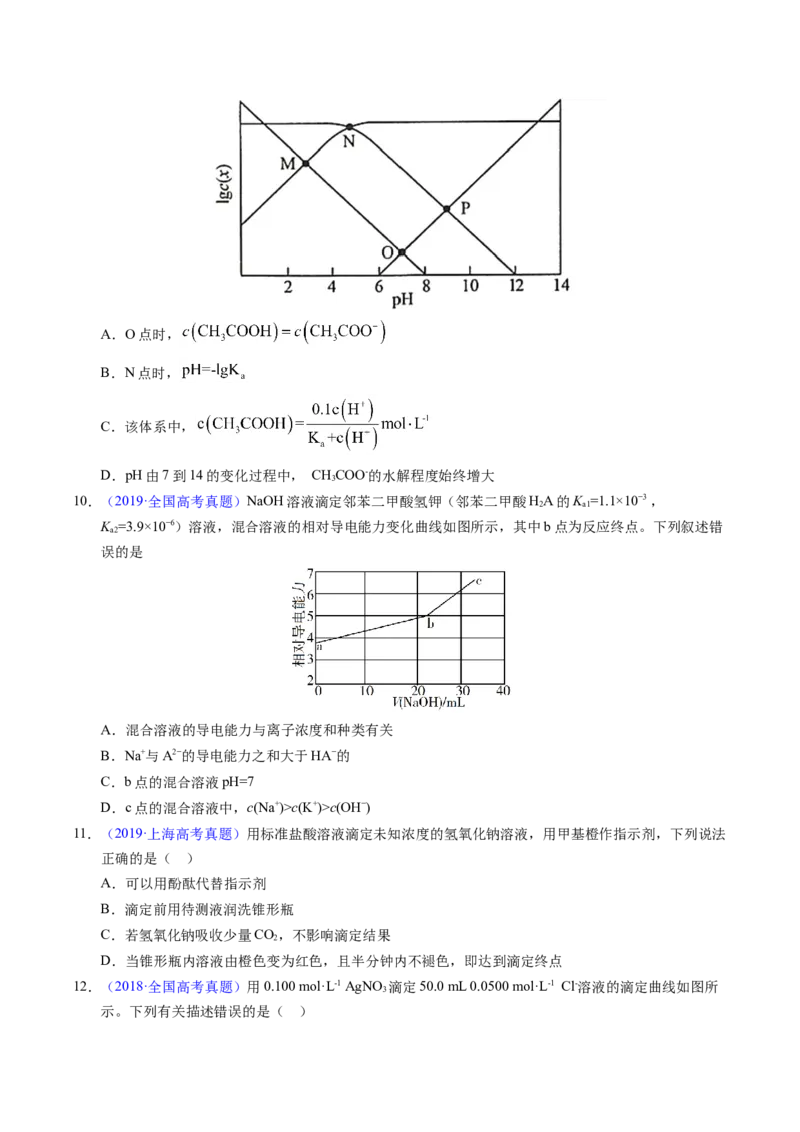
9.(2020·山东高考真题)25℃时,某混合溶液中 ,
1gc( CH COOH)、1gc(CHCOO-)、lgc(H+)和1gc(OH-)随pH变化的关系如下图所示。K 为CHCOOH
3 3 a 3
的电离常数,下列说法正确的是A.O点时,
B.N点时,
C.该体系中,
D.pH由7到14的变化过程中, CHCOO-的水解程度始终增大
3
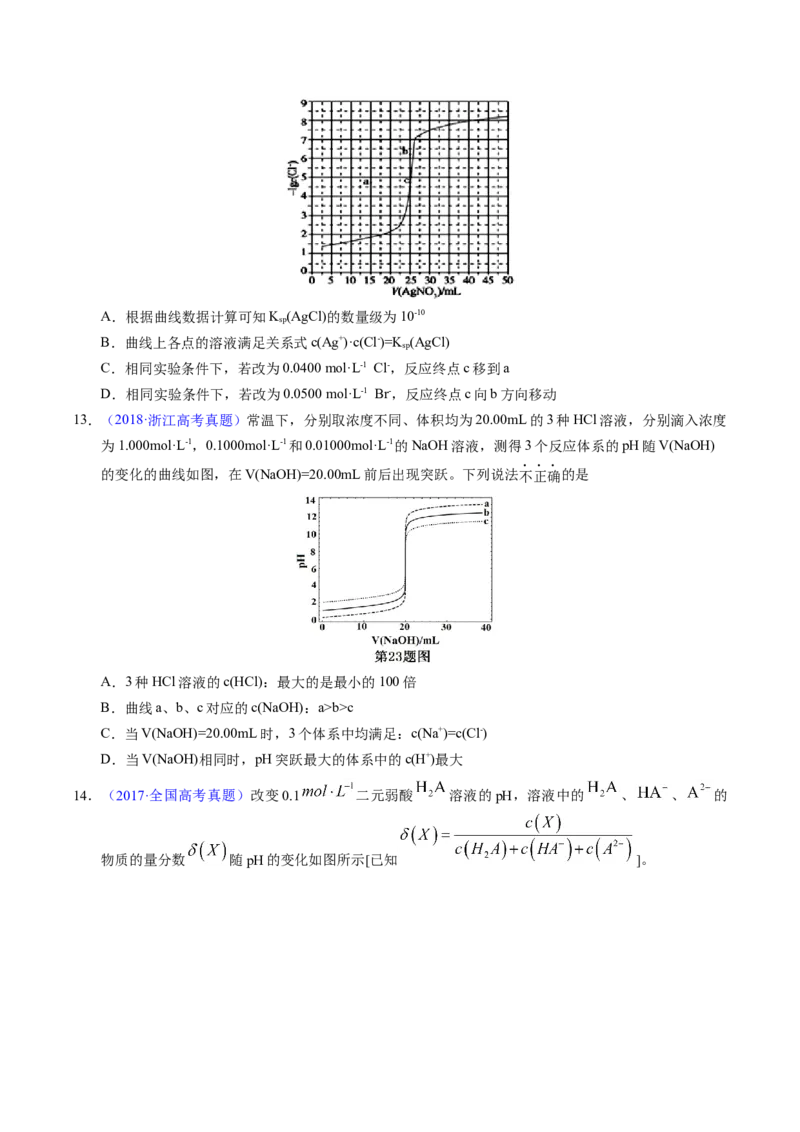
10.(2019·全国高考真题)NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸HA的K =1.1×10−3 ,
2 a1
K =3.9×10−6)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。下列叙述错
a2
误的是
A.混合溶液的导电能力与离子浓度和种类有关
B.Na+与A2−的导电能力之和大于HA−的
C.b点的混合溶液pH=7
D.c点的混合溶液中,c(Na+)>c(K+)>c(OH−)
11.(2019·上海高考真题)用标准盐酸溶液滴定未知浓度的氢氧化钠溶液,用甲基橙作指示剂,下列说法
正确的是( )
A.可以用酚酞代替指示剂
B.滴定前用待测液润洗锥形瓶
C.若氢氧化钠吸收少量CO,不影响滴定结果
2
D.当锥形瓶内溶液由橙色变为红色,且半分钟内不褪色,即达到滴定终点
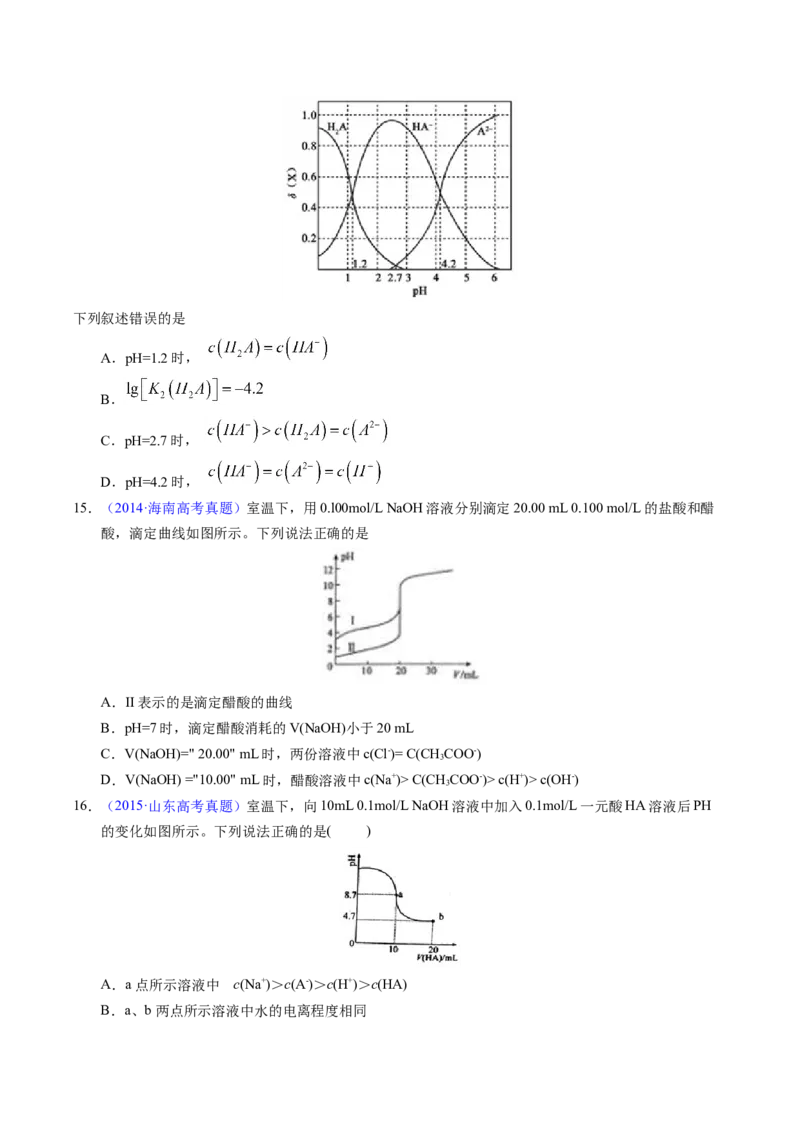
12.(2018·全国高考真题)用0.100 mol·L-1 AgNO 滴定50.0 mL 0.0500 mol·L-1 Cl-溶液的滴定曲线如图所
3
示。下列有关描述错误的是( )A.根据曲线数据计算可知K (AgCl)的数量级为10-10
sp
B.曲线上各点的溶液满足关系式c(Ag+)·c(Cl-)=K (AgCl)
sp
C.相同实验条件下,若改为0.0400 mol·L-1 Cl-,反应终点c移到a
D.相同实验条件下,若改为0.0500 mol·L-1 Br-,反应终点c向b方向移动
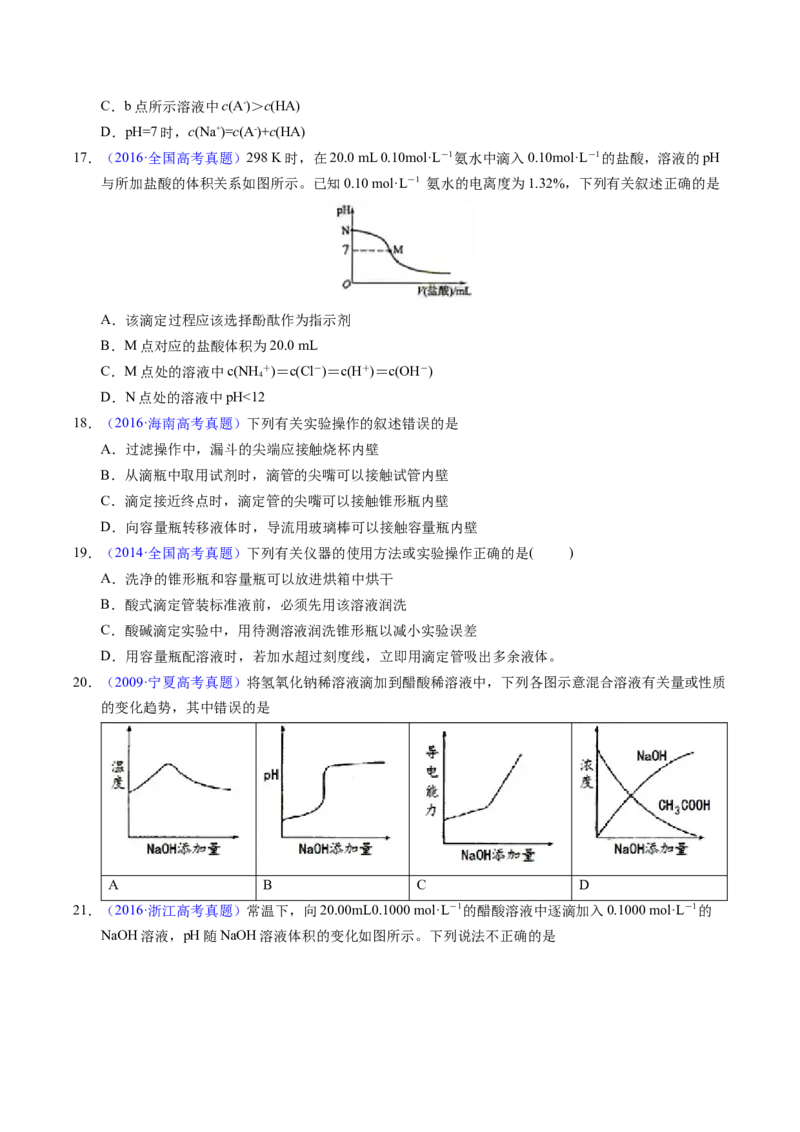
13.(2018·浙江高考真题)常温下,分别取浓度不同、体积均为20.00mL的3种HCl溶液,分别滴入浓度
为1.000mol·L-1,0.1000mol·L-1和0.01000mol·L-1的NaOH溶液,测得3个反应体系的pH随V(NaOH)
的变化的曲线如图,在V(NaOH)=20.00mL前后出现突跃。下列说法不正确的是
A.3种HCl溶液的c(HCl):最大的是最小的100倍
B.曲线a、b、c对应的c(NaOH):a>b>c
C.当V(NaOH)=20.00mL时,3个体系中均满足:c(Na+)=c(Cl-)
D.当V(NaOH)相同时,pH突跃最大的体系中的c(H+)最大
14.(2017·全国高考真题)改变0.1 二元弱酸 溶液的pH,溶液中的 、 、 的
物质的量分数 随pH的变化如图所示[已知 ]。下列叙述错误的是
A.pH=1.2时,
B.
C.pH=2.7时,
D.pH=4.2时,
15.(2014·海南高考真题)室温下,用0.l00mol/L NaOH溶液分别滴定20.00 mL 0.100 mol/L的盐酸和醋
酸,滴定曲线如图所示。下列说法正确的是
A.II表示的是滴定醋酸的曲线
B.pH=7时,滴定醋酸消耗的V(NaOH)小于20 mL
C.V(NaOH)=" 20.00" mL时,两份溶液中c(Cl-)= C(CH COO-)
3
D.V(NaOH) ="10.00" mL时,醋酸溶液中c(Na+)> C(CH COO-)> c(H+)> c(OH-)
3
16.(2015·山东高考真题)室温下,向10mL 0.1mol/L NaOH溶液中加入0.1mol/L一元酸HA溶液后PH
的变化如图所示。下列说法正确的是( )
A.a 点所示溶液中 c(Na+)>c(A-)>c(H+)>c(HA)
B.a、b 两点所示溶液中水的电离程度相同C.b点所示溶液中c(A-)>c(HA)
D.pH=7时,c(Na+)=c(A-)+c(HA)
17.(2016·全国高考真题)298 K时,在20.0 mL 0.10mol·L-1氨水中滴入0.10mol·L-1的盐酸,溶液的pH
与所加盐酸的体积关系如图所示。已知0.10 mol·L-1 氨水的电离度为1.32%,下列有关叙述正确的是
A.该滴定过程应该选择酚酞作为指示剂
B.M点对应的盐酸体积为20.0 mL
C.M点处的溶液中c(NH +)=c(Cl-)=c(H+)=c(OH-)
4
D.N点处的溶液中pH<12
18.(2016·海南高考真题)下列有关实验操作的叙述错误的是
A.过滤操作中,漏斗的尖端应接触烧杯内壁
B.从滴瓶中取用试剂时,滴管的尖嘴可以接触试管内壁
C.滴定接近终点时,滴定管的尖嘴可以接触锥形瓶内壁
D.向容量瓶转移液体时,导流用玻璃棒可以接触容量瓶内壁
19.(2014·全国高考真题)下列有关仪器的使用方法或实验操作正确的是( )
A.洗净的锥形瓶和容量瓶可以放进烘箱中烘干
B.酸式滴定管装标准液前,必须先用该溶液润洗
C.酸碱滴定实验中,用待测溶液润洗锥形瓶以减小实验误差
D.用容量瓶配溶液时,若加水超过刻度线,立即用滴定管吸出多余液体。
20.(2009·宁夏高考真题)将氢氧化钠稀溶液滴加到醋酸稀溶液中,下列各图示意混合溶液有关量或性质
的变化趋势,其中错误的是
A B C D
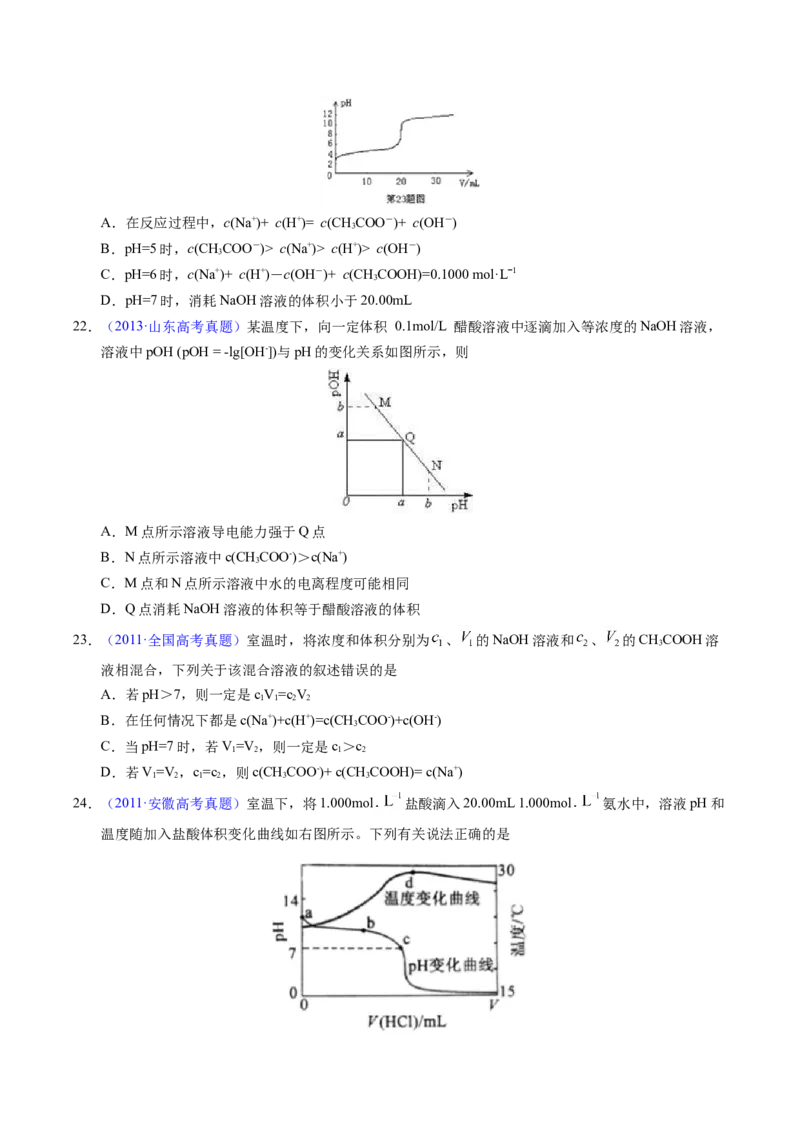
21.(2016·浙江高考真题)常温下,向20.00mL0.1000 mol·L-1的醋酸溶液中逐滴加入0.1000 mol·L-1的
NaOH溶液,pH随NaOH溶液体积的变化如图所示。下列说法不正确的是A.在反应过程中,c(Na+)+ c(H+)= c(CHCOO-)+ c(OH-)
3
B.pH=5时,c(CHCOO-)> c(Na+)> c(H+)> c(OH-)
3
C.pH=6时,c(Na+)+ c(H+)-c(OH-)+ c(CHCOOH)=0.1000 mol·Lˉ1
3
D.pH=7时,消耗NaOH溶液的体积小于20.00mL
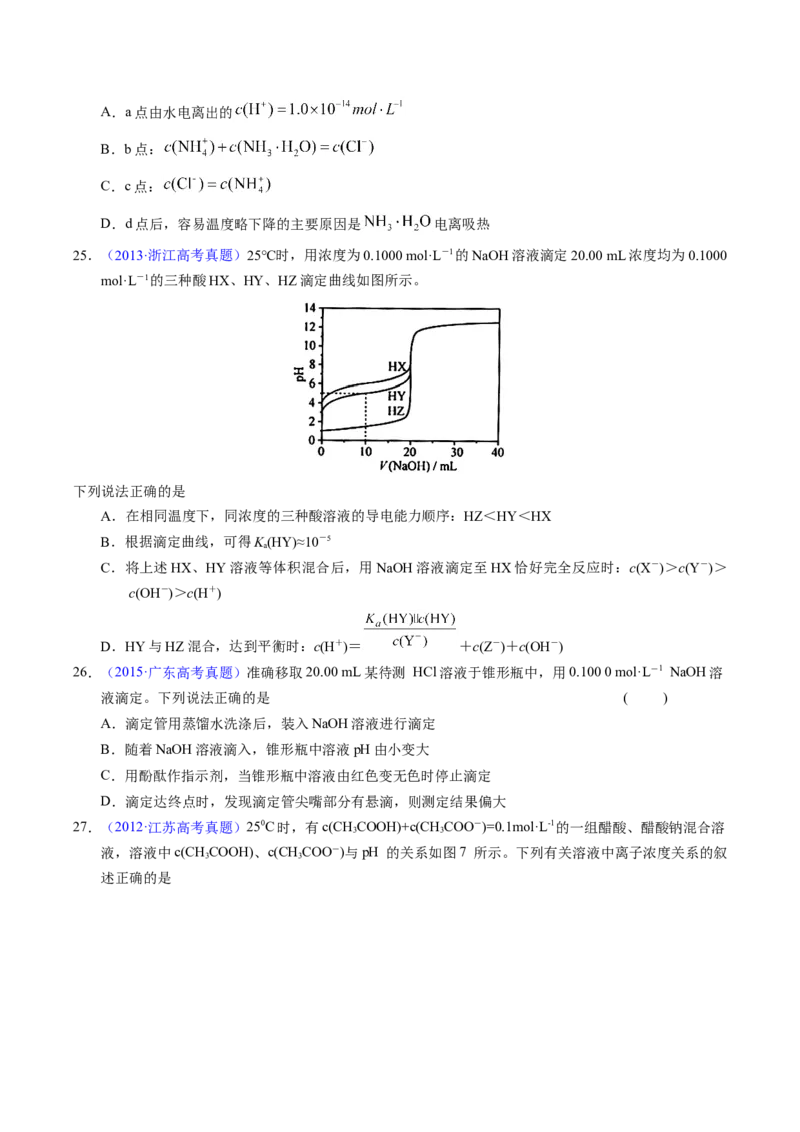
22.(2013·山东高考真题)某温度下,向一定体积 0.1mol/L 醋酸溶液中逐滴加入等浓度的NaOH溶液,
溶液中pOH (pOH = -lg[OH-])与pH的变化关系如图所示,则
A.M点所示溶液导电能力强于Q点
B.N点所示溶液中c(CHCOO-)>c(Na+)
3
C.M点和N点所示溶液中水的电离程度可能相同
D.Q点消耗NaOH溶液的体积等于醋酸溶液的体积
23.(2011·全国高考真题)室温时,将浓度和体积分别为 、 的NaOH溶液和 、 的CHCOOH溶
3
液相混合,下列关于该混合溶液的叙述错误的是
A.若pH>7,则一定是cV=cV
1 1 2 2
B.在任何情况下都是c(Na+)+c(H+)=c(CH COO-)+c(OH-)
3
C.当pH=7时,若V=V ,则一定是c>c
1 2 1 2
D.若V=V ,c=c,则c(CHCOO-)+ c(CHCOOH)= c(Na+)
1 2 1 2 3 3
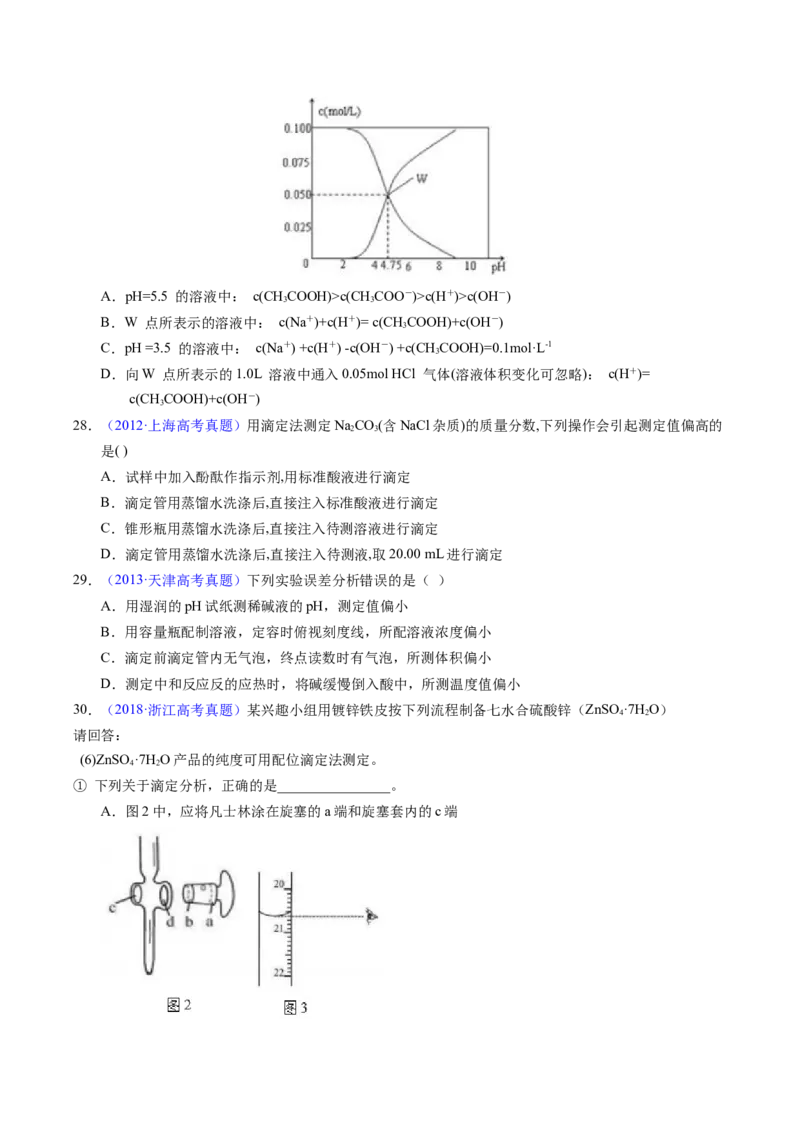
24.(2011·安徽高考真题)室温下,将1.000mol 盐酸滴入20.00mL 1.000mol 氨水中,溶液pH和
温度随加入盐酸体积变化曲线如右图所示。下列有关说法正确的是A.a点由水电离出的
B.b点:
C.c点:
D.d点后,容易温度略下降的主要原因是 电离吸热
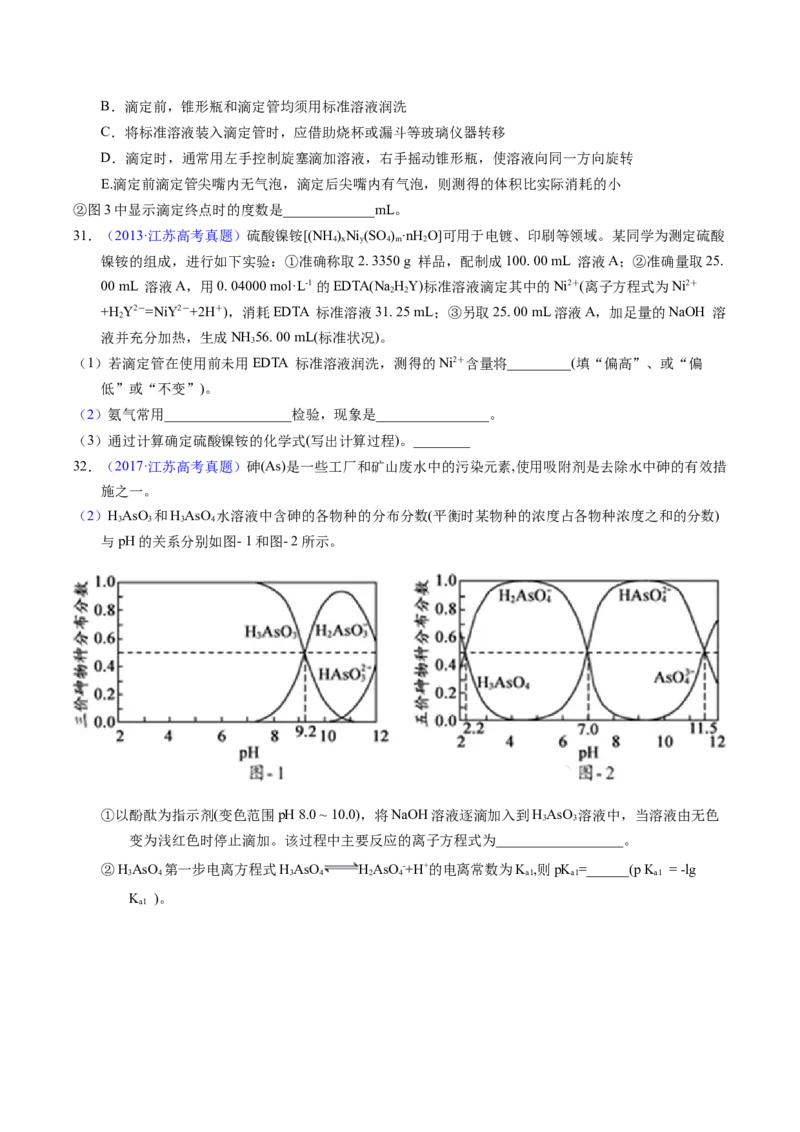
25.(2013·浙江高考真题)25℃时,用浓度为0.1000 mol·L-1的NaOH溶液滴定20.00 mL浓度均为0.1000
mol·L-1的三种酸HX、HY、HZ滴定曲线如图所示。
下列说法正确的是
A.在相同温度下,同浓度的三种酸溶液的导电能力顺序:HZ<HY<HX
B.根据滴定曲线,可得K(HY)≈10-5
a
C.将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时:c(X-)>c(Y-)>
c(OH-)>c(H+)
D.HY与HZ混合,达到平衡时:c(H+)= +c(Z-)+c(OH-)
26.(2015·广东高考真题)准确移取20.00 mL某待测 HCl溶液于锥形瓶中,用0.100 0 mol·L-1 NaOH溶
液滴定。下列说法正确的是 ( )
A.滴定管用蒸馏水洗涤后,装入NaOH溶液进行滴定
B.随着NaOH溶液滴入,锥形瓶中溶液pH由小变大
C.用酚酞作指示剂,当锥形瓶中溶液由红色变无色时停止滴定
D.滴定达终点时,发现滴定管尖嘴部分有悬滴,则测定结果偏大
27.(2012·江苏高考真题)250C时,有c(CHCOOH)+c(CH COO-)=0.1mol·L-1的一组醋酸、醋酸钠混合溶
3 3
液,溶液中c(CHCOOH)、c(CHCOO-)与pH 的关系如图7 所示。下列有关溶液中离子浓度关系的叙
3 3
述正确的是A.pH=5.5 的溶液中: c(CHCOOH)>c(CH COO-)>c(H+)>c(OH-)
3 3
B.W 点所表示的溶液中: c(Na+)+c(H+)= c(CHCOOH)+c(OH-)
3
C.pH =3.5 的溶液中: c(Na+) +c(H+) -c(OH-) +c(CHCOOH)=0.1mol·L-1
3
D.向W 点所表示的1.0L 溶液中通入0.05mol HCl 气体(溶液体积变化可忽略): c(H+)=
c(CHCOOH)+c(OH-)
3
28.(2012·上海高考真题)用滴定法测定NaCO(含NaCl杂质)的质量分数,下列操作会引起测定值偏高的
2 3
是( )
A.试样中加入酚酞作指示剂,用标准酸液进行滴定
B.滴定管用蒸馏水洗涤后,直接注入标准酸液进行滴定
C.锥形瓶用蒸馏水洗涤后,直接注入待测溶液进行滴定
D.滴定管用蒸馏水洗涤后,直接注入待测液,取20.00 mL进行滴定
29.(2013·天津高考真题)下列实验误差分析错误的是( )
A.用湿润的pH试纸测稀碱液的pH,测定值偏小
B.用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小
C.滴定前滴定管内无气泡,终点读数时有气泡,所测体积偏小
D.测定中和反应反的应热时,将碱缓慢倒入酸中,所测温度值偏小
30.(2018·浙江高考真题)某兴趣小组用镀锌铁皮按下列流程制备七水合硫酸锌(ZnSO·7H O)
4 2
请回答:
(6)ZnSO ·7H O产品的纯度可用配位滴定法测定。
4 2
① 下列关于滴定分析,正确的是________________。
A.图2中,应将凡士林涂在旋塞的a端和旋塞套内的c端B.滴定前,锥形瓶和滴定管均须用标准溶液润洗
C.将标准溶液装入滴定管时,应借助烧杯或漏斗等玻璃仪器转移
D.滴定时,通常用左手控制旋塞滴加溶液,右手摇动锥形瓶,使溶液向同一方向旋转
E.滴定前滴定管尖嘴内无气泡,滴定后尖嘴内有气泡,则测得的体积比实际消耗的小
②图3中显示滴定终点时的度数是_____________mL。
31.(2013·江苏高考真题)硫酸镍铵[(NH )Ni (SO ) ·nH O]可用于电镀、印刷等领域。某同学为测定硫酸
4 x y 4 m 2
镍铵的组成,进行如下实验:①准确称取2. 3350 g 样品,配制成100. 00 mL 溶液A;②准确量取25.
00 mL 溶液A,用0. 04000 mol·L-1 的EDTA(Na HY)标准溶液滴定其中的Ni2+(离子方程式为Ni2+
2 2
+H Y2-=NiY2-+2H+),消耗EDTA 标准溶液31. 25 mL;③另取25. 00 mL溶液A,加足量的NaOH 溶
2
液并充分加热,生成NH 56. 00 mL(标准状况)。
3
(1)若滴定管在使用前未用EDTA 标准溶液润洗,测得的Ni2+含量将_________(填“偏高”、或“偏
低”或“不变”)。
(2)氨气常用__________________检验,现象是________________。
(3)通过计算确定硫酸镍铵的化学式(写出计算过程)。________
32.(2017·江苏高考真题)砷(As)是一些工厂和矿山废水中的污染元素,使用吸附剂是去除水中砷的有效措
施之一。
(2)HAsO 和HAsO 水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)
3 3 3 4
与pH的关系分别如图- 1和图- 2所示。
①以酚酞为指示剂(变色范围pH 8.0 ~ 10.0),将NaOH溶液逐滴加入到HAsO 溶液中,当溶液由无色
3 3
变为浅红色时停止滴加。该过程中主要反应的离子方程式为__________________。
②HAsO 第一步电离方程式HAsO HAsO -+H+的电离常数为K ,则pK =______(p K = -lg
3 4 3 4 2 4 a1 a1 a1
K )。
a1