文档内容
2024 年高考山东卷化学试题
一、单选题
1.中国书画是世界艺术瑰宝,古人所用文房四宝制作过程中发生氧化还原反应的是
A.竹管、动物尾毫→湖笔 B.松木→油烟→徽墨
C.楮树皮→纸浆纤维→宣纸 D.端石→端砚
2.化学品在食品工业中也有重要应用,下列说法错误的是
A.活性炭可用作食品脱色剂 B.铁粉可用作食品脱氧剂
C.谷氨酸钠可用作食品增味剂 D.五氧化二磷可用作食品干燥剂
3.下列化学用语或图示正确的是
A. 的系统命名:2-甲基苯酚
B.O 分子的球棍模型:
3
C.激发态H原子的轨道表示式:
D.p-pπ键形成的轨道重叠示意图:
4.下列物质均为共价晶体且成键结构相似,其中熔点最低的是
A.金刚石(C) B.单晶硅(Si) C.金刚砂(SiC) D.氮化硼(BN,立方相)
5.物质性质决定用途,下列两者对应关系错误的是
A.石灰乳除去废气中二氧化硫,体现了Ca(OH) 的碱性
2
B.氯化铁溶液腐蚀铜电路板,体现了Fe3+的氧化性
C.制作豆腐时添加石膏,体现了CaSO 的难溶性
4
D.用氨水配制银氨溶液,体现了NH 的配位性
3
6.下列图示实验中,操作规范的是
A.调控滴定速度 B.用pH试纸测定溶液pH C.加热试管中的液体 D.向试管中滴加溶液
A.A B.B C.C D.D
7.我国科学家在青蒿素研究方面为人类健康作出了巨大贡献。在青蒿素研究实验中,下列叙述错误的是
A.通过萃取法可获得含青蒿素的提取液
B.通过X射线衍射可测定青蒿素晶体结构
C.通过核磁共振谱可推测青蒿素相对分子质量
D.通过红外光谱可推测青蒿素分子中的官能团
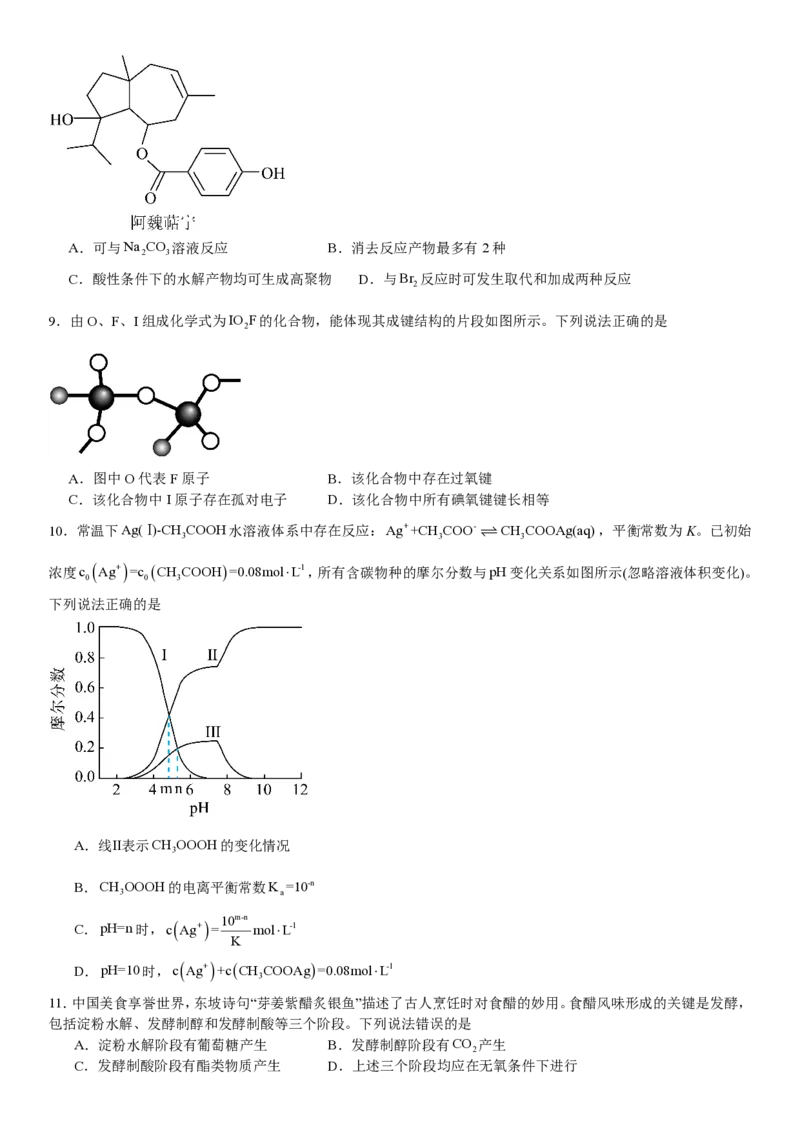
8.植物提取物阿魏萜宁具有抗菌活性,其结构简式如图所示。下列关于阿魏萜宁的说法错误的是A.可与Na CO 溶液反应 B.消去反应产物最多有2种
2 3
C.酸性条件下的水解产物均可生成高聚物 D.与Br 反应时可发生取代和加成两种反应
2
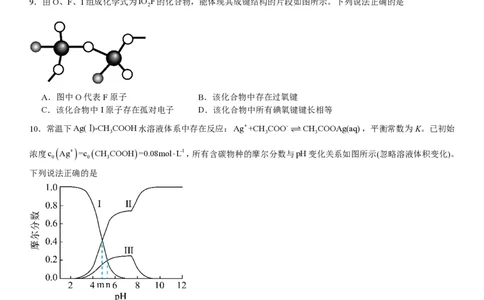
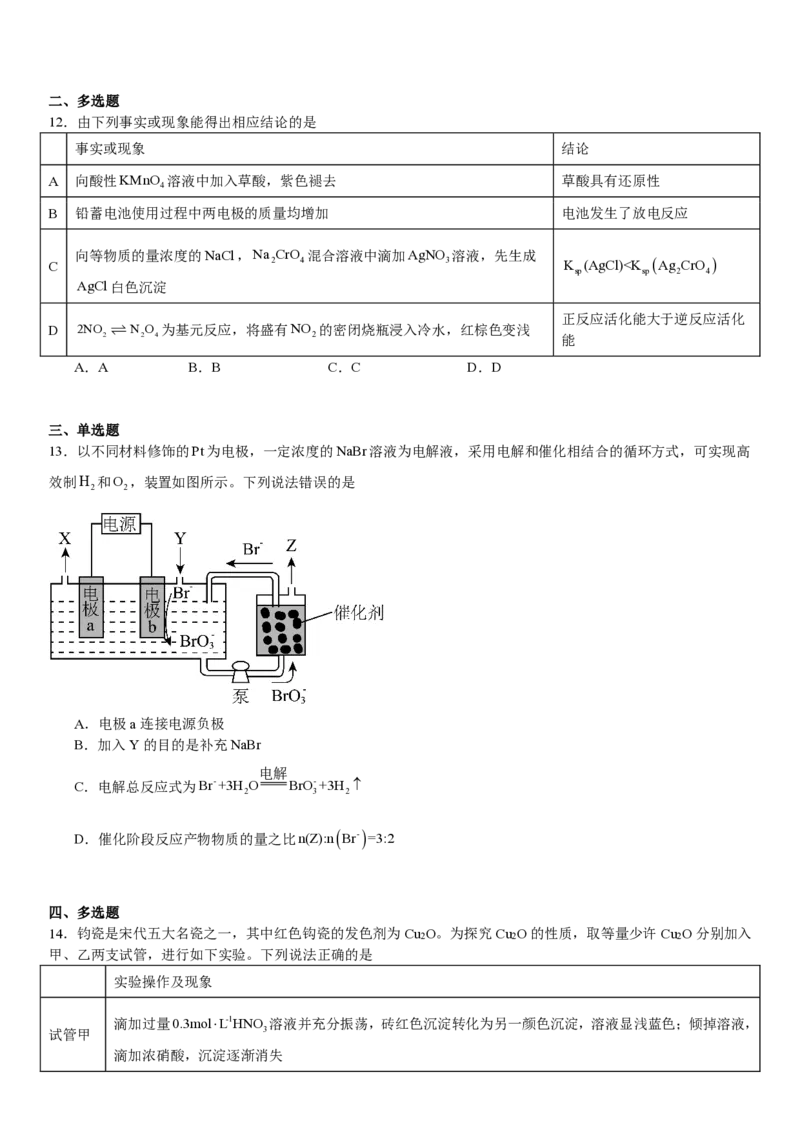
9.由O、F、I组成化学式为IO F的化合物,能体现其成键结构的片段如图所示。下列说法正确的是
2
A.图中O代表F原子 B.该化合物中存在过氧键
C.该化合物中I原子存在孤对电子 D.该化合物中所有碘氧键键长相等
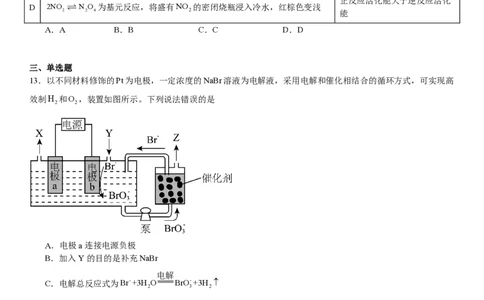
10.常温下Ag(Ⅰ)-CH COOH水溶液体系中存在反应:Ag++CH COO- CH COOAg(aq),平衡常数为K。已初始
3 3 3
浓度c ( Ag+) =c (CH COOH)=0.08mol⋅L-1,所有含碳物种的摩尔分数与pH变化关系如图所示(忽略溶液体积变化)。
0 0 3
下列说法正确的是
A.线Ⅱ表示CH OOOH的变化情况
3
B.CH OOOH的电离平衡常数K =10-n
3 a
C.pH=n时,c ( Ag+) =
10m-n
mol⋅L-1
K
D.pH=10时,c ( Ag+) +c(CH COOAg)=0.08mol⋅L-1
3
11.中国美食享誉世界,东坡诗句“芽姜紫醋炙银鱼”描述了古人烹饪时对食醋的妙用。食醋风味形成的关键是发酵,
包括淀粉水解、发酵制醇和发酵制酸等三个阶段。下列说法错误的是
A.淀粉水解阶段有葡萄糖产生 B.发酵制醇阶段有CO 产生
2
C.发酵制酸阶段有酯类物质产生 D.上述三个阶段均应在无氧条件下进行二、多选题
12.由下列事实或现象能得出相应结论的是
事实或现象 结论
A 向酸性KMnO 溶液中加入草酸,紫色褪去 草酸具有还原性
4
B 铅蓄电池使用过程中两电极的质量均增加 电池发生了放电反应
向等物质的量浓度的NaCl,Na CrO 混合溶液中滴加AgNO 溶液,先生成
C 2 4 3 K (AgCl)0。一定压力下,按CO ,H 物质的量之比
2 2 2 2 2
n(CO ):n(H )=1:1投料,T,T 温度时反应物摩尔分数随时间变化关系如图所示。已知该反应的速率方程为
2 2 1 2
v=kc0.5(H )c(CO ),T,T 温度时反应速率常数k分别为k ,k 。下列说法错误的是
2 2 1 2 1 2
A.k >k
1 2
v(T )
k
B.T,T 温度下达平衡时反应速率的比值: 1 < 1
1 2 v(T ) k
2 2
C.温度不变,仅改变体系初始压力,反应物摩尔分数随时间的变化曲线不变
D.T 温度下,改变初始投料比例,可使平衡时各组分摩尔分数与T温度时相同
2 1
五、解答题
16.锰氧化物具有较大应用价值,回答下列问题:
(1)Mn在元素周期表中位于第 周期 族;同周期中,基态原子未成对电子数比Mn多的元素是 (填
元素符号)。
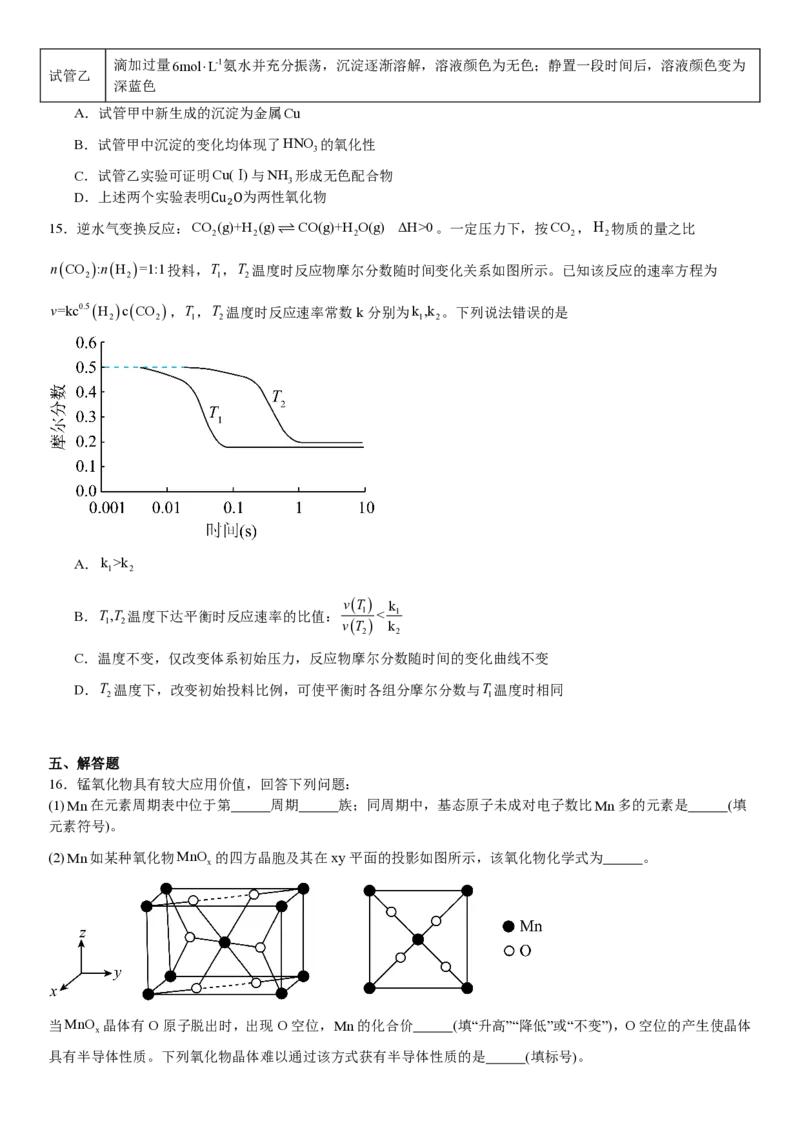
(2)Mn如某种氧化物MnO 的四方晶胞及其在xy平面的投影如图所示,该氧化物化学式为 。
x
当MnO 晶体有O原子脱出时,出现O空位,Mn的化合价 (填“升高”“降低”或“不变”),O空位的产生使晶体
x
具有半导体性质。下列氧化物晶体难以通过该方式获有半导体性质的是 (填标号)。A. B. C. D.
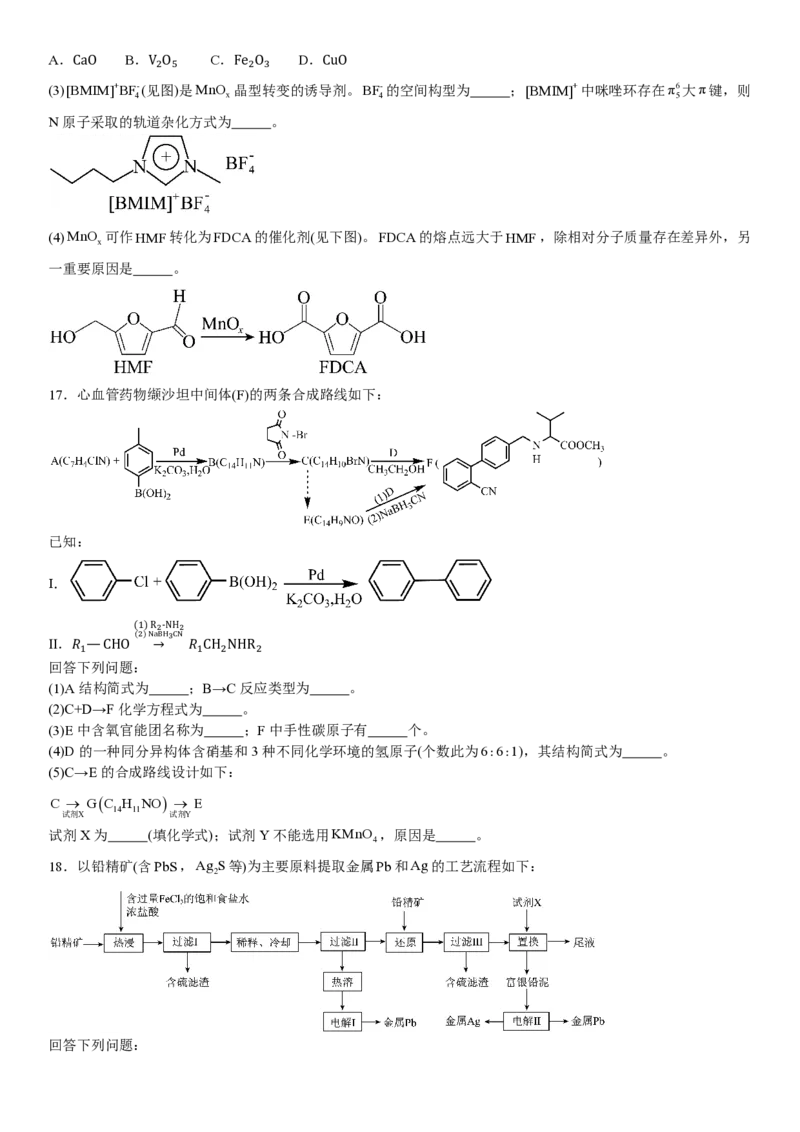
(3)[BCMaOIM]+BF-(见V2图O5)是MnO 晶Fe型2O转3 变的诱导Cu剂O。BF-的空间构型为 ;[BMIM]+中咪唑环存在π6大π键,则
4 x 4 5
N原子采取的轨道杂化方式为 。
(4)MnO 可作HMF转化为FDCA的催化剂(见下图)。FDCA的熔点远大于HMF,除相对分子质量存在差异外,另
x
一重要原因是 。
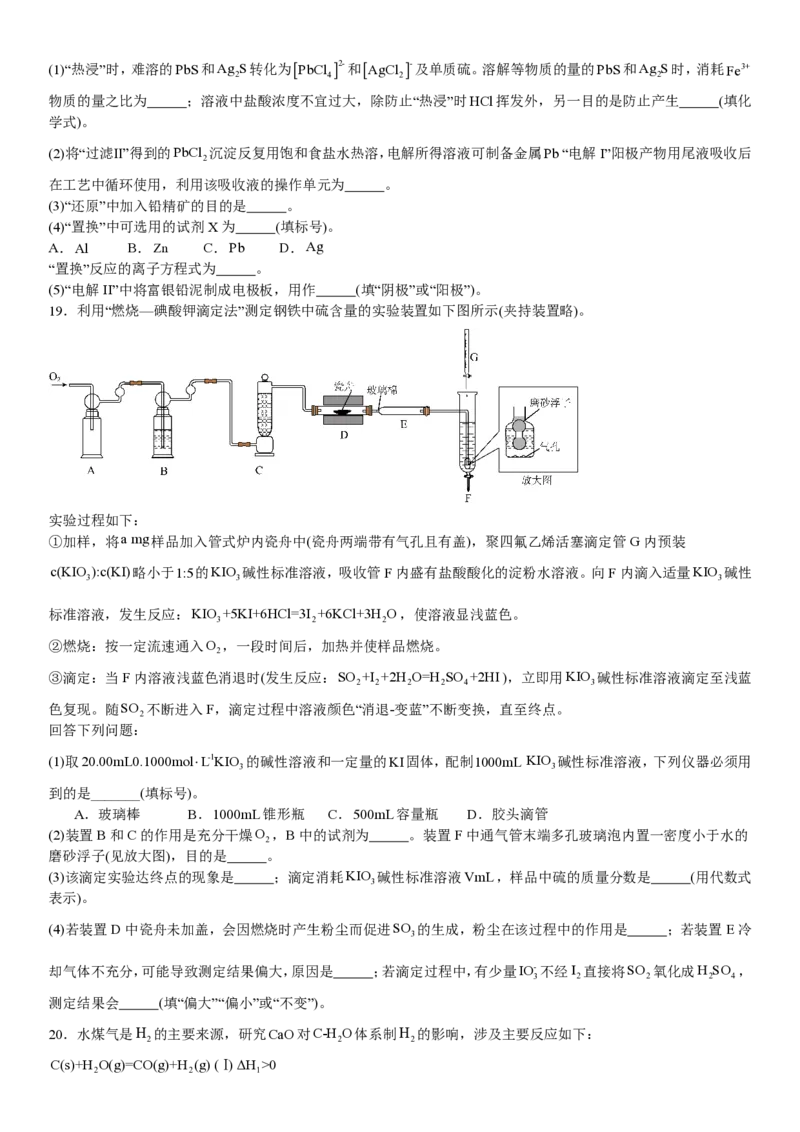
17.心血管药物缬沙坦中间体(F)的两条合成路线如下:
已知:
I.
Ⅱ.
(1) R2-NH2
(2) NaBH3CN
回答下列问题:
𝑅𝑅1—CHO → 𝑅𝑅1CH2NHR2
(1)A结构简式为 ;B→C反应类型为 。
(2)C+D→F化学方程式为 。
(3)E中含氧官能团名称为 ;F中手性碳原子有 个。
(4)D的一种同分异构体含硝基和3种不同化学环境的氢原子(个数此为6:6:1),其结构简式为 。
(5)C→E的合成路线设计如下:
C → G(C H NO) → E
试剂X 14 11 试剂Y
试剂X为 (填化学式);试剂Y不能选用KMnO ,原因是 。
4
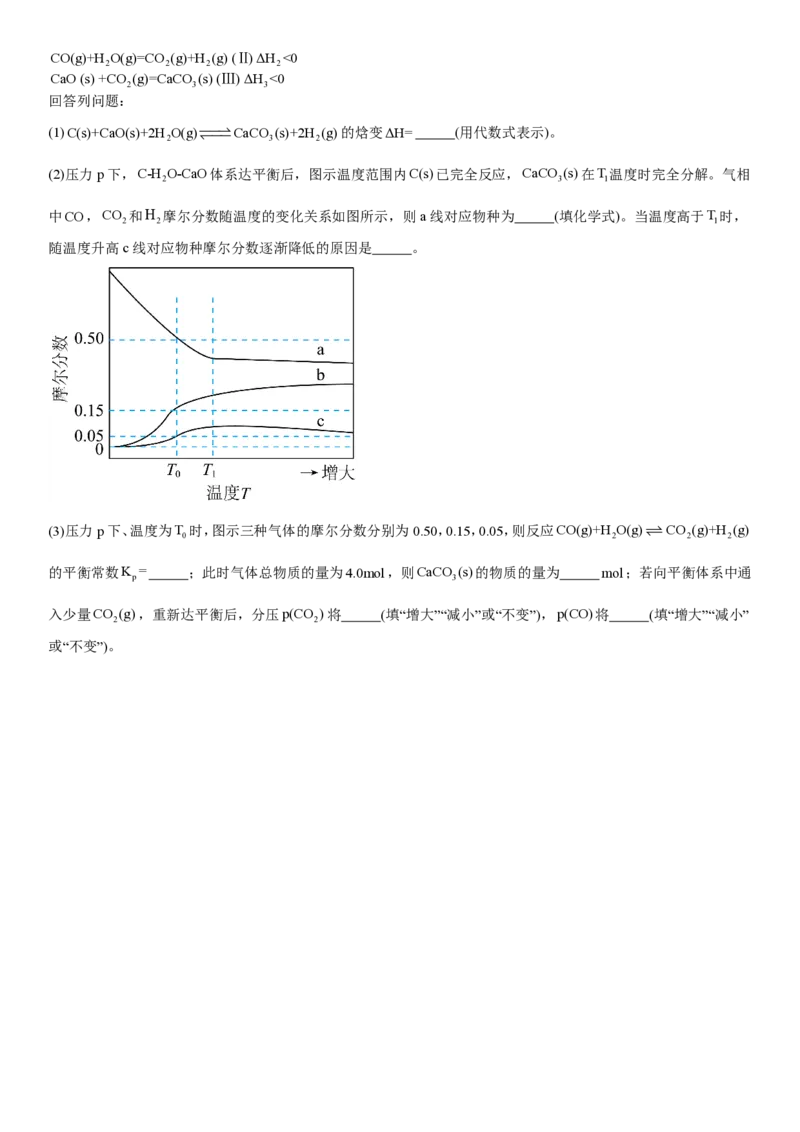
18.以铅精矿(含PbS,Ag S等)为主要原料提取金属Pb和Ag的工艺流程如下:
2
回答下列问题:(1)“热浸”时,难溶的PbS和Ag S转化为[PbCl ]2-和[AgCl ]-及单质硫。溶解等物质的量的PbS和Ag S时,消耗Fe3+
2 4 2 2
物质的量之比为 ;溶液中盐酸浓度不宜过大,除防止“热浸”时HCl挥发外,另一目的是防止产生 (填化
学式)。
(2)将“过滤Ⅱ”得到的PbCl 沉淀反复用饱和食盐水热溶,电解所得溶液可制备金属Pb“电解I”阳极产物用尾液吸收后
2
在工艺中循环使用,利用该吸收液的操作单元为 。
(3)“还原”中加入铅精矿的目的是 。
(4)“置换”中可选用的试剂X为 (填标号)。
A.Al B.Zn C.Pb D.Ag
“置换”反应的离子方程式为 。
(5)“电解II”中将富银铅泥制成电极板,用作 (填“阴极”或“阳极”)。
19.利用“燃烧—碘酸钾滴定法”测定钢铁中硫含量的实验装置如下图所示(夹持装置略)。
实验过程如下:
①加样,将a mg样品加入管式炉内瓷舟中(瓷舟两端带有气孔且有盖),聚四氟乙烯活塞滴定管G内预装
c(KIO ):c(KI)略小于1:5的KIO 碱性标准溶液,吸收管F内盛有盐酸酸化的淀粉水溶液。向F内滴入适量KIO 碱性
3 3 3
标准溶液,发生反应:KIO +5KI+6HCl=3I +6KCl+3H O,使溶液显浅蓝色。
3 2 2
②燃烧:按一定流速通入O ,一段时间后,加热并使样品燃烧。
2
③滴定:当F内溶液浅蓝色消退时(发生反应:SO +I +2H O=H SO +2HI),立即用KIO 碱性标准溶液滴定至浅蓝
2 2 2 2 4 3
色复现。随SO 不断进入F,滴定过程中溶液颜色“消退-变蓝”不断变换,直至终点。
2
回答下列问题:
(1)取20.00mL0.1000mol⋅L-1KIO 的碱性溶液和一定量的KI固体,配制1000mL KIO 碱性标准溶液,下列仪器必须用
3 3
到的是_______(填标号)。
A.玻璃棒 B.1000mL锥形瓶 C.500mL容量瓶 D.胶头滴管
(2)装置B和C的作用是充分干燥O ,B中的试剂为 。装置F中通气管末端多孔玻璃泡内置一密度小于水的
2
磨砂浮子(见放大图),目的是 。
(3)该滴定实验达终点的现象是 ;滴定消耗KIO 碱性标准溶液VmL,样品中硫的质量分数是 (用代数式
3
表示)。
(4)若装置D中瓷舟未加盖,会因燃烧时产生粉尘而促进SO 的生成,粉尘在该过程中的作用是 ;若装置E冷
3
却气体不充分,可能导致测定结果偏大,原因是 ;若滴定过程中,有少量IO-不经I 直接将SO 氧化成H SO ,
3 2 2 2 4
测定结果会 (填“偏大”“偏小”或“不变”)。
20.水煤气是H 的主要来源,研究CaO对C-H O体系制H 的影响,涉及主要反应如下:
2 2 2
C(s)+H O(g)=CO(g)+H (g) (Ⅰ) ΔH >0
2 2 1CO(g)+H O(g)=CO (g)+H (g) (Ⅱ) ΔH <0
2 2 2 2
CaO (s) +CO (g)=CaCO (s) (Ⅲ) ΔH <0
2 3 3
回答列问题:
(1)C(s)+CaO(s)+2H O(g)CaCO (s)+2H (g)的焓变ΔH= (用代数式表示)。
2 3 2
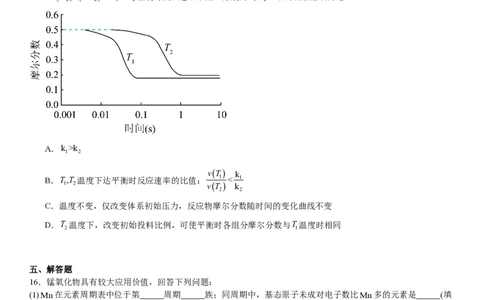
(2)压力p下,C-H O-CaO体系达平衡后,图示温度范围内C(s)已完全反应,CaCO (s)在T温度时完全分解。气相
2 3 1
中CO,CO 和H 摩尔分数随温度的变化关系如图所示,则a线对应物种为 (填化学式)。当温度高于T时,
2 2 1
随温度升高c线对应物种摩尔分数逐渐降低的原因是 。
(3)压力p下、温度为T 时,图示三种气体的摩尔分数分别为0.50,0.15,0.05,则反应CO(g)+H O(g)CO (g)+H (g)
0 2 2 2
的平衡常数K = ;此时气体总物质的量为4.0mol,则CaCO (s)的物质的量为 mol;若向平衡体系中通
p 3
入少量CO (g),重新达平衡后,分压p(CO )将 (填“增大”“减小”或“不变”),p(CO)将 (填“增大”“减小”
2 2
或“不变”)。