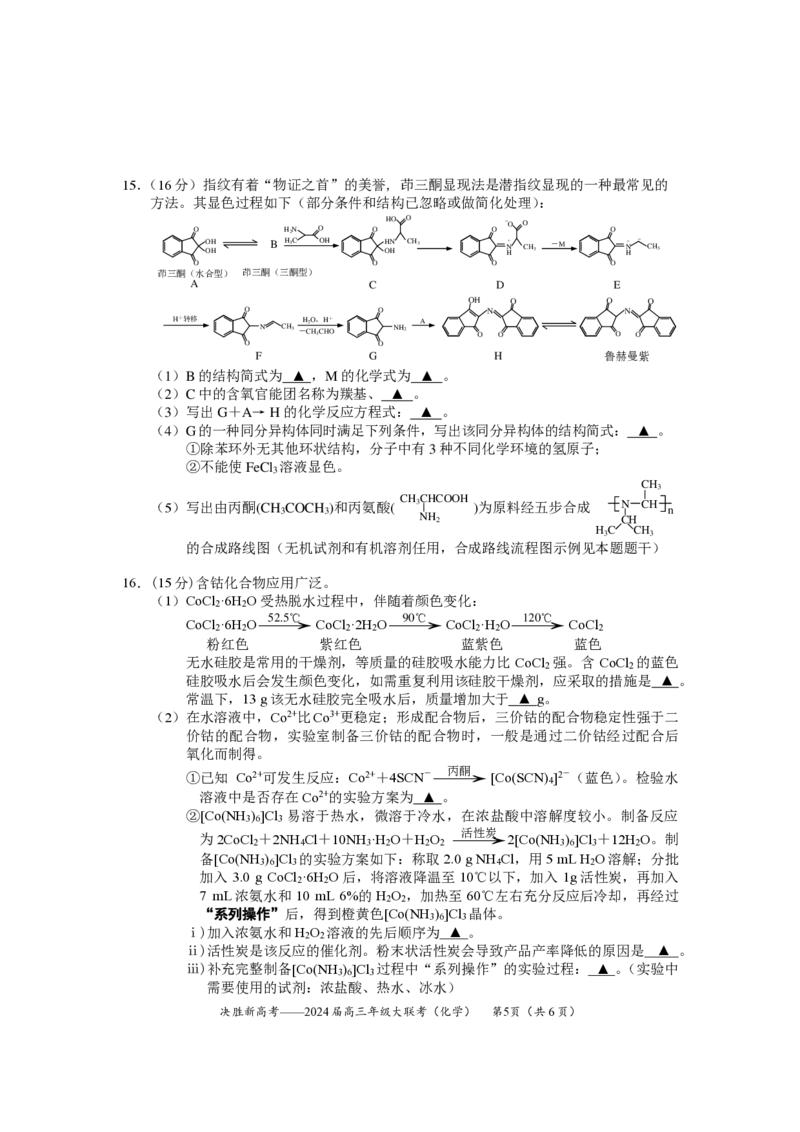文档内容
决胜新高考——2024届高三年级大联考
化 学
可能用到的相对原子质量:H 1 C 12 O 16 Cl 35.5 Co 59
一、单项选择题:共13题,每题3分,共39分。每题只有一个选项最符合题意。
1.2023年9月23日,第19届杭州亚运会开幕式首次使用废碳再生的绿色甲醇作为主火
炬塔燃料,实现循环内二氧化碳零排放。该措施最积极的意义在于
.
A.有利于实现碳中和 B.有利于降低火炬燃料成本
C.有利于燃料充分燃烧 D.使开幕式点火场面更壮观
2.下列化学用语表示正确的是
A.HClO的结构式:H-Cl-O B.Na O 的电子式:
2 2
决胜新高考——2024届高三年级大联考(化学) 第1页(共6页)
N a O O N a
C.NH 的空间构型:平面三角形 D.16O的原子结构示意图: 3 + 8 2 6
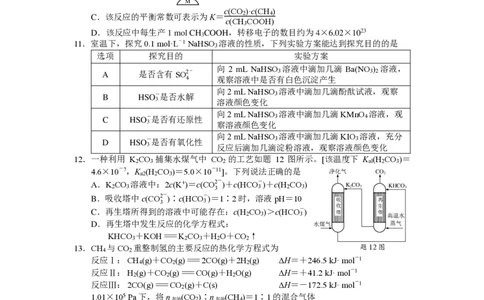
3.实验室制备少量SO 并探究其性质,下列实验原理与装置能达到实验目的的是
2
C
稀
u
硫
粉
酸
S O
2
K
酸M 性n
S
O
O
4
2
H
S
O2
O
2
注 意 事 项
考生在答题前请认真阅读本注意事项及各题答题要求
1.本试卷共6页,满分为100分,考试时间为75分钟。考试结束后,请将本试卷和答题卡一
并交回。
2.答题前,请务必将自己的姓名、准考证号用0.5毫米黑色墨水的签字笔填写在试卷及答题
卡的规定位置。
3.请认真核对监考员在答题卡上所粘贴的条形码上的姓名、准考证号与本人是否相符。
4.作答选择题,必须用2B铅笔将答题卡上对应选项的方框涂满涂黑;如需改动,请用橡皮擦
干净后,再选涂其他答案。作答非选择题,必须用0.5毫米黑色墨水的签字笔在答题卡上
的指定位置作答,在其他位置作答一律无效。
5.如需作图,必须用2B铅笔绘、写清楚,线条、符号等须加黑、加粗。
A.制取 SO B.收集 SO C.验证 SO 还原性 D.吸收SO 尾气
2 2 2 2
4.前四周期主族元素 X、Y、Z、Q 的原子序数依次增大,基态X原子核外电子占据两种
形状不同的原子轨道,且两种轨道中电子总数相等,Q与X处于同一主族。Y的周期
序数与族序数相等,Z的第二电离能远小于第三电离能。下列说法正确的是
A.电负性:χ(X)<χ(Q)
B.最高价氧化物对应水化物的碱性:Y<Z
C.Z的氯化物是工业漂白粉的有效成分
D.X形成的氢化物中只有极性共价键
{#{QQABAQSUoggIABJAAAgCAwFCCkKQkBACAAoOxAAAoAAAABNABAA=}#}阅读下列材料,完成 5~7题:
碳元素能形成CO、CO 、CH 、CaC 、CH COOH等多种化合物;其单质也有多种用
2 4 2 3
途,如足量 C(s)与 H O(g)反应生成 1 mol H (g)和 1 mol CO(g)时,吸收 131.3kJ 的热量,该
2 2
反应可用于制取水煤气;被称为“黑金”的石墨烯也是一种碳单质,石墨烯是碳原子以
sp2杂化构成的六边形结构、只有一层原子厚度的二维晶体,又称为“新材料之王”。
5.下列说法正确的是
A.12C、13C、14C都属于碳的同素异形体
B.CaC 晶体中存在离子键和极性共价键
2
C.CH 和H O分子中中心原子的杂化方式均为sp3
4 2
D.石墨烯属于芳香烃的一种
6.下列化学反应表示正确的是
A.制取水煤气的热化学方程式:C(s)+H O(g)=H (g)+CO(g) ΔH=-131.3 kJ·mol-1
2 2
高温
B.高温下甲烷还原氧化铜:CH +CuO===== Cu +2H O+CO
4 2 2
C.乙酸除水垢:2H++CaCO =Ca2++CO ↑+H O
3 2 2
D.CaC 与水反应:CaC +2H O=Ca(OH) +C H ↑
2 2 2 2 2 2
7.下列物质结构与性质或物质性质与用途具有对应关系的是
A.CO具有还原性,可用作冶炼铁的原料
B.甲醛能溶于水,可用于制备酚醛树脂
C.石墨烯中碳原子采取sp2杂化,石墨烯具有导电性
D.C H OH分子间能形成氢键,C H OH与H O互溶
2 5 2 5 2
8.在给定条件下,下列选项所示的物质间转化能实现的是
A.NH
3
决胜新高考——2024届高三年级大联考(化学) 第2页(共6页)
O ,2 催 化 剂
NO
O
,2
H O2
HNO
3
B.HCl(aq)
M n O
2 Cl
2 点
F e
燃
FeCl
3
C.SO2- SO 2 S OH- SO2-
4 3
D.淀粉
稀 硫 酸
葡萄糖
银 氨 溶 液
CH CHO
3
9.芘主要存在于煤焦油、沥青的蒸馏物中,经氧化后可进一步用于染料、合成树脂、工
程塑料等的合成。以下是芘的一种转化路线:
芘
1 ) O
2 ) H
3
O A c , K I
O
O
X
O
O
1
2
) 6
) H
m
+
o l/L N a O H
O
O
O
Y
O
+
O
O
O
OZ
下列叙述正确的是
A.X、Y、Z互为同系物
B.Y中的所有原子都在同一平面上
C.X能发生氧化、还原、消去反应
D.Y的水解产物不能与FeCl 溶液发生显色反应
3
{#{QQABAQSUoggIABJAAAgCAwFCCkKQkBACAAoOxAAAoAAAABNABAA=}#}10.一种CH -CO 分步梯阶转化合成乙酸的可能反应机理如下(M为一种金属催化剂)
4 2
决胜新高考——2024届高三年级大联考(化学) 第3页(共6页)
C H 4
M
H 2
X
C O 2 C H Ox C
M
O H 2
C H C3 O O H
M
下列说法正确的是
A.该反应机理中H 是催化剂
2
B.中间体X可表示为
C
M
H
x
c(CO )·c(CH )
C.该反应的平衡常数可表示为 K= 2 4
c(CH COOH)
3
D.该反应中每生产 1 mol CH COOH,转移电子的数目约为 4×6.02×1023
3
11.室温下,探究 0.1 mol·L-1 NaHSO 溶液的性质,下列实验方案能达到探究目的的是
3
选项 探究目的 实验方案
向 2 mL NaHSO 溶液中滴加几滴 Ba(NO ) 溶液,
A 是否含有SO2- 3 3 2
4 观察溶液中是否有白色沉淀产生
向2 mL NaHSO 溶液中滴加几滴酚酞试液,观察
B HSO-是否水解 3
3 溶液颜色变化
向2 mL NaHSO 溶液中滴加几滴KMnO 溶液,观
C HSO-是否有还原性 3 4
3 察溶液颜色变化
向2 mL NaHSO 溶液中滴加几滴KIO 溶液,充分
D HSO-是否有氧化性 3 3
3 反应后滴加几滴淀粉溶液,观察溶液颜色变化
12.一种利用 K CO 捕集水煤气中 CO 的工艺如题 12 图所示。[该温度下 K (H CO )=
2 3 2 al 2 3
4.6×10-7,K (H CO )=5.0×10-11]。下列说法正确的是 a2 2 3
A.K CO 溶液中:2c(K+)=c(CO2-)+c(HCO-)+c(H CO ) 2 3 3 3 2 3
B.吸收塔中c(CO2-)∶c(HCO-)=1∶2时,溶液pH=10
3 3
C.再生塔所得到的溶液中可能存在:c(H CO )>c(HCO-)
2 3 3
D.再生塔中发生反应的化学方程式:
KHCO +KOH=K CO +H O+CO ↑
3 2 3 2 2
13.CH 与CO 重整制氢的主要反应的热化学方程式为
4 2
反应Ⅰ: CH (g)+CO (g)=2CO(g)+2H (g) ΔH=+246.5 kJ· mol-1
4 2 2
反应Ⅱ: H (g)+CO (g)=CO(g)+H O(g) ΔH=+41.2 kJ· mol-1
2 2 2
反应Ⅲ: 2CO(g)=CO (g)+C(s) ΔH=-172.5 kJ· mol-1
2
1.01×105 Pa下,将n (CO )∶n (CH )=1∶1的混合气体
起始 2 起始 4
置于密闭容器中,不同温度下重整体系中CH 和CO 的平衡
4 2
转化率如题13图所示。下列说法正确的是
A.反应Ⅰ的ΔS>0,反应Ⅱ的ΔS<0
B.反应3CH (g)+CO (g)+2H O(g)=4CO(g)+8H (g) 4 2 2 2
ΔH=+821.9 kJ· mol-1
C.500℃~800 ℃,反应Ⅲ进行的程度始终比反应Ⅱ的大
D.向重整体系中加入选择性更高的催化剂有助于提高 H 的
2
平衡产率
水 煤
净
气
%/率化转衡平
化
吸收塔
9 5
8 5
7 5
6 5
5 5
4 5
气
5
K
0 0
C2
C
O
H
3
4
C O 2
6 0 0
温 度
C O
再生塔
/
2
K H
高 温
蒸
7 0 0
C O 3
水
气
8 0 0
题12图
题13图
{#{QQABAQSUoggIABJAAAgCAwFCCkKQkBACAAoOxAAAoAAAABNABAA=}#}二、非选择题:共4题,共61分。
14.(15分)磷酸在工业中具有广泛应用,一种以氟磷灰石[主要含Ca F(PO ) ,还含SiO
5 4 3 2
等杂质]为原料生产磷酸的工艺流程如下。
决胜新高考——2024届高三年级大联考(化学) 第4页(共6页)
氟 磷 灰 石
H
酸
2 S O
解
4
过
石
滤
膏
粗 磷 酸
N a 2 C O 3
精
C
、
制
O
B
2
a C O 3
过
滤
滤
渣
磷 酸
已知: K (CaSO )=9.0×10-4; K (BaSiF )=1.0×10-6;K (Na SiF )=4.0×10-6。
sp 4 sp 6 sp 2 6
(1)①下列措施能提高“酸解”效率的是 ▲ (填序号)。
A.将磷灰石充分研磨 B.加快搅拌速率 C.使用90%的浓硫酸
②粗磷酸中含有H SiF 杂质,写出“酸解”生成H SiF 的化学方程式: ▲ 。
2 6 2 6
(2)“精制”时,先按物质的量之比n(Na CO )∶n(SiF2-)=1∶1加入Na CO 脱氟,
2 3 6 2 3
充分反应后,c(Na+)= ▲ mol·L-1;再加入BaCO ,加入BaCO 的目的是 ▲ 。
3 3
(3)氢氧化锆[Zr(OH) ]与磷酸反应可制得磷酸锆结合剂,磷酸锆结合剂中具有胶结
4
性能的化合物为磷酸二氢锆[Zr(H PO ) ]和磷酸一氢锆[Zr(HPO ) ],中和度
2 4 4 4 2
n(ZrO )
N [N = 2 ]在0.5~1之间的物质具有胶结性能。
m m n(P O )
2 5
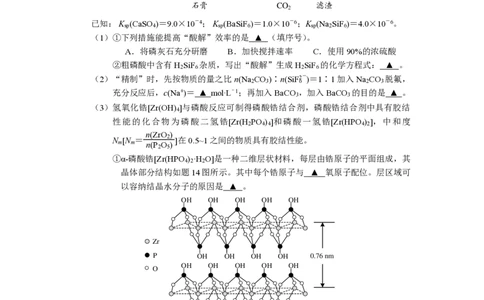
①α-磷酸锆[Zr(HPO ) ·H O]是一种二维层状材料,每层由锆原子的平面组成,其
4 2 2
晶体部分结构如题14图所示。其中每个锆原子与 ▲ 氧原子配位。层区域可
以容纳结晶水分子的原因是 ▲ 。
OH OH OH OH OH
Zr
P OH OH OH OH 0.76 nm
OH OH OH OH OH
O
OH OH OH OH
题14图
②当N =0.6时,结合剂中磷酸二氢锆和磷酸一氢锆物质的量之比为 ▲ (写
m
出计算过程)。
{#{QQABAQSUoggIABJAAAgCAwFCCkKQkBACAAoOxAAAoAAAABNABAA=}#}15.(16分)指纹有着“物证之首”的美誉, 茚三酮显现法是潜指纹显现的一种最常见的
方法。其显色过程如下(部分条件和结构已忽略或做简化处理):
O H2N O O
HO O
O
-O O
O
O O H H B H3C OH H O N H CH3 N H + CH3 -M N H + - CH3
O O O O
茚三酮(水合型) 茚三酮(三酮型)
A C D E
OH O O O
O O N N
H+转移
N CH3 -
H
C
2O
H
,
3C
H
H
+
O NH2
A
O O O O
O O
F G H 鲁赫曼紫
(1)B的结构简式为 ▲ ,M的化学式为 ▲ 。
(2)C中的含氧官能团名称为羰基、 ▲ 。
(3)写出G+A→ H 的化学反应方程式: ▲ 。
(4)G的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式: ▲ 。
①除苯环外无其他环状结构,分子中有3种不同化学环境的氢原子;
②不能使FeCl 溶液显色。
3
CH
3
CHCHCOOH
(5)写出由丙酮(CH 3 COCH 3 )和丙氨酸( 3 )为原料经五步合成 N CH n
NH 2 CH
HC CH
3 3
的合成路线图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)
16.(15分)含钴化合物应用广泛。
(1)CoCl ·6H O受热脱水过程中,伴随着颜色变化:
2 2
CoCl ·6H
O→52.5℃
CoCl ·2H
O→90℃
CoCl ·H
O→120℃
CoCl
2 2 2 2 2 2 2
粉红色 紫红色 蓝紫色 蓝色
无水硅胶是常用的干燥剂,等质量的硅胶吸水能力比 CoCl 强。含 CoCl 的蓝色
2 2
硅胶吸水后会发生颜色变化,如需重复利用该硅胶干燥剂,应采取的措施是 ▲ 。
常温下,13 g该无水硅胶完全吸水后,质量增加大于 ▲ g。
(2)在水溶液中,Co2+比Co3+更稳定;形成配合物后,三价钴的配合物稳定性强于二
价钴的配合物,实验室制备三价钴的配合物时,一般是通过二价钴经过配合后
氧化而制得。
丙酮
①已知 Co2+可发生反应:Co2++4SCN-→ [Co(SCN) ]2-(蓝色)。检验水
4
溶液中是否存在Co2+的实验方案为 ▲ 。
②[Co(NH ) ]Cl 易溶于热水,微溶于冷水,在浓盐酸中溶解度较小。制备反应
3 6 3
活性炭
为2CoCl +2NH Cl+10NH ·H O+H O →2[Co(NH ) ]Cl +12H O。制
2 4 3 2 2 2 3 6 3 2
备[Co(NH ) ]Cl 的实验方案如下:称取2.0 g NH Cl,用5 mL H O溶解;分批
3 6 3 4 2
加入 3.0 g CoCl ·6H O后,将溶液降温至 10℃以下,加入1g活性炭,再加入
2 2
7 mL浓氨水和 10 mL 6%的H O ,加热至 60℃左右充分反应后冷却,再经过
2 2
“系列操作”后,得到橙黄色[Co(NH ) ]Cl 晶体。
3 6 3
ⅰ)加入浓氨水和H O 溶液的先后顺序为 ▲ 。
2 2
ⅱ)活性炭是该反应的催化剂。粉末状活性炭会导致产品产率降低的原因是 ▲ 。
ⅲ)补充完整制备[Co(NH ) ]Cl 过程中“系列操作”的实验过程: ▲ 。(实验中
3 6 3
需要使用的试剂:浓盐酸、热水、冰水)
决胜新高考——2024届高三年级大联考(化学) 第5页(共6页)
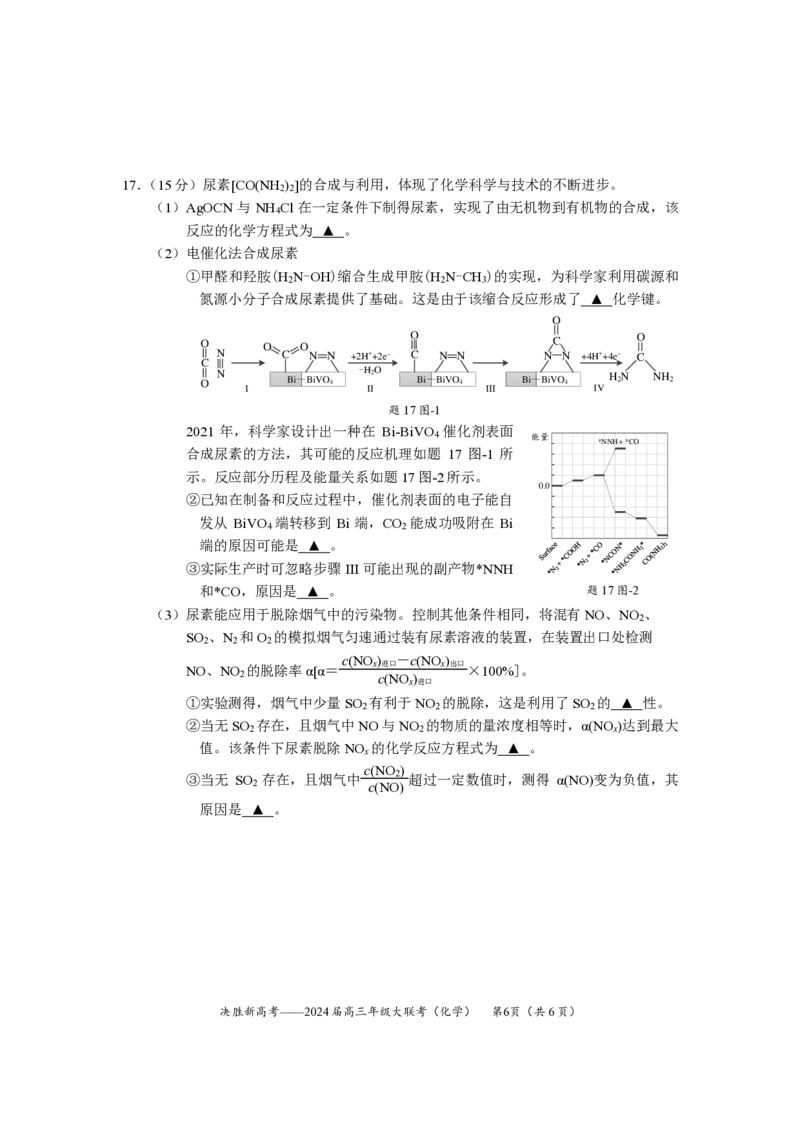
{#{QQABAQSUoggIABJAAAgCAwFCCkKQkBACAAoOxAAAoAAAABNABAA=}#}17.(15分)尿素[CO(NH ) ]的合成与利用,体现了化学科学与技术的不断进步。
2 2
(1)AgOCN与 NH Cl在一定条件下制得尿素,实现了由无机物到有机物的合成,该
4
反应的化学方程式为 ▲ 。
(2)电催化法合成尿素
①甲醛和羟胺(H N-OH)缩合生成甲胺(H N-CH )的实现,为科学家利用碳源和
2 2 3
氮源小分子合成尿素提供了基础。这是由于该缩合反应形成了 ▲ 化学键。
决胜新高考——2024届高三年级大联考(化学) 第6页(共6页)
O
C
O
N
N
I
O
C
B
O
—i
N
B iV O
N
4
+ + 2 H + 2
- H O2
II
e -
O
C
B —i
N
B iV O
N
4
III
B —i
O
C
N
B iV O
N
4
+ 4 + H +
IV
4
H
- e
N2
O
C
N H 2
题17图-1
2021 年,科学家设计出一种在 Bi-BiVO 催化剂表面
4 能量
*NNH + *CO
合成尿素的方法,其可能的反应机理如题 17 图-1 所
示。反应部分历程及能量关系如题17图-2所示。
0.0
②已知在制备和反应过程中,催化剂表面的电子能自
发从 BiVO 端转移到 Bi 端,CO 能成功吸附在 Bi
4 2
端的原因可能是 ▲ 。
③实际生产时可忽略步骤 III可能出现的副产物*NNH
和*CO,原因是 ▲ 。 题17图-2
(3)尿素能应用于脱除烟气中的污染物。控制其他条件相同,将混有NO、NO 、
2
SO 、N 和O 的模拟烟气匀速通过装有尿素溶液的装置,在装置出口处检测
2 2 2
c(NO) -c(NO)
NO、NO 的脱除率α[α= x 进口 x 出口×100%]。
2 c(NO)
x 进口
①实验测得,烟气中少量SO 有利于NO 的脱除,这是利用了SO 的 ▲ 性。
2 2 2
②当无SO 存在,且烟气中NO与NO 的物质的量浓度相等时,α(NO )达到最大
2 2 x
值。该条件下尿素脱除NO 的化学反应方程式为 ▲ 。
x
c(NO )
③当无 SO 存在,且烟气中 2 超过一定数值时,测得 α(NO)变为负值,其
2 c(NO)
原因是 ▲ 。
{#{QQABAQSUoggIABJAAAgCAwFCCkKQkBACAAoOxAAAoAAAABNABAA=}#}