文档内容
高三上学期化学第一次阶段测试题
(时间:90分钟,满分:100分)2023.10
注意事项:
1.答卷前,考生务必将姓名、班级、准考证号填在答题纸规定的位置上。
2.第Ⅰ卷每小题选出答案后,用2B铅笔把答题纸上对应的答案标号涂黑;如需改动,用橡皮擦
干净后,再选涂其他答案标号。
3.第II卷必须用中性笔作答,答案必须写在答题纸各题目指定区域内相应位置;如需改动,先
划掉原来的答案,然后再写上新的答案;不准使用涂改液、胶带纸、修正带。
卷Ⅰ(选择题共40分)
注意事项:
1.答卷Ⅱ前务必将自己的姓名、班级、考号、座号填在答卷纸规定的地方。
2.答卷Ⅱ时用中性笔直接填写在答卷纸规定的地方。
3.交卷时只交答题卷。
相对原子量:H1 C12 O16 P31 S32 Cu64 Zn65 Fe56 Ba137
一、单选题(每小题只有一个选项,1个2分,共20分)
1.诗词是中华民族的文化瑰宝,下列分析中不正确的是( )
A.“白云深处有人家”:“白云”是一种胶体
B.“蜡炬成灰泪始干”:该过程中只发生了物理变化
C.“爆竹声中一岁除”:燃放爆竹过程中涉及氧化还原反应
D.“烈火焚烧若等闲”:描述了碳酸钙的分解,碳酸钙是一种电解质
2.某合作学习小组讨论辨析:
①漂白粉和酸雨都是混合物②煤和石油都是可再生能源③蔗糖、硫酸钡和水分别属于非电解质、电解质和弱
电解质④不锈钢和目前流通的硬币都是合金⑤硫酸、纯碱、醋酸钠和生石灰分别属于醋碱、盐和氧化物⑥豆
浆和雾都是胶体
上述说法正确的是( )
A.①②④ B.①⑤⑥ C.①③④⑥ D.②③④⑤
3.类比推理是化学学习中的一种重要方法.下列类推结论中,正确的是( )
类比对象 结论
A
B
C
D
4.设 为阿伏加德罗常数的值。下列有关叙述不正确的是( )
A.乙烯和环丁烷( )的混合气体共28g含有的原子数目为
学科网(北京)股份有限公司B.已知白磷分子( )呈正四面体结构,则31g白磷中含P—P键的数目为
C. 溶液中, 、 和 的微粒数之和为
D.在 反应中,若反应中电子转移的数目为 ,则有212g
氯气生成
5.下列分子或离子在指定的分散系中能大量共存的一组是( )
A.空气:HCl、 、 、NO
B.含有 溶液: 、 、 、
C.高锰酸钾溶液: 、 、 、
D.氢氧化铁胶体: 、 、 、
6.下列反应的方程式不正确的是( )
A.苯酚与氯化铁溶液反应显紫色:
B.硫酸铜溶液中加入少量的氨水:
C.用 溶液吸收少量
D.向 溶液中滴加 溶液至沉淀质量最大:
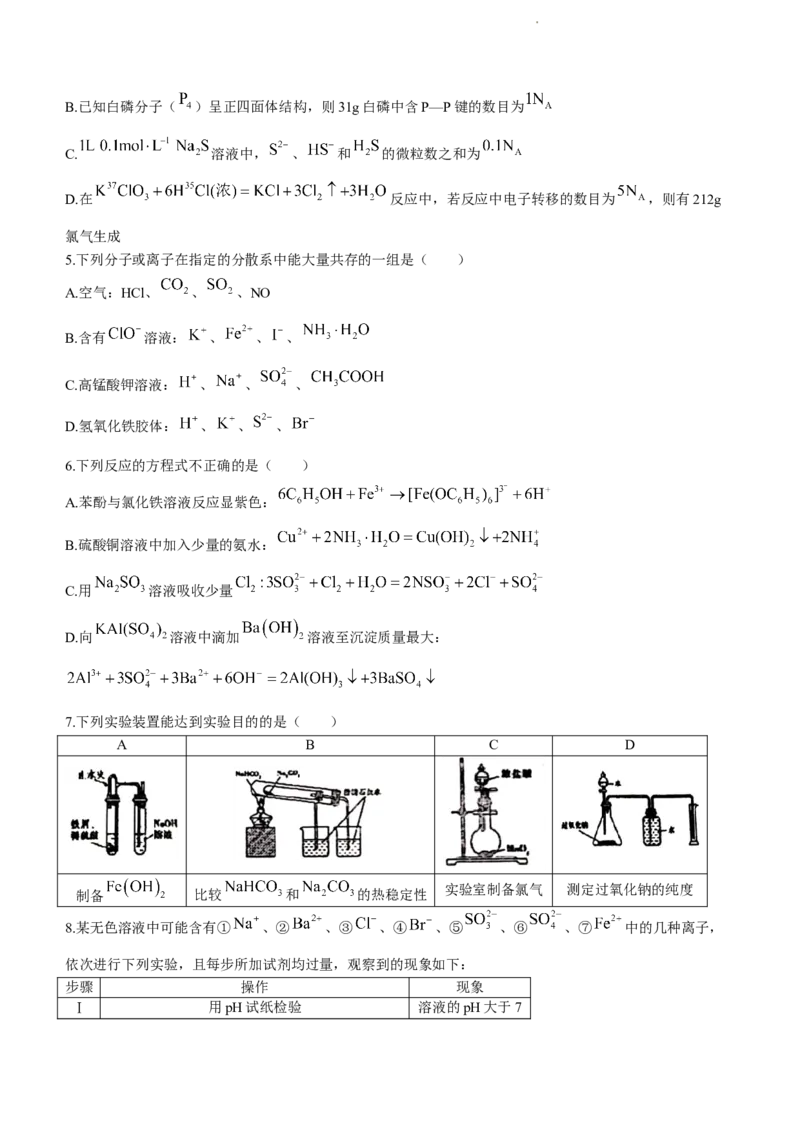
7.下列实验装置能达到实验目的的是( )
A B C D
实验室制备氯气 测定过氧化钠的纯度
制备 比较 和 的热稳定性
8.某无色溶液中可能含有① 、② 、③ 、④ 、⑤ 、⑥ 、⑦ 中的几种离子,
依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
步骤 操作 现象
Ⅰ 用pH试纸检验 溶液的pH大于7
学科网(北京)股份有限公司层呈橙红色
Ⅱ
向溶液中滴加氯水,再加入 ,振荡,静置
Ⅲ 有白色沉淀产生
取Ⅱ的上层溶液,加入 溶液和稀硝酸
有白色沉淀产生
Ⅳ
将Ⅲ过滤,向滤液中加入 溶液和稀硝酸
下列结论正确的是( )
A.肯定含有的离子是①④⑤ B.肯定没有的离子是②⑤⑦
C.可能含有的离子是①②⑥ D.不能确定的离子是①③⑥
9.在一密闭容器中有CO、 、 共16.5g和足量的 ,用电火花引燃,使其完全反应, 增重
7.5g,则原混合气体中 的质量分数是( )
A.54.5% B.40% C.36% D.33.3%
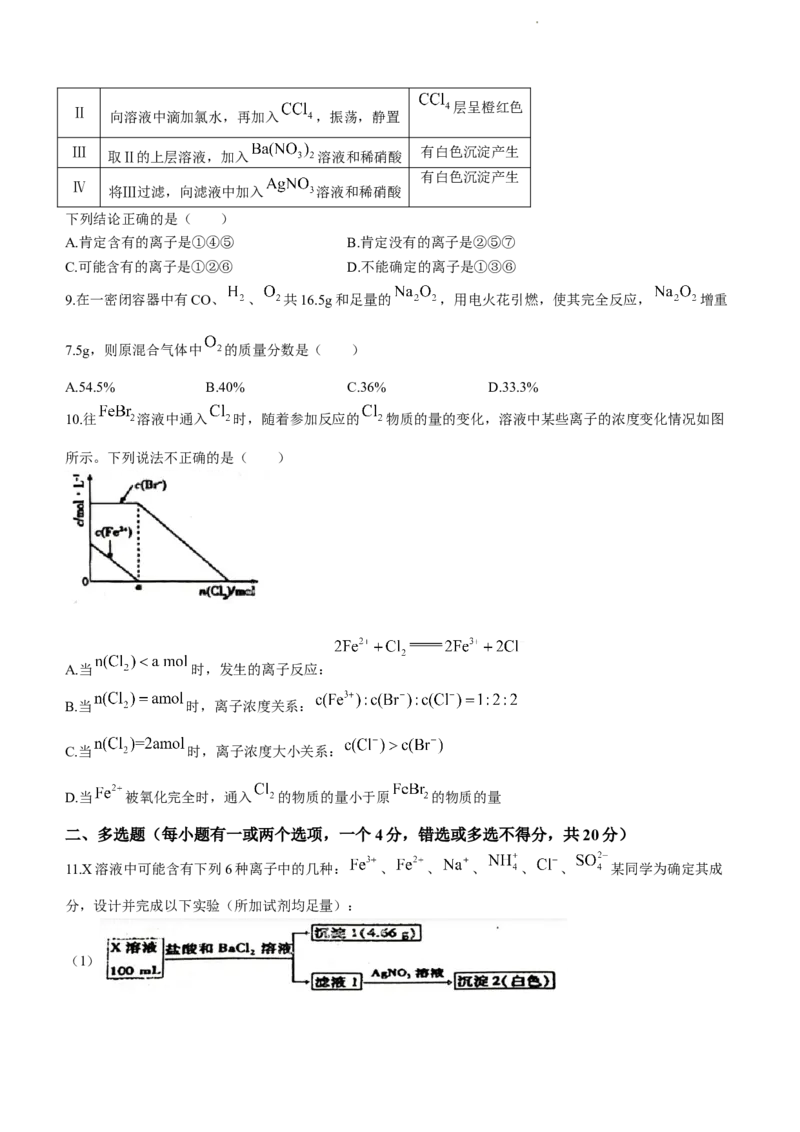
10.往 溶液中通入 时,随着参加反应的 物质的量的变化,溶液中某些离子的浓度变化情况如图
所示。下列说法不正确的是( )
A.当 时,发生的离子反应:
B.当 时,离子浓度关系:
C.当 时,离子浓度大小关系:
D.当 被氧化完全时,通入 的物质的量小于原 的物质的量
二、多选题(每小题有一或两个选项,一个4分,错选或多选不得分,共20分)
11.X溶液中可能含有下列6种离子中的几种: 、 、 、 、 、 某同学为确定其成
分,设计并完成以下实验(所加试剂均足量):
(1)
学科网(北京)股份有限公司(2)
下列说法正确的是( )
A.X溶液中一定存在 、
B.X溶液中一定存在 、 ,至少含有 、 、中的一种,可能含有
C.取少量X溶液,先加入适量氯水,再加少量KSCN溶液,若溶液呈红色,则含有
D.X溶液中一定含有 ,且
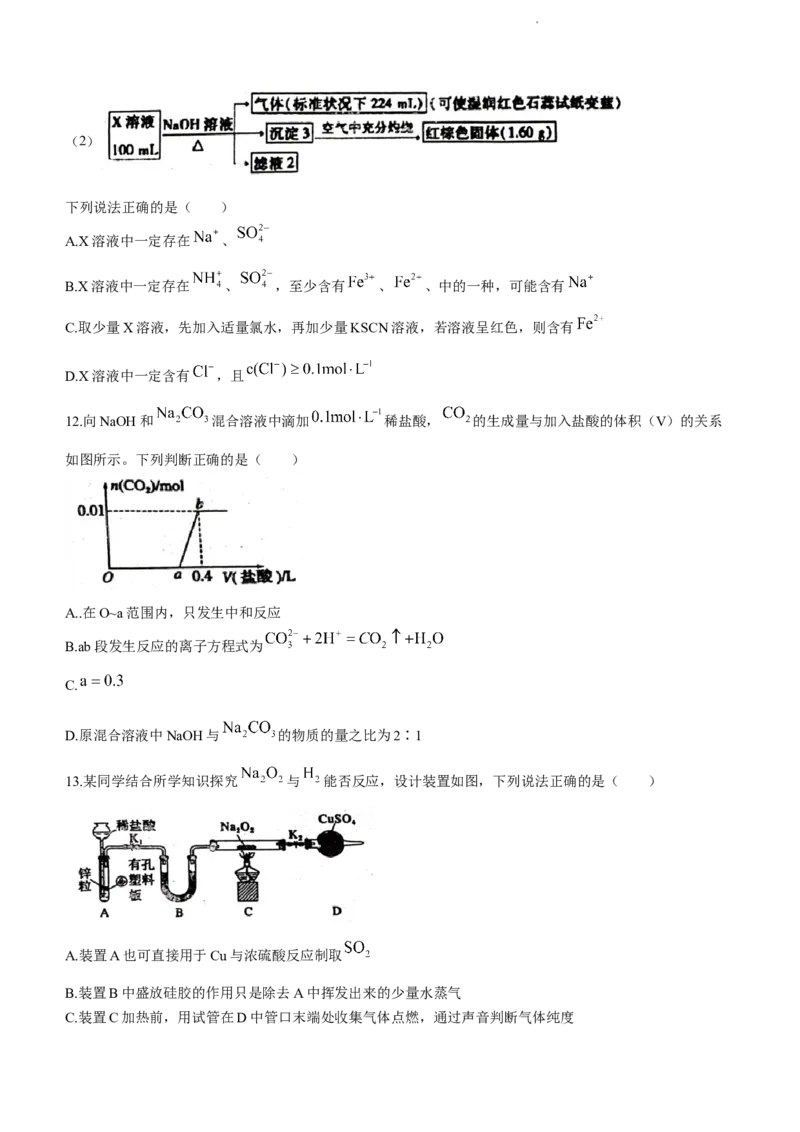
12.向NaOH和 混合溶液中滴加 稀盐酸, 的生成量与加入盐酸的体积(V)的关系
如图所示。下列判断正确的是( )
A..在O~a范围内,只发生中和反应
B.ab段发生反应的离子方程式为
C.
D.原混合溶液中NaOH与 的物质的量之比为2∶1
13.某同学结合所学知识探究 与 能否反应,设计装置如图,下列说法正确的是( )
A.装置A也可直接用于Cu与浓硫酸反应制取
B.装置B中盛放硅胶的作用只是除去A中挥发出来的少量水蒸气
C.装置C加热前,用试管在D中管口末端处收集气体点燃,通过声音判断气体纯度
学科网(北京)股份有限公司D.装置A气密性检查的方法:直接向长颈漏斗中加水,当漏斗中液面高于试管液面且高度不变说明气密性良
好
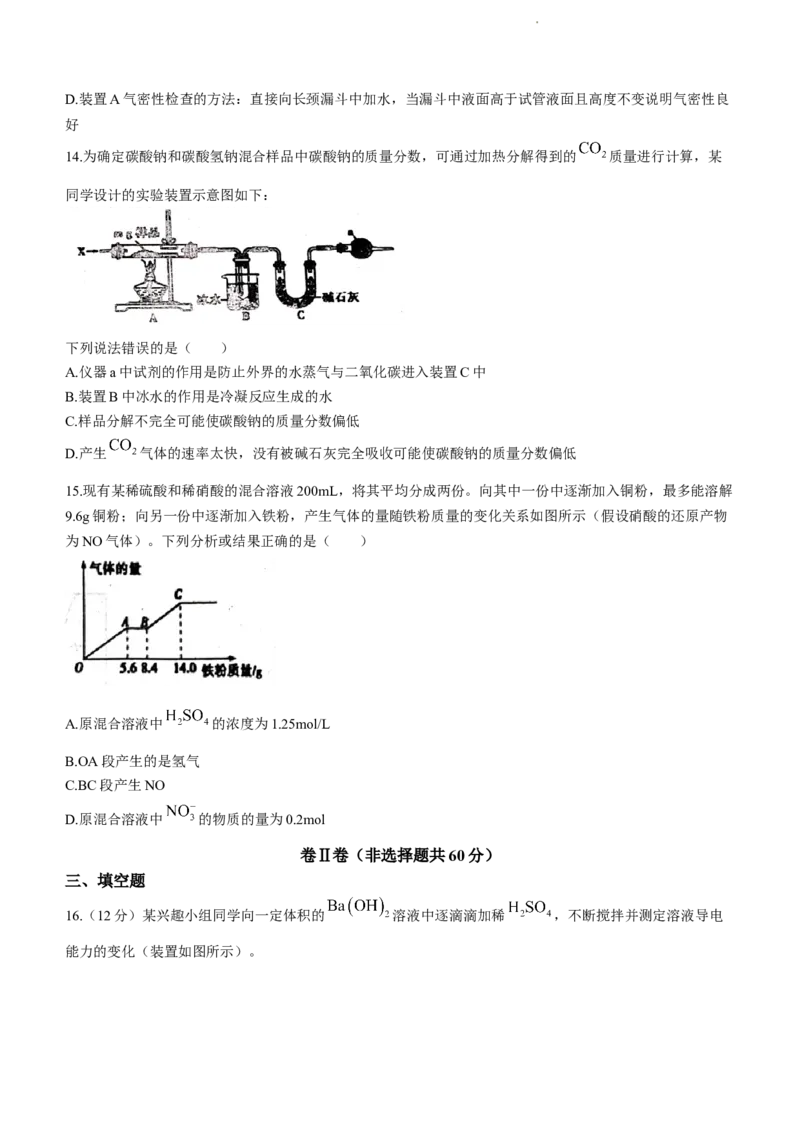
14.为确定碳酸钠和碳酸氢钠混合样品中碳酸钠的质量分数,可通过加热分解得到的 质量进行计算,某
同学设计的实验装置示意图如下:
下列说法错误的是( )
A.仪器a中试剂的作用是防止外界的水蒸气与二氧化碳进入装置C中
B.装置B中冰水的作用是冷凝反应生成的水
C.样品分解不完全可能使碳酸钠的质量分数偏低
D.产生 气体的速率太快,没有被碱石灰完全吸收可能使碳酸钠的质量分数偏低
15.现有某稀硫酸和稀硝酸的混合溶液200mL,将其平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解
9.6g铜粉;向另一份中逐渐加入铁粉,产生气体的量随铁粉质量的变化关系如图所示(假设硝酸的还原产物
为NO气体)。下列分析或结果正确的是( )
A.原混合溶液中 的浓度为1.25mol/L
B.OA段产生的是氢气
C.BC段产生NO
D.原混合溶液中 的物质的量为0.2mol
卷Ⅱ卷(非选择题共60分)
三、填空题
16.(12分)某兴趣小组同学向一定体积的 溶液中逐滴滴加稀 ,不断搅拌并测定溶液导电
能力的变化(装置如图所示)。
学科网(北京)股份有限公司Ⅰ.实验测得混合溶液的导电能力随时间变化的曲线如图所示。
(1)实验现象烧杯中有白色沉淀产生,小灯泡______。
(2)下列说法正确的是______(填字母)。
a.AB段溶液的导电能力不断减弱,说明生成的 不是电解质
b.B处溶液的导电能力约为0,说明溶液中几乎没有自由移动的离子
c.a时刻 溶液与稀 恰好中和
d.BC段溶液的导电能力不断增大,主要是由于过量的 电离出的离子导电
Ⅱ.配制 溶液
(1)计算:需要 溶液______mL(计算结果精确到小数点后一位)。
(2)配制过程中,不需要使用的仪器有______(填序号)。
①量筒②托盘天平③烧瓶④250mL容量瓶⑤烧杯⑥玻璃棒⑦胶头滴管
(3)配制过程中正确的操作顺序是b、d、______、e(填字母)。
a.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液均注入容量瓶
b.用量筒量取所需体积的 溶液注入盛有约50mL蒸馏水的烧杯
c.用胶头滴管滴加蒸馏水,至溶液的凹液面与刻度线相切
d.用玻璃棒慢慢搅动,混合均匀
e.盖好容量瓶瓶塞,反复上下颠倒,摇匀
f.将稀释后的 溶液沿玻璃棒注入250mL容量瓶
g.往容量瓶中加入蒸馏水,直到液面在容量瓶刻度线下1~2cm处
(4)下列操作将导致所配制的 溶液浓度偏大的是______(填字母)。
a.移液过程有 溶液溅出瓶外
b.移液后未洗涤烧杯和玻璃棒
学科网(北京)股份有限公司c.定容时俯视容量瓶刻度线
d.加水超过刻度线,用胶头滴管吸出多余液体
17.(8分)钒性能优良,用途广泛,有金属“维生素”之称。完成下列填空:
(1)将废钒催化剂(主要成分 )与稀硫酸、亚硫酸钾溶液混合,充分反应后生成 等离子,该反
应的化学方程式是__________________。
(2)向上述所得溶液中加入 溶液,完善并配平反应的离子方程式。
(3) 能与盐酸反应产生 和一种黄绿色气体,该气体能与 溶液反应被吸收,则 、
、 还原性由大到小的顺序是______。
(4)在: 溶液中,加入0.195g锌粉,恰好完全反应,则还原产物可能是______。
a. B. C. D.V
18.(10分)铜镉渣主要含锌、铜、铁、镉(Cd)、钴(Co)等单质。湿法炼锌产生的铜镉渣用于生产金属
镉的工艺流程如下:
下表列出了相关金属离子生成氢氧化物沉淀的pH(金属离子的起始浓度为 )。
氢氧化物
开始沉淀的pH 1.5 6.5 7.2
沉淀完全的pH 3.3 9.9 9.5
(1)酸浸时粉碎铜镉渣的目的是______。
(2)操作Ⅰ产生的滤渣Ⅰ主要成分为______(填化学式)。
(3)①操作Ⅲ中先加入适量 ,发生反应的离子方程式为______。
②再加入ZnO控制反应液的pH,pH范围为______。
③若加入的 不足,加入ZnO后所得的电解液中会含有Fe元素。如果要检验电解液中的铁元素,可以加
入的试剂是________________。
四、实验题
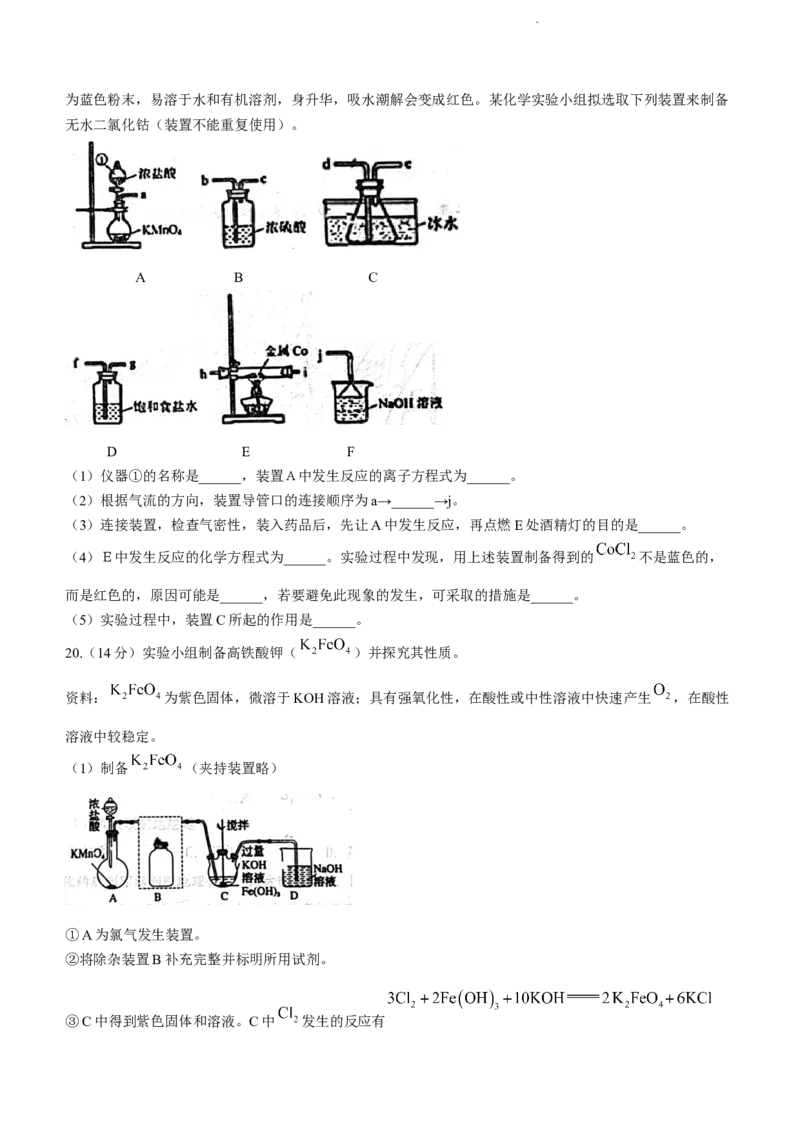
19.(16分)无水二氯化钴( )常用作干湿指示剂、氨的吸收剂、防毒面具和肥料添加剂等。
学科网(北京)股份有限公司为蓝色粉末,易溶于水和有机溶剂,身升华,吸水潮解会变成红色。某化学实验小组拟选取下列装置来制备
无水二氯化钴(装置不能重复使用)。
A B C
D E F
(1)仪器①的名称是______,装置A中发生反应的离子方程式为______。
(2)根据气流的方向,装置导管口的连接顺序为a→______→j。
(3)连接装置,检查气密性,装入药品后,先让A中发生反应,再点燃E处酒精灯的目的是______。
(4)E中发生反应的化学方程式为______。实验过程中发现,用上述装置制备得到的 不是蓝色的,
而是红色的,原因可能是______,若要避免此现象的发生,可采取的措施是______。
(5)实验过程中,装置C所起的作用是______。
20.(14分)实验小组制备高铁酸钾( )并探究其性质。
资料: 为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生 ,在酸性
溶液中较稳定。
(1)制备 (夹持装置略)
①A为氯气发生装置。
②将除杂装置B补充完整并标明所用试剂。
③C中得到紫色固体和溶液。C中 发生的反应有
学科网(北京)股份有限公司,另外还有__________________
(2)探究 的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有 。为证明是否
氧化了 而产生 ,设计以下方案:
方案Ⅰ 取少量a,滴加KSCN溶液至过量,溶液呈红色
方案Ⅱ
用KOH溶液充分洗涤C中所得固体,再用KOH溶液将 溶出,得到紫色溶液b,取少量
b,滴加盐酸,有 产生
ⅰ.由方案Ⅰ中溶液变红可知a中含有______,但该离子的产生不能判断一定是 将 氧化,还可能
由____________产生(用方程式表示)。
ⅱ.方案Ⅱ可证明 氧化了 。用KOH溶液洗涤的目的是______。
②根据 的制备实验得出:氧化性: ______ (填“>”或“<”),而方案Ⅱ实验表明,
和 的氧化性强弱关系相反,原因是______。
③资料表明,酸性溶液中的氧化性: > ,验证实验如下:将溶液b滴入 和足量
的混合溶液中,振荡后溶液呈浅紫色。该现象能否证明氧化性: > 。若能,请说明理由;若不
能,进一步设计实验方案。
理由或方案:______。
(3)铁矿石中的铁元素通常以氧化物形式存在,可用通式 表示。为了确定某铁矿石中的 的组
成,现进行如下实验:将少量该铁矿石样品粉碎,称取12.5g样品于烧杯中,加入稀硫酸充分溶解,并不断
加热、搅拌(假设只有Fe的氧化物溶解),过滤后,向所得滤液中加入5.0g铜粉,充分反应后过滤、洗涤、
干燥得剩余固体1.8g,再将该过程所得滤液用浓度为1.0mol/L的酸性 溶液滴定至终点,此时消耗酸
性 溶液的体积为25.0mL。
已知: ,
的化学式(m、n为正整数)为____________
学科网(北京)股份有限公司