文档内容
2024 北京丰台高三一模
化 学
2024.03
本试卷共10页,100分。考试时长90分钟。考生务必将答案答在答题卡上,在试卷上作答无效。考试
结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 O 16 Cu 64 Se 79
第一部分
本部分共14题,每题3分,共42分。在每题列出的四个选项中,选出最符合题目要求的一项。
1.我国科学家通过机械化学方法,在氢化镧(LaH )晶格中制造大量的缺陷和纳米微晶,研发出首个
1.95~3
室温环境下超快氢负离子(H−)导体。下列说法不正确的是
...
A.电负性:La > H B.氢属于s区元素
C.H−具有还原性 D.超快氢负离子导体有望用于新型电池研发
2.下列化学用语或图示表达正确的是
A.丙烯的结构简式为C H
3 6
B.SO 的空间结构示意图为
2
C.基态Si原子的价层电子的轨道表示式为
D.HF分子中σ键的形成示意图为
H F H F HF
3.我国研究人员开发出的铝/镁/铝层压板,质量轻、耐腐蚀。下说法不正确的是
...
A.原子半径:Mg > Al B.第一电离能:Mg < Al
C.碱性:Mg(OH) > Al(OH) D.氧化性:Mg2+ < Al3+
2 3
4.下列事实能用平衡移动原理解释的是
A.用热的纯碱溶液更易去除油脂 B.保存FeSO 溶液时,加入适量铁粉
4
C.船底镶嵌锌块,以防船体被腐蚀 D.工业合成氨(放热反应),选择高温
5.下列方程式与所给事实不相符的是
...
A.切开金属钠,切面迅速变暗:4Na + O === 2Na O
2 2
B.用饱和碳酸钠溶液将水垢中的CaSO 转化为CaCO :Ca2++ CO2- === CaCO ↓
4 3 3 3
C.Cl 制备84消毒液(主要成分是NaClO):Cl + 2OH- === Cl- + ClO- + H O
2 2 2
D.向苯酚钠溶液中通少量CO,溶液变浑浊: + H O + CO + HCO-
2 2 2 3
6.实验室制备下列气体所选试剂、制备装置及收集方法均正确的是
第1页/共11页气体 试剂 制备装置 收集方法
A NH NH Cl a e
3 4
B Cl 2 MnO 2 + 浓盐酸 c d
C SO 2 Cu + 浓硫酸 b d
D NO 2 Cu + 浓硝酸 b f
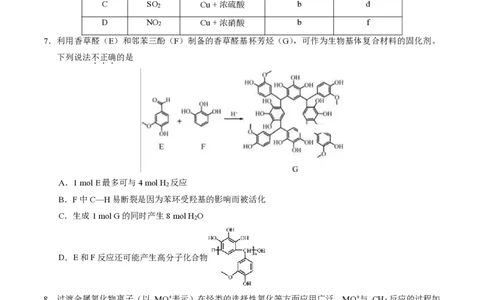
7.利用香草醛(E)和邻苯三酚(F)制备的香草醛基杯芳烃(G),可作为生物基体复合材料的固化剂。
下列说法不正确的是
...
A.1 mol E最多可与4 mol H 反应
2
B.F中C—H易断裂是因为苯环受羟基的影响而被活化
C.生成1 mol G的同时产生8 mol H O
2
D.E和F反应还可能产生高分子化合物
8.过渡金属氧化物离子(以 MO+表示)在烃类的选择性氧化等方面应用广泛。MO+与 CH 反应的过程如
4
下图所示。
第2页/共11页下列说法不正确的是
...
A.反应速率:步骤Ⅰ< 步骤Ⅱ
B.CH OH分子中,键角:H—C—H > H—O—C
3
C.若MO+与CH D反应,生成的氘代甲醇有2种
3
D.CH (g) + MO+(g) === CH OH(g) + M+(g) △H = E +E -E -E
4 3 2 4 1 3
9.用电解法从含MnSO 废水中提取Mn和H SO 的原理如下图所示,阴极室中会加入适量(NH ) SO 。
4 2 4 4 2 4
已知:i.电解时,适当减慢反应速率,有利于得到致密的金属锰。
ii.电解效率(B)=
𝑛(生成B所用的电子)
100 %
𝑛(通过电极的电子)
下列说法不正确的是
...
A.阳极反应式为2H O – 4e- === O ↑ + 4H+
2 2
B.离子交换膜为阴离子交换膜
C.阴极室产生的NH 可与Mn2+形成配合物,
3
c(Mn2+)降低,利于形成致密的金属锰
D.若(Mn)= 80 %,当析出1 mol Mn时,产生O 的体积为8.96 L(标准状况)
2
10. 我国科学家合成了一种咪唑基聚离子液体(PIL/AcO),该离子液体可用于制备离子导体。PIL/AcO 的合
成路线如下:
已知:高分子链之间形成氢键可显著提高材料的力学性能。
下列说法不正确的是
...
A.L和M不是同系物
B. 生成PIL/AcO时,参加反应的K和N的物质的量之比为x∶y
C.该反应的副产物不可能是网状结构的高分子
D. x与y的和一定时,改变x与y的比值可调控离子导体的力学性能
11. 恒温条件下,用图1所示装置研究铁的电化学腐蚀,测定结果如图2。
图1 图2
下列说法不正确的是
...
A.AB段主要发生析氢腐蚀
第3页/共11页B.AD段负极反应式为Fe- 2e- === Fe2+
C.BC段正极反应式主要为O + 4e- + 2H O === 4OH-
2 2
D.DE段溶液pH基本不变,可能的原因:相同时间内,2Fe + O + 4H+ === 2Fe2+ + 2H O消耗H+的量
2 2
与4Fe2+ + O + 10H O === 4Fe(OH) + 8H+产生H+的量基本相同
2 2 3
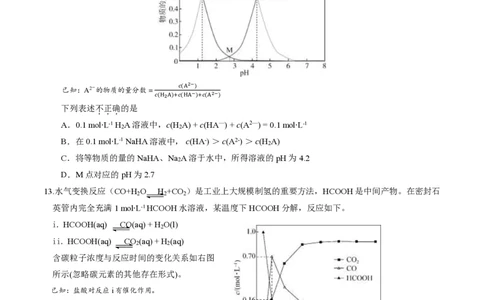
12.常温下,Na A溶液中H A、HA-、A2-的物质的量分数与pH的关系如下图。
2 2
已知:A2-的物质的量分数 =
𝑐(A2−)
𝑐(H2A)+𝑐(HA−)+𝑐(A2−)
下列表述不正确的是
...
A.0.1 mol·L-1 H A溶液中,c(H A) + c(HA—) + c(A2—) = 0.1 mol·L-1
2 2
B.在 0.1 mol·L-1 NaHA溶液中, c(HA-) > c(A2-) > c(H A)
2
C.将等物质的量的NaHA、Na A溶于水中,所得溶液的pH为4.2
2
D.M点对应的pH为2.7
13.水气变换反应(CO+H O H +CO )是工业上大规模制氢的重要方法,HCOOH是中间产物。在密封石
2 2 2
英管内完全充满1 mol·L-1 HCOOH水溶液,某温度下HCOOH分解,反应如下。
i. HCOOH(aq) CO(aq) + H O(l)
2
ii. HCOOH(aq) CO (aq)+ H (aq)
2 2
含碳粒子浓度与反应时间的变化关系如右图
所示(忽略碳元素的其他存在形式)。
已知:盐酸对反应i有催化作用。
下列说法不正确的是
...
A.反应开始至t ,反应速率:i > ii
1
B.t 时,HCOOH的分解率为86%
1
C.相同条件下,若起始时溶液中同时还含有0.1 mol·L-1 盐酸,c(CO)的最大值将变大
D.相同条件下,若起始时溶液中同时还含有0.1 mol·L-1 盐酸,c(CO )的最大值将变小
2
14. 某兴趣小组探究高锰酸钾和氨水的反应,实验如下:
序号 试剂 实验现象
第4页/共11页2 mL KMnO 溶液 + 1 mL 10 mol·L-1氨水 + 溶液完全褪色所需时间: ③ < ②
4
①
0.5 mL蒸馏水 < ①。
2 mL KMnO 溶液 + 1 mL 10 mol·L-1氨水 + 实验均产生棕褐色固体(经检验
4
②
0.5 mL 1 mol·L-1稀硫酸 为 MnO 2 ),都伴有少量气泡产生
2 mL KMnO 溶液 + 1 mL 10 mol·L-1氨水 +
(经检验为N
2
)。
4
③
0.5 mL 1 mol·L-1 Na SO 溶液
2 4
2 mL KMnO 溶液 + 1 mL 5 mol·L-1 (NH ) SO 溶 无明显变化
4 4 2 4
④
液 + 0.5 mL蒸馏水
注:实验中c(KMnO4) = 0.01 mol·L-1。
下列说法不正确的是
...
A.实验①中发生了反应2MnO- + 2NH === 2MnO + N ↑ + 2OH- + 2H O
4 3 2 2 2
B.溶液完全褪色所需时间② < ①的主要原因:c(H+)增大,MnO- 的氧化性增强
4
C. 对比实验③④可得出,还原性:NH > NH +
3 4
D. 在实验④的试剂中,逐滴加入浓NaOH溶液,可观察到溶液褪色
第二部分
本部分共5题,共58分。
15.(10分)寻找安全高效、低成本的储氢材料对于实现氢能经济具有重要意义,以下列举了三种常见的储
氢材料。
Ⅰ.氰基配合物Cu [Co(CN) ] ·xH O
3 6 2 2
(1)基态Cu原子的价层电子排布式为 。
(2)H O能参与配位的原因是 。
2
(3)CN-中C为正价,从原子结构的角度说明理由 。
Ⅱ.三维多孔金属有机骨架材料MOFs
MOF-5 的低温储氢性能非常优异,其晶体结构如下图所示。对苯二甲酸(BDC)作为有机配体,与无
机基团[Zn O]6+连接,化学式为 Zn O(BDC) 。
4 4 3
(4)[Zn O]6+中O原子的杂化轨道类型为 。
4
(5)下列也可以作为有机配体与[Zn O]6+连接形成三维多孔骨架的是 。
4
第5页/共11页Ⅲ. 金属氢化物
Mg FeH 是非常有潜力的储氢材料。其晶胞形状为立方体,边长为a nm,如下图所示。
2 6
(6)Mg FeH 晶胞中H原子个数为 。
2 6
(7)已知Mg FeH 的摩尔质量是M
2 6
第6页/共11页
g m o l - 1 ,阿伏加德罗
常数为N ,该晶体的密度为
A
g c m - 3 。
(1 nm = 1 0 - 7 cm)
16.(11分)AOPs(高级氧化技术)通过产生·OH(羟基自由基)能有效去除废水中有机污染物。
I. 芬顿反应是AOPs中使用最广泛的方法,主要反应过程如下:
i. Fe2+ + H O + H+ === Fe3+ + ·OH + H O (快反应)
2 2 2
ii. ·OH + OM → CO
2
+ H
2
O(快反应,OM为有机物)
iii. 2Fe3+ + H O === 2Fe2+ + O + 2H+(慢反应)
2 2 2
反应过程中存在副反应:·OH + Fe2+ + H+ === Fe3+ + H O。
2
(1)决定芬顿反应速率的是过程 (填“i”“ii”或“iii”)。
(2)·OH氧化苯酚的化学方程式为 。
II. 用铁粉代替Fe2+,并加入硼(B),可加快Fe3+转化为Fe2+,提高有机污染物的去除率。
(3)① B与Fe3+反应生成硼酸(H BO )的离子方程式为______
3 3
② 相同时间内,铁粉投加量与有机污染物去除率的关系如下图所示(k越大,去除效果越好)。
铁粉质量浓度大于0.02 g∙L−1时,有机污染物去除率下降的原因可能是 。
III. 相比于传统的芬顿反应,电芬顿反应具有无需投加H O 等优点。该方法是利用O 在电极放电生成
2 2 2
H O ,与加入的Fe2+构成芬顿体系,如图1所示。
2 2
(4)石墨做 极。
(5)溶液pH对H O 生成量的影响如图2所示。
2 2图1 图2
① pH=3,电解时间在0 ~ 60 min内,v(H O ) = mol·L-1·min-1.
2 2
② 电解相同时间,随着溶液 pH 升高,生成的 H O 浓度逐渐减小,结合电极反应式分析原
2 2
因 。
17.(11分)冶炼金属产生的酸泥属于有价值危险物。从某酸泥(含 Se单质,HgSe及锌、铜的化合物等)
中回收汞和硒的一种工艺如下:
(1)“氧化浸出”时,酸泥中硒、汞、锌、铜分别以H SeO 、Hg2+、Zn2+、Cu2+形式进入溶液。
2 3
①分离氧化浸出液和浸出渣的操作是 。
②不溶于水的HgSe被氧化的离子方程式为 。
③浸出时间等其他条件相同时,不同的NaClO 投加量对汞、
3
硒浸出率的影响如右图所示。选择最佳 NaClO 投加量并说明理
3
由 。
(2)沉汞后液中磷以最高价形式存在。“还原沉汞”的主要反应
中,氧化剂和还原剂的物质的量加之热比 为 。
(3)已知Se(s) + Na SO (aq) Na SeSO (aq),粗硒中的杂质不溶于Na SO 溶液。利用该原理对粗硒进行
2 3 2 3 2 3
冷却
提纯,实验操作是 。
(4)粗硒中硒的纯度测定
i. 取0.1 g 粗硒于锥形瓶中,加入15 mL浓盐酸和1mL浓硝酸,沸水浴加热,使Se全部转化为H SeO ;
2 3
ii.除去过量的HNO 和溶解的NO ;
3 2
iii.加入 2 mL KI溶液、5 mL淀粉溶液,然后用 c mol·L-1 Na S O 标准溶液进行滴定,到达滴定终点
2 2 3
时,消耗Na S O 标准溶液V mL。
2 2 3
已知:H2SeO3 + 4KI + 4HCl ==== Se + 2I2 + 4KCl + 3H2O
H2SeO3 + 4Na2S2O3 + 4HCl ==== Se + 2Na2S4O6 + 4NaCl + 3H2O
I2 + 2Na2S2O3 ==== Na2S4O6 + 2NaI
①到达滴定终点时的现象为 。
第7页/共11页②依据现有数据能否计算出粗硒中硒的纯度?若能,请写出计算式;若不能,请写出还需要的数据。
18.(13分)L是合成某雌酮药物的中间体,其合成路线如下。
(1)A的核磁共振氢谱有两组峰。A的结构简式是 。
(2)检验B中官能团的试剂是 。
(3)D→E的化学方程式是 。
(4)2E + a 一 定 条 F件 + 2C H OH,试剂a的结构简式是 。
2 5
(5)已知: ,I的结构简式为 。
(6)G + J → K的反应类型是 。
(7)由G经过多步反应合成P后可制备双环内酰胺的衍生物X。
写出Q 、W的结构简式 、 。
已知:
第8页/共11页19.(13分)某研究小组探究Fe3+盐溶液与Cu的反应,进行了如下实验。
实验装置 序号 试剂a 实验现象
0.25 mol·L-1 溶液逐渐变为蓝色。2天后,Cu片有
Ⅰ
Fe
2
(SO
4
)
3
溶液 较大量剩余,溶液仍为蓝色。
溶液逐渐变为蓝绿色,铜片表面覆盖
0.5 mol·L-1 有白色固体(经检验为 CuCl)。2 天
Ⅱ
FeCl
3
溶液 后,白色固体消失,Cu 片无剩余,
溶液中产生大量红褐色沉淀。
溶液逐渐变为绿色,实验过程中未见
0.5 mol·L-1
Ⅲ 气泡产生。 2天后,Cu片少量剩余,
Fe(NO ) 溶液
3 3
溶液中产生大量红褐色沉淀。
资料:ⅰ. CuCl、CuSCN是难溶于水的白色固体;
ⅱ. Fe2+ + NO [Fe(NO)]2+ (棕色)。
(1)用化学用语解释Fe3+盐溶液显酸性的原因_________。
(2)实验Ⅰ中发生反应的离子方程式为__________。
(3)小组同学取2 mL实验Ⅰ中反应2天后的溶液于试管中,加入2滴1 mol·L-1 KSCN溶液,观察到溶
液迅速变红,产生大量白色沉淀。
甲同学猜想Fe2+可能在该条件下被Cu2+氧化了。
①用离子方程式表示甲同学的猜想__________。
②甲同学通过实验证实了其猜想,实验方案是__________。
(4)对比实验Ⅰ和实验Ⅱ,小组同学推测Cl-可以催化Fe3+与Cu反应。其理由是_____。
(5)实验Ⅱ中产生大量红褐色沉淀的原因是__________。
(6)实验Ⅲ所得溶液的颜色不是蓝色,小组同学猜测反应中生成了[Fe(NO)]2+,设计并实施了以下实验,
验证了其猜想。
步骤 实验操作 实验现象
2天后溶液颜色无明显变化,铜
① 向盛有2 g金属Cu片的烧杯中加入试剂X
片表面有细小气泡附着
② 继续加入少量FeSO 固体 溶液迅速变为浅棕色
4
试剂X是__________。
(7)综合以上实验,Fe3+盐溶液与Cu反应的多样性与阴离子种类、生成物存在形式等有关。
第9页/共11页参考答案
第一部分共14题,每题3分,共42分。
1 2 3 4 5 6 7
A D B A B B C
8 9 10 11 12 13 14
D D C C C D B
第二部分共5题,共58分。
15.(10分)
(1)3d104s1
(2)H O中的O原子能提供孤电子对
2
(3)C和N电子层数相同,核电荷数 C < N,原子半径C > N,原子核对最外层电子的吸引力 C < N ,
电负性 C < N
(4)sp3 (5)BC (6) 24
(7)
16.(11分)
(1)iii (2)C H OH + 28· OH == 6CO + 17H O
6 5 2 2
(3) ① B + 3Fe3+ + 3H O == H BO + 3Fe2+ + 3H+
2 3 3
② 产生的Fe2+量较多,Fe2+和· OH发生副反应,c(·OH)下降,导致反应ii速率下降
(4)阳
(5)①
② O + 2e− + 2H+ = H O pH升高, c(H+)下降,反应速率下降(或氧气的氧化性减弱)
2 2 2
17.(11分)
(1)①过滤 ②HgSe + ClO - + 2H+ = Hg2+ + Cl- + H SeO
3 2 3
③70 g/L 氯酸钠的投加量>70 g/L时,汞、硒浸出率增加不明显,浪费试剂
(2)4:1
(3)将粗硒溶于热的Na SO 溶液中,趁热过滤,将滤液冷却结晶,过滤、洗涤、干燥
2 3
(4)①溶液由蓝色变为无色,且半分钟内颜色不恢复
②
18. (13分)
(1)HOCH CH OH
2 2
(2)银氨溶液或新制氢氧化铜
浓硫酸
(3)HOOC—COOH + 2C H OH C H OOC—COOC H + 2H O
2 5 2 5 2 5 2
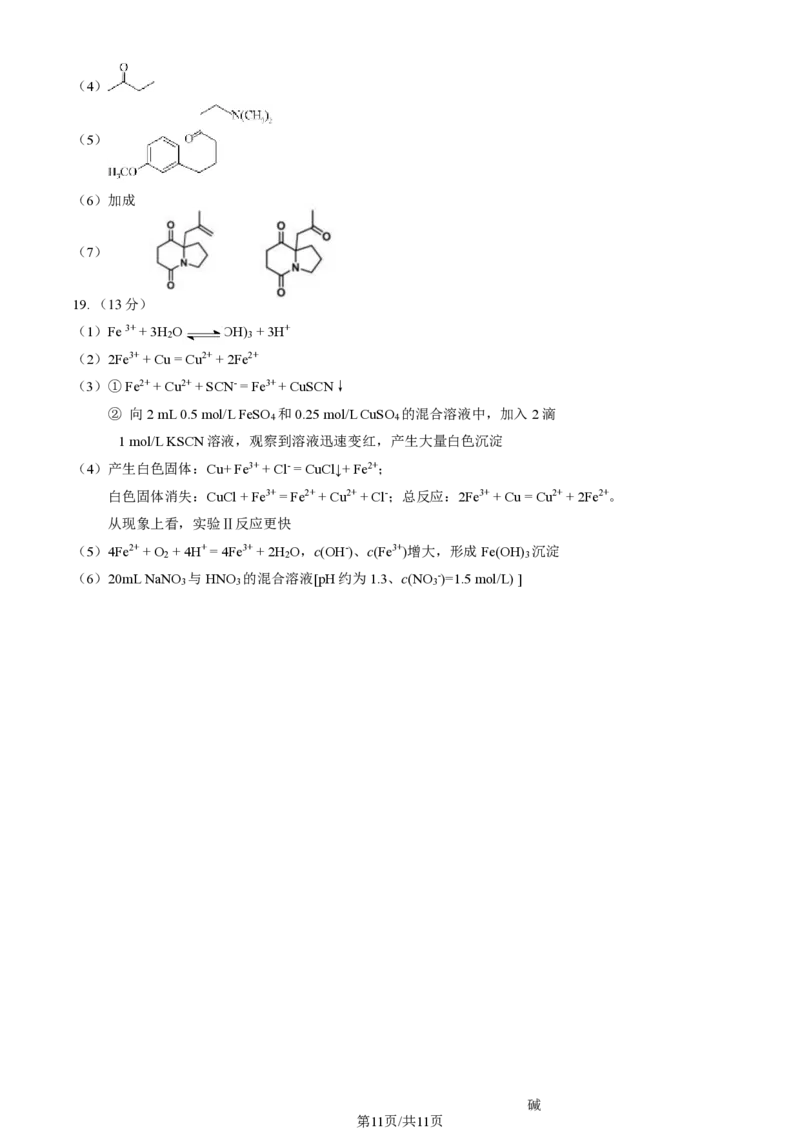
第10页/共11页(4)
(5)
(6)加成
(7)
19. (13分)
(1)Fe 3+ + 3H O Fe(OH) + 3H+
2 3
(2)2Fe3+ + Cu = Cu2+ + 2Fe2+
(3)① Fe2+ + Cu2+ + SCN- = Fe3+ + CuSCN↓
② 向2 mL 0.5 mol/L FeSO 和0.25 mol/L CuSO 的混合溶液中,加入2 滴
4 4
1 mol/L KSCN溶液,观察到溶液迅速变红,产生大量白色沉淀
(4)产生白色固体:Cu+ Fe3+ + Cl- = CuCl↓+ Fe2+;
白色固体消失:CuCl + Fe3+ = Fe2+ + Cu2+ + Cl-;总反应:2Fe3+ + Cu = Cu2+ + 2Fe2+。
从现象上看,实验Ⅱ反应更快
(5)4Fe2+ + O + 4H+ = 4Fe3+ + 2H O,c(OH-)、c(Fe3+)增大,形成Fe(OH) 沉淀
2 2 3
(6)20mL NaNO 与HNO 的混合溶液[pH约为1.3、c(NO -)=1.5 mol/L) ]
3 3 3
碱
第11页/共11页