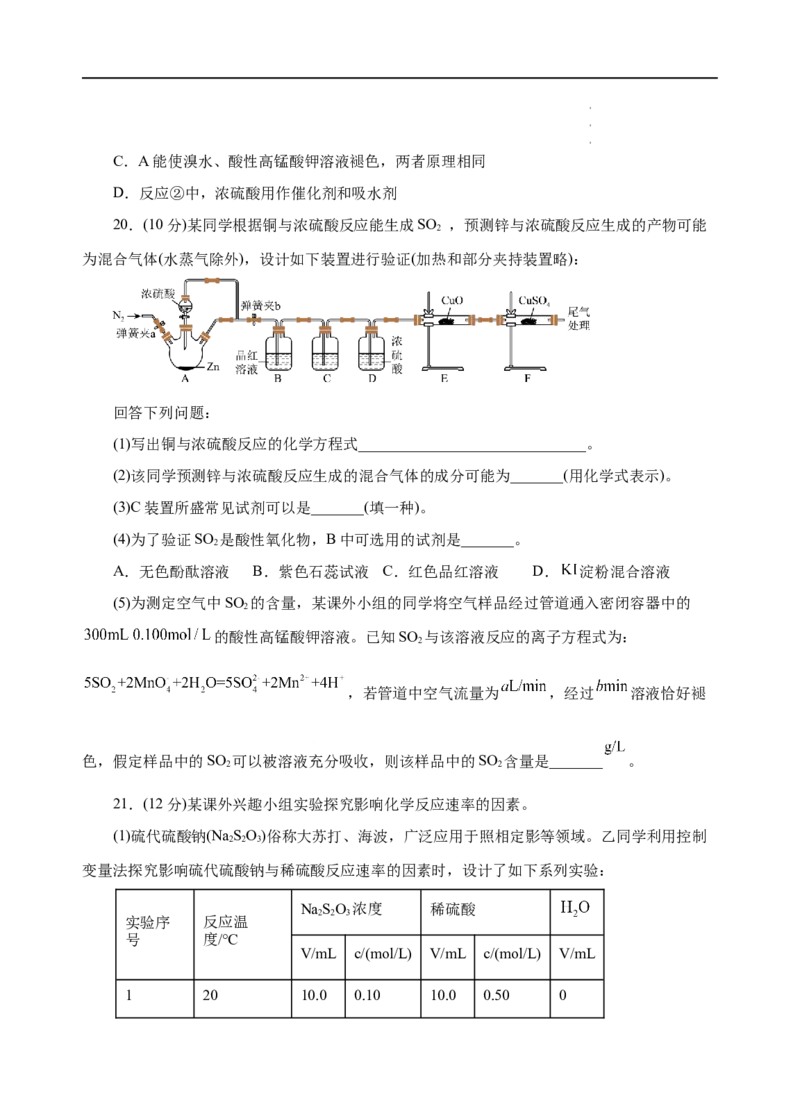文档内容
高一化学高频考题期末测试卷 03
(考试时间:90分钟 试卷满分:100分)
考试内容:新教材人教必修二 难度:★★★★☆
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 Al-27 Si-28 S-32
Cl-35.5 Fe-56 Cu-64
一、选择题(本题共16个小题,每小题3分。在每小题给出的四个选项中,只有一项是符合
题目要求的。)
1.我国在科技上不断取得重大成果。下列各项中使用的材料不属于无机非金属材料的是(
)
“神舟十三
用于吊装港珠澳大桥的 “嫦娥五号”探测器使
应用于5G手机中的石墨 号”载人飞船
超高分子量聚乙烯纤维 用的砷化镓太阳能电池
烯导热膜 使用的石英挠
吊绳 板
性加速度计
A B C D
2.下列物品的俗名、有效成分和用途都正确的是( )
A.漂白粉,有效成分Ca(ClO ),做消毒剂 B.小苏打,NaHCO ,做发酵粉
3 2 3
C.碱石灰,Ca (OH),做干燥剂 D.铝热剂,Al O 和Fe,冶炼金属
2 2 3
3.化学与科技、社会、生活有着密切联系。下列有关说法不正确的是( )
A.港珠澳大桥路面使用了沥青和混凝土,沥青可以通过石油分馏得到
B.As O 是治疗白血病的一线药物,我国首次实现其仿生递送,As O 是碱性氧化物
2 3 2 3
C.北京冬奥会采用光伏发电以减少CO 排放,有利于实现碳达峰
2
D.神舟十三号飞船成功发射,航天员的头盔主要成分是聚碳酸酯,属于有机高分子
学学学科科科网网网(((北北北京京京)股))份股股有份份限有有公限限司公公司司4.下列说法不正确的是( )
A.O、O 同素异形体
2 3
B.35Cl 与37Cl 互为同位素
2 2
C.乙烷和戊烷互为同系物
D.CH-CH-CH-CH 与 互为同分异构体
3 2 2 3
5.下列表示乙烯的表示方法不正确的是( )
A.电子式: B.球棍模型:
C.结构式: D.结构简式:CH=CH
2 2
6.年度热播扶贫剧《山海情》中有部分农民用硫磺熏制枸杞,遭到有正义感村民的反对,
下列说法错误的是( )
A.硫磺熏制枸杞是利用了SO 的漂白性
2
B.二氧化硫是强致癌物,不可用于食品添加剂
C.某些中药材利用硫磺熏制也起到了一定的杀菌消毒作用
D.硫磺熏制过的枸杞可能呈现鲜红色,而未熏制过的枸杞可能呈现暗红色
7.近期我国多地开始施行限电令,减少工业用电。为了改善人类的生存环境与社会可持续
发展,节能和寻找清洁的新能源成为人类的必然选择。下列选项不符合这一理念的是( )
A.贯彻落实国家政策,尽可能节约用电
B.改进锅炉的炉型和燃料空气比、清理积灰
学学学科科科网网网(((北北北京京京)股))份股股有份份限有有公限限司公公司司C.禁止使用燃油车,大力发展新能源汽车
D.为减少化石燃料的使用,积极进行技术创新
8.近年来,我国在探索太空、开发5G等方面都取得了举世瞩目的成就,这些成就都离不
开化学材料的开发和利用,下列有关说法正确的是( )
A.小米全自动扫拖一体机“T7PrO”搭载骁龙八核芯片的主要成分是二氧化硅
B.我国新一代运载火箭长征八号使用的碳化硅陶瓷是传统无机非金属材料
C.5G技术的应用离不开光缆,我国光缆线路总长度超过了三千万千米,光缆的主要成分
是晶体硅
D.碳纳米管有相当高的强度和优良的电学性能,可用于生产复合材料、电池和传感器等
9.已知2SO +O 2SO 为放热反应,对该反应的下列说法正确的是( )
2 2 3
A.O 的能量一定高于SO 的能量
2 3
B.SO 和O 的总能量一定高于SO 的总能量
2 2 3
C.SO 的能量一定高于SO 的能量
2 3
D.因该反应为放热反应,故不必加热就可发生
10.新冠病毒是一种具有包膜的RNA病毒,包膜的主要成分是蛋白质和脂质。核酸检测就
是检测新冠病毒的RNA。下列说法不正确的是( )
A.核酸和蛋白质都是生物大分子
B.核酸和蛋白质都不能发生水解反应
C.核酸中核苷酸之间通过磷酯键连接
D.一定浓度的含氯消毒液可使新冠病毒中的蛋白质变性
11.构建和谐社会的内容之一是人类与环境的和谐发展,而“绿色化学”的内容是指从技
术经济上设计可行的化学反应,尽可能减少对环境的副作用,下列化学反应不符合“绿色化
学”理念的是( )
A.消除硫酸厂尾气中的SO :SO +2NH+H O=(NH )SO
2 2 3 2 4 2 3
B.消除硝酸工业尾气的氮氧化物的污染:NO+NO +2NaOH=2NaNO +H O
2 2 2
C.制CuSO :Cu+2H SO (浓) CuSO +SO↑+2H O
4 2 4 4 2 2
D.制CuSO :2Cu+O +2H SO 2CuSO +2H O
4 2 2 4 4 2
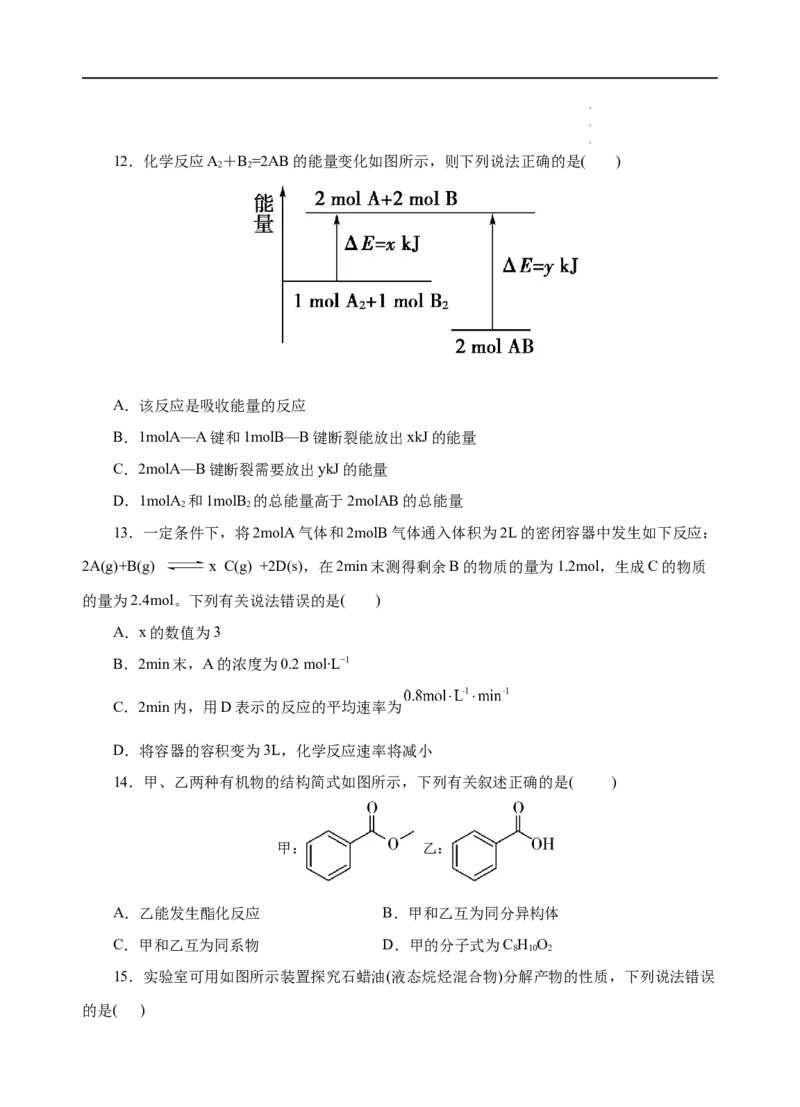
学学学科科科网网网(((北北北京京京)股))份股股有份份限有有公限限司公公司司12.化学反应A+B =2AB的能量变化如图所示,则下列说法正确的是( )
2 2
A.该反应是吸收能量的反应
B.1molA—A键和1molB—B键断裂能放出xkJ的能量
C.2molA—B键断裂需要放出ykJ的能量
D.1molA 和1molB 的总能量高于2molAB的总能量
2 2
13.一定条件下,将2molA气体和2molB气体通入体积为2L的密闭容器中发生如下反应:
2A(g)+B(g) x C(g) +2D(s),在2min末测得剩余B的物质的量为1.2mol,生成C的物质
的量为2.4mol。下列有关说法错误的是( )
A.x的数值为3
B.2min末,A的浓度为0.2 mol∙L−1
C.2min内,用D表示的反应的平均速率为
D.将容器的容积变为3L,化学反应速率将减小
14.甲、乙两种有机物的结构简式如图所示,下列有关叙述正确的是( )
甲: 乙:
A.乙能发生酯化反应 B.甲和乙互为同分异构体
C.甲和乙互为同系物 D.甲的分子式为C H O
8 10 2
15.实验室可用如图所示装置探究石蜡油(液态烷烃混合物)分解产物的性质,下列说法错误
的是( )
学学学科科科网网网(((北北北京京京)股))份股股有份份限有有公限限司公公司司A.仪器①可控制石蜡油的滴加速率
B.装置②起防倒吸的作用
C.实验过程中,关闭 、打开 ,装置②中溶液颜色逐渐褪去证明有烯烃等生成
D.加热一段时间后,关闭 、打开 ,在③处点燃气体可看到淡蓝色火焰
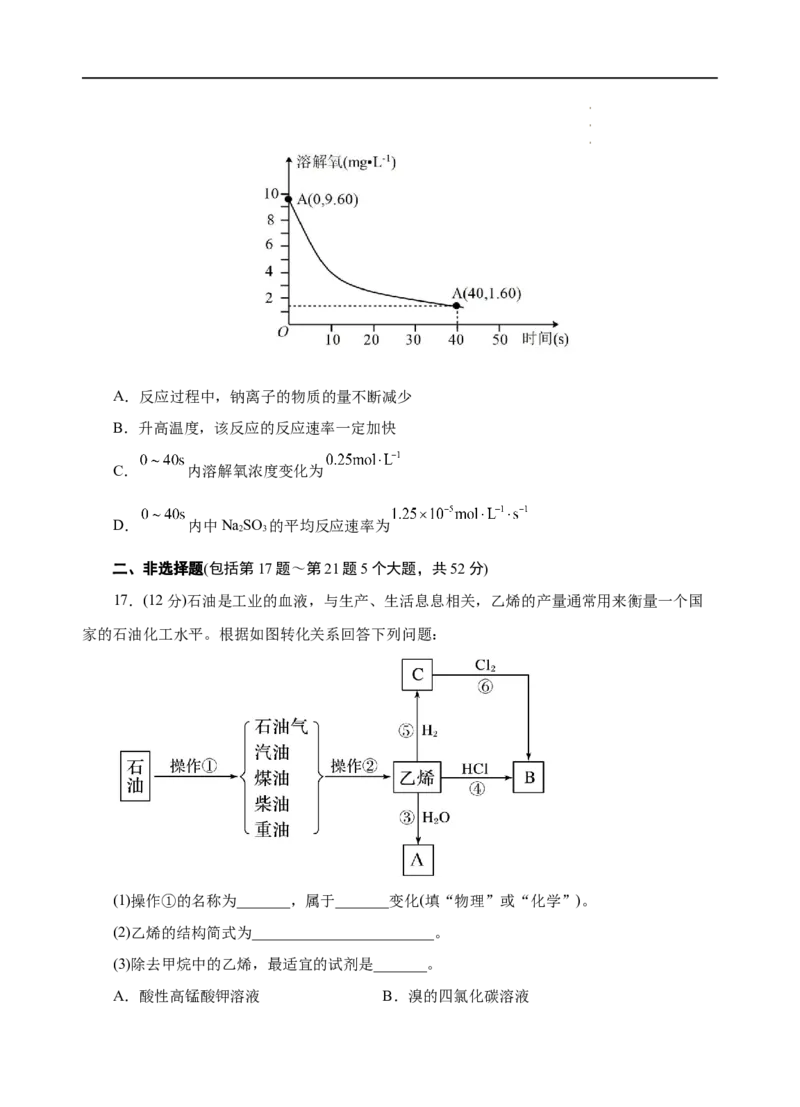
16.已知反应:2 Na SO +O =2 Na SO 。在 时, 溶液中NaSO 初始量为
2 3 2 2 4 2 3
,每 记录一次溶解氧浓度,一段时间后实验结果如下图所示。则下
列说法正确的是( )
学学学科科科网网网(((北北北京京京)股))份股股有份份限有有公限限司公公司司A.反应过程中,钠离子的物质的量不断减少
B.升高温度,该反应的反应速率一定加快
C. 内溶解氧浓度变化为
D. 内中NaSO 的平均反应速率为
2 3
二、非选择题(包括第17题~第21题5个大题,共52分)
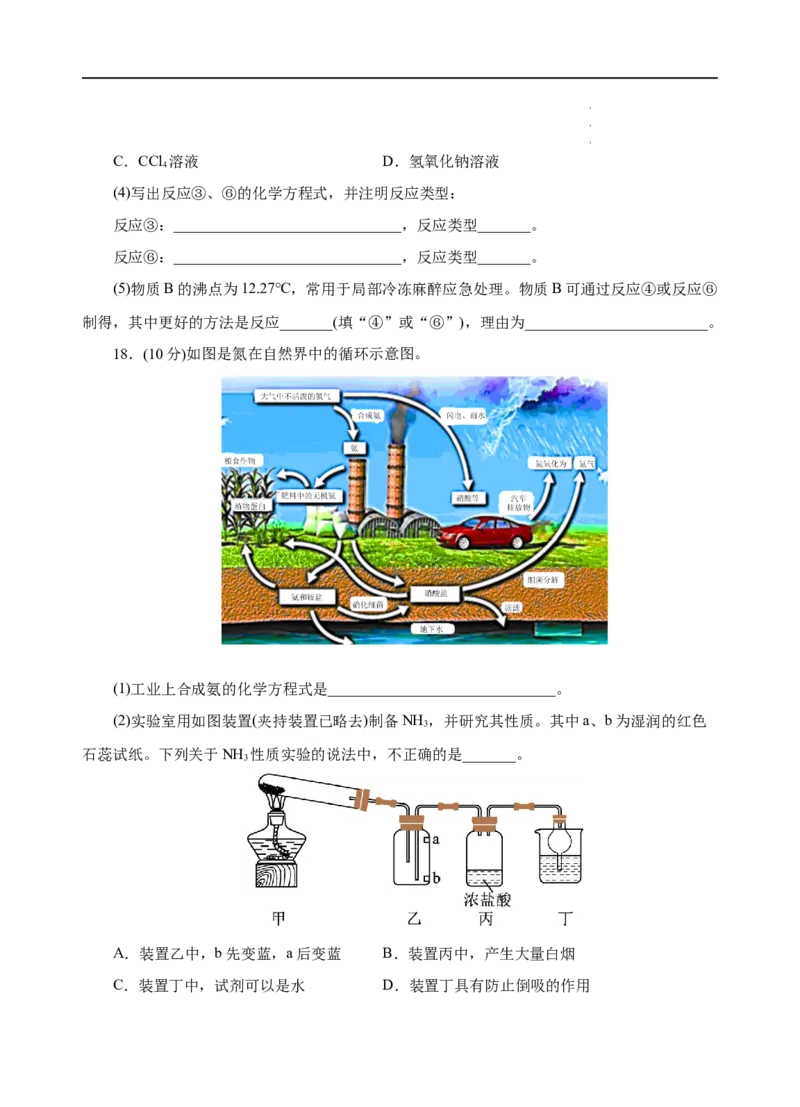
17.(12分)石油是工业的血液,与生产、生活息息相关,乙烯的产量通常用来衡量一个国
家的石油化工水平。根据如图转化关系回答下列问题:
(1)操作①的名称为_______,属于_______变化(填“物理”或“化学”)。
(2)乙烯的结构简式为________________________。
(3)除去甲烷中的乙烯,最适宜的试剂是_______。
A.酸性高锰酸钾溶液 B.溴的四氯化碳溶液
学学学科科科网网网(((北北北京京京)股))份股股有份份限有有公限限司公公司司C.CCl 溶液 D.氢氧化钠溶液
4
(4)写出反应③、⑥的化学方程式,并注明反应类型:
反应③:______________________________,反应类型_______。
反应⑥:______________________________,反应类型_______。
(5)物质B的沸点为12.27℃,常用于局部冷冻麻醉应急处理。物质B可通过反应④或反应⑥
制得,其中更好的方法是反应_______(填“④”或“⑥”),理由为________________________。
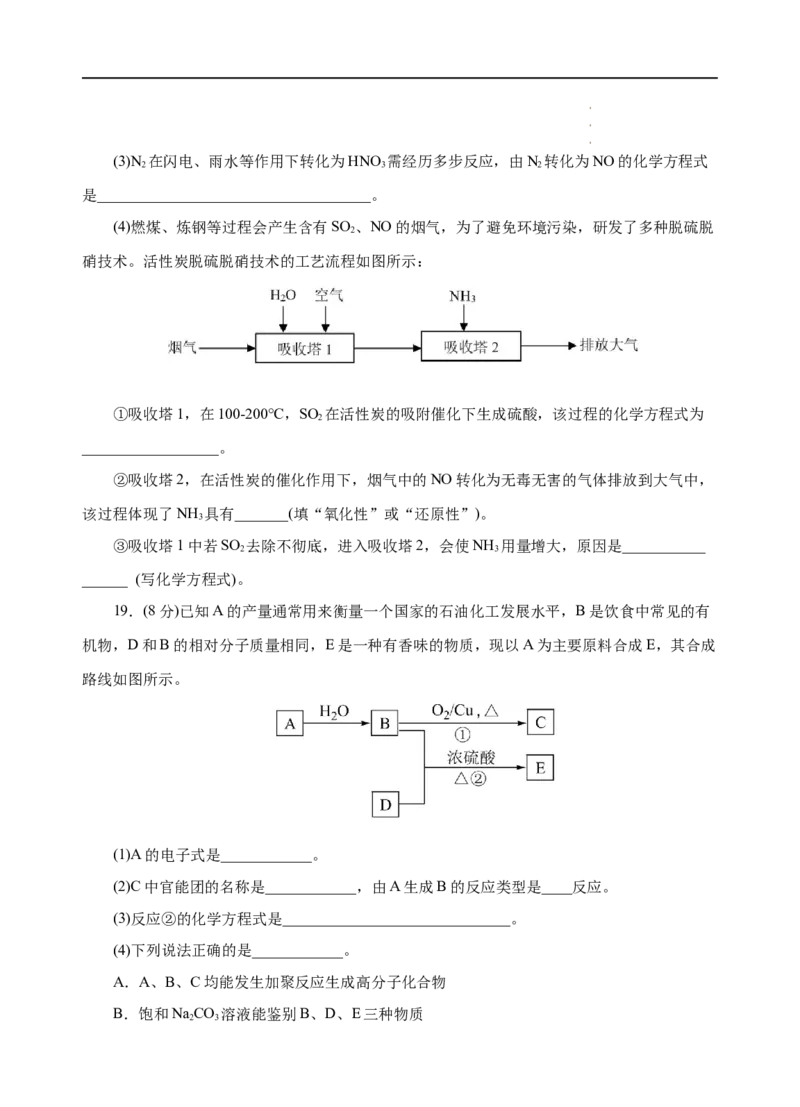
18.(10分)如图是氮在自然界中的循环示意图。
(1)工业上合成氨的化学方程式是______________________________。
(2)实验室用如图装置(夹持装置已略去)制备NH ,并研究其性质。其中a、b为湿润的红色
3
石蕊试纸。下列关于NH 性质实验的说法中,不正确的是_______。
3
A.装置乙中,b先变蓝,a后变蓝 B.装置丙中,产生大量白烟
C.装置丁中,试剂可以是水 D.装置丁具有防止倒吸的作用
学学学科科科网网网(((北北北京京京)股))份股股有份份限有有公限限司公公司司(3)N 在闪电、雨水等作用下转化为HNO 需经历多步反应,由N 转化为NO的化学方程式
2 3 2
是____________________________________。
(4)燃煤、炼钢等过程会产生含有SO 、NO的烟气,为了避免环境污染,研发了多种脱硫脱
2
硝技术。活性炭脱硫脱硝技术的工艺流程如图所示:
①吸收塔1,在100-200℃,SO 在活性炭的吸附催化下生成硫酸,该过程的化学方程式为
2
__________________。
②吸收塔2,在活性炭的催化作用下,烟气中的NO转化为无毒无害的气体排放到大气中,
该过程体现了NH 具有_______(填“氧化性”或“还原性”)。
3
③吸收塔1中若SO 去除不彻底,进入吸收塔2,会使NH 用量增大,原因是___________
2 3
______ (写化学方程式)。
19.(8分)已知A的产量通常用来衡量一个国家的石油化工发展水平,B是饮食中常见的有
机物,D和B的相对分子质量相同,E是一种有香味的物质,现以A为主要原料合成E,其合成
路线如图所示。
(1)A的电子式是____________。
(2)C中官能团的名称是____________,由A生成B的反应类型是____反应。
(3)反应②的化学方程式是______________________________。
(4)下列说法正确的是____________。
A.A、B、C均能发生加聚反应生成高分子化合物
B.饱和NaCO 溶液能鉴别B、D、E三种物质
2 3
学学学科科科网网网(((北北北京京京)股))份股股有份份限有有公限限司公公司司C.A能使溴水、酸性高锰酸钾溶液褪色,两者原理相同
D.反应②中,浓硫酸用作催化剂和吸水剂
20.(10分)某同学根据铜与浓硫酸反应能生成SO ,预测锌与浓硫酸反应生成的产物可能
2
为混合气体(水蒸气除外),设计如下装置进行验证(加热和部分夹持装置略):
回答下列问题:
(1)写出铜与浓硫酸反应的化学方程式______________________________。
(2)该同学预测锌与浓硫酸反应生成的混合气体的成分可能为_______(用化学式表示)。
(3)C装置所盛常见试剂可以是_______(填一种)。
(4)为了验证SO 是酸性氧化物,B中可选用的试剂是_______。
2
A.无色酚酞溶液 B.紫色石蕊试液 C.红色品红溶液 D. 淀粉混合溶液
(5)为测定空气中SO 的含量,某课外小组的同学将空气样品经过管道通入密闭容器中的
2
的酸性高锰酸钾溶液。已知SO 与该溶液反应的离子方程式为:
2
,若管道中空气流量为 ,经过 溶液恰好褪
色,假定样品中的SO 可以被溶液充分吸收,则该样品中的SO 含量是_______ 。
2 2
21.(12分)某课外兴趣小组实验探究影响化学反应速率的因素。
(1)硫代硫酸钠(NaSO)俗称大苏打、海波,广泛应用于照相定影等领域。乙同学利用控制
2 2 3
变量法探究影响硫代硫酸钠与稀硫酸反应速率的因素时,设计了如下系列实验:
NaSO 浓度 稀硫酸
2 2 3
实验序 反应温
号 度/℃
V/mL c/(mol/L) V/mL c/(mol/L) V/mL
1 20 10.0 0.10 10.0 0.50 0
学学学科科科网网网(((北北北京京京)股))份股股有份份限有有公限限司公公司司2 40 V 0.10 V 0.50 V
1 2 3
3 20 V 0.10 4.0 0.50 V
4 5
①从类别的角度分析,硫代硫酸钠(NaSO)属于_______(填标号)。
2 2 3
A.盐 B.碱 C.酸 D.氧化物
②写出硫代硫酸钠与硫酸反应的化学方程式______________________________。
③该实验1和2可探究____________对反应速率的影响,因此V 是_______。实验1和3可
1
探究硫酸浓度对反应速率的影响,因此V=_______。
5
(2)为更精确地研究浓度对反应速率的影响,小组同学利用压强传感器等数字化实验设备,
探究镁与不同浓度硫酸的反应速率,两组实验所用药品如下:
硫酸
序
镁条的质量/g
号
物质的量浓度(mol/L) 体积/mL
Ⅰ 0.01 1.0 2
Ⅱ 0.01 0.5 2
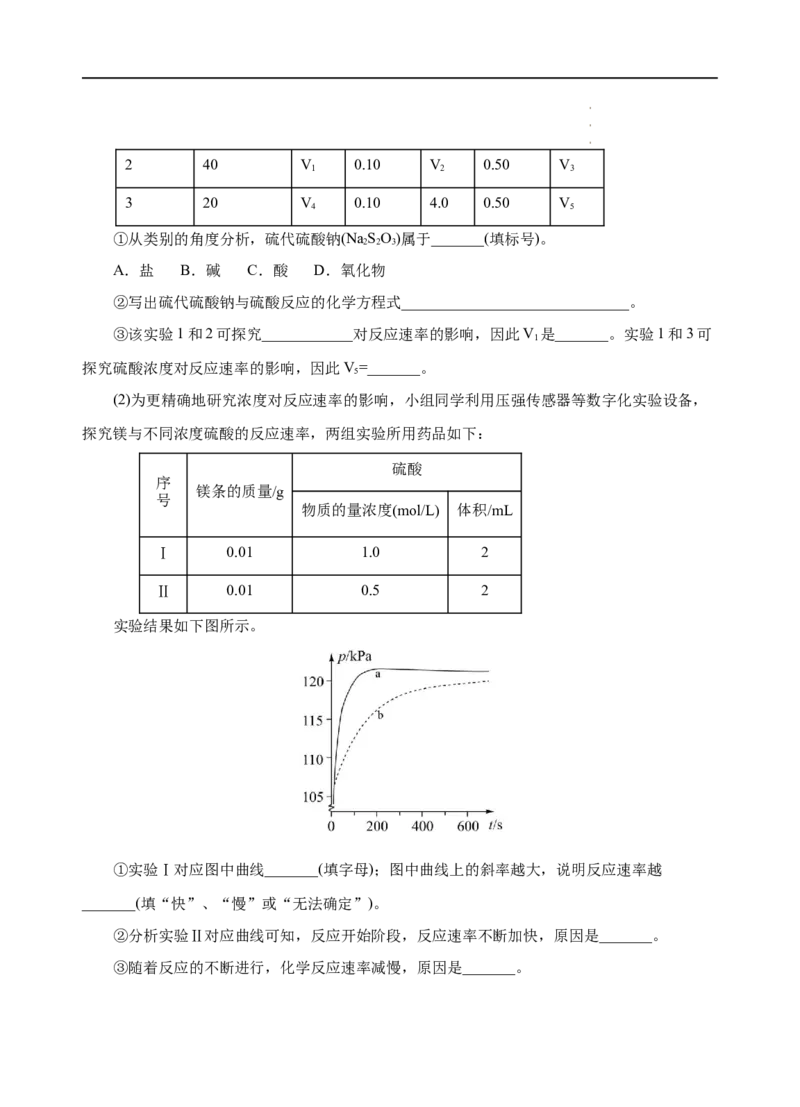
实验结果如下图所示。
①实验Ⅰ对应图中曲线_______(填字母);图中曲线上的斜率越大,说明反应速率越
_______(填“快”、“慢”或“无法确定”)。
②分析实验Ⅱ对应曲线可知,反应开始阶段,反应速率不断加快,原因是_______。
③随着反应的不断进行,化学反应速率减慢,原因是_______。
学学学科科科网网网(((北北北京京京)股))份股股有份份限有有公限限司公公司司学学学科科科网网网(((北北北京京京)股))份股股有份份限有有公限限司公公司司