文档内容
第三单元 金属材料
第一节 铁及其化合物(一)
一、基础巩固
1.下列物质混合后,能产生蓝色沉淀的是( )
A.FeCl 溶液与NaOH溶液
3
B.FeSO 溶液与K [Fe(CN) ]溶液
4 3 6
C.AgNO 溶液与氨水
3
D.鸡蛋清与浓硝酸
2.某固体混合物X,含有Cu、Fe O 、K SO 、K SiO 、K SO 、KAlO 中的几种。进行如下实验:①X
2 3 2 4 2 3 2 3 2
与盐酸作用,产生白色沉淀Y和蓝色强酸性溶液Z;②溶液Z中加入BaCl 溶液,产生白色沉淀M.下列
2
说法正确的是( )
A.白色沉淀Y能分别溶于HF溶液和氨水
B.往溶液Z中加入过量氨水,产生白色沉淀,说明X中一定含有KAlO
2
C.X中一定含有Cu、Fe O 、K SiO ,可能含有K SO
2 3 2 3 2 4
D.沉淀M含有BaSO 、BaSO 中的至少一种
4 3
3. 某同学采用硫铁矿焙烧取硫后的烧渣(主要成分为 Fe O 、SiO 、Al O ,不考虑其他杂质)制取七水合
2 3 2 2 3
硫酸亚铁(FeSO •7H O),设计了如图流程:下列说法不正确的是( )
4 2
A.溶液1中的阳离子可与NH +、HCO ﹣、I﹣、SO 2﹣在同一溶液中大量共存
4 3 4
B.向溶液2中加入3﹣5滴K [Fe(CN) ](铁氰化钾)溶液,可观察到有蓝色沉淀生成
3 6
C.向固体2中加入足量NaOH溶液,发生反应的离子方程式:Al(OH) +OH﹣=AlO ﹣+2H O
3 2 2
D.从溶液2得到FeSO •7H O产品的过程中,须控制条件防止其氧化和分解
4 2
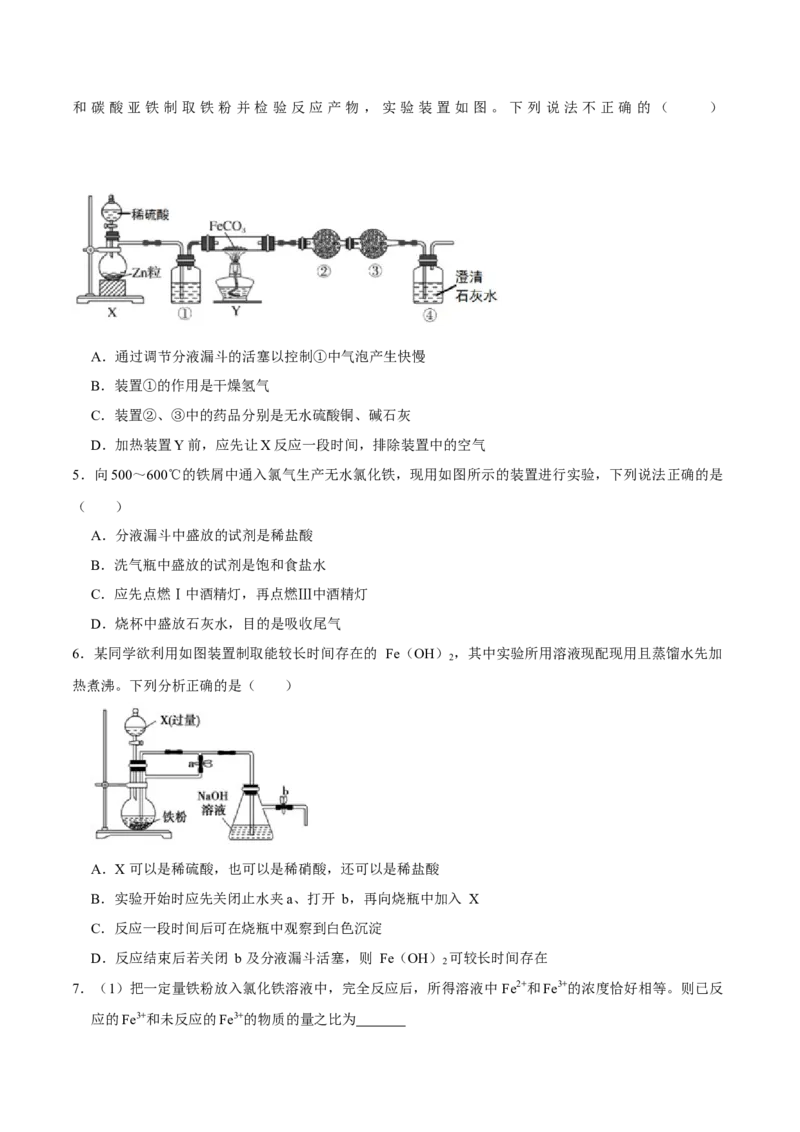
4.铁粉具有平肝镇心,消痈解毒之功效,主治惊痫、癫狂、脚气冲心、贫血等。某兴趣小组探究用氢气和 碳 酸 亚 铁 制 取 铁 粉 并 检 验 反 应 产 物 , 实 验 装 置 如 图 。 下 列 说 法 不 正 确 的 ( )
A.通过调节分液漏斗的活塞以控制①中气泡产生快慢
B.装置①的作用是干燥氢气
C.装置②、③中的药品分别是无水硫酸铜、碱石灰
D.加热装置Y前,应先让X反应一段时间,排除装置中的空气
5.向500~600℃的铁屑中通入氯气生产无水氯化铁,现用如图所示的装置进行实验,下列说法正确的是
( )
A.分液漏斗中盛放的试剂是稀盐酸
B.洗气瓶中盛放的试剂是饱和食盐水
C.应先点燃Ⅰ中酒精灯,再点燃Ⅲ中酒精灯
D.烧杯中盛放石灰水,目的是吸收尾气
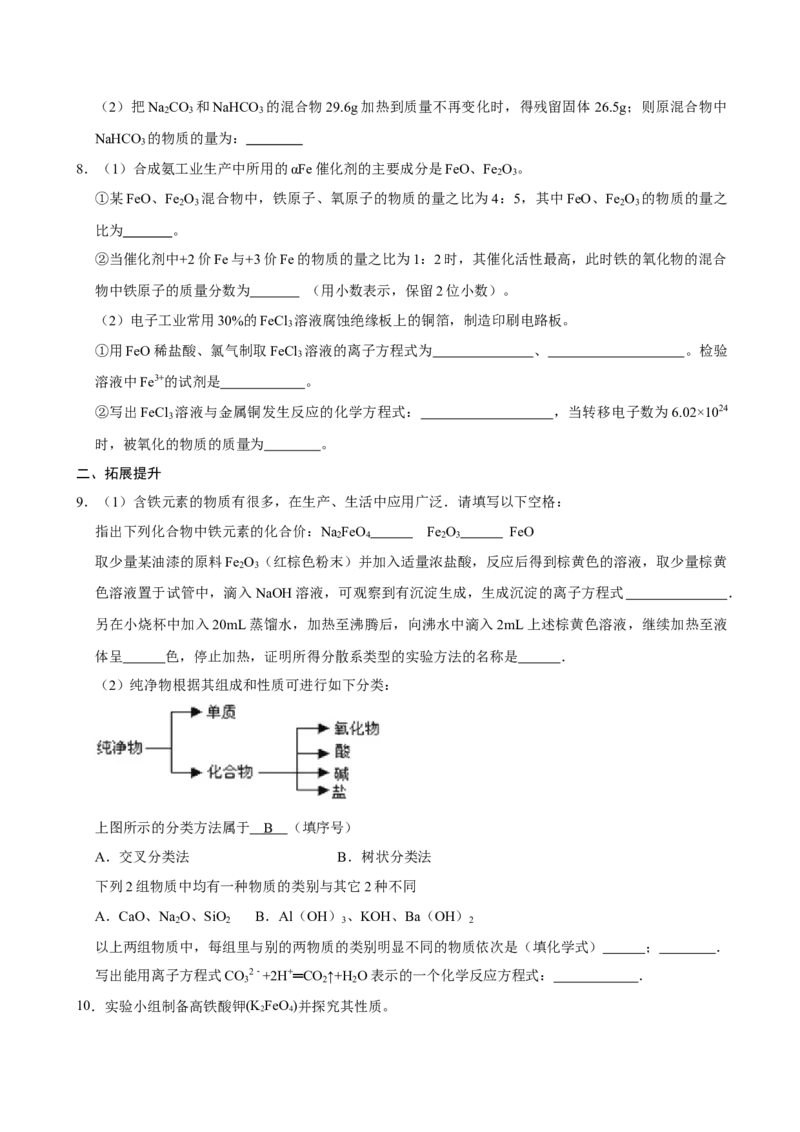
6.某同学欲利用如图装置制取能较长时间存在的 Fe(OH) ,其中实验所用溶液现配现用且蒸馏水先加
2
热煮沸。下列分析正确的是( )
A.X 可以是稀硫酸,也可以是稀硝酸,还可以是稀盐酸
B.实验开始时应先关闭止水夹a、打开 b,再向烧瓶中加入 X
C.反应一段时间后可在烧瓶中观察到白色沉淀
D.反应结束后若关闭 b 及分液漏斗活塞,则 Fe(OH) 可较长时间存在
2
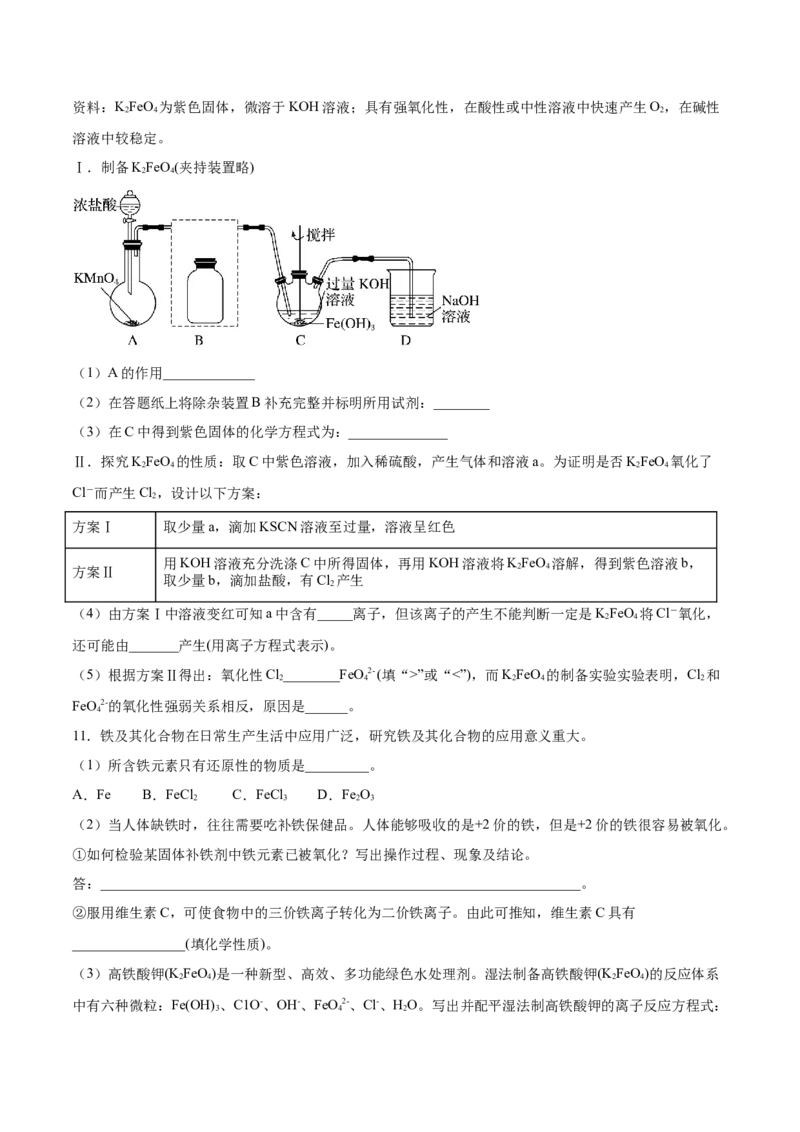
7.(1)把一定量铁粉放入氯化铁溶液中,完全反应后,所得溶液中 Fe2+和Fe3+的浓度恰好相等。则已反
应的Fe3+和未反应的Fe3+的物质的量之比为(2)把Na CO 和NaHCO 的混合物29.6g加热到质量不再变化时,得残留固体26.5g;则原混合物中
2 3 3
NaHCO 的物质的量为:
3
8.(1)合成氨工业生产中所用的αFe催化剂的主要成分是FeO、Fe O 。
2 3
①某FeO、Fe O 混合物中,铁原子、氧原子的物质的量之比为4:5,其中FeO、Fe O 的物质的量之
2 3 2 3
比为 。
②当催化剂中+2价Fe与+3价Fe的物质的量之比为1:2时,其催化活性最高,此时铁的氧化物的混合
物中铁原子的质量分数为 (用小数表示,保留2位小数)。
(2)电子工业常用30%的FeCl 溶液腐蚀绝缘板上的铜箔,制造印刷电路板。
3
①用FeO稀盐酸、氯气制取FeCl 溶液的离子方程式为 、 。检验
3
溶液中Fe3+的试剂是 。
②写出FeCl 溶液与金属铜发生反应的化学方程式: ,当转移电子数为6.02×1024
3
时,被氧化的物质的质量为 。
二、拓展提升
9.(1)含铁元素的物质有很多,在生产、生活中应用广泛.请填写以下空格:
指出下列化合物中铁元素的化合价:Na FeO Fe O FeO
2 4 2 3
取少量某油漆的原料Fe O (红棕色粉末)并加入适量浓盐酸,反应后得到棕黄色的溶液,取少量棕黄
2 3
色溶液置于试管中,滴入NaOH溶液,可观察到有沉淀生成,生成沉淀的离子方程式 .
另在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入2mL 上述棕黄色溶液,继续加热至液
体呈 色,停止加热,证明所得分散系类型的实验方法的名称是 .
(2)纯净物根据其组成和性质可进行如下分类:
上图所示的分类方法属于 B (填序号)
A.交叉分类法 B.树状分类法
下列2组物质中均有一种物质的类别与其它2种不同
A.CaO、Na O、SiO B.Al(OH) 、KOH、Ba(OH)
2 2 3 2
以上两组物质中,每组里与别的两物质的类别明显不同的物质依次是(填化学式) ; .
写出能用离子方程式CO 2﹣+2H+═CO ↑+H O表示的一个化学反应方程式: .
3 2 2
10.实验小组制备高铁酸钾(K FeO)并探究其性质。
2 4资料:KFeO 为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O,在碱性
2 4 2
溶液中较稳定。
Ⅰ.制备KFeO(夹持装置略)
2 4
(1)A的作用_____________
(2)在答题纸上将除杂装置B补充完整并标明所用试剂:________
(3)在C中得到紫色固体的化学方程式为:______________
Ⅱ.探究KFeO 的性质:取C中紫色溶液,加入稀硫酸,产生气体和溶液a。为证明是否KFeO 氧化了
2 4 2 4
Cl-而产生Cl,设计以下方案:
2
方案Ⅰ 取少量a,滴加KSCN溶液至过量,溶液呈红色
用KOH溶液充分洗涤C中所得固体,再用KOH溶液将KFeO 溶解,得到紫色溶液b,
方案Ⅱ 2 4
取少量b,滴加盐酸,有Cl 产生
2
(4)由方案Ⅰ中溶液变红可知a中含有_____离子,但该离子的产生不能判断一定是KFeO 将Cl-氧化,
2 4
还可能由_______产生(用离子方程式表示)。
(5)根据方案Ⅱ得出:氧化性Cl________FeO2- (填“>”或“<”),而KFeO 的制备实验实验表明,Cl 和
2 4 2 4 2
FeO2-的氧化性强弱关系相反,原因是______。
4
11.铁及其化合物在日常生产生活中应用广泛,研究铁及其化合物的应用意义重大。
(1)所含铁元素只有还原性的物质是_________。
A.Fe B.FeCl C.FeCl D.Fe O
2 3 2 3
(2)当人体缺铁时,往往需要吃补铁保健品。人体能够吸收的是+2价的铁,但是+2价的铁很容易被氧化。
①如何检验某固体补铁剂中铁元素已被氧化?写出操作过程、现象及结论。
答:____________________________________________________________________。
②服用维生素C,可使食物中的三价铁离子转化为二价铁离子。由此可推知,维生素C具有
________________(填化学性质)。
(3)高铁酸钾(K FeO)是一种新型、高效、多功能绿色水处理剂。湿法制备高铁酸钾(K FeO)的反应体系
2 4 2 4
中有六种微粒:Fe(OH) 、C1O-、OH-、FeO2-、Cl-、HO。写出并配平湿法制高铁酸钾的离子反应方程式:
3 4 2_____Fe(OH) +_____ClO-+_________=_____FeO 2-+_____Cl-+_________
3 4
(4)工业上用氯化铁腐蚀铜箔、制造电路板。某工程师为了从使用过的腐蚀废液中回收铜,并获得氯化
铁晶体,准备采用下列步骤:
回答下列问题:
①试剂a是___________,操作I用到的玻璃仪器有烧杯、玻璃棒和___________。
②滤液X、Z中都有同一种溶质,它们转化为溶液W的离子方程式为___________。
③上述流程中操作III包括________________、________________、过滤、洗涤。