文档内容
必修第一册 第三章 第二节 金属材料 测试题
榆次一中 李金虎
一、选择题(每小题只有一个正确选项,每小题4分,共40分)
1. 下列所用材料不属于合金的是( )
B.不锈钢手术器 D.火箭外壳镁铝合
A.出土文物青铜器 C.青花瓷将军罐
械 金
2. 钢铁是铁和碳的合金的总称,其强度高、价格便宜、应用广泛。在以下关于不锈钢和普通钢的
认识中,你认为正确的是( )
A.它们的组成元素是相同的
B.耐腐蚀的性能不同
C.它们都属于钢,因此物理性质相同
D.构成普通钢和不锈钢的主要元素都是铁,因此它们的化学性质相同
3. 2020年11月10日,中国“奋斗者”号载人潜水器在马里亚纳海沟成功坐底。“奋斗者”号使
用了钛合金材料。有关合金的说法中正确的是( )
A.钛合金是一种新型金属单质
B.在合金中加入稀土金属,对改善合金的性能无太大影响
C.钛合金熔点比成分金属低,但硬度大
D.钛合金的化学性质与钛单质相同
4. 2021年5月15日,“天问一号”探测器成功软着陆于火星。这是中国火星探测史上的历史性
事件。新型铝基碳化硅复合材料被大量应用于火星车的车身。下列关于该复合材料可能的性质
描述不正确的是( )
A.密度小 B.硬度大
1
学科网(北京)股份有限公司C.熔点低 D.抗氧化
5. 下列关于铝单质的叙述中正确的是( )
A.不能用铝制的器皿来盛放酸梅汤或碱水是因为铝会和酸或碱反应
B.铝制品在空气中有很强的抗腐蚀性是因为铝的化学性质很稳定
C.铝和NaOH溶液反应:Al+2OH-===AlO+2H↑
2
D.用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热,熔化后的液态铝会滴落下
来,是因为金属铝的熔点较低
6. 某同学通过系列实验探究Al及其化合物的性质,下列操作正确且能达到目的的是( )
A.将水加入浓硫酸中得到稀硫酸,将铝条置于其中探究Al的活泼性
B.将NaOH溶液缓慢滴入Al (SO ) 溶液中至过量,最终观察到有沉淀生成
2 4 3
C.将Al(OH) 浊液直接倒入已装好滤纸的漏斗中过滤,洗涤并收集沉淀
3
D.将Al(OH) 沉淀转入蒸发皿中,加足量稀硫酸,加热蒸干得无水Al (SO ) 固体
3 2 4 3
7. 下列除去杂质的方法不正确的是( )
A.镁粉中混有少量铝粉:加入过量烧碱溶液充分反应,过滤、洗涤、干燥
B.用过量氨水除去Fe3+溶液中的少量Al3+
C.Al(OH) 中混有少量Mg(OH) :加入足量烧碱溶液,充分反应,过滤,向滤液中通入过量
3 2
CO 后过滤
2
D.MgO中混有少量Al O:加入足量烧碱溶液,充分反应,过滤、洗涤、干燥得到MgO
2 3
8.如图所示的反应均是在高温或引燃条件下进行,选项中的物质表示A和B,不合理的是( )
A.CO、Mg B.MgO、Al
2
C.Fe O、Al D.CuO、H
2 3 2
9. 铝热反应常用于冶炼高熔点金属,某小组探究 Al粉与Fe O 发生反应所得黑色固体的成分,实
3 4
验过程及现象如下:
下列说法不正确的是( )
A.反应①产生的气体是H
2
B.反应②为Al O+2OH-===2AlO+HO
2 3 2
C.反应③的白色沉淀是Al(OH)
3
D.黑色固体中不含Al和Fe O
3 4
10.铝是一种很重要的金属,可以发生一系列反应制备物质,如图所示:
2
学科网(北京)股份有限公司下列说法错误的是( )
A.反应①又称铝热反应,可用于野外焊接铁轨
B.反应②、③都有氢气生成,产生等量的氢气时转移的电子数相等
C.常用反应⑥制备Al(OH) ,方法是向Al (SO ) 溶液中滴加足量的NaOH溶液
3 2 4 3
D.工业上用反应⑦制备铝时,常加入冰晶石以降低氧化铝的熔融温度
二、填空题(本题包括5个小题,共60分)
11.(8分)铝是中学化学学习阶段的唯一一种既能与酸(非氧化性酸)反应又能与强碱溶液反应放
出H 的金属,就铝的这一特殊性质,回答下列问题:
2
(1)等质量的两份铝分别与足量的盐酸、氢氧化钠溶液反应,所得H 的体积之比是________。
2
(2)足量的两份铝分别投入到等体积、等物质的量浓度的盐酸和氢氧化钠溶液中,产生 H 的体
2
积之比是____________。
(3)足量的两份铝分别投入到等体积、一定物质的量浓度的 HCl、NaOH溶液中,二者产生的H
2
相等,则HCl和NaOH的物质的量浓度之比是____________。
(4)甲、乙两烧杯中各盛有100 mL 3 mol·L-1的盐酸和NaOH溶液,向两烧杯中分别加入等质量
的铝粉,反应结束后,测得生成的气体体积比为 V(甲)∶V(乙)=1∶2,则加入铝粉的质量为
_____________(填字母)。
A.5.4 g B.3.6 g C.2.7 g D.1.8 g
12.(14分)A是一种红棕色金属氧化物,B、D是金属单质,J是一种难溶于水的白色化合物,
受热后容易发生分解。
(1)写出下列物质的化学式:
A:_______,E: ______,J:_______,G:_______。
(2)按要求写方程式:
A与B在高温条件下生成C和D的化学方程式:_____________________________;
F在空气中转化为G的化学方程式:_______________________________________;
C转化为I的离子方程式:___________________________________________。
13.(16分)铝、铁、铜及其化合物在日常生活中应用广泛,根据下列事实回答问题。
3
学科网(北京)股份有限公司(1)铝土矿的主要成分是氧化铝,写出铝土矿与硫酸反应的离子方程式 。
(2)铁矿石主要分为赤铁矿和磁铁矿。写出赤铁矿主要成分的化学式_________________。磁铁
矿与铝粉在一定条件下发生铝热反应,写出反应的化学方程式______________________。
(3)用FeCl 固体配置FeCl 溶液时,需加入少量铁屑,其目的是__________________。
2 2
(4)现有一定浓度的FeCl 溶液,检验溶液是否变质的方法是:取少量溶液,向其中加入几滴
2
KSCN溶液,如果溶液__________,证明溶液变质。
(5)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式是________________。
(6)向新制的FeCl 溶液中滴加氢氧化钠溶液,可以观察到的现象__________________。
2
(7)Cu不活泼,通常情况下不与稀硫酸反应,但向Cu和稀硫酸的混合物中通入O 后,溶液很
2
快变蓝色,试写出该反应的离子方程式________________________。
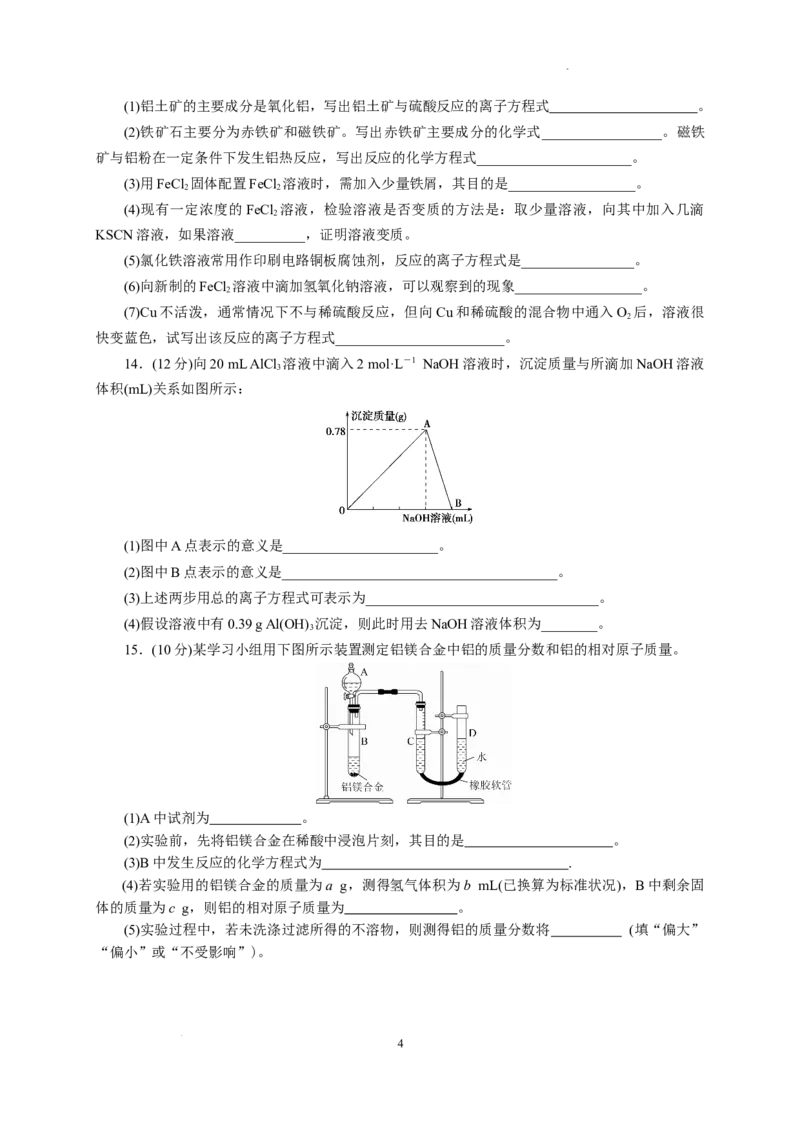
14.(12分)向20 mL AlCl 溶液中滴入2 mol·L-1 NaOH溶液时,沉淀质量与所滴加NaOH溶液
3
体积(mL)关系如图所示:
(1)图中A点表示的意义是______________________。
(2)图中B点表示的意义是_______________________________________。
(3)上述两步用总的离子方程式可表示为_________________________________。
(4)假设溶液中有0.39 g Al(OH) 沉淀,则此时用去NaOH溶液体积为________。
3
15.(10分)某学习小组用下图所示装置测定铝镁合金中铝的质量分数和铝的相对原子质量。
(1)A中试剂为 。
(2)实验前,先将铝镁合金在稀酸中浸泡片刻,其目的是 。
(3)B中发生反应的化学方程式为 .
(4)若实验用的铝镁合金的质量为a g,测得氢气体积为b mL(已换算为标准状况),B中剩余固
体的质量为c g,则铝的相对原子质量为 。
(5)实验过程中,若未洗涤过滤所得的不溶物,则测得铝的质量分数将 (填“偏大”
“偏小”或“不受影响”)。
4
学科网(北京)股份有限公司1.解析:C
2.解析:B 不锈钢是在普通钢的基础上加入Cr、Ni等多种元素炼成的钢材,它具有在常温下、
空气中不易生锈的特点,B项正确。
3.解析:C 合金是指在一种金属中加热熔合其他金属或非金属而形成的具有金属特性的物质
钛合金中含有多种物质,属于混合物,不是新型金属单质,故A错误;在合金中加入稀土金属或稀
土金属的化合物,能大大改善合金的性能,使合金具有更优良的性能,故 B错误;根据合金的性质
可知,合金的熔点比成分金属低,硬度大,故钛合金熔点比成分金属低,但硬度大,故 C正确;合
金的化学性质与其各成分金属的化学性质是相同的,钛合金除具备钛单质的性质外,还具备其他组
成成分的性质,故D错误。
4.解析:C
5.解析:A A项,无论是铝还是其氧化物都能与酸或碱反应,正确;B项,铝制品在空气中
有很强的抗腐蚀性是因为铝表面形成了致密的氧化膜,错误;C项,电荷、原子均不守恒,正确的
离子方程式为2Al+2OH-+2HO===2AlO+3H↑,错误;D项,打磨后的铝箔在酒精灯上灼烧表
2 2
面生成Al O,高熔点的Al O 兜住了熔融的液态铝,不会滴落,错误。
2 3 2 3
6. 解析:D A项,稀释浓硫酸时应将浓硫酸加入水中并不断搅拌;B项,将过量的NaOH溶
液滴入Al (SO ) 溶液中,最终生成NaAlO 溶液,无沉淀。
2 4 3 2
7.解析:B Al(OH) 不溶于氨水,故向含少量Al3+的Fe3+溶液中加入过量氨水时,Fe3+、Al3+
3
均转化为氢氧化物沉淀,达不到除杂的目的。
8.解析:B Mg高温下与CO 反应生成C和MgO,C、Mg与足量氧气引燃分别能生成CO 与
2 2
MgO,故A项正确;Al的还原性比Mg弱,故不能置换出Mg,故B项错误;Al与Fe O 高温下反
2 3
应生成Al O 与Fe,Fe与氧气在高温加热条件下生成Fe O,故C项正确;H 还原CuO生成HO与
2 3 2 3 2 2
Cu,H、Cu与氧气引燃反应分别生成HO和CuO,故D项正确。
2 2
9.解析:D 探究Al粉与Fe O 发生反应所得黑色固体的成分,由实验可知,黑色固体与稀硫
3 4
酸反应生成气体,且溶液b加KSCN溶液不变色,可知溶液b不含铁离子;黑色固体与NaOH溶液
反应无气体,则一定不含Al,溶液a与二氧化碳反应生成白色沉淀为氢氧化铝,则黑色固体中一定
含氧化铝。由上述分析可知,黑色固体一定含氧化铝、Fe,一定不含Al,可能含Fe O 。金属与稀
3 4
硫酸反应生成H ,故A正确;固体含氧化铝,则反应②为Al O +2OH-===2AlO+HO,故B正确;
2 2 3 2
反应③中AlO与二氧化碳反应,可知白色沉淀是Al(OH) ,故C正确;黑色固体中不含Al,可能含
3
Fe O,故D错误。
3 4
10.解析:C 铝热反应指Al与某些金属氧化物间的置换反应,反应①为铝热反应,因反应剧
烈放热,生成熔融的铁水,可用于野外焊接铁轨,选项A正确;Al既能与酸反应放出氢气又能与
碱反应放出氢气,根据元素化合价的变化,产生等量的氢气时转移的电子数相等,选项 B正确;
Al(OH) 具有两性,因此制备时不能使用强酸、强碱,用Al (SO ) 溶液制备Al(OH) 沉淀应选用氨
3 2 4 3 3
水,选项C错误;Al O 熔点高,电解时要耗费更多的能源,加入冰晶石与氧化铝形成共熔物,可
2 3
降低氧化铝的熔融温度,选项D正确。
5
学科网(北京)股份有限公司11.答案 (1)1∶1 (2)1∶3 (3)3∶1 (4)A
解析 (1)根据化学方程式:2Al+6HCl===2AlCl +3H↑、2Al+2NaOH+2HO===2NaAlO +
3 2 2 2
3H↑,得Al与H 的关系式均为2Al~3H,故只要参加反应的Al的量相等,所得H 的量必相等。
2 2 2 2
(2)因为在反应中Al过量,产生的H 由HCl和NaOH的量决定。根据化学反应中的关系式:
2
6HCl~3H、2NaOH~3H,故当HCl、NaOH物质的量相等时,二者产生H 的体积比为1∶3。
2 2 2
(3)因为铝足量且产生H 的量相等,根据关系式n(HCl)∶n(NaOH)=3∶1,又因为两溶液体
2
积相等,故物质的量浓度c(HCl)∶c(NaOH)=n(HCl)∶n(NaOH)=3∶1。
(4)可见当参加反应的HCl和NaOH的物质的量一样多时,产生H 的体积比是1∶3,而题设
2
条件体积比为1∶2,说明此题投入的铝粉对盐酸来说是过量的,而对于NaOH来说是不足的。
2Al + 6HCl === 2AlCl + 3H↑
3 2
6 mol 3 mol
3 mol·L-1×0.1 L 0.15 mol
则Al与NaOH反应生成的H 为0.15 mol×2=0.3 mol。
2
2Al+2NaOH+2HO===2NaAlO+3H↑
2 2 2
2×27 g 3 mol
5.4 g 0.3 mol
即投入的铝粉为5.4 g。
12.【答案】 (1) Fe O FeCl Al(OH) Fe(OH)
2 3 2 3 3
(2) Fe O+2Al=====Al O+2Fe4Fe(OH) +O+2HO===4Fe(OH)
2 3 2 3 2 2 2 3
Al O+2OH-===2AlO+HO
2 3 2
【解析】 由题可知:A为Fe O,F为Fe(OH) ,G为Fe(OH) 。
2 3 2 3
因为Fe O+B――→D+C,则D为Fe,C为Al O,J为Al(OH) 。
2 3 2 3 3
13. 答案:(1)AlO+6H+===3H O+2Al3+
2 3 2
(2)Fe O 3Fe O+8Al===4AlO+9Fe
2 3 3 4 2 3
(3)防止Fe2+转化为Fe3+
(4)变红色
(5)2Fe3++Cu===2Fe2++Cu2+
(6)产生白色沉淀,迅速变为灰绿色,最终变为红褐色
(7)2Cu+O+4H+===2Cu2++2HO
2 2
解析:(1)铝土矿的主要成分是氧化铝,氧化铝与硫酸反应生成硫酸铝和水,硫酸和硫酸铝是强
电解质,并且溶于水,拆成离子的形式,其离子方程式为Al O+6H+===3H O+2Al3+;
2 3 2
(2)铁矿石主要分为赤铁矿和磁铁矿。赤铁矿的主要成分是氧化铁,其化学式为Fe O 。磁铁矿
2 3
与铝粉在一定条件下发生铝热反应,生成氧化铝和铁,反应的化学方程式是 3Fe O +8Al===4AlO
3 4 2 3
+9Fe;
6
学科网(北京)股份有限公司(3)用FeCl 固体配置FeCl 溶液时,亚铁离子具有还原性,在空气中容易被氧化生成铁离子,
2 2
需加入少量铁屑,其目的是防止Fe2+转化为Fe3+;
(4)现有一定浓度的FeCl 溶液,检验溶液是否变质的方法是:取少量溶液,向其中加入几滴
2
KSCN溶液,如果溶液变红色,证明溶液变质;
(5)氯化铁溶液常用作印刷电路铜板腐蚀剂,氯化铁与铜反应生成氯化亚铁和氯化铜,反应的离
子方程式是2Fe3++Cu===2Fe2++Cu2+;
(6)向新制的FeCl 溶液中滴加氢氧化钠溶液,生成氢氧化亚铁沉淀,氢氧化亚铁不稳定,容易
2
被空气中的氧气氧化成氢氧化铁沉淀,可以观察到的现象是产生白色沉淀,迅速变为灰绿色,最终
变为红褐色;
(7)Cu不活泼,通常情况下不与稀硫酸反应,但向Cu和稀硫酸的混合物中通入O 后,溶液很
2
快变蓝色,根据现象可以判断出氧气在酸性环境下把铜单质氧化生成铜离子,该反应的离子方程式
为2Cu+O+4H+===2Cu2++2HO。
2 2
14.答案:(1)滴入NaOH溶液产生沉淀量最大
(2)滴入NaOH溶液沉淀恰好完全溶解
(3)Al3++4OH-===AlO+2HO
2
(4)7.5 mL或17.5 mL
解析: (4)0.39 g Al(OH) 为0.005 mol。
3
若NaOH不足:n(OH-)=3n[Al(OH) ]=0.015 mol V(NaOH)=7.5 mL。
3
若NaOH过量:n(OH-)=4n(Al3+)-n[Al(OH) ]=(0.04-0.005)mol=0.035 mol,V(NaOH)=17.5
3
mL。
15. 答案:(1)氢氧化钠溶液
(2)除去铝镁合金表面的氧化膜
(3) 2Al+2NaOH+2HO===2NaAlO+3H↑。
2 2 2
(4) 。
(5)偏小
解析 (1)铝镁合金中二者都与酸反应,但铝与碱反应而镁不与碱反应,所以 A中的试剂应选
择氢氧化钠溶液。(4)铝的摩尔质量可利用产生的氢气求解,M==(g·mol-1)= (g·mol-1),则铝的
相对原子质量为。(5)如果在实验过程中未洗涤不溶物,则残留物质的质量偏大,铝的质量偏小,则
测得铝的质量分数偏小。
7
学科网(北京)股份有限公司8
学科网(北京)股份有限公司