文档内容
课时作业
A篇·知识对点训练
知识点1 浓硫酸的性质
1.下列关于硫酸的叙述正确的是( )
A.稀硫酸具有强氧化性
B.浓硫酸敞口放置在空气中浓度会变小
C.稀硫酸能使蔗糖脱水
D.SO 溶于水,可得到稀硫酸
2
答案 B
解析 A项,浓硫酸具有强氧化性,错误;B项,浓硫酸可吸收空气中的水
蒸气而使浓度变小,正确;C项,稀硫酸没有脱水性,不能使蔗糖脱水,错误;
D项,SO 溶于水,可得到亚硫酸,错误。
2
2.向盐酸中加入浓硫酸时,会有白雾生成。下列叙述不属于导致产生该现
象的原因的是( )
A.浓硫酸具有脱水性
B.浓硫酸具有吸水性
C.盐酸具有挥发性
D.气态溶质的溶解度随温度升高而降低
答案 A
解析 浓硫酸具有吸水性,且溶于水时放出热量,使盐酸挥发,和浓硫酸的
脱水性无关。
3.下列叙述正确的是( )
A.浓硫酸是一种干燥剂,能够干燥氢气、氧气、氨气等气体,但不能干燥
有较强还原性的HI、H S等气体
2
B.浓硫酸与单质硫反应的方程式为 S+2H SO (浓)=====3SO ↑+2H O,
2 4 2 2
在此反应中,浓硫酸既表现了其强氧化性又表现了其酸性
C.把足量铜粉投入到含2 mol H SO 的浓硫酸中,反应后得到标准状况下气
2 4
体体积为22.4 L
D.常温下能够用铁、铝等容器盛放浓 H SO ,是因为浓H SO 的强氧化性
2 4 2 4使其钝化
答案 D
解析 不能用浓硫酸干燥NH ,A不正确;浓硫酸与S作用时,只表现其强
3
氧化性,B不正确;Cu与浓H SO 反应时,浓H SO 浓度逐渐降低,当成为稀
2 4 2 4
H SO 时,反应停止,参加反应的 H SO 少于2 mol,故C项产生的SO 在标准
2 4 2 4 2
状况下不足22.4 L。
4.下列反应中,浓硫酸既表现强氧化性,又表现酸性的是( )
①2NaCl(固)+H SO (浓)=====Na SO +2HCl↑
2 4 2 4
②C+2H SO (浓)=====CO ↑+2SO ↑+2H O
2 4 2 2 2
③Cu+2H SO (浓)=====CuSO +SO ↑+H O
2 4 4 2 2
④2FeO+4H SO (浓)===Fe (SO ) +SO ↑+4H O
2 4 2 4 3 2 2
A.①② B.③④ C.①③ D.②④
答案 B
解析 金属、金属氧化物(具有变价的金属元素处于低价态)与浓H SO 反应
2 4
时,浓H SO 既表现强氧化性又表现酸性;非金属与浓H SO 反应时,浓H SO
2 4 2 4 2 4
只表现强氧化性。
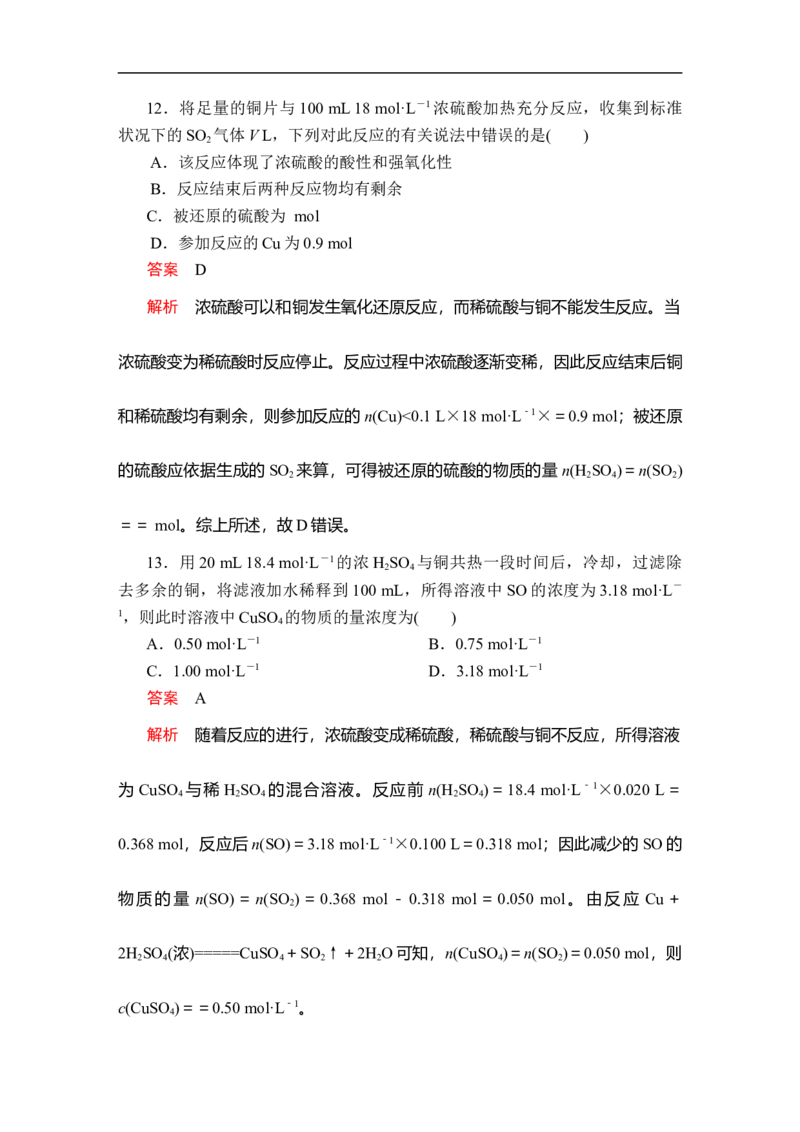
5.用如图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应。
下列实验不合理的是( )A.上下移动①中铜丝可控制SO 的量
2
B.②中选用品红溶液验证SO 的生成
2
C.③中选用NaOH溶液吸收多余的SO
2
D.为确认CuSO 生成,向①中加水,观察颜色
4
答案 D
解析 上下移动铜丝可以使铜丝与浓硫酸接触与分离,从而可以控制反应生
成SO 的量,A正确;SO 可使品红溶液褪色,B正确;SO 有毒,要用 NaOH
2 2 2
溶液吸收处理,C正确;反应液中H SO 的浓度较高,不能向①中加水,应将①
2 4
中溶液沿器壁慢慢加入水中,D错误。
6.(1)浓硫酸与木炭在加热条件下的化学方程式为______________________。
(2)试用下列各装置设计一个实验,验证上述反应所产生的各种产物。这些
装置的连接顺序(按产物气流从左到右的方向)是(填装置的编号):
________→________→________→________。
编号 ① ② ③ ④
装置
(3)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色。A瓶溶液
的作用是________________,B瓶溶液的作用是________________,C瓶溶液的
作用是________________。
(4)装置②中所加的固体药品是________,可确定的产物是________,确定装
置②在整套装置中位置的理由是_________________________。
(5)装置③中所盛溶液是________,可验证的产物是________。
答案 (1)C+2H SO (浓)=====2SO ↑+CO ↑+2H O
2 4 2 2 2
(2)④ ② ① ③
(3)验证产物中有SO 将SO 全部氧化吸收 确定产物中SO 已被B瓶溶液
2 2 2
全部吸收(4)无水CuSO 水蒸气 由于产物气流通过①③时会带出水蒸气,所以②必
4
须设置在①③之前
(5)澄清石灰水 CO
2
解析 木炭与浓硫酸加热反应,生成H O、CO 和SO 。CO 和SO 在化学性
2 2 2 2 2
质上的相同点都是酸性氧化物,都能使澄清石灰水变浑浊,会相互干扰鉴别。
CO 和SO 在化学性质上的明显不同点为SO 有漂白性,CO 则没有;SO 有较强
2 2 2 2 2
的还原性,CO 则没有。在SO 、CO 混合气体中,首先用品红溶液检验 SO 的
2 2 2 2
存在,然后将SO 氧化除去,再用澄清石灰水检验 CO 的存在,是一种确认 SO
2 2 2
和CO 共存的好方案。由于对CO 、SO 的确认都是在溶液中进行的,所以应在
2 2 2
确认CO 和SO 之前先确认H O。与H O发生作用并伴有明显现象的物质,中学
2 2 2 2
生应该熟知的是无水CuSO 。白色的粉末与H O反应生成蓝色的晶体。CuSO 与
4 2 4
CO 和SO 都不发生任何作用。
2 2
知识点2 硫酸盐、SO的检验
7.下列对于某些离子的检验及结论一定正确的是( )
A.加入稀盐酸产生无色气体,原物质一定有CaCO
3
B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO
C.加入稀盐酸后再加入硝酸银,产生白色沉淀,则原溶液一定有Cl-
D.加入碳酸钠溶液产生白色沉淀,再加盐酸,白色沉淀消失,不一定有
Ba2+
答案 D
解析 A项,能与盐酸反应产生气体的有很多物质,如 Na CO 、KHCO 等,
2 3 3
错误;B项,原溶液也可能含Ag+,错误;C项,加入盐酸就引入了Cl-,错误;
D项,也可能含Ca2+,正确。8.有一包白色粉末状混合物,可能含有 Na CO 、NaCl、CaCO 、CuSO 、
2 3 3 4
Na SO 、MgCl 中的某几种,现进行如下实验:
2 4 2
①将混合物溶于水,得到无色透明溶液。
②取少量上述溶液两份,其中一份加入 BaCl 溶液,立即产生白色沉淀,再
2
加入稀硝酸,沉淀不溶解,向另一份中加入NaOH溶液,也产生白色沉淀。
根据上述实验现象回答:
(1)原混合物中肯定没有____________________________________。
(2)原混合物中肯定有______________________________________。
(3)不能确定是否含有______________________________________。
答案 (1)CuSO 、CaCO 、Na CO
4 3 2 3
(2)Na SO 、MgCl
2 4 2
(3)NaCl
解析 根据实验①混合物溶于水得无色溶液,可推断原白色粉末中肯定没有
CuSO 和CaCO (因为CuSO 溶液显蓝色,CaCO 难溶于水)。根据实验②向一份
4 3 4 3
溶液中加入BaCl 溶液,立即产生白色沉淀,再加稀 HNO ,沉淀不溶解,可推
2 3
断原白色粉末中肯定有Na SO ,肯定没有Na CO (因为BaSO 和BaCO 都是白色
2 4 2 3 4 3
沉淀,但BaCO 溶于稀HNO )。根据实验②向另一份溶液中加入NaOH溶液有
3 3
白色沉淀产生,可推断原混合物中含有 MgCl [因为Mg(OH) 是白色沉淀]。对于
2 2
NaCl题目中没有进一步用实验检验,因此不能确定是否含有。
B篇·综合提升训练
9.下列关于浓硫酸和稀硫酸的说法正确的是( )
A.浓硫酸、稀硫酸都难挥发
B.浓硫酸、稀硫酸都能氧化金属锌,反应的化学方程式相同
C.浓硫酸、稀硫酸在加热时都能与铜反应
D.浓硫酸、稀硫酸在常温下都能用铁制容器贮存
答案 A
解析 B项,浓硫酸与锌反应生成二氧化硫,稀硫酸与锌反应生成氢气,错误;C项,稀硫酸与铜在加热条件下不反应,错误;D项,常温下稀硫酸能与铁
反应,所以不能用铁制容器贮存稀硫酸,错误。
10.下列有关浓H SO 的叙述正确的是( )
2 4
A.浓H SO 与铜片共热的反应中,浓 H SO 既表现出强氧化性,又表现出
2 4 2 4
酸性
B.浓 H SO 与金属活动性顺序中氢后面的金属反应生成的气体一般为
2 4
SO ,与氢前面的金属反应生成的气体一般为H
2 2
C.常温下,铁或铝不与浓 H SO 反应,所以可用铁或铝制的容器贮存浓
2 4
H SO
2 4
D.浓H SO 是不挥发性强酸,氢硫酸是挥发性弱酸,所以可用浓 H SO 与
2 4 2 4
FeS反应制取H S气体
2
答案 A
解析 在浓硫酸中存在的是H SO 分子,其分子中+6价的硫易得到电子,
2 4
它把金属氧化的同时本身被还原为硫的低价化合物 SO ,即使是遇到活泼金属如
2
Zn、Fe等也是如此,故B错误。常温下铁或铝不是不与浓 H SO 反应,而是发
2 4
生钝化,故C错误。浓H SO 有强氧化性,H S有强还原性,二者发生氧化还原
2 4 2
反应,得不到H S气体,故D错误。
2
11.一定量的Cu粉与浓H SO 共热产生SO 气体的体积为2.24 L(标准状况
2 4 2
下),则下列情况不可能的是( )
A.加入Cu的质量为6.4 g
B.加入浓H SO 中含溶质为0.2 mol
2 4
C.加入Cu的质量大于6.4 g
D.加入浓H SO 中含溶质多于0.2 mol
2 4
答案 B
解析 随反应进行,浓H SO 会变为稀H SO ,稀H SO 在加热条件下难与
2 4 2 4 2 4
Cu反应产生SO 。
212.将足量的铜片与100 mL 18 mol·L-1浓硫酸加热充分反应,收集到标准
状况下的SO 气体V L,下列对此反应的有关说法中错误的是( )
2
A.该反应体现了浓硫酸的酸性和强氧化性
B.反应结束后两种反应物均有剩余
C.被还原的硫酸为 mol
D.参加反应的Cu为0.9 mol
答案 D
解析 浓硫酸可以和铜发生氧化还原反应,而稀硫酸与铜不能发生反应。当
浓硫酸变为稀硫酸时反应停止。反应过程中浓硫酸逐渐变稀,因此反应结束后铜
和稀硫酸均有剩余,则参加反应的n(Cu)<0.1 L×18 mol·L-1×=0.9 mol;被还原
的硫酸应依据生成的SO 来算,可得被还原的硫酸的物质的量n(H SO )=n(SO )
2 2 4 2
== mol。综上所述,故D错误。
13.用20 mL 18.4 mol·L-1的浓H SO 与铜共热一段时间后,冷却,过滤除
2 4
去多余的铜,将滤液加水稀释到 100 mL,所得溶液中SO的浓度为3.18 mol·L-
1,则此时溶液中CuSO 的物质的量浓度为( )
4
A.0.50 mol·L-1 B.0.75 mol·L-1
C.1.00 mol·L-1 D.3.18 mol·L-1
答案 A
解析 随着反应的进行,浓硫酸变成稀硫酸,稀硫酸与铜不反应,所得溶液
为 CuSO 与稀 H SO 的混合溶液。反应前 n(H SO )=18.4 mol·L-1×0.020 L=
4 2 4 2 4
0.368 mol,反应后n(SO)=3.18 mol·L-1×0.100 L=0.318 mol;因此减少的SO的
物质的量 n(SO)=n(SO )=0.368 mol-0.318 mol=0.050 mol。由反应 Cu+
2
2H SO (浓)=====CuSO +SO ↑+2H O可知,n(CuSO )=n(SO )=0.050 mol,则
2 4 4 2 2 4 2
c(CuSO )==0.50 mol·L-1。
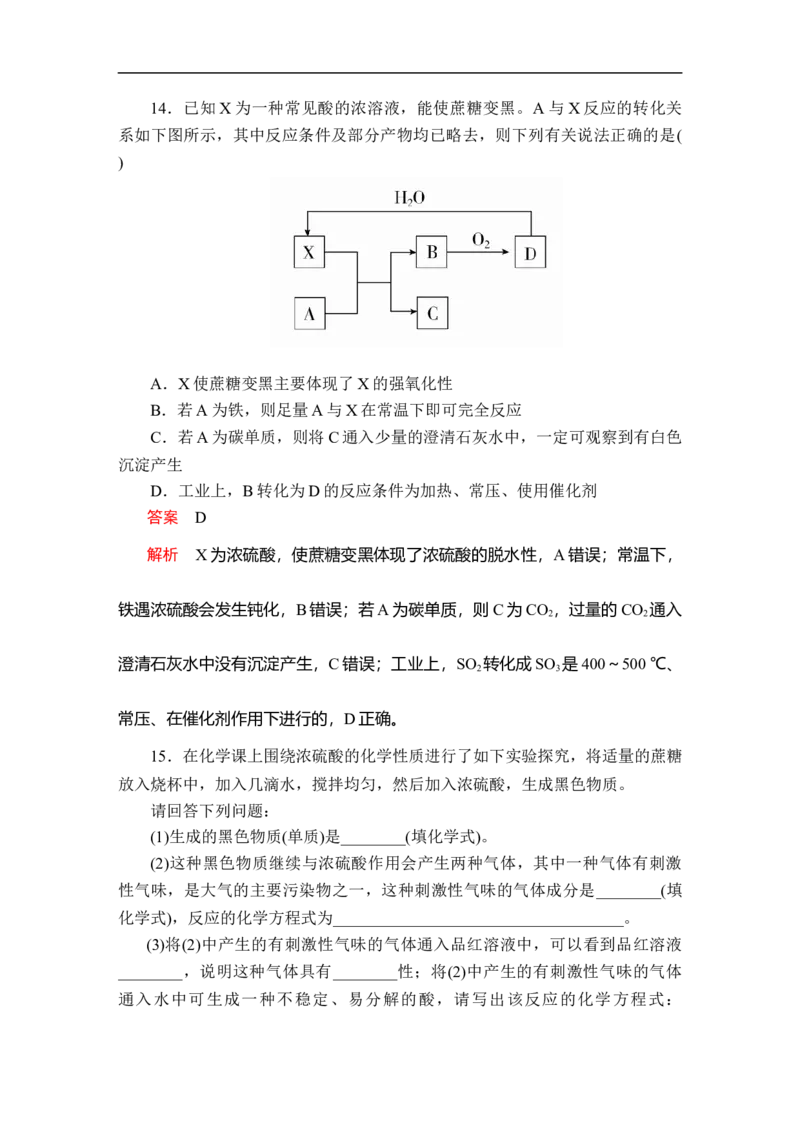
414.已知X为一种常见酸的浓溶液,能使蔗糖变黑。A与X反应的转化关
系如下图所示,其中反应条件及部分产物均已略去,则下列有关说法正确的是(
)
A.X使蔗糖变黑主要体现了X的强氧化性
B.若A为铁,则足量A与X在常温下即可完全反应
C.若A为碳单质,则将C通入少量的澄清石灰水中,一定可观察到有白色
沉淀产生
D.工业上,B转化为D的反应条件为加热、常压、使用催化剂
答案 D
解析 X为浓硫酸,使蔗糖变黑体现了浓硫酸的脱水性,A错误;常温下,
铁遇浓硫酸会发生钝化,B错误;若A为碳单质,则C为CO ,过量的CO 通入
2 2
澄清石灰水中没有沉淀产生,C错误;工业上,SO 转化成SO 是400~500 ℃、
2 3
常压、在催化剂作用下进行的,D正确。
15.在化学课上围绕浓硫酸的化学性质进行了如下实验探究,将适量的蔗糖
放入烧杯中,加入几滴水,搅拌均匀,然后加入浓硫酸,生成黑色物质。
请回答下列问题:
(1)生成的黑色物质(单质)是________(填化学式)。
(2)这种黑色物质继续与浓硫酸作用会产生两种气体,其中一种气体有刺激
性气味,是大气的主要污染物之一,这种刺激性气味的气体成分是________(填
化学式),反应的化学方程式为____________________________________。
(3)将(2)中产生的有刺激性气味的气体通入品红溶液中,可以看到品红溶液
________,说明这种气体具有________性;将(2)中产生的有刺激性气味的气体
通入水中可生成一种不稳定、易分解的酸,请写出该反应的化学方程式:________。
(4)能否用澄清石灰水鉴别这两种气体?________(填“能”或“不能”),若
不能,请填写两种能鉴别的试剂:____________。
答案 (1)C
(2)SO C+2H SO (浓)=====CO ↑+2SO ↑+2H O
2 2 4 2 2 2
(3)褪色 漂白 SO +H OH SO
2 2 2 3
(4)不能 品红溶液、溴水(其他合理答案均可)
解析 (1)浓硫酸具有脱水性,能使蔗糖炭化,所以生成的黑色物质(单质)是
C。
(2)浓硫酸具有强氧化性,能与炭反应生成 CO 、SO 和水,其中SO 气体有
2 2 2
刺激性气味,是大气的主要污染物之一,该反应的化学方程式为 C+
2H SO (浓)=====CO ↑+2SO ↑+2H O。
2 4 2 2 2
(3)SO 具有漂白性,因此将(2)中产生的有刺激性气味的气体通入品红溶液中,
2
可以看到品红溶液褪色;SO 与水反应生成亚硫酸,亚硫酸不稳定,反应的化学
2
方程式为SO +H OH SO 。
2 2 2 3
(4)SO 、CO 均能使澄清石灰水变浑浊,且气体过量后沉淀又溶解,所以不
2 2
能用澄清石灰水鉴别这两种气体;由于 SO 具有漂白性和还原性,所以能鉴别两
2
种气体的试剂可以是品红溶液、溴水等。