文档内容
荆州中学 2024~2025 学年高二上学期九月月考
化学试题
(全卷满分100分 考试用时75分钟)
可能用到的相对原子质量:H-1 C-12 N-14 O-16
一、单选题:本题共15小题,每小题3分,共45分。
1.化学与生活密切相关,下列做法与化学反应速率控制无关的是( )
A.使用含氟牙膏防龋齿 B.洗衣服时使用加酶洗衣粉
C.夏天将牛奶放在冰箱保存 D.在月饼包装内放置抗氧化剂
2.反应 在四种不同情况下的反应速率分别为:
① ;②
③ ;④
该反应进行的快慢顺序为( )
A.①>②=③>④ B.④>③=②>① C.②>①=④>③ D.①>④>②=③
3.下列离子方程式书写正确的是( )
A.酸性 溶液与 溶液反应:
B.少量 气体通入足量NaClO溶液中:
C. 和HI的反应:
D.向 溶液中通入少量 :
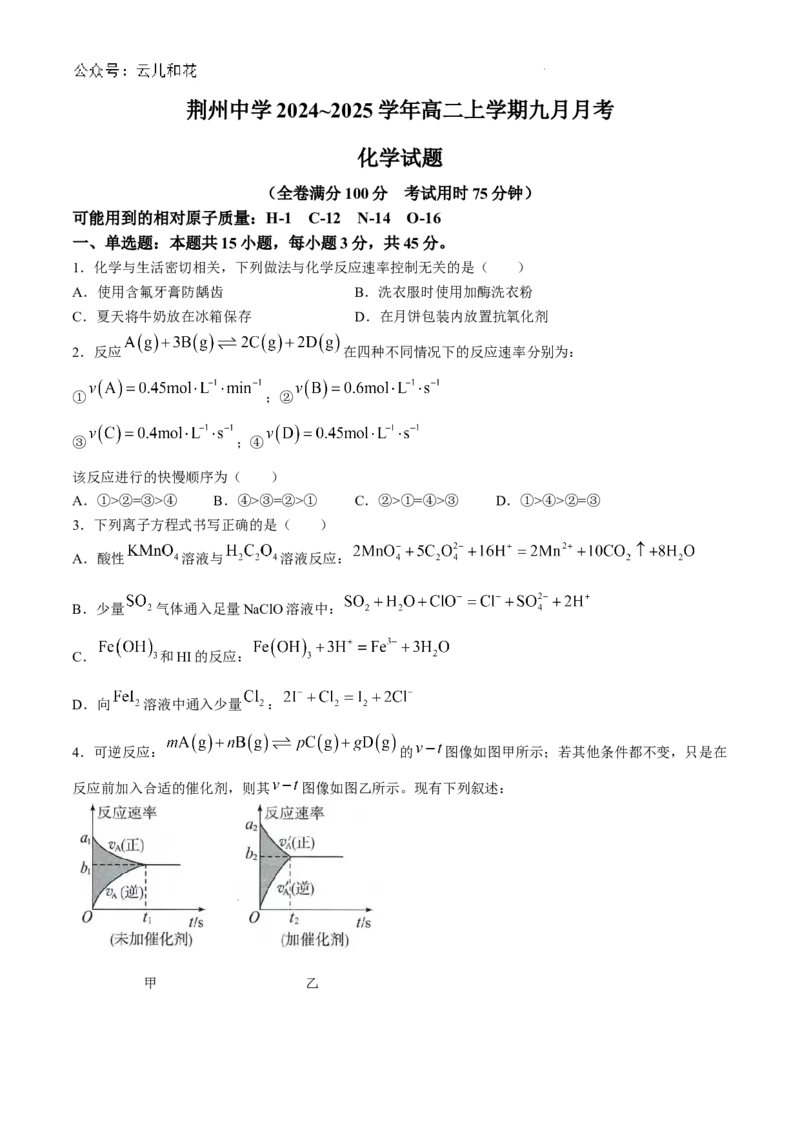
4.可逆反应: 的 图像如图甲所示;若其他条件都不变,只是在
反应前加入合适的催化剂,则其 图像如图乙所示。现有下列叙述:
甲 乙
学科网(北京)股份有限公司① ;② ;③ ;④ ;⑤ ;⑥ ;⑦甲图与乙图中阴影部分的面积相
等;⑧图乙中阴影部分面积更大。则以上所述各项正确的组合为( )
A.②④⑤⑦ B.②④⑥⑧ C.②③⑤⑦ D.②④⑤⑧
5.下列事实不能用勒夏特列原理来解释的是( )
A.实验室中常用排饱和食盐水的方法收集
B.鼓入过量空气有利于 转化为
C. 、 、HI三者的平衡混合气,加压(缩小容器体积)后颜色变深
D.开启啤酒瓶后,压强变小,瓶中立刻泛起大量泡沫
6.下列热化学方程式中说法正确的是( )
A.CO的燃烧热是 ,则:
B.已知 1g 液态肼和足量液态过氧化氢反应生成氮气和水蒸气时放出 20.05kJ 的热量,则
C. ,则含20gNaOH的稀溶液与过量浓硫酸完全
反应,放出的热量为28.7kJ
D. ,在密闭容器中充入 、 ,
充分反应后放出47.2kJ的热量
7.下列实验方案的设计和实验目的都正确的是( )
选项 实验方案 实验目的
向等体积等浓度的 溶液中分别加入5滴等浓度的
A 比较 和 的催化效果
和 溶液,观察气体产生的速度
B ,在平衡体系中加 探究生成物浓度对化学平衡的影响
入KCl晶体
分别向盛有2g锌粒(大小基本相同)的锥形瓶中加入
C 40mL1mol/L和40mL18mol/L的硫酸,比较两者收集10mL 探究硫酸浓度对反应速率影响
气体所用的时间
D 探究温度对化学平衡的影响
将 球分别浸泡在冰水和热水中
A.A B.B C.C D.D
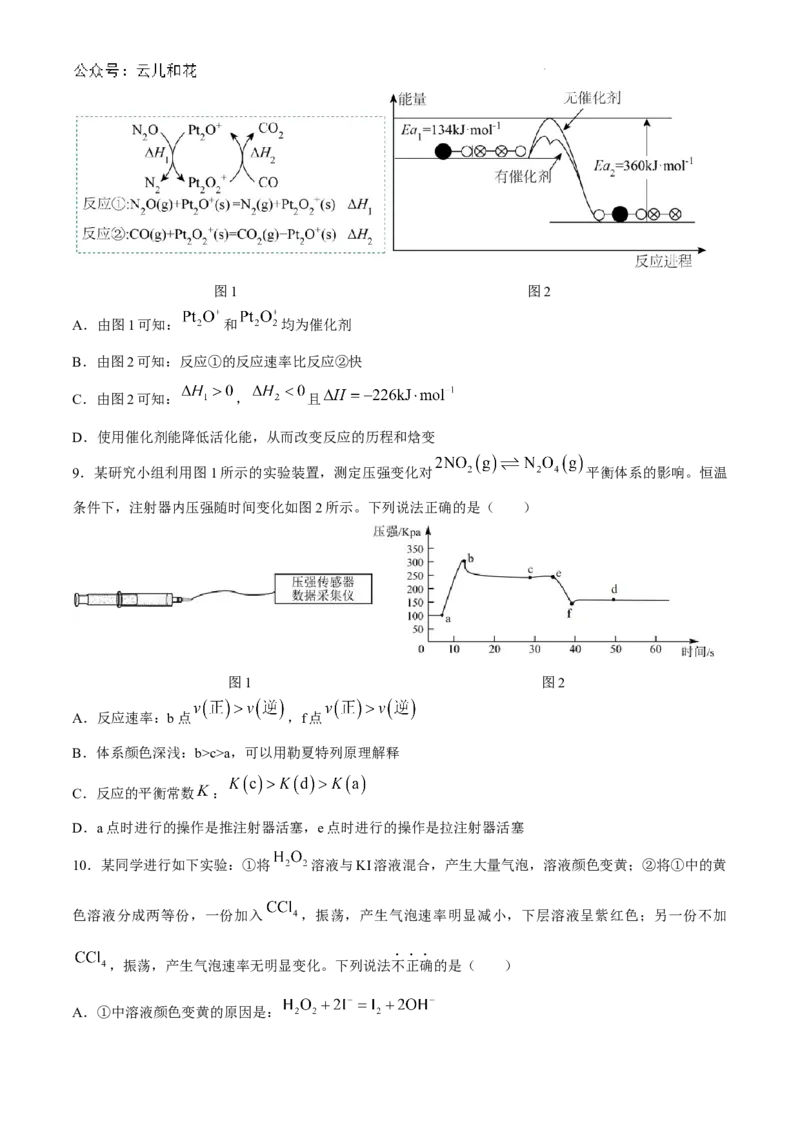
8 . 和 CO 是 环 境 污 染 性 气 体 , 可 在 表 面 转 化 为 无 害 气 体 , 其 反 应 为
,有关化学反应的物质变化过程如图1,能量变化过程如
图2。下列说法正确的是( )
学科网(北京)股份有限公司图1 图2
A.由图1可知: 和 均为催化剂
B.由图2可知:反应①的反应速率比反应②快
C.由图2可知: , 且
D.使用催化剂能降低活化能,从而改变反应的历程和焓变
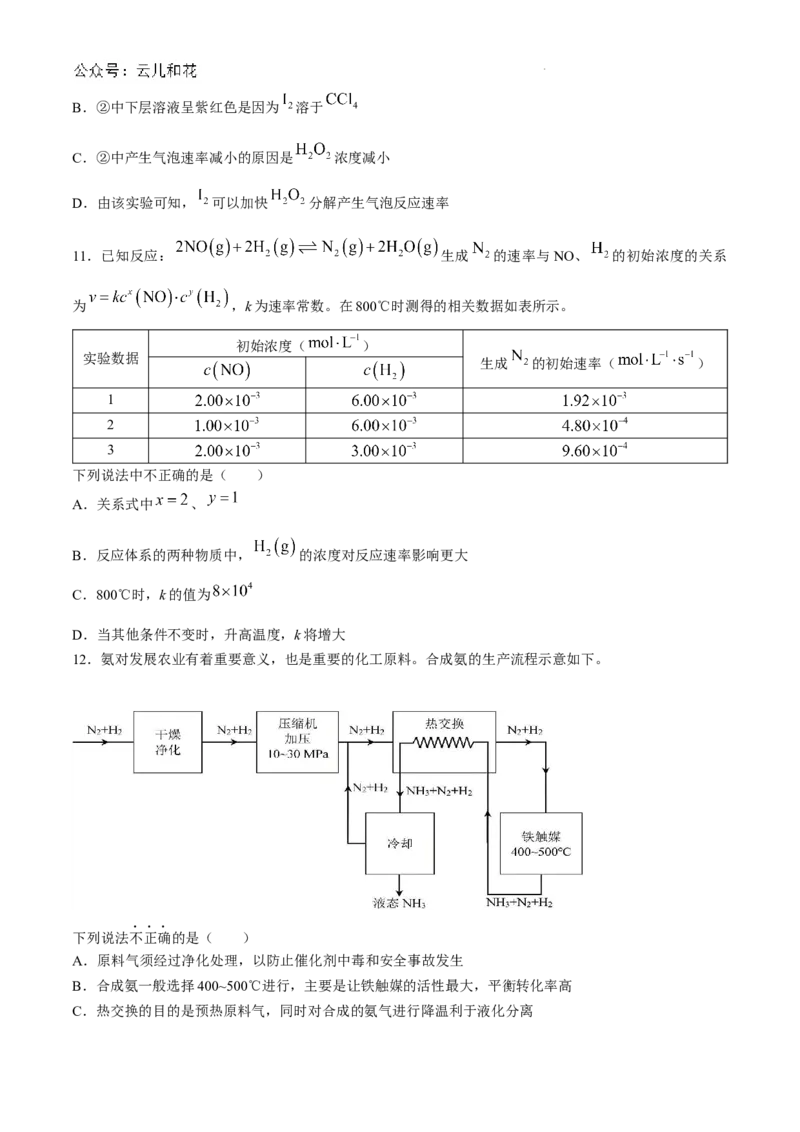
9.某研究小组利用图1所示的实验装置,测定压强变化对 平衡体系的影响。恒温
条件下,注射器内压强随时间变化如图2所示。下列说法正确的是( )
图1 图2
A.反应速率:b点 ,f点
B.体系颜色深浅:b>c>a,可以用勒夏特列原理解释
C.反应的平衡常数 :
D.a点时进行的操作是推注射器活塞,e点时进行的操作是拉注射器活塞
10.某同学进行如下实验:①将 溶液与KI溶液混合,产生大量气泡,溶液颜色变黄;②将①中的黄
色溶液分成两等份,一份加入 ,振荡,产生气泡速率明显减小,下层溶液呈紫红色;另一份不加
,振荡,产生气泡速率无明显变化。下列说法不正确的是( )
A.①中溶液颜色变黄的原因是:
学科网(北京)股份有限公司B.②中下层溶液呈紫红色是因为 溶于
C.②中产生气泡速率减小的原因是 浓度减小
D.由该实验可知, 可以加快 分解产生气泡反应速率
11.已知反应: 生成 的速率与NO、 的初始浓度的关系
为 ,k为速率常数。在800℃时测得的相关数据如表所示。
初始浓度( )
实验数据
生成 的初始速率( )
1
2
3
下列说法中不正确的是( )
A.关系式中 、
B.反应体系的两种物质中, 的浓度对反应速率影响更大
C.800℃时,k的值为
D.当其他条件不变时,升高温度,k将增大
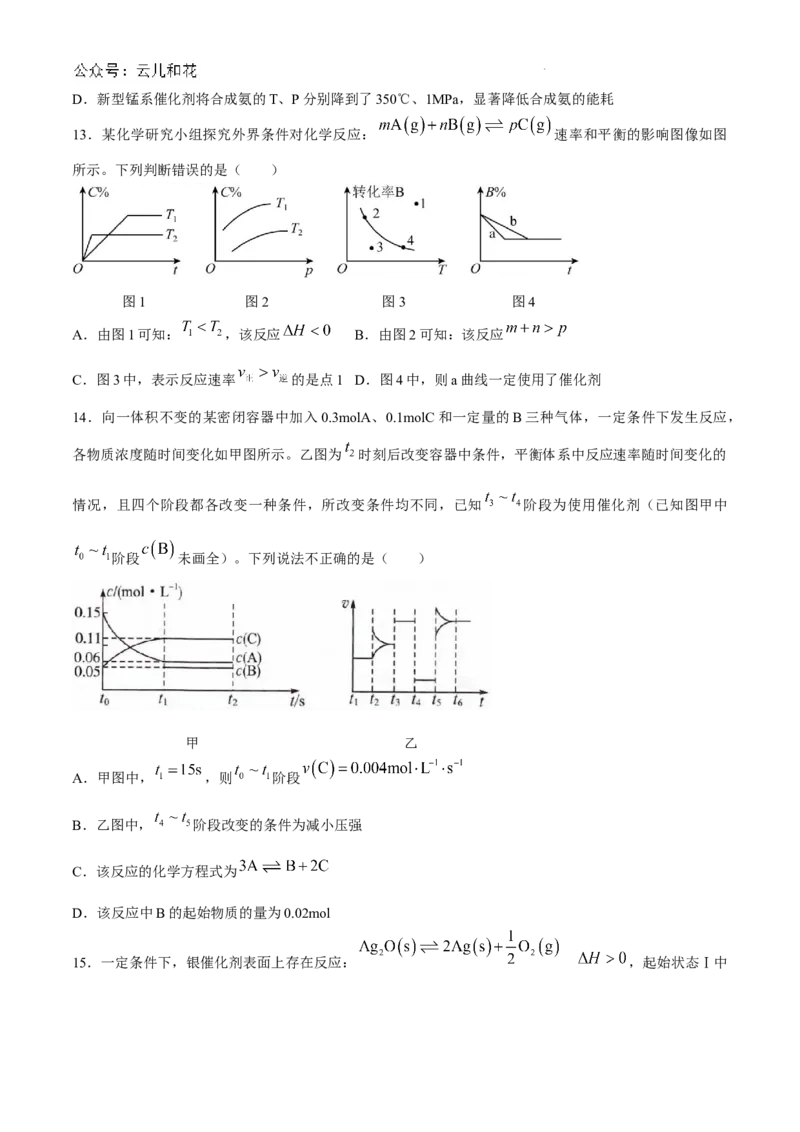
12.氨对发展农业有着重要意义,也是重要的化工原料。合成氨的生产流程示意如下。
下列说法不正确的是( )
A.原料气须经过净化处理,以防止催化剂中毒和安全事故发生
B.合成氨一般选择400~500℃进行,主要是让铁触媒的活性最大,平衡转化率高
C.热交换的目的是预热原料气,同时对合成的氨气进行降温利于液化分离
学科网(北京)股份有限公司D.新型锰系催化剂将合成氨的T、P分别降到了350℃、1MPa,显著降低合成氨的能耗
13.某化学研究小组探究外界条件对化学反应: 速率和平衡的影响图像如图
所示。下列判断错误的是( )
图1 图2 图3 图4
A.由图1可知: ,该反应 B.由图2可知:该反应
C.图3中,表示反应速率 的是点1 D.图4中,则a曲线一定使用了催化剂
14.向一体积不变的某密闭容器中加入0.3molA、0.1molC和一定量的B三种气体,一定条件下发生反应,
各物质浓度随时间变化如甲图所示。乙图为 时刻后改变容器中条件,平衡体系中反应速率随时间变化的
情况,且四个阶段都各改变一种条件,所改变条件均不同,已知 阶段为使用催化剂(已知图甲中
阶段 未画全)。下列说法不正确的是( )
甲 乙
A.甲图中, ,则 阶段
B.乙图中, 阶段改变的条件为减小压强
C.该反应的化学方程式为
D.该反应中B的起始物质的量为0.02mol
15.一定条件下,银催化剂表面上存在反应: ,起始状态Ⅰ中
学科网(北京)股份有限公司有 、Ag和 ,经下列过程达到各平衡状态(已知状态Ⅰ和Ⅲ的固体质量相等),下列叙述正确的
是( )
A.从Ⅰ到Ⅱ的过程 B.反应的平衡压强:
C.平衡常数: D.若体积 ,则
二、填空题:四大题,共55分。
16.某研究性学习小组利用 溶液和酸性 溶液之间的反应来探究“外界条件改变对化学反
应速率的影响”,实验如下,回答下列问题:
参加反应的物质
溶液颜色褪至
实验 实验温
无色时所需时
序号 度/K 溶液(含硫酸) 溶液
间/s
A 293 20 0.2 40 1 0
B 20 0.2 30 1 8
C 313 20 0.2 1 0
(1)通过实验 A、B,可探究__________的改变对反应速率的影响,其中 __________,
__________。
(2)通过实验__________(填序号)可探究出温度变化对化学反应速率的影响。
(3)依据实验B,用 的浓度变化表示的反应速率 __________。(保留2位有效数
字)
(4)在实验中发现高锰酸钾酸性溶液和草酸溶液反应时,开始一段时间反应较慢,溶液变色不明显;但
不久突然褪色,反应明显加快。某同学认为是反应放热导致溶液温度升高所致,重做 B组实验,测定反应
过程中不同时间溶液的温度,结果如表:
时间/s 0 2 4 6 8 10
温度/℃ 20 21 21 21.5 22 22
①结合实验目的与表中数据,你得出的结论是__________。
②从影响化学反应速率的因素看,你认为还可能是__________的影响。若用实验证明你的猜想,除了酸性
高锰酸钾溶液和草酸溶液外,还需要选择的试剂最合理的是__________(填字母)。
A.硫酸钾 B.水 C.二氧化锰 D.硫酸锰
17.二甲醚(DME)被誉为“21世纪的清洁燃料”,由合成气制备二甲醚的主要原理如下:
①
学科网(北京)股份有限公司②
③
回答下列问题:
(1)反应 的平衡常数 __________(用 、 、
表示)
(2)在保持反应物投料不变的情况下,请写出一条提高甲醇产率的措施__________。
(3)一定温度下,将0.2molCO和 通入2L恒容密闭容器中,发生反应③,5min后达到化
学平衡,平衡后测得 的体积分数为 0.1。则 0~5min 内 __________,CO 的转化率为
__________。
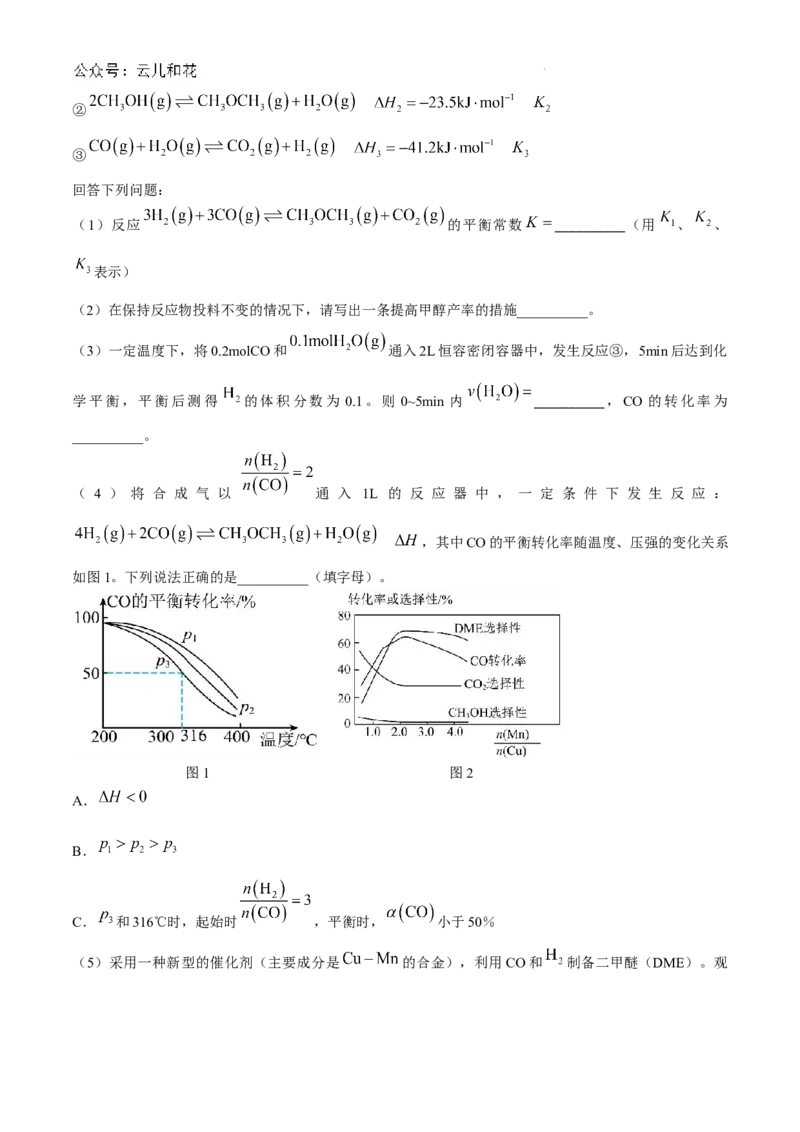
( 4 ) 将 合 成 气 以 通 入 1L 的 反 应 器 中 , 一 定 条 件 下 发 生 反 应 :
,其中CO的平衡转化率随温度、压强的变化关系
如图1。下列说法正确的是__________(填字母)。
图1 图2
A.
B.
C. 和316℃时,起始时 ,平衡时, 小于50%
(5)采用一种新型的催化剂(主要成分是 的合金),利用CO和 制备二甲醚(DME)。观
学科网(北京)股份有限公司察上图2,当 约为__________时最有利于二甲醚的合成。
18.丙酮蒸气热裂解可生产乙烯酮, ,现对该
热裂解反应进行研究,回答下列问题:
(1)①已知 、 、 键能分别为 、 、 ,计算
__________ 。
②该反应在__________(填“低温”或“高温”或“任意温度”)条件下可自发进行。
(2)在恒容绝热密闭容器中,充入丙酮蒸气,不能判断下列到达平衡状态的是__________。
A. 消耗速率与 生成速率相等
B.容器内压强不再变化
C.反应的平衡常数不再变化
D.混合气体的平均相对分子质量不再变化
E. 和 的浓度比保持不变
F.混合气体的密度不再变化
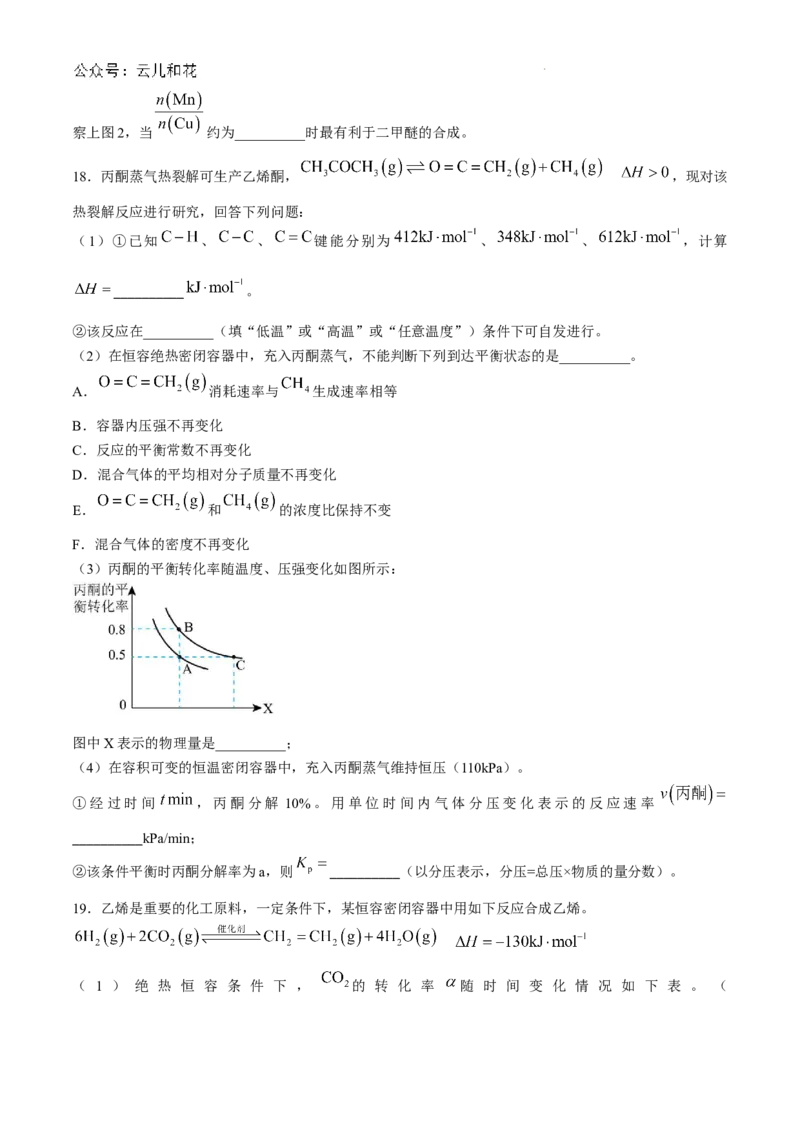
(3)丙酮的平衡转化率随温度、压强变化如图所示:
图中X表示的物理量是__________;
(4)在容积可变的恒温密闭容器中,充入丙酮蒸气维持恒压(110kPa)。
①经过时间 ,丙酮分解 10%。用单位时间内气体分压变化表示的反应速率
__________kPa/min;
②该条件平衡时丙酮分解率为a,则 __________(以分压表示,分压=总压×物质的量分数)。
19.乙烯是重要的化工原料,一定条件下,某恒容密闭容器中用如下反应合成乙烯。
( 1 ) 绝 热 恒 容 条 件 下 , 的 转 化 率 随 时 间 变 化 情 况 如 下 表 。 (
学科网(北京)股份有限公司)
时间/min 5 10 15 20 25 30 35 40 45 50
转化率/% 1.0 3.0 6.7 11.2 21.5 22.9 23.5 23.7 23.7 23.7
①0~25min内,反应速率的变化趋势为__________,其原因可能是__________。
②25min~40min内,转化率变化较小,其原因可能是__________;40min时反应__________(填“达到”
或“未达到”)化学平衡状态。
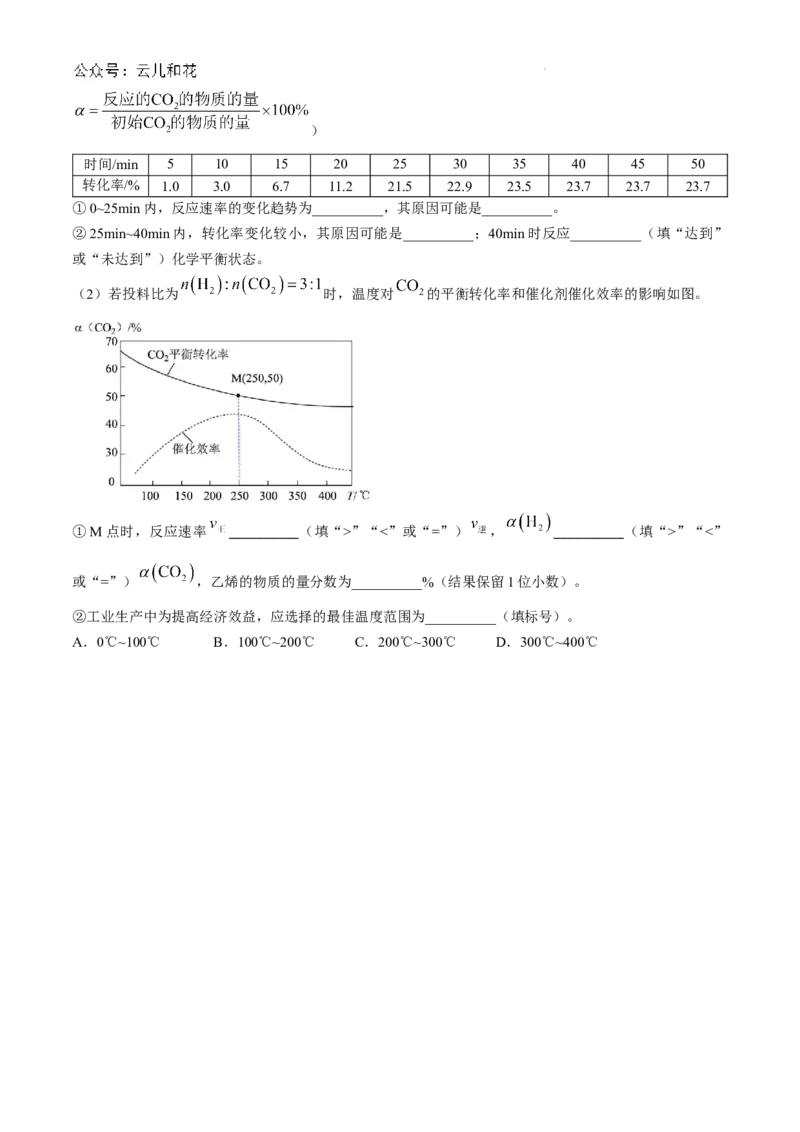
(2)若投料比为 时,温度对 的平衡转化率和催化剂催化效率的影响如图。
①M点时,反应速率 __________(填“>”“<”或“=”) , __________(填“>”“<”
或“=”) ,乙烯的物质的量分数为__________%(结果保留1位小数)。
②工业生产中为提高经济效益,应选择的最佳温度范围为__________(填标号)。
A.0℃~100℃ B.100℃~200℃ C.200℃~300℃ D.300℃~400℃
学科网(北京)股份有限公司参考答案:
1.ABDAC 6.BDCDC 11.BBCDD
16.(共14分,每空2分,除标注外)
(1)反应物(草酸)浓度 10(1分) 293(1分)
(2)A、C
(3)
(4)温度不是反应速率突然加快的原因 催化剂 D
17.(共12分,每空2分)
(1)
(2)将甲醇从体系中分离出来、增大压强
(3) 15%
(4)AB
(5)2.0
18.(共13分,每空2分,除标注外)
(1)+84 高温
(2)EF
(3)压强
(4) (3分)
19.(共16分,每空2分)
(1)①增大 随着反应的进行,温度升高,反应速率变快
②随着反应进行,反应物浓度降低,反应速率降低 达到
(2)①= = 7.7;②C
学科网(北京)股份有限公司