文档内容
2024—2025 学年度下学期 2023 级
5 月月考化学试卷
命题人:李德植 审题人:尚邦全
考试时间:2025 年 5 月 16 日
一、选择题
1.化学与人类的生活息息相关,下列有关说法错误的是
A.苯酚有毒,使用时若不慎沾到皮肤上,应立即用水冲洗
B.液态的氯乙烷汽化时大量吸热,可用于运动中急性损伤的镇痛剂
C.蚂蚁会分泌蚁酸,被蚂蚁叮咬后可及时涂抹肥皂水,起到止痒作用
D.喝酒后脸红.昏迷等症状,是由于酒精代谢过程中产生的乙醛刺激毛细血管
2.下列化学用语的表达正确的是
A.2-丁烯的键线式: B. 的电子式:
C.基态碳原子价层电子排布式: D.四氯化碳的球棍模型:
3.用 表示阿伏加德罗常数的值,下列说法正确的是
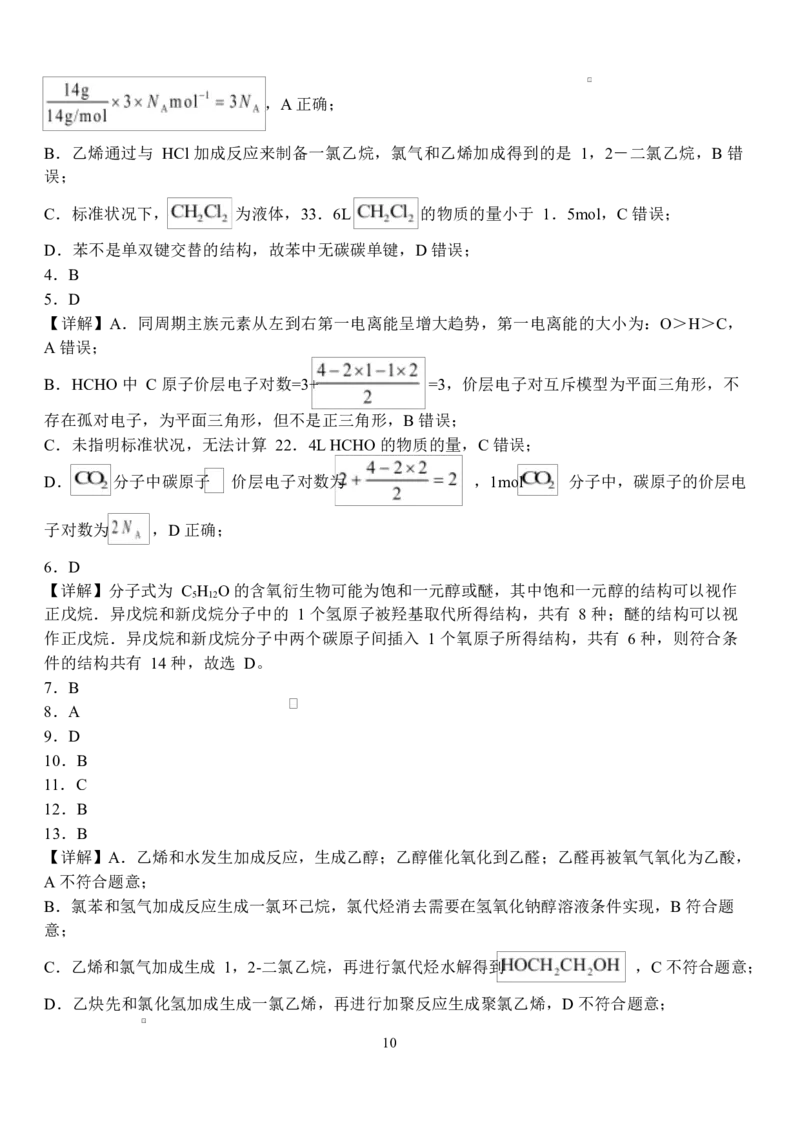
A.14g 的丙烯和 1-丁烯的混合气体,其原子数为
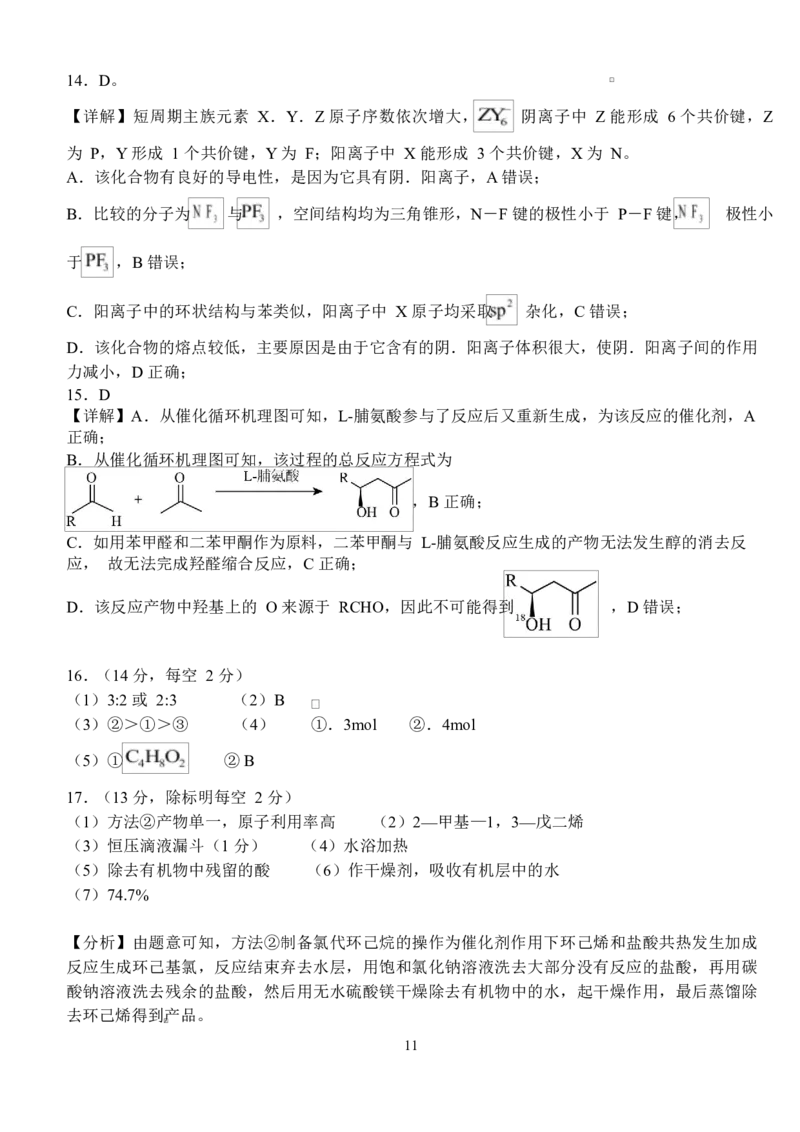
B.由乙烯制备 1mol 一氯乙烷,需 个 分子
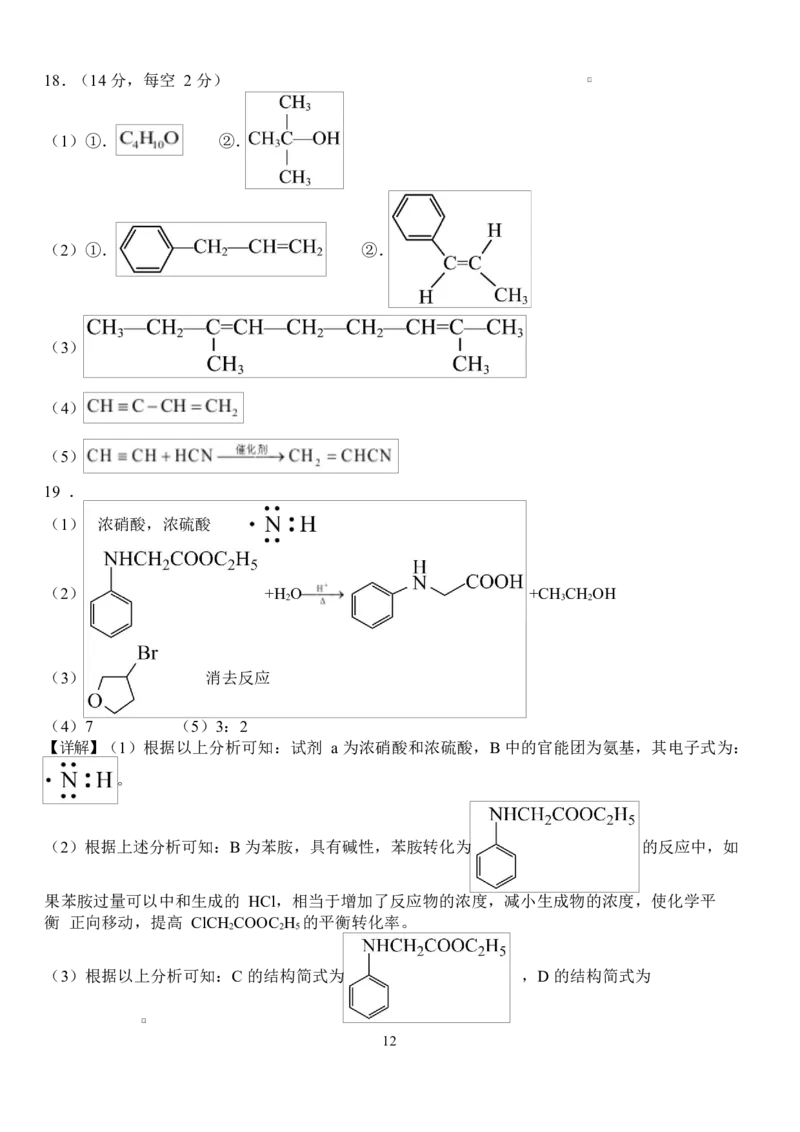
C.标准状况下,33.6L 的分子数为 1.5mol
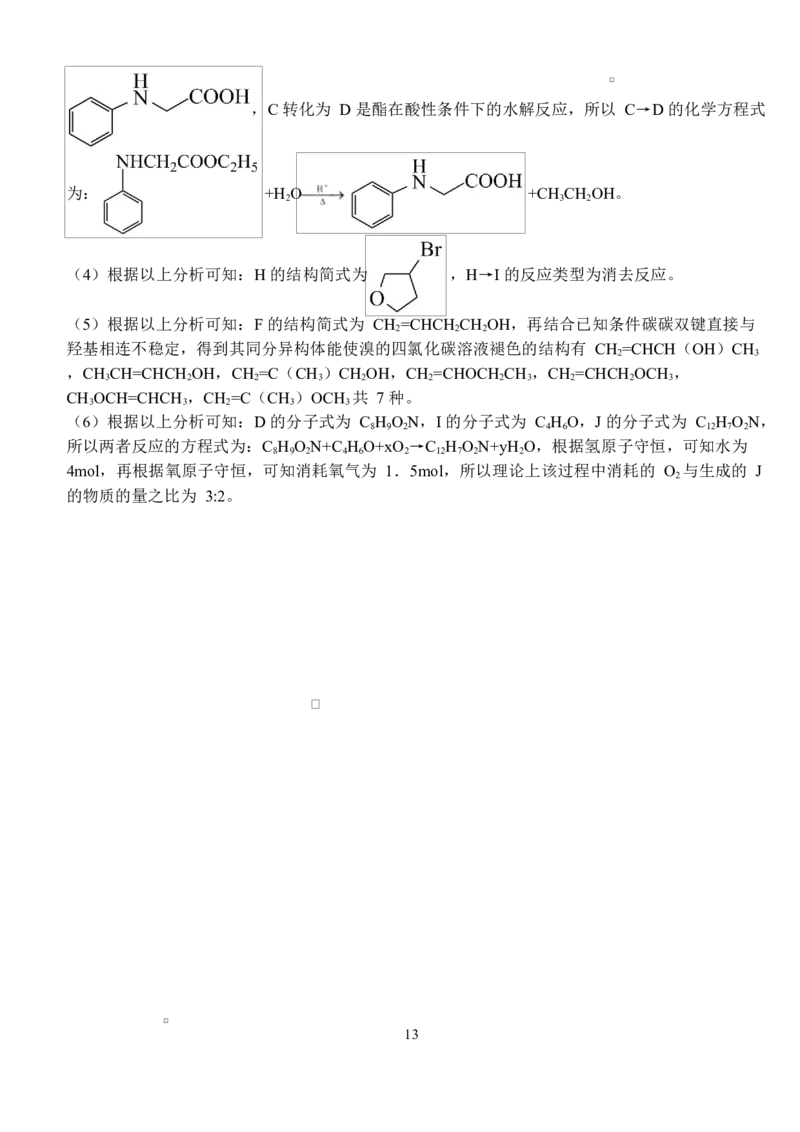
D.1mol 苯分子中含有的碳碳单键的数目为
4.下列物质的系统命名正确的是
A. :2-甲基-1-丙醇 B.2-甲基苯酚:
C. :二氯乙烷 D. :2,3-二甲基-2-乙基丁烷
15.我国科学家研制出一种催化剂,能在室温下高效催化空气中甲醛转化为二氧化碳和水,反应化
学方程式为: ,用 表示阿伏加德罗常数的值,下列有
关说法正确的是
A.该反应涉及元素中第一电离能最大的是 C
B.HCHO 为含极性键的平面正三角形分子
C.处理 22.4L HCHO 转移电子数目为
D.1mol 分子中,碳原子的价层电子对数为
6.分子式为 的有机物的同分异构体数目为
A.8 B.10 C.13 D.14
7.藿香蓟具有清热解毒功效,其有效成分结构如下。下列有关该物质的
说法错误的是( )
A.可以发生水解反应 B.所有碳原子处于同一平面
C.含有 2 种含氧官能团 D.能与溴水发生加成反应
8.下列说法不正确的是( )
A.乙醇和丙三醇( )互为同系物
B.35Cl 和 37Cl 互为同位素
C.O 和 O 互为同素异形体
2 3
D.丙酮( )和环氧丙烷( )互为同分异构体
9.精细化学品 Z 是 X 与 HBr 反应的主产物,X→Z 的反应机理如下:
+HBr + Br-
X Y Z
下列说法不正确的是( )
A.X 与 互为顺反异构体 B.X 能使溴的 CCl4 溶液褪色
2C.X 与 HBr 反应有副产物 生成 D.Z 分子中含有 2 个手性碳原子
10.丙烯可发生如下转化,下列说法不正确的是( )
A.丙烯分子中最多 7 个原子共平面
B.X 的结构简式为 CH CH CHBr
3
C.Y 的同分异构体有 3 种(不包含 Y 本身,
不考虑立体异构)
D.聚合物 Z 的链节为
11.实验室常用浓硫酸和乙醇混合加热制取乙烯,下列说法中正确的个数是( )
①浓硫酸作催化剂、脱水剂
②在反应容器中放入几片碎瓷片,是为了防止混合液暴沸
③反应温度缓慢上升至 170℃
④用排水法或向下排空气法收集乙烯
⑤圆底烧瓶中装的是 4 mL 乙醇和 12 mL 3 mol·L-1 H SO 混合液
2 4
⑥温度计应插入反应溶液液面下,以便控制温度
A.1 B.2 C.3 D.4
12.分子式为 C H O 的有机物 A 能在酸性条件下进行下列转化,同温同压下,相同质量的 B 和
9 18 2
C 的蒸气所占体积相同,下列说法不正确的是(A.B.C.D.E 均为有机物)( )
A.E 酸化后的有机物与 C 一定互为同系物
B.符合上述转化关系的有机物 A 的结构有 9 种(不
考虑立体异构)
C.1 mol B 完全转化为 D 转移 2 mol 电子
D.D 到 E 发生氧化反应
13.某同学设计了下列合成路线,你认为不能实现的是
A.用乙烯合成乙酸:
B.用氯苯合成环己烯:
C.用乙烯合成乙二醇:
D.用乙炔合成聚氯乙烯:
314.离子液体具有良好的导电性,某种咪唑盐结构如下图所示,X.Y.Z 原子序数依次增大,均
为短周期主族元素。已知阳离子中的环状结构与苯类似,下列说法正确的是
A.该化合物具有良好的导电性,是因为它含有有机环状结构
B.分子的极性:
C.阳离子中 X 原子有 . 两种杂化方式
D.该化合物的熔点较低,主要是由于它含有体积很大的阴.阳离子
15.2021 年诺贝尔化学奖授予了对有机小分子不对称催化作出重大贡献的科学家,其研究成果羟
醛缩合反应的催化循环机理如下图所示。下列说法不正确的是
A.L-脯氨酸是该反应的催化剂
B.该过程的总反应方程式为
C.根据该机理,用苯甲醛和二苯甲酮( )作为原料,无法完成羟醛缩合反应
4D.若用含 H 18O 的溶剂和不含 18O 的 RCHO 和丙酮进行该反应,得到的产物可能为
2
二、填空题
16.(14 分)回答下列问题:
(1) 有机物的核磁共振氢谱出现的峰面积之比为______。
(2)只用一种试剂鉴别 、 、苯、硝基苯,可选用的化学试剂
为______(填字母)
A. B. 溶液 C. D.溴水
(3)下列有机化合物在水中的溶解度由大到小的顺序为:______(填序号)
① ② ③
(4)中草药秦皮中含有七叶树内酯,其结构简式为 ,具有抗菌作用。
若 1mol 七叶树内酯分别与足量浓溴水和足量 NaOH 溶液完全反应,则消耗 的物质的量为
______;消耗 NaOH 的物质的量为______。
(5)某研究小组为测定某有机化合物 X 的结构,进行如下实验:
①准确称取 6.6g 某有机物样品 X(只含 C.H.O 三种元素),经充分燃烧后的产物依次通
过浓硫酸和碱石灰,二者质量分别增加 5.4g 和 13.2g。
②使用现代仪器对有机化合物 X 的分子结构进行测定,相关结果如下:
5则该有机物 X 的分子式为______,结构简式可能为______(填序号)。
A. B.
C. D.
17.(13 分)氯代环己烷为无色液体,具有窒息性气味,不溶于水,溶于乙醇,可生产农药.橡胶
b 防焦剂.医药等。请回答下列问题:
Ⅰ.制备氯代环已烷有两种方法:
①环己烷氯化法:
②环己烯氯化氢加成法:
(1)工业上多采用方法②制备氯代环己烷,原因是________。
(2) 是环己烯的同分异构体,其名称为________。
Ⅱ.现用如图所示装置模拟方法②制备氯代环已烷,具体操作步骤如下:在 250mL 三口烧瓶
中加入 35mL(0.35mol)环己烯,3g 催化剂,搅拌升温,打开仪器 a 的活塞向三口烧瓶中加入
100mL30%(约 0.95mol)的盐酸,调节反应温度为 75℃,搅拌反应 1.5 小时,待反应结束,
冷却静置。分别使用饱和氯化钠溶液和碳酸钠溶液洗涤有机
层 3 次,再向有机层中加入适量无水硫酸镁后蒸馏,得产品
31g 。
6(3)仪器 a 的名称是________。
(4)该实验中合适的加热方式是________。
(5)使用碳酸钠溶液洗涤有机层的目的是:________。
(6)加入适量无水硫酸镁的目的是:________。
(7)该实验氯代环己烷的产率为________。(结果保留三位有效数字)
18.(14 分)Ⅰ.请回答下列问题:
(1)某有机物 14.8g 与足量氧气在密闭容器中完全燃烧后,将反应生成的气体依次通过浓
硫酸和碱石灰。测得浓硫酸质量增加 18 克,碱石灰质量增加 35.2 克,则该有机物的分子式为
________,已知该有机物分子中含有一个羟基,核磁共振氢谱含有两组峰,峰面积之比为 1:9,则
该有机物的结构简式为________。
(2)苯丙烯( )具有 A.B 两种直链位置异构体,其中 A 具有顺式 C 和反式 D 两种
异构体,则 B.D 的结构简式分别为________.________。
(3)已知烯烃能被酸性 溶液氧化,例如:
某烃的分子式为 ,1mol 该烃在催化剂作用下可以吸收 ;用热的酸性
溶液氧化,得到下列三种有机物: ; ;
。由此推断该烃的结构简式为________。
Ⅱ.乙炔是一种重要的有机化工原料,以乙炔为主要原料可以合成氯丁橡胶和聚丙烯腈。有
关合成路线如图:
7已知:
(4)A 的结构简式为___________。
(5) 的化学方程式为________。
19.(14 分)我国科学家实现了喹啉并内酯的高选择性制备。合成路线如下图。
已知:
i.R―Br+R'CHO
ii.ROH+R'Br ROR'
iii.碳碳双键直接与羟基相连不稳定
(1)试剂 a 为 ;B 中官能团的电子式为 。
(2)C→D 的化学方程式为 。
(3)H 的结构简式为 ;H→I 的反应类型为 。
(4)K 是 F 的同分异构体,其中能使溴的四氯化碳溶液褪色的结构还有 种(不考虑
立体异构)。
(5)D 和 I 转化成 J 的反应过程中还生成水,理论上该过程中消耗的 与生成的 J 的物质的
8量之比为 。
高二年级 5 月月考化学参考答案
1.A
【详解】A.苯酚有毒,对皮肤有腐蚀性,如不慎沾到皮肤上,应立即用乙醇冲洗,再用水冲洗,
A 错误;
B.液态氯乙烷汽化时大量吸热,具有冷冻麻醉作用,可在身体局部产生快速镇痛效果,常用于运
动中急性损伤的镇痛剂,B 正确;
C.由于肥皂水显碱性,可消除蚁酸带来的酸性,起到止痒作用,C 正确;
D.酒精在人体内的代谢:乙醇通过乙醇脱氢酶转化成乙醛,乙醛通过乙醛脱氢酶转化为乙酸,一
些人缺少乙醛脱氢酶,使得体内的乙醛不易被氧化成乙酸,从而使得人脸部毛细血管扩张充血,
并产生其他醉酒症状,D 正确;
2.B
【详解】A.2-丁烯的键线式: 故 A 错误;
B. 的电子式为 ,故 B 正确;
C.基态碳原子的价电子排布为 ,轨道表示式为: ,故 C 错误;
D.四氯化碳分子中氯原子半径比碳原子半径大,故 D 错误;
故选 B。
3.A
【 详 解 】 A. 丙 烯 . 1- 丁 烯 的 最 简 式 均 为 , 则 14g 混 合 气 体 所 含 有
的 原 子 数 是
9,A 正确;
B.乙烯通过与 HCl 加成反应来制备一氯乙烷,氯气和乙烯加成得到的是 1,2-二氯乙烷,B 错
误;
C.标准状况下, 为液体,33.6L 的物质的量小于 1.5mol,C 错误;
D.苯不是单双键交替的结构,故苯中无碳碳单键,D 错误;
4.B
5.D
【详解】A.同周期主族元素从左到右第一电离能呈增大趋势,第一电离能的大小为:O>H>C,
A 错误;
B.HCHO 中 C 原子价层电子对数=3+ =3,价层电子对互斥模型为平面三角形,不
存在孤对电子,为平面三角形,但不是正三角形,B 错误;
C.未指明标准状况,无法计算 22.4L HCHO 的物质的量,C 错误;
D. 分子中碳原子 价层电子对数为 ,1mol 分子中,碳原子的价层电
子对数为 ,D 正确;
6.D
【详解】分子式为 C H O 的含氧衍生物可能为饱和一元醇或醚,其中饱和一元醇的结构可以视作
5 12
正戊烷.异戊烷和新戊烷分子中的 1 个氢原子被羟基取代所得结构,共有 8 种;醚的结构可以视
作正戊烷.异戊烷和新戊烷分子中两个碳原子间插入 1 个氧原子所得结构,共有 6 种,则符合条
件的结构共有 14 种,故选 D。
7.B
8.A
9.D
10.B
11.C
12.B
13.B
【详解】A.乙烯和水发生加成反应,生成乙醇;乙醇催化氧化到乙醛;乙醛再被氧气氧化为乙酸,
A 不符合题意;
B.氯苯和氢气加成反应生成一氯环己烷,氯代烃消去需要在氢氧化钠醇溶液条件实现,B 符合题
意;
C.乙烯和氯气加成生成 1,2-二氯乙烷,再进行氯代烃水解得到 ,C 不符合题意;
D.乙炔先和氯化氢加成生成一氯乙烯,再进行加聚反应生成聚氯乙烯,D 不符合题意;
1014.D。
【详解】短周期主族元素 X.Y.Z 原子序数依次增大, 阴离子中 Z 能形成 6 个共价键,Z
为 P,Y 形成 1 个共价键,Y 为 F;阳离子中 X 能形成 3 个共价键,X 为 N。
A.该化合物有良好的导电性,是因为它具有阴.阳离子,A 错误;
B.比较的分子为 与 ,空间结构均为三角锥形,N-F 键的极性小于 P-F 键, 极性小
于 ,B 错误;
C.阳离子中的环状结构与苯类似,阳离子中 X 原子均采取 杂化,C 错误;
D.该化合物的熔点较低,主要原因是由于它含有的阴.阳离子体积很大,使阴.阳离子间的作用
力减小,D 正确;
15.D
【详解】A.从催化循环机理图可知,L-脯氨酸参与了反应后又重新生成,为该反应的催化剂,A
正确;
B.从催化循环机理图可知,该过程的总反应方程式为
,B 正确;
C.如用苯甲醛和二苯甲酮作为原料,二苯甲酮与 L-脯氨酸反应生成的产物无法发生醇的消去反
应, 故无法完成羟醛缩合反应,C 正确;
D.该反应产物中羟基上的 O 来源于 RCHO,因此不可能得到 ,D 错误;
16.(14 分,每空 2 分)
(1)3:2 或 2:3 (2)B
(3)②>①>③ (4) ①.3mol ②.4mol
(5)① ②B
17.(13 分,除标明每空 2 分)
(1)方法②产物单一,原子利用率高 (2)2—甲基—1,3—戊二烯
(3)恒压滴液漏斗(1 分) (4)水浴加热
(5)除去有机物中残留的酸 (6)作干燥剂,吸收有机层中的水
(7)74.7%
【分析】由题意可知,方法②制备氯代环己烷的操作为催化剂作用下环己烯和盐酸共热发生加成
反应生成环己基氯,反应结束弃去水层,用饱和氯化钠溶液洗去大部分没有反应的盐酸,再用碳
酸钠溶液洗去残余的盐酸,然后用无水硫酸镁干燥除去有机物中的水,起干燥作用,最后蒸馏除
去环己烯得到产品。
1118.(14 分,每空 2 分)
(1)①. ②.
(2)①. ②.
(3)
(4)
(5)
19 .
(1) 浓硝酸,浓硫酸
(2) +H O +CH CH OH
2 3 2
(3) 消去反应
(4)7 (5)3:2
【详解】(1)根据以上分析可知:试剂 a 为浓硝酸和浓硫酸,B 中的官能团为氨基,其电子式为:
。
(2)根据上述分析可知:B 为苯胺,具有碱性,苯胺转化为 的反应中,如
果苯胺过量可以中和生成的 HCl,相当于增加了反应物的浓度,减小生成物的浓度,使化学平
衡 正向移动,提高 ClCH COOC H 的平衡转化率。
2 2 5
(3)根据以上分析可知:C 的结构简式为 ,D 的结构简式为
12,C 转化为 D 是酯在酸性条件下的水解反应,所以 C→D 的化学方程式
为: +H O +CH CH OH。
2 3 2
(4)根据以上分析可知:H 的结构简式为 ,H→I 的反应类型为消去反应。
(5)根据以上分析可知:F 的结构简式为 CH =CHCH CH OH,再结合已知条件碳碳双键直接与
2 2 2
羟基相连不稳定,得到其同分异构体能使溴的四氯化碳溶液褪色的结构有 CH =CHCH(OH)CH
2 3
,CH CH=CHCH OH,CH =C(CH )CH OH,CH =CHOCH CH ,CH =CHCH OCH ,
3 2 2 3 2 2 2 3 2 2 3
CH OCH=CHCH ,CH =C(CH )OCH 共 7 种。
3 3 2 3 3
(6)根据以上分析可知:D 的分子式为 C H O N,I 的分子式为 C H O,J 的分子式为 C H O N,
8 9 2 4 6 12 7 2
所以两者反应的方程式为:C H O N+C H O+xO →C H O N+yH O,根据氢原子守恒,可知水为
8 9 2 4 6 2 12 7 2 2
4mol,再根据氧原子守恒,可知消耗氧气为 1.5mol,所以理论上该过程中消耗的 O 与生成的 J
2
的物质的量之比为 3:2。
13