文档内容
新高中创新联盟 TOP 二十名校高三 10 月调研考试
化 学
全卷满分100分,考试时间75分钟
注意事项:
1.答卷前,考生务必将自己的姓名,准考证号填写在答题卡上,并将条形码粘贴在答
题卡上的指定位置。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。
如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。
写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并收回。
4.可能用到的相对原子质量:H 1 C 12 O 16 K 39 Mn 55 Cu 64
一、选择题(本题共14小题,每小题3分,共计42分。在每小题列出的四个选项中,只有
一项是符合题目要求的)
1.化学与科学、技术、社会、环境等密切联系。下列说法错误的是
A.利用臭氧的氧化性处理污水中的NO-
3
B.用铝粉与烧碱作固体疏通剂疏通堵塞的厨卫管道
C.纳米铁能快速除去水中溶解氧与其高效的吸附能力有关
D.用于制造喷气式飞机发动机叶片的铁钴合金具有耐高温、强度高等优点
2.氮化铝(AlN)是一种新型材料,能溶于强碱溶液发生反应:AlN+NaOH+3H O
2
Na[Al(OH) ]+NH ↑。下列说法正确的是
4 3
A.NH 空间填充模型:
3
B.Na+的结构示意图:
C.用电子式表示H O的形成过程:
2
D.用NaOH溶液、MgCl 溶液和AlCl 溶液可以验证Mg、Al金属性强弱
2 3
3.下列叙述正确的是
A.Li在O 中燃烧得到Li O
2 2 2
B.金属钠起火可用泡沫灭火器灭火
C.化工厂通过氨的催化氧化等过程制硝酸
D.高温下,铁与水蒸气反应生成Fe(OH) 和H
3 2
4.物质转化在工业生产中有重要作用。在指定条件下,下列工业生产中涉及的物质转化关
系正确的是
1
学科网(北京)股份有限公司高温
A.制粗硅:SiO +C Si+CO ↑
2 2
B.制CCl :CH +2Cl 光照→CCl +2H
4 4 2 4 2
C.制甲醇:CO +3H 催化剂→CH OH+H O
2 2 ∆ 3 2
点燃
D.制SO :2S+3O (过量) 2SO
3 2 3
5.已知C H O (葡萄糖)酒化酶→2C H OH+2CO ↑。N 为阿伏加德罗常数的值。下列
6 12 6 2 5 2 A
说法正确的是
A.该反应生成22 g CO ,转移电子数目为4N
2 A
B.1 mol葡萄糖分子中含有羟基的数目为6N
A
C.100 g质量分数46%的乙醇溶液含有O-H键数目为7N
A
D.标准状况下,22.4 L C H OH共用电子对数目为8N
2 5 A
6.下列陈述Ⅰ与陈述Ⅱ均正确,且具有因果关系的是
7.下列离子方程式正确的是
A.用稀硝酸溶解FeO:FeO+2H+ Fe2++H O
2
B.向Na CO 溶液中滴加少量稀盐酸:CO2-+H+ HCO-
2 3 3 3
C.向硅酸钠溶液中滴加盐酸制备硅酸胶体:SiO2−+2H+ H SiO ↓
3 2 3
D.氯气能用于自来水的杀菌消毒:Cl +H O 2H++Cl-+ClO-
2 2
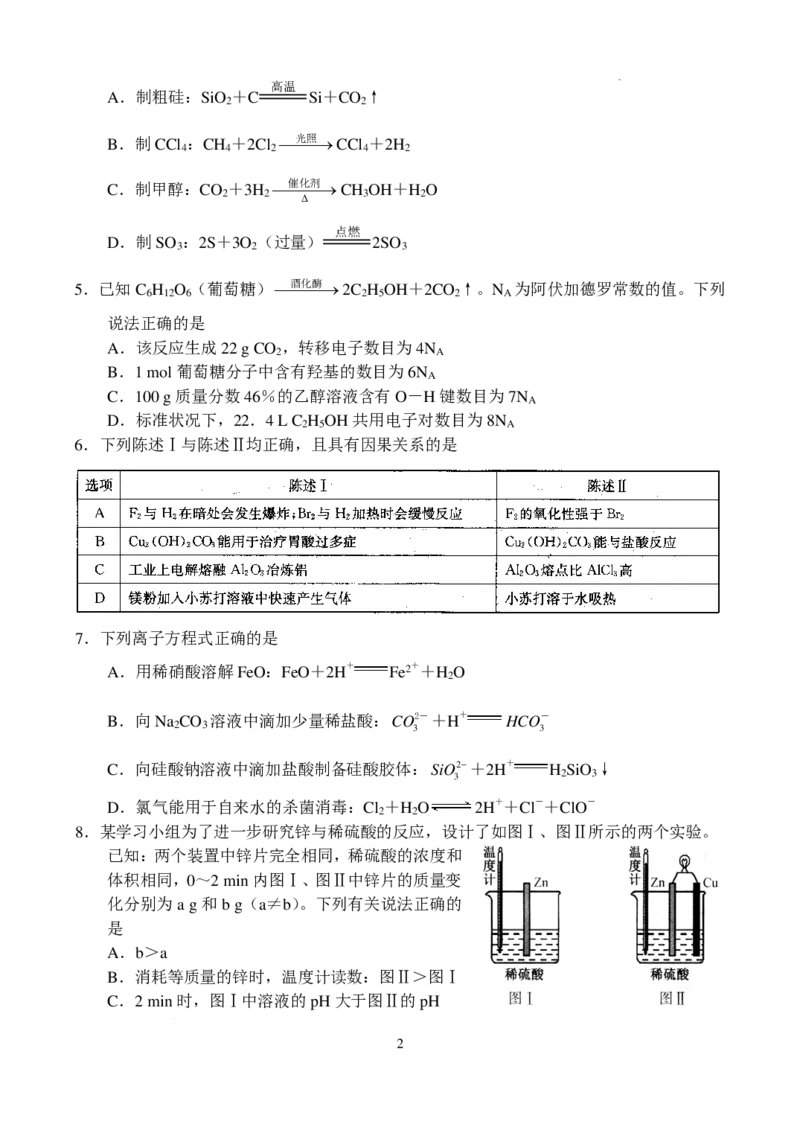
8.某学习小组为了进一步研究锌与稀硫酸的反应,设计了如图Ⅰ、图Ⅱ所示的两个实验。
已知:两个装置中锌片完全相同,稀硫酸的浓度和
体积相同,0~2 min内图Ⅰ、图Ⅱ中锌片的质量变
化分别为a g和b g(a≠b)。下列有关说法正确的
是
A.b>a
B.消耗等质量的锌时,温度计读数:图Ⅱ>图Ⅰ
C.2 min时,图Ⅰ中溶液的pH大于图Ⅱ的pH
2
学科网(北京)股份有限公司D.若图Ⅰ中的锌换成粗锌,与图Ⅰ装置相比,反应速率不变
9.化合物(YX ) W Z 能用作高分子聚合物的引发剂,其组成元素 X、Y、Z、W 为原子
4 2 2 8
序数依次增大的短周期主族元素,Y元素最简单氢化物的水溶液显碱性,地壳中Z元素
的质量分数最高,W的原子序数等于X、Y、Z的原子序数之和。下列叙述正确的是
A.原子半径:W>Z>Y>X B.氧化物对应的水化物的酸性:W>Y
C.简单阴离子的还原性:Z>W D.X、Y、W三种元素能组成离子化合物
10.钛有“二十一世纪的金属”、“全能金属”、“现代金属”的美称。以钛铁矿(FeTiO 中Ti
3
为+4价)为原料,经高温“氯化”制取金属钛的流程如下。下列叙述错误的是
A.“氯化”时矿料(FeTiO +C)与Cl 逆向而行,有利于反应充分进行
3 2
B.“氯化”时理论上参加反应的Cl 与CO物质的量之比为7 :6
2
C.Mg高温还原TiCl 反应,应在N 氛围中进行
4 2
D.流程中所需要的“Mg”,可通过电解熔融MgCl 制取
2
11.下列操作、现象和结论均正确的是
12.白色固体样品X,可能含Na S O 、K S、Na SO 、KOH、Na CO 和CaCO 之中一种、
2 2 3 2 2 3 2 3 3
两种或三种。某同学为探究样品X的组成,取适量样品进行如下实验。下列说法错误的
是
3
学科网(北京)股份有限公司注:本题分析溶液中离子种类时,不考虑水解以及水的电离。
A.X可能是Na S O
2 2 3
B.X可能是Na SO 和Na S O
2 3 2 2 3
C.溶液2中的阴离子不可能含有S2-和OH-
D.向溶液3中加入Ba(OH) 溶液,可能会产生白色沉淀
2
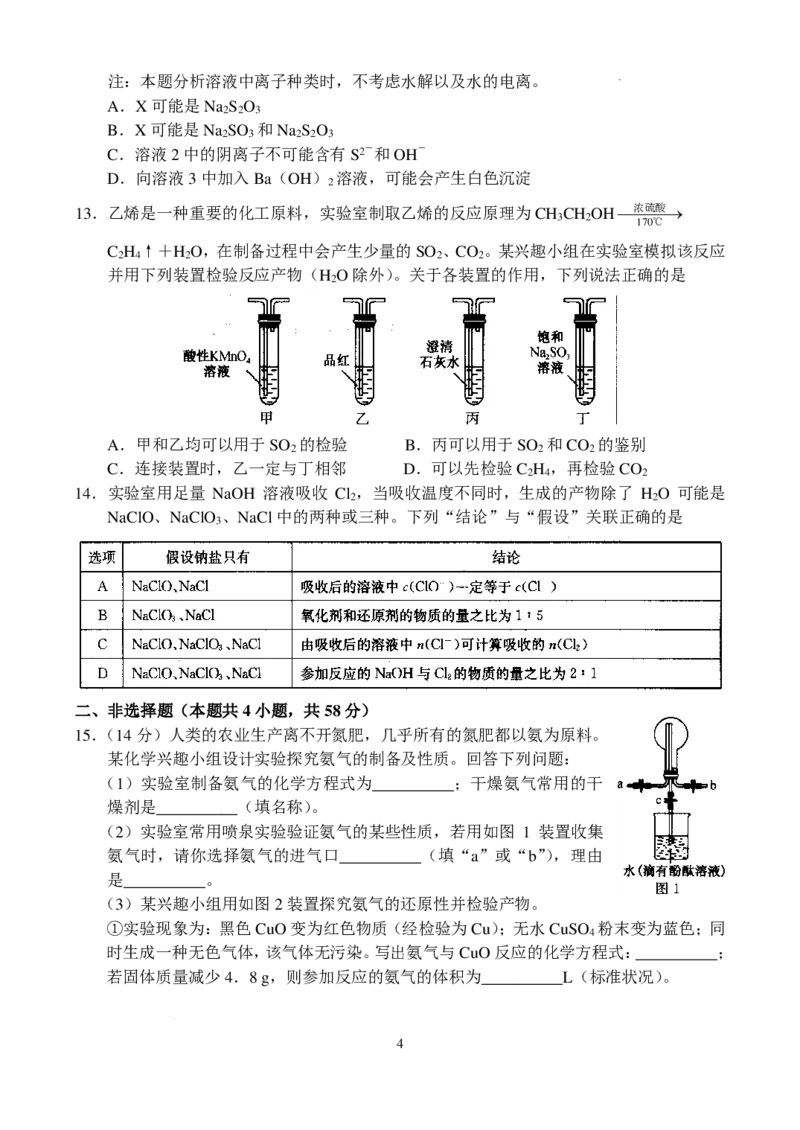
13.乙烯是一种重要的化工原料,实验室制取乙烯的反应原理为CH CH OH浓硫酸→
3 2 170℃
C H ↑+H O,在制备过程中会产生少量的SO 、CO 。某兴趣小组在实验室模拟该反应
2 4 2 2 2
并用下列装置检验反应产物(H O除外)。关于各装置的作用,下列说法正确的是
2
A.甲和乙均可以用于SO 的检验 B.丙可以用于SO 和CO 的鉴别
2 2 2
C.连接装置时,乙一定与丁相邻 D.可以先检验C H ,再检验CO
2 4 2
14.实验室用足量 NaOH 溶液吸收 Cl ,当吸收温度不同时,生成的产物除了 H O 可能是
2 2
NaClO、NaClO 、NaCl中的两种或三种。下列“结论”与“假设”关联正确的是
3
二、非选择题(本题共4小题,共58分)
15.(14分)人类的农业生产离不开氮肥,几乎所有的氮肥都以氨为原料。
某化学兴趣小组设计实验探究氨气的制备及性质。回答下列问题:
(1)实验室制备氨气的化学方程式为__________;干燥氨气常用的干
燥剂是__________(填名称)。
(2)实验室常用喷泉实验验证氨气的某些性质,若用如图 1 装置收集
氨气时,请你选择氨气的进气口__________(填“a”或“b”),理由
是__________。
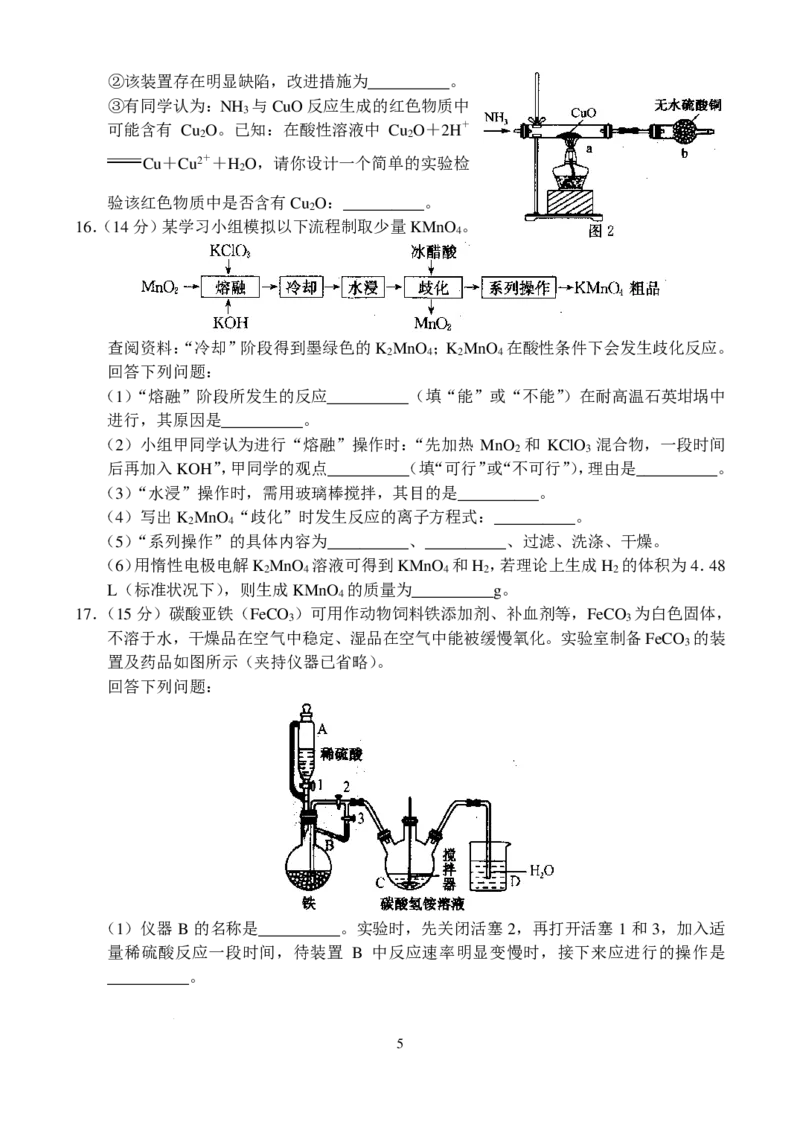
(3)某兴趣小组用如图2装置探究氨气的还原性并检验产物。
①实验现象为:黑色CuO变为红色物质(经检验为Cu);无水CuSO 粉末变为蓝色;同
4
时生成一种无色气体,该气体无污染。写出氨气与CuO反应的化学方程式:__________;
若固体质量减少4.8 g,则参加反应的氨气的体积为__________L(标准状况)。
4
学科网(北京)股份有限公司②该装置存在明显缺陷,改进措施为__________。
③有同学认为:NH 与CuO反应生成的红色物质中
3
可能含有 Cu O。已知:在酸性溶液中 Cu O+2H+
2 2
Cu+Cu2++H O,请你设计一个简单的实验检
2
验该红色物质中是否含有Cu O:__________。
2
16.(14分)某学习小组模拟以下流程制取少量KMnO 。
4
查阅资料:“冷却”阶段得到墨绿色的K MnO ;K MnO 在酸性条件下会发生歧化反应。
2 4 2 4
回答下列问题:
(1)“熔融”阶段所发生的反应__________(填“能”或“不能”)在耐高温石英坩埚中
进行,其原因是__________。
(2)小组甲同学认为进行“熔融”操作时:“先加热 MnO 和 KClO 混合物,一段时间
2 3
后再加入KOH”,甲同学的观点__________(填“可行”或“不可行”),理由是__________。
(3)“水浸”操作时,需用玻璃棒搅拌,其目的是__________。
(4)写出K MnO “歧化”时发生反应的离子方程式:__________。
2 4
(5)“系列操作”的具体内容为__________、__________、过滤、洗涤、干燥。
(6)用惰性电极电解K MnO 溶液可得到KMnO 和H ,若理论上生成H 的体积为4.48
2 4 4 2 2
L(标准状况下),则生成KMnO 的质量为__________g。
4
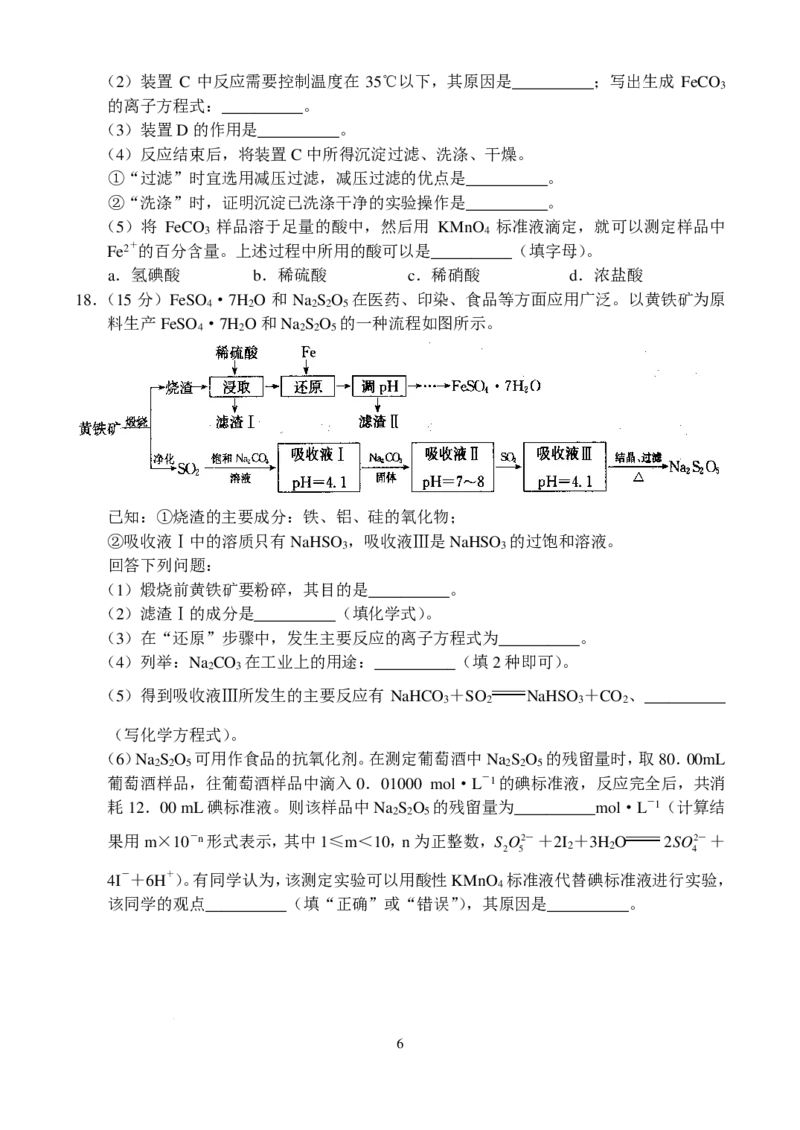
17.(15分)碳酸亚铁(FeCO )可用作动物饲料铁添加剂、补血剂等,FeCO 为白色固体,
3 3
不溶于水,干燥品在空气中稳定、湿品在空气中能被缓慢氧化。实验室制备FeCO 的装
3
置及药品如图所示(夹持仪器已省略)。
回答下列问题:
(1)仪器 B 的名称是__________。实验时,先关闭活塞 2,再打开活塞1 和 3,加入适
量稀硫酸反应一段时间,待装置 B 中反应速率明显变慢时,接下来应进行的操作是
__________。
5
学科网(北京)股份有限公司(2)装置 C 中反应需要控制温度在 35℃以下,其原因是__________;写出生成 FeCO
3
的离子方程式:__________。
(3)装置D的作用是__________。
(4)反应结束后,将装置C中所得沉淀过滤、洗涤、干燥。
①“过滤”时宜选用减压过滤,减压过滤的优点是__________。
②“洗涤”时,证明沉淀已洗涤干净的实验操作是__________。
(5)将 FeCO 样品溶于足量的酸中,然后用 KMnO 标准液滴定,就可以测定样品中
3 4
Fe2+的百分含量。上述过程中所用的酸可以是__________(填字母)。
a.氢碘酸 b.稀硫酸 c.稀硝酸 d.浓盐酸
18.(15 分)FeSO ·7H O 和 Na S O 在医药、印染、食品等方面应用广泛。以黄铁矿为原
4 2 2 2 5
料生产FeSO ·7H O和Na S O 的一种流程如图所示。
4 2 2 2 5
已知:①烧渣的主要成分:铁、铝、硅的氧化物;
②吸收液Ⅰ中的溶质只有NaHSO ,吸收液Ⅲ是NaHSO 的过饱和溶液。
3 3
回答下列问题:
(1)煅烧前黄铁矿要粉碎,其目的是__________。
(2)滤渣Ⅰ的成分是__________(填化学式)。
(3)在“还原”步骤中,发生主要反应的离子方程式为__________。
(4)列举:Na CO 在工业上的用途:__________(填2种即可)。
2 3
(5)得到吸收液Ⅲ所发生的主要反应有 NaHCO +SO NaHSO +CO 、__________
3 2 3 2
(写化学方程式)。
(6)Na S O 可用作食品的抗氧化剂。在测定葡萄酒中Na S O 的残留量时,取80.00mL
2 2 5 2 2 5
葡萄酒样品,往葡萄酒样品中滴入 0.01000 mol·L-1的碘标准液,反应完全后,共消
耗12.00 mL碘标准液。则该样品中Na S O 的残留量为__________mol·L-1(计算结
2 2 5
果用m×10-n形式表示,其中1≤m<10,n为正整数,S O2-+2I +3H O 2SO2-+
2 5 2 2 4
4I-+6H+)。有同学认为,该测定实验可以用酸性KMnO 标准液代替碘标准液进行实验,
4
该同学的观点__________(填“正确”或“错误”),其原因是__________。
6
学科网(北京)股份有限公司