文档内容
试卷类型: A
深圳外国语学校(集团)龙华高中部 2025 届高三年级
第一次月考化学试卷
本试卷共11页,21小题,满分100分。考试用时75分钟。
注意事项:
1. 答卷前,考生务必将自己的姓名、考生号、考场号和座位号填写在答题卡上。用 2B 铅笔将试卷类型(A)填涂在答题卡
相应位置上。将条形码横贴在答题卡右上角“条形码粘贴处”。
2. 作答选择题时,选出每小题答案后,用2B铅笔在答题卡上对应题目选项的答案信息点涂黑;如需改动.用橡皮擦干净后,
再选涂其他答案。答案不能答在试卷上。
3. 非选择题必须用黑色字迹的钢笔或签字笔作答,答案必须写在答题卡各题目指定区域内相应位置上;如需改动,先划掉原
来的答案,然后再写上新答案;不准使用铅笔和涂改液。不按以上要求作答无效。
4. 考生必须保持答题卡的整洁。考试结束后,只需将答题卡交回。
可能用到的相对原子质量:H-1 Na-23 O-16 C-12 Li -7 Na-23 Fe -56 Cu-64 Cl-35.5 S-32
一、选择题(共44分,其中 1~10题,每小题 2分,共20 分;11~16题,每小题4分,共24分。在每小
题给出的四个选项中,只有一项是符合题目要求的。)
1.广东有众多非物质文化遗产,如粤绣、剪纸、制香和藤编技艺等。下列物质的主要成分不是有机高分子
材料的是
选项 A B C D
文化遗产
名称 佛山剪纸中的“纸” 粤绣中的“线” 莞香中的“香油” 南海藤编中的“藤”
2.下列有关化学用语使用正确的是
A.KOH的电子式: B.HClO分子的VSEPR模型:直线形
C.乙烷的空间填充模型: D.基态Fe2+的价层电子排布式:
3.北京冬奥会成功举办、“华龙一号”核电站、神舟十五号载人飞船发射成功及“C919”飞机等,均展示了我
国科技发展的巨大成就。下列相关叙述正确的是
化学试卷 第 1 页 共 11
学科网(北京)股份有限公司A.冬奥会“飞扬”火炬所用的燃料H 为极性分子
2
B.“C919”飞机机身使用的碳纤维材料属于新型无机非金属材料
C.载人飞船采用了太阳能刚性电池阵,将化学能转化为电能供飞船使用
D.“华龙一号”核电站以铀为核裂变原料,235U与238U互为同素异形体
92 92
4.生命活动需要一系列的复杂的化学过程来维持,食物中的营养物质是这些过程的能量基础。下列关于糖
类、油脂、蛋白质的说法正确的是
A.糖类、油脂、蛋白质是人体必需的基本营养物质,在人体内都可以发生水解
B.向蔗糖溶液中加入稀硫酸并加热,再加入新制Cu(OH) 悬浊液,加热,未见砖红色沉淀,则蔗糖不发生
2
水解
C.油脂在酸性条件下水解的反应叫皂化反应
D.农业上用波尔多液(由硫酸铜溶液和石灰乳制成)来防治植物病毒的原理是重金属阳离子和强碱能使蛋白
质发生变性
5.在生产、生活中金属腐蚀所带来的损失非常严重,下列有关金属腐蚀与防护的说法正确的是
A.生铁浸泡在食盐水中会发生析氢腐蚀
B.钢铁发生吸氧腐蚀的正极的电极反应式为O +4e−+2H O=4OH−
2 2
C.在轮船的底部镶嵌不易腐蚀的铜块,可以提高船体的使用寿命,利用了牺牲阳极法
D.将钢铁闸门与电源正极相连的防腐措施属于外加电流法
6.某粗苯甲酸样品中含有少量氯化钠和泥沙,提纯苯甲酸用到的分离提纯方法叫重结晶,在提纯苯甲酸过
程中用到的主要实验操作组合是
A.萃取、分液、过滤 B.蒸馏、分液、结晶
C.加热、蒸馏、结晶 D.溶解、过滤、结晶
7.下列劳动项目与所述的化学知识没有关联的是
劳动项目 化学知识
A 环保行动:用FeS除去废水中的Hg2+ 溶度积:K (FeS)>K (HgS)
sp sp
B 帮厨活动:炖鱼时加入料酒和醋 乙醇和醋酸反应生成有香味的酯
C 医疗消毒:用苯酚水溶液进行环境消毒 苯酚有强氧化性
化学试卷 第 2 页 共 11
学科网(北京)股份有限公司D 学农活动:施肥时铵态氮肥和草木灰不能同时使用 NH+与CO2-在一定条件反应
4 3
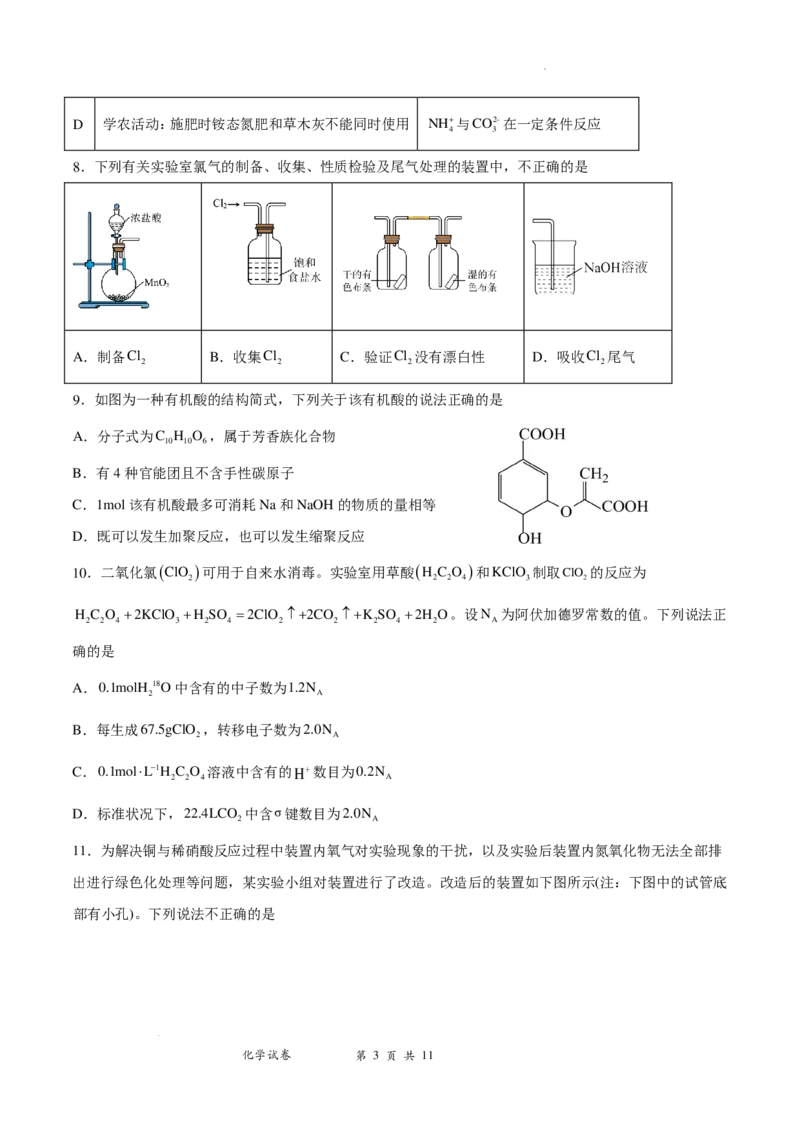
8.下列有关实验室氯气的制备、收集、性质检验及尾气处理的装置中,不正确的是
A.制备Cl B.收集Cl C.验证Cl 没有漂白性 D.吸收Cl 尾气
2 2 2 2
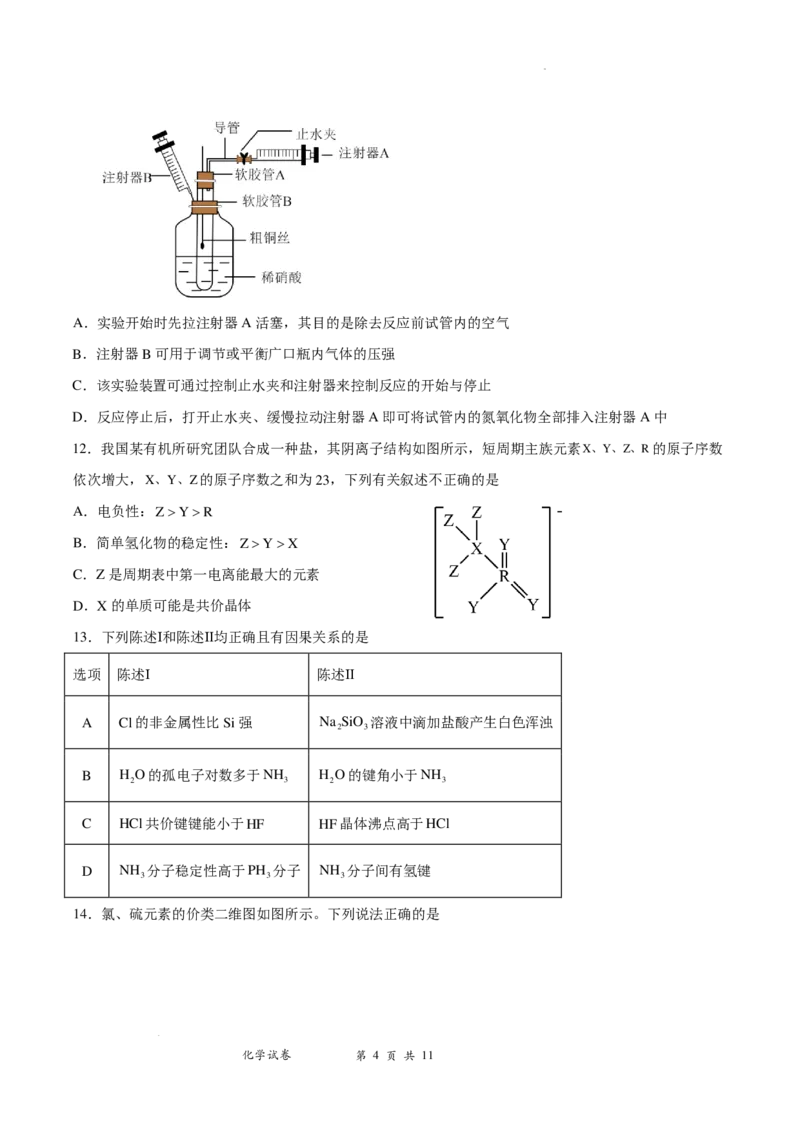
9.如图为一种有机酸的结构简式,下列关于该有机酸的说法正确的是
A.分子式为C H O ,属于芳香族化合物
10 10 6
B.有4种官能团且不含手性碳原子
C.1mol该有机酸最多可消耗Na和NaOH的物质的量相等
D.既可以发生加聚反应,也可以发生缩聚反应
10.二氧化氯(ClO )可用于自来水消毒。实验室用草酸(H C O )和KClO 制取ClO 的反应为
2 2 2 4 3 2
H C O +2KClO +H SO =2ClO ↑+2CO ↑+K SO +2H O。设N 为阿伏加德罗常数的值。下列说法正
2 2 4 3 2 4 2 2 2 4 2 A
确的是
A.0.1molH 18O中含有的中子数为1.2N
2 A
B.每生成67.5gClO ,转移电子数为2.0N
2 A
C.0.1mol⋅L−1H C O 溶液中含有的H+数目为0.2N
2 2 4 A
D.标准状况下,22.4LCO 中含σ键数目为2.0N
2 A
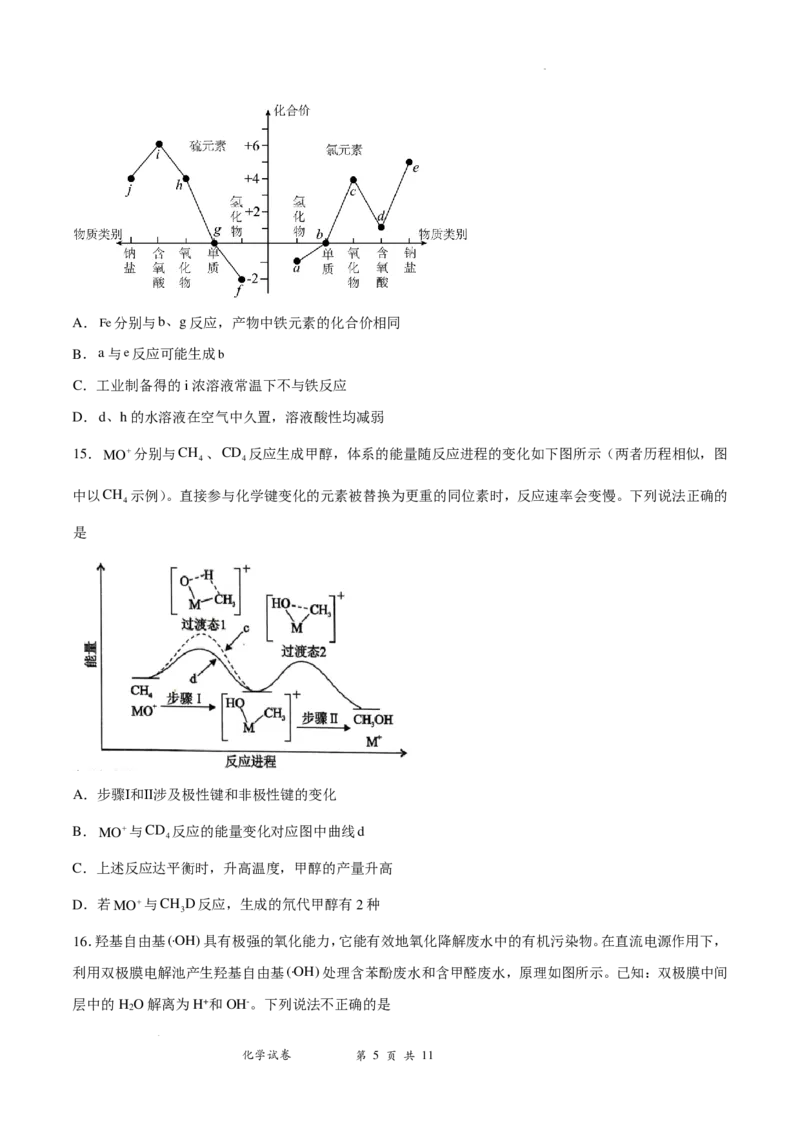
11.为解决铜与稀硝酸反应过程中装置内氧气对实验现象的干扰,以及实验后装置内氮氧化物无法全部排
出进行绿色化处理等问题,某实验小组对装置进行了改造。改造后的装置如下图所示(注:下图中的试管底
部有小孔)。下列说法不正确的是
化学试卷 第 3 页 共 11
学科网(北京)股份有限公司A.实验开始时先拉注射器A活塞,其目的是除去反应前试管内的空气
B.注射器B可用于调节或平衡广口瓶内气体的压强
C.该实验装置可通过控制止水夹和注射器来控制反应的开始与停止
D.反应停止后,打开止水夹、缓慢拉动注射器A即可将试管内的氮氧化物全部排入注射器A中
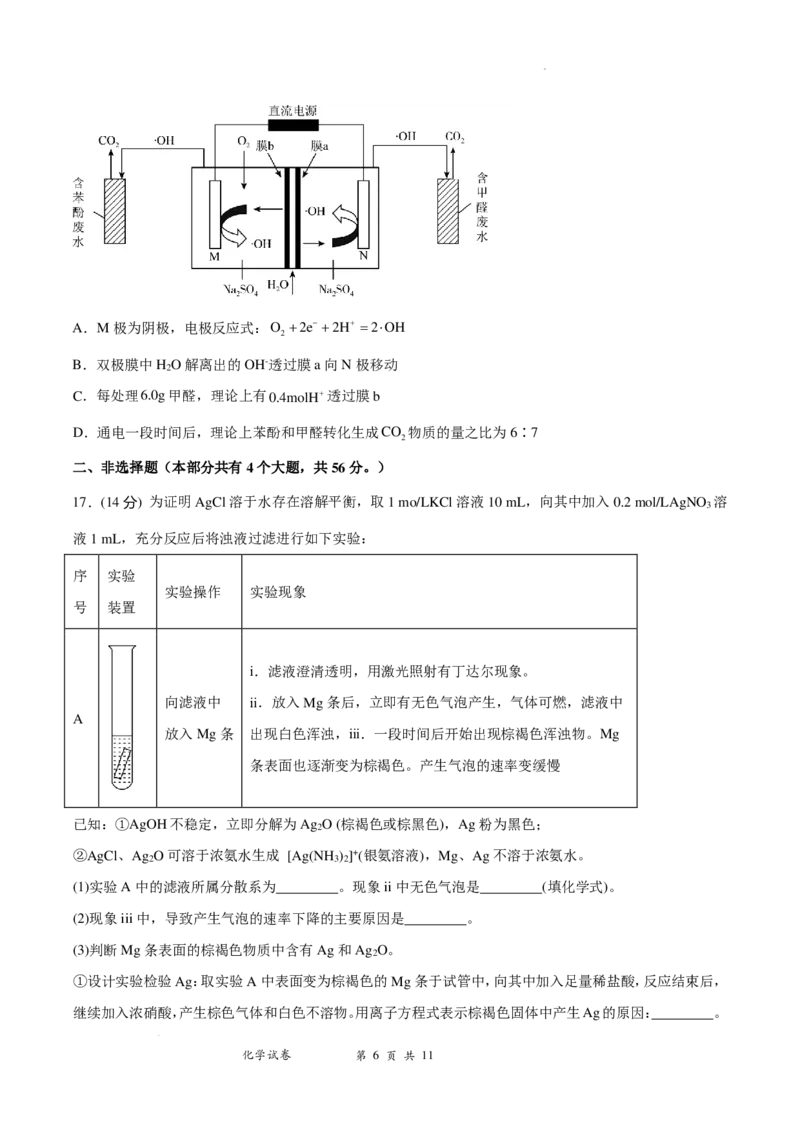
12.我国某有机所研究团队合成一种盐,其阴离子结构如图所示,短周期主族元素X、Y、Z、R的原子序数
依次增大,X、Y、Z的原子序数之和为23,下列有关叙述不正确的是
A.电负性:Z>Y>R
B.简单氢化物的稳定性:Z>Y>X
C.Z是周期表中第一电离能最大的元素
D.X的单质可能是共价晶体
13.下列陈述Ⅰ和陈述Ⅱ均正确且有因果关系的是
选项 陈述Ⅰ 陈述Ⅱ
A Cl的非金属性比Si强 Na SiO 溶液中滴加盐酸产生白色浑浊
2 3
B H O的孤电子对数多于NH H O的键角小于NH
2 3 2 3
C HCl共价键键能小于HF HF晶体沸点高于HCl
D NH 分子稳定性高于PH 分子 NH 分子间有氢键
3 3 3
14.氯、硫元素的价类二维图如图所示。下列说法正确的是
化学试卷 第 4 页 共 11
学科网(北京)股份有限公司A.Fe分别与b、g反应,产物中铁元素的化合价相同
B.a与e反应可能生成b
C.工业制备得的i浓溶液常温下不与铁反应
D.d、h的水溶液在空气中久置,溶液酸性均减弱
15.MO+分别与CH 、CD 反应生成甲醇,体系的能量随反应进程的变化如下图所示(两者历程相似,图
4 4
中以CH 示例)。直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢。下列说法正确的
4
是
A.步骤Ⅰ和Ⅱ涉及极性键和非极性键的变化
B.MO+与CD 反应的能量变化对应图中曲线d
4
C.上述反应达平衡时,升高温度,甲醇的产量升高
D.若MO+与CH D反应,生成的氘代甲醇有2种
3
16.羟基自由基(⋅OH)具有极强的氧化能力,它能有效地氧化降解废水中的有机污染物。在直流电源作用下,
利用双极膜电解池产生羟基自由基(⋅OH)处理含苯酚废水和含甲醛废水,原理如图所示。已知:双极膜中间
层中的H O解离为H+和OH-。下列说法不正确的是
2
化学试卷 第 5 页 共 11
学科网(北京)股份有限公司A.M极为阴极,电极反应式:O +2e−+2H+ =2⋅OH
2
B.双极膜中H O解离出的OH-透过膜a向N极移动
2
C.每处理6.0g甲醛,理论上有0.4molH+透过膜b
D.通电一段时间后,理论上苯酚和甲醛转化生成CO 物质的量之比为6∶7
2
二、非选择题(本部分共有4个大题,共56分。)
17.(14分) 为证明AgCl溶于水存在溶解平衡,取1 mo/LKCl溶液10 mL,向其中加入0.2 mol/LAgNO 溶
3
液1 mL,充分反应后将浊液过滤进行如下实验:
序 实验
实验操作 实验现象
号 装置
ⅰ.滤液澄清透明,用激光照射有丁达尔现象。
向滤液中 ⅱ.放入Mg条后,立即有无色气泡产生,气体可燃,滤液中
A
放入Mg条 出现白色浑浊,ⅲ.一段时间后开始出现棕褐色浑浊物。Mg
条表面也逐渐变为棕褐色。产生气泡的速率变缓慢
已知:①AgOH不稳定,立即分解为Ag O (棕褐色或棕黑色),Ag粉为黑色;
2
②AgCl、Ag O可溶于浓氨水生成 [Ag(NH ) ]+(银氨溶液),Mg、Ag不溶于浓氨水。
2 3 2
(1)实验A中的滤液所属分散系为 。现象ii中无色气泡是 (填化学式)。
(2)现象iii中,导致产生气泡的速率下降的主要原因是 。
(3)判断Mg条表面的棕褐色物质中含有Ag和Ag O。
2
①设计实验检验Ag:取实验A中表面变为棕褐色的Mg条于试管中,向其中加入足量稀盐酸,反应结束后,
继续加入浓硝酸,产生棕色气体和白色不溶物。用离子方程式表示棕褐色固体中产生Ag的原因: 。
化学试卷 第 6 页 共 11
学科网(北京)股份有限公司实验中加入稀盐酸的目的: 。
②设计检验棕褐色物质中有Ag O,实验方案是:取实验A中表面变为棕褐色的Mg条用蒸馏水洗净后,加
2
入 (填化学式)中浸泡,取上层清液于葡萄糖溶液中,水浴加热,若有 (填实验现象),则
证明Ag O存在。
2
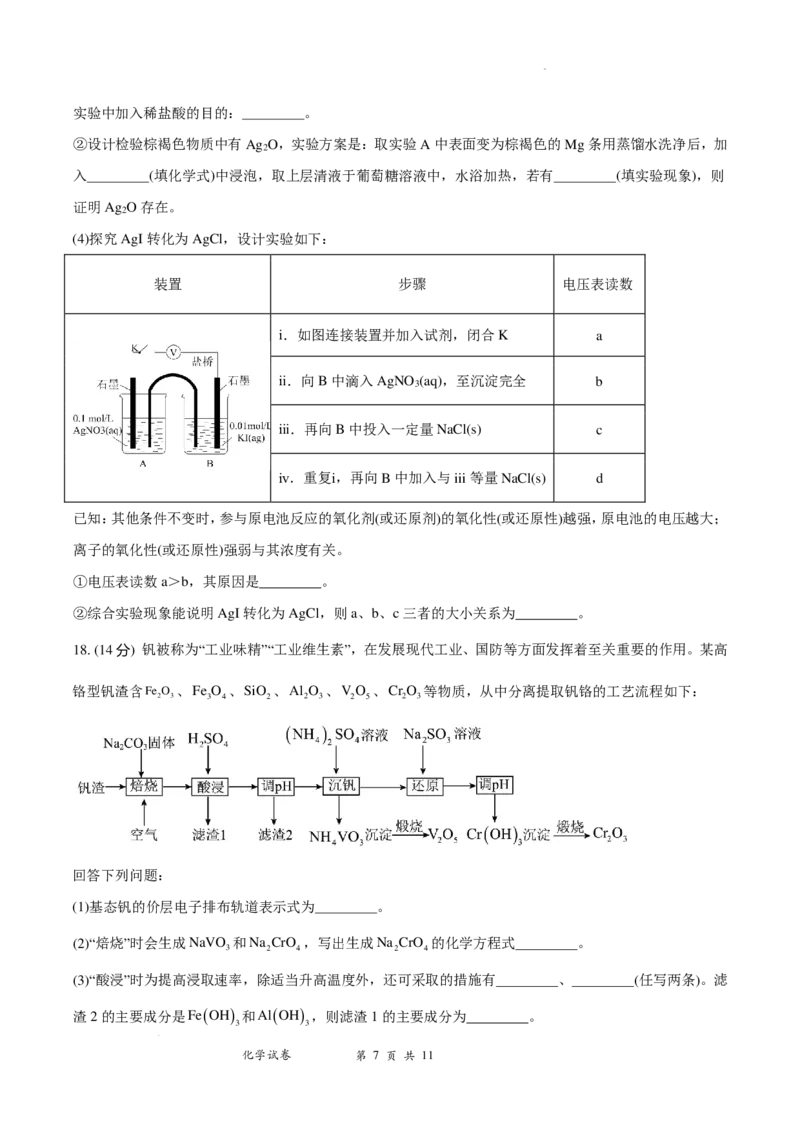
(4)探究AgI转化为AgCl,设计实验如下:
装置 步骤 电压表读数
ⅰ.如图连接装置并加入试剂,闭合K a
ⅱ.向B中滴入AgNO (aq),至沉淀完全 b
3
ⅲ.再向B中投入一定量NaCl(s) c
ⅳ.重复ⅰ,再向B中加入与iii等量NaCl(s) d
已知:其他条件不变时,参与原电池反应的氧化剂(或还原剂)的氧化性(或还原性)越强,原电池的电压越大;
离子的氧化性(或还原性)强弱与其浓度有关。
①电压表读数a>b,其原因是 。
②综合实验现象能说明AgI转化为AgCl,则a、b、c三者的大小关系为 。
18. (14分) 钒被称为“工业味精”“工业维生素”,在发展现代工业、国防等方面发挥着至关重要的作用。某高
铬型钒渣含Fe O 、Fe O 、SiO 、Al O 、VO 、CrO 等物质,从中分离提取钒铬的工艺流程如下:
2 3 3 4 2 2 3 2 5 2 3
回答下列问题:
(1)基态钒的价层电子排布轨道表示式为 。
(2)“焙烧”时会生成NaVO 和Na CrO ,写出生成Na CrO 的化学方程式 。
3 2 4 2 4
(3)“酸浸”时为提高浸取速率,除适当升高温度外,还可采取的措施有 、 (任写两条)。滤
渣2的主要成分是Fe(OH) 和Al(OH) ,则滤渣1的主要成分为 。
3 3
化学试卷 第 7 页 共 11
学科网(北京)股份有限公司(4)“还原”时可用双氧水代替Na SO 溶液作还原剂,此时溶液中的CrO2−发生反应的离子方程式
2 3 2 7
为 。
(5)工业上可用电解还原法处理含CrO2−的酸性废水。用铁板作阳极,电解过程中废水pH逐渐上升,Cr3+、
2 7
Fe3+都以氢氧化物沉淀析出,达到废水净化的目的。其中阳极的电极反应式为 。
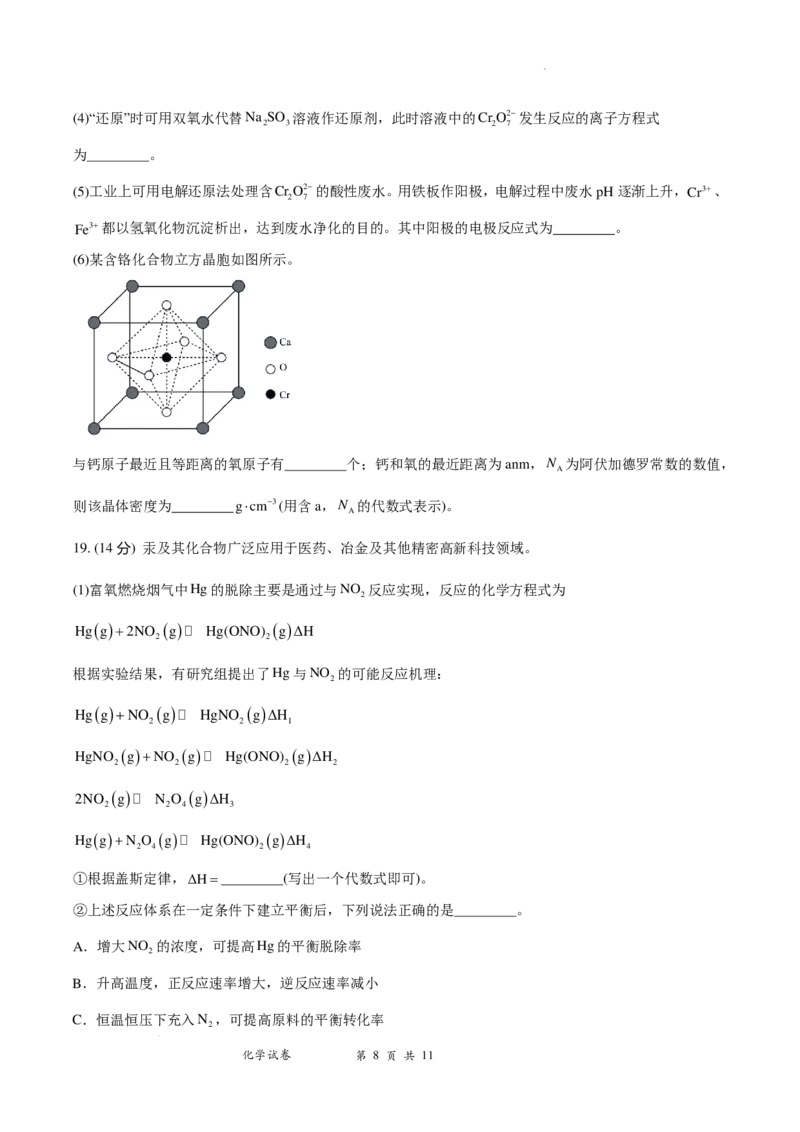
(6)某含铬化合物立方晶胞如图所示。
与钙原子最近且等距离的氧原子有 个;钙和氧的最近距离为anm,N 为阿伏加德罗常数的数值,
A
则该晶体密度为 g⋅cm−3(用含a,N 的代数式表示)。
A
19. (14分) 汞及其化合物广泛应用于医药、冶金及其他精密高新科技领域。
(1)富氧燃烧烟气中Hg的脱除主要是通过与NO 反应实现,反应的化学方程式为
2
Hg(g)+2NO (g) Hg(ONO) (g)ΔH
2 2
根据实验结果,有研究组提出了Hg与NO 的可能反应机理:
2
Hg(g)+NO (g) HgNO (g)ΔH
2 2 1
HgNO (g)+NO (g) Hg(ONO) (g)ΔH
2 2 2 2
2NO (g) N O (g)ΔH
2 2 4 3
Hg(g)+N O (g) Hg(ONO) (g)ΔH
2 4 2 4
①根据盖斯定律,ΔH= (写出一个代数式即可)。
②上述反应体系在一定条件下建立平衡后,下列说法正确的是 。
A.增大NO 的浓度,可提高Hg的平衡脱除率
2
B.升高温度,正反应速率增大,逆反应速率减小
C.恒温恒压下充入N ,可提高原料的平衡转化率
2
化学试卷 第 8 页 共 11
学科网(北京)股份有限公司D.加入催化剂,可降低反应活化能,提高脱除速率
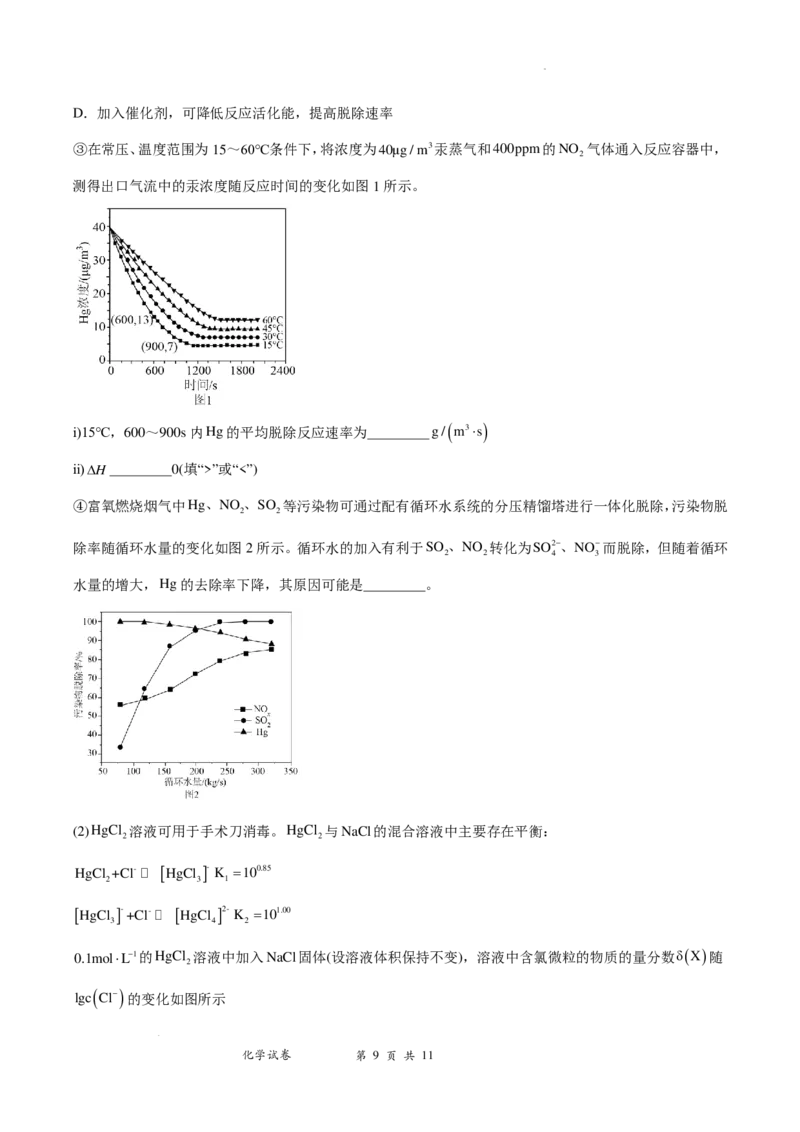
③在常压、温度范围为15~60℃条件下,将浓度为40μg/m3汞蒸气和400ppm的NO 气体通入反应容器中,
2
测得出口气流中的汞浓度随反应时间的变化如图1所示。
ⅰ)15℃,600~900s内Hg的平均脱除反应速率为 g/ ( m3⋅s )
ⅱ)∆H 0(填“>”或“<”)
④富氧燃烧烟气中Hg、NO、SO 等污染物可通过配有循环水系统的分压精馏塔进行一体化脱除,污染物脱
2 2
除率随循环水量的变化如图2所示。循环水的加入有利于SO、NO 转化为SO2−、NO−而脱除,但随着循环
2 2 4 3
水量的增大,Hg的去除率下降,其原因可能是 。
(2)HgCl 溶液可用于手术刀消毒。HgCl 与NaCl的混合溶液中主要存在平衡:
2 2
HgCl +Cl- [HgCl ]- K =100.85
2 3 1
[HgCl ]- +Cl- [HgCl ]2- K =101.00
3 4 2
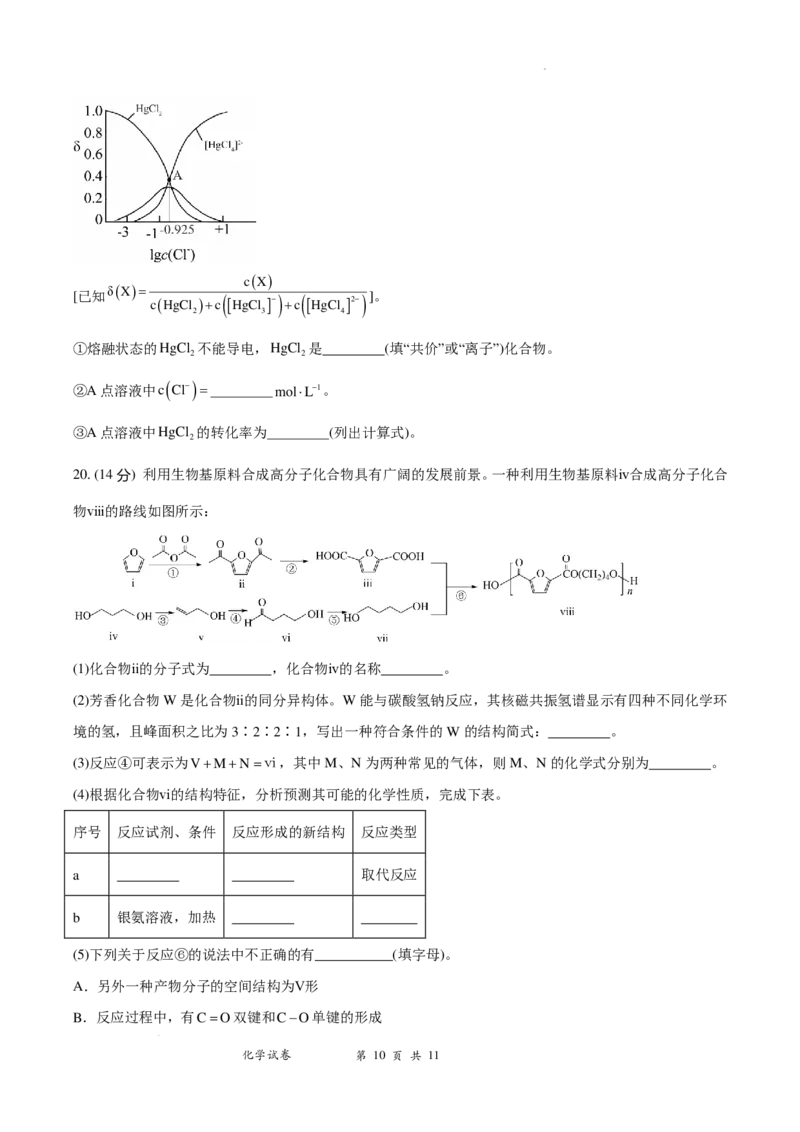
0.1mol⋅L−1的HgCl 溶液中加入NaCl固体(设溶液体积保持不变),溶液中含氯微粒的物质的量分数δ(X)随
2
lgc
( Cl−)
的变化如图所示
化学试卷 第 9 页 共 11
学科网(北京)股份有限公司c(X)
[已知δ(X)=
c(HgCl )+c
(
[HgCl
]−)
+c
(
[HgCl
]2−)]。
2 3 4
①熔融状态的HgCl 不能导电,HgCl 是 (填“共价”或“离子”)化合物。
2 2
②A点溶液中c
( Cl−)
= mol⋅L−1。
③A点溶液中HgCl 的转化率为 (列出计算式)。
2
20. (14分) 利用生物基原料合成高分子化合物具有广阔的发展前景。一种利用生物基原料ⅳ合成高分子化合
物ⅷ的路线如图所示:
(1)化合物ⅱ的分子式为 ,化合物ⅳ的名称 。
(2)芳香化合物W是化合物ⅱ的同分异构体。W能与碳酸氢钠反应,其核磁共振氢谱显示有四种不同化学环
境的氢,且峰面积之比为3∶2∶2∶1,写出一种符合条件的W的结构简式: 。
(3)反应④可表示为V+M+N=ⅵ,其中M、N为两种常见的气体,则M、N的化学式分别为 。
(4)根据化合物ⅵ的结构特征,分析预测其可能的化学性质,完成下表。
序号 反应试剂、条件 反应形成的新结构 反应类型
a 取代反应
b 银氨溶液,加热
(5)下列关于反应⑥的说法中不正确的有___________(填字母)。
A.另外一种产物分子的空间结构为Ⅴ形
B.反应过程中,有C=O双键和C−O单键的形成
化学试卷 第 10 页 共 11
学科网(北京)股份有限公司C.化合物ⅲ中碳原子均为sp2杂化,化合物ⅶ 中碳原子均为sp3杂化
D.化合物ⅷ 中存在手性碳原子
(6)以乙烯为有机含碳原料,利用上述流程中反应④的原理,合成化合物 。基于你设计的合
成路线,回答下列问题:
(a)利用反应④的原理得到的产物的结构简式为 。
(b)相关步骤涉及卤代烃的水解反应,其化学方程式为 (注明反应的条件)。
化学试卷 第 11 页 共 11
学科网(北京)股份有限公司