文档内容
化学试卷
本试卷满分100分,考试用时75分钟。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1.贝壳的无机成分主要是 ,下列说法错误的是( )
A.金刚石和石墨互为同素异形体
B.基态 原子的价层电子排布式为
C. 和 互为同位素
D.氧原子的 能级轨道数为3
2.现代生活离不开方便实用的化学电源,下列装置能产生电流的是( )
A. B. C. D.
3.工业上处理废水时, 和 均可用于除去废水中的 ,下列说法错误的是( )
A.氧化性:
B. 溶液中,
C. 在水中的电离方程式为
D. 在水中存在沉淀溶解平衡:
4.丁二酮肟常用于检验 ,在稀氨水介质中,丁二酮肟与 反应可生成鲜红色沉淀(M), 的结
构如图所示,下列说法正确的是( )A.电负性: B.原子半径:
C. 中含有 键 D. 位于元素周期表第四周期第ⅦB族
5.下列说法错误的是( )
A.锅炉内壁安装若干锌块——牺牲阳极法保护锅炉内壁
B.精炼粗铜时,粗铜通常与电源的负极相连
C.钢铁在酸性条件下易发生析氢腐蚀
D.氯碱工业中,阳极的产物主要为氯气
6.马日夫盐 是一种白色晶体,易溶于水,常用于机械设备的磷化处理。下列说法
正确的是( )
A.红磷转化为白磷属于物理变化 B.沸点:
C.离子半径: D. 的空间结构:正四面体形
7.关于可逆反应 ,下列关于示意图的解释与图像相符的是
( )
B. 时刻改变的条件为升高 C. 可表示平衡时 的质
D.②表示加入了催
A. 化剂
温度 量分数
A.A B.B C.C D.D
8.化学是一门以实验为基础的学科,下列叙述与图示相符的是( )
A.外加电流法保护钢闸门 B.探究吸氧腐蚀
C.铁片上镀铜 D.检验试管中溶液是否含有9.甲醇是重要的化工原料,应用前景广阔。研究表明,二氧化碳与氢气反应可以合成甲醇。在某一密闭容
器中,充入一定量的 和 ,发生的反应为 ,
下列说法错误的是( )
A. 甲醇在纯 中燃烧时,最多可消耗
B.第一电离能:
C. 元素不能形成 的原因:共价键具有饱和性
D.混合气体的总质量不再发生改变,不能用来判断该反应达到平衡状态
10.足量铁粉与盐酸反应,下列措施能加快该反应速率且不影响产生的氢气的量的是( )
①适当加热 ②加入少量 ③加入少量铜粉 ④加入 的硝酸溶液 ⑤通入HCl气体
⑥加入少量醋酸 ⑦将铁粉改为铁片
A.①②③ B.②③④ C.③④⑤ D.⑤⑥⑦
11.已知:常温下, 。常温下, 在
某溶液中形成饱和溶液时, ,则该溶液的 为( )
A. B. C. D.
12.X、Y、Z、W、R为五种原子序数依次增大的短周期主族元素。X元素的一种核素中质子数与质量数在
数值上相等; 的单质分子中有三对共用电子;Z、W同主族,且核电荷数之比为 。下列说法错误的
是( )
A. 可用作自来水的消毒剂
B.仅由X、Y、R也能形成离子化合物
C.将 缓慢通过 溶液,充分反应后,溶液的 减小
D.XR与 混合时会产生白色烟雾
13.常温下,用含少量 的 溶液制备 的过程如图所示,下列说法错误的是( )已知:常温下, , , 。
A.反应 的平衡常数为0.3
B.常温下, 的 溶液中,
C.常温下, 的 溶液中,
D.“沉锰”时,发生反应的离子方程式为
14.全钒液流电池是一种以钒为活性物质呈循环流动液态的氧化还原电池,其充电时工作原理如图所示。下
列说法正确的是( )
A.充电时,电极a与电源的正极相连,发生还原反应
B.放电时总反应为
C.充电一段时间后,右侧电解液的 降低
D.放电时,电路中转移 ,则有 由右侧移向左侧
15.常温下,用 溶液分别滴定 浓度均为 的 溶液和
溶液,所得滴定曲线如图所示。下列说法错误的是( )
已知: , 。A.常温下, 溶液中,
B.常温下,
C. 的过程中,溶液中水的电离程度一直增大
D.常温下, 溶液中,
二、非选择题:本题共4小题,共55分。
16.(14分)高氯酸三碳酰肼合镍 是一种新型的起爆药,回答下列问题:
(1)基态氯原子的简化电子排布式为_____。
(2)基态氧原子核外电子云有_____种不同的伸展方向。
(3) 的中心原子的价层电子对数为_____, 的VSEPR模型是_____。
(4)化学式中的 为碳酰肼,其结构为 ,是一种新型的环保锅炉水除氧剂:
①CHZ中氮原子的杂化轨道类型为_____。
② 中含有的 键数目为_____ 。
③键角: _____(填“>”“<”或“=”) 。
(5)常温下, 的 溶液的 约为_____[已知: , ]。
17.(13分)硫及其化合物与生产、生活及环境息息相关。回答下列问题:
(1) 和氮的氧化物的大量排放会导致酸雨,它们的主要来源是煤和石油的燃烧。酸雨可导致的危害
有_____(填标号)。
A.腐蚀建筑物 B.使树木枯萎 C.土壤碱化 D.恶化人类环境
为了减少硫酸型酸雨的形成,必须减少 的排放量,可对燃料中的硫化物进行_____(填一种措施)。
(2)石油炼制过程中产生的大量 废气的去除方法如图,该方法对 的去除率可达99%以上。“吸收 ”步骤的反应的离子方程式为_________________________。
(3)某化学学习小组设计如图所示的实验装置,测定工业原料气(含 、 、 )中 的含
量。
①写出装置A中发生反应的离子方程式:_______________。
当装置A中出现__________(填现象)时,立即停止通气。
②可用来代替A中碘的淀粉溶液且能达到实验目的的最合适的试剂是_____(填标号),此时A中发生反
应的离子方程式为____________________。
A.酸性 溶液 B. 溶液 C. 溶液
③若 中碘的淀粉溶液体积为 ,其中碘的浓度为 ,收集到的 与 的体积共
(已折算为标准状况下的体积),则该工业原料气中 的含量是_____ 。(忽略气体
在水中的溶解)
18.(14分)磁选后的炼铁高钛炉渣,主要成分有 、 、 、 、 以及少量的
。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
常温下,有关金属离子开始沉淀和沉淀完全的 见下表:
金属离子
开始沉淀的 1.5 3.4 8.9 12.0金属离子
沉淀完全( )的 2.8 4.7 10.9 13.8
已知:①常温下, ;
②“水浸”后的 约为2.0,在“分步沉淀”时用氨水逐步调节 至11.6;
③“焙烧”中, 、 几乎不发生反应, 、 、 、 转化为相应的硫酸盐。
回答下列问题:
(1)“焙烧”时,常将高钛炉渣粉碎的目的是_____。
(2)“焙烧”时, 与 反应转化为 :
①常温下, 的 溶液中, _____(填“>”“<”或“=”)
。
②常温下, 的 溶液中, _____(填“>”“<”或“=”) 。
③工业上电解熔融的 制 时,常加入冰晶石 ,其作用为_____。
(3)检验 时,可加入 溶液,观察到的现象为_____,此时发生反应的离子方程式为
_____。
(4)利用表中数据,可计算出 _____。
(5)“酸溶”后,将溶液适当稀释并加热, 水解析出 沉淀,该反应的离子方程式为
_____。
19.(14分)甲烷在工业上有很多用途,利用甲烷催化还原 消除氮氧化物的污染的反应如下:
ⅰ. ;
ⅱ. ;
ⅲ. 。
回答下列问题:
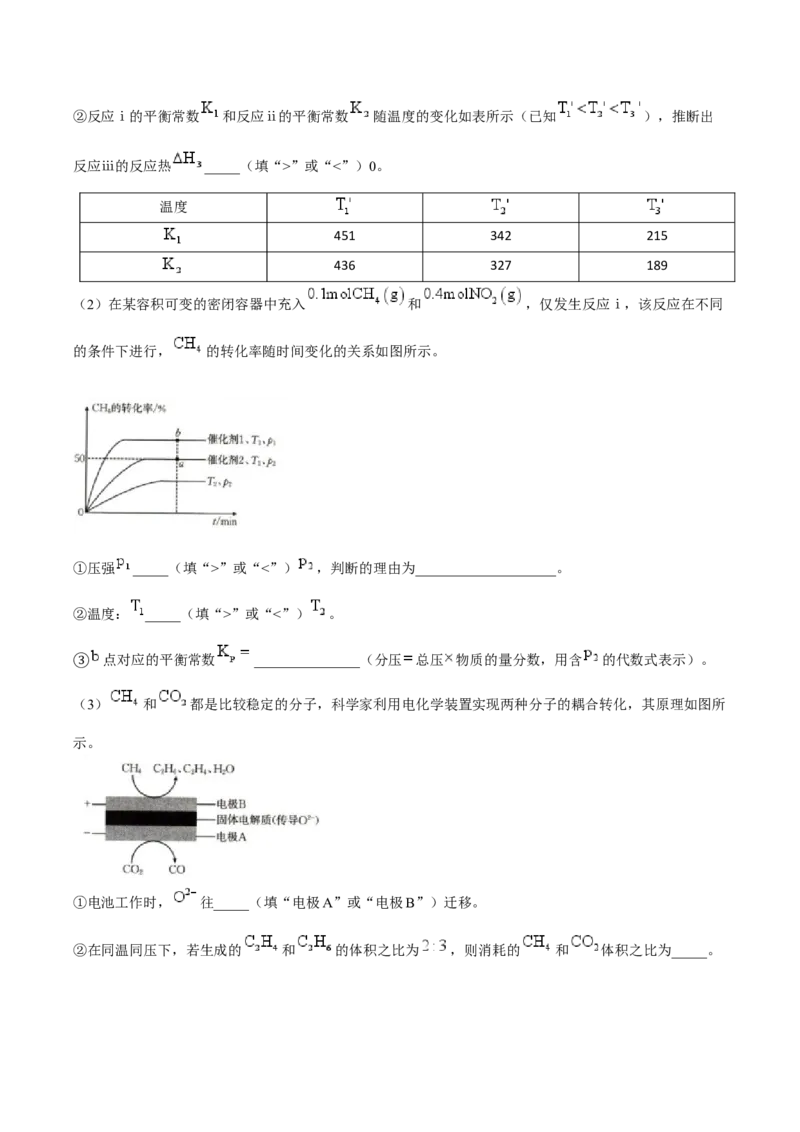
(1)① _____(用含 、 的代数式表示)。②反应ⅰ的平衡常数 和反应ⅱ的平衡常数 随温度的变化如表所示(已知 ),推断出
反应ⅲ的反应热 _____(填“>”或“<”)0。
温度
451 342 215
436 327 189
(2)在某容积可变的密闭容器中充入 和 ,仅发生反应ⅰ,该反应在不同
的条件下进行, 的转化率随时间变化的关系如图所示。
①压强 _____(填“>”或“<”) ,判断的理由为____________________。
②温度: _____(填“>”或“<”) 。
点对应的平衡常数 _______________(分压 总压 物质的量分数,用含 的代数式表示)。
③
(3) 和 都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图所
示。
①电池工作时, 往_____(填“电极A”或“电极B”)迁移。
②在同温同压下,若生成的 和 的体积之比为 ,则消耗的 和 体积之比为_____。化学试卷参考答案
1.B【解析】基态 原子的价层电子排布式为 ,B项错误。
2.C【解析】没有形成闭合回路且不会发生氧化还原反应,A项不符合题意;两电极未区分活动性,B项不
符合题意;无水乙醇不是电解质溶液,D项不符合题意。
3.A【解析】氧化性为 ,A项错误。
4.C【解析】电负性: ,A项错误;原子半径: ,B项错误。
5.B【解析】精炼粗铜时,粗铜通常与电源的正极相连,B项错误。
6.D【解析】沸点: ,B项错误;离子半径: ,C项错误。
7.C【解析】 ,A项不符合题意;升高温度,正、逆反应速率都要增大,B项不符合题意;加入催
化剂反应速率加快,①表示加入了催化剂,D项不符合题意。
8.C【解析】牺牲阳极法,A项不符合题意;不是密封装置,B项不符合题意;应用 溶液检
验 ,D项不符合题意。
9.B【解析】第一电离能: ,B项错误。
10.A【解析】加入硝酸溶液、通入 气体、加入少量醋酸均会影响生成的氢气的量,将铁粉改为铁片会
减慢反应速率,A项符合题意。
11.D【解析】由 ,可得 ,则 ,即 ,D项符
合题意。
12.D【解析】依题意可知,X、Y、Z、W、R分别为H、N、O、S、Cl。HCl和 混合时会产生白烟,
D项错误。
13.A【解析】反应 的平衡常数为 ,A项错误。
14.C
15.D【解析】常温下, 溶液中, ,D项错
误。16.(1) (2分) (2)4(1分) (3)4(2分);正四面体形(2分)
(4)① (2分) ②11(2分) ③=(1分)
(5)4.7(2分)
【解析】(5) ,则
,则 。
17.(1)ABD(对2个得1分,选错不得分,2分);脱硫处理(1分)
(2) (2分)
(3)① (2分);溶液由蓝色恰好变成无色(1分)
②A(1分); (2分)
③200(2分)
【解析】(3)② 也能被酸性 溶液氧化且有明显的实验现象; 与 不反应;
溶液能消耗 ,但无明显实验现象,故选择A(酸性 溶液)。
③由条件知 ,即 的体积为 (已折算为
标准状况下的体积),所以工业原料气总体积为 ,其中 的质量为
,故 的含量为 。
18.(1)增大接触面积,加快“焙烧”速率,提高原料的利用率(2分)
(2)①=(1分) ② (1分) ③降低 的熔点,节约能源(2分)
>
(3)出现蓝色沉淀(2分); (2分)(4) (2分)
(5) (2分)
【解析】(2)②由表中数据可得 ,则 ,同
理可求得 , 水解程度更小,故 。
19.(1)① (2分) ② (1分)
<
(2)①<(2分);该反应为气体分子数增加的反应,降低压强,有利于该反应正向进行,可提高 的
平衡转化率(2分) ② (2分) ③ (2分)
<
(3)①电极B(1分) ②10:7(2分)
【解析】(2)③根据温度不变,平衡常数相等,再利用“三段法”结合 点对应的转化率可知:
平衡时混合气体总物质的量为 ,混合气体中气体的分压为 、
、 、 、 ,再代入平衡
常数表达式可得 。(3)②利用电子得失守恒可得, 转化为 和 ,转移的电子数为 ,则
转化为 时转移的电子数为 ,即 ,再利用碳原子个数相等,可求得
,综上所述,消耗的 和 的体积之比为 。