文档内容
抚顺一中 2024-2025 学年度高二年级下学期期初测试化学试卷
可能用到的原子量:C-12 O-16 Na-23 Si-28 P-31 S-32 K-39
第Ⅰ卷
一、单选题(每题3分,共45分)
1.化学处处呈现美。下列有关说法正确的是
A.CO 分子呈现完美对称,为V形结构
2
B.NaCl焰色试验为黄色,与氯原子的电子跃迁有关
C.冰雪融化时需要破坏氢键和范德华力
D.镁条燃烧发出耀眼的白光,只将化学能转化为光能
2.总共含有6个能级的能层符号为
A.M B.N C.P D.Q
催化剂
3.工业制硝酸转化器中发生反应:4NH +5O 4NO+6H O。下列说法正确的是
3 2 2
Δ
A.半径大小:r(N)<r(O)
B.电离能大小:I (N)<I (O)
1 1
C.电负性大小:χ(N)<χ(O)
D.热稳定性:H O<NH
2 3
4.分析下列各物质的性质,判断其固态属于共价晶体的是
A.固态时或熔融后易导电,熔点在1000℃左右
B.黄色晶体,熔点2200℃,熔融态不导电
C.选择性良好的氟化试剂,在室温下易升华
D.无色晶体,沸点2980℃,固态不导电,熔融态能导电
5.硒被誉为人体微量元素的“抗癌之王”。下列有关硒的说法正确的是
A.基态硒原子价电子层有2个未成对电子
B.基态硒原子电子排布式为[Ar]4s24p4
C.基态硒的原子半径大于砷
H SeO
D.硒的最高价氧化物对应的水化物为 2 3
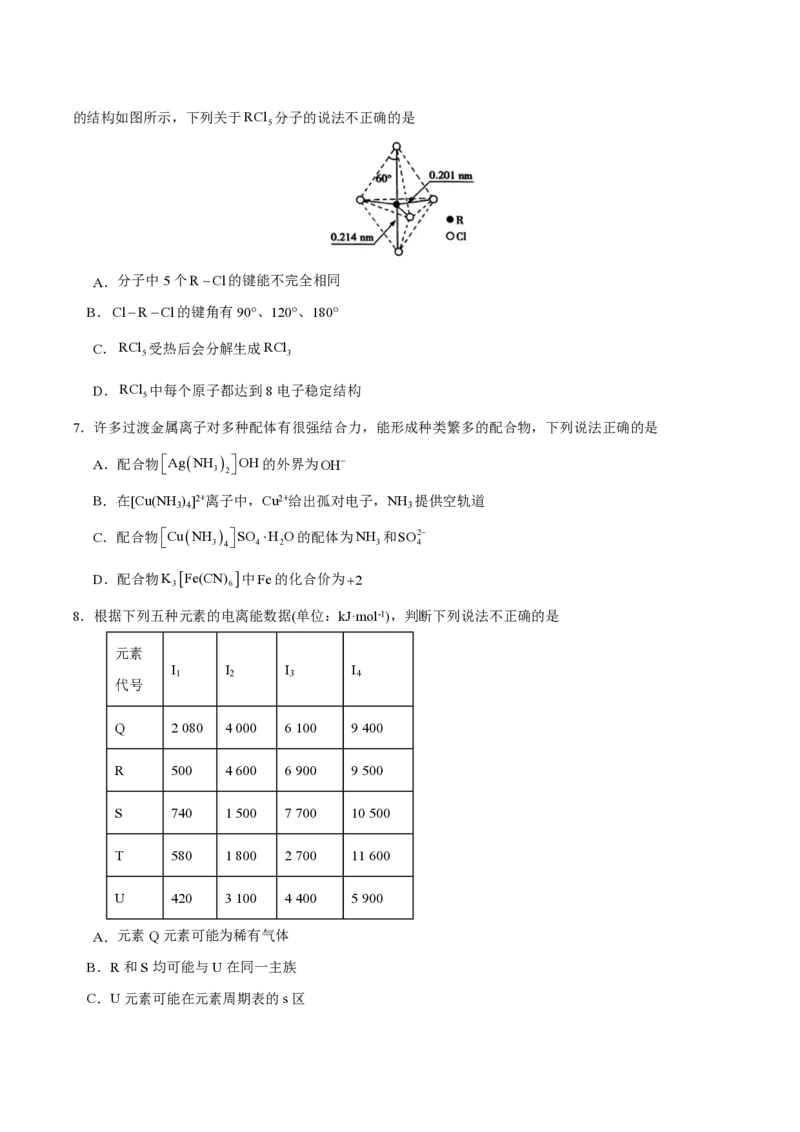
6.第ⅤA族元素的原子R与A原子结合形成RA 气态分子,其空间结构呈三角锥形。RCl 在气态和液态时
3 5的结构如图所示,下列关于RCl 分子的说法不正确的是
5
A.分子中5个RCl的键能不完全相同
B.ClRCl的键角有90°、120°、180°
C.RCl 受热后会分解生成RCl
5 3
D.RCl 中每个原子都达到8电子稳定结构
5
7.许多过渡金属离子对多种配体有很强结合力,能形成种类繁多的配合物,下列说法正确的是
A.配合物
AgNH
3
2
OH的外界为OH
B.在[Cu(NH ) ]2+离子中,Cu2+给出孤对电子,NH 提供空轨道
3 4 3
C.配合物
CuNH
3
4
SO
4
H
2
O的配体为NH
3
和SO2
4
D.配合物K Fe(CN) 中Fe的化合价为2
3 6
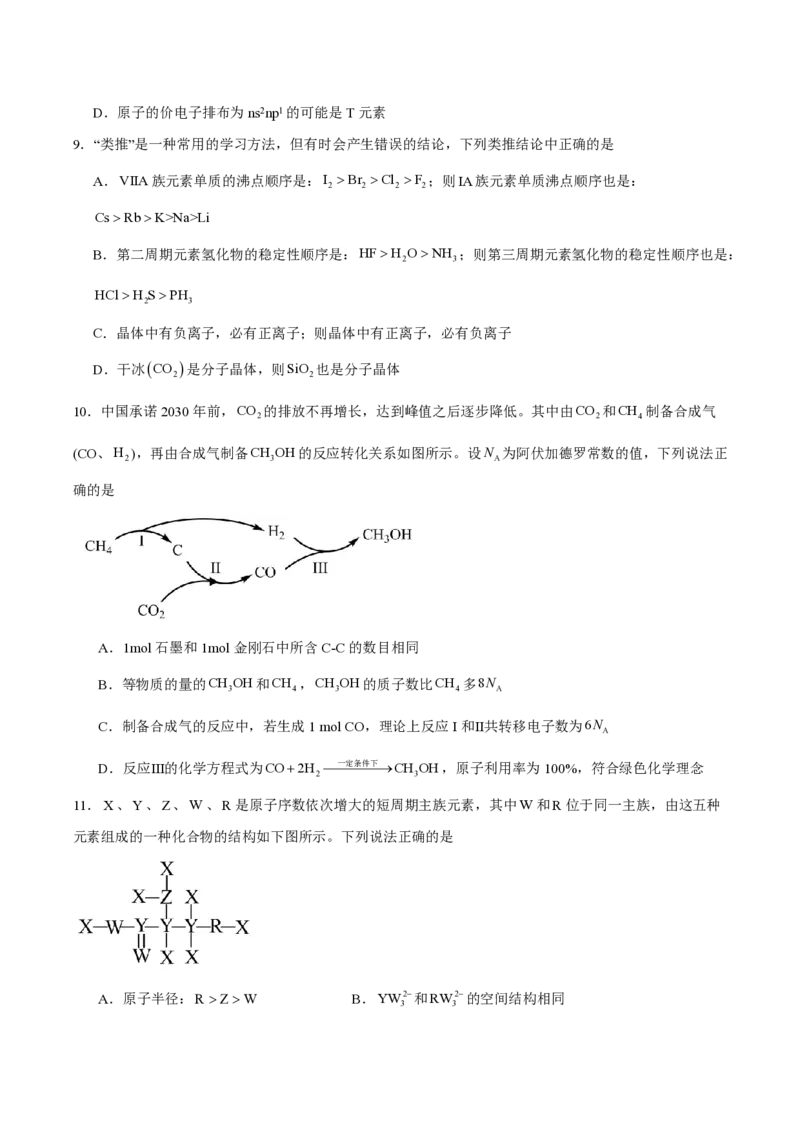
8.根据下列五种元素的电离能数据(单位:kJ·mol-1),判断下列说法不正确的是
元素
I I I I
1 2 3 4
代号
Q 2 080 4 000 6 100 9 400
R 500 4 600 6 900 9 500
S 740 1 500 7 700 10 500
T 580 1 800 2 700 11 600
U 420 3 100 4 400 5 900
A.元素Q元素可能为稀有气体
B.R和S均可能与U在同一主族
C.U元素可能在元素周期表的s区D.原子的价电子排布为ns2np1的可能是T元素
9.“类推”是一种常用的学习方法,但有时会产生错误的结论,下列类推结论中正确的是
A.VIIA族元素单质的沸点顺序是:I Br Cl F ;则IA族元素单质沸点顺序也是:
2 2 2 2
CsRbK>Na>Li
B.第二周期元素氢化物的稳定性顺序是:HFH ONH ;则第三周期元素氢化物的稳定性顺序也是:
2 3
HClH SPH
2 3
C.晶体中有负离子,必有正离子;则晶体中有正离子,必有负离子
D.干冰CO 是分子晶体,则SiO 也是分子晶体
2 2
10.中国承诺2030年前,CO 的排放不再增长,达到峰值之后逐步降低。其中由CO 和CH 制备合成气
2 2 4
(CO、H ),再由合成气制备CH OH的反应转化关系如图所示。设N 为阿伏加德罗常数的值,下列说法正
2 3 A
确的是
A.1mol石墨和1mol金刚石中所含C-C的数目相同
B.等物质的量的CH OH和CH ,CH OH的质子数比CH 多8N
3 4 3 4 A
C.制备合成气的反应中,若生成1 mol CO,理论上反应I和Ⅱ共转移电子数为6N
A
D.反应Ⅲ的化学方程式为CO2H 一定条件下CH OH,原子利用率为100%,符合绿色化学理念
2 3
11.X、Y、Z、W、R是原子序数依次增大的短周期主族元素,其中W和R位于同一主族,由这五种
元素组成的一种化合物的结构如下图所示。下列说法正确的是
A.原子半径:R ZW B.YW2和RW2的空间结构相同
3 3C.简单氢化物的沸点:YZW D.第一电离能:YZW
12.物质结构决定物质性质。下列性质差异与结构因素匹配错误的是
选项 性质差异 结构因素
A 正戊烷的沸点高于新戊烷 正戊烷分子极性大于新戊烷,范德华力强
B 金刚石的熔点高于C 金刚石为共价晶体,C 为分子晶体
60 60
C 三氟乙酸的Ka大于三氯乙酸的Ka F电负性大于Cl,三氟乙酸O-H键极性强
D Cl 在水中的溶解度大于CO Cl 为非极性分子,CO为极性分子
2 2
13.下列说法正确的是(N 为阿伏伽德罗常数)
A
A.124 g P 含有P—P键的个数为4N
4 A
B.12 g石墨中含有C—C键的个数为1.5N
A
C.28 g晶体硅中含有Si—Si键的个数为4N
A
D.78g Na O 晶体中含离子的个数为4N
2 2 A
14.软硬酸碱理论认为,常见的硬酸有Li、Be2、Fe3等,软酸有Ag、Hg2、Cs等;硬碱有F、NH
3
等,软碱有I、CN等;酸碱结合的原则为:“硬酸优先与硬碱结合,软酸优先与软碱结合,软和硬结合一
般不稳定”。该原则一般可用于判断物质稳定性及反应发生的方向等。下列叙述正确的是
A.稳定性比较:CsCNLiCN
B.稳定性比较:AgNH Ag(CN)
3 2 2
C.反应LiICsFLiFCsI难以向右进行
D.含FeSCN 3的红色溶液中加入适量NaF后溶液褪色,说明碱的“硬度”:F SCN
6
15.我国古代四大发明之一的黑火药爆炸时发生的反应为2KNO +S+3C=K S+N ↑+3CO ↑。生成物K S的晶
3 2 2 2 2
体结构如图。下列有关说法错误的是
A.反应产物中有两种非极性分子B.1mol CO 和1mol N 含有的π键数目之比为1:1
2 2
C.K S晶体中阴离子周围最近的阳离子有4个
2
4.41023
D.若K S晶体的晶胞边长为a nm,则该晶体的密度为 g·cm-3
2 a3N
A
第Ⅱ卷
二、非选择题(共55分)
16.(17分)近年来我国科学家发现了一系列意义重大的铁系超导材料,其中一类为Fe-Sm-As-F-O组成的
化合物。回答下列问题:
(1)元素As与N同主族。预测As的氢化物分子的立体结构为 ,其沸点比NH 的 (填“高”
3
或“低”),其判断理由是 。
(2)Fe成为阳离子时首先失去 轨道电子,Sm的价层电子排布式为4f66s2,Sm3+的价层电子排布式
为 。
(3)比较离子半径:F- O2-(填“大于”“等于”或“小于”)。
(4)磷酸亚铁锂(LiFePO )可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点,
4
文献报道可采用FeCl 、NH H PO 、LiCl和苯胺等作为原料制备。
3 4 2 4
①在周期表中,与Li的化学性质最相似的邻族元素是 (元素名称),该元素基态原子核外M层电
子的自旋状态 (填“相同”或“相反”)。
②NH H PO 中,电负性最高的元素是 ,P的 杂化轨道与O的2p轨道形成
4 2 4
键。
17.(14分)铜是人类最早使用的金属之一,最近科学家发现Cu元素有很强的杀菌作用,还可代替Al布
线在硅芯片上。用黄铜矿(主要成分为CuFeS )生产粗铜,其反应原理如下:
2
CuFeS O 2Cu SO2 ΔCu 2 SΔCu
2 800℃ 2 ① ②
回答下列问题:
(1)基态Cu原子的价层电子排布式为 。Cu O的熔点 Cu S的熔点(填写“<”、“>”或
2 2
“=”)。
(2)反应①、②中生成的气体SO ,分子的空间结构为 。
2
(3)Cu2+能与NH 形成配位数为4的配合物,向CuSO 溶液中加入氨水,最终形成配合物[Cu(NH ) ]SO 。请
3 4 3 4 4
判断:[Cu(NH ) ]SO 。中存在的化学键的类型有 (填序号)。
3 4 4
a.离子键 b.金属键 c.配位键 d.非极性共价键 e.极性共价键
(4)如图是铜的一种氮化物晶体的晶胞结构。该化合物的化学式为 ,每个N原子周围与它最近且等距离的Cu原子有 个,每个Cu原子周围与它最近且等距离的N原子有 个。
18.(24分)Ⅰ.铁和硒都是人体所必需的微量元素,且在医药、催化、材料等领域有广泛应用,回答下列问
题:
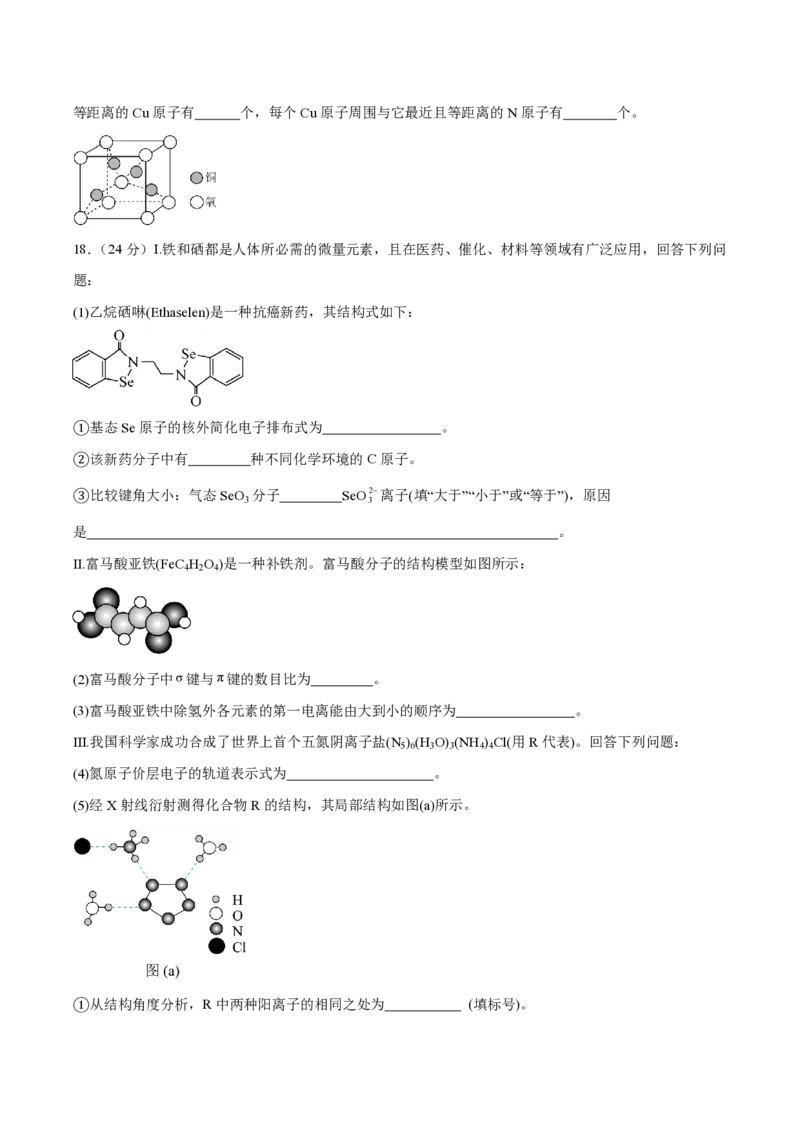
(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如下:
①基态Se原子的核外简化电子排布式为 。
②该新药分子中有 种不同化学环境的C原子。
③比较键角大小:气态SeO 分子 SeO2离子(填“大于”“小于”或“等于”),原因
3 3
是 。
Ⅱ.富马酸亚铁(FeC H O )是一种补铁剂。富马酸分子的结构模型如图所示:
4 2 4
(2)富马酸分子中σ键与π键的数目比为 。
(3)富马酸亚铁中除氢外各元素的第一电离能由大到小的顺序为 。
Ⅲ.我国科学家成功合成了世界上首个五氮阴离子盐(N ) (H O) (NH ) Cl(用R代表)。回答下列问题:
5 6 3 3 4 4
(4)氮原子价层电子的轨道表示式为 。
(5)经X射线衍射测得化合物R的结构,其局部结构如图(a)所示。
①从结构角度分析,R中两种阳离子的相同之处为 (填标号)。A.中心原子的杂化轨道类型 B.中心原子的价层电子对数
C.立体结构 D.共价键类型
② R中阴离子N中的σ键总数为 个。分子中的大π键可用符号Ⅱn 表示,其中m代表参与形成
5 m
大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π6),则N中的大Π键应
6 5
表示为 。
③图(a)中虚线代表氢键,其表示式为(NH)N—H…Cl、 、
4
。化学答案
1- 5 C C C B A
6 -10 D A B B D
11-15 A D B D C
16.(1)(每题2分)三角锥形 低 NH 分子间存在氢键
3
(2)(每题2分)4s 4f5
(3)(每题2分) 小于
(4)(每题1分)镁 相反 O sp3 σ
17【答案】(每题2分)
(1) 3d104s1 >
(2)V形
(3)ace
(4) Cu N 4 2
2
18.(每题2分)(1) [Ar]3d104s24p4 8 大于 SeO 的中心原子杂化轨道为sp2,SeO2的中
3 3
心原子杂化轨道为sp3 (或SeO 的空间构型为平面三角形,SeO2的空间构型为三角锥形)
3 3
(2)11:3
(3)O>C>Fe
(4)
(5) ABD 5 Π6 (H O+)O—H…N(N) (NH)N—H…N(N)
5 3 5 4 5