文档内容
陕西省西安中学高 2025 届高三第二次质量检测考试
化学试题
(时间:75分钟 满分:100分 命题人:冯维娟)
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 S-32 Pb-207
一、选择题(本题共14小题,每小题3分,共42分。每小题只有一个选项符合题
目要求。)
1.化学与生活密切相关,下列说法正确的是( )
A.维生素C可用作水果罐头的抗氧化剂是由于其难以被氧化
B.废弃的秸秆通过发酵获得生物质燃料乙醇
C.SO 可用于丝织品漂白是由于其能氧化丝织品中有色成分
2
D.利用CO 合成高级脂肪酸的甘油酯,实现无机小分子向有机高分子的转化
2
2.下列离子组在指定条件下能大量共存的是( )
A.无色溶液中:Al3+、NH +、Cl-、HCO -
4 3
B.2mol·L-1 H SO 溶液中:Na+、Mg2+、ClO-、Cl-
2 4
C.常温下,pH=1的溶液中:Fe3+、K+、I-、SO 2-
3
D.使酚酞变红的溶液中:Na+、K+、Cl- 、NO -
3
3.设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.等物质的量的C H 和C H O完全燃烧,消耗O 分子数目均为3N
2 4 2 6 2 A
B.25℃,1LpH=12 Ba(OH) 溶液中含有OH-数目为0.02N
2 A
C.Na O 与CO 反应生成标准状况下O 44.8L,转移电子数目为4N
2 2 2 2 A
D.标准状况下,22.4mLCH Cl 中含有碳原子数目为1×10-3 N
2 2 A
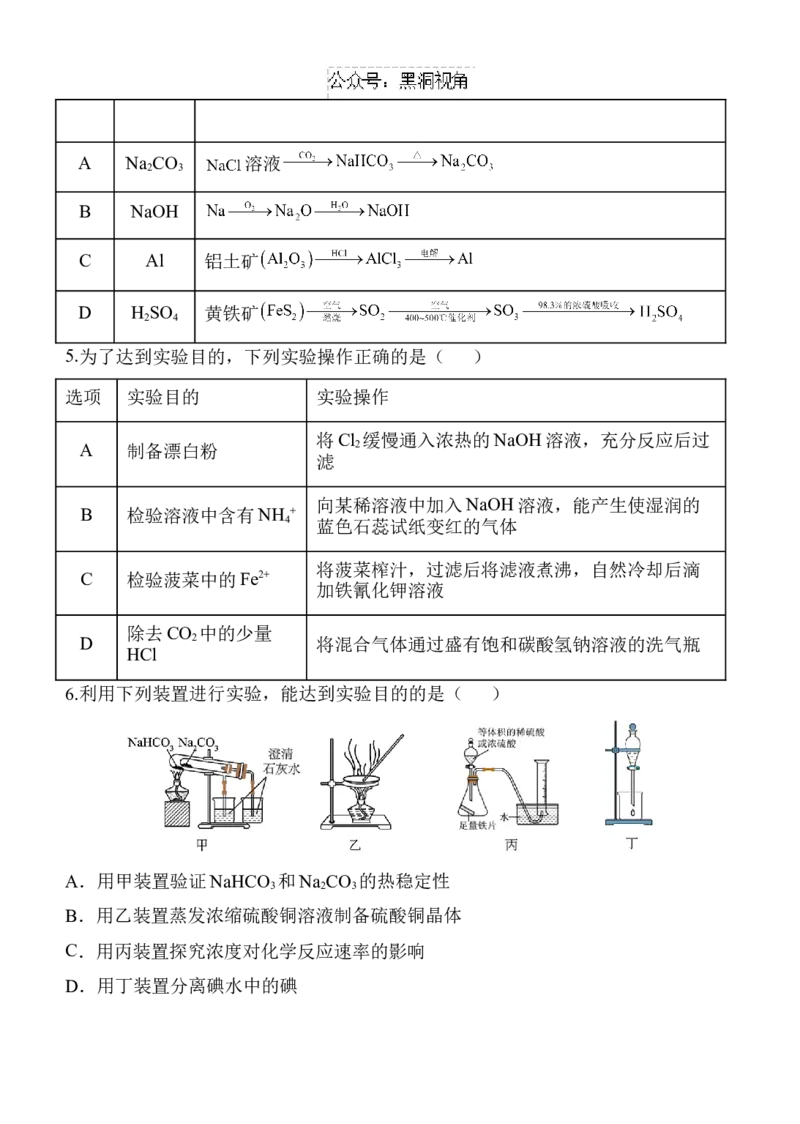
4.工业生产需综合考虑反应进行的可能性、原料来源、成本高低和绿色环保等多种
因素。工业生产下列物质时,对应的转化过程符合要求的是( )
选项 物质 转化过程A Na CO 溶液
2 3
B NaOH
C Al 铝土矿
D H SO 黄铁矿
2 4
5.为了达到实验目的,下列实验操作正确的是( )
选项 实验目的 实验操作
将Cl 缓慢通入浓热的NaOH溶液,充分反应后过
A 制备漂白粉 2
滤
向某稀溶液中加入NaOH溶液,能产生使湿润的
B 检验溶液中含有NH +
4 蓝色石蕊试纸变红的气体
将菠菜榨汁,过滤后将滤液煮沸,自然冷却后滴
C 检验菠菜中的Fe2+
加铁氰化钾溶液
除去CO 中的少量
D 2 将混合气体通过盛有饱和碳酸氢钠溶液的洗气瓶
HCl
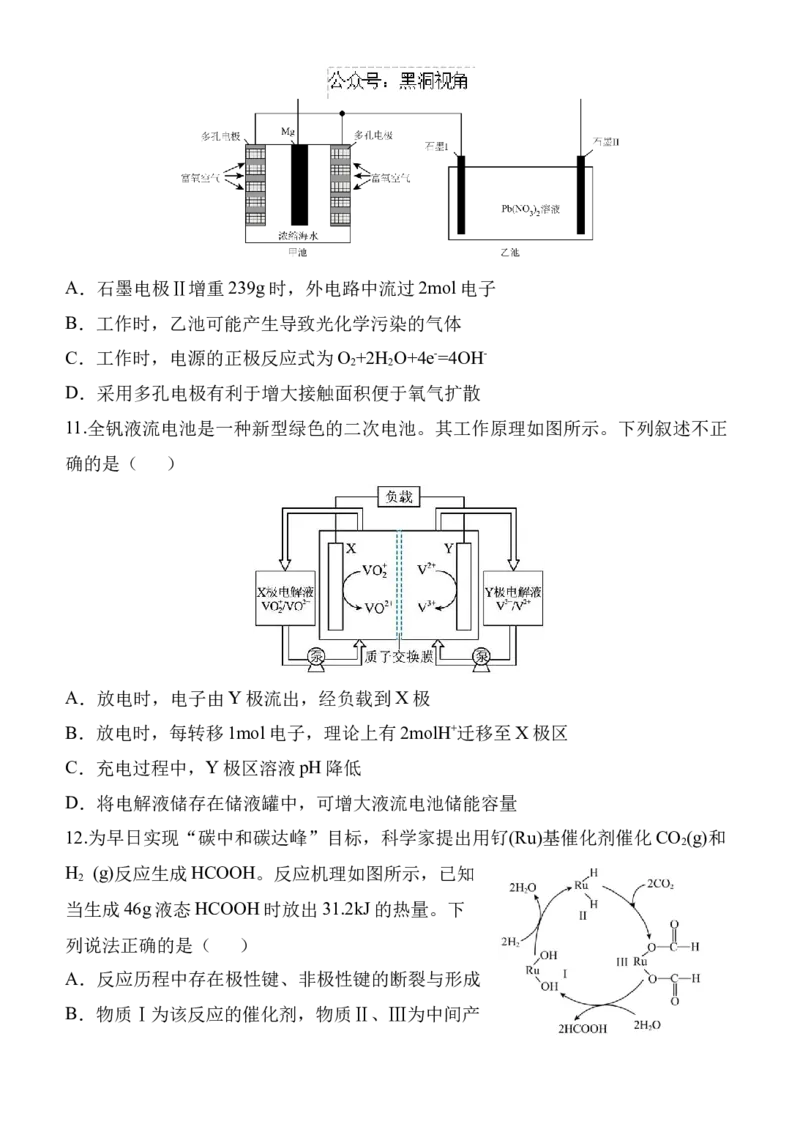
6.利用下列装置进行实验,能达到实验目的的是( )
A.用甲装置验证NaHCO 和Na CO 的热稳定性
3 2 3
B.用乙装置蒸发浓缩硫酸铜溶液制备硫酸铜晶体
C.用丙装置探究浓度对化学反应速率的影响
D.用丁装置分离碘水中的碘7.能正确表示下列反应的离子方程式是( )
A.Cl 通入石灰乳中:Cl +2OH- =Cl-+ClO-+H O
2 2 2
B.FeBr 溶液中通足量Cl :2Fe2++2Br-+2Cl =2Fe3++4Cl-+Br
2 2 2 2
C.将Na O 固体投入H 18O中:2H 18O+2Na O =4Na++218OH-+2OH-+O ↑
2 2 2 2 2 2 2
D.向酸性高锰酸钾溶液中滴加双氧水:2MnO -+H O +6H+=2Mn2++4H O+3O ↑
4 2 2 2 2
8.利用CH OH可将废水中的NO -转化为对环境无害的物质后排放。反应原理为:H+
3 3
+CH OH+ NO -→X+CO +H O (未配平)。下列说法正确的是( )
3 3 2 2
A.X表示NO
2
B.可用O 替换CH OH
3 3
C.氧化剂与还原剂物质的量之比为6:5
D.若生成标准状况下的CO 气体11.2L,则反应转移的电子数为2N (N 表示阿伏
2 A A
加德罗常数的值)
9.通过下列实验以印刷线路板碱性蚀刻废液(主要成分为[Cu(NH ) ]Cl )为原料制备还
3 4 2
原性物质CuCl。下列说法不正确的是( )
A.“沉铜”得到的沉淀主要为Cu(OH)
2
B.“还原”时离子方程式为SO +Cu2++Cl-+H O=CuCl↓+SO +2H+
2
C.“过滤”、“洗涤”时应该在隔绝空气的条件下进行
D.可循环利用的物质为H SO
2 4
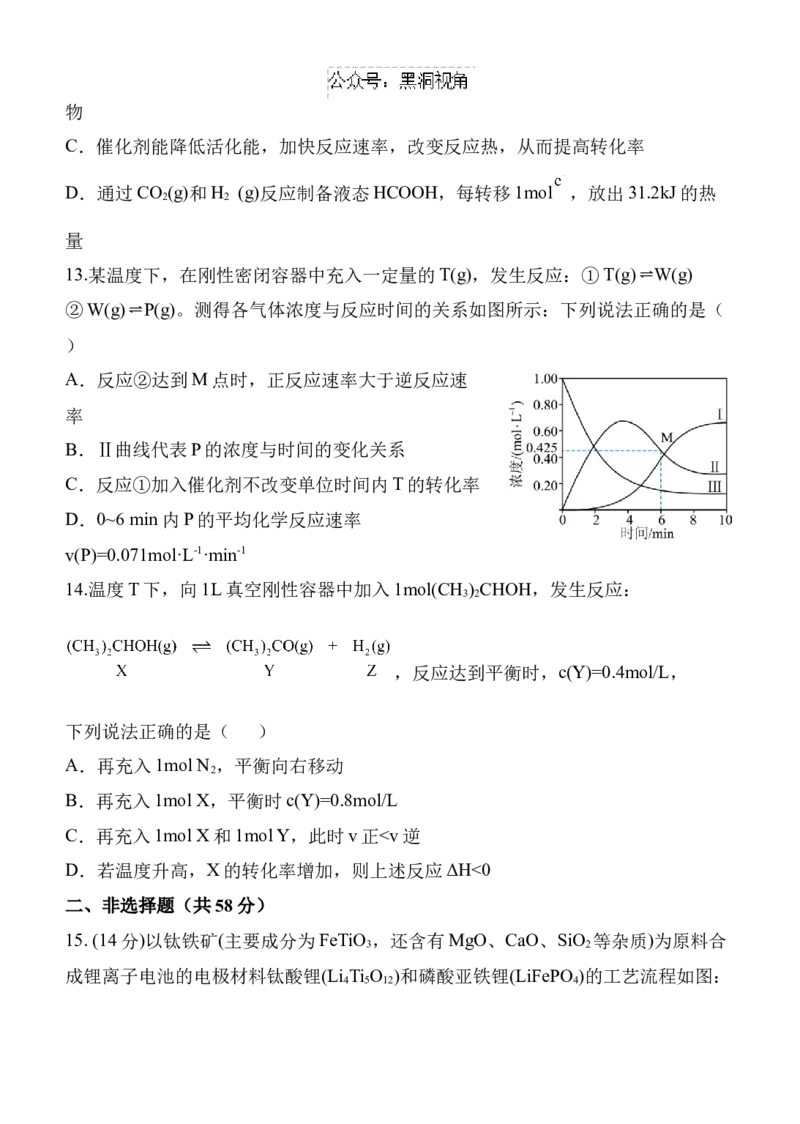
10.镁―空气中性燃料电池是一种能被海水激活的电池,其能量比干电池高20~50倍。
实验小组以该燃料电池为电源制备PbO ,工作原理示意图如图所示。下列说法错误
2
的是( )A.石墨电极Ⅱ增重239g时,外电路中流过2mol电子
B.工作时,乙池可能产生导致光化学污染的气体
C.工作时,电源的正极反应式为O +2H O+4e-=4OH-
2 2
D.采用多孔电极有利于增大接触面积便于氧气扩散
11.全钒液流电池是一种新型绿色的二次电池。其工作原理如图所示。下列叙述不正
确的是( )
A.放电时,电子由Y极流出,经负载到X极
B.放电时,每转移1mol电子,理论上有2molH+迁移至X极区
C.充电过程中,Y极区溶液pH降低
D.将电解液储存在储液罐中,可增大液流电池储能容量
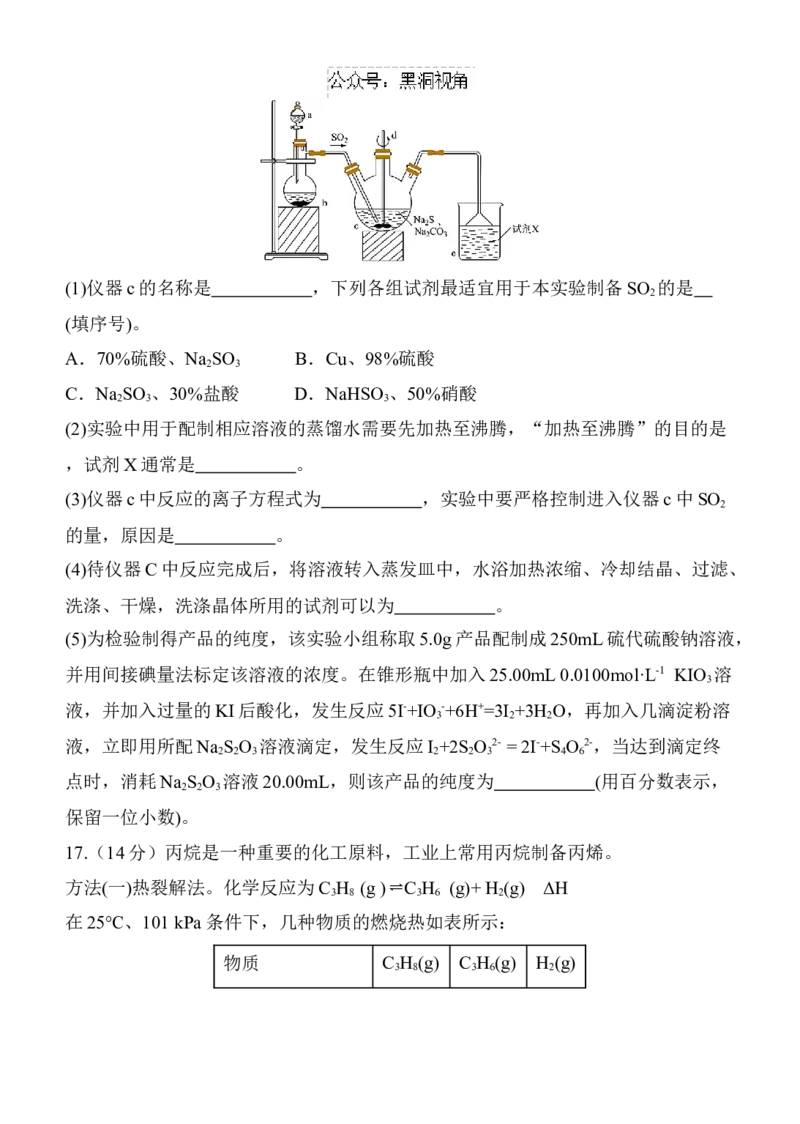
12.为早日实现“碳中和碳达峰”目标,科学家提出用钌(Ru)基催化剂催化CO (g)和
2
H (g)反应生成HCOOH。反应机理如图所示,已知
2
当生成46g液态HCOOH时放出31.2kJ的热量。下
列说法正确的是( )
A.反应历程中存在极性键、非极性键的断裂与形成
B.物质Ⅰ为该反应的催化剂,物质Ⅱ、Ⅲ为中间产物
C.催化剂能降低活化能,加快反应速率,改变反应热,从而提高转化率
D.通过CO (g)和H (g)反应制备液态HCOOH,每转移1mol ,放出31.2kJ的热
2 2
量
13.某温度下,在刚性密闭容器中充入一定量的T(g),发生反应:①T(g)⇌W(g)
②W(g)⇌P(g)。测得各气体浓度与反应时间的关系如图所示:下列说法正确的是(
)
A.反应②达到M点时,正反应速率大于逆反应速
率
B.Ⅱ曲线代表P的浓度与时间的变化关系
C.反应①加入催化剂不改变单位时间内T的转化率
D.0~6 min内P的平均化学反应速率
v(P)=0.071mol·L-1·min-1
14.温度T下,向1L真空刚性容器中加入1mol(CH ) CHOH,发生反应:
3 2
,反应达到平衡时,c(Y)=0.4mol/L,
下列说法正确的是( )
A.再充入1mol N ,平衡向右移动
2
B.再充入1mol X,平衡时c(Y)=0.8mol/L
C.再充入1mol X和1mol Y,此时v正