文档内容
化学部分
可能用到的相对原子质量:H-1 C-12 O-16 F-19 Na-23 S-32 C1-35.5 Ca-40 Fe-56
Cu-64 Ba-137
一、选择题:本大题共15小题,每小题只有一个正确选项,每小题2分,共30分。
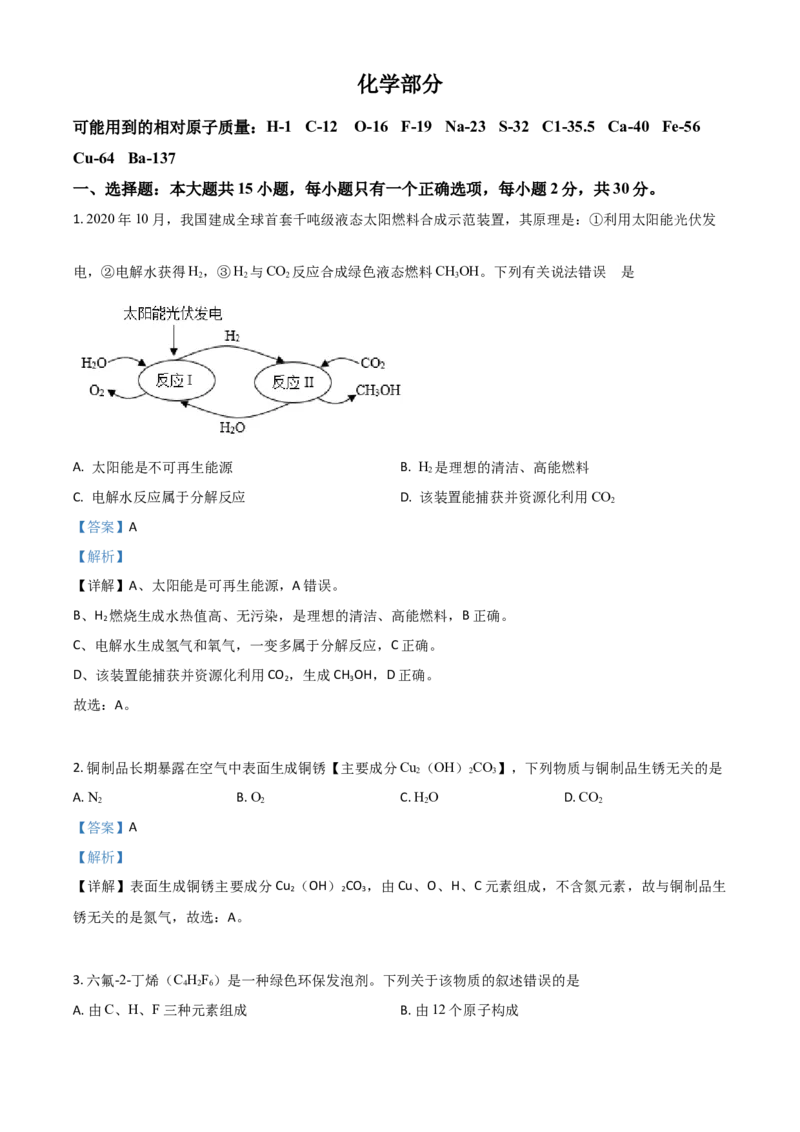
1. 2020年10月,我国建成全球首套千吨级液态太阳燃料合成示范装置,其原理是:①利用太阳能光伏发
的
电,②电解水获得H,③H 与CO 反应合成绿色液态燃料CHOH。下列有关说法错误 是
2 2 2 3
A. 太阳能是不可再生能源 B. H 是理想的清洁、高能燃料
2
C. 电解水反应属于分解反应 D. 该装置能捕获并资源化利用CO
2
【答案】A
【解析】
【详解】A、太阳能是可再生能源,A错误。
B、H 燃烧生成水热值高、无污染,是理想的清洁、高能燃料,B正确。
2
C、电解水生成氢气和氧气,一变多属于分解反应,C正确。
D、该装置能捕获并资源化利用CO ,生成CH OH,D正确。
2 3
故选:A。
2. 铜制品长期暴露在空气中表面生成铜锈【主要成分Cu (OH)CO】,下列物质与铜制品生锈无关的是
2 2 3
A. N B. O C. HO D. CO
2 2 2 2
【答案】A
【解析】
【详解】表面生成铜锈主要成分Cu (OH) CO ,由Cu、O、H、C元素组成,不含氮元素,故与铜制品生
2 2 3
锈无关的是氮气,故选:A。
3. 六氟-2-丁烯(C HF)是一种绿色环保发泡剂。下列关于该物质的叙述错误的是
4 2 6
A. 由C、H、F三种元素组成 B. 由12个原子构成C. 氢元素的质量分数最小 D. 属于有机化合物
【答案】B
【解析】
【详解】A、六氟-2-丁烯由C、H、F三种元素组成,A正确。
B、一个六氟-2-丁烯分子由12个原子构成,B错误。
C、六氟-2-丁烯C、H、F三种元素质量比为 ,氢元素质量分数最小,C
正确。
D、含碳元素的化合物,属于有机物,六氟-2-丁烯由C、H、F三种元素组成,属于有机物,D正确。
故选:B。
阅读下列资料,完成以下小题:“科枝是国之利器,国家赖之以强,企业赖之以赢,人民生活赖之以
好。”
天津大学科学团队制备出二氧化碳加氢的催化剂——Ag/In O,该催化剂比InO 具备更好的催化稳定性。
2 3 2 3
(2021年5月12日《 Green Energy& Environment》)
浙江大学科学团队发现:在尼龙,蚕丝等传统纤维表面涂上——层氧化石墨烯,可形成有特殊性能的新材
料一氧化石墨烯纤维。(2021年5月7日《Science》)
中国科学院研究团队首次合成新原子——铀-214。(2021年4月14日《物理评论快报》)
4. InO 中In的化合价为
2 3
A. +5 B. +3 C. 0 D. -2
5. 氧化石墨烯纤维属于
A. 金属材料 B. 合成材料 C. 复合材料 D. 天然材料
6. 铀-214的质子数为92,相对原子质量为214。下列有关铀的说法正确的是
A. 属于非金属元素 B. 核电荷数为92
C. 中子数为92 D. 铀-214与铀-235属于不同种元素
【答案】4. B 5. C 6. B
【解析】
【详解】(1)设In的化和价为x,根据化合价代数和为零, , x=+3,故选:B。
(2)氧化石墨烯纤维是在尼龙(合成材料),蚕丝(天然材料)等传统纤维表面涂上一层氧化石墨烯
(无机非金属材料),属于复合材料,故选:C。
(3)A、铀带“钅”属于金属元素,A错误。
B、在原子中,质子数=核电荷数=核外电子数,质子数为92,故核电荷数为92,B正确。C、相对原子质量=质子数+中子数,中子数=214-92=122,C错误。
D、轴-214与铀-235质子数相同,属于同种元素,D错误。
故选:B。
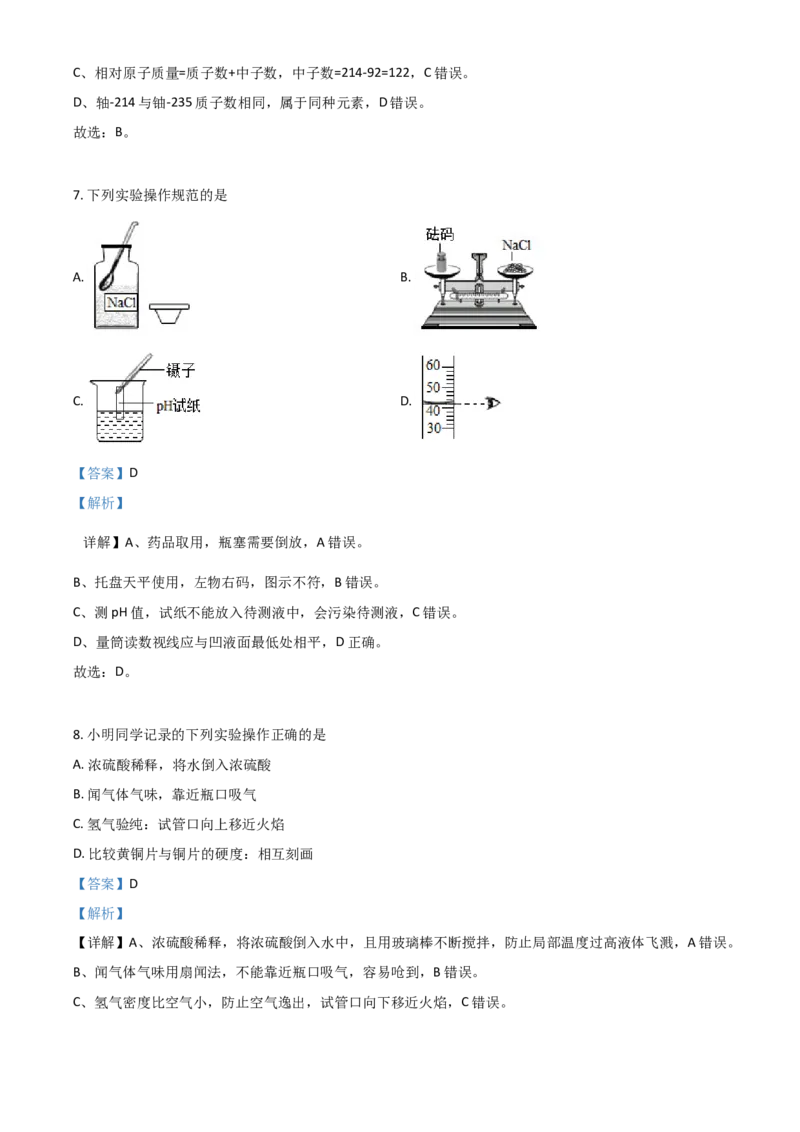
7. 下列实验操作规范的是
A. B.
C. D.
【答案】D
【解析】
【
详解】A、药品取用,瓶塞需要倒放,A错误。
B、托盘天平使用,左物右码,图示不符,B错误。
C、测pH值,试纸不能放入待测液中,会污染待测液,C错误。
D、量筒读数视线应与凹液面最低处相平,D正确。
故选:D。
8. 小明同学记录的下列实验操作正确的是
A. 浓硫酸稀释,将水倒入浓硫酸
B. 闻气体气味,靠近瓶口吸气
C. 氢气验纯:试管口向上移近火焰
D. 比较黄铜片与铜片的硬度:相互刻画
【答案】D
【解析】
【详解】A、浓硫酸稀释,将浓硫酸倒入水中,且用玻璃棒不断搅拌,防止局部温度过高液体飞溅,A错误。
B、闻气体气味用扇闻法,不能靠近瓶口吸气,容易呛到,B错误。
C、氢气密度比空气小,防止空气逸出,试管口向下移近火焰,C错误。D、比较黄铜片与铜片的硬度:相互刻画,D正确。
故选:D。
阅读下列料,完成以下小题,中华文明源远流长,“凝聚着深邃的哲学智慧和中华民族几千年理念及其实
践经验”。
蒙冲斗舰数十艘,实以薪草,膏油灌其中,……盖放诸船,同时发火,时风盛猛,悉延烧岸上营落。
(晋﹒陈寿《三国志》)
墙角数支梅,凌寒独自开,遥知不是雪,为有暗香来。(宋﹒王安石《梅花》)
烧铁器浮于胆矾水中,即成铜色也。(明﹒宋应星《天工开物》)
9. 下列认知有误的是
A. “薪草”“膏油”是可燃物 B. “同时发火”降低了“诸船”的着火点
C. “时风盛猛”提供充足的氧气 D. “膏油”着火不宜用水灭火
的
10. 下列理解不当 是
A. 数枝梅的暗香指的是梅花的物理性质
B. 梅花开的过程中发生的变化是化学变化
C. 作者判断是而不是雪的依据是不同的物质具有不同的化学性质
D. 暗香来是分子运动的结果
11. 下列说法符合事实的是
A. “烧铁器”中的“烧”属于反应条件 B. “即成铜色也”中的“铜色”指黄色
C. “成铜色“后“胆矾水“质量增加 D. “铁器”适宜盛放“胆矾水”
【答案】9. B 10. C 11. A
【解析】
【分析】
【9题详解】
A、根据“蒙冲斗舰数十艘,实以薪草,膏油灌其中,……盖放诸船,同时发火”,可知“薪草”“膏
油”是可燃物,说法正确;
B、“同时发火”提高了可燃物的温度,并不是降低了“诸船”的着火点,说法错误;
C、“时风盛猛”提供充足的氧气,使可燃物燃烧更充分,说法正确;
D、“膏油”密度比水小,可浮在水面燃烧,“膏油”着火不宜用水灭火,说法正确;
故选:B。
【10题详解】
A、数枝梅的暗香指的是梅花的气味,属于物理性质,说法正确;B、梅花开的过程中梅花内部有新物质生成,发生的变化是化学变化,说法正确;
C、作者判断是而不是雪的依据是梅花有香气,而雪没有,此处根据不同的物质具有不同的物理性质,说
法错误;
D、分子是不断运动的,人在远处闻到香味,是分子运动的结果,说法正确;
故选:C。
【11题详解】
A、“烧铁器”中的“烧”属于反应条件,说法正确;
B、“即成铜色也”中的“铜色”指紫红色,因为铜是紫红色金属,说法错误;
C、铁与稀硫酸反应生成硫酸亚铁和铜,根据 ,“成铜色“后“胆矾水“质量
减小,说法错误;
D、铁与稀硫酸反应生成硫酸亚铁和铜,“铁器”不适宜盛放“胆矾水”,说法错误;
故选:A。
12. 两种固体物质NaCl和KCl的溶解度曲线如图所示,现有40gNaC1、40gKCl两份固体,分别置于两只
烧杯中,各倒入100g50°C蒸馏水充分溶解,实验现象如下图所示,下列推断正确的是
A. 甲中加入的固体是NaCl
B. 乙中溶液的质量是140g
C. 50℃时,甲中溶液恰好达到饱和状态
D. 分别将甲、乙中的溶液降温至10°C,乙中溶质的质量分数大于甲中溶质的质量分数
【答案】D
【解析】
【详解】A、现有40gNaC1、40gKCl两份固体,分别置于两只烧杯中,各倒入100g50°C蒸馏水充分溶解,甲全部溶解,乙部分溶解,说明50°C时,甲溶解度大,乙溶解度小,由图可知甲加入的固体是氯化钾,A
错误。
B、甲中固体是氯化钾,乙中为氯化钠,50°C时氯化钠溶解度小于40g,氯化钠部分溶解,乙中溶液的质量
小于140g,B错误。
C、甲中固体是氯化钾,50℃时溶解度大于40g,甲中溶液不饱和状态,C错误。
D、分别将甲、乙中的溶液降温至10°C,甲溶解度变小,小于40g是饱和溶液,乙溶解度变化不大,还是
小于40g,还是饱和溶液,甲乙饱和溶液,10°C乙氯化钠溶解度大于氯化钾溶解度,故乙中溶质的质量分
数大于甲中溶质的质量分数,D正确。
故选:D。
13. 对下列事实的解释不合理的是
A. 铁和钢的性能不同——含碳量不同
B. 镁原子和镁离子化学性质不同——最外层电子数不同
C. 粗盐提纯得到精盐的产率偏高一一蒸发时未用玻璃棒搅拌
D. 将糖水密封放置,温度不变,蔗糖与水不会分离——溶液具有稳定性
【答案】C
【解析】
【
详解】A、铁和钢的含碳量不同,所以性能不同,A正确。
B、最外层电子决定化学性质,镁原子和镁离子最外层电子数不同化学性质不同,B正确。
C、蒸发时未用玻璃棒搅拌,液体容易飞溅,粗盐提纯得到精盐的产率偏低,C错误。
D、将糖水密封放置,温度不变,蔗糖与水不会分离,因为溶液具有稳定性,D正确。
故选:C。
14. 下列实验方案能达到实验目的的是
选
实验目的 实验方案
项
A 检验酒精中是否含有氧元素 在空气中点燃,检验生成物
B 除去KCl溶液中的MgCl 滴加适量Ba(OH) 溶液
2
取样,分别溶于水中,观察溶液温度变
C 鉴别固体NaOH与NH NO
4 3 化
D 分离Cu粉和Fe粉的混合物 加入足量的稀硫酸,过滤、洗涤、干燥A. A B. B C. C D. D
【答案】C
【解析】
【详解】A、检验酒精中是否含有氧元素,在空气中点燃,检验生成物,酒精燃烧,因为氧气中含氧元素,
无论酒精是否含氧元素,都能检测到氧元素,A错误。
B、氯化镁和氢氧化钡反应生成氢氧化镁沉淀和氯化钡,引入新杂质,B错误。
C、氢氧化钠溶解放热,硝酸铵溶解吸热,取样,分别溶于水中,观察溶液温度变化,可鉴别氢氧化钠和
硝酸铵,C正确。
D、分离Cu粉和Fe粉的混合物,既要得到铜粉还要得到铁粉,加入稀硫酸铁粉反应生成硫酸亚铁和氢气,
不符合题意,D错误。
故选:C。
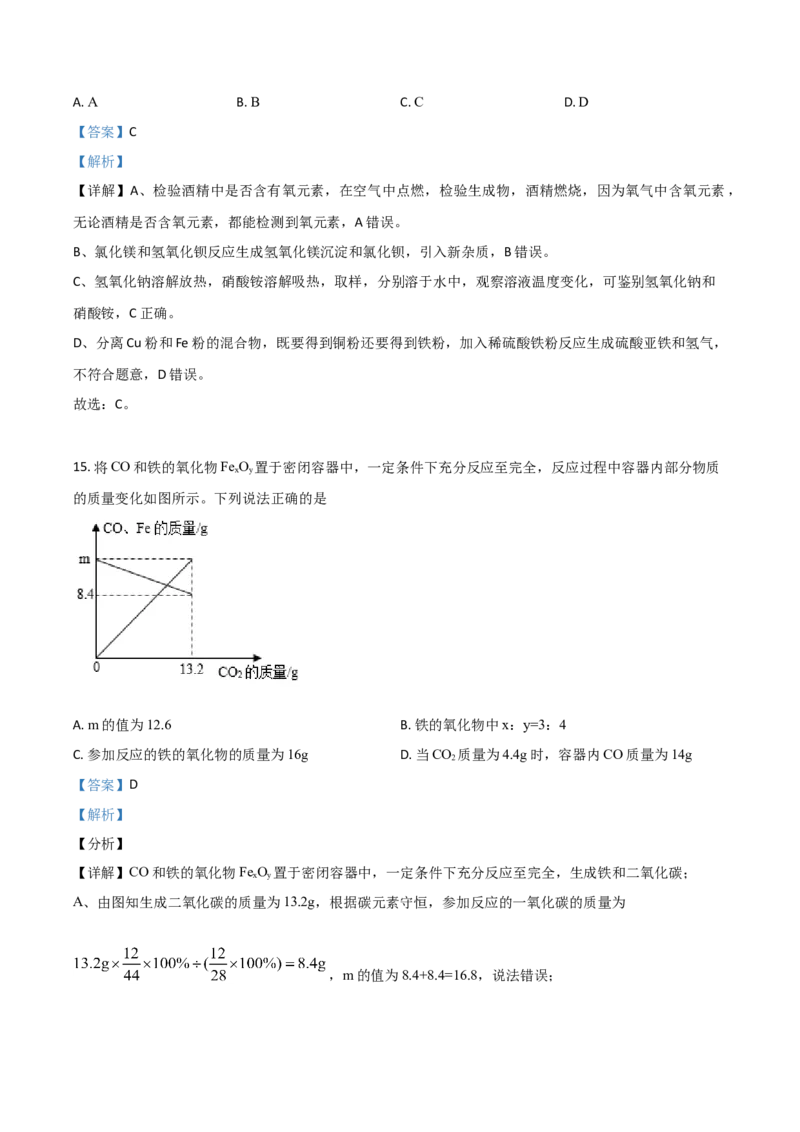
15. 将CO和铁的氧化物Fe O 置于密闭容器中,一定条件下充分反应至完全,反应过程中容器内部分物质
x y
的质量变化如图所示。下列说法正确的是
A. m的值为12.6 B. 铁的氧化物中x:y=3:4
C. 参加反应的铁的氧化物的质量为16g D. 当CO 质量为4.4g时,容器内CO质量为14g
2
【答案】D
【解析】
【分析】
【详解】CO和铁的氧化物Fe O 置于密闭容器中,一定条件下充分反应至完全,生成铁和二氧化碳;
x y
A、由图知生成二氧化碳的质量为13.2g,根据碳元素守恒,参加反应的一氧化碳的质量为
,m的值为8.4+8.4=16.8,说法错误;B、由于m=16.8,即生成铁的质量为16.8g,根据质量守恒定律,Fe O 的质量为13.2g+16.8g-8.4g=21.6g,
x y
根据 ,生成的二氧化碳中的氧元素,一半来自Fe O,Fe O 中氧元素的质
x y x y
量为 ,Fe O 中铁元素、氧元素质量比为 ,铁的氧化物中
x y
x:y=1:1,说法错误;
C、参加反应的铁的氧化物的质量为13.2g+16.8g-8.4g=21.6g,说法错误;
D、由以上分析知,该铁的氧化物为FeO,设当二氧化碳质量为4.4g时,消耗一氧化碳的质量为z,则
解得z=2.8g;
此时容器内CO质量为16.8g-2.8g=14g,说法正确。
故选:D。
二、非选择题:本大题共4小题,共40分。
16. 化学就在我们身边,人类的生活离不开化学。
(1)从下列选项中选择一种适当的物质填空,并将字母序号填写在横线上。
A 水果 B 钛合金 C 湿毛巾 D 碳酸氢钠 E 医用酒精 F 点燃的蜡烛
①健康:食用______以预防坏血病,可用______擦拭物品消毒。
②医疗:可用______治疗胃酸过多,可用______制造人造骨骼。
③安全:取用______捂口逃离火场,取用______探查废弃地窖。
(2)“杂交水稻之父”袁隆平“一稻济天下”,在不断培育高产杂交水稻的同时,还成功培育出了适宜
在盐碱地上种植的“海水稻”。
①“杂交水稻”富含淀粉,淀粉属于六大基本营养素中的______。
②“海水稻”富含硒,硒是人体必需的______(选填“微量”“常量”)元素。
【答案】 ①. A ②. E ③. D ④. B ⑤. C ⑥. F ⑦. 糖类 ⑧. 微量
【解析】【分析】
【详解】(1)
①健康:水果中富含维生素,食用水果以预防坏血病,酒精能使蛋白质失去活性,可用医用酒擦拭物品消
毒;
故填:A;E。
②医疗:碳酸氢钠能与稀盐酸反应,可用碳酸氢钠治疗胃酸过多,钛合金与人体具有很好的“相容性”,
可用钛合金制造人造骨骼;
故填:D;B。
③安全:取用湿毛巾捂口逃离火场,防止烟尘吸入,取用点燃的蜡烛探查废弃地窖,检验氧气是否充足;
故填:C;F。
(2)①“杂交水稻”富含淀粉,淀粉属于六大基本营养素中的糖类。
②“海水稻”富含硒,硒是人体必需的微量元素。
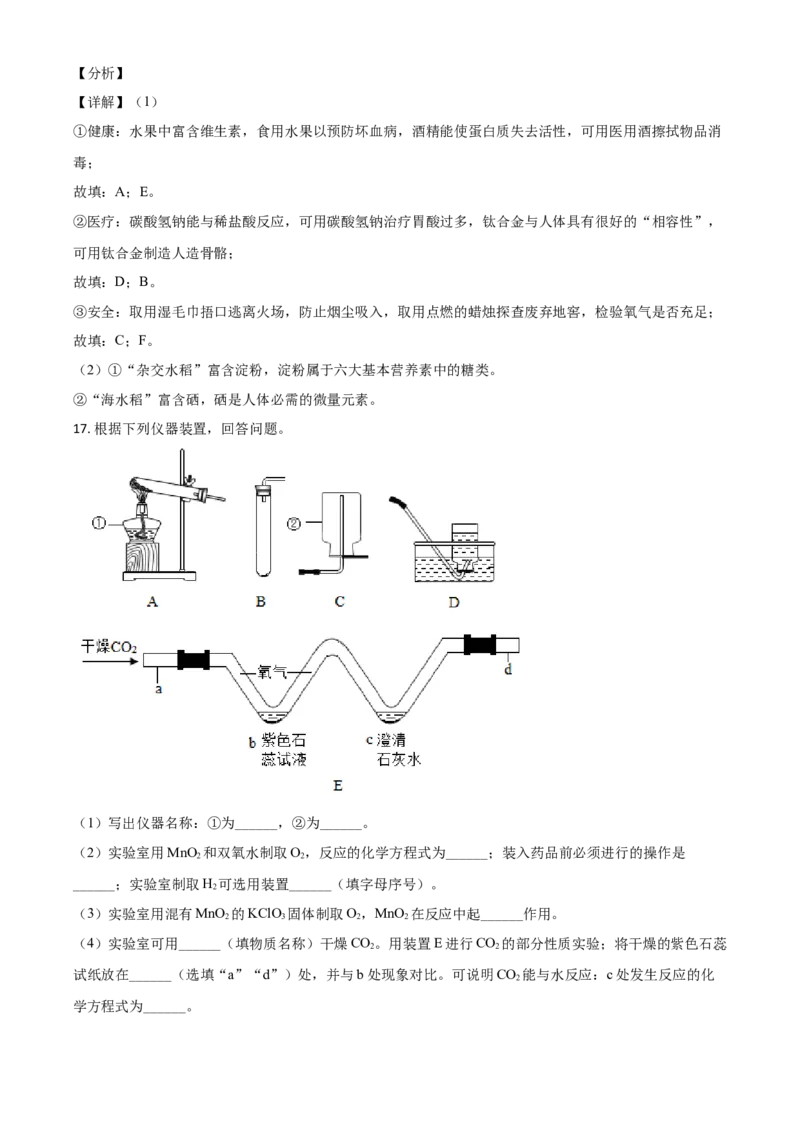
17. 根据下列仪器装置,回答问题。
(1)写出仪器名称:①为______,②为______。
(2)实验室用MnO 和双氧水制取O,反应的化学方程式为______;装入药品前必须进行的操作是
2 2
______;实验室制取H 可选用装置______(填字母序号)。
2
(3)实验室用混有MnO 的KClO 固体制取O,MnO 在反应中起______作用。
2 3 2 2
(4)实验室可用______(填物质名称)干燥CO。用装置E进行CO 的部分性质实验;将干燥的紫色石蕊
2 2
试纸放在______(选填“a”“d”)处,并与b处现象对比。可说明CO 能与水反应:c处发生反应的化
2
学方程式为______。【答案】 ①. 酒精灯 ②. 集气瓶 ③. 2HO 2HO+O ④. 检查装置气密性 ⑤. BC或
2 2 2 2
↑
BD ⑥. 催化 ⑦. 浓硫酸 ⑧. a ⑨. Ca(OH) +CO =CaCO +H O
2 2 3 2
【解析】 ↓
【分析】
【详解】(1)由图可知,①为酒精灯,②为集气瓶,故填:酒精灯;集气瓶。
(2)过氧化氢分解生成水和氧气,实验室用MnO 和双氧水制取O,反应的化学方程式为 2HO
2 2 2 2
2HO+O ;装入药品前必须进行的操作是检查装置气密性;实验室制取H 可反应不需要加热,发生装置
2 2 2
选B,氢↑气密度比空气小,难溶于水,可用向下排空气法收集或排水法收集,故选用装置BC或BD,故填:
2HO 2HO+O ;BC或BD。
2 2 2 2
↑
(3)实验室用混有MnO 的KClO 固体制取O,MnO 在反应中是催化剂,起催化作用,故填:催化。
2 3 2 2
(4)浓硫酸具有吸水性,实验室可用浓硫酸干燥CO。用装置E进行CO 的部分性质实验;将干燥的紫色
2 2
石蕊试纸放在a处,试纸不变红,b处紫色石蕊试液刚开始不变红,通入二氧化碳之后变红,a处与b处现
象对比。可说明CO 能与水反应:c氢氧化钙和二氧化碳生成碳酸钙和水,c处发生反应的化学方程式为
2
Ca(OH) +CO =CaCO ↓+H O,故填:浓硫酸;a;Ca(OH) +CO =CaCO ↓+H O。
2 2 3 2 2 2 3 2
18. 大美湿地,水城绿都——生态新盐城的美好画卷正在黄海之滨徐徐铺陈。
(1)保护沿海湿地,擦亮生态名片。
①湿地旅游要做好垃圾分类,野营产生的厨余垃圾应该投放到印有______(选填“可回收物”“不可回收
物”)标识的垃圾箱。
②保护湿地,从我做起。下列建议合理的是______(填字母序号)。
A 禁止围猎捕食野生动物,人与自然和谐共生
B 滩涂湿地大量植树造林,改善海边空气质量
C 就地焚烧枯枝、落叶,防止植物腐败污染水体
D 组织黄海湿地世界自然遗产保护宣传系列活动
E 沿海区域建设核电站,便于向海水中排放核废水
(2)瞄准低碳目标,发展生态能源。
①目前,我市使用的燃料大多数来自化石燃料,如煤、石油、______等。
②风从海上来,电在风中生。我市大力发展风力发电,常选用具有良好______(填写具体性质)的铜质或铝质电线、电缆进行电力传输。
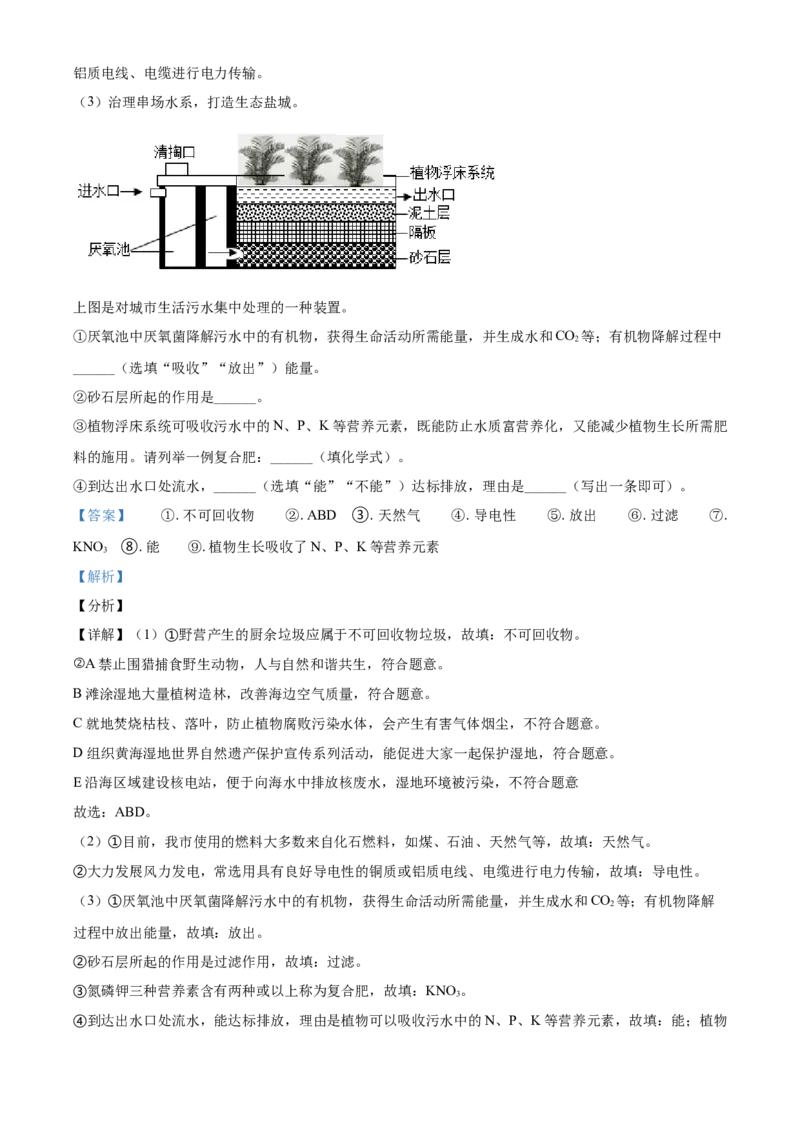
(3)治理串场水系,打造生态盐城。
上图是对城市生活污水集中处理的一种装置。
①厌氧池中厌氧菌降解污水中的有机物,获得生命活动所需能量,并生成水和CO 等;有机物降解过程中
2
______(选填“吸收”“放出”)能量。
②砂石层所起的作用是______。
③植物浮床系统可吸收污水中的N、P、K等营养元素,既能防止水质富营养化,又能减少植物生长所需肥
料的施用。请列举一例复合肥:______(填化学式)。
④到达出水口处流水,______(选填“能”“不能”)达标排放,理由是______(写出一条即可)。
【答案】 ①. 不可回收物 ②. ABD ③. 天然气 ④. 导电性 ⑤. 放出 ⑥. 过滤 ⑦.
KNO ⑧. 能 ⑨. 植物生长吸收了N、P、K等营养元素
3
【解析】
【分析】
【详解】(1)①野营产生的厨余垃圾应属于不可回收物垃圾,故填:不可回收物。
②A 禁止围猎捕食野生动物,人与自然和谐共生,符合题意。
B滩涂湿地大量植树造林,改善海边空气质量,符合题意。
C 就地焚烧枯枝、落叶,防止植物腐败污染水体,会产生有害气体烟尘,不符合题意。
D 组织黄海湿地世界自然遗产保护宣传系列活动,能促进大家一起保护湿地,符合题意。
。
E 沿海区域建设核电站,便于向海水中排放核废水,湿地环境被污染,不符合题意
故选:ABD。
(2)①目前,我市使用的燃料大多数来自化石燃料,如煤、石油、天然气等,故填:天然气。
②大力发展风力发电,常选用具有良好导电性的铜质或铝质电线、电缆进行电力传输,故填:导电性。
(3)①厌氧池中厌氧菌降解污水中的有机物,获得生命活动所需能量,并生成水和CO 等;有机物降解
2
过程中放出能量,故填:放出。
②砂石层所起的作用是过滤作用,故填:过滤。
③氮磷钾三种营养素含有两种或以上称为复合肥,故填:KNO。
3
④到达出水口处流水,能达标排放,理由是植物可以吸收污水中的N、P、K等营养元素,故填:能;植物生长吸收了N、P、K等营养元素。
19. 化学是一门以实验为基础的科学,实验是科学探究的重要手段。
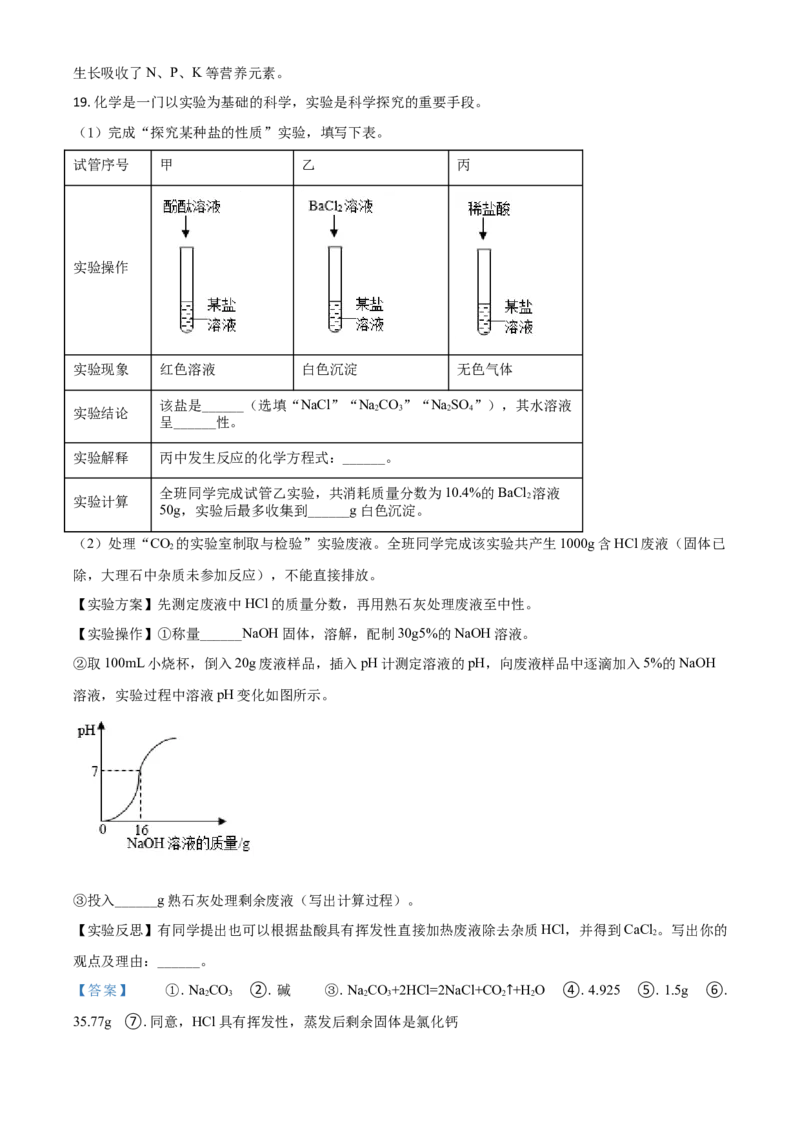
(1)完成“探究某种盐的性质”实验,填写下表。
试管序号 甲 乙 丙
实验操作
实验现象 红色溶液 白色沉淀 无色气体
该盐是______(选填“NaCl”“NaCO”“NaSO ”),其水溶液
实验结论 2 3 2 4
呈______性。
实验解释 丙中发生反应的化学方程式:______。
全班同学完成试管乙实验,共消耗质量分数为10.4%的BaCl 溶液
实验计算 2
50g,实验后最多收集到______g白色沉淀。
(2)处理“CO 的实验室制取与检验”实验废液。全班同学完成该实验共产生1000g含HCl废液(固体已
2
除,大理石中杂质未参加反应),不能直接排放。
【实验方案】先测定废液中HCl的质量分数,再用熟石灰处理废液至中性。
【实验操作】①称量______NaOH固体,溶解,配制30g5%的NaOH溶液。
②取100mL小烧杯,倒入20g废液样品,插入pH计测定溶液的pH,向废液样品中逐滴加入5%的NaOH
溶液,实验过程中溶液pH变化如图所示。
③投入______g熟石灰处理剩余废液(写出计算过程)。
【实验反思】有同学提出也可以根据盐酸具有挥发性直接加热废液除去杂质HCl,并得到CaCl 。写出你的
2
观点及理由:______。
【答案】 ①. NaCO ②. 碱 ③. NaCO+2HCl=2NaCl+CO +H O ④. 4.925 ⑤. 1.5g ⑥.
2 3 2 3 2 2
35.77g ⑦. 同意,HCl具有挥发性,蒸发后剩余固体是氯化钙 ↑【解析】
【分析】
【详解】(1)该盐能使酚酞溶液变红,说明溶液显碱性,能和氯化钡生成沉淀,能和稀盐酸生成气体,
该盐是碳酸钠,显碱性,丙中碳酸钠和稀盐酸生成氯化钠二氧化碳和水,故填:NaCO ;碱;
2 3
NaCO+2HCl=2NaCl+CO +H O。
2 3 2 2
实验计算: ↑
解:设生成白色沉淀质量为x。
x=4.925g
故填:4.925。
(2)[实验操作]
①配制30g5%的NaOH溶液,需要氢氧化钠30g×5%=1.5g,故填:1.5g。
③解设20g废液中HCl的质量为y,需要氢氧化钙质量为z。
y=0.73g,HCl质量分数
Z=35.77g[实验反思]
同意,HCl具有挥发性,蒸发后剩余固体是氯化钙,故填:同意,HCl具有挥发性,蒸发后剩余固体是氯
化钙。