文档内容
娄底市2019年初中毕业学业考试试题卷化学
亲爱的同学:甜蜜的初中生活即将过去,展示自己的时候到啦。你可要冷静思考、沉着答卷、细心检查哦!
祝你成功!理科综合时量120分钟,化学满分100分。请将答案填涂在答题卡上的相应位置
可能用到的相对原子质量:H-1C-12N-14 O-16Cl-35.5Ca-40
五、选择题(本大题共15个小题,每小题只有一个正确答案,每小题2分,共30分)
24.空气中含量较多且化学性质比较活泼的气体是
A.氧气 B.氮气 C.稀有气体 D.二氧化碳
25.化学知识有助于我们正确认识、理智选择、科学生活,下列说法正确的是
A.鼓励焚烧秸杆节约能源 B.工业废水处理未达标就排放
C.煤炉上放一壶水就能防止CO中毒 D.生活垃圾分类回收,科学处理
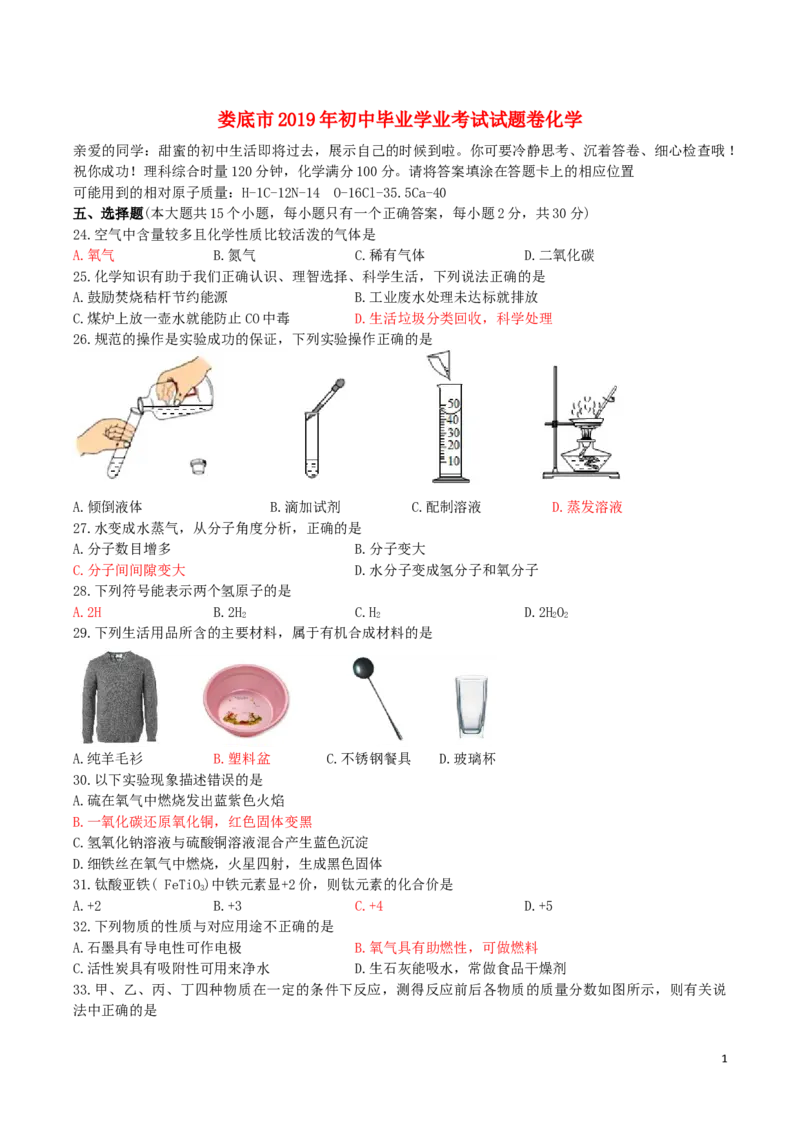
26.规范的操作是实验成功的保证,下列实验操作正确的是
A.倾倒液体 B.滴加试剂 C.配制溶液 D.蒸发溶液
27.水变成水蒸气,从分子角度分析,正确的是
A.分子数目增多 B.分子变大
C.分子间间隙变大 D.水分子变成氢分子和氧分子
28.下列符号能表示两个氢原子的是
A.2H B.2H C.H D.2HO
2 2 2 2
29.下列生活用品所含的主要材料,属于有机合成材料的是
A.纯羊毛衫 B.塑料盆 C.不锈钢餐具 D.玻璃杯
30.以下实验现象描述错误的是
A.硫在氧气中燃烧发出蓝紫色火焰
B.一氧化碳还原氧化铜,红色固体变黑
C.氢氧化钠溶液与硫酸铜溶液混合产生蓝色沉淀
D.细铁丝在氧气中燃烧,火星四射,生成黑色固体
31.钛酸亚铁( FeTiO)中铁元素显+2价,则钛元素的化合价是
3
A.+2 B.+3 C.+4 D.+5
32.下列物质的性质与对应用途不正确的是
A.石墨具有导电性可作电极 B.氧气具有助燃性,可做燃料
C.活性炭具有吸附性可用来净水 D.生石灰能吸水,常做食品干燥剂
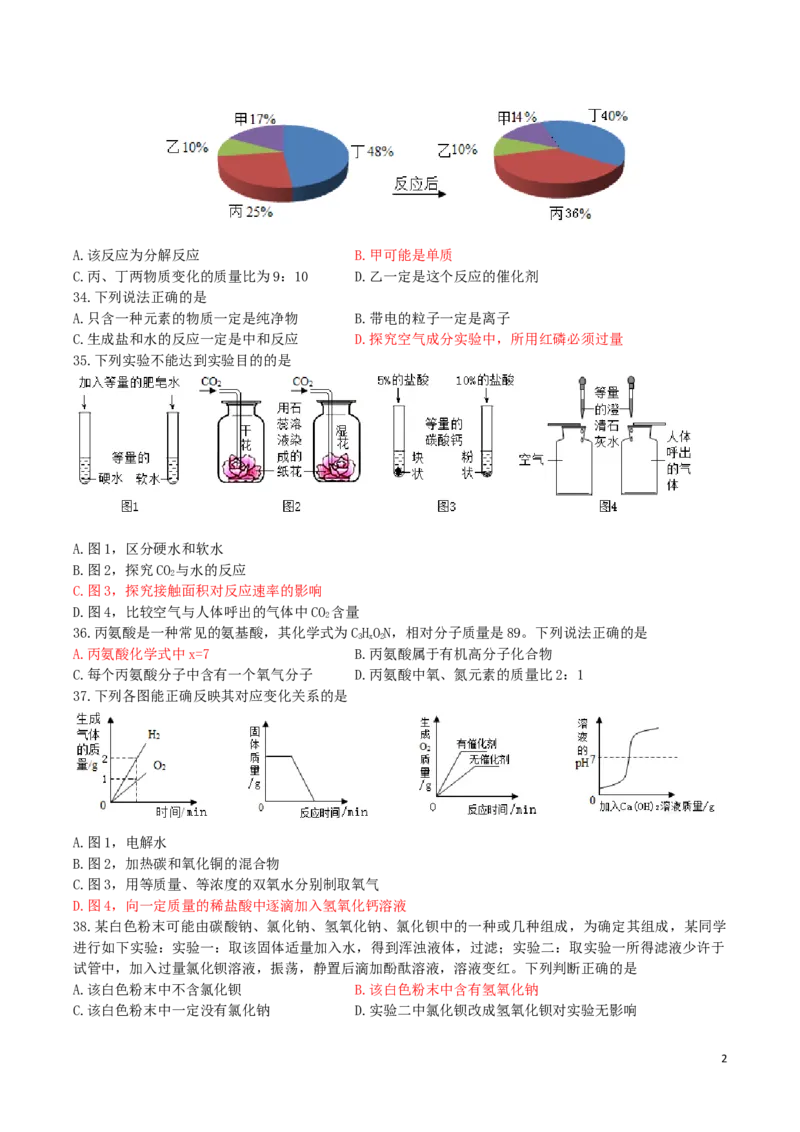
33.甲、乙、丙、丁四种物质在一定的条件下反应,测得反应前后各物质的质量分数如图所示,则有关说
法中正确的是
1A.该反应为分解反应 B.甲可能是单质
C.丙、丁两物质变化的质量比为9:10 D.乙一定是这个反应的催化剂
34.下列说法正确的是
A.只含一种元素的物质一定是纯净物 B.带电的粒子一定是离子
C.生成盐和水的反应一定是中和反应 D.探究空气成分实验中,所用红磷必须过量
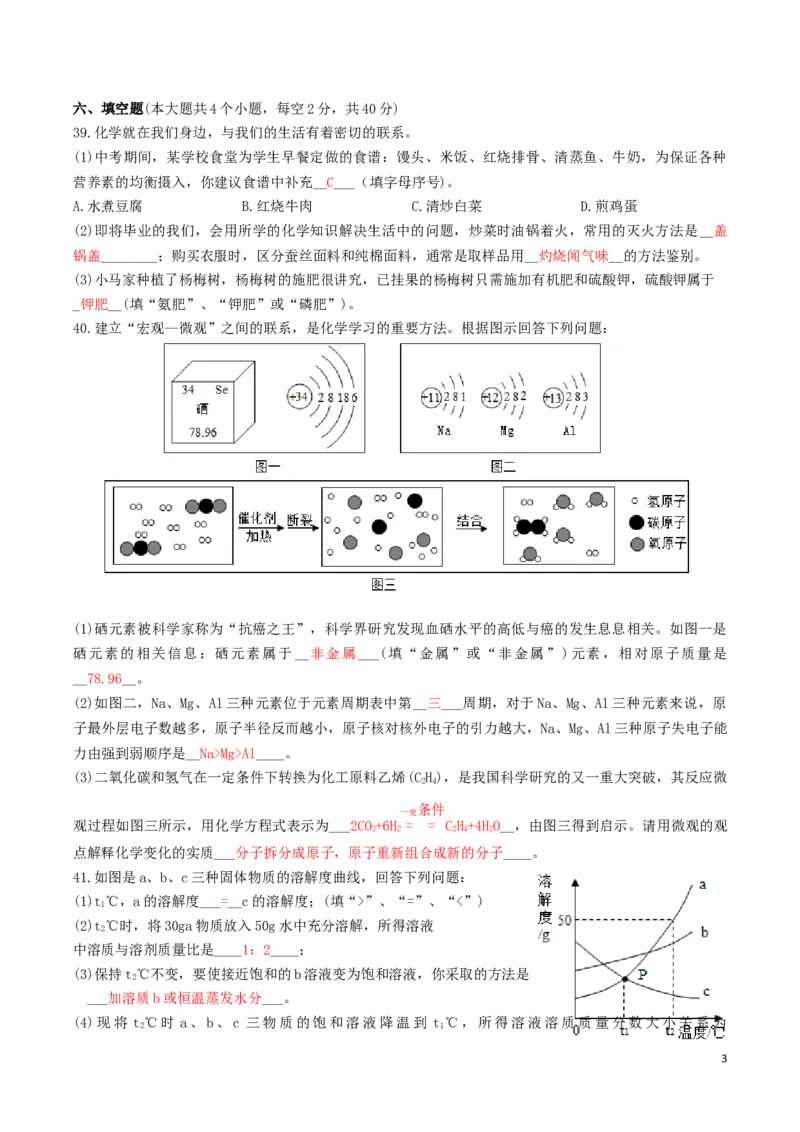
35.下列实验不能达到实验目的的是
A.图1,区分硬水和软水
B.图2,探究CO 与水的反应
2
C.图3,探究接触面积对反应速率的影响
D.图4,比较空气与人体呼出的气体中CO 含量
2
36.丙氨酸是一种常见的氨基酸,其化学式为CHON,相对分子质量是89。下列说法正确的是
3 x 2
A.丙氨酸化学式中x=7 B.丙氨酸属于有机高分子化合物
C.每个丙氨酸分子中含有一个氧气分子 D.丙氨酸中氧、氮元素的质量比2:1
37.下列各图能正确反映其对应变化关系的是
A.图1,电解水
B.图2,加热碳和氧化铜的混合物
C.图3,用等质量、等浓度的双氧水分别制取氧气
D.图4,向一定质量的稀盐酸中逐滴加入氢氧化钙溶液
38.某白色粉末可能由碳酸钠、氯化钠、氢氧化钠、氯化钡中的一种或几种组成,为确定其组成,某同学
进行如下实验:实验一:取该固体适量加入水,得到浑浊液体,过滤;实验二:取实验一所得滤液少许于
试管中,加入过量氯化钡溶液,振荡,静置后滴加酚酞溶液,溶液变红。下列判断正确的是
A.该白色粉末中不含氯化钡 B.该白色粉末中含有氢氧化钠
C.该白色粉末中一定没有氯化钠 D.实验二中氯化钡改成氢氧化钡对实验无影响
2六、填空题(本大题共4个小题,每空2分,共40分)
39.化学就在我们身边,与我们的生活有着密切的联系。
(1)中考期间,某学校食堂为学生早餐定做的食谱:馒头、米饭、红烧排骨、清蒸鱼、牛奶,为保证各种
营养素的均衡摄入,你建议食谱中补充__C___(填字母序号)。
A.水煮豆腐 B.红烧牛肉 C.清炒白菜 D.煎鸡蛋
(2)即将毕业的我们,会用所学的化学知识解决生活中的问题,炒菜时油锅着火,常用的灭火方法是__盖
锅盖________;购买衣服时,区分蚕丝面料和纯棉面料,通常是取样品用__灼烧闻气味__的方法鉴别。
(3)小马家种植了杨梅树,杨梅树的施肥很讲究,已挂果的杨梅树只需施加有机肥和硫酸钾,硫酸钾属于
_钾肥__(填“氨肥”、“钾肥”或“磷肥”)。
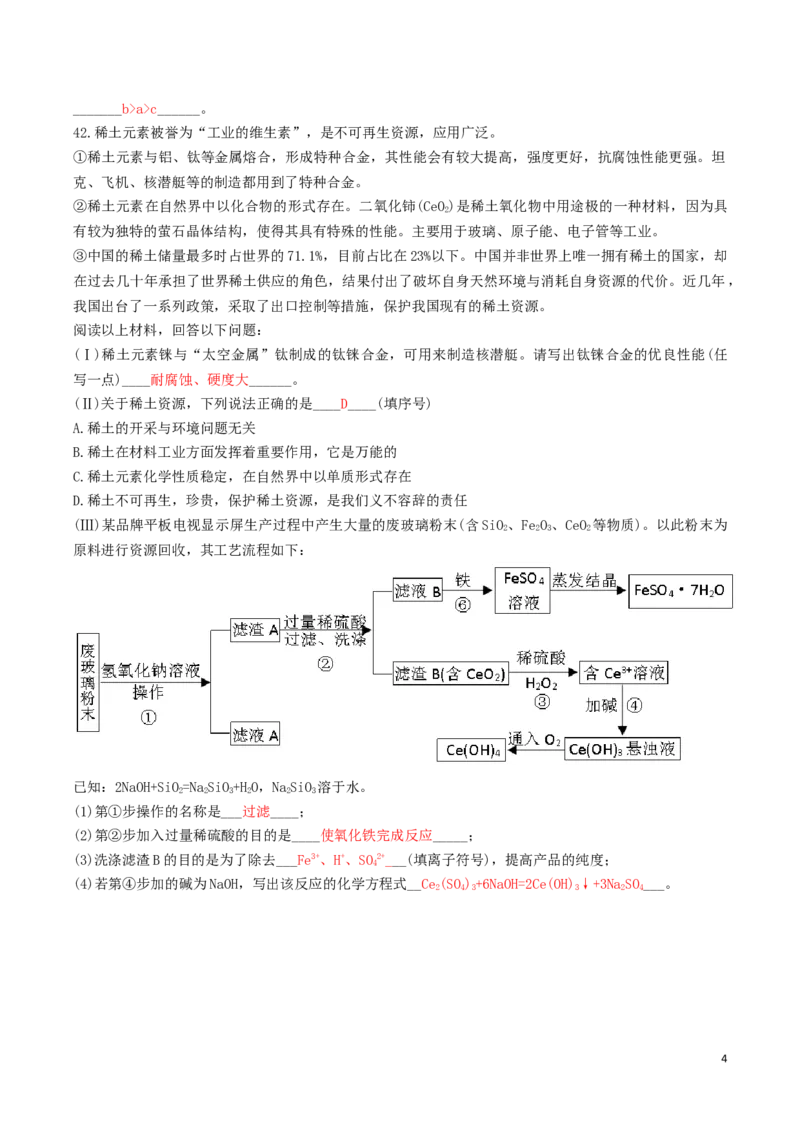
40.建立“宏观—微观”之间的联系,是化学学习的重要方法。根据图示回答下列问题:
(1)硒元素被科学家称为“抗癌之王”,科学界研究发现血硒水平的高低与癌的发生息息相关。如图一是
硒元素的相关信息:硒元素属于__非金属___(填“金属”或“非金属”)元素,相对原子质量是
__78.96__。
(2)如图二,Na、Mg、Al三种元素位于元素周期表中第__三___周期,对于Na、Mg、Al三种元素来说,原
子最外层电子数越多,原子半径反而越小,原子核对核外电子的引力越大,Na、Mg、Al三种原子失电子能
力由强到弱顺序是__Na>Mg>Al____。
(3)二氧化碳和氢气在一定条件下转换为化工原料乙烯(CH),是我国科学研究的又一重大突破,其反应微
2 4
条件
一定
观过程如图三所示,用化学方程式表示为___2CO+6H = = CH+4HO__,由图三得到启示。请用微观的观
2 2 2 4 2
点解释化学变化的实质___分子拆分成原子,原子重新组合成新的分子____。
41.如图是a、b、c三种固体物质的溶解度曲线,回答下列问题:
(1)t℃,a的溶解度___=__c的溶解度;(填“>”、“=”、“<”)
1
(2)t℃时,将30ga物质放入50g水中充分溶解,所得溶液
2
中溶质与溶剂质量比是____1:2____;
(3)保持t℃不变,要使接近饱和的b溶液变为饱和溶液,你采取的方法是
2
___加溶质b或恒温蒸发水分___。
(4)现将 t℃时 a、b、c 三物质的饱和溶液降温到 t℃,所得溶液溶质质量分数大小关系为
2 1
3_______b>a>c______。
42.稀土元素被誉为“工业的维生素”,是不可再生资源,应用广泛。
①稀土元素与铝、钛等金属熔合,形成特种合金,其性能会有较大提高,强度更好,抗腐蚀性能更强。坦
克、飞机、核潜艇等的制造都用到了特种合金。
②稀土元素在自然界中以化合物的形式存在。二氧化铈(CeO)是稀土氧化物中用途极的一种材料,因为具
2
有较为独特的萤石晶体结构,使得其具有特殊的性能。主要用于玻璃、原子能、电子管等工业。
③中国的稀土储量最多时占世界的71.1%,目前占比在23%以下。中国并非世界上唯一拥有稀土的国家,却
在过去几十年承担了世界稀土供应的角色,结果付出了破坏自身天然环境与消耗自身资源的代价。近几年,
我国出台了一系列政策,采取了出口控制等措施,保护我国现有的稀土资源。
阅读以上材料,回答以下问题:
(Ⅰ)稀土元素铼与“太空金属”钛制成的钛铼合金,可用来制造核潜艇。请写出钛铼合金的优良性能(任
写一点)____耐腐蚀、硬度大______。
(Ⅱ)关于稀土资源,下列说法正确的是____D____(填序号)
A.稀土的开采与环境问题无关
B.稀土在材料工业方面发挥着重要作用,它是万能的
C.稀土元素化学性质稳定,在自然界中以单质形式存在
D.稀土不可再生,珍贵,保护稀土资源,是我们义不容辞的责任
(Ⅲ)某品牌平板电视显示屏生产过程中产生大量的废玻璃粉末(含SiO 、FeO 、CeO 等物质)。以此粉末为
2 2 3 2
原料进行资源回收,其工艺流程如下:
已知:2NaOH+SiO=NaSiO+HO,NaSiO 溶于水。
2 2 3 2 2 3
(1)第①步操作的名称是___过滤____;
(2)第②步加入过量稀硫酸的目的是____使氧化铁完成反应_____;
(3)洗涤滤渣B的目的是为了除去___Fe3+、H+、SO2+___(填离子符号),提高产品的纯度;
4
(4)若第④步加的碱为NaOH,写出该反应的化学方程式__Ce(SO)+6NaOH=2Ce(OH)↓+3NaSO___。
2 4 3 3 2 4
4七、实验探究题(本题共2个小题,每空2分,共24分)
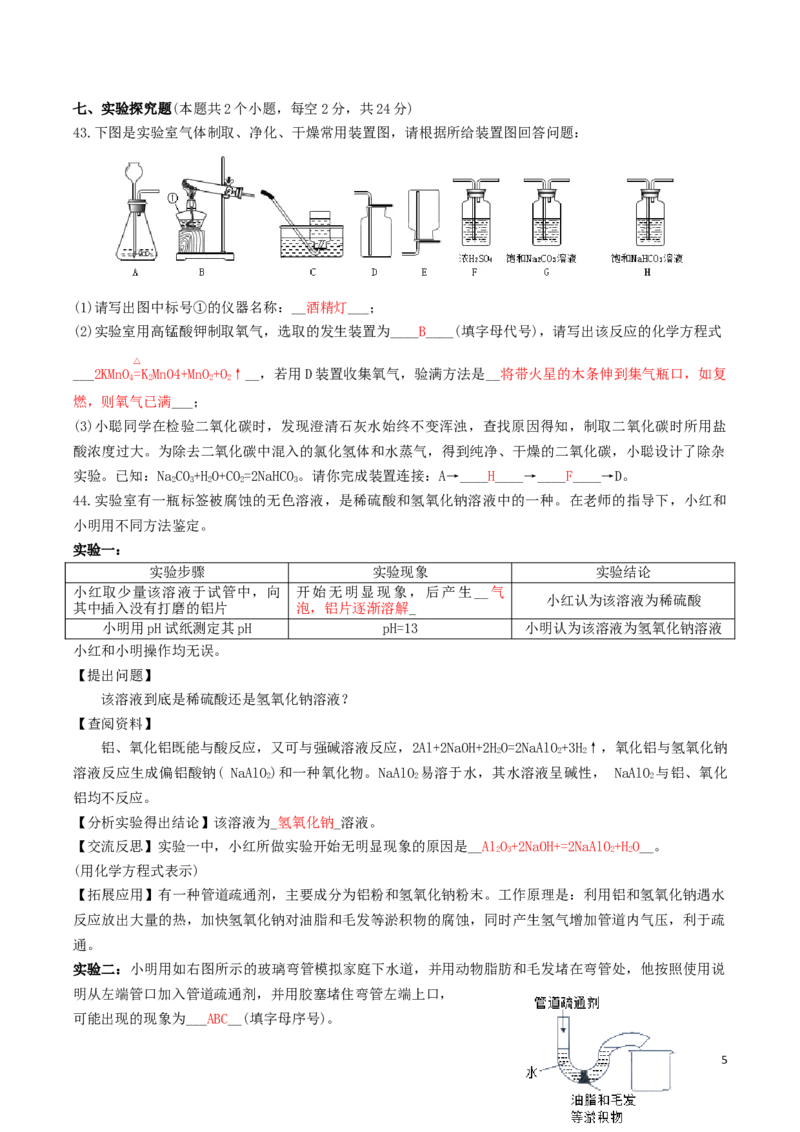
43.下图是实验室气体制取、净化、干燥常用装置图,请根据所给装置图回答问题:
(1)请写出图中标号①的仪器名称:__酒精灯___;
(2)实验室用高锰酸钾制取氧气,选取的发生装置为____B____(填字母代号),请写出该反应的化学方程式
△
___2KMnO =KMnO4+MnO+O↑__,若用D装置收集氧气,验满方法是__将带火星的木条伸到集气瓶口,如复
4 2 2 2
燃,则氧气已满___;
(3)小聪同学在检验二氧化碳时,发现澄清石灰水始终不变浑浊,查找原因得知,制取二氧化碳时所用盐
酸浓度过大。为除去二氧化碳中混入的氯化氢体和水蒸气,得到纯净、干燥的二氧化碳,小聪设计了除杂
实验。已知:NaCO+HO+CO=2NaHCO。请你完成装置连接:A→____H____→____F____→D。
2 3 2 2 3
44.实验室有一瓶标签被腐蚀的无色溶液,是稀硫酸和氢氧化钠溶液中的一种。在老师的指导下,小红和
小明用不同方法鉴定。
实验一:
实验步骤 实验现象 实验结论
小红取少量该溶液于试管中,向 开始无明显现象,后产生__气
小红认为该溶液为稀硫酸
其中插入没有打磨的铝片 泡,铝片逐渐溶解_
小明用pH试纸测定其pH pH=13 小明认为该溶液为氢氧化钠溶液
小红和小明操作均无误。
【提出问题】
该溶液到底是稀硫酸还是氢氧化钠溶液?
【查阅资料】
铝、氧化铝既能与酸反应,又可与强碱溶液反应,2Al+2NaOH+2HO=2NaAlO+3H↑,氧化铝与氢氧化钠
2 2 2
溶液反应生成偏铝酸钠( NaAlO)和一种氧化物。NaAlO 易溶于水,其水溶液呈碱性, NaAlO 与铝、氧化
2 2 2
铝均不反应。
【分析实验得出结论】该溶液为_氢氧化钠_溶液。
【交流反思】实验一中,小红所做实验开始无明显现象的原因是__AlO+2NaOH+=2NaAlO+HO__。
2 3 2 2
(用化学方程式表示)
【拓展应用】有一种管道疏通剂,主要成分为铝粉和氢氧化钠粉末。工作原理是:利用铝和氢氧化钠遇水
反应放出大量的热,加快氢氧化钠对油脂和毛发等淤积物的腐蚀,同时产生氢气增加管道内气压,利于疏
通。
实验二:小明用如右图所示的玻璃弯管模拟家庭下水道,并用动物脂肪和毛发堵在弯管处,他按照使用说
明从左端管口加入管道疏通剂,并用胶塞堵住弯管左端上口,
可能出现的现象为___ABC__(填字母序号)。
5A.产生大量气体
B.弯管内温度升高
C.堵塞物变软被气体赶出,落入烧杯中
实验三:为了证明烧杯中废液里是否还含有氢氧化钠,小明做了如下实验
实验操作 实验现象 实验结论
取少量澄清废液于试管中,滴入酚酞 溶液变红 废液中有氢氧化钠剩余
小红对小明的结论提出了质疑,理由是___NaAlO 易溶于水,其水溶液呈碱性,也能使无色酚酞试液变红__,
2
小红把酚酞改用_硫酸铜溶液等_(填药品)进行实验,得出废液中还含有氢氧化钠。
管道疏通剂中氢氧化钠过量,可确保铝粉反应完全,并且过量的氢氧化钠对下水道有清污的作用。
八、计算题(本大题共1个小题,共6分)
45.钙是人体中的常量元素,缺钙时可通过食用保健药剂来增加摄入量。某品牌补钙药剂主要含酸酸钙,
为了测定该品牌补钙药剂中CaCO 的质量分数,取该补钙剂制成的粉末20g,逐滴滴入稀盐酸(补钙剂中其
3
他成分不与盐酸反应),得到数据如下图所示,请根据有关信息回答问题:
(1)该补钙剂刚好完全反应时产生气体的质量为__4.4_g。
(2)该品牌补钙药剂中CaCO 的质量分数是___50%___。
3
(3)求该盐酸中溶质的质量分数。(写出计算过程)_7.3%__
67