文档内容
2011 年重庆高考理综化学试题及解析
6. “化学,让生活更美好”,下列叙述不能直接体现这一主旨的是
A. 风力发电,让能源更清洁 B.合成光纤,让通讯更快捷
C.合成药物,让人类更健康 D.环保涂料,让环境更宜居
8. 对滴有酚酞试液的下列溶液,操作后颜色变深的是
A.明矾溶液加热 B.CH COONa溶液加热
3
C.氨水中加入少量NH Cl固体 D.小苏打溶液中加入少量NaCl固体
4
【答案】B
【解析】明矾KAl(SO ) ·12H O在水中电离后产生的Al3+水解使溶液呈酸性,加热导致水解程度增大,但酚
4 2 2
酞遇酸性溶液颜色不变化,因此A项不符合题意。CH COONa为强碱弱酸盐,水解呈碱性,滴加酚酞后溶
3
液显红色,加热使碱性增强,因此红色变深。氨水为弱碱,发生不完全电离:NH ·H O NH ++OH-,
3 2 4
加入酚酞后溶液变为红色,而NH Cl=NH ++Cl-,其中的NH +会抑制氨水的电离,使溶液碱性减弱,颜色
4 4 4
变浅。NaCl对NaHCO 溶液中HCO -的水解无影响
3 3
9. 在实验室进行下列实验, 括号内的实验用品都能用到的是
A.硫酸铜晶体里结晶水含量的测定(坩埚、温度计、硫酸铜晶体)
B.蛋白质的盐析(试管、醋酸铅溶液、鸡蛋白溶液)
C.钠的焰色反应(铂丝、氯化钠溶液、稀盐酸)
D.肥皂的制取(蒸发皿、玻璃棒、甘油)
【答案】C【解析】A项中不使用温度计,B项中醋酸铅属于重金属盐,因此会使蛋白质变性,而不是盐析,D项中
制取肥皂的药品是硬脂酸甘油酯和氢氧化钠溶液,不用甘油。
10. 一定条件下,下列反应中水蒸气含量随反应时间的变化趋势符合题图10 的是
A.CO (g)+2NH (g) CO(NH ) (s)+H O(g); △H<0
2 3 2 2 2
B.CO (g)+H (g) CO(g)+H O(g); △H>0C.CH CH OH (g) CH =CH (g)+H O(g); △H>0
2 2 2 [ 3 2 2 2 2
D.2C H CH CH (g)+O (g) 2 C H CH=CH (g)+2H O(g); △H<0
6 5 2 3 2 6 5 2 2
【答案】A
【解析】左边图像是温度与时间的图像,在拐点之前可以判断斜率较大的T 对应的反应速率快,因此温
2
度较高,即T >T ,拐点之后,T 温度下达到平衡时,水蒸气的含量较少,因此确定升高温度,平衡逆向
2 1 2
移动,即此反应正向为放热反应,排除B、C。右边图像为压强与时间的图像,拐点前可判断P >P ,拐点
1 2
后可判断增大压强平衡正向移动,确定此反应生成物的气体的物质的量之和小于反应物气体的物质的量
之和,排除D。
11. 不能鉴别AgNO 、BaCl 、K SO 和Mg(NO ) 四种溶液(不考虑他们间的相互反应)的试剂组是
3 2 2 3 3 2
A. 盐酸、硫酸 B. 盐酸、氢氧化钠溶液
C. 氨水、硫酸 D. 氨水、氢氧化钠溶液
12.NM-3和D-58是正处于临床试验阶段的小分子抗癌药物,结构如下:关于NM-3和D-58的叙述,错误的是
A.都能与NaOH溶液反应,原因不完全相同
B.都能与溴水反应,原因不完全相同
C.都不能发生消去反应,原因相同
D.遇FeCl 溶液都显色,原因相同
3
【答案】C
【解析】NM-3中能够与NaOH溶液反应反应的官能团为酚羟基、酯基和羧基,所以既有中和反应又有水
解反应,而D-58能与NaOH溶液反应的只有酚羟基,即只有中和反应,A项正确。NM-3中能够与溴单质
反应的官能团为碳碳双键的加成反应,酚羟基的邻、对位的取代反应,而 D-58与溴单质只能是酚羟基邻、
对位的取代反应,B项正确。常见的能够发生消去反应的官能团为卤素原子和羟基,NM-3中无此官能团,
而D-58中因接羟基的碳原子的邻位碳上无氢原子而不能发生消去反应,C项错误。由于两种物质中均有
酚羟基,因此可以与FeCl 发生显色反应,D项正确。
3
13. SF 是一种优良的绝缘气体,分子结构中只存在S-F键。已知:1molS (s)转化为气态硫原子吸收
6
能量280kJ,断裂1molF-F 、S-F键需吸收的能量分别为160kJ、330kJ。则S(s)+3F (g)=SF (g)的反应热△H
2 6
为
A. -1780kJ/mol B. -1220 kJ/mol
C.-450 kJ/mol D. +430 kJ/mol
【答案】B
【解析】根据题意可判断1molSF 中含有6molS—F键,1mol F 中含有1molF—F键,因此
6 2
ΔH=280kJ/mol+160kJ/mol×3-330kJ/mol×6=-1220kJ//mol。
第二部分(非选择题共174分)
26.(15分)用于金属焊接的某种焊条,其药皮由大理石、水泥、硅铁等配制而成。
(1)Al的原子结构示意图为_____________________;Al与NaOH溶液反应的离子方程式为
________________________________________________。
(2)30Si的原子的中子数为_________;SiO 晶体类型为__________________。
2
(3)Al3+与Yn-的电子数相同,Y所在族的各元素的氢化物的水溶液均显酸性,则该族氢化物中沸点最低的是________。
(4)焊接过程中,药皮在高温下产生了熔渣和使金属不被氧化的气体,该气体是__________。
(5)经处理后的熔渣36.0g(仅含Fe O 、Al O 、SiO ),加入足量稀盐酸,分离得到11.0g固体;
2 3 2 3 2
滤液中加入过量NaOH溶液,分离得到21.4g固体;则此熔渣中Al O 的质量分数为__________________。
2 3
答案:(1) 2Al+2OH-+2H O=2AlO -+3H ↑
2 2 2
(2)16 原子晶体
(3)HCl
(4)CO
2
(5)25%
【解析】(2)30Si的质子数为14,质量数为30,因此中子数为30-14=16。
(3)Yn-离子的形成可排除第ⅣA族元素,根据气态氢化物显酸性判断Y为第ⅦA族元素(第ⅥA族的
H O为中性,第ⅤA族的NH 的水溶液显碱性),该族元素形成的气态氢化物均为分子晶体,由于HF中含
2 3
有氢键,使其熔沸点较高,其余氢化物由于结构相似,因此相对分子质量越小者,熔沸点越低,因此HCl
的沸点最低。
27.(15分)固态化合物A由两种短周期元素组成,可与水发生复分解反应,甲组同学用题 27图装
置(夹持装置略)对其进行探究实验。(1)仪器B的名称是____________。
(2)试验中,Ⅱ中的试纸变蓝,Ⅳ中黑色粉末逐渐变为红色并有M生成,则Ⅲ中的试剂为
__________________;Ⅳ发生反应的化学方程式为____________;Ⅴ中的试剂为____________________。
(3)乙组同学进行同样实验,但装置连接顺序为Ⅰ——Ⅲ——Ⅳ——Ⅱ——Ⅴ——Ⅵ,此时Ⅱ中现象
为________,原因是__________________。
(4)经上述反应,2.5g 化合物 A 理论上可得 0.56L(标准状况)M;则 A 的化学式为
________________。
答案:(1)分液漏斗
(2)碱石灰 CuO+2NH △ 3 C u+3H O+N ↑
3 2 2
(3)试纸变蓝 CuO与氨气反应生成的水和未反应的氨气形成氨水,使试纸变蓝
(4)Mg N
3 2
【解析】根据Ⅱ中干燥的红色石蕊试纸变蓝说明有湿润的碱性气体生成,中学阶段学习的碱性气体为氨气,
即A中含有氮元素。氨气具有还原性,干燥的氨气可以还原氧化铜,因此装置Ⅲ起干燥作用,用碱性干
燥剂来干燥氨气,结合反应物中的元素及性质,可确定生成的单质气体为氮气。收集氮气前,应将反应
剩余的氨气吸收,因此选择浓硫酸。
(4)根据质量守恒可知,生成氮气中的氮元素的质量即为A中氮元素的质量,所以2.5gA中含有氮原子
0.56L
的质量为 ,因此A中氮元素与另一种元素的质量比为
2 14g/mol 0.7g
22.4L/mol
0.7g 7
,结合此物质可以水解,则推测为Mg N 。
3 2
2.5g 0.7g 18
28.(16分)食品添加剂必须严格按照食品安全国家标准(GB2760-2011)的规定使用。作为食品添
加剂中的防腐剂G和W,可经下列反应路线得到(部分反应条件略)。
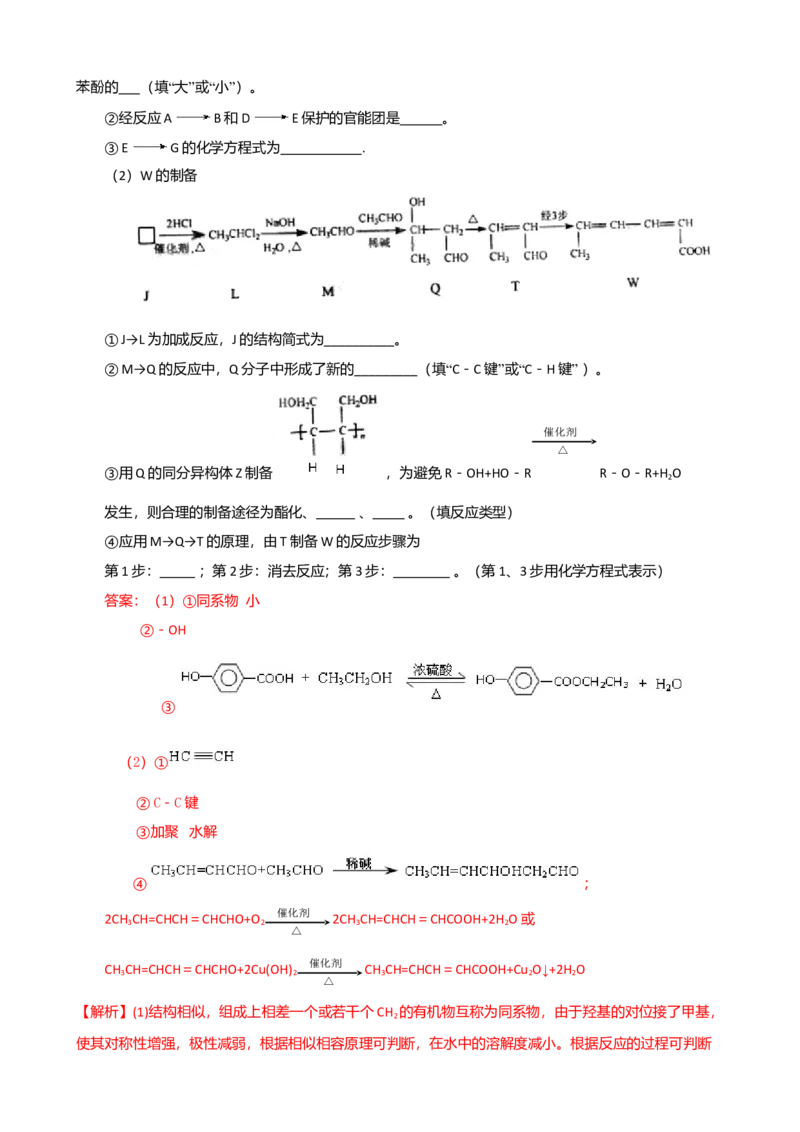
(1)G的制备
①A与苯酚在分在组成上相差一个CH 原子团,他们互称为 ;常温下A在水中的溶解度比
2苯酚的 (填“大”或“小”)。
②经反应A B和D E保护的官能团是 。
③E G的化学方程式为 .
(2)W的制备
①J→L为加成反应,J的结构简式为__________。
②M→Q的反应中,Q分子中形成了新的_________(填“C-C键”或“C-H键” )。
催化剂
△
③用Q的同分异构体Z制备 ,为避免R-OH+HO-R R-O-R+H O
2
发生,则合理的制备途径为酯化、 、 。(填反应类型)
④应用M→Q→T的原理,由T制备W的反应步骤为
第1步: ;第2步:消去反应;第3步: 。(第1、3步用化学方程式表示)
答案:(1)①同系物 小
②-OH
③
(2)①
②C-C键
③加聚 水解
④ ;
催化剂
2CH CH=CHCH=CHCHO+O 2CH CH=CHCH=CHCOOH+2H O或
3 2 3 2
△
催化剂
CH CH=CHCH=CHCHO+2Cu(OH) CH CH=CHCH=CHCOOH+Cu O↓+2H O
3 2 3 2 2
△
【解析】(1)结构相似,组成上相差一个或若干个CH 的有机物互称为同系物,由于羟基的对位接了甲基,
2
使其对称性增强,极性减弱,根据相似相容原理可判断,在水中的溶解度减小。根据反应的过程可判断在E中又生成了羟基,因此确定是为了保护羟基。结合E和G的结构可知,此反应生成了酯基,因此反应
为酯化反应。
29.(14分)臭氧是一种强氧化剂,常用于消毒、灭菌等。
(1)O 与KI溶液反应生成的两种单质是___________和_________。(填分子式)
3
(2)O 在水中易分解,一定条件下,O 的浓度减少一半所需的时间(t)如题29表所示。已知:O
3 3 3
的起始浓度为0.0216 mol/L。
①pH增大能加速O 分解,表明对O 分解起催化作用的是___________.
3 3
②在30°C、pH=4.0条件下,O 的分解速率为__________ mol/(L·min)。
3
③据表中的递变规律,推测O 在下列条件下分解速率依次增大的顺序为______.(填字母代号)
3
a. 40°C、pH=3.0 b. 10°C、pH=4.0 c. 30°C、pH=7.0
(3)O 可由臭氧发生器(原理如题29图)电解稀硫酸制得。
3
①图中阴极为_____(填“A”或“B”),其电极反应式为_____。
②若C处通入O ,则A极的电极反应式为_____.
2
③若C处不通入O ,D、E处分别收集到xL和有yL气体(标准情况),则E处收集的气体中O 所占的
2 3
体积分数为_____。(忽略O 的分解)。
3答案:(1)O I
2 2
(2)①OH-;
②1.00×10-4
③b、a、c
(3)①2H++2e-=H ↑
2
②O +4H++4e-=2H O;
2 2
v(O) v(O) x
2 4 3 6 2,生成氧气和臭氧的体积共yL,则v(O 2 )v(O 3 ) y,因此
22.4 22.4 22.4
v(O) x 2y
3 。
y y
x2y
③
y