文档内容
2014年全国统一高考化学试卷(新课标Ⅰ)
一、选择题(本题共7小题,每小题6分,共42分)
1.(6分)下列化合物中同分异构体数目最少的是( )
A.戊烷 B.戊醇 C.戊烯 D.乙酸乙酯
2.(6分)化学与社会、生活密切相关,对下列现象或事实的解释正确的是(
)
选项 现象或事实 解释
A 用热的烧碱溶液洗去油污 Na CO 可直接和油污反应
2 3
B 漂白粉在空气中久置变质 漂白粉中的CaCl 与空气中的
2
CO 反应生成CaCO
2 3
C 施肥时,草木灰(有效成分为K CO )不 K CO 与NH Cl反应生成氨气会
2 3 2 3 4
能与NH Cl混合使用 降低肥效
4
D FeCl 溶液可用于铜质印刷线路板制作 FeCl 能从含有Cu2+的溶液中置
3 3
换出铜
A.A B.B C.C D.D
3.(6分)已知分解1mol H O 放出热量98kJ,在含少量I﹣的溶液中,H O 分
2 2 2 2
解的机理为:
H O +I﹣→H O+IO﹣ 慢
2 2 2
H O +IO﹣→H O+O +I﹣ 快
2 2 2 2
下列有关该反应的说法正确的是( )
A.反应速率与I﹣的浓度有关 B.IO﹣也是该反应的催化剂
C.反应活化能等于98kJ•mol﹣1 D.v(H O )=v(H O)=v(O )
2 2 2 2
4.(6分)X,Y,Z均为短周期元素,X,Y处于同一周期,X,Z的最低价
离子分别为X2﹣和Z﹣,Y+和Z﹣具有相同的电子层结构。下列说法正确的是
( )
A.原子最外层电子数:X>Y>Z B.单质沸点:X>Y>Z
C.离子半径:X2﹣>Y+>Z﹣ D.原子序数:X>Y>Z
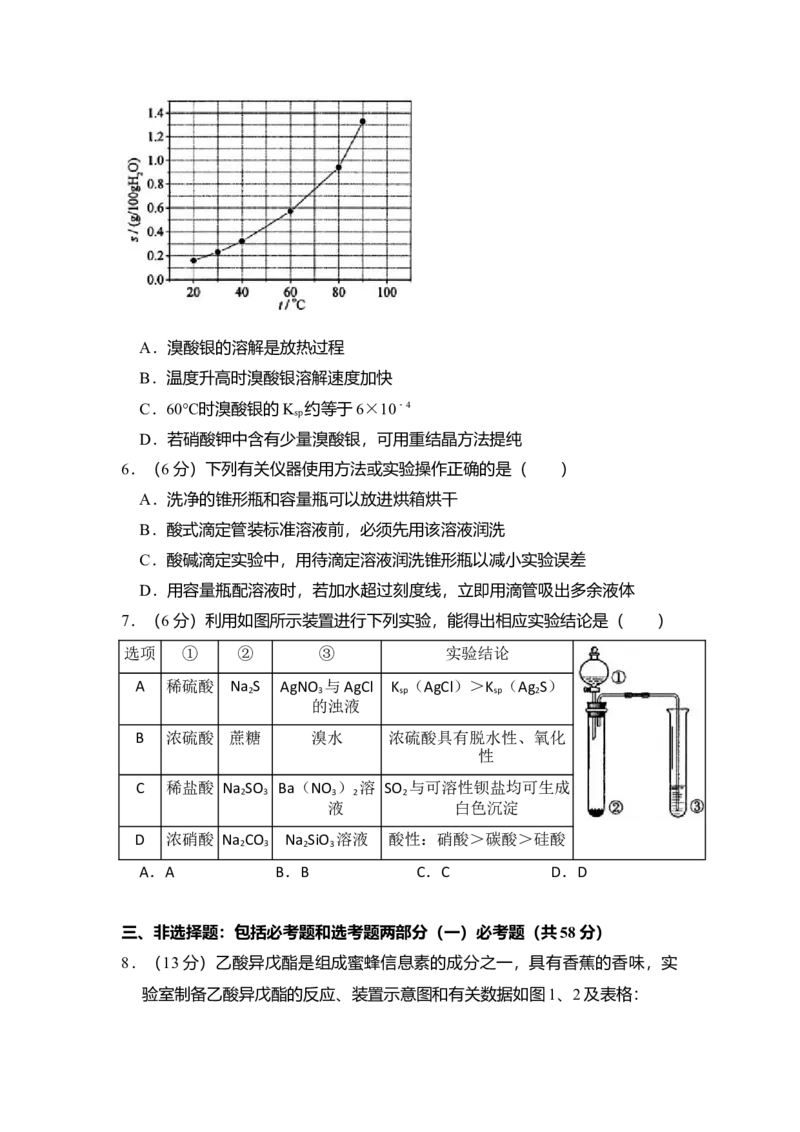
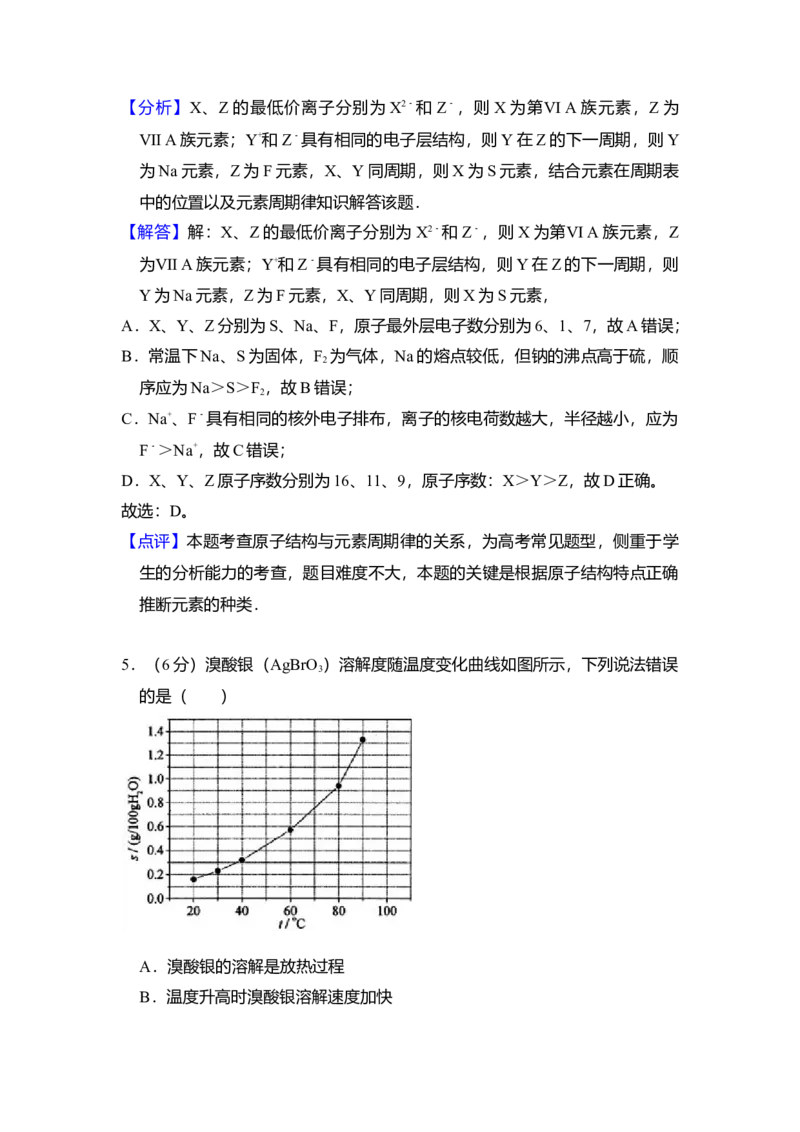
5.(6分)溴酸银(AgBrO )溶解度随温度变化曲线如图所示,下列说法错误
3
的是( )A.溴酸银的溶解是放热过程
B.温度升高时溴酸银溶解速度加快
C.60℃时溴酸银的K 约等于6×10﹣4
sp
D.若硝酸钾中含有少量溴酸银,可用重结晶方法提纯
6.(6分)下列有关仪器使用方法或实验操作正确的是( )
A.洗净的锥形瓶和容量瓶可以放进烘箱烘干
B.酸式滴定管装标准溶液前,必须先用该溶液润洗
C.酸碱滴定实验中,用待滴定溶液润洗锥形瓶以减小实验误差
D.用容量瓶配溶液时,若加水超过刻度线,立即用滴管吸出多余液体
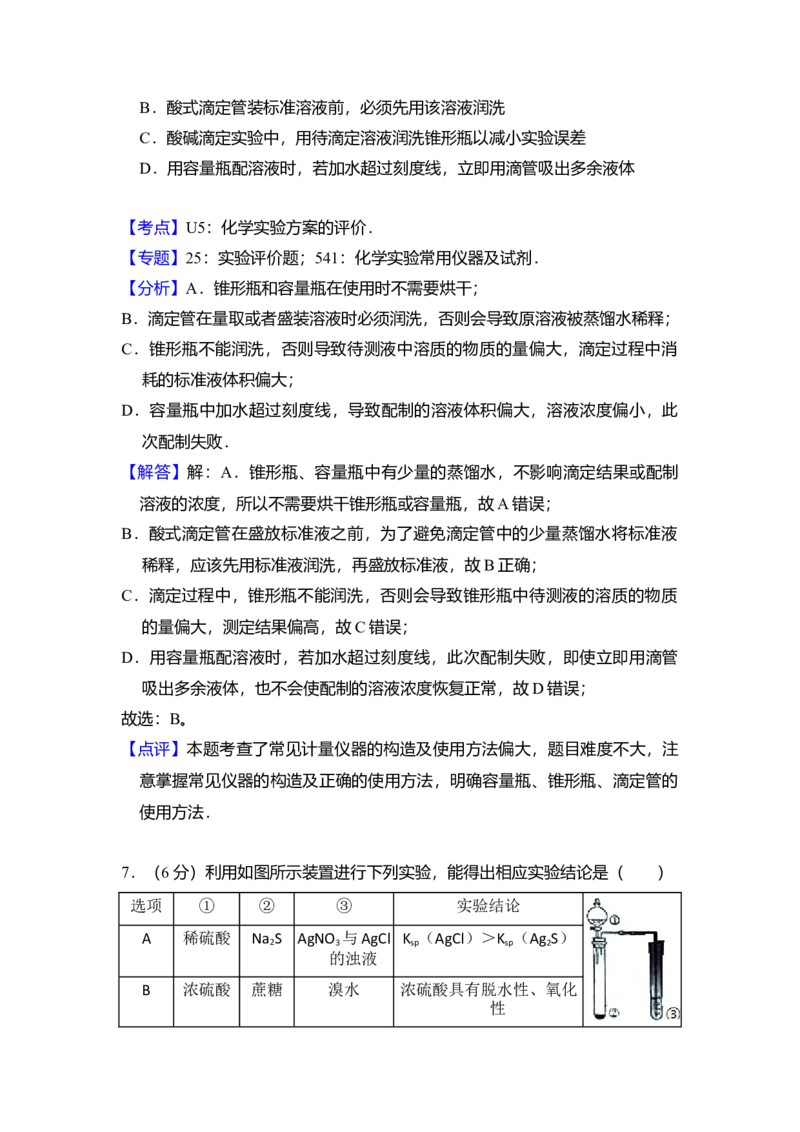
7.(6分)利用如图所示装置进行下列实验,能得出相应实验结论是( )
选项 ① ② ③ 实验结论
A 稀硫酸 Na S AgNO 与AgCl K (AgCl)>K (Ag S)
2 3 sp sp 2
的浊液
B 浓硫酸 蔗糖 溴水 浓硫酸具有脱水性、氧化
性
C 稀盐酸 Na SO Ba(NO ) 溶 SO 与可溶性钡盐均可生成
2 3 3 2 2
液 白色沉淀
D 浓硝酸 Na CO Na SiO 溶液 酸性:硝酸>碳酸>硅酸
2 3 2 3
A.A B.B C.C D.D
三、非选择题:包括必考题和选考题两部分(一)必考题(共58分)
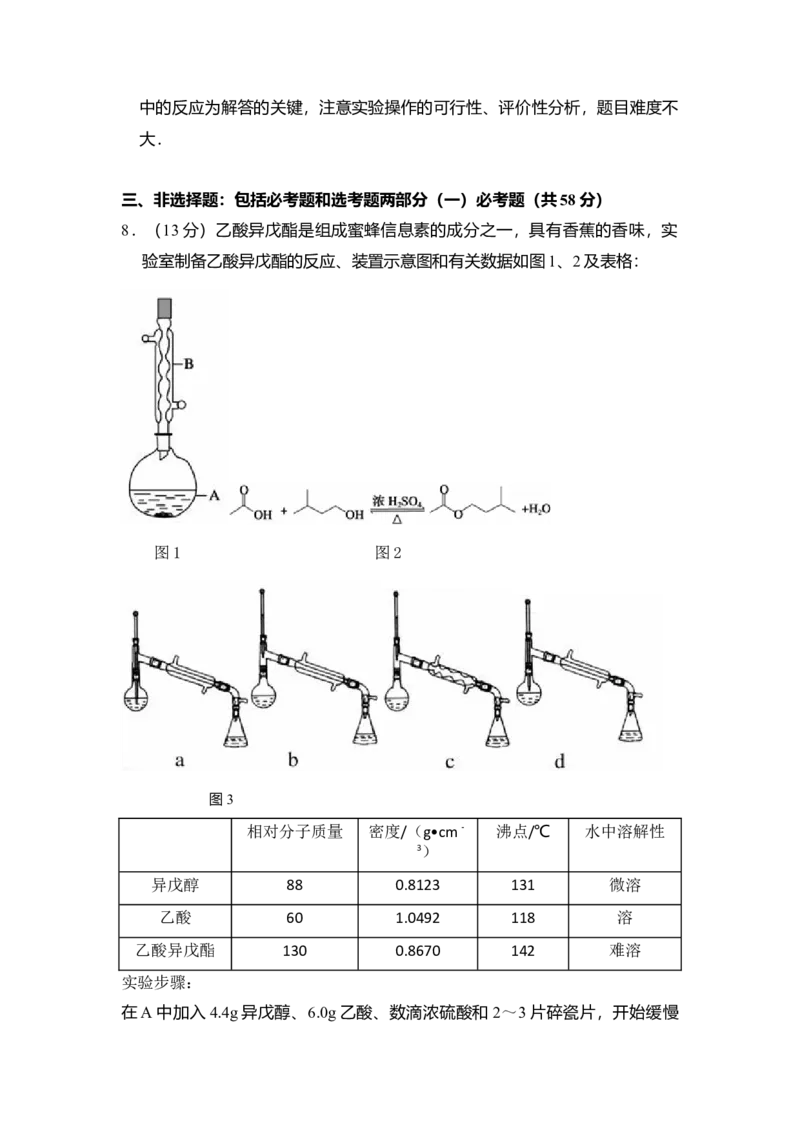
8.(13分)乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味,实
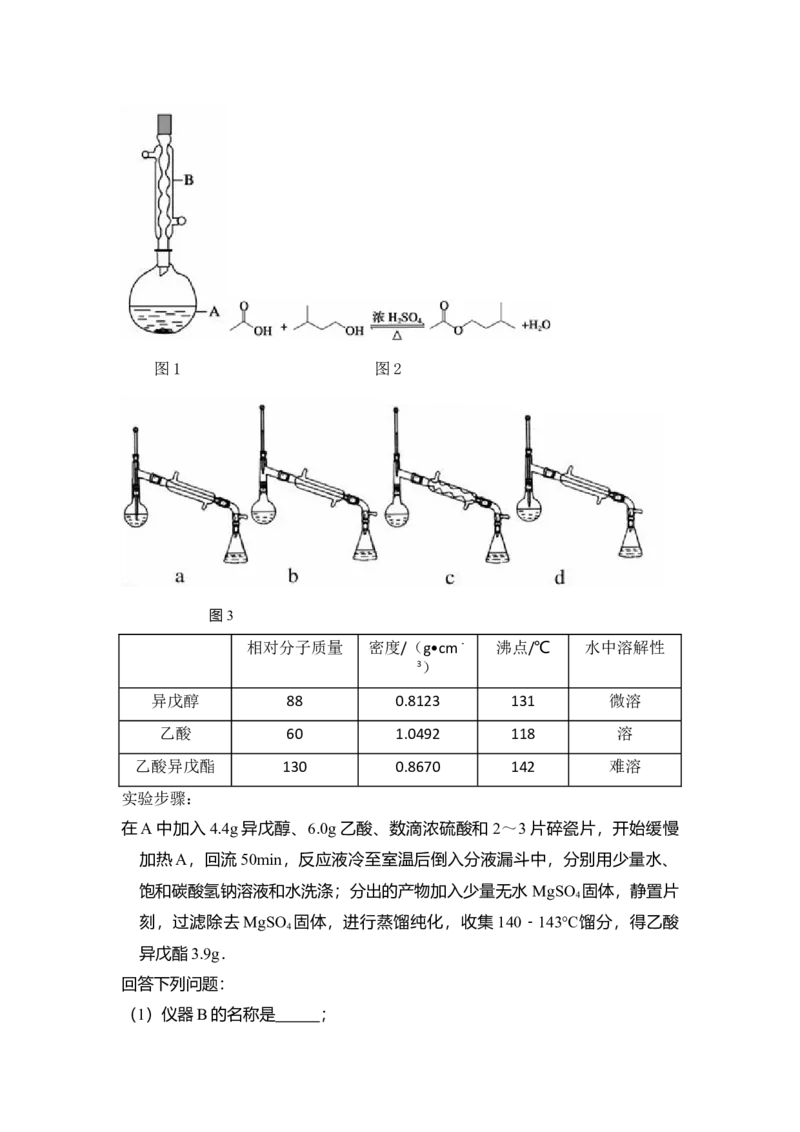
验室制备乙酸异戊酯的反应、装置示意图和有关数据如图1、2及表格:图1 图2
图3
相对分子质量 密度/(g•cm﹣ 沸点/℃ 水中溶解性
3)
异戊醇 88 0.8123 131 微溶
乙酸 60 1.0492 118 溶
乙酸异戊酯 130 0.8670 142 难溶
实验步骤:
在A中加入4.4g异戊醇、6.0g乙酸、数滴浓硫酸和 2~3片碎瓷片,开始缓慢
加热A,回流50min,反应液冷至室温后倒入分液漏斗中,分别用少量水、
饱和碳酸氢钠溶液和水洗涤;分出的产物加入少量无水 MgSO 固体,静置片
4
刻,过滤除去MgSO 固体,进行蒸馏纯化,收集 140﹣143℃馏分,得乙酸
4
异戊酯3.9g.
回答下列问题:
(1)仪器B的名称是 ;(2)在洗涤操作中,第一次水洗的主要目的是 ,第二次水洗的主要目的
是 ;
(3)在洗涤、分液操作中,应充分振荡、然后静置,待分层后 (填标
号)
a.直接将乙酸异戊酯从分液漏斗的上口倒出
b.直接将乙酸异戊酯从分液漏斗的下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口倒出
(4)本实验中加入过量乙酸的目的是 ;
(5)实验中加入少量无水MgSO 的目的是 ;
4
(6)在蒸馏操作中,仪器选择及安装都正确的是(如图3) (填标号)
(7)本实验的产率是 (填标号)
a.30% b.40% c.60% d.90%
(8)在进行蒸馏操作时,若从 130℃便开始收集馏分,会使实验的产率偏
(填“高”或“低”),其原因是 .
9.(15分)次磷酸(H PO )是一种精细磷化工产品,具有较强还原性,回答
3 2
下列问题:
(1)H PO 是一元中强酸,写出其电离方程式 ;
3 2
(2)H PO 及NaH PO 均可将溶液中的Ag+还原为银,从而可用于化学镀银。
3 2 2 2
①H PO 中,P元素的化合价为 ;
3 2
②利用H PO 进行化学镀银反应中,氧化剂与还原剂的物质的量之比为 4:1,
3 2
则氧化产物为 (填化学式);
③NaH PO 为 (填“正盐”或“酸式盐”),其溶液显 (填“弱酸性”、
2 2
“中性”或“弱碱性”);
(3)H PO 的工业制法是:将白磷(P )与Ba(OH) 溶液反应生成PH 气体
3 2 4 2 3
和Ba(H PO ) ,后者再与H SO 反应,写出白磷与Ba(OH) 溶液反应的
2 2 2 2 4 2
化学方程式 ;
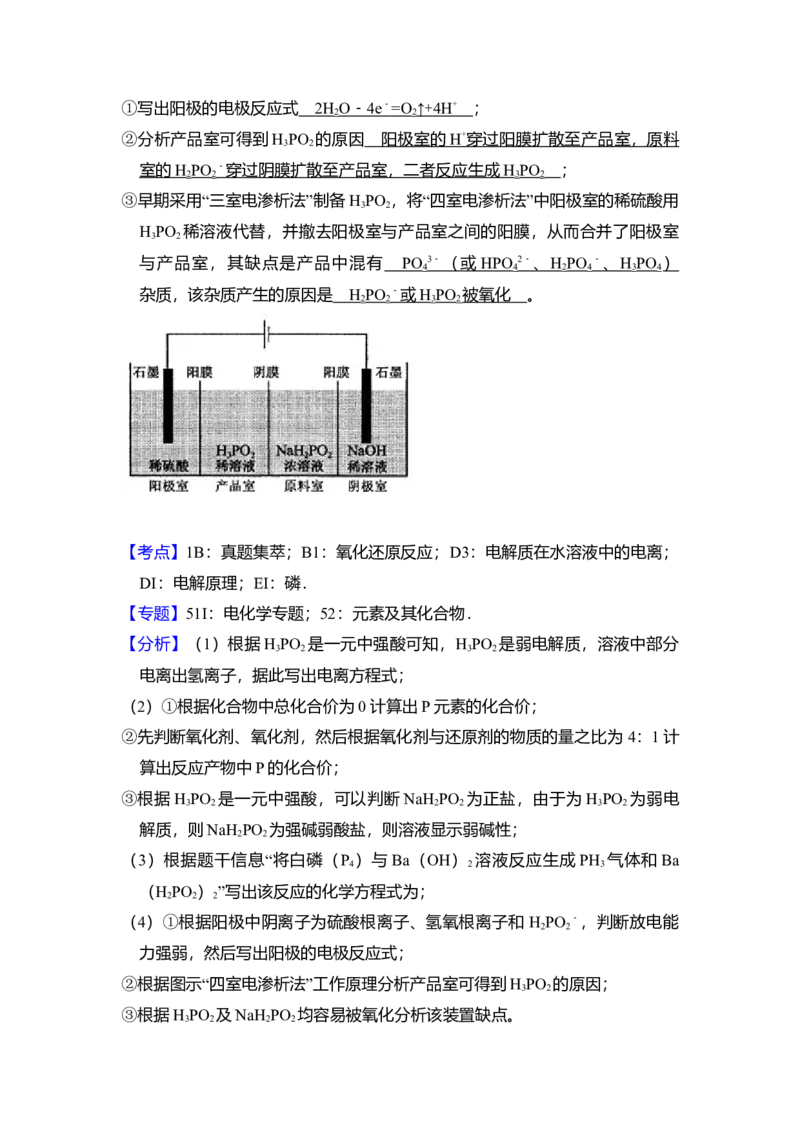
(4)H PO 也可用电渗析法制备。“四室电渗析法”工作原理如图所示(阳膜和
3 2
阴膜分别只允许阳离子、阴离子通过):
①写出阳极的电极反应式 ;②分析产品室可得到H PO 的原因 ;
3 2
③早期采用“三室电渗析法”制备H PO ,将“四室电渗析法”中阳极室的稀硫酸用
3 2
H PO 稀溶液代替,并撤去阳极室与产品室之间的阳膜,从而合并了阳极室
3 2
与产品室,其缺点是产品中混有 杂质,该杂质产生的原因是 。
10.(15分)乙醇是重要的有机化工原料,可由乙烯气相直接水合法或间接水
合法生产,回答下列问题:
(1)间接水合法是指先将乙烯与浓硫酸反应生成硫酸氢乙酯(C H OSO H),
2 5 3
再水解生成乙醇,写出相应反应的化学方程式 ;
(2)已知:
甲醇脱水反应 2CH OH(g)═CH OCH (g)+H O(g)△H =﹣23.9kJ•mol﹣1
3 3 3 2 1
甲醇制烯烃反应 2CH OH(g)═C H (g)+2H O(g)△H =﹣29.1kJ•mol﹣1
3 2 4 2 2
乙醇异构化反应 C H OH(g)═CH OCH (g)△H =+50.7kJ•mol﹣1
2 5 3 3 3
则乙烯气相直接水合反应 C H (g)+H O(g)═C H OH(g)的△H=
2 4 2 2 5
kJ•mol﹣1,与间接水合法相比,气相直接水合法的优点是 ;
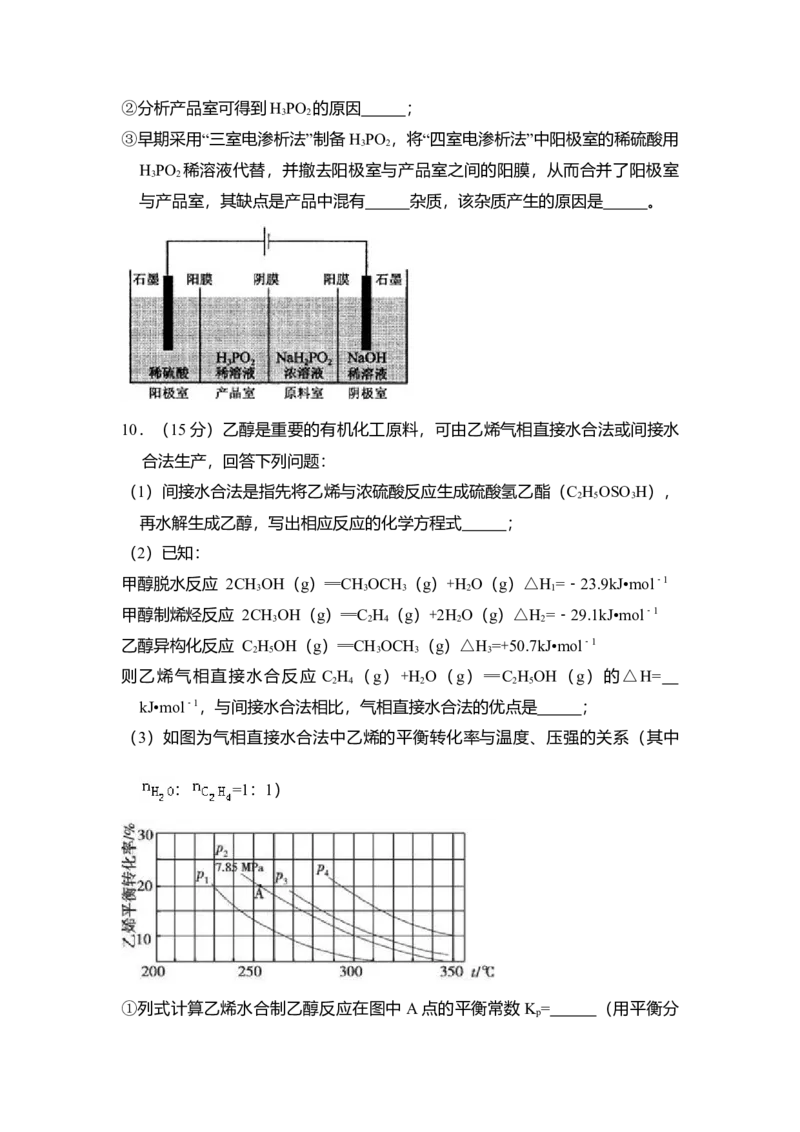
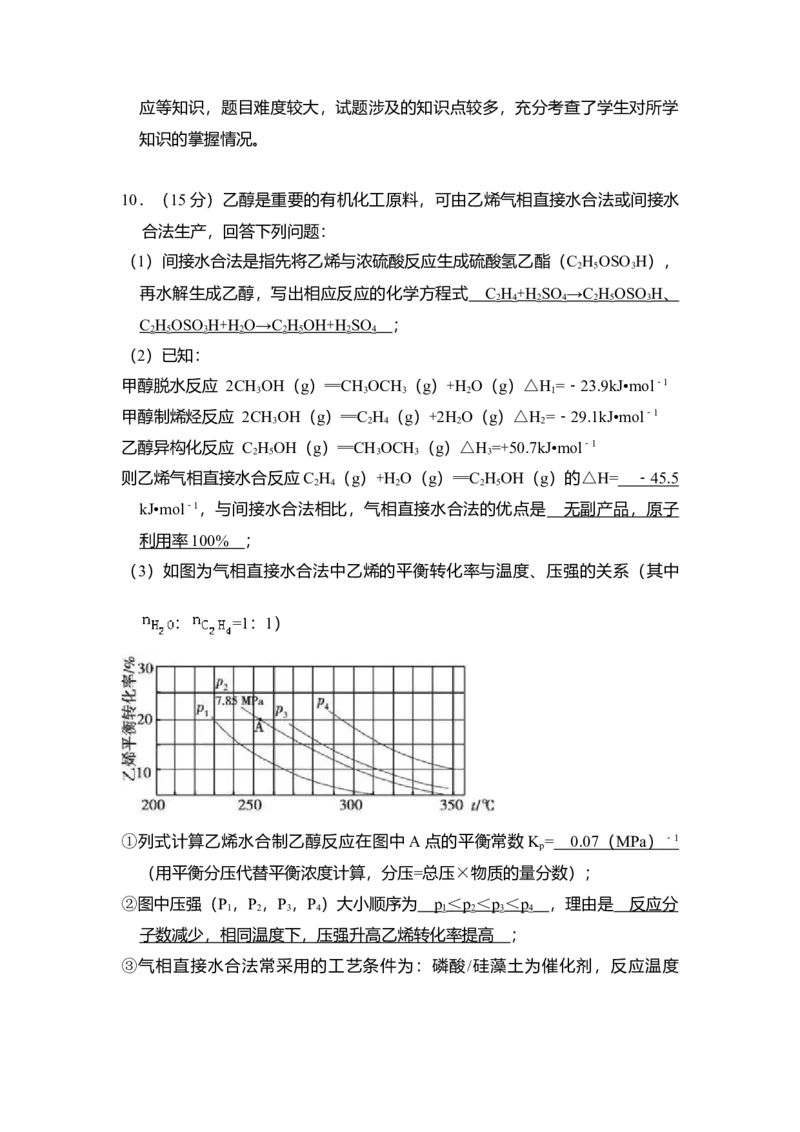
(3)如图为气相直接水合法中乙烯的平衡转化率与温度、压强的关系(其中
: =1:1)
①列式计算乙烯水合制乙醇反应在图中 A点的平衡常数K = (用平衡分
p压代替平衡浓度计算,分压=总压×物质的量分数);
②图中压强(P ,P ,P ,P )大小顺序为 ,理由是 ;
1 2 3 4
③气相直接水合法常采用的工艺条件为:磷酸/硅藻土为催化剂,反应温度
290℃,压强6.9MPa, : =0.6:1,乙烯的转化率为5%,若要进一
步提高乙烯转化率,除了可以适当改变反应温度和压强外,还可以采取的措
施有 、 。
【化学-选修2:化学与技术】
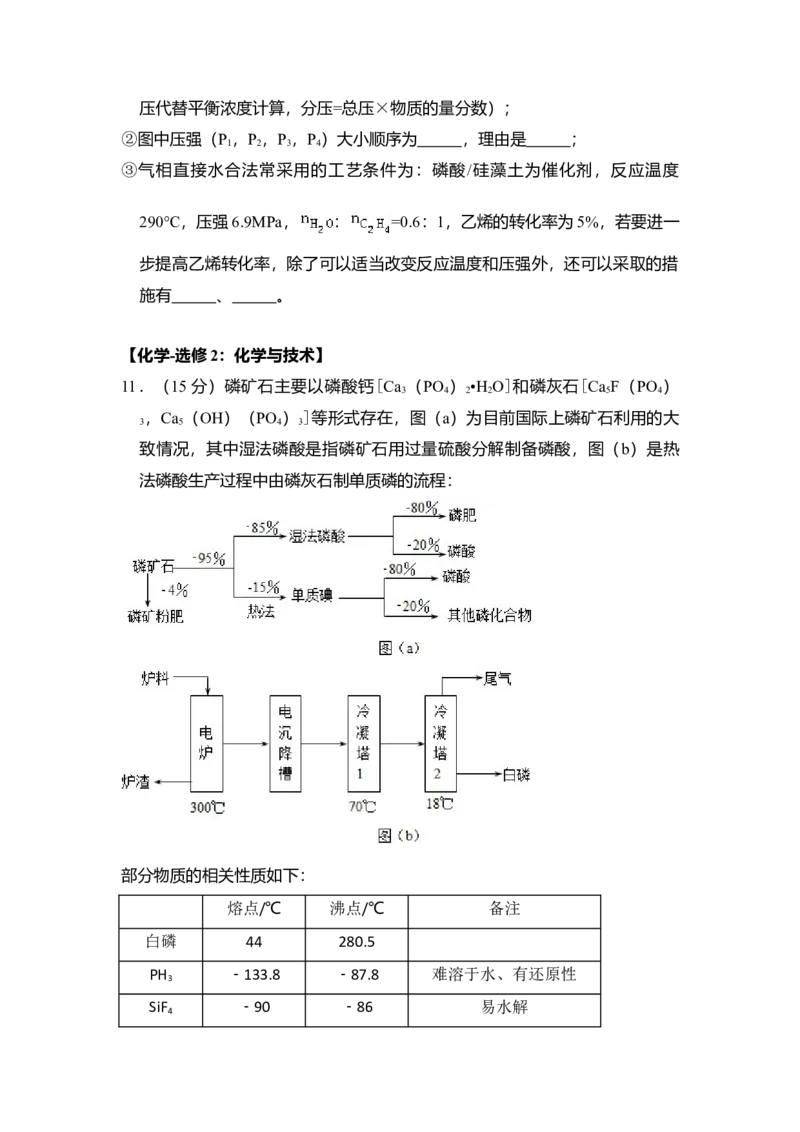
11.(15分)磷矿石主要以磷酸钙[Ca (PO ) •H O]和磷灰石[Ca F(PO )
3 4 2 2 5 4
,Ca (OH)(PO ) ]等形式存在,图(a)为目前国际上磷矿石利用的大
3 5 4 3
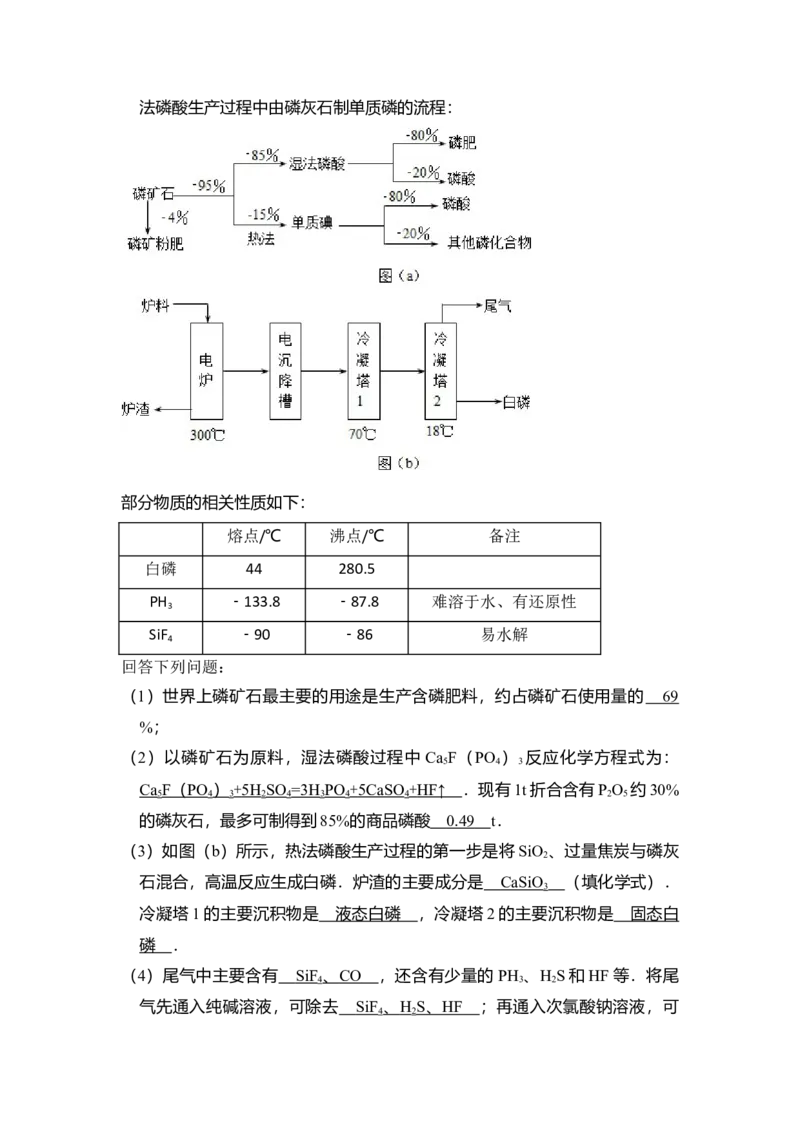
致情况,其中湿法磷酸是指磷矿石用过量硫酸分解制备磷酸,图(b)是热
法磷酸生产过程中由磷灰石制单质磷的流程:
部分物质的相关性质如下:
熔点/℃ 沸点/℃ 备注
白磷 44 280.5
PH ﹣133.8 ﹣87.8 难溶于水、有还原性
3
SiF ﹣90 ﹣86 易水解
4回答下列问题:
(1)世界上磷矿石最主要的用途是生产含磷肥料,约占磷矿石使用量的
%;
(2)以磷矿石为原料,湿法磷酸过程中 Ca F(PO ) 反应化学方程式为:
5 4 3
.现有1t折合含有P O 约30%的磷灰石,最多可制得到85%的商品磷酸
2 5
t.
(3)如图(b)所示,热法磷酸生产过程的第一步是将SiO 、过量焦炭与磷灰
2
石混合,高温反应生成白磷.炉渣的主要成分是 (填化学式).冷凝
塔1的主要沉积物是 ,冷凝塔2的主要沉积物是 .
(4)尾气中主要含有 ,还含有少量的PH 、H S和HF等.将尾气先通入
3 2
纯碱溶液,可除去 ;再通入次氯酸钠溶液,可除去 .(均填化
学式)
(5)相比于湿法磷酸,热法磷酸工艺复杂,能耗高,但优点是 .
【化学-选修3:物质结构与性质】
12.早期发现的一种天然二十面体准晶颗粒由Al、Cu、Fe三种金属元素组成,
回答下列问题:
(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过
方法区分晶体、准晶体和非晶体.
(2)基态Fe原子有 个未成对电子,Fe3+的电子排布式为 ,可用硫
氰化钾检验Fe3+,形成的配合物的颜色为 .
(3)新制备的 Cu(OH) 可将乙醛(CH CHO)氧化成乙酸,而自身还原成
2 3
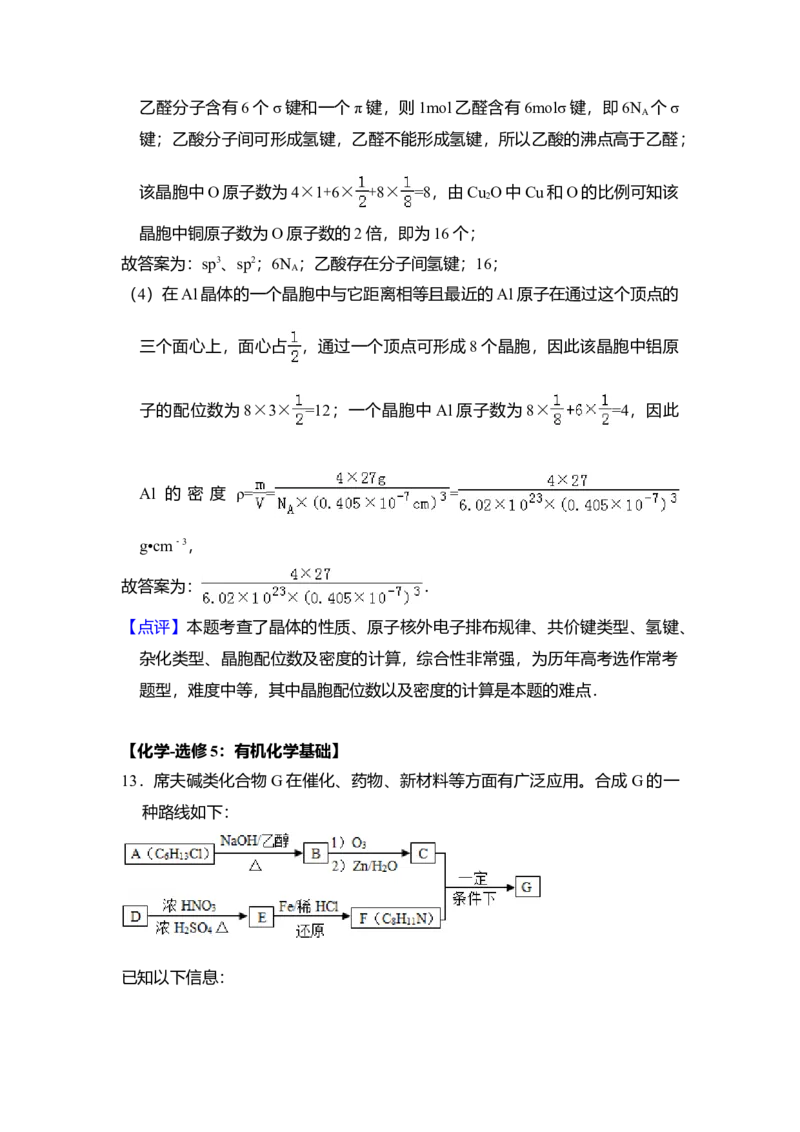
Cu O,乙醛中碳原子的杂化轨道类型为 ;1mol乙醛分子中含有的σ键
2
的数目为 ,乙酸的沸点明显高于乙醛,其主要原因是 .Cu O为
2
半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,
则该晶胞中有 个铜原子.
(4)Al单质为面心立方晶体,其晶胞参数a=0.405nm,晶胞中铝原子的配位数
为 ,列式表示Al单质的密度 g•cm﹣3(不必计算出结果).
【化学-选修5:有机化学基础】13.席夫碱类化合物G在催化、药物、新材料等方面有广泛应用。合成 G的一
种路线如下:
已知以下信息:
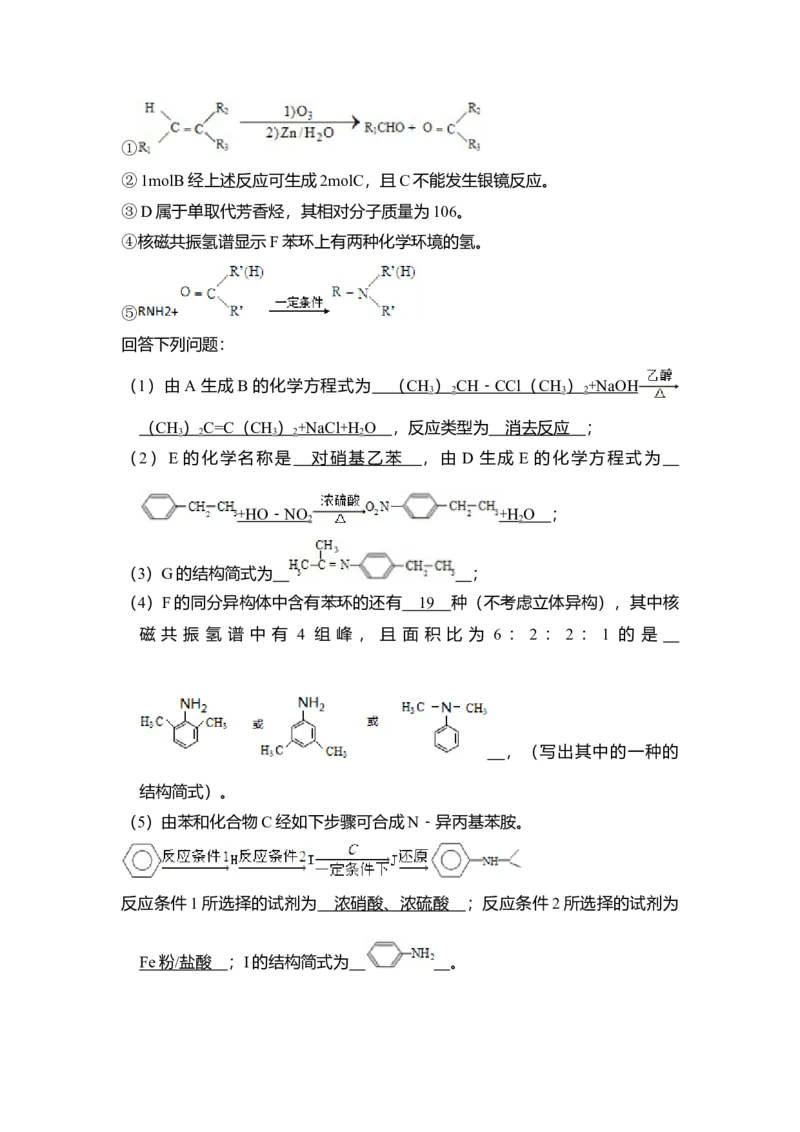
①
②1molB经上述反应可生成2molC,且C不能发生银镜反应。
③D属于单取代芳香烃,其相对分子质量为106。
④核磁共振氢谱显示F苯环上有两种化学环境的氢。
⑤
回答下列问题:
(1)由A生成B的化学方程式为 ,反应类型为 ;
(2)E的化学名称是 ,由D生成E的化学方程式为 ;
(3)G的结构简式为 ;
(4)F的同分异构体中含有苯环的还有 种(不考虑立体异构),其中核
磁共振氢谱中有4组峰,且面积比为6:2:2:1的是 ,(写出其中的
一种的结构简式)。
(5)由苯和化合物C经如下步骤可合成N﹣异丙基苯胺。
反应条件1所选择的试剂为 ;反应条件2所选择的试剂为 ;I的结
构简式为 。2014 年全国统一高考化学试卷(新课标Ⅰ)
参考答案与试题解析
一、选择题(本题共7小题,每小题6分,共42分)
1.(6分)下列化合物中同分异构体数目最少的是( )
A.戊烷 B.戊醇 C.戊烯 D.乙酸乙酯
【考点】I4:同分异构现象和同分异构体.
菁优网版权所有
【专题】531:同系物和同分异构体.
【分析】戊烷只存在碳链异构,戊醇和戊烯存在碳链异构、位置异构,乙酸乙
酯存在碳链异构、官能团异构、位置异构.
【解答】解:戊烷只存在碳链异构,同分异构体为3种,而戊醇和戊烯存在碳
链异构、位置异构,乙酸乙酯存在碳链异构、官能团异构、位置异构,异构
类型越多,同分异构体的数目越多,因此戊醇、戊烯和乙酸乙酯的同分异构
体的数目均大于3种,
故选:A。
【点评】本题主要考查了同分异构体数目的判断,可通过同分异构体的类型进
行简单判断,难度不大.
2.(6分)化学与社会、生活密切相关,对下列现象或事实的解释正确的是(
)
选项 现象或事实 解释
A 用热的烧碱溶液洗去油污 Na CO 可直接和油污反
2 3
应
B 漂白粉在空气中久置变质 漂白粉中的 CaCl 与空气
2
中的CO 反
2
应生成CaCO
3
C 施肥时,草木灰(有效成分为K CO )K CO 与 NH Cl 反应生成
2 3 2 3 4不能 氨气会降低
与NH Cl混合使用 肥效
4
D FeCl 溶液可用于铜质印刷线路板制作 FeCl 能从含有 Cu2+的溶
3 3
液中置换出铜
A.A B.B C.C D.D
【考点】FH:硅和二氧化硅;GF:钠的重要化合物;GL:两性氧化物和两性
氢氧化物;IC:乙烯的用途.
菁优网版权所有
【分析】A.依据盐类水解的性质及油脂水解的性质解答;
B.漂白粉漂白原理为次氯酸钙与二氧化碳、水反应生成碳酸钙和次氯酸;
C.依据盐类水解的性质解答;
D.氯化铁能够与铜反应生成氯化亚铁和氯化铜.
【解答】解:A.油脂在碱性环境下水解生成可溶性物质,碳酸钠为强碱弱酸
盐水解显碱性,升高温度促进盐类水解,所以用热的纯碱溶液洗去油污,碳
酸钠与油脂不直接反应,故A错误;
B.漂白粉漂白原理为次氯酸钙与二氧化碳、水反应生成碳酸钙和次氯酸,次
氯酸具有漂白作用,二氧化碳与氯化钙不反应,故B错误;
C.碳酸钾和氯化铵在溶液中水解促进生成氨气,降低肥效,施肥时,草木灰
(有效成分为K CO )不能与NH Cl混合使用,故C正确;
2 3 4
D.氯化铁能够与铜反应生成氯化亚铁和氯化铜,铜不能置换铁,故D错误。
故选:C。
【点评】本题考查化学实验方案的评价,涉及盐类水解的分析应用、氧化性强
弱判断等,掌握物质性质和反应实质是关键,为高考常见题型,注意相关知
识的学习与积累,难度不大.
3.(6分)已知分解1mol H O 放出热量98kJ,在含少量I﹣的溶液中,H O 分
2 2 2 2
解的机理为:
H O +I﹣→H O+IO﹣ 慢
2 2 2
H O +IO﹣→H O+O +I﹣ 快
2 2 2 2
下列有关该反应的说法正确的是( )
A.反应速率与I﹣的浓度有关 B.IO﹣也是该反应的催化剂C.反应活化能等于98kJ•mol﹣1 D.v(H O )=v(H O)=v(O )
2 2 2 2
【考点】16:化学反应的基本原理;17:化学反应的能量变化规律;BB:反应
热和焓变;CA:化学反应速率的影响因素.
菁优网版权所有
【专题】513:物质的性质和变化专题;517:化学反应中的能量变化.
【分析】A、反应速率的快慢主要决定于反应速率慢的第一步反应;
B、反应的催化剂是I﹣;
C、分解1mol过氧化氢放出的热量是其△H.而非活化能;
D、在一个化学反应中,用各物质表示的速率之比等于化学计量数之比;
【解答】解:A、已知:①H O +I﹣→H O+IO﹣ 慢 ②H O +IO﹣→H O+O +I﹣ 快,
2 2 2 2 2 2 2
过氧化氢分解快慢决定于反应慢的①,I﹣是①的反应物之一,其浓度大小对
反应不可能没有影响,例如,其浓度为0时反应不能发生,故A正确;
B、将反应①+②可得总反应方程式,反应的催化剂是I﹣,IO﹣只是中间产物,
故B错误;
C、1mol过氧化氢分解的△H=﹣98KJ/mol,△H不是反应的活化能,是生成物
与反应物的能量差,故C错误;
D、因为反应是在含少量I﹣的溶液中进行的,溶液中水的浓度是常数,不能用
其浓度变化表示反应速率,故D错误。故选:A。
【点评】本题是2014年河北高考题,题目主要考查催化剂、活化能、化学反应
速率的相关知识,题目难度不大.
4.(6分)X,Y,Z均为短周期元素,X,Y处于同一周期,X,Z的最低价
离子分别为X2﹣和Z﹣,Y+和Z﹣具有相同的电子层结构。下列说法正确的是
( )
A.原子最外层电子数:X>Y>Z B.单质沸点:X>Y>Z
C.离子半径:X2﹣>Y+>Z﹣ D.原子序数:X>Y>Z
【考点】1B:真题集萃;8F:原子结构与元素周期律的关系.
菁优网版权所有
【专题】51C:元素周期律与元素周期表专题.【分析】X、Z 的最低价离子分别为 X2﹣和 Z﹣,则 X 为第Ⅵ A 族元素,Z 为
ⅦA族元素;Y+和Z﹣具有相同的电子层结构,则Y在Z的下一周期,则Y
为Na元素,Z为F元素,X、Y同周期,则X为S元素,结合元素在周期表
中的位置以及元素周期律知识解答该题.
【解答】解:X、Z的最低价离子分别为 X2﹣和Z﹣,则X为第ⅥA族元素,Z
为ⅦA族元素;Y+和Z﹣具有相同的电子层结构,则Y在Z的下一周期,则
Y为Na元素,Z为F元素,X、Y同周期,则X为S元素,
A.X、Y、Z分别为S、Na、F,原子最外层电子数分别为6、1、7,故A错误;
B.常温下Na、S为固体,F 为气体,Na的熔点较低,但钠的沸点高于硫,顺
2
序应为Na>S>F ,故B错误;
2
C.Na+、F﹣具有相同的核外电子排布,离子的核电荷数越大,半径越小,应为
F﹣>Na+,故C错误;
D.X、Y、Z原子序数分别为16、11、9,原子序数:X>Y>Z,故D正确。
故选:D。
【点评】本题考查原子结构与元素周期律的关系,为高考常见题型,侧重于学
生的分析能力的考查,题目难度不大,本题的关键是根据原子结构特点正确
推断元素的种类.
5.(6分)溴酸银(AgBrO )溶解度随温度变化曲线如图所示,下列说法错误
3
的是( )
A.溴酸银的溶解是放热过程
B.温度升高时溴酸银溶解速度加快C.60℃时溴酸银的K 约等于6×10﹣4
sp
D.若硝酸钾中含有少量溴酸银,可用重结晶方法提纯
【考点】62:溶解度、饱和溶液的概念;DH:难溶电解质的溶解平衡及沉淀转
化的本质.
菁优网版权所有
【专题】519:物质的量浓度和溶解度专题.
【分析】A.根据图象中温度对溴酸银的溶解度影响可知溴酸银的溶解过程为
吸热过程;
B.温度升高,可以加快物质的溶解速率;
C.根据溶度积表达式及溶液中银离子和溴酸根离子的浓度计算;
D.溴酸银的溶解度受温度的影响较小,可以通过重结晶法分离硝酸钾与溴酸
银的混合物。
【解答】解:A.根据图象可知,升高温度,溴酸银的溶解度增大,说明溴酸
银的溶解过程为吸热过程,故A错误;
B.升高温度,溴酸银的溶解度增大,所以温度升高时溴酸银溶解速度加快,
故B正确;
C.60℃时溴酸银的溶解度为0.6g,溴酸银的物质的量为: ≈2.5×10﹣
3mol,100.6g溴酸银溶液的体积约为 100.6mL,溶液中银离子、溴酸根离子
浓度约为 2.5×10﹣2mol/L,所以 60℃时溴酸银的 K =2.5×10﹣2×2.5×10﹣
sp
2≈6×10﹣4,故C正确;
D.根据图象可知,溴酸银的溶解度受温度的影响不大,而硝酸钾的溶解度受
温度影响较大,所以硝酸钾中含有少量溴酸银,可用重结晶方法提纯,故 D
正确;
故选:A。
【点评】本题考查了难溶物的溶解平衡、溶度积的表达式及计算、物质的分离
与提纯,题目难度中等,注意掌握难溶物的溶解平衡及其影响因素,明确溶
度积的概念及计算方法。
6.(6分)下列有关仪器使用方法或实验操作正确的是( )
A.洗净的锥形瓶和容量瓶可以放进烘箱烘干B.酸式滴定管装标准溶液前,必须先用该溶液润洗
C.酸碱滴定实验中,用待滴定溶液润洗锥形瓶以减小实验误差
D.用容量瓶配溶液时,若加水超过刻度线,立即用滴管吸出多余液体
【考点】U5:化学实验方案的评价.
菁优网版权所有
【专题】25:实验评价题;541:化学实验常用仪器及试剂.
【分析】A.锥形瓶和容量瓶在使用时不需要烘干;
B.滴定管在量取或者盛装溶液时必须润洗,否则会导致原溶液被蒸馏水稀释;
C.锥形瓶不能润洗,否则导致待测液中溶质的物质的量偏大,滴定过程中消
耗的标准液体积偏大;
D.容量瓶中加水超过刻度线,导致配制的溶液体积偏大,溶液浓度偏小,此
次配制失败.
【解答】解:A.锥形瓶、容量瓶中有少量的蒸馏水,不影响滴定结果或配制
溶液的浓度,所以不需要烘干锥形瓶或容量瓶,故A错误;
B.酸式滴定管在盛放标准液之前,为了避免滴定管中的少量蒸馏水将标准液
稀释,应该先用标准液润洗,再盛放标准液,故B正确;
C.滴定过程中,锥形瓶不能润洗,否则会导致锥形瓶中待测液的溶质的物质
的量偏大,测定结果偏高,故C错误;
D.用容量瓶配溶液时,若加水超过刻度线,此次配制失败,即使立即用滴管
吸出多余液体,也不会使配制的溶液浓度恢复正常,故D错误;
故选:B。
【点评】本题考查了常见计量仪器的构造及使用方法偏大,题目难度不大,注
意掌握常见仪器的构造及正确的使用方法,明确容量瓶、锥形瓶、滴定管的
使用方法.
7.(6分)利用如图所示装置进行下列实验,能得出相应实验结论是( )
选项 ① ② ③ 实验结论
A 稀硫酸 Na S AgNO 与AgCl K (AgCl)>K (Ag S)
2 3 sp sp 2
的浊液
B 浓硫酸 蔗糖 溴水 浓硫酸具有脱水性、氧化
性C 稀盐酸 Na SO Ba(NO ) SO 与可溶性钡盐均可生
2 3 3 2 2
溶液 成白色沉淀
D 浓硝酸 Na CO Na SiO 溶液 酸性:硝酸>碳酸>硅酸
2 3 2 3
A.A B.B C.C D.D
【考点】U5:化学实验方案的评价.
菁优网版权所有
【专题】25:实验评价题.
【分析】A.不发生沉淀的转化,AgNO 与AgCl的浊液中,Qc(Ag S)>K
3 2 sp
(Ag S),则生成Ag S;
2 2
B.浓硫酸使蔗糖变黑,然后C与浓硫酸发生氧化还原反应生成二氧化硫,二
氧化硫与溴水发生氧化还原反应使其褪色;
C.盐酸与亚硫酸钠生成二氧化硫,与 Ba(NO ) 溶液发生氧化还原反应生成
3 2
硫酸钡沉淀;
D.浓硝酸与碳酸钠反应生成二氧化碳,但浓硝酸易挥发,硝酸、碳酸均可与
硅酸钠溶液反应生成硅酸沉淀.
【解答】解:A.图中装置和试剂不发生沉淀的转化,对AgNO 与AgCl的浊液
3
中,Qc(Ag S)>K (Ag S),则生成Ag S,可发生沉淀的生成,则不能
2 sp 2 2
比较溶度积,故A错误;
B.浓硫酸具有脱水性使蔗糖变黑,然后 C与浓硫酸发生氧化还原反应生成二
氧化硫,体现其强氧化性,最后二氧化硫与溴水发生氧化还原反应使其褪色,
故B正确;
C.盐酸与亚硫酸钠生成二氧化硫,与 Ba(NO ) 溶液发生氧化还原反应生成
3 2
硫酸钡沉淀,但SO 与可溶性钡盐不一定生成白色沉淀,如与氯化钡不反应,
2
故C错误;
D.浓硝酸与碳酸钠反应生成二氧化碳,但浓硝酸易挥发,硝酸、碳酸均可与
硅酸钠溶液反应生成硅酸沉淀,则不能比较碳酸与硅酸的酸性,应排除硝酸
的干扰,故D错误;
故选:B。
【点评】本题考查化学实验方案的评价,为高频考点,涉及沉淀的生成与转化、
浓硫酸的性质、酸性比较、氧化还原反应等,把握化学反应原理及实验装置中的反应为解答的关键,注意实验操作的可行性、评价性分析,题目难度不
大.
三、非选择题:包括必考题和选考题两部分(一)必考题(共58分)
8.(13分)乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味,实
验室制备乙酸异戊酯的反应、装置示意图和有关数据如图1、2及表格:
图1 图2
图3
相对分子质量 密度/(g•cm﹣ 沸点/℃ 水中溶解性
3)
异戊醇 88 0.8123 131 微溶
乙酸 60 1.0492 118 溶
乙酸异戊酯 130 0.8670 142 难溶
实验步骤:
在A中加入4.4g异戊醇、6.0g乙酸、数滴浓硫酸和 2~3片碎瓷片,开始缓慢加热A,回流50min,反应液冷至室温后倒入分液漏斗中,分别用少量水、
饱和碳酸氢钠溶液和水洗涤;分出的产物加入少量无水 MgSO 固体,静置片
4
刻,过滤除去MgSO 固体,进行蒸馏纯化,收集 140﹣143℃馏分,得乙酸
4
异戊酯3.9g.
回答下列问题:
(1)仪器B的名称是 球形冷凝管 ;
(2)在洗涤操作中,第一次水洗的主要目的是 洗掉大部分硫酸和醋酸 ,第
二次水洗的主要目的是 洗掉碳酸氢钠 ;
(3)在洗涤、分液操作中,应充分振荡、然后静置,待分层后 d (填标
号)
a.直接将乙酸异戊酯从分液漏斗的上口倒出
b.直接将乙酸异戊酯从分液漏斗的下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口倒出
(4)本实验中加入过量乙酸的目的是 提高醇的转化率 ;
(5)实验中加入少量无水MgSO 的目的是 干燥乙酸异戊酯 ;
4
(6)在蒸馏操作中,仪器选择及安装都正确的是(如图3) b (填标号)
(7)本实验的产率是 c (填标号)
a.30% b.40% c.60% d.90%
(8)在进行蒸馏操作时,若从 130℃便开始收集馏分,会使实验的产率偏 高
(填“高”或“低”),其原因是 会收集少量未反应的异戊醇 .
【考点】U3:制备实验方案的设计.
菁优网版权所有
【专题】24:实验设计题.
【分析】(1)根据题中仪器B的构造判断该仪器的名称;
(2)在洗涤操作中,第一次洗涤的主要目的是除去大部分催化剂硫酸和醋酸;
第二次水洗,主要目的是除去产品中残留的碳酸氢钠;
(3)根据乙酸异戊酯的密度及正确的分液操作方法进行解答;
(4)根据反应物对增加一种反应物的浓度,可以使另一种反应物的转化率提高
进行判断加入过量乙酸的目的;
(5)少量无水硫酸镁能够吸收乙酸异戊酯中少量的水分,起到干燥作用;(6)先根据温度计在蒸馏操作中的作用排除ad,再根据球形冷凝管容易使产
品滞留,不能全部收集到锥形瓶中,得出正确结论;
(7)先计算出乙酸和异戊醇的物质的量,然后判断过量情况,根据不足量计算
出理论上生成乙酸异戊酯的物质的量,最后根据实际上制取的乙酸异戊酯计
算出产率;
(8)若从130℃便开始收集馏分此时的蒸气中含有异戊醇,会收集少量的未反
应的异戊醇,导致获得的乙酸异戊酯质量偏大.
【解答】解:(1)由装置中仪器B的构造可知,仪器B的名称为球形冷凝管,
故答案为:球形冷凝管;
(2)反应后的溶液要经过多次洗涤,在洗涤操作中,第一次洗涤的主要目的是
除去大部分催化剂硫酸和醋酸;第一步中饱和碳酸氢钠溶液既可以除去未洗
净的醋酸,也可以降低酯的溶解度,但第一步洗涤后生成的酯中混有碳酸氢
钠,所以第二次水洗,主要目的是除去产品中残留的碳酸氢钠,
故答案为:洗掉大部分硫酸和醋酸;洗掉碳酸氢钠;
(3)由于酯的密度比水小,二者互不相溶,因此水在下层,酯在上层;分液时,
要先将水层从分液漏斗的下口放出,待到两层液体界面时关闭分液漏斗的活
塞,再将乙酸异戊酯从上口放出,所以正确的为d,
故答案为:d;
(4)酯化反应是可逆反应,增大反应物的浓度可以使平衡正向移动;增加一种
反应物的浓度,可以使另一种反应物的转化率提高,因此本实验中加入过量
乙酸的目的是提高转化率,
故答案为:提高醇的转化率;
(5)实验中加入少量无水硫酸镁的目的是吸收酯中少量的水分,对其进行干燥,
故答案为:干燥乙酸异戊酯;
(6)在蒸馏操作中,温度计的水银球要放在蒸馏烧瓶的支管口处,所以 ad错
误;c中使用的是球形冷凝管容易使产品滞留,不能全部收集到锥形瓶中,
因此仪器及装置安装正确的是b,
故答案为:b;
(7)乙酸的物质的量为:n= =0.1mol,异戊醇的物质的量为:n==0.05mol,由于乙酸和异戊醇是按照1:1进行反应,所以乙酸过量,
生成乙酸异戊酯的量要按照异戊醇的物质的量计算,即理论上生成0.05mol
乙酸异戊酯;实际上生成的乙酸异戊酯的物质的量为: =0.03mol,
所以实验中乙酸异戊酯的产率为: ×100%=60%,
故答案为:c;
(8)在进行蒸馏操作时,若从130℃便开始收集馏分此时的蒸气中含有异戊醇,
会收集少量的未反应的异戊醇,因此会导致产率偏高,
故答案为:高;会收集少量未反应的异戊醇.
【点评】本题为一道高考题,考查了常见仪器的构造与安装、混合物的分离、
提纯、物质的制取、药品的选择及使用、物质产率的计算等知识,题目难度
较大,试题涉及的题量较大,知识点较多,充分培养了学生的分析、理解能
力及灵活应用所学知识的能力.
9.(15分)次磷酸(H PO )是一种精细磷化工产品,具有较强还原性,回答
3 2
下列问题:
(1)H PO 是一元中强酸,写出其电离方程式 H PO H PO ﹣ + H + ;
3 2 3 2 2 2
(2)H PO 及NaH PO 均可将溶液中的Ag+还原为银,从而可用于化学镀银。
3 2 2 2 ⇌
①H PO 中,P元素的化合价为 + 1 ;
3 2
②利用H PO 进行化学镀银反应中,氧化剂与还原剂的物质的量之比为 4:1,
3 2
则氧化产物为 H PO (填化学式);
3 4
③NaH PO 为 正盐 (填“正盐”或“酸式盐”),其溶液显 弱碱性 (填“弱
2 2
酸性”、“中性”或“弱碱性”);
(3)H PO 的工业制法是:将白磷(P )与Ba(OH) 溶液反应生成PH 气体
3 2 4 2 3
和Ba(H PO ) ,后者再与H SO 反应,写出白磷与Ba(OH) 溶液反应的
2 2 2 2 4 2
化学方程式 2P + 3B a ( OH ) + 6H O=3Ba ( H PO ) + 2PH ↑ ;
4 2 2 2 2 2 3
(4)H PO 也可用电渗析法制备。“四室电渗析法”工作原理如图所示(阳膜和
3 2
阴膜分别只允许阳离子、阴离子通过):①写出阳极的电极反应式 2H O﹣4e ﹣ =O ↑ + 4H + ;
2 2
②分析产品室可得到H PO 的原因 阳极室的 H + 穿过阳膜扩散至产品室,原料
3 2
室的 H PO ﹣ 穿过阴膜扩散至产品室,二者反应生成 H PO ;
2 2 3 2
③早期采用“三室电渗析法”制备H PO ,将“四室电渗析法”中阳极室的稀硫酸用
3 2
H PO 稀溶液代替,并撤去阳极室与产品室之间的阳膜,从而合并了阳极室
3 2
与产品室,其缺点是产品中混有 PO 3﹣ (或 HPO 2﹣ 、 H PO ﹣ 、 H PO )
4 4 2 4 3 4
杂质,该杂质产生的原因是 H PO ﹣ 或 H PO 被氧化 。
2 2 3 2
【考点】1B:真题集萃;B1:氧化还原反应;D3:电解质在水溶液中的电离;
DI:电解原理;EI:磷.
菁优网版权所有
【专题】51I:电化学专题;52:元素及其化合物.
【分析】(1)根据H PO 是一元中强酸可知,H PO 是弱电解质,溶液中部分
3 2 3 2
电离出氢离子,据此写出电离方程式;
(2)①根据化合物中总化合价为0计算出P元素的化合价;
②先判断氧化剂、氧化剂,然后根据氧化剂与还原剂的物质的量之比为 4:1计
算出反应产物中P的化合价;
③根据H PO 是一元中强酸,可以判断NaH PO 为正盐,由于为H PO 为弱电
3 2 2 2 3 2
解质,则NaH PO 为强碱弱酸盐,则溶液显示弱碱性;
2 2
(3)根据题干信息“将白磷(P )与Ba(OH) 溶液反应生成 PH 气体和Ba
4 2 3
(H PO ) ”写出该反应的化学方程式为;
2 2 2
(4)①根据阳极中阴离子为硫酸根离子、氢氧根离子和 H PO ﹣,判断放电能
2 2
力强弱,然后写出阳极的电极反应式;
②根据图示“四室电渗析法”工作原理分析产品室可得到H PO 的原因;
3 2
③根据H PO 及NaH PO 均容易被氧化分析该装置缺点。
3 2 2 2【解答】解:(1)H PO 是一元中强酸,溶液中部分电离出氢离子,所以其电
3 2
离方程式为:H PO H PO ﹣+H+,
3 2 2 2
故答案为:H PO H PO ﹣+H+;
3 2 2 ⇌2
(2)①H PO 中,总化合价为0,其中氢元素为+1价,氧元素为﹣2价,则P
3 2 ⇌
元素的化合价为:+1价,
故答案为:+1;
②该反应中Ag+为氧化剂,H PO 为还原剂,氧化剂与还原剂的物质的量之比为
3 2
4:1,设反应产物中P的化合价为x,根据化合价升降相等可得,4×(1﹣
0)=1×(x﹣1),解得x=5,所以氧化产物为+5价的H PO ,
3 4
故答案为:H PO ;
3 4
③由于H PO 是一元中强酸,所以NaH PO 为正盐,由于为H PO 为弱电解质,
3 2 2 2 3 2
则NaH PO 为强碱弱酸盐,溶液显示弱碱性,
2 2
故答案为:正盐;弱碱性;
(3)H PO 的工业制法是:将白磷(P )与Ba(OH) 溶液反应生成PH 气体
3 2 4 2 3
和 Ba(H PO ) ,该反应的化学方程式为:2P +3Ba(OH) +6H O=3Ba
2 2 2 4 2 2
(H PO ) +2PH ↑,
2 2 2 3
故答案为:2P +3Ba(OH) +6H O=3Ba(H PO ) +2PH ↑;
4 2 2 2 2 2 3
(4)①由于阳极中阴离子为硫酸根离子、氢氧根离子和 H PO ﹣,其中放电能
2 2
力最强的是氢氧根离子,则阳极发生的电极反应为:2H O﹣4e﹣=O ↑+4H+,
2 2
故答案为:2H O﹣4e﹣=O ↑+4H+;
2 2
②产品室可得到H PO 的原因是因为:阳极室的H+穿过阳膜扩散至产品室,原
3 2
料室的H PO ﹣穿过阴膜扩散至产品室,二者反应生成H PO ,
2 2 3 2
故答案为:阳极室的H+穿过阳膜扩散至产品室,原料室的H PO ﹣穿过阴膜扩散
2 2
至产品室,二者反应生成H PO ;
3 2
③早期采用“三室电渗析法”制备H PO ,将“四室电渗析法”中阳极室的稀硫酸用
3 2
H PO 稀溶液代替,并撤去阳极室与产品室之间的阳膜,从而合并了阳极室
3 2
与产品室,其缺点是阳极产生的氧气会把 H PO ﹣或H PO 氧化成PO 3﹣,产
2 2 3 2 4
品中混有PO 3﹣(或HPO 2﹣、H PO ﹣、H PO ),
4 4 2 4 3 4
故答案为:PO 3﹣(或HPO 2﹣、H PO ﹣、H PO );H PO ﹣或H PO 被氧化。
4 4 2 4 3 4 2 2 3 2
【点评】本题考查了盐的水解原理、电解原理、弱电解质的电离、氧化还原反应等知识,题目难度较大,试题涉及的知识点较多,充分考查了学生对所学
知识的掌握情况。
10.(15分)乙醇是重要的有机化工原料,可由乙烯气相直接水合法或间接水
合法生产,回答下列问题:
(1)间接水合法是指先将乙烯与浓硫酸反应生成硫酸氢乙酯(C H OSO H),
2 5 3
再水解生成乙醇,写出相应反应的化学方程式 C H + H SO →C H OSO H 、
2 4 2 4 2 5 3
C H OSO H + H O→C H OH + H SO ;
2 5 3 2 2 5 2 4
(2)已知:
甲醇脱水反应 2CH OH(g)═CH OCH (g)+H O(g)△H =﹣23.9kJ•mol﹣1
3 3 3 2 1
甲醇制烯烃反应 2CH OH(g)═C H (g)+2H O(g)△H =﹣29.1kJ•mol﹣1
3 2 4 2 2
乙醇异构化反应 C H OH(g)═CH OCH (g)△H =+50.7kJ•mol﹣1
2 5 3 3 3
则乙烯气相直接水合反应C H (g)+H O(g)═C H OH(g)的△H= ﹣ 45.5
2 4 2 2 5
kJ•mol﹣1,与间接水合法相比,气相直接水合法的优点是 无副产品,原子
利用率 100% ;
(3)如图为气相直接水合法中乙烯的平衡转化率与温度、压强的关系(其中
: =1:1)
①列式计算乙烯水合制乙醇反应在图中A点的平衡常数K = 0.07 ( MPa ) ﹣ 1
p
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数);
②图中压强(P ,P ,P ,P )大小顺序为 p < p < p < p ,理由是 反应分
1 2 3 4 1 2 3 4
子数减少,相同温度下,压强升高乙烯转化率提高 ;
③气相直接水合法常采用的工艺条件为:磷酸/硅藻土为催化剂,反应温度290℃,压强6.9MPa, : =0.6:1,乙烯的转化率为5%,若要进一
步提高乙烯转化率,除了可以适当改变反应温度和压强外,还可以采取的措
施有 将产物乙醇液化移去 、 增加 : 比 。
【考点】1B:真题集萃;BE:热化学方程式;C8:化学平衡常数的含义;
CB:化学平衡的影响因素;CM:转化率随温度、压强的变化曲线.
菁优网版权所有
【专题】517:化学反应中的能量变化;51E:化学平衡专题.
【分析】(1)乙烯与浓硫酸反应生成硫酸氢乙酯(C H OSO H),效仿乙酸乙
2 5 3
酯水解,将水分成氢原子和羟基生成乙醇和硫酸;
(2)利用盖斯定律构造目标热化学方程式并求焓变,气相直接水合法原子利用
率100%;
(3)①列出Kp表达式,利用三段法计算平衡分压带入表达式计算即可;
②在相同温度下由于乙烯转化率为 p <p <p <p ,由 C H (g)+H O(g)
1 2 3 4 2 4 2
→C H OH(g)可知正反应为气体体积减小的反应,根据压强对平衡移动的
2 5
影响分析;
③若要进一步提高乙烯转化率,除了可以适当改变反应温度和压强外,还可以
改变物质的浓度。
【解答】解:(1)乙烯与浓硫酸反应生成硫酸氢乙酯(C H OSO H),化学方
2 5 3
程式为C H +H SO →C H OSO H,硫酸氢乙酯水解生成乙醇和硫酸,化学方
2 4 2 4 2 5 3
程式为C H OSO H+H O→C H OH+H SO ,
2 5 3 2 2 5 2 4
故答案为:C H +H SO →C H OSO H、C H OSO H+H O→C H OH+H SO ;
2 4 2 4 2 5 3 2 5 3 2 2 5 2 4
(2)已知:甲醇脱水反应 ①2CH OH(g)═CH OCH (g)+H O(g)△H =
3 3 3 2 1
﹣23.9kJ•mol﹣1
甲醇制烯烃反应 ②2CH OH(g)═C H (g)+2H O(g)△H =﹣29.1kJ•mol﹣1
3 2 4 2 2
乙醇异构化反应 ③C H OH(g)═CH OCH (g)△H =+50.7kJ•mol﹣1,
2 5 3 3 3
根据盖斯定律①﹣②﹣③可得:C H (g)+H O(g)═C H OH(g)△H=(﹣
2 4 2 2 5
23.9+29.1﹣50.7)kJ/mol=﹣45.5kJ/mol;
乙烯直接水化法中反应物中所有原子全部都变成生成物,所以原子利用率
100%,没有副产品,故答案为:﹣45.5;无副产品,原子利用率100%;
(3)①C H (g)+H O(g)═C H OH(g)
2 4 2 2 5
开始:1 1 0
转化:0.2 0.2 0.2
平衡:0.8 0.8 0.2
乙醇占 = ,乙烯和水各占 = ,则乙醇的分压为
7.85MPa× =0.87MPa,乙烯和水的分压为7.85MPa× =3.49MPa,
所以Kp= = =0.07(MPa)﹣1,
故答案为:0.07(MPa)﹣1;
②在相同温度下由于乙烯转化率为 p <p <p <p ,由 C H (g)+H O(g)
1 2 3 4 2 4 2
═C H OH(g)可知正反应为气体体积减小的反应,所以增大压强,平衡正
2 5
向移动,乙烯的转化率提高,因此压强关系是p <p <p <p ,
1 2 3 4
故答案为:p <p <p <p ;反应分子数减少,相同温度下,压强升高乙烯转化
1 2 3 4
率提高;
③若要进一步提高乙烯转化率,除了可以适当改变反应温度和压强外,还可以
改变物质的浓度,如从平衡体系中将产物乙醇分离出来,或增大水蒸气的浓
度,改变二者物质的量的比等,
故答案为:将产物乙醇液化移去;增加 : 比。
【点评】本题考查了化学方程式的书写、压强对平衡移动的影响、物质制取方
案的比较、反应热及平衡常数的计算等知识,综合性非常强,该题是高考中
的常见题型,属于中等难度较大,侧重于学生分析问题、解决问题、知识迁
移能力的培养。
【化学-选修2:化学与技术】
11.(15分)磷矿石主要以磷酸钙[Ca (PO ) •H O]和磷灰石[Ca F(PO )
3 4 2 2 5 4
,Ca (OH)(PO ) ]等形式存在,图(a)为目前国际上磷矿石利用的大
3 5 4 3
致情况,其中湿法磷酸是指磷矿石用过量硫酸分解制备磷酸,图(b)是热法磷酸生产过程中由磷灰石制单质磷的流程:
部分物质的相关性质如下:
熔点/℃ 沸点/℃ 备注
白磷 44 280.5
PH ﹣133.8 ﹣87.8 难溶于水、有还原性
3
SiF ﹣90 ﹣86 易水解
4
回答下列问题:
(1)世界上磷矿石最主要的用途是生产含磷肥料,约占磷矿石使用量的 69
%;
(2)以磷矿石为原料,湿法磷酸过程中 Ca F(PO ) 反应化学方程式为:
5 4 3
Ca F ( PO ) + 5H SO =3H PO + 5CaSO + HF ↑ .现有1t折合含有P O 约30%
5 4 3 2 4 3 4 4 2 5
的磷灰石,最多可制得到85%的商品磷酸 0.49 t.
(3)如图(b)所示,热法磷酸生产过程的第一步是将SiO 、过量焦炭与磷灰
2
石混合,高温反应生成白磷.炉渣的主要成分是 CaSiO (填化学式).
3
冷凝塔1的主要沉积物是 液态白磷 ,冷凝塔2的主要沉积物是 固态白
磷 .
(4)尾气中主要含有 SiF 、 CO ,还含有少量的PH 、H S和HF等.将尾
4 3 2
气先通入纯碱溶液,可除去 SiF 、 H S 、 HF ;再通入次氯酸钠溶液,可
4 2除去 PH .(均填化学式)
3
(5)相比于湿法磷酸,热法磷酸工艺复杂,能耗高,但优点是 产品纯度高 .
【考点】U3:制备实验方案的设计.
菁优网版权所有
【专题】18:实验分析题;25:实验评价题;43:演绎推理法;548:制备实验
综合.
【分析】(1)由图(a)可知生产含磷肥料,约占磷矿石使用量的比例为:4%
+96%×85%×80%=69%;
(2)以磷矿石为原料,用过量的硫酸溶解 Ca F(PO ) 可制得磷酸,根据质
5 4 3
量守恒书写化学方程式;根据P元素守恒可得关系式P O ~2H PO ,依据此
2 5 3 4
关系式计算;
(3)将SiO 、过量焦炭与磷灰石混合,高温除了反应生成白磷之外,得到的难
2
溶性固体是CaSiO ;根据冷却塔1、2的温度与白磷的熔点比较分析白磷的
3
状态;
(4)二氧化硅和 HF 反应生成四氟化硅气体,过量的焦炭不完全燃烧生成
CO,因此在尾气中主要含有SiF 、CO,还含有少量的PH 、H S和HF等;
4 3 2
将尾气通入纯碱溶液,SiF 、HF、H S与碳酸钠反应而除去,次氯酸具有强
4 2
氧化性,可除掉强还原性的PH ;
3
(5)相比于湿法磷酸,热法磷酸工艺所得产品纯度大;
【解答】解:(1)由图(a)可知生产含磷肥料,约占磷矿石使用量的比例为:
4%+96%×85%×80%=69%,
故答案为:69;
(2)以磷矿石为原料,用过量的硫酸溶解 Ca F(PO ) 可制得磷酸,根据质
5 4 3
量 守 恒 定 律 可 得 反 应 的 化 学 方 程 式 为 Ca F ( PO )
5 4
+5H SO =3H PO +5CaSO +HF↑;
3 2 4 3 4 4
根据P元素守恒可得关系式 P O ~2H PO ,142份P O 可制取196份磷酸,1t
2 5 3 4 2 5
折合含有P O 约30%的磷灰石,含有P O 的质量为0.3t,所以可制得到85%
2 5 2 5
的商品磷酸的质量为 =0.49t,
故答案为:Ca F(PO ) +5H SO =3H PO +5CaSO +HF↑;0.49;
5 4 3 2 4 3 4 4(3)将SiO 、过量焦炭与磷灰石混合,高温除了反应生成白磷之外,得到的难
2
溶性固体是CaSiO ;冷却塔1的温度是70℃,280.5℃>t>44℃,所以此时
3
主要的沉积物是液态白磷;冷却塔 2的温度是18℃,低于白磷的熔点,故此
时的主要沉积物是固体白磷,
故答案为:CaSiO ;液态白磷;固态白磷;
3
(4)二氧化硅和 HF 反应生成四氟化硅气体,过量的焦炭不完全燃烧生成
CO,因此在尾气中主要含有SiF 、CO,还含有少量的PH 、H S和HF等;
4 3 2
将尾气通入纯碱溶液,SiF 、HF、H S与碳酸钠反应而除去,次氯酸具有强
4 2
氧化性,可除掉强还原性的PH ,
3
故答案为:SiF 、CO;SiF 、H S、HF;PH ;
4 4 2 3
(5)相比于湿法磷酸,热法磷酸工艺复杂,能耗高,但是所得产品纯度大,杂
质少,因此逐渐被采用,
故答案为:产品纯度高.
【点评】本题考查了化工生产流程图,涉及磷矿石的主要用途、反应原理和有
关计算,该题是高考中的常见题型,题目难度中等,侧重对学生分析问题、
解答问题能力的培养.
【化学-选修3:物质结构与性质】
12.早期发现的一种天然二十面体准晶颗粒由Al、Cu、Fe三种金属元素组成,
回答下列问题:
(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过
X 射线衍射 方法区分晶体、准晶体和非晶体.
( 2 ) 基 态 Fe 原 子 有 4 个 未 成 对 电 子 , Fe3+ 的 电 子 排 布 式 为
1s 2 2s 2 2p 6 3s 2 3p 6 3d 5 ,可用硫氰化钾检验Fe3+,形成的配合物的颜色为 血红
色 .
(3)新制备的 Cu(OH) 可将乙醛(CH CHO)氧化成乙酸,而自身还原成
2 3
Cu O,乙醛中碳原子的杂化轨道类型为 sp 3 、 sp 2 ;1mol乙醛分子中含有
2
的σ键的数目为 6N ,乙酸的沸点明显高于乙醛,其主要原因是 乙酸
A
存在分子间氢键 .Cu O为半导体材料,在其立方晶胞内部有4个氧原子,
2
其余氧原子位于面心和顶点,则该晶胞中有 16 个铜原子.(4)Al单质为面心立方晶体,其晶胞参数a=0.405nm,晶胞中铝原子的配位数
为 12 ,列式表示Al单质的密度 g•cm
﹣3(不必计算出结果).
【考点】1B:真题集萃;86:原子核外电子排布;96:共价键的形成及共价键
的主要类型;99:配合物的成键情况;9I:晶胞的计算;A6:不同晶体的结
构微粒及微粒间作用力的区别.
菁优网版权所有
【专题】51C:元素周期律与元素周期表专题;51D:化学键与晶体结构.
【分析】(1)晶体对X射线发生衍射,非晶体不发生衍射,准晶体介于二者
之间;
(2)根据Fe原子的核外电子排布式确定未成对电子数,失去电子变为铁离子
时,先失去4s上的电子后失去3d上的电子,硫氰化铁为血红色;
(3)乙醛中甲基上的C采取sp3杂化类型,醛基中的C采取sp2杂化类型;1个
乙醛分子含有6个σ键和一个π键;乙酸分子间可形成氢键导致沸点较高;
根据O数目和Cu O中Cu和O的比例计算晶胞中Cu原子的数目;
2
(4)在Al晶体的一个晶胞中与它距离相等且最近的Al原子在通过这个顶点的
三个面心上,面心占 ,通过一个顶点可形成8个晶胞.
【解答】解:(1)从外观无法区分三者,但用X光照射挥发现:晶体对X射
线发生衍射,非晶体不发生衍射,准晶体介于二者之间,因此通过有无衍射
现象即可确定,
故答案为:X射线衍射;
(2)26号元素Fe基态原子核外电子排布式为1s22s22p63s23p63d64s2,可知在3d
上存在4个未成对电子,失去电子变为铁离子时,先失去 4s上的2个电子后
失去3d上的1个电子,因此Fe3+的电子排布式为1s22s22p63s23p63d5,硫氰化
铁为血红色,
故答案为:4;1s22s22p63s23p63d5;血红色;
(3)乙醛中甲基上的C形成4条σ键,无孤电子对,因此采取sp3杂化类型,
醛基中的C形成3条σ键和1条π键,无孤电子对,采取sp2杂化类型;1个乙醛分子含有6个σ键和一个π键,则1mol乙醛含有6molσ键,即6N 个σ
A
键;乙酸分子间可形成氢键,乙醛不能形成氢键,所以乙酸的沸点高于乙醛;
该晶胞中O原子数为4×1+6× +8× =8,由Cu O中Cu和O的比例可知该
2
晶胞中铜原子数为O原子数的2倍,即为16个;
故答案为:sp3、sp2;6N ;乙酸存在分子间氢键;16;
A
(4)在Al晶体的一个晶胞中与它距离相等且最近的Al原子在通过这个顶点的
三个面心上,面心占 ,通过一个顶点可形成 8个晶胞,因此该晶胞中铝原
子的配位数为 8×3× =12;一个晶胞中Al原子数为 8× =4,因此
Al 的 密 度 ρ= = =
g•cm﹣3,
故答案为: .
【点评】本题考查了晶体的性质、原子核外电子排布规律、共价键类型、氢键、
杂化类型、晶胞配位数及密度的计算,综合性非常强,为历年高考选作常考
题型,难度中等,其中晶胞配位数以及密度的计算是本题的难点.
【化学-选修5:有机化学基础】
13.席夫碱类化合物G在催化、药物、新材料等方面有广泛应用。合成 G的一
种路线如下:
已知以下信息:①
②1molB经上述反应可生成2molC,且C不能发生银镜反应。
③D属于单取代芳香烃,其相对分子质量为106。
④核磁共振氢谱显示F苯环上有两种化学环境的氢。
⑤
回答下列问题:
(1)由 A 生成 B 的化学方程式为 ( CH ) CH﹣CCl ( CH ) + NaOH
3 2 3 2
( CH ) C=C ( CH ) + NaC l + H O ,反应类型为 消去反应 ;
3 2 3 2 2
(2)E 的化学名称是 对硝基乙苯 ,由 D 生成 E 的化学方程式为
+ HO﹣NO + H O ;
2 2
(3)G的结构简式为 ;
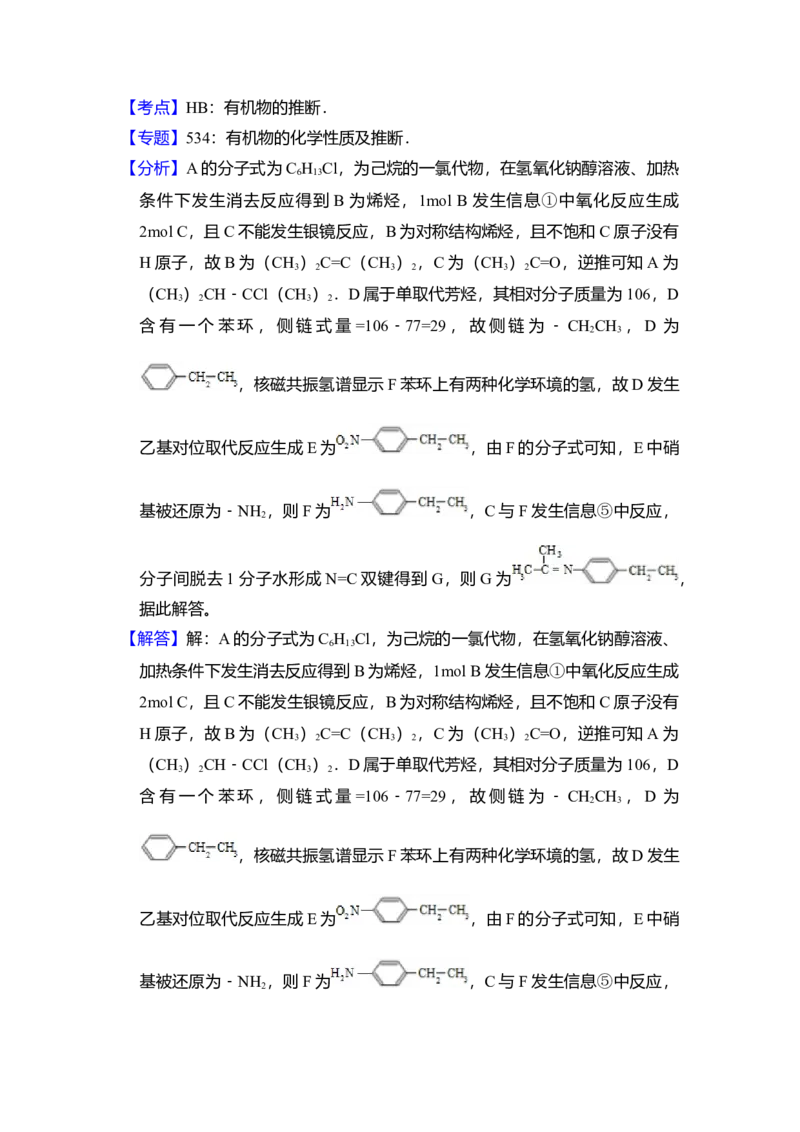
(4)F的同分异构体中含有苯环的还有 19 种(不考虑立体异构),其中核
磁 共 振 氢 谱 中 有 4 组 峰 , 且 面 积 比 为 6 : 2 : 2 : 1 的 是
,(写出其中的一种的
结构简式)。
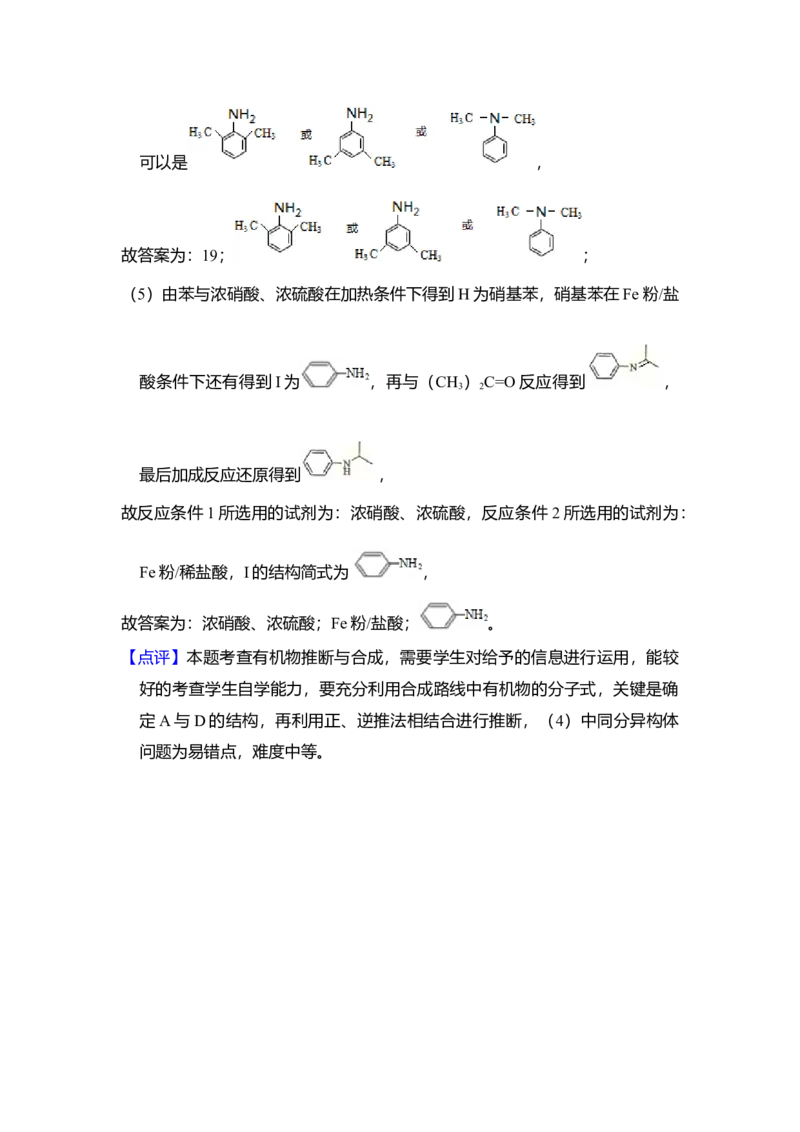
(5)由苯和化合物C经如下步骤可合成N﹣异丙基苯胺。
反应条件1所选择的试剂为 浓硝酸、浓硫酸 ;反应条件2所选择的试剂为
Fe 粉 / 盐酸 ;I的结构简式为 。【考点】HB:有机物的推断.
菁优网版权所有
【专题】534:有机物的化学性质及推断.
【分析】A的分子式为C H Cl,为己烷的一氯代物,在氢氧化钠醇溶液、加热
6 13
条件下发生消去反应得到 B 为烯烃,1mol B 发生信息①中氧化反应生成
2mol C,且C不能发生银镜反应,B为对称结构烯烃,且不饱和 C原子没有
H原子,故B为(CH ) C=C(CH ) ,C为(CH ) C=O,逆推可知A为
3 2 3 2 3 2
(CH ) CH﹣CCl(CH ) .D属于单取代芳烃,其相对分子质量为 106,D
3 2 3 2
含有一个苯环,侧链式量=106﹣77=29,故侧链为﹣CH CH ,D 为
2 3
,核磁共振氢谱显示F苯环上有两种化学环境的氢,故D发生
乙基对位取代反应生成E为 ,由F的分子式可知,E中硝
基被还原为﹣NH ,则F为 ,C与F发生信息⑤中反应,
2
分子间脱去 1分子水形成 N=C双键得到G,则G为 ,
据此解答。
【解答】解:A的分子式为C H Cl,为己烷的一氯代物,在氢氧化钠醇溶液、
6 13
加热条件下发生消去反应得到B为烯烃,1mol B发生信息①中氧化反应生成
2mol C,且C不能发生银镜反应,B为对称结构烯烃,且不饱和 C原子没有
H原子,故B为(CH ) C=C(CH ) ,C为(CH ) C=O,逆推可知A为
3 2 3 2 3 2
(CH ) CH﹣CCl(CH ) .D属于单取代芳烃,其相对分子质量为 106,D
3 2 3 2
含有一个苯环,侧链式量=106﹣77=29,故侧链为﹣CH CH ,D 为
2 3
,核磁共振氢谱显示F苯环上有两种化学环境的氢,故D发生
乙基对位取代反应生成E为 ,由F的分子式可知,E中硝
基被还原为﹣NH ,则F为 ,C与F发生信息⑤中反应,
2分子间脱去1分子水形成N=C双键得到G,则G为 。
(1)由 A 生成 B 的化学方程式为:(CH ) CH﹣CCl(CH ) +NaOH
3 2 3 2
(CH ) C=C(CH ) +NaCl+H O,属于消去反应,
3 2 3 2 2
故答案为:(CH ) CH﹣CCl(CH ) +NaOH (CH ) C=C(CH )
3 2 3 2 3 2 3
+NaCl+H O;消去反应;
2 2
(2)由上述分析可知,E为 ,化学名称是对硝基乙苯,由D
生成E的化学方程式为: +HO﹣NO
2
+H O,
2
故答案为:对硝基乙苯; +HO﹣NO
2
+H O;
2
(3)由上述分析可知,G的结构简式为 ,
故答案为: ;
(4)F为 ,含有苯环同分异构体中,
若取代基为氨基、乙基,还有邻位、间位2种,
若只有一个取代基,可以为﹣CH(NH )CH 、﹣CH CH NH 、﹣NH﹣
2 3 2 2 2
CH CH 、﹣CH NHCH 、﹣N(CH ) ,有5种;
2 3 2 3 3 2
若取代为2个,还有﹣CH 、﹣CH NH 或﹣CH 、﹣NHCH ,各有邻、间、对
3 2 2 3 3
三种,共有6种;
若取代基有3个,即﹣CH 、﹣CH 、﹣NH ,2个甲基相邻,氨基有2种位置,
3 3 2
2个甲基处于间位,氨基有3种位置,2个甲基处于对位,氨基有1种位置,
共有2+3+1=6种,
故符合条件的同分异构体有:2+5+6+6=19,
其中核磁共振氢谱为4组峰,且面积比为6:2:2:1,说明含有2个﹣CH ,
3可以是 ,
故答案为:19; ;
(5)由苯与浓硝酸、浓硫酸在加热条件下得到H为硝基苯,硝基苯在Fe粉/盐
酸条件下还有得到I为 ,再与(CH ) C=O反应得到 ,
3 2
最后加成反应还原得到 ,
故反应条件1所选用的试剂为:浓硝酸、浓硫酸,反应条件 2所选用的试剂为:
Fe粉/稀盐酸,I的结构简式为 ,
故答案为:浓硝酸、浓硫酸;Fe粉/盐酸; 。
【点评】本题考查有机物推断与合成,需要学生对给予的信息进行运用,能较
好的考查学生自学能力,要充分利用合成路线中有机物的分子式,关键是确
定A与D的结构,再利用正、逆推法相结合进行推断,(4)中同分异构体
问题为易错点,难度中等。