文档内容
山西省2011 年中考毕业生学业考试
化 学 试 卷
可能用到的相对原子质量:
H:1 C:12 N:14 O:16 S:32 Cu:64 Zn:65
第Ⅰ卷 选择题
一、选择题(在每小题给出的四个选项中,只有一项符合题目要求,请选出并在答题卡上
将该选项涂黑。每小题2分,本题共20分)
1.下列变化属于物理变化的是()
A. 冰雪融化 B. 粮食酿酒 C. 工业炼铁 D. 火箭点火
2.下列气体属于空气污染物的是()
A. O B. N C. SO D. CO
2 2 2 2
3.下列物质的用途主要利用其化学性质的是()
A. 氧气用于医疗急救 B. 干冰用于人工降雨
C. 铜、铝用于制作导线 D. 汽油用于衣物除油
4.下列物质由分子直接构成的是()
A. 铁 B. 水 C. 氯化钠 D. 金刚石
5.物质的性质决定其保存方法。固体氢氧化钠具有以下性质:①白色固体;②有腐蚀性;
③易吸收水分;④能与空气中的二氧化碳反应。由此可知,氢氧化钠固体必须密封保存
的主要原因是()
21世纪教育网
A. ①② B. ②③ C. ①③ D. ③④
6.尿素[CO(NH)]是一种常用的化肥,它可以促进植物的生长发育。下列说法正确的是()
2 2
A. 尿素是一种复合化肥
B. 尿素中碳、氧、氮、氢四种元素的质量比为1:1:2:4
C. 一个年审分子中含有一个一氧化碳分子
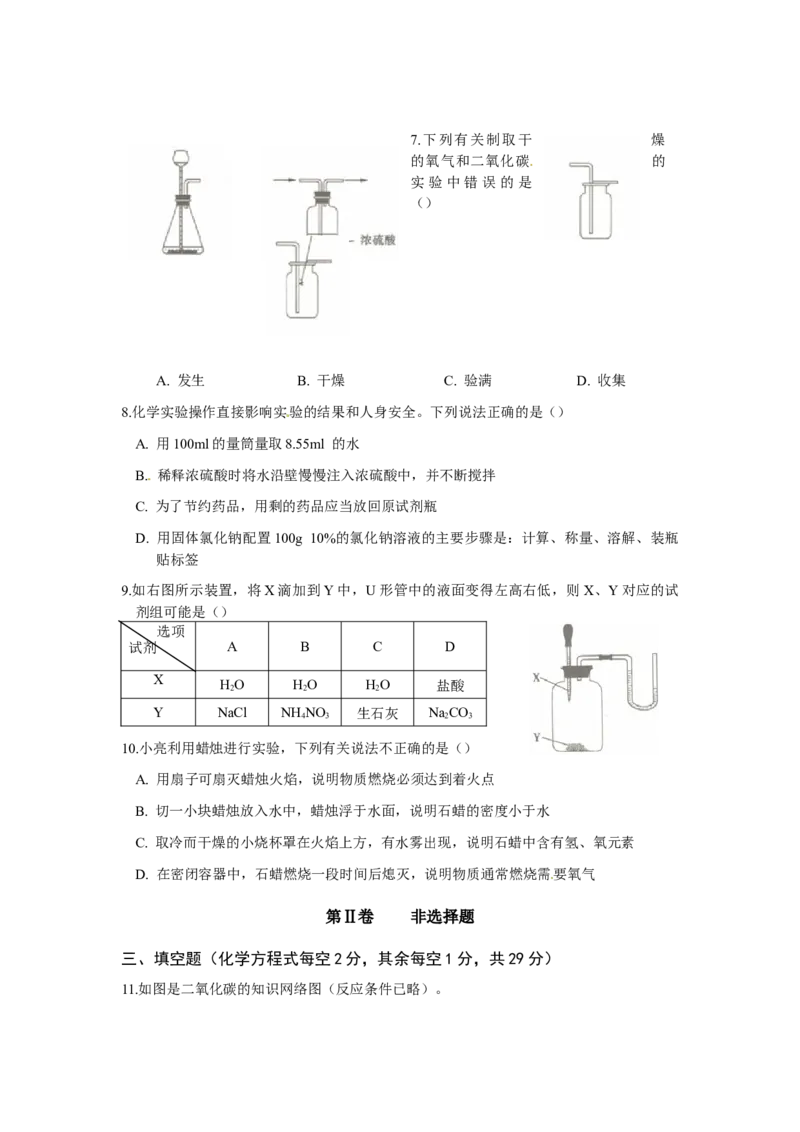
D. 尿素中氮元素的质量分数为46.7%7.下列有关制取干 燥
的氧气和二氧化碳 的
实验中错误的是
()
A. 发生 B. 干燥 C. 验满 D. 收集
8.化学实验操作直接影响实验的结果和人身安全。下列说法正确的是()
A. 用100ml的量筒量取8.55ml 的水
B. 稀释浓硫酸时将水沿壁慢慢注入浓硫酸中,并不断搅拌
C. 为了节约药品,用剩的药品应当放回原试剂瓶
D. 用固体氯化钠配置100g 10%的氯化钠溶液的主要步骤是:计算、称量、溶解、装瓶
贴标签
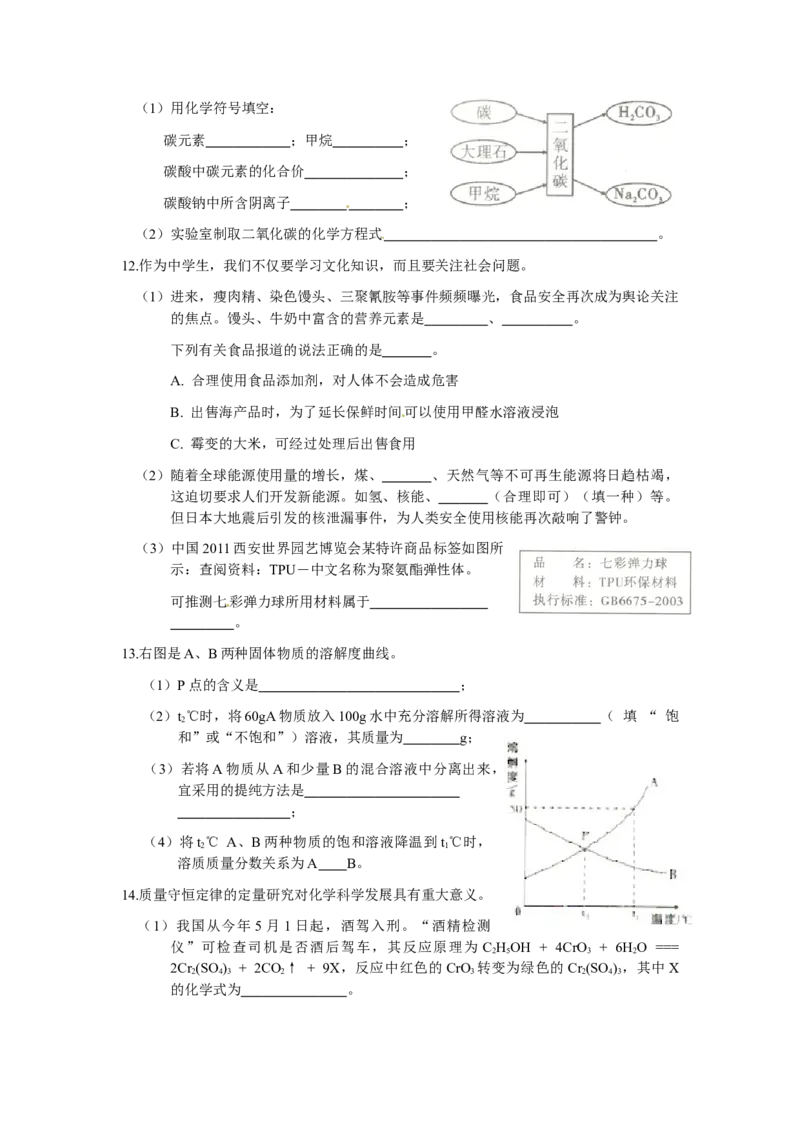
9.如右图所示装置,将X滴加到Y中,U形管中的液面变得左高右低,则X、Y对应的试
剂组可能是()
选项
试剂 A B C D
X
HO HO HO 盐酸
2 2 2
Y NaCl NH NO 生石灰 NaCO
4 3 2 3
10.小亮利用蜡烛进行实验,下列有关说法不正确的是()
A. 用扇子可扇灭蜡烛火焰,说明物质燃烧必须达到着火点
B. 切一小块蜡烛放入水中,蜡烛浮于水面,说明石蜡的密度小于水
C. 取冷而干燥的小烧杯罩在火焰上方,有水雾出现,说明石蜡中含有氢、氧元素
D. 在密闭容器中,石蜡燃烧一段时间后熄灭,说明物质通常燃烧需要氧气
[来源:21世纪教育网]
第Ⅱ卷 非选择题
三、填空题(化学方程式每空2分,其余每空1分,共29分)
[来源:21世纪教育网]
11.如图是二氧化碳的知识网络图(反应条件已略)。(1)用化学符号填空:
碳元素 ;甲烷 ;
碳酸中碳元素的化合价 ;
碳酸钠中所含阴离子 ;
(2)实验室制取二氧化碳的化学方程式 。
12.作为中学生,我们不仅要学习文化知识,而且要关注社会问题。
(1)进来,瘦肉精、染色馒头、三聚氰胺等事件频频曝光,食品安全再次成为舆论关注
的焦点。馒头、牛奶中富含的营养元素是 、 。
下列有关食品报道的说法正确的是 。
A. 合理使用食品添加剂,对人体不会造成危害
B. 出售海产品时,为了延长保鲜时间可以使用甲醛水溶液浸泡
C. 霉变的大米,可经过处理后出售食用
(2)随着全球能源使用量的增长,煤、 、天然气等不可再生能源将日趋枯竭,
这迫切要求人们开发新能源。如氢、核能、 (合理即可)(填一种)等。
但日本大地震后引发的核泄漏事件,为人类安全使用核能再次敲响了警钟。
(3)中国2011西安世界园艺博览会某特许商品标签如图所
示:查阅资料:TPU―中文名称为聚氨酯弹性体。
可推测七彩弹力球所用材料属于
。
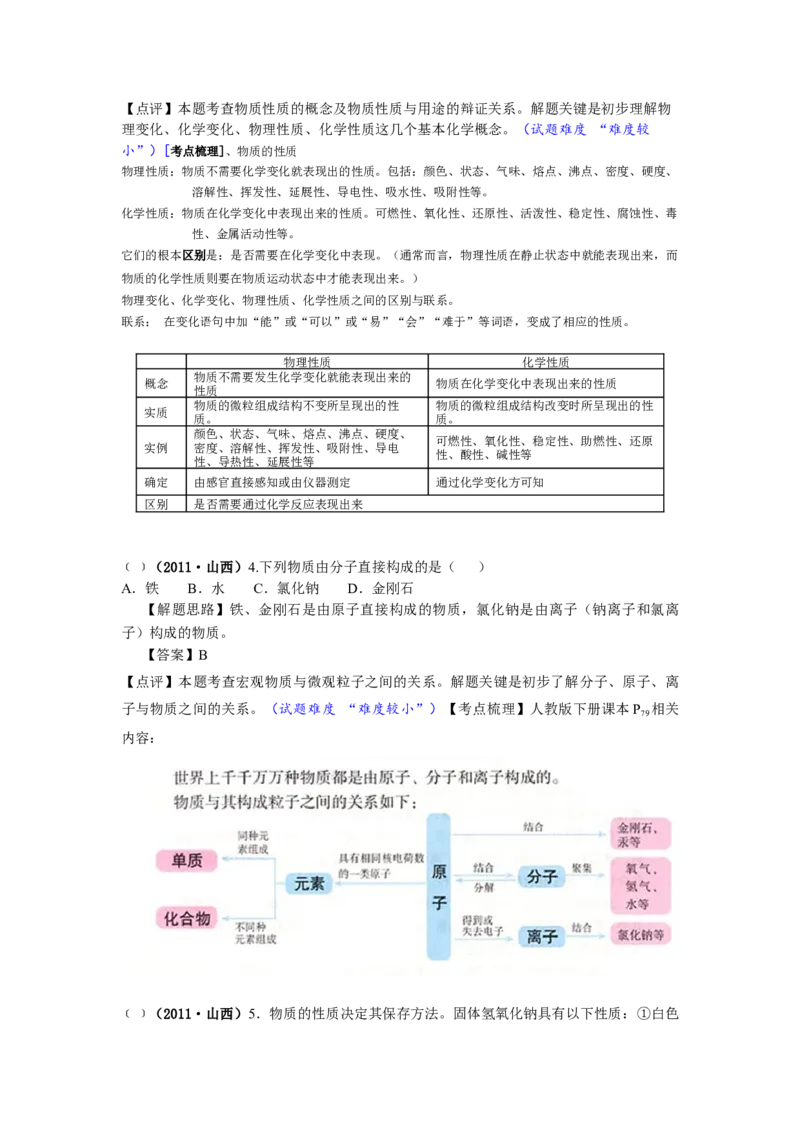
13.右图是A、B两种固体物质的溶解度曲线。
(1)P点的含义是 ;
(2)t℃时,将60gA物质放入100g水中充分溶解所得溶液为 ( 填 “ 饱
2
和”或“不饱和”)溶液,其质量为 g;
(3)若将A物质从A和少量B的混合溶液中分离出来,
宜采用的提纯方法是
;
(4)将t℃ A、B两种物质的饱和溶液降温到t℃时,
2 1
溶质质量分数关系为A B。
[来源:21世纪教育网]
14.质量守恒定律的定量研究对化学科学发展具有重大意义。
(1)我国从今年 5月1日起,酒驾入刑。“酒精检测
仪”可检查司机是否酒后驾车,其反应原理为 C HOH + 4CrO + 6HO ===
2 5 3 2
2Cr (SO ) + 2CO↑ + 9X,反应中红色的CrO 转变为绿色的Cr (SO ) ,其中X
2 4 3 2 3 2 4 3
的化学式为 。○
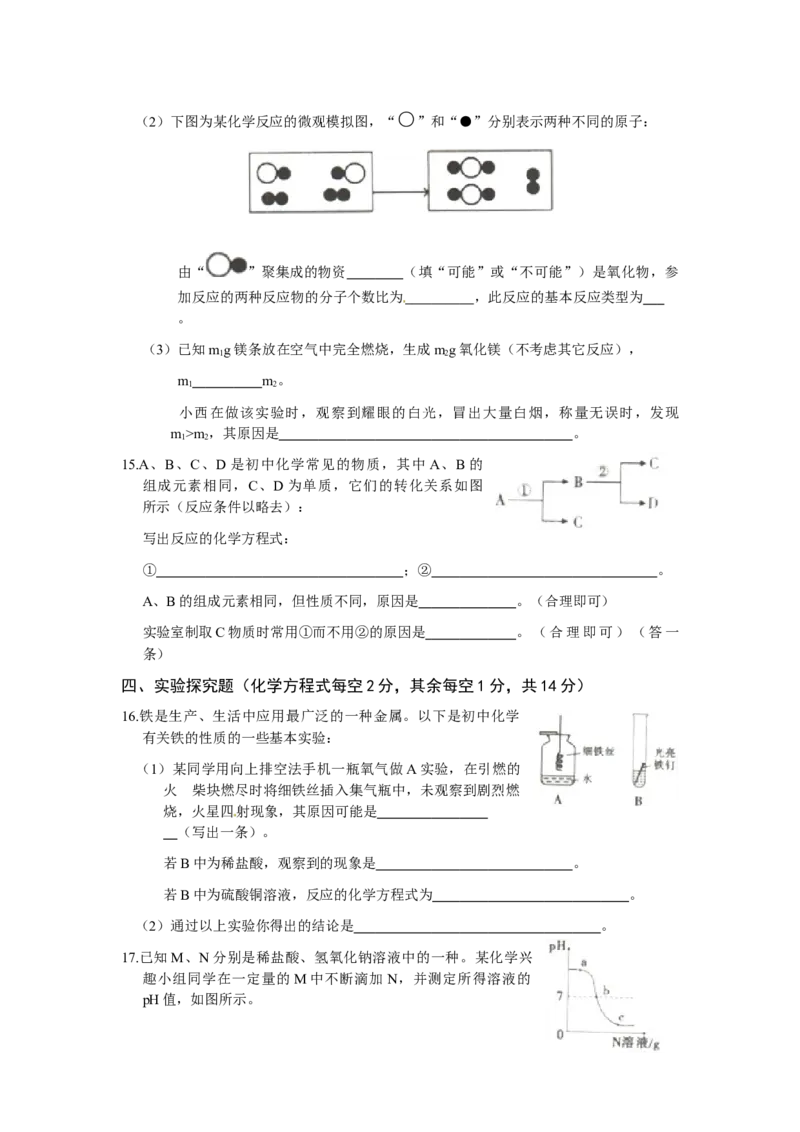
(2)下图为某化学反应的微观模拟图,“ ”和“●”分别表示两种不同的原子:
由“ ”聚集成的物资 (填“可能”或“不可能”)是氧化物,参
加反应的两种反应物的分子个数比为 ,此反应的基本反应类型为
。
(3)已知mg镁条放在空气中完全燃烧,生成mg氧化镁(不考虑其它反应),
1 2
m m。
1 2
小西在做该实验时,观察到耀眼的白光,冒出大量白烟,称量无误时,发现
m>m,其原因是 。
1 2
15.A、B、C、D是初中化学常见的物质,其中 A、B的
组成元素相同,C、D为单质,它们的转化关系如图
所示(反应条件以略去):
写出反应的化学方程式:
① ;② 。
A、B的组成元素相同,但性质不同,原因是 。(合理即可)
实验室制取C物质时常用①而不用②的原因是 。(合理即可)(答一
条)
四、实验探究题(化学方程式每空2分,其余每空1分,共14分)
16.铁是生产、生活中应用最广泛的一种金属。以下是初中化学
有关铁的性质的一些基本实验:
(1)某同学用向上排空法手机一瓶氧气做A实验,在引燃的
火 柴块燃尽时将细铁丝插入集气瓶中,未观察到剧烈燃
烧,火星四射现象,其原因可能是
(写出一条)。
若B中为稀盐酸,观察到的现象是 。
若B中为硫酸铜溶液,反应的化学方程式为 。
(2)通过以上实验你得出的结论是 。
17.已知M、N分别是稀盐酸、氢氧化钠溶液中的一种。某化学兴
趣小组同学在一定量的M中不断滴加N,并测定所得溶液的
pH值,如图所示。(1)M是一种 ,该反应的化学方程式 。
(2)反应过程中,老师取a、b、c三处反应后的溶液,打乱顺序后,请同学们不测定
溶液的pH值,用其它方法对三种溶液进行探究。
小明和小红分别取其中一种溶液进行实验:
小明向所取溶液中加入 溶液,观察到有蓝色沉淀生成。
结论:是a处溶液。
小红向少量另一种溶液中滴加酚酞溶液,观察到 。
结论:是b处或c处溶液。
为进一步确定该溶液成分,小红又设计并完成如下实验:
实验步骤 实验现象 结论
取少量该溶液,向 为c处溶液,并推知溶液中的离
其中滴加石蕊溶液 溶液变红 子有
(合理即可) (填写离子符号)
剩余一种为b处溶液。
通过实验,同学们知道了酸碱反应过程中pH的变化和用不同方法确定溶液成分。
五、计算题(本题共7分)
18.黄铜是铜、锌合金,它可用来制造机器、电器零件及日用品。为测定某黄铜中铜的质量
分数,现取10g该样品粉碎,加入到50g稀硫酸中,恰好完全反应,测得剩余固体质量
为3.5g。计算:
(1)黄铜样品中铜的质量分数。
(2)稀硫酸中溶质的质量分数。
2011 年山西省中考
化学试题解析
可能用到的相对原子质量:H—l C—12 NV14 O—16 S—32 Cu—64 Zn—65
一、选择题(在每小题给出的四个选项中,只有一项符合题目要求,每小题 2分,本题共
20分)
﹝﹞(2011·山西)1.下列变化属于物理变化的是( )
A.冰雪融化 B.粮食酿酒 C.工业炼铁 D.火箭点火
【解题思路】化学变化和物理变化的根本区别是有无其他质生成。粮食酿酒将粮食内营养成分(以淀粉为主的粮食)发酵生成新物质酒精,工业炼铁是将铁矿石(如富含Fe O
2 3
的赤铁矿和富含Fe O 的磁铁矿)、焦炭等在高炉内反应冶炼出以新物质单质铁为主的生
3 4
铁,火箭点火是将高能燃料(如液态氢等)与液态氧发生燃烧反应,生成新物质水并放出
大量的热。所以B、C、D均为化学变化;冰雪融化只是水的状态改变,没有新物质出现。
所以A属于物理变化。
【答案】A
【点评】本题考查了物理变化和化学变化的区别,关键是根据是否有新物质生成这个依据
加以判断,有新质生成的是化学变化,没有新物质生成是物理变化。(试题难度 “难度较
小”)[考点梳理]、物质的变化
1)、概念:物理变化——没有生成其它物质的变化。例:石蜡熔化、水结成冰、汽油挥发
化学变化——有其它物质生成的变化 例:煤燃烧、铁生锈、食物腐败、呼吸
2)、判断变化依据:是否有其它(新)物质生成。 有则是化学变化,无则是物理变化
3)、相互关系:常常伴随发生,有化学变化一定有物理变化,有物理变化不一定有化学变化。
4)、化学变化伴随现象:放热、吸热、发光、变色、放出气体和生成沉淀。
物理变化 化学变化
概念 没有生成其他物质的变化 生成其他物质的变化
常伴随有放热、发光、变色,放出气
伴随现象 物质的形状、状态等发生变化
体、生成沉淀等
本质区别 变化时是否有其他物质生成
实例 石蜡熔化、水结成冰、汽油挥发 煤燃烧、铁生锈、食物腐败、呼吸
物质在发生化学变化的过程中一定伴随物理变化,如石蜡燃烧时先发生石蜡熔化现
相互关系
象。在发生物理变化时不一定伴随化学变化。
﹝﹞(2011·山西)2.下列气体属于空气污染物的是( )
A.O B.N C.SO D.CO2
2 2 2
【解题思路】目前计入空气污染指数的项目暂定为:SO 、CO、NO 、可吸入颗粒物和
2 2
臭氧等。所以选C。
【答案】C
【点评】本题考查空气污染的基本常识。(试题难度 “难度较小”)
﹝﹞(2011·山西)3.下列物质的用途主要利用其化学性质的是( )
A.氧气用于医疗急救 B.干冰用于人工降雨
C.铜、铝用于制作导线 D.汽油用于衣物除油
【解题思路】物质在化学变化中表现出来的性质叫做化学性质,物质不需要发生化学变
化就表现出来的性质叫做物理性质。物质的性质在一定程度上决定了物质的用途,物质的
用途体现了物质的性质。人工降雨是利用了干冰升华吸热的原理,制作导线是利用了铜、
铝的延展性和导电性,汽油清洗油污是利用了汽油能溶解油污(相似相容原理),均是以
物理性质为主,所以B、C、D不合题意;医疗急救是利用氧气参与体内的呼吸作用,呼吸
作用是一种缓慢氧化过程。所以氧气用于医疗急救主要利用了氧气的化学性质。所以A符
合题意。
【答案】A【点评】本题考查物质性质的概念及物质性质与用途的辩证关系。解题关键是初步理解物
理变化、化学变化、物理性质、化学性质这几个基本化学概念。(试题难度 “难度较
小”)[考点梳理]、物质的性质
物理性质:物质不需要化学变化就表现出的性质。包括:颜色、状态、气味、熔点、沸点、密度、硬度、
溶解性、挥发性、延展性、导电性、吸水性、吸附性等。
化学性质:物质在化学变化中表现出来的性质。可燃性、氧化性、还原性、活泼性、稳定性、腐蚀性、毒
性、金属活动性等。
它们的根本区别是:是否需要在化学变化中表现。(通常而言,物理性质在静止状态中就能表现出来,而
物质的化学性质则要在物质运动状态中才能表现出来。)
物理变化、化学变化、物理性质、化学性质之间的区别与联系。
联系: 在变化语句中加“能”或“可以”或“易”“会”“难于”等词语,变成了相应的性质。
物理性质 化学性质
物质不需要发生化学变化就能表现出来的
概念 物质在化学变化中表现出来的性质
性质
物质的微粒组成结构不变所呈现出的性 物质的微粒组成结构改变时所呈现出的性
实质
质。 质。
颜色、状态、气味、熔点、沸点、硬度、
可燃性、氧化性、稳定性、助燃性、还原
实例 密度、溶解性、挥发性、吸附性、导电
性、酸性、碱性等
性、导热性、延展性等
确定 由感官直接感知或由仪器测定 通过化学变化方可知
区别 是否需要通过化学反应表现出来
﹝﹞(2011·山西)4.下列物质由分子直接构成的是( )
A.铁 B.水 C.氯化钠 D.金刚石
【解题思路】铁、金刚石是由原子直接构成的物质,氯化钠是由离子(钠离子和氯离
子)构成的物质。
【答案】B
【点评】本题考查宏观物质与微观粒子之间的关系。解题关键是初步了解分子、原子、离
子与物质之间的关系。(试题难度 “难度较小”)【考点梳理】人教版下册课本P 相关
79
内容:
﹝﹞(2011·山西)5.物质的性质决定其保存方法。固体氢氧化钠具有以下性质:①白色固体,②有腐蚀性,③易吸收水分,④能与空气中的二氧化碳反应。由此可知,氢氧化钠
固体必须密封保存的主要原因是( )
A.①② B.②③ C.①③ D.③④
【解题思路】固体一般用广口瓶保存。“①白色固体”不是密封保存氢氧化钠的原因。
氢氧化钠等强碱性溶液应贮存在带橡胶塞(或塑料塞、或软木塞)的细口瓶里(因使用玻
璃塞很容易造成瓶塞与瓶口的粘连)。显然“②有腐蚀性”决定了氢氧化钠保存时选择哪
种仪器,不是密封保存的主要原因。氢氧化钠固体易吸水而潮解,也容易与空气中的二氧
化碳反应而变质。“③易吸收水分,④能与空气中的二氧化碳反应”才是氢氧化钠必须密
封保存的主要原因。所以选D.
【答案】D
【点评】本题考查保存方法的选择问题。解题关键是初步理解物质保存方法是由物质的
具体性质决定的。物质的一些性质直接决定了物质的保存方法。(试题难度 “难度中
等”)
﹝﹞(2011·山西)6.尿素[CO(NH )]是一种常用的化肥,它可以促进植物的生长发育。
2 2
下列说法正确的是( )
A.尿素是一种复合肥料
B.尿素中碳、氧、氮、氢四种元素的质量比为1:1:2:4
C.一个尿素分子中含有一个一氧化碳分子
D.尿素中氮元素的质量分数为46.7 %
【解题思路】复合肥料指同时含有氮、磷、钾中两种或两种以上营养元素的肥料。显然,
尿素不是复合肥料。分子是由原子构成的,一种分子中不可能还有另一种分子。尿素中碳
氧、氮、氢四种元素的原子数目比为1:1:2:4,元素质量比是12:16:(14×2):
(1×4)=3:4:7:1,所以A、B、D不正确。尿素中氮元素的质量分数=7/15=46.7 %,
所以D正确。
【答案】D
【点评】本题综合考查复合肥料、分子构成及化学式的基本计算。解题关键是理解一个
分子里不可能有另一个分子,以及复合肥料的概念。本题易错点是计算时把尿素分子里氮
原子的个数按1计算而出错。(试题难度 “难度中等”)
﹝﹞(2011·山西)7.下列有关制取干燥的氧气和二氧化碳的实验中错误的是( )
A.发生 B.干燥 C.验满 D.收集
【解题思路】反应物地状态和反应条件决定了气体的发生装置,气体的性质决定了气体
的干燥、收集和验满。氧气和二氧化碳都可以用“固体和液体不加热”的方法原理来制备
都可用A发生装置;二者都不溶于浓硫酸,都可以用装有浓硫酸的洗气瓶B干燥;二者密度都比空气的大(可用比较相对分子质量法比较气体密度大小,空气的平均相对分子质量
为29),都可用D向上排空气法收集。氧气具有助燃性,可用带火星的木条放在瓶口验满;
二氧化碳不能燃烧,也不能支持燃烧,可用燃着的木条放在瓶口验满。所以C错误。
【答案】C
【点评】本题综合考查氧气和二氧化碳的发生、干燥、验满、收集等实验基本知识点。
解题关键是掌握制取常见气体的反应原理和气体的物化性质,进而分析气体发生装置的适
用范围与反应物状态和反应条件的关系,干燥装置和干燥剂的选择、气体的验满方法和气
体的收集方法分别由气体的什么性质决定的。(试题难度 “难度中等”)【考点梳理】
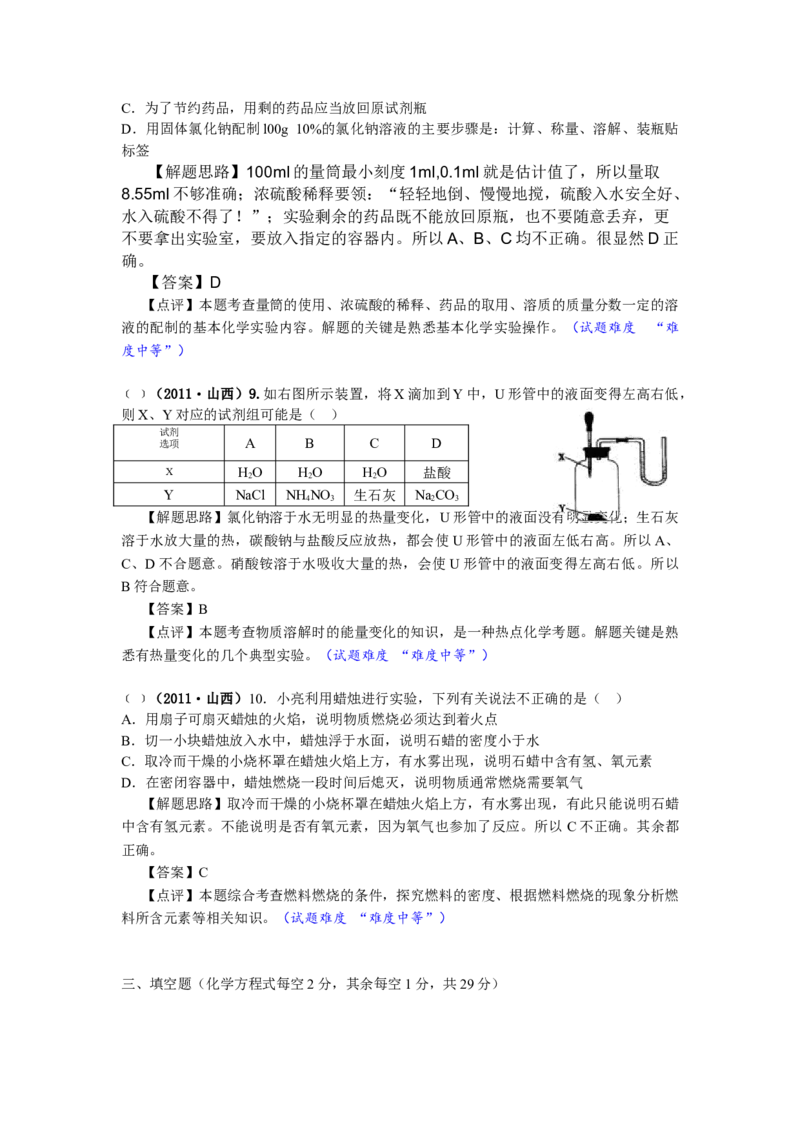
氧气、氢气和二氧化碳的实验室制法列表比较:
氧气 氢气 二氧化碳
药 KClO 和MnO 或KMnO Zn和稀HSO 大理石(或石灰石)
3 2 4 2 4
药 和稀HCl
品
反2KClO
3
M n
△
O 2 2KCl+3O
2
↑ Zn+H 2 SO 4(稀) =ZnSO 4 +H 2 ↑ C +H aC
2
O O + 3 + C O 2H
2
↑ Cl=CaCl 2
反
应 △
2KMnO KMnO +MnO
原 4 2 4 2
理 +O ↑
2
发
发
生
装
置
和
收
集
装
置
收 排水法或 排水法或 向上排空气法
收 向上排空气法 向下排空气法
集
检 使带火星的木条复燃 点燃,火焰呈淡蓝 使澄清石灰水变浑浊
检 色,产物只有水
验
﹝﹞(2011·山西)8.化学实验操作直接影响实验的结果和人身安全。下列说法正确的是
( )
A.用l00ml的量筒量取8.55ml的水
B.稀释浓硫酸时将水沿器壁慢慢注入浓硫酸中,并不断搅拌C.为了节约药品,用剩的药品应当放回原试剂瓶
D.用固体氯化钠配制l00g 10%的氯化钠溶液的主要步骤是:计算、称量、溶解、装瓶贴
标签
【解题思路】100ml的量筒最小刻度1ml,0.1ml就是估计值了,所以量取
8.55ml不够准确;浓硫酸稀释要领:“轻轻地倒、慢慢地搅,硫酸入水安全好、
水入硫酸不得了!”;实验剩余的药品既不能放回原瓶,也不要随意丢弃,更
不要拿出实验室,要放入指定的容器内。所以A、B、C均不正确。很显然D正
确。
【答案】D
【点评】本题考查量筒的使用、浓硫酸的稀释、药品的取用、溶质的质量分数一定的溶
液的配制的基本化学实验内容。解题的关键是熟悉基本化学实验操作。(试题难度 “难
度中等”)
﹝﹞(2011·山西)9.如右图所示装置,将X滴加到Y中,U形管中的液面变得左高右低,
则X、Y对应的试剂组可能是( )
试剂
选项 A B C D
X HO HO HO 盐酸
2 2 2
Y NaCl NH NO 生石灰 NaCO
4 3 2 3
【解题思路】氯化钠溶于水无明显的热量变化,U形管中的液面没有明显变化;生石灰
溶于水放大量的热,碳酸钠与盐酸反应放热,都会使 U形管中的液面左低右高。所以A、
C、D不合题意。硝酸铵溶于水吸收大量的热,会使 U形管中的液面变得左高右低。所以
B符合题意。
【答案】B
【点评】本题考查物质溶解时的能量变化的知识,是一种热点化学考题。解题关键是熟
悉有热量变化的几个典型实验。(试题难度 “难度中等”)
﹝﹞(2011·山西)10.小亮利用蜡烛进行实验,下列有关说法不正确的是( )
A.用扇子可扇灭蜡烛的火焰,说明物质燃烧必须达到着火点
B.切一小块蜡烛放入水中,蜡烛浮于水面,说明石蜡的密度小于水
C.取冷而干燥的小烧杯罩在蜡烛火焰上方,有水雾出现,说明石蜡中含有氢、氧元素
D.在密闭容器中,蜡烛燃烧一段时间后熄灭,说明物质通常燃烧需要氧气
【解题思路】取冷而干燥的小烧杯罩在蜡烛火焰上方,有水雾出现,有此只能说明石蜡
中含有氢元素。不能说明是否有氧元素,因为氧气也参加了反应。所以 C不正确。其余都
正确。
【答案】C
【点评】本题综合考查燃料燃烧的条件,探究燃料的密度、根据燃料燃烧的现象分析燃
料所含元素等相关知识。(试题难度 “难度中等”)
三、填空题(化学方程式每空2分,其余每空1分,共29分)﹝﹞(2011·山西)11.如图是二氧化碳的知
识网络图(反应条件已略)。 碳
H CO
(1)用化学符号填空: 2 3
二
碳元素 ;甲烷 ;
氧
碳酸中碳元素的化合价 ; 化
大理
碳酸钠中所含阴离子 ; 碳
石
(2)实验室制取二氧化碳的化学方程式
。
Na CO
甲烷 2 3
【解题思路】回忆二氧化碳的产生、实验
室制法、工业制法及二氧化碳的性质。只要清
晰记忆碳及其化合物的相互转化关系图,熟练掌握常用的元素符号、化合价、离子符号、
化学式及化学方程式,便可顺利作答。
【答案】
【点评】本题考查碳及其化合物之间的相互转化关系。解题关键是熟练掌握碳及其化合
物相互转换关系图:
(人教版上册P )
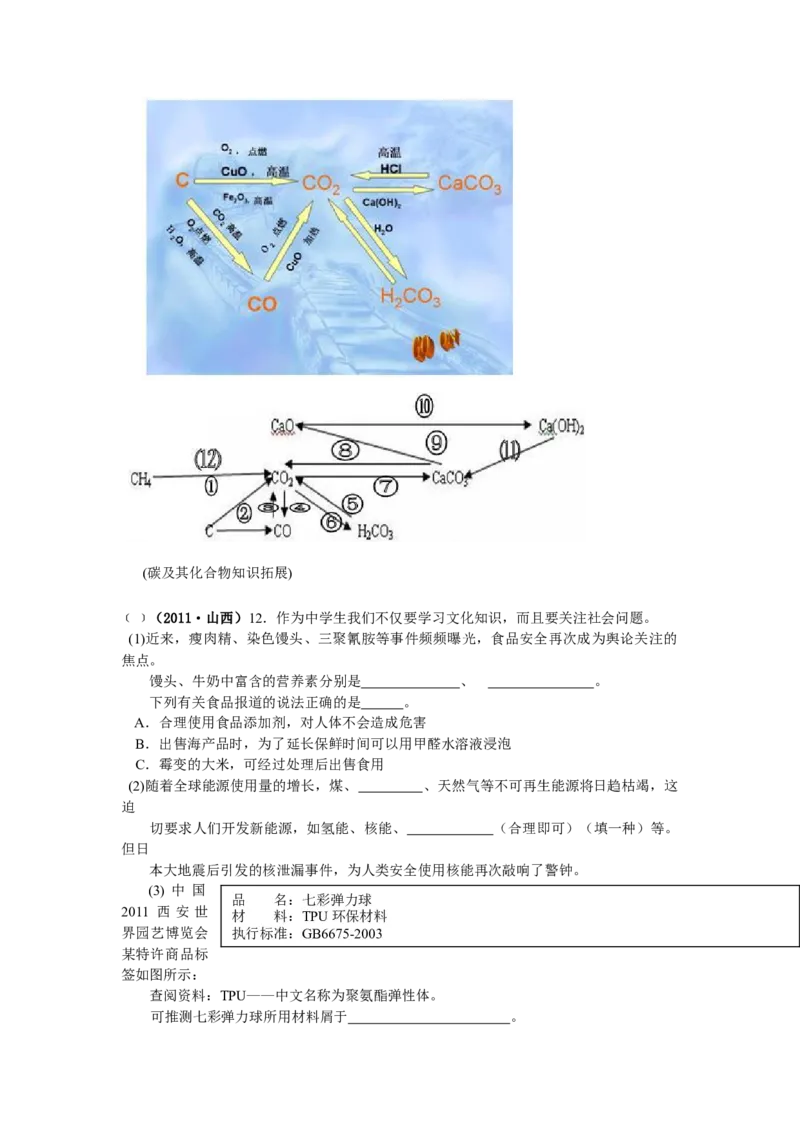
122(碳及其化合物知识拓展)
﹝﹞(2011·山西)12.作为中学生我们不仅要学习文化知识,而且要关注社会问题。
(1)近来,瘦肉精、染色馒头、三聚氰胺等事件频频曝光,食品安全再次成为舆论关注的
焦点。
馒头、牛奶中富含的营养素分别是 、 。
下列有关食品报道的说法正确的是 。
A.合理使用食品添加剂,对人体不会造成危害
B.出售海产品时,为了延长保鲜时间可以用甲醛水溶液浸泡
C.霉变的大米,可经过处理后出售食用
(2)随着全球能源使用量的增长,煤、 、天然气等不可再生能源将日趋枯竭,这
迫
切要求人们开发新能源,如氢能、核能、 (合理即可)(填一种)等。
但日
本大地震后引发的核泄漏事件,为人类安全使用核能再次敲响了警钟。
(3) 中 国
品 名:七彩弹力球
2011 西 安 世 材 料:TPU环保材料
界园艺博览会 执行标准:GB6675-2003
某特许商品标
签如图所示:
查阅资料:TPU——中文名称为聚氨酯弹性体。
可推测七彩弹力球所用材料屑于 。【解题思路】本题联系社会问题,解答相关的食品问题、能源问题、材料问题所涉及的
相关化学知识。
【答案】
【点评】本题考查与化学有关的时事热点问题:食品安全
问题、能源问题、材料问题等,渗透了“高起点、低落
点”的命题理念。解题关键是揭开热点信息的面纱,洞察
热点问题所体现的基本化学知识:饮食与六大营养素、环
境与能源、新型材料等。
【考点梳理】1)根据能源使用的类型可将能源分为常规能
源 和新型能源
利用技术上成熟,使用比较普遍的能源叫做常规能源。包括一次能源中
的可再生的水力资源和不可再生的煤炭、石油、天然气等资源。
新近利用或正在着手开发的能源叫做新型能源。新型能源是相对于常规
能源而言的,包括太阳能 、风能 、地热能 、海洋能 、生物能 、氢能 以及用于
核能发电的核燃料等能源。由于新能源的能量密度较小,或品位较低,或有
间歇性,按已有的技术条件转换利用的经济性尚差,还处于研究、发展阶段,
只能因地制宜地开发和利用;但新能源大多数是再生能源。资源丰富,分布广
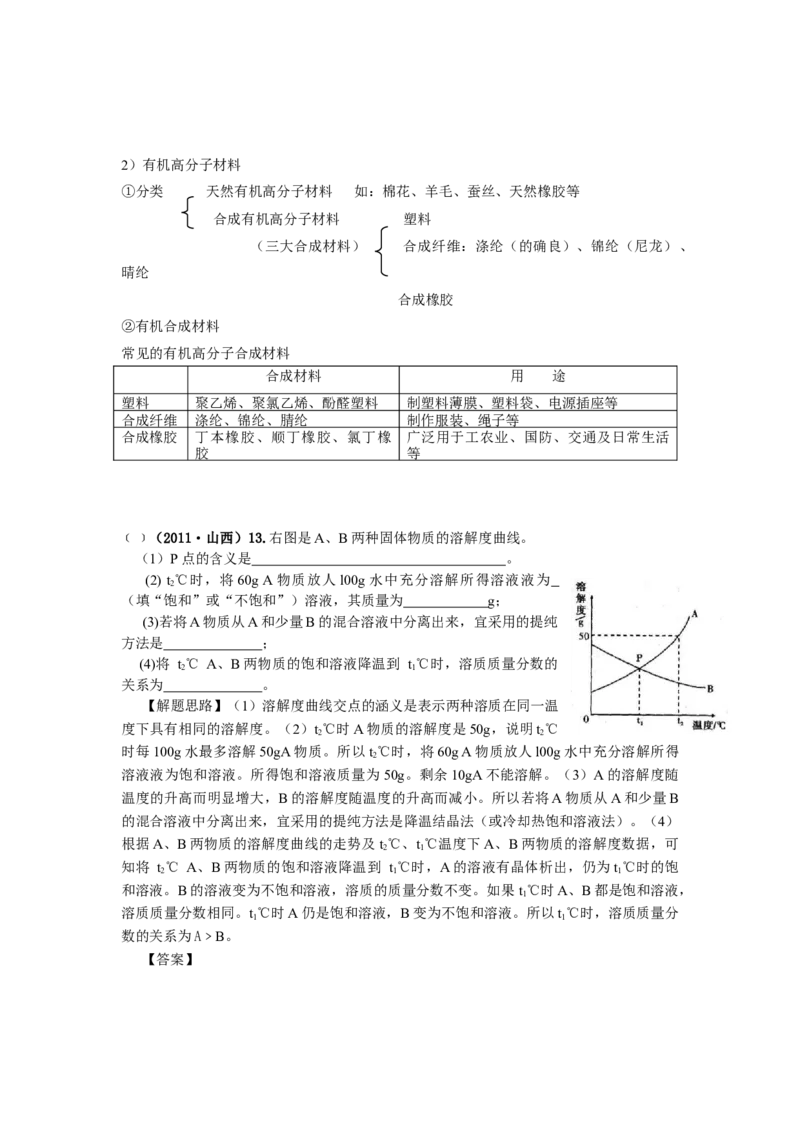
阔,是未来的主要能源之一。2)有机高分子材料
①分类 天然有机高分子材料 如:棉花、羊毛、蚕丝、天然橡胶等
合成有机高分子材料 塑料
(三大合成材料) 合成纤维:涤纶(的确良)、锦纶(尼龙)、
晴纶
合成橡胶
②有机合成材料
常见的有机高分子合成材料
合成材料 用 途
塑料 聚乙烯、聚氯乙烯、酚醛塑料 制塑料薄膜、塑料袋、电源插座等
合成纤维 涤纶、锦纶、腈纶 制作服装、绳子等
合成橡胶 丁本橡胶、顺丁橡胶、氯丁橡 广泛用于工农业、国防、交通及日常生活
胶 等
﹝﹞(2011·山西)13.右图是A、B两种固体物质的溶解度曲线。
(1)P点的含义是 。
(2) t ℃时,将60g A物质放人 l00g水中充分溶解所得溶液液为
2
(填“饱和”或“不饱和”)溶液,其质量为 g;
(3)若将A物质从A和少量B的混合溶液中分离出来,宜采用的提纯
方法是 ;
(4)将 t℃ A、B两物质的饱和溶液降温到 t℃时,溶质质量分数的
2 1
关系为 。
【解题思路】(1)溶解度曲线交点的涵义是表示两种溶质在同一温
度下具有相同的溶解度。(2)t℃时A物质的溶解度是50g,说明t℃
2 2
时每100g水最多溶解50gA物质。所以t℃时,将60g A物质放人l00g水中充分溶解所得
2
溶液液为饱和溶液。所得饱和溶液质量为50g。剩余10gA不能溶解。(3)A的溶解度随
温度的升高而明显增大,B的溶解度随温度的升高而减小。所以若将A物质从A和少量B
的混合溶液中分离出来,宜采用的提纯方法是降温结晶法(或冷却热饱和溶液法)。(4)
根据A、B两物质的溶解度曲线的走势及t℃、t℃温度下A、B两物质的溶解度数据,可
2 1
知将 t℃ A、B两物质的饱和溶液降温到 t℃时,A的溶液有晶体析出,仍为t℃时的饱
2 1 1
和溶液。B的溶液变为不饱和溶液,溶质的质量分数不变。如果t℃时A、B都是饱和溶液,
1
溶质质量分数相同。t℃时A仍是饱和溶液,B变为不饱和溶液。所以t℃时,溶质质量分
1 1
数的关系为A﹥B。
【答案】【点评】本题考查溶解度曲线的知识。解题关键是熟悉溶解度曲线的意义、曲线上的点、
曲线之间的交点的涵义、曲线的走势、根据溶解度曲线的走势判断混合物的分离方法。
【考点梳理】初步了解溶解度曲线:能看得懂溶解度曲线图。能根据图上的数据进行计算。
①曲线的意义:表示某物质在不同温度下的溶解度或溶解度随温度变化的情况
②曲线上的每一点表示溶质在某温度下的溶解度,溶液是饱和溶液。
③两曲线的交点表示两种溶质在同一温度下具有相同的溶解度。
结晶的两种方法
①蒸发溶剂:适用于得到溶解度受温度影响较小的物质。如NaCl(海水晒盐)
②降低温度(冷却热的饱和溶液):适用于得到溶解度随温度升高而升高的物质,如KNO
3
能根据图上的数据进行计算。
﹝﹞(2011·山西)14.质量守恒定律的定量研究对化学科学发展具有重大作用。
(1)我国从今年5月1日起,酒驾入刑。“酒精检测仪”可检查司机是否酒后驾车,其反
应原理为C HOH+4CrO+6H SO ==== 2Cr ( SO )+CO ↑+9X,反应中红色的CrO 转变为
2 5 3 2 4 2 4 3 2 3
绿色Cr ( SO),其中X的化学式为 。
2 4 3
(2)下图为某化学反应的微观模拟图,“O”和“●”分别表示两种不同元素的原子:
由“O●”聚集成的物质 (填“可能”或“不可能”)是氧化物,参加反
应的两种反应物的分子个数比为 ,此反应的基本反应类型为
。
(3)已知mg镁条在空气中完全燃烧,生成mg氧化镁(不考虑其它反应),m
1 2 1
m(选填“=”、“﹥”或“﹤”)。
2
【解题思路】(1)根据反应前后原子的种类和个数不变,可判断出X的化学式为HO。
2
(2)“O●”分子是由两种不同的原子构成的分子,有可能是氧化物。根据反应前后,有
一个“ ”分子相同,说明根据图示的微粒数量关系看,反应后有一个“ ”分子
剩余,所以,参加反应的两种反应物的分子个数比为 2:1(或1:2)。右图是可知:该反
应是由两种分子生成一种分子的反应,所以是化合反应。
(3) 镁条在空气中完全燃烧,氧气也参加了反应,所以生成物的质量比原来镁条的质量大。
【答案】【点评】本题 考查质量守恒定律的应用、氧化物的判断以及宏观、微观和化学符号结合的
思维能力。[考点梳理]1) 质量守恒定律:含义: 参加化学反应的各物质的质量总和,等于反应后生
成的各物质的质量总和。
说明:①质量守恒定律只适用于化学变化,不适用于物理变化;
②没有参加反应的物质质量及不是反应生成的物质质量不能计入“总和”。
③要考虑空气中的物质是否参加反应或物质(如气体)有无遗漏。
微观解释:在化学反应前后,原子的种类、数目、质量均保持不变(原子的“三不变”)。
化学反应前后
(1)一定不变 宏观: 反应物、生成物的总质量不变;元素种类、质量不变
微观:原子的种类、数目、质量不变
(2)一定改变 宏观:物质的种类一定变
微观:分子种类一定变
(3)可能改变:分子总数可能变
2)从反应物和生成物的类别以及反应前后物质种类的多少的角度划分,也就是所谓的“基
本反应类型”。如下表:
反应类型 表达式 举例
化合反应 A+B=AB
分解反应 AB=A+B
置换反应 A+BC=AC+B
复分解反应 AB+CD=AD+CB﹝﹞(2011·山西)15.A、B、C、D是初中化学的常见物质,其中
A、B的组成元素相同,C、D为单质,它们的转化关系如图所示(反
应条件已略去):
写出反应的化学方程式:
① ;② 。
A、B的组成元素相同,但性质不同,原因是 。
(合理即可)
实验室制取C物质时常用①而不用②的原因是 。
(合理即可)(答一条)
【解题思路】根据图示反应关系以及题干信息“A、B、C、D是初中化学的常见物质,
其中A、B的组成元素相同,C、D为单质”很容易推出:A、B、C、D分别为:HO 、
2 2
HO、O 、H 。显然① 2H O ==== 2H O + O ↑ ;② 2H O ====2H ↑ + O ↑ 。根
2 2 2 2 2 2 2 2 2 2
据物质的结构决定物质的性质,可推知HO 、HO的组成元素相同,但性质不同,原因是
2 2 2
分子构成不同。①②两种方法都可制取氧气,但前者只需加催化剂如 MnO 即可在常温下
2
迅速反应,装置简单、节约能源,后者需要通电,装置复杂、消耗电能且不安全。
【答案】
【点评】本题综合考查物质推断题的解题能力。解题关键是挖掘“题眼”,熟悉所学的
基本化学反应,并能根据题干信息很快联想相应的特征反应。(试题难度 “难度较
大”)【考点梳理】
①KClO
3
②KMnO
4 ③H 2 O 2
C ④ ⑦Mg
氧气
S ⑤ ( O ) ⑧ Fe
2
P ⑥ ⑨ Cu
(10)CO
(11)CH
4 (12)C H OH
2 5
四、实验探究题(化学方程式每空2分,其余每空1分,共14分)﹝﹞(2011·山西)16.铁是生产、生活中应用最广泛的一种金属。以
下是初中化学有关铁的性质的一些基本实验:
(1)某同学用向上排空气法收集一瓶氧气做 A实验,在引燃的火柴快燃
尽时将细铁丝插入集气瓶中,未观察到剧烈燃烧,火星四射现象,其原
因可能是 (写出一条)。
若B中为稀盐酸,观察到的现象是 ;
若B中为硫酸铜溶液,反应的化学方程式为 ;
若B中为水,一段时间后,产物主要成分的化学式为 。
(2)通过以上实验你得出的结论是 。
【解题思路】(1)细铁丝在氧气中燃烧实验的关键是铁丝表面要除锈、氧气纯度要高。
铁钉在稀盐酸中反应的现象是:铁钉表面产生气泡,溶液有无色变成浅绿色。铁钉在硫酸
铜溶液中反应的化学方程式是:Fe+CuSO=Cu+FeSO 。铁生锈的主要产物是Fe O 。(2)
4 4 2 3
根据这些实验,可得出铁是一种化学性质比较活泼的金属。
【答案】
【点评】本题考查常见的金属材料铁的性质。解题关键是熟悉铁的化学性质:与氧气、
氧气和水、酸溶液以及排在铁后金属的盐溶液等的反应及其现象,并能根据现象从不同角
度总结氧气的化学性质。要求考生必须熟悉实验成功的关键。【考点梳理】略
﹝﹞(2011·山西)17.已知M、N分别是稀硫酸、氢氧化钠溶液中的一种。某化学兴趣
小组同学在一定量的M中不断滴加N,并测定所得溶液的pH,如图所示。
(1)M 是 , 该 反 应 的 化 学 方 程 式
。
(2)反应过程中,老师取a、b、c三处反应后的溶液,打乱顺序后,请同学们不测定溶液
pH,用其它实验方法对三种溶液进行探究。小明和小红分别取其中一种溶液进行实验:
小明向所取溶液中加入 溶液,观察到有蓝色沉淀生成。
结论:是a处溶液。
小 红 向 少 量 另 一 种 溶 液 中 滴 加 酚 酞 溶 液 , 观 察 到
。
结论:是b处或c处溶液。
为进一步确定该处溶液成分,小红又设计并完成如下实验:
实验步骤 实验现象 结 论
为c处溶液,并推知溶液中的离子有
(填离子符号)
剩余一种为b处溶液。
通过实验,同学们知道了酸碱反应过程中溶液pH的变化和用不同方法确定溶液成
分。
【解题思路】(1)根据图像可知:M是碱,N是酸,所以M是氢氧化钠溶液,N是稀硫酸。
反应的化学方程式为:HSO +2NaOH=Na SO +2HO。(2)根据实验现象和结论可逆推,
2 4 2 4 2
小明使用了可溶性铜盐溶液(如硫酸铜溶液、硝酸铜溶液)来证明所取溶液是否为碱性溶
液。根据小红的实验用试剂和结论,可逆推小红实验现象应该是:溶液仍为无色(或酚酞
试液不变色)。根据小红进一步的实验结论,可逆推小红的实验步骤是:取少许反应后的
溶液,向其中加入锌粒(或氧化铁、氢氧化铜、碳酸钙等),实验现象是:产生气泡(或
溶液变为黄色、溶液变为蓝色、产生气泡)。实验的完整结论是:为c处溶液,并推知溶
液中的离子有:H+、Na+、SO 2-。
4
【答案】
【点评】本题考查中和反应这一重点热点实验。解题关键是熟悉中和反应的原理和本质,
酸、碱、盐具有的化学性质以及酸、碱、盐的检验方法。五、计算题(本题共7分)
﹝﹞(2011·山西)18.黄铜是铜、锌合金,它可用来制造机器、电器零件及日用品。
为测定某黄铜样品中铜的质量分数,现取l0g该样品粉碎,加入到50g稀硫酸中,恰好完
全反应,测得剩余固体质量为3.5g。计算:
(1)黄铜样品中铜的质量分数。
(2)稀硫酸中溶质的质量分数。
(3)由此得到启示是:在使用黄铜制品时应注意 。(合理即
可)
【解题思路】(1)根据题目涉及反应原理,很容易分析出剩余固体质量为3.5g,即原
l0g该样品中铜的质量为3.5g。所以黄铜样品中铜的质量分数= ×100%=35%。(2)
根据原l0g该样品中铜的质量为3.5g,可知原l0g该样品中锌的质量为10g-3.5g=6.5g,用锌
的质量很容易利用化学方程式求得硫酸溶质的质量为9.8g,所以稀硫酸中溶质的质量分数=
×100%=19.6%。(3)显然,根据锌与稀硫酸可以反应,得出在使用黄铜制品时应
注意避免与酸接触。
【答案】
【点评】本题考查金属与酸反应的有关化学方程式的基本计算。解题关键是准确判断黄
铜中的铜与酸不反应(因为铜排在氢后),只有黄铜中的锌与稀硫酸中的溶质硫酸发生反
应,根据恰好完全反应,可知每一种反应物均无剩余。由此可知 10g样品中铜的质量为
3.5g,锌的质量为6.5g。以此为突破口可顺利作答。