文档内容
选择题标准练(七)
1.(2024·安徽黄山二模)化学与人类生活密切相关,下列说法错误的是( )
A.二氧化硫可作漂白剂、防腐剂,还是一种食品添加剂
B.葡萄糖制备“碳量子点”是一种绿色、低成本的方法
C.研发催化剂将二氧化碳转化为甲醇,有助于我国2060年前实现碳中和的目标
D.三星堆青铜大立人以合金为材料,其深埋于地下生锈是发生了析氢腐蚀
2.(2024·辽宁重点高中协作校二模)类比是一种重要的学习方法,下列“类比”中错误的是( )
A.电解熔融NaCl可制Na,则电解熔融MgCl 可制Mg
2
B.Na N与盐酸反应生成NaCl和NH Cl,则MgN 与盐酸反应生成MgCl 和NH Cl
3 4 3 2 2 4
C.NaOH溶液与少量AgNO 溶液反应生成AgOH和NaNO ,则氨水与少量AgNO 溶液反应生成
3 3 3
AgOH和NH NO
4 3
D.Al3+与HCO- 在溶液中可发生相互促进的水解反应生成沉淀和气体,Fe3+与HCO-
也如此
3 3
3.(2024·江苏连云港第一次调研)周期表中ⅡA族元素及其化合物应用广泛。铍的化合物性质与铝相
似,BeO的熔点为2 575 ℃,熔融时BeF 能导电,而BeCl 不能导电;Mg的燃烧热为610 kJ·mol-1,实验室
2 2
中常用酸性KMnO 溶液测定物品中不溶性CaC O 的含量。下列化学反应表示正确的是 (
4 2 4
)
A.BeO与NaOH溶液反应:BeO+NaOH Na[Be(OH) ]
4
B.镁的燃烧:2Mg(s)+O(g) 2MgO(s)
2
ΔH=-610 kJ·mol-1
C.向Mg(HCO )
溶液中滴加足量NaOH溶液:Mg2++2HCO-
+4OH- Mg(OH)
↓+2CO2-
+2H O
3 2 3 2 3 2
D.用酸性KMnO 溶液测定CaC O
的含量:5CO2- +2MnO-
+16H+ 2Mn2++10CO ↑+8H O
4 2 4 2 4 4 2 2
4.(2024·黑龙江齐齐哈尔一模)下列实验能达到实验目的的是( )
A. B.
通过控制止水夹a来制取Fe(OH) 灼烧Cu (OH) CO 制备CuO
2 2 2 3
C. D.用于分离苯和液溴的混合物 铁件镀铜
5.(2024·江西九江十校第二次联考)以叶蛇纹石[主要成分是Mg(Si O )(OH) ,含少量Fe O、FeO、
6 4 10 8 2 3
Al O 等]为原料提取高纯硅的流程如下:
2 3
叶蛇纹石 SiO 粗硅 SiHCl 高纯硅
2 3
下列说法错误的是( )
A.操作1为过滤
B.反应2的副产物可作燃料
C.反应3和反应4的副产物可循环利用
D.上述流程中有两步发生了氧化还原反应
6.(2024·甘肃张掖第三次诊断)物质的结构决定其性质。下列实例与解释相符的是( )
选项 实例 解释
酸性:
A
的相对分子质量大,酸性强
>C HCOOH
2 5
B 分子的极性:BF CH HO分子间存在氢键,CH 分子间不存在氢键
2 4 2 4
D NH 比PH 易液化 NH 分子间能形成氢键
3 3 3
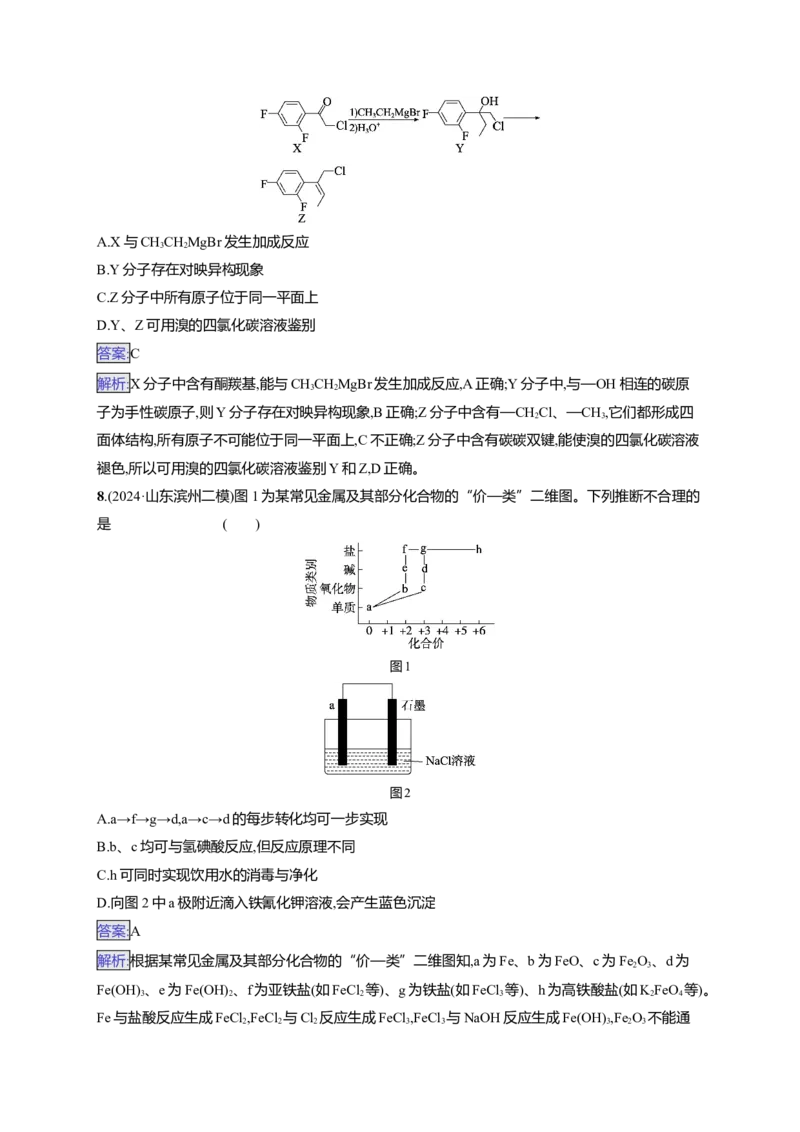
7.(2024·江苏盐城一模)化合物Z是合成药物艾氟康唑的中间体,下列说法不正确的是( )
A.X与CHCHMgBr发生加成反应
3 2
B.Y分子存在对映异构现象
C.Z分子中所有原子位于同一平面上
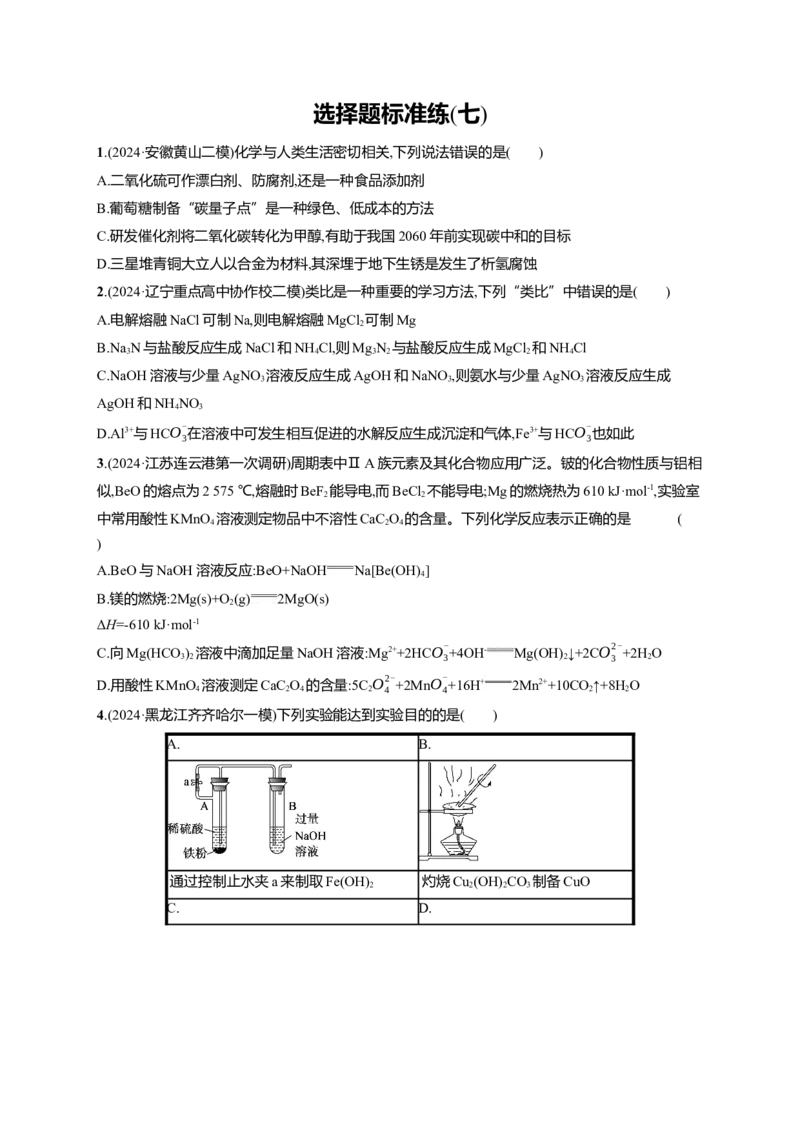
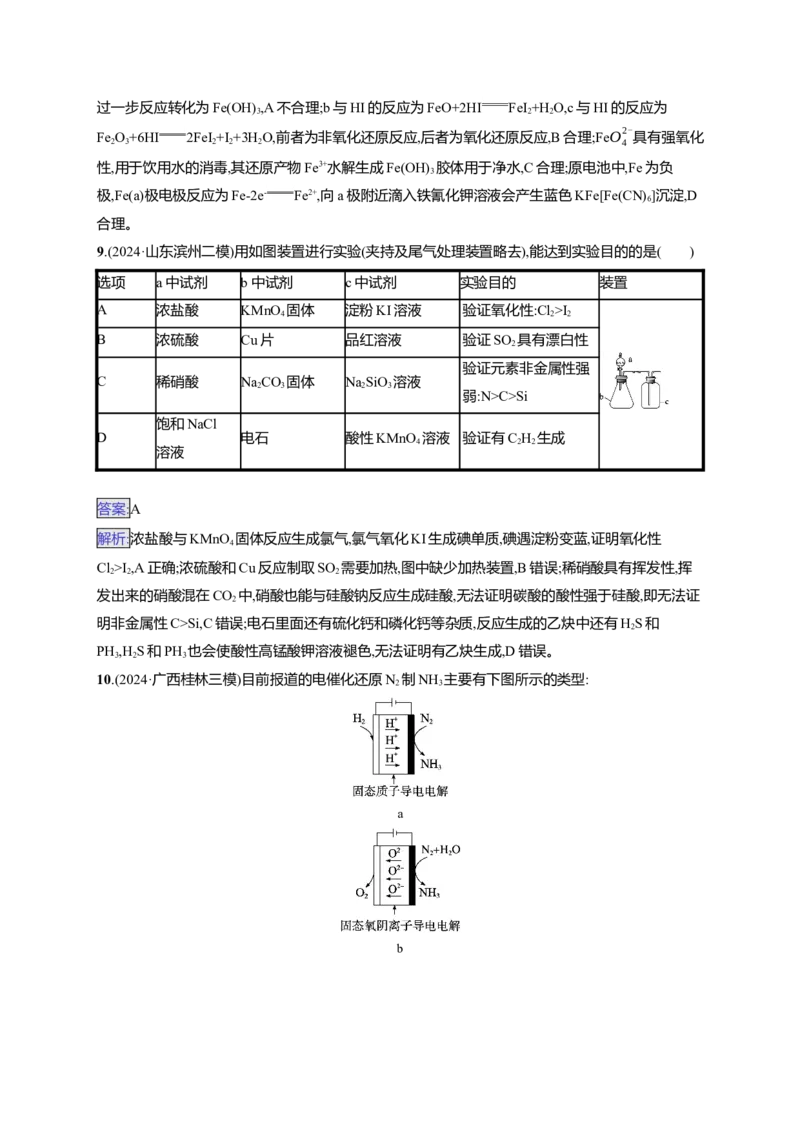
D.Y、Z可用溴的四氯化碳溶液鉴别8.(2024·山东滨州二模)图1为某常见金属及其部分化合物的“价—类”二维图。下列推断不合理的
是 ( )
图1
图2
A.a→f→g→d,a→c→d的每步转化均可一步实现
B.b、c均可与氢碘酸反应,但反应原理不同
C.h可同时实现饮用水的消毒与净化
D.向图2中a极附近滴入铁氰化钾溶液,会产生蓝色沉淀
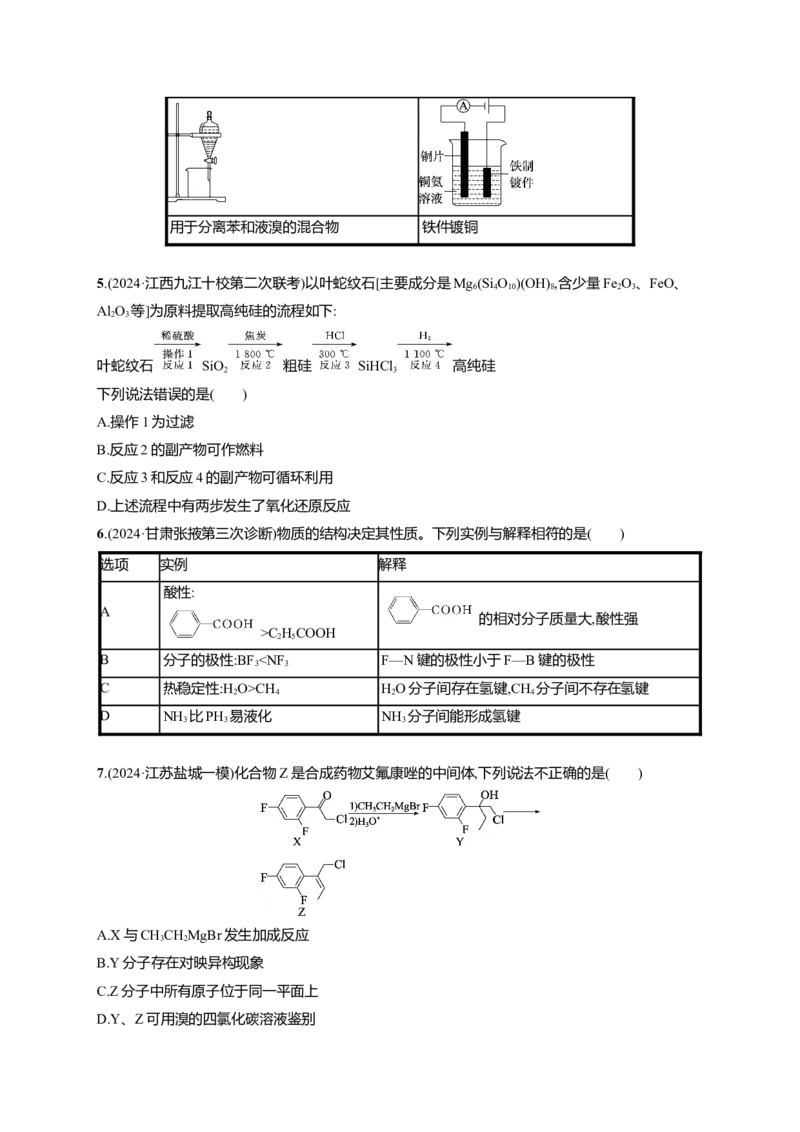
9.(2024·山东滨州二模)用如图装置进行实验(夹持及尾气处理装置略去),能达到实验目的的是( )
选项 a中试剂 b中试剂 c中试剂 实验目的 装置
A 浓盐酸 KMnO 固体 淀粉KI溶液 验证氧化性:Cl >I
4 2 2
B 浓硫酸 Cu片 品红溶液 验证SO 具有漂白性
2
验证元素非金属性强
C 稀硝酸 NaCO 固体 NaSiO 溶液
2 3 2 3
弱:N>C>Si
饱和NaCl
D 电石 酸性KMnO 溶液 验证有C H 生成
4 2 2
溶液
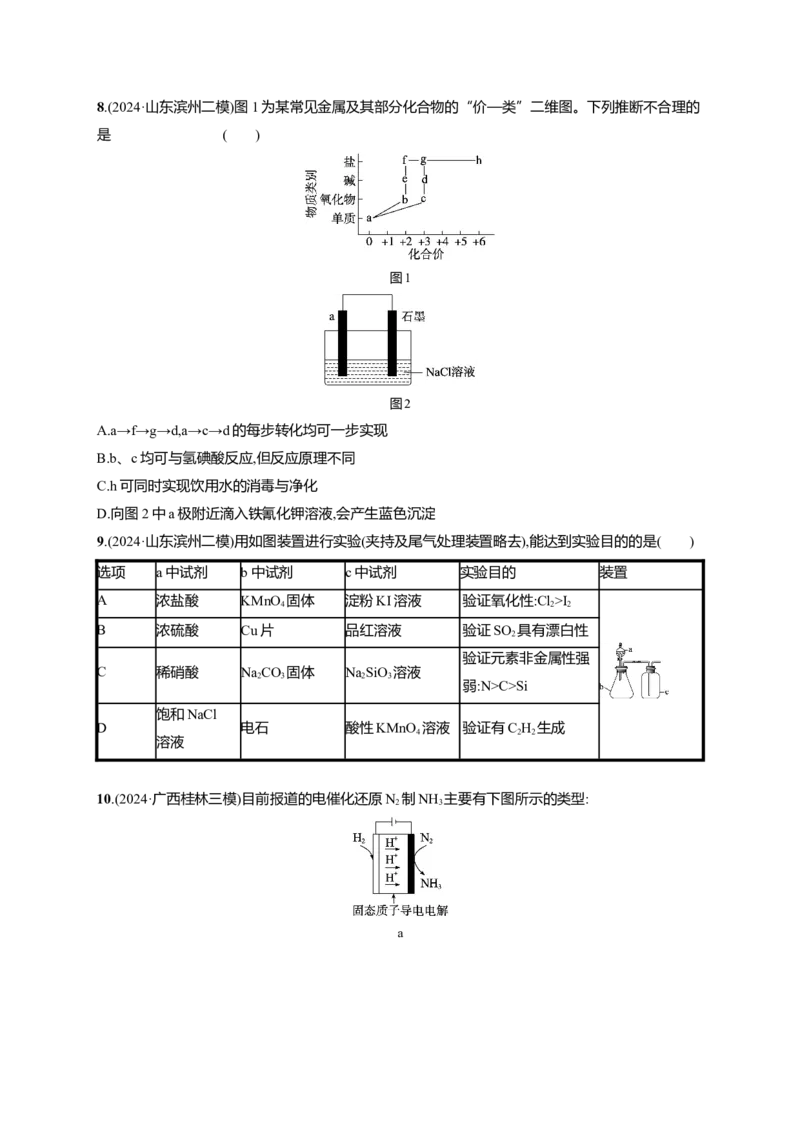
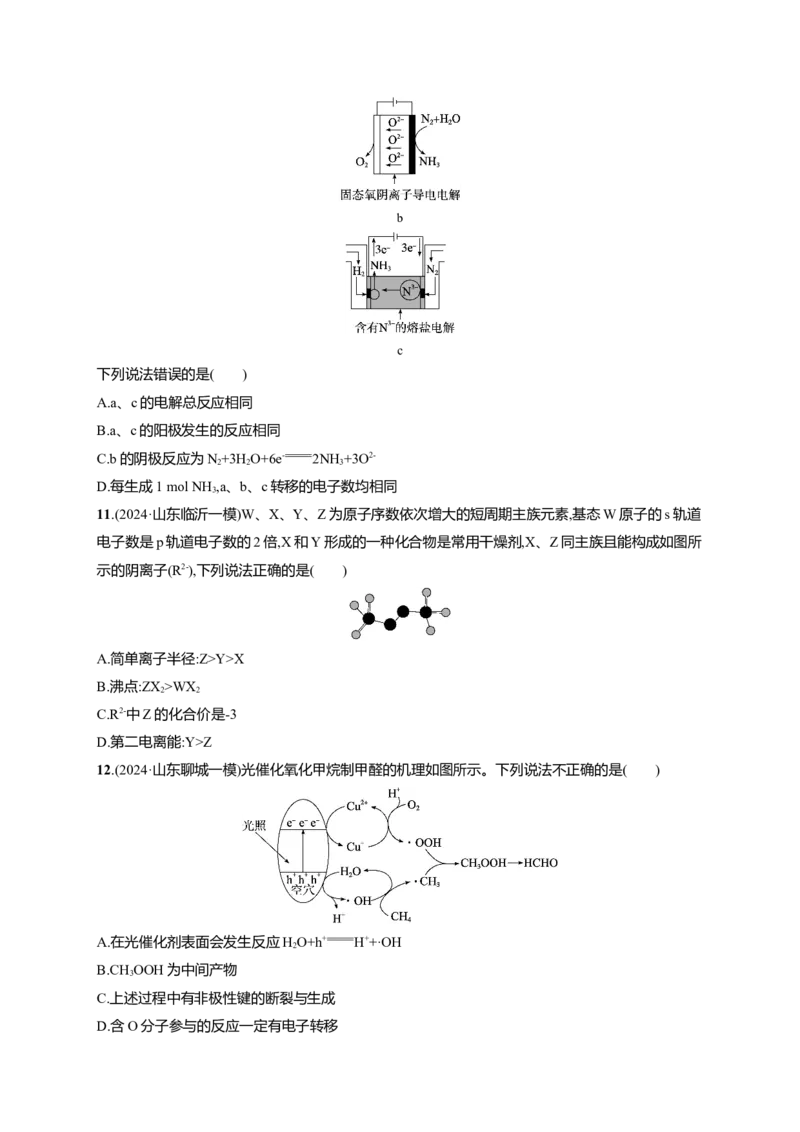
10.(2024·广西桂林三模)目前报道的电催化还原N 制NH 主要有下图所示的类型:
2 3
ab
c
下列说法错误的是( )
A.a、c的电解总反应相同
B.a、c的阳极发生的反应相同
C.b的阴极反应为N+3H O+6e- 2NH +3O2-
2 2 3
D.每生成1 mol NH ,a、b、c转移的电子数均相同
3
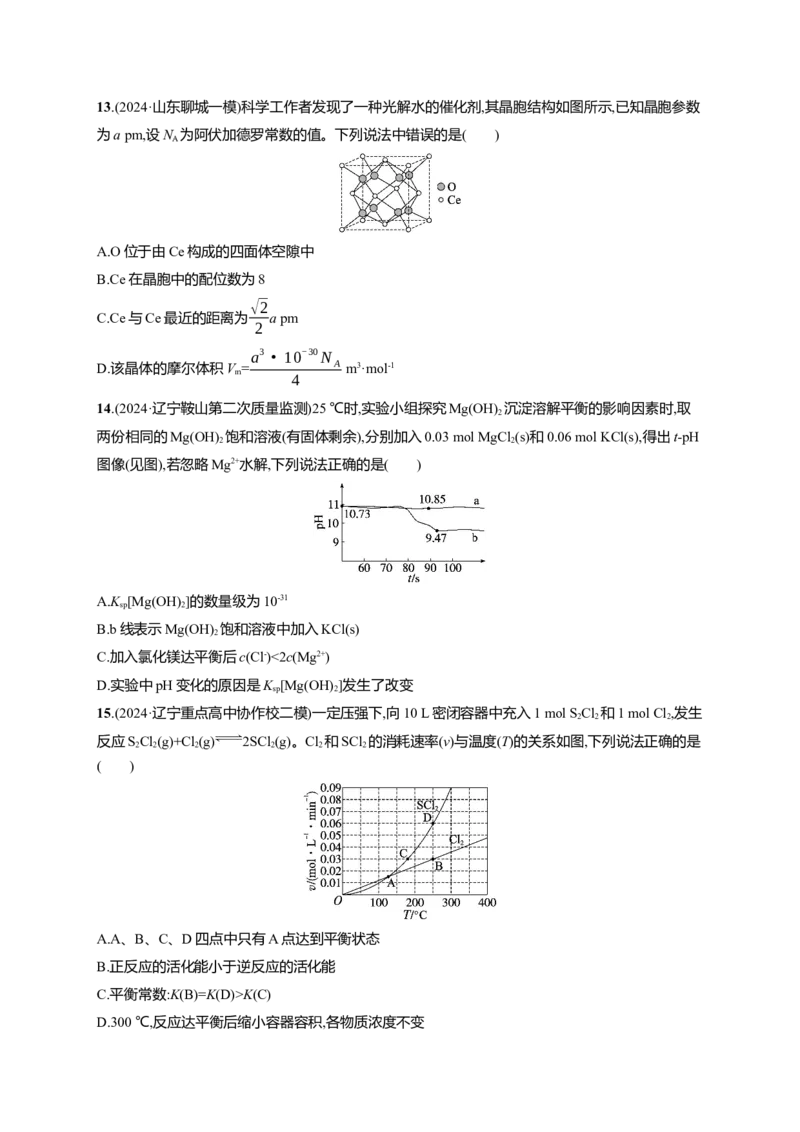
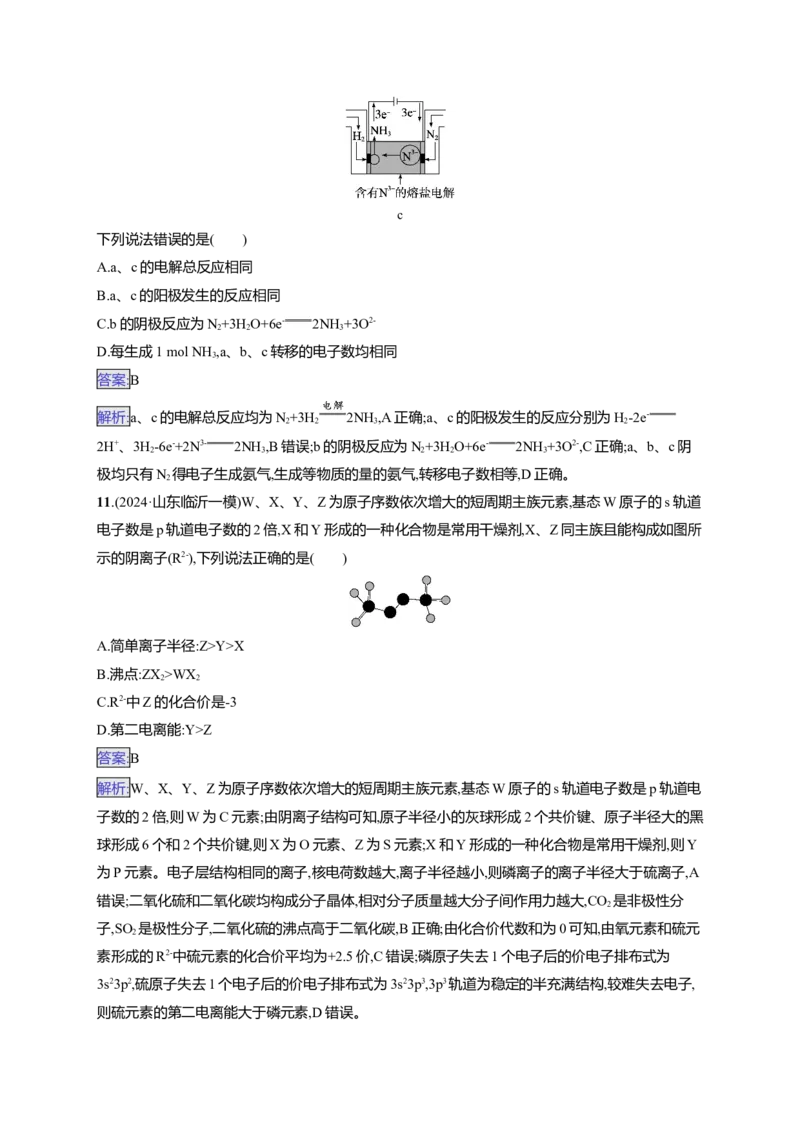
11.(2024·山东临沂一模)W、X、Y、Z为原子序数依次增大的短周期主族元素,基态W原子的s轨道
电子数是p轨道电子数的2倍,X和Y形成的一种化合物是常用干燥剂,X、Z同主族且能构成如图所
示的阴离子(R2-),下列说法正确的是( )
A.简单离子半径:Z>Y>X
B.沸点:ZX >WX
2 2
C.R2-中Z的化合价是-3
D.第二电离能:Y>Z
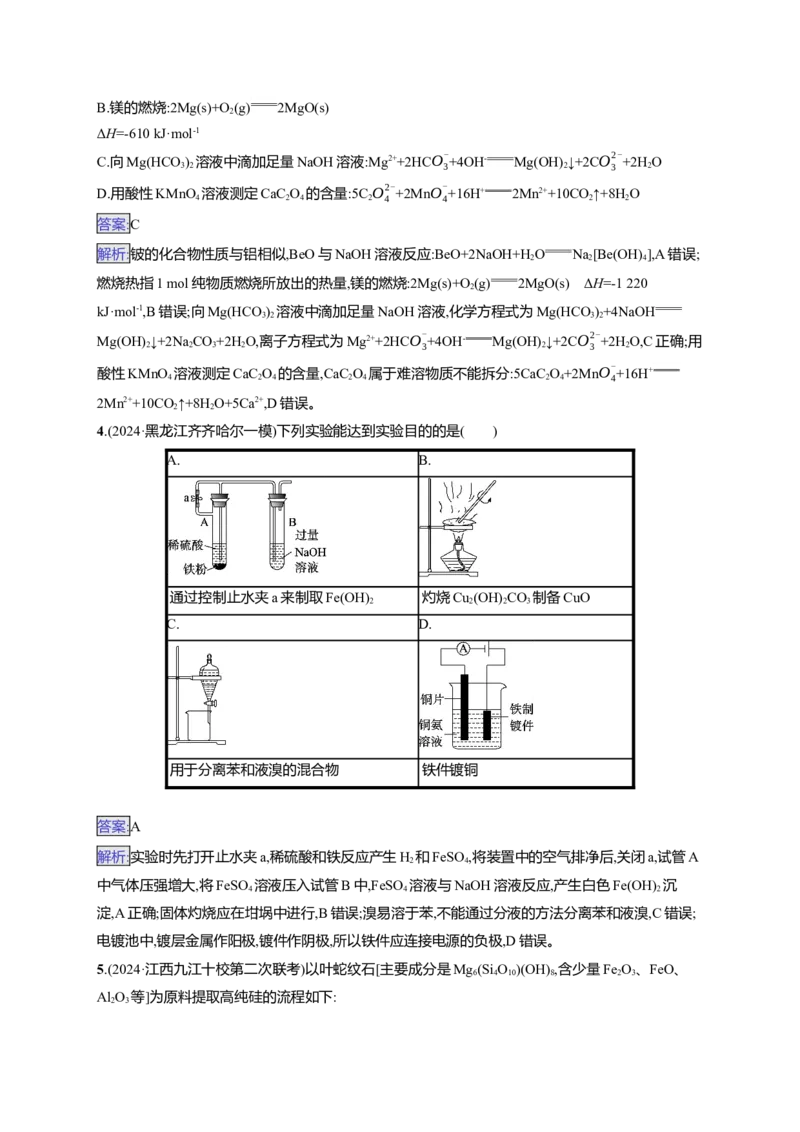
12.(2024·山东聊城一模)光催化氧化甲烷制甲醛的机理如图所示。下列说法不正确的是( )
A.在光催化剂表面会发生反应HO+h+ H++·OH
2
B.CH OOH为中间产物
3
C.上述过程中有非极性键的断裂与生成
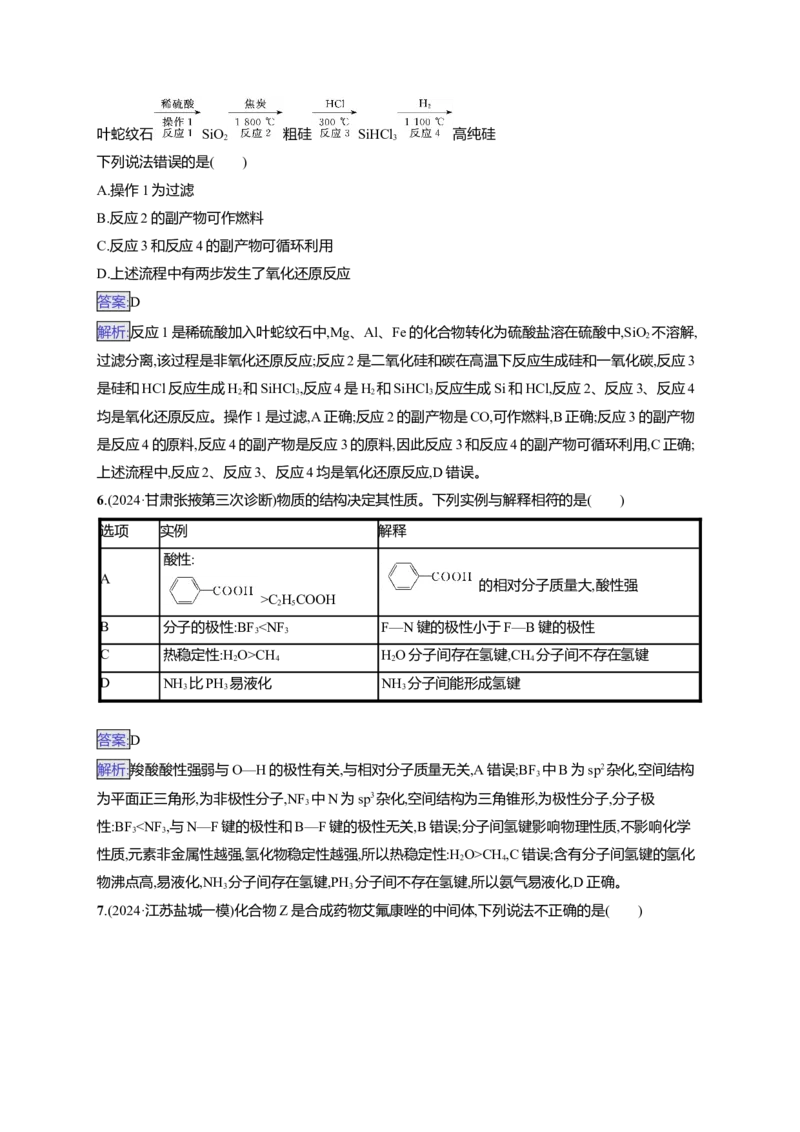
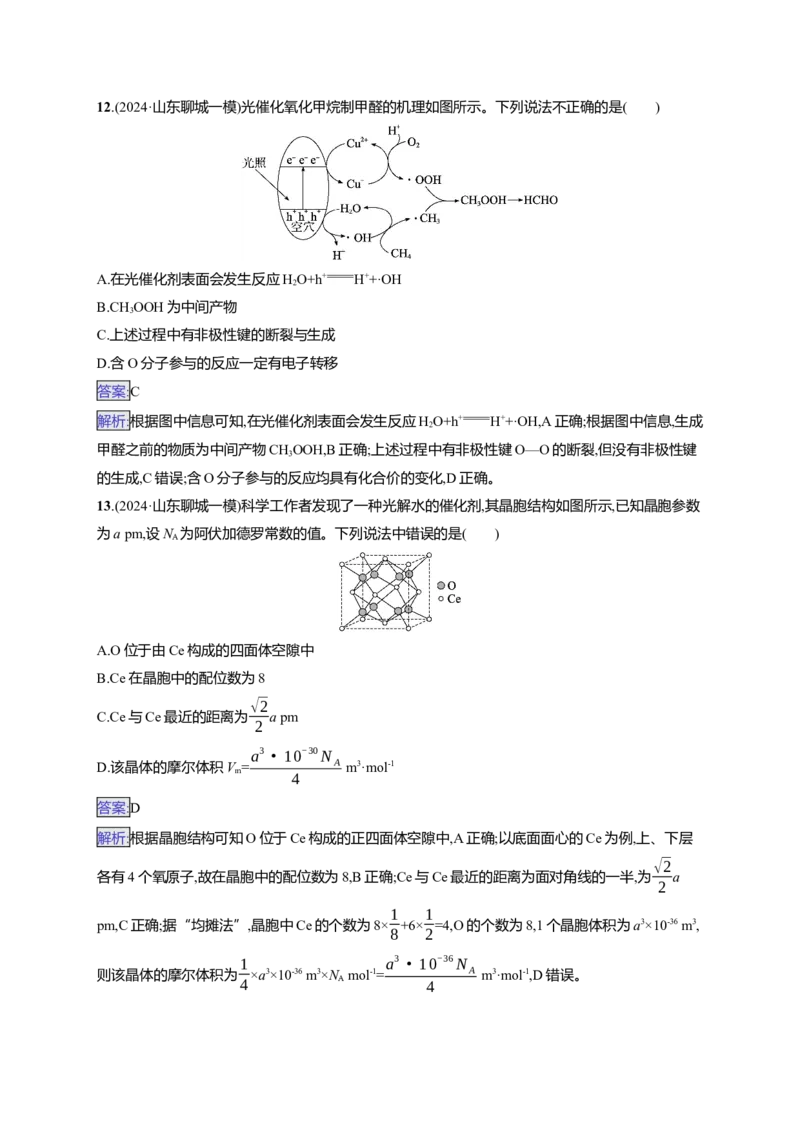
D.含O分子参与的反应一定有电子转移13.(2024·山东聊城一模)科学工作者发现了一种光解水的催化剂,其晶胞结构如图所示,已知晶胞参数
为a pm,设N 为阿伏加德罗常数的值。下列说法中错误的是( )
A
A.O位于由Ce构成的四面体空隙中
B.Ce在晶胞中的配位数为8
√2
C.Ce与Ce最近的距离为 a pm
2
a3·10-30N
D.该晶体的摩尔体积V = A m3·mol-1
m
4
14.(2024·辽宁鞍山第二次质量监测)25 ℃时,实验小组探究Mg(OH) 沉淀溶解平衡的影响因素时,取
2
两份相同的Mg(OH) 饱和溶液(有固体剩余),分别加入0.03 mol MgCl (s)和0.06 mol KCl(s),得出t-pH
2 2
图像(见图),若忽略Mg2+水解,下列说法正确的是( )
A.K [Mg(OH) ]的数量级为10-31
sp 2
B.b线表示Mg(OH) 饱和溶液中加入KCl(s)
2
C.加入氯化镁达平衡后c(Cl-)<2c(Mg2+)
D.实验中pH变化的原因是K [Mg(OH) ]发生了改变
sp 2
15.(2024·辽宁重点高中协作校二模)一定压强下,向10 L密闭容器中充入1 mol S Cl 和1 mol Cl ,发生
2 2 2
反应SCl(g)+Cl (g) 2SCl (g)。Cl 和SCl 的消耗速率(v)与温度(T)的关系如图,下列说法正确的是
2 2 2 2 2 2
( )
A.A、B、C、D四点中只有A点达到平衡状态
B.正反应的活化能小于逆反应的活化能
C.平衡常数:K(B)=K(D)>K(C)
D.300 ℃,反应达平衡后缩小容器容积,各物质浓度不变选择题标准练(七)
1.(2024·安徽黄山二模)化学与人类生活密切相关,下列说法错误的是( )
A.二氧化硫可作漂白剂、防腐剂,还是一种食品添加剂
B.葡萄糖制备“碳量子点”是一种绿色、低成本的方法
C.研发催化剂将二氧化碳转化为甲醇,有助于我国2060年前实现碳中和的目标
D.三星堆青铜大立人以合金为材料,其深埋于地下生锈是发生了析氢腐蚀
答案:D
解析:二氧化硫有毒,可以起到杀菌的作用,二氧化硫具有还原性,是一种常见的抗氧化剂,所以二氧化
硫可作漂白剂、防腐剂,还是一种食品添加剂,A正确;葡萄糖来源丰富、廉价易得,所以用葡萄糖制备
“碳量子点”是一种绿色、低成本的方法,B正确;将二氧化碳转化为甲醇可以减少二氧化碳的排放,
有助于我国2060年前实现碳中和的目标,C正确;青铜深埋于地下生锈是因为发生了吸氧腐蚀,D错误。
2.(2024·辽宁重点高中协作校二模)类比是一种重要的学习方法,下列“类比”中错误的是( )
A.电解熔融NaCl可制Na,则电解熔融MgCl 可制Mg
2
B.Na N与盐酸反应生成NaCl和NH Cl,则MgN 与盐酸反应生成MgCl 和NH Cl
3 4 3 2 2 4
C.NaOH溶液与少量AgNO 溶液反应生成AgOH和NaNO ,则氨水与少量AgNO 溶液反应生成
3 3 3
AgOH和NH NO
4 3
D.Al3+与HCO- 在溶液中可发生相互促进的水解反应生成沉淀和气体,Fe3+与HCO-
也如此
3 3
答案:C
解析:Na和Mg均为活泼金属,工业上电解熔融NaCl可制金属Na,电解熔融MgCl 可制金属Mg,A正
2
确;Na N与盐酸反应生成NaCl和NH Cl,根据相似规律,Mg N 与盐酸反应生成MgCl 和NH Cl,B正
3 4 3 2 2 4
确;NaOH溶液与少量AgNO 溶液反应生成AgOH和NaNO ,氨水与少量AgNO 溶液反应生成
3 3 3
[Ag(NH)]OH和NH NO
,C错误;Al3+与HCO-
在溶液中可发生相互促进的水解反应生成氢氧化铝沉
3 2 4 3 3
淀和二氧化碳气体,Fe3+与HCO-
在溶液中也可以发生相互促进的水解反应生成氢氧化铁沉淀和二氧
3
化碳气体,D正确。
3.(2024·江苏连云港第一次调研)周期表中ⅡA族元素及其化合物应用广泛。铍的化合物性质与铝相
似,BeO的熔点为2 575 ℃,熔融时BeF 能导电,而BeCl 不能导电;Mg的燃烧热为610 kJ·mol-1,实验室
2 2
中常用酸性KMnO 溶液测定物品中不溶性CaC O 的含量。下列化学反应表示正确的是 (
4 2 4
)
A.BeO与NaOH溶液反应:BeO+NaOH Na[Be(OH) ]
4B.镁的燃烧:2Mg(s)+O(g) 2MgO(s)
2
ΔH=-610 kJ·mol-1
C.向Mg(HCO )
溶液中滴加足量NaOH溶液:Mg2++2HCO-
+4OH- Mg(OH)
↓+2CO2-
+2H O
3 2 3 2 3 2
D.用酸性KMnO 溶液测定CaC O
的含量:5CO2- +2MnO-
+16H+ 2Mn2++10CO ↑+8H O
4 2 4 2 4 4 2 2
答案:C
解析:铍的化合物性质与铝相似,BeO与NaOH溶液反应:BeO+2NaOH+H O Na[Be(OH) ],A错误;
2 2 4
燃烧热指1 mol纯物质燃烧所放出的热量,镁的燃烧:2Mg(s)+O(g) 2MgO(s) ΔH=-1 220
2
kJ·mol-1,B错误;向Mg(HCO ) 溶液中滴加足量NaOH溶液,化学方程式为Mg(HCO )+4NaOH
3 2 3 2
Mg(OH) ↓+2Na CO+2H
O,离子方程式为Mg2++2HCO-
+4OH- Mg(OH)
↓+2CO2-
+2H O,C正确;用
2 2 3 2 3 2 3 2
酸性KMnO 溶液测定CaC O 的含量,CaC O 属于难溶物质不能拆分:5CaC
O+2MnO-
+16H+
4 2 4 2 4 2 4 4
2Mn2++10CO ↑+8H O+5Ca2+,D错误。
2 2
4.(2024·黑龙江齐齐哈尔一模)下列实验能达到实验目的的是( )
A. B.
通过控制止水夹a来制取Fe(OH) 灼烧Cu (OH) CO 制备CuO
2 2 2 3
C. D.
用于分离苯和液溴的混合物 铁件镀铜
答案:A
解析:实验时先打开止水夹a,稀硫酸和铁反应产生H 和FeSO ,将装置中的空气排净后,关闭a,试管A
2 4
中气体压强增大,将FeSO 溶液压入试管B中,FeSO 溶液与NaOH溶液反应,产生白色Fe(OH) 沉
4 4 2
淀,A正确;固体灼烧应在坩埚中进行,B错误;溴易溶于苯,不能通过分液的方法分离苯和液溴,C错误;
电镀池中,镀层金属作阳极,镀件作阴极,所以铁件应连接电源的负极,D错误。
5.(2024·江西九江十校第二次联考)以叶蛇纹石[主要成分是Mg(Si O )(OH) ,含少量Fe O、FeO、
6 4 10 8 2 3
Al O 等]为原料提取高纯硅的流程如下:
2 3叶蛇纹石 SiO 粗硅 SiHCl 高纯硅
2 3
下列说法错误的是( )
A.操作1为过滤
B.反应2的副产物可作燃料
C.反应3和反应4的副产物可循环利用
D.上述流程中有两步发生了氧化还原反应
答案:D
解析:反应1是稀硫酸加入叶蛇纹石中,Mg、Al、Fe的化合物转化为硫酸盐溶在硫酸中,SiO 不溶解,
2
过滤分离,该过程是非氧化还原反应;反应2是二氧化硅和碳在高温下反应生成硅和一氧化碳,反应3
是硅和HCl反应生成H 和SiHCl ,反应4是H 和SiHCl 反应生成Si和HCl,反应2、反应3、反应4
2 3 2 3
均是氧化还原反应。操作1是过滤,A正确;反应2的副产物是CO,可作燃料,B正确;反应3的副产物
是反应4的原料,反应4的副产物是反应3的原料,因此反应3和反应4的副产物可循环利用,C正确;
上述流程中,反应2、反应3、反应4均是氧化还原反应,D错误。
6.(2024·甘肃张掖第三次诊断)物质的结构决定其性质。下列实例与解释相符的是( )
选项 实例 解释
酸性:
A
的相对分子质量大,酸性强
>C HCOOH
2 5
B 分子的极性:BF CH HO分子间存在氢键,CH 分子间不存在氢键
2 4 2 4
D NH 比PH 易液化 NH 分子间能形成氢键
3 3 3
答案:D
解析:羧酸酸性强弱与O—H的极性有关,与相对分子质量无关,A错误;BF 中B为sp2杂化,空间结构
3
为平面正三角形,为非极性分子,NF 中N为sp3杂化,空间结构为三角锥形,为极性分子,分子极
3
性:BF CH,C错误;含有分子间氢键的氢化
2 4
物沸点高,易液化,NH 分子间存在氢键,PH 分子间不存在氢键,所以氨气易液化,D正确。
3 3
7.(2024·江苏盐城一模)化合物Z是合成药物艾氟康唑的中间体,下列说法不正确的是( )A.X与CHCHMgBr发生加成反应
3 2
B.Y分子存在对映异构现象
C.Z分子中所有原子位于同一平面上
D.Y、Z可用溴的四氯化碳溶液鉴别
答案:C
解析:X分子中含有酮羰基,能与CHCHMgBr发生加成反应,A正确;Y分子中,与—OH相连的碳原
3 2
子为手性碳原子,则Y分子存在对映异构现象,B正确;Z分子中含有—CHCl、—CH,它们都形成四
2 3
面体结构,所有原子不可能位于同一平面上,C不正确;Z分子中含有碳碳双键,能使溴的四氯化碳溶液
褪色,所以可用溴的四氯化碳溶液鉴别Y和Z,D正确。
8.(2024·山东滨州二模)图1为某常见金属及其部分化合物的“价—类”二维图。下列推断不合理的
是 ( )
图1
图2
A.a→f→g→d,a→c→d的每步转化均可一步实现
B.b、c均可与氢碘酸反应,但反应原理不同
C.h可同时实现饮用水的消毒与净化
D.向图2中a极附近滴入铁氰化钾溶液,会产生蓝色沉淀
答案:A
解析:根据某常见金属及其部分化合物的“价—类”二维图知,a为Fe、b为FeO、c为Fe O、d为
2 3
Fe(OH) 、e为Fe(OH) 、f为亚铁盐(如FeCl 等)、g为铁盐(如FeCl 等)、h为高铁酸盐(如KFeO 等)。
3 2 2 3 2 4
Fe与盐酸反应生成FeCl ,FeCl 与Cl 反应生成FeCl ,FeCl 与NaOH反应生成Fe(OH) ,Fe O 不能通
2 2 2 3 3 3 2 3过一步反应转化为Fe(OH) ,A不合理;b与HI的反应为FeO+2HI FeI+H O,c与HI的反应为
3 2 2
Fe O+6HI 2FeI+I +3H
O,前者为非氧化还原反应,后者为氧化还原反应,B合理;FeO2-
具有强氧化
2 3 2 2 2 4
性,用于饮用水的消毒,其还原产物Fe3+水解生成Fe(OH) 胶体用于净水,C合理;原电池中,Fe为负
3
极,Fe(a)极电极反应为Fe-2e- Fe2+,向a极附近滴入铁氰化钾溶液会产生蓝色KFe[Fe(CN) ]沉淀,D
6
合理。
9.(2024·山东滨州二模)用如图装置进行实验(夹持及尾气处理装置略去),能达到实验目的的是( )
选项 a中试剂 b中试剂 c中试剂 实验目的 装置
A 浓盐酸 KMnO 固体 淀粉KI溶液 验证氧化性:Cl >I
4 2 2
B 浓硫酸 Cu片 品红溶液 验证SO 具有漂白性
2
验证元素非金属性强
C 稀硝酸 NaCO 固体 NaSiO 溶液
2 3 2 3
弱:N>C>Si
饱和NaCl
D 电石 酸性KMnO 溶液 验证有C H 生成
4 2 2
溶液
答案:A
解析:浓盐酸与KMnO 固体反应生成氯气,氯气氧化KI生成碘单质,碘遇淀粉变蓝,证明氧化性
4
Cl>I ,A正确;浓硫酸和Cu反应制取SO 需要加热,图中缺少加热装置,B错误;稀硝酸具有挥发性,挥
2 2 2
发出来的硝酸混在CO 中,硝酸也能与硅酸钠反应生成硅酸,无法证明碳酸的酸性强于硅酸,即无法证
2
明非金属性C>Si,C错误;电石里面还有硫化钙和磷化钙等杂质,反应生成的乙炔中还有HS和
2
PH ,H S和PH 也会使酸性高锰酸钾溶液褪色,无法证明有乙炔生成,D错误。
3 2 3
10.(2024·广西桂林三模)目前报道的电催化还原N 制NH 主要有下图所示的类型:
2 3
a
bc
下列说法错误的是( )
A.a、c的电解总反应相同
B.a、c的阳极发生的反应相同
C.b的阴极反应为N+3H O+6e- 2NH +3O2-
2 2 3
D.每生成1 mol NH ,a、b、c转移的电子数均相同
3
答案:B
解析:a、c的电解总反应均为N+3H 2NH ,A正确;a、c的阳极发生的反应分别为H-2e-
2 2 3 2
2H+、3H-6e-+2N3- 2NH ,B错误;b的阴极反应为N+3H O+6e- 2NH +3O2-,C正确;a、b、c阴
2 3 2 2 3
极均只有N 得电子生成氨气,生成等物质的量的氨气,转移电子数相等,D正确。
2
11.(2024·山东临沂一模)W、X、Y、Z为原子序数依次增大的短周期主族元素,基态W原子的s轨道
电子数是p轨道电子数的2倍,X和Y形成的一种化合物是常用干燥剂,X、Z同主族且能构成如图所
示的阴离子(R2-),下列说法正确的是( )
A.简单离子半径:Z>Y>X
B.沸点:ZX >WX
2 2
C.R2-中Z的化合价是-3
D.第二电离能:Y>Z
答案:B
解析:W、X、Y、Z为原子序数依次增大的短周期主族元素,基态W原子的s轨道电子数是p轨道电
子数的2倍,则W为C元素;由阴离子结构可知,原子半径小的灰球形成2个共价键、原子半径大的黑
球形成6个和2个共价键,则X为O元素、Z为S元素;X和Y形成的一种化合物是常用干燥剂,则Y
为P元素。电子层结构相同的离子,核电荷数越大,离子半径越小,则磷离子的离子半径大于硫离子,A
错误;二氧化硫和二氧化碳均构成分子晶体,相对分子质量越大分子间作用力越大,CO 是非极性分
2
子,SO 是极性分子,二氧化硫的沸点高于二氧化碳,B正确;由化合价代数和为0可知,由氧元素和硫元
2
素形成的R2-中硫元素的化合价平均为+2.5价,C错误;磷原子失去1个电子后的价电子排布式为
3s23p2,硫原子失去1个电子后的价电子排布式为3s23p3,3p3轨道为稳定的半充满结构,较难失去电子,
则硫元素的第二电离能大于磷元素,D错误。12.(2024·山东聊城一模)光催化氧化甲烷制甲醛的机理如图所示。下列说法不正确的是( )
A.在光催化剂表面会发生反应HO+h+ H++·OH
2
B.CH OOH为中间产物
3
C.上述过程中有非极性键的断裂与生成
D.含O分子参与的反应一定有电子转移
答案:C
解析:根据图中信息可知,在光催化剂表面会发生反应HO+h+ H++·OH,A正确;根据图中信息,生成
2
甲醛之前的物质为中间产物CHOOH,B正确;上述过程中有非极性键O—O的断裂,但没有非极性键
3
的生成,C错误;含O分子参与的反应均具有化合价的变化,D正确。
13.(2024·山东聊城一模)科学工作者发现了一种光解水的催化剂,其晶胞结构如图所示,已知晶胞参数
为a pm,设N 为阿伏加德罗常数的值。下列说法中错误的是( )
A
A.O位于由Ce构成的四面体空隙中
B.Ce在晶胞中的配位数为8
√2
C.Ce与Ce最近的距离为 a pm
2
a3·10-30N
D.该晶体的摩尔体积V = A m3·mol-1
m
4
答案:D
解析:根据晶胞结构可知O位于Ce构成的正四面体空隙中,A正确;以底面面心的Ce为例,上、下层
√2
各有4个氧原子,故在晶胞中的配位数为8,B正确;Ce与Ce最近的距离为面对角线的一半,为 a
2
1 1
pm,C正确;据“均摊法”,晶胞中Ce的个数为8× +6× =4,O的个数为8,1个晶胞体积为a3×10-36 m3,
8 2
1 a3·10-36N
则该晶体的摩尔体积为 ×a3×10-36 m3×N mol-1= A m3·mol-1,D错误。
4 A 414.(2024·辽宁鞍山第二次质量监测)25 ℃时,实验小组探究Mg(OH) 沉淀溶解平衡的影响因素时,取
2
两份相同的Mg(OH) 饱和溶液(有固体剩余),分别加入0.03 mol MgCl (s)和0.06 mol KCl(s),得出t-pH
2 2
图像(见图),若忽略Mg2+水解,下列说法正确的是( )
A.K [Mg(OH) ]的数量级为10-31
sp 2
B.b线表示Mg(OH) 饱和溶液中加入KCl(s)
2
C.加入氯化镁达平衡后c(Cl-)<2c(Mg2+)
D.实验中pH变化的原因是K [Mg(OH) ]发生了改变
sp 2
答案:C
解析:从图中可知Mg(OH) 饱和溶液的pH=10.73,可知饱和溶液中c(OH-)=1×10-3.27
2
mol·L-1,c(Mg2+)=5×10-4.27 mol·L-1。K [Mg(OH) ]=c(Mg2+)·c2(OH-)=5×10-4.27×(1×10-3.27)2=5×10-10.81,数量级
sp 2
为10-11,A错误;温度不变,K 不变,加入MgCl (s)使得沉淀溶解平衡Mg(OH) (s) Mg2+(aq)+2OH-(aq)
sp 2 2
逆向进行,Mg(OH) 的溶解度减小,溶液pH减小,故b线表示Mg(OH) 饱和溶液中加入MgCl (s),B错
2 2 2
误;加入MgCl (s),平衡后溶液呈碱性,c(OH-)>c(H+),结合电荷守恒表达式2c(Mg2+)+c(H+)=c(OH-)
2
+c(Cl-),可得c(Cl-)<2c(Mg2+),C正确;温度不变,K 不变,故实验中pH变化不是K 变化引起的,而是
sp sp
Mg(OH) 的沉淀溶解平衡移动引起的,D错误。
2
15.(2024·辽宁重点高中协作校二模)一定压强下,向10 L密闭容器中充入1 mol S Cl 和1 mol Cl ,发生
2 2 2
反应SCl(g)+Cl (g) 2SCl (g)。Cl 和SCl 的消耗速率(v)与温度(T)的关系如图,下列说法正确的是
2 2 2 2 2 2
( )
A.A、B、C、D四点中只有A点达到平衡状态
B.正反应的活化能小于逆反应的活化能
C.平衡常数:K(B)=K(D)>K(C)
D.300 ℃,反应达平衡后缩小容器容积,各物质浓度不变
答案:B解析:Cl 的消耗速率表示正反应速率,SCl 的消耗速率表示逆反应速率,当v (Cl )∶v (SCl )=1∶2
2 2 消耗 2 消耗 2
时,说明正逆反应速率相等,反应到达平衡,所以图像的平衡点应为B和D点。A点v (Cl )∶v
消耗 2 消耗
(SCl )=1∶1,未达到平衡,A错误;随着温度升高,SCl 的消耗速率大于Cl 的消耗速率的2倍,则逆反应
2 2 2
速率大于正反应速率,说明温度升高,平衡逆向移动,是放热反应,则正反应的活化能小于逆反应的活
化能,B正确;该反应为放热反应,温度升高,K减小,由图可知,B、C、D三点中C点温度最低,则K最大,
故K(C)>K(B)=K(D),C错误;300 ℃时,反应达平衡后缩小容器容积,平衡不移动,但是容积缩小,各组分
浓度均增大,D错误。