文档内容
押广东卷第 15 题
化学反应速率与平衡 水溶液中的离子平衡
核心考点 考情统计 考向预测 备考策略
2023·广东卷,15
化学反应 考查反应机理和催化剂,平衡 1.化学平衡和反应速率的题
2022·广东卷,13,
速率与平 移动的影响因素,体现综合 目,应以分析图像为主,尤其
15
衡 性; 是曲线的分析。
2021·广东卷,14
考查溶液中的离子平衡,涉及 2.水溶液中的离子平衡,广
溶液中发生的反应,离子浓度 东卷大概率出现在原理大题,
水溶液中
大小比较,体现综合性和应用 选择题以基础为主,应回归基
的离子平 2021·广东卷,8
性。 本图像。
衡
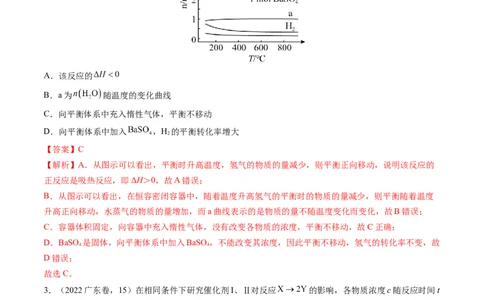
1.(2023广东卷,15)催化剂Ⅰ和Ⅱ均能催化反应 。反应历程(下图)中,M为中间产物。其
它条件相同时,下列说法不正确的是
A.使用Ⅰ和Ⅱ,反应历程都分4步进行 B.反应达平衡时,升高温度,R的浓度增大
C.使用Ⅱ时,反应体系更快达到平衡 D.使用Ⅰ时,反应过程中M所能达到的最高浓度更大
【答案】C
【解析】A.由图可知两种催化剂均出现四个波峰,所以使用Ⅰ和Ⅱ,反应历程都分4步进行,A正确;
B.由图可知该反应是放热反应,所以达平衡时,升高温度平衡向左移动,R的浓度增大,B正确;
C.由图可知Ⅰ的最高活化能小于Ⅱ的最高活化能,所以使用Ⅰ时反应速率更快,反应体系更快达到平
衡,C错误;D.由图可知在前两个历程中使用Ⅰ活化能较低反应速率较快,后两个历程中使用Ⅰ活化能较高反应速率
较慢,所以使用Ⅰ时,反应过程中M所能达到的最高浓度更大,D正确;
故选C。
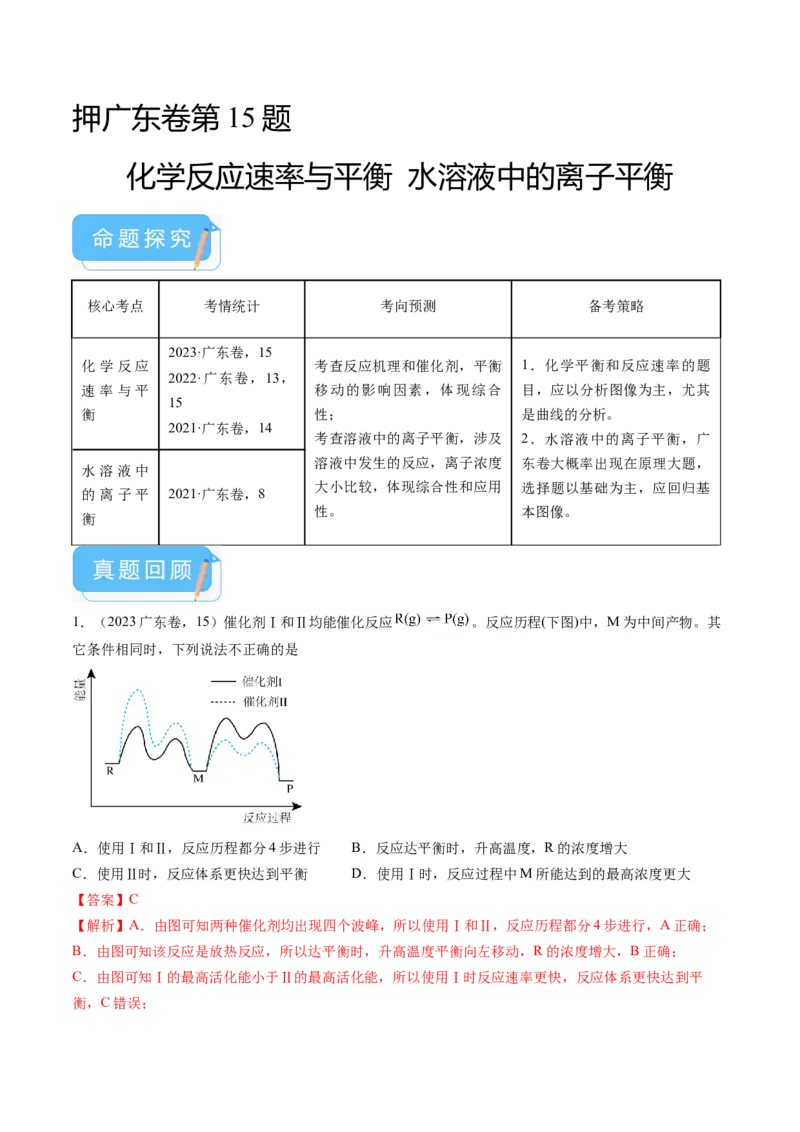
2.(2022广东卷,13)恒容密闭容器中, 在不同温度下达平衡
时,各组分的物质的量(n)如图所示。下列说法正确的是
A.该反应的
B.a为 随温度的变化曲线
C.向平衡体系中充入惰性气体,平衡不移动
D.向平衡体系中加入 ,H 的平衡转化率增大
2
【答案】C
【解析】A.从图示可以看出,平衡时升高温度,氢气的物质的量减少,则平衡正向移动,说明该反应的
正反应是吸热反应,即ΔH>0,故A错误;
B.从图示可以看出,在恒容密闭容器中,随着温度升高氢气的平衡时的物质的量减少,则平衡随着温度
升高正向移动,水蒸气的物质的量增加,而a曲线表示的是物质的量不随温度变化而变化,故B错误;
C.容器体积固定,向容器中充入惰性气体,没有改变各物质的浓度,平衡不移动,故C正确;
D.BaSO 是固体,向平衡体系中加入BaSO,不能改变其浓度,因此平衡不移动,氢气的转化率不变,故
4 4
D错误;
故选C。
3.(2022广东卷,15)在相同条件下研究催化剂I、Ⅱ对反应 的影响,各物质浓度c随反应时间t
的部分变化曲线如图,则
A.无催化剂时,反应不能进行B.与催化剂Ⅰ相比,Ⅱ使反应活化能更低
C.a曲线表示使用催化剂Ⅱ时X的浓度随t的变化
D.使用催化剂Ⅰ时, 内,
【答案】D
【解析】A.由图可知,无催化剂时,随反应进行,生成物浓度也在增加,说明反应也在进行,故A错
误;
B.由图可知,催化剂I比催化剂II催化效果好,说明催化剂I使反应活化能更低,反应更快,故B错误;
C.由图可知,使用催化剂II时,在0~2min 内Y的浓度变化了2.0mol/L,而a曲线表示的X的浓度变化
了2.0mol/L,二者变化量之比不等于化学计量数之比,所以a曲线不表示使用催化剂II时X浓度随时间t
的变化,故C错误;
D.使用催化剂I时,在0~2min 内,Y的浓度变化了4.0mol/L,则 (Y) = = =2.0
, (X) = (Y) = 2.0 =1.0 ,故D正确;
答案选D。
4.(2021广东卷,8)鸟嘌呤( )是一种有机弱碱,可与盐酸反应生成盐酸盐(用 表示)。已知
水溶液呈酸性,下列叙述正确的是
A. 水溶液的
B. 水溶液加水稀释, 升高
C. 在水中的电离方程式为:
D. 水溶液中:
【答案】B
【解析】
A.GHCl为强酸弱碱盐,电离出的GH+会发生水解,弱离子的水解较为微弱,因此0.001mol/L GHCl水溶
液的pH>3,故A错误;
B.稀释GHCl溶液时,GH+水解程度将增大,根据勒夏特列原理可知溶液中c(H+)将减小,溶液pH将升
高,故B正确;
C.GHCl为强酸弱碱盐,在水中电离方程式为GHCl=GH++Cl-,故C错误;
D.根据电荷守恒可知,GHCl溶液中c(OH-)+c(Cl-)=c(H+)+c(GH+),故D错误;
综上所述,叙述正确的是B项,故答案为B。
5.(2021广东卷,14)反应 经历两步:① ;② 。反应体系中 、 、 的浓度c
随时间t的变化曲线如图所示。下列说法不正确的是A.a为 随t的变化曲线
B. 时,
C. 时, 的消耗速率大于生成速率
D. 后,
【答案】D
【分析】
由题中信息可知,反应 经历两步:① ;② 。因此,图中呈不断减小趋势的a线为X
的浓度 随时间 的变化曲线,呈不断增加趋势的线为Z的浓度 随时间 的变化曲线,先增加后减小的线
为Y的浓度 随时间 的变化曲线。
【解析】
A.X是唯一的反应物,随着反应的发生,其浓度不断减小,因此,由图可知, 为 随 的变化曲
线,A正确;
B.由图可知,分别代表3种不同物质的曲线相交于 时刻,因此, 时 ,B正确;
C.由图中信息可知, 时刻以后,Y的浓度仍在不断减小,说明 时刻反应两步仍在向正反应方向发生,
而且反应①生成Y的速率小于反应②消耗Y的速率,即 时 的消耗速率大于生成速率,C正确;
D.由图可知, 时刻反应①完成,X完全转化为Y,若无反应②发生,则 ,由于反应②
的发生, 时刻Y浓度的变化量为 ,变化量之比等于化学计量数之比,所以Z的浓度的变化量为
,这种关系在 后仍成立, 因此,D不正确。
综上所述,本题选D。
一、化学反应速率与平衡
知能点1 化学反应机理与历程
1.反应机理
(1)反应机理是用来描述某反应物到反应产物所经由的全部基元反应,就是把一个复杂反应分解成若干个基元反应,以图示的形式来描述某一化学变化所经由的全部反应,然后按照一定规律组合起来,从而阐述复
杂反应的内在联系,以及总反应与基元反应内在联系。
(2)反应机理详细描述了每一步转化的过程,包括过渡态的形成、键的断裂和生成以及各步的相对速率大小
等。典型的反应机理理论是基元反应碰撞理论和基元反应过渡态理论。
(3)反应机理中包含的基元反应是单分子反应或双分子反应。完整的反应机理需要考虑到反应物、催化剂、
反应的立体化学、产物以及各物质的用量。
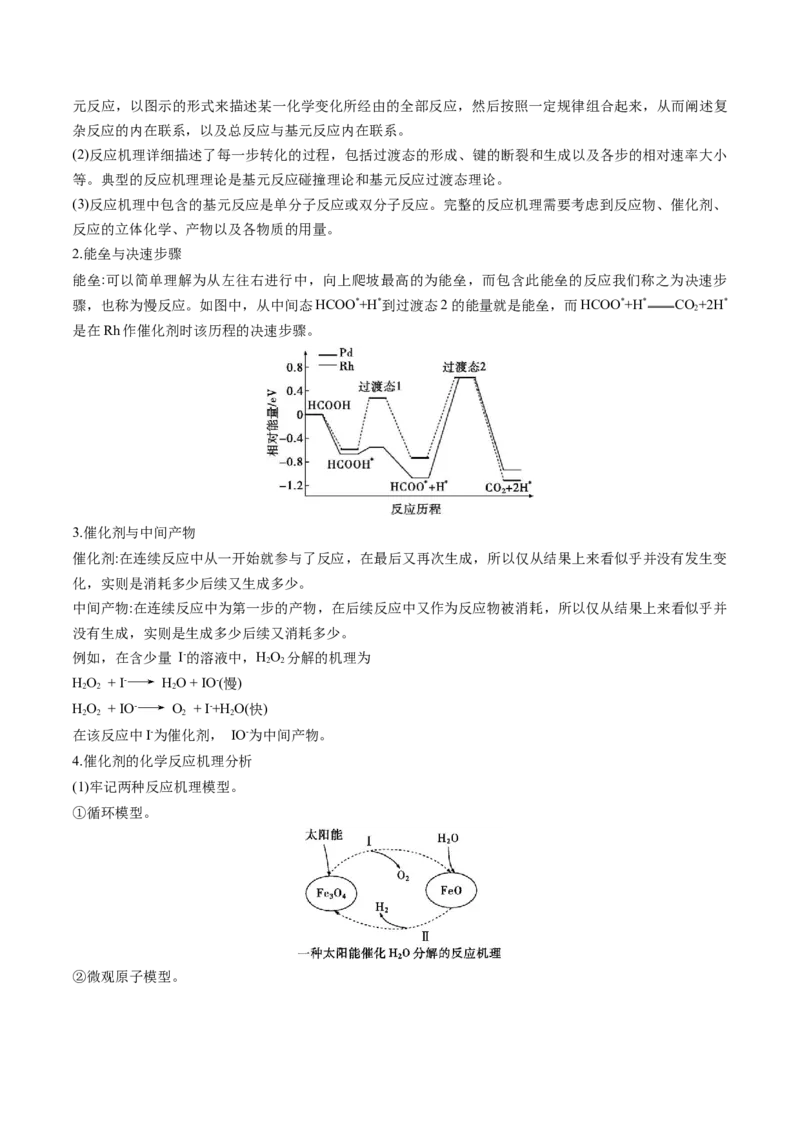
2.能垒与决速步骤
能垒:可以简单理解为从左往右进行中,向上爬坡最高的为能垒,而包含此能垒的反应我们称之为决速步
骤,也称为慢反应。如图中,从中间态HCOO*+H*到过渡态2的能量就是能垒,而HCOO*+H* CO+2H*
2
是在Rh作催化剂时该历程的决速步骤。
3.催化剂与中间产物
催化剂:在连续反应中从一开始就参与了反应,在最后又再次生成,所以仅从结果上来看似乎并没有发生变
化,实则是消耗多少后续又生成多少。
中间产物:在连续反应中为第一步的产物,在后续反应中又作为反应物被消耗,所以仅从结果上来看似乎并
没有生成,实则是生成多少后续又消耗多少。
例如,在含少量 I-的溶液中,HO 分解的机理为
2 2
HO + I- HO + IO-(慢)
2 2 2
HO + IO- O + I-+H O(快)
2 2 2 2
在该反应中I-为催化剂, IO-为中间产物。
4.催化剂的化学反应机理分析
(1)牢记两种反应机理模型。
①循环模型。
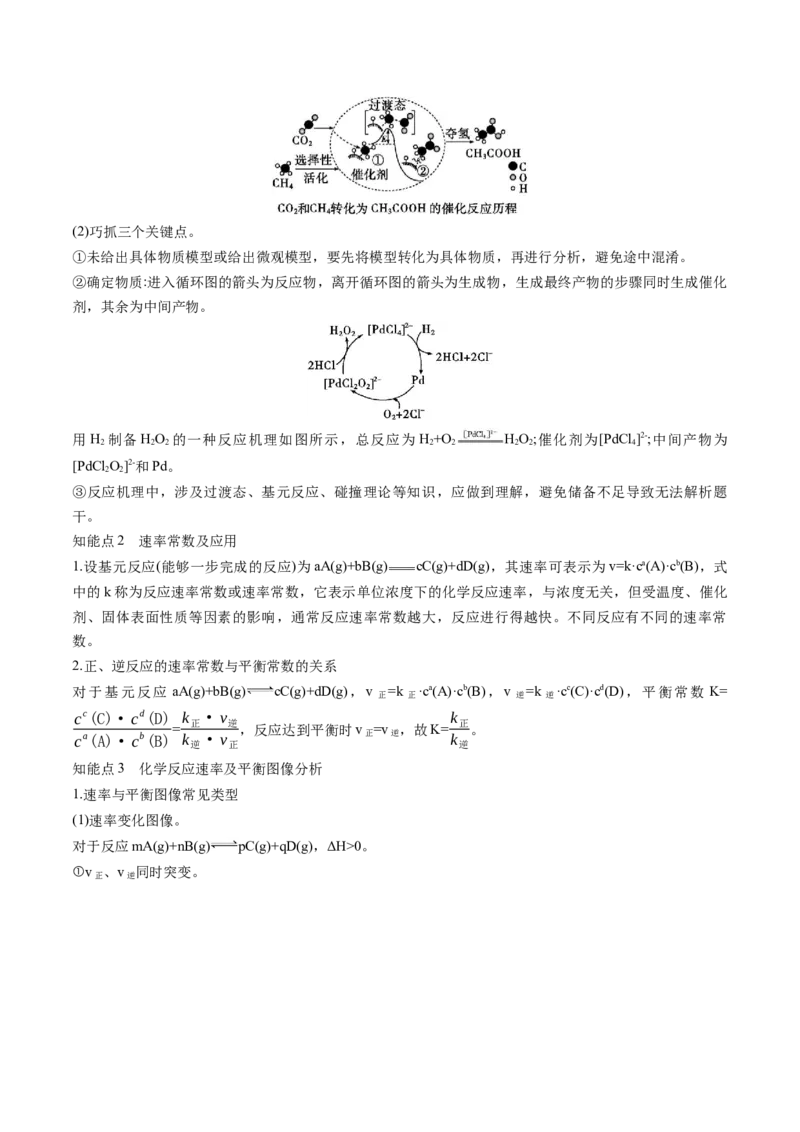
②微观原子模型。(2)巧抓三个关键点。
①未给出具体物质模型或给出微观模型,要先将模型转化为具体物质,再进行分析,避免途中混淆。
②确定物质:进入循环图的箭头为反应物,离开循环图的箭头为生成物,生成最终产物的步骤同时生成催化
剂,其余为中间产物。
用H 制备HO 的一种反应机理如图所示,总反应为 H+O HO;催化剂为[PdCl ]2-;中间产物为
2 2 2 2 2 2 2 4
[PdCl O]2-和Pd。
2 2
③反应机理中,涉及过渡态、基元反应、碰撞理论等知识,应做到理解,避免储备不足导致无法解析题
干。
知能点2 速率常数及应用
1.设基元反应(能够一步完成的反应)为aA(g)+bB(g) cC(g)+dD(g),其速率可表示为v=k·ca(A)·cb(B),式
中的k称为反应速率常数或速率常数,它表示单位浓度下的化学反应速率,与浓度无关,但受温度、催化
剂、固体表面性质等因素的影响,通常反应速率常数越大,反应进行得越快。不同反应有不同的速率常
数。
2.正、逆反应的速率常数与平衡常数的关系
对于基元反应 aA(g)+bB(g) cC(g)+dD(g),v =k ·ca(A)·cb(B),v =k ·cc(C)·cd(D),平衡常数 K=
正 正 逆 逆
cc(C)·cd(D) k ·v k
正 逆 正
= ,反应达到平衡时v =v ,故K= 。
ca(A)·cb(B) k ·v 正 逆 k
逆 正 逆
知能点3 化学反应速率及平衡图像分析
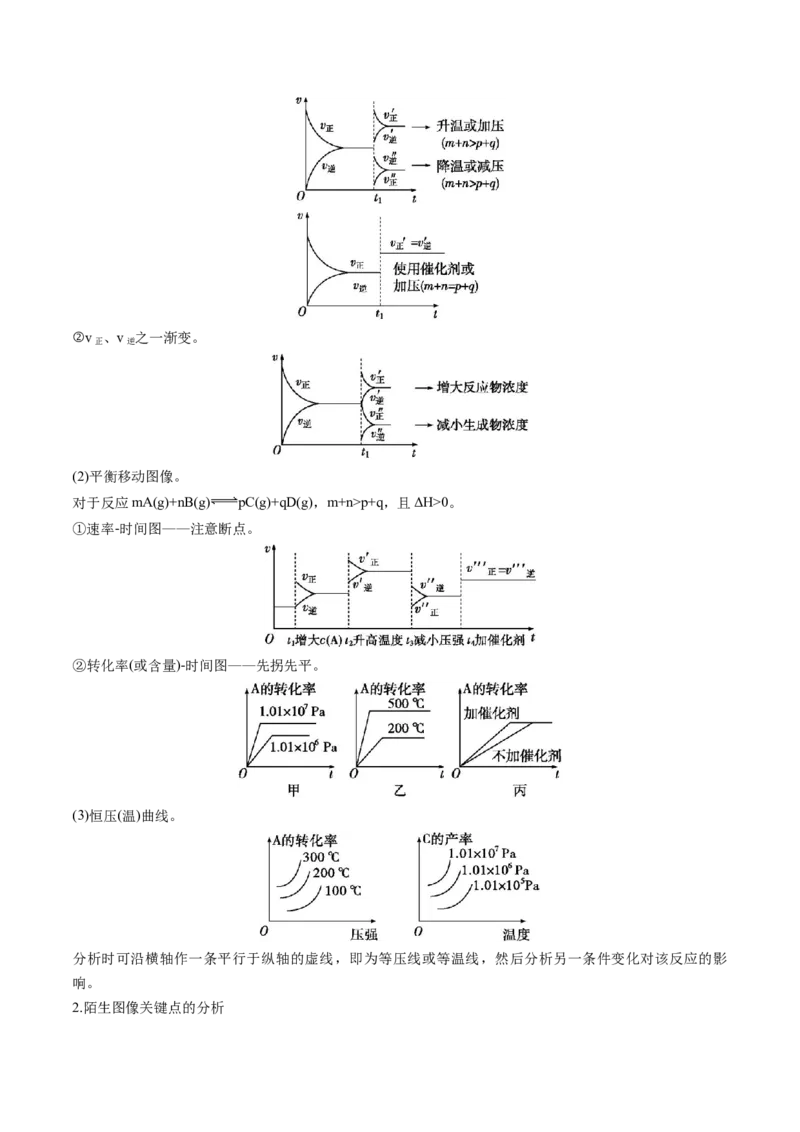
1.速率与平衡图像常见类型
(1)速率变化图像。
对于反应mA(g)+nB(g) pC(g)+qD(g),ΔH>0。
①v 、v 同时突变。
正 逆②v 、v 之一渐变。
正 逆
(2)平衡移动图像。
对于反应mA(g)+nB(g) pC(g)+qD(g),m+n>p+q,且ΔH>0。
①速率-时间图——注意断点。
②转化率(或含量)-时间图——先拐先平。
(3)恒压(温)曲线。
分析时可沿横轴作一条平行于纵轴的虚线,即为等压线或等温线,然后分析另一条件变化对该反应的影
响。
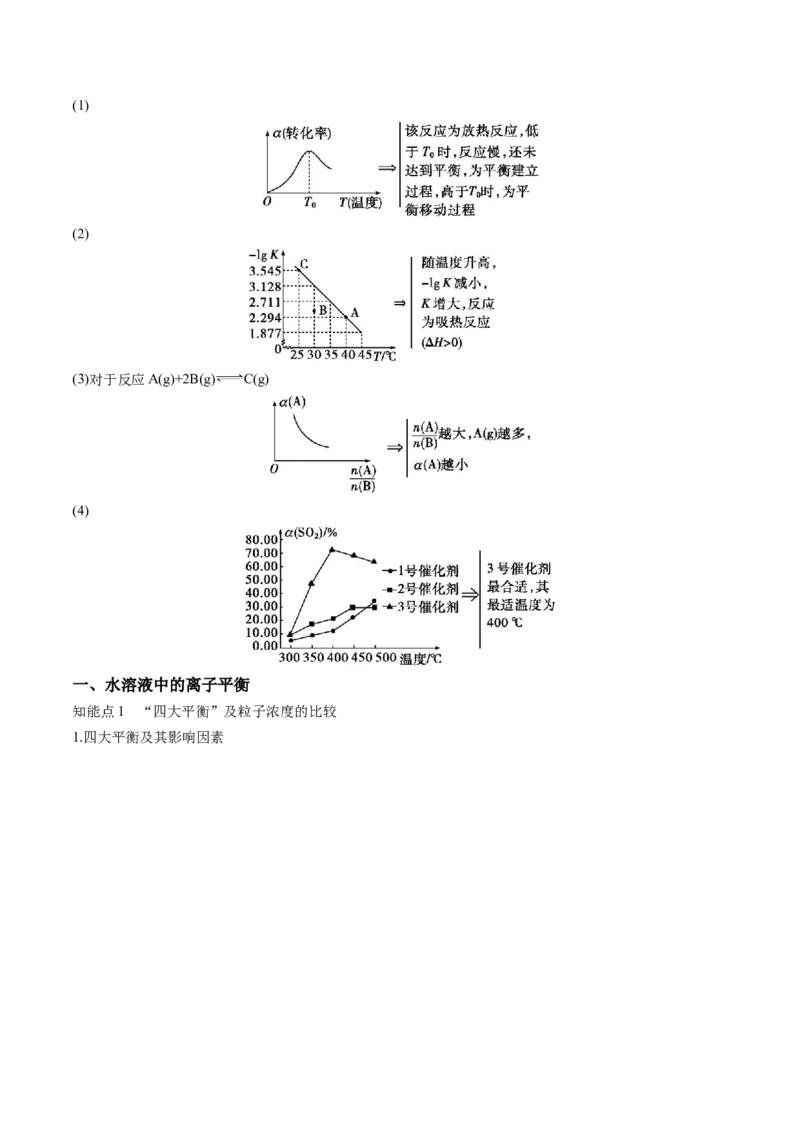
2.陌生图像关键点的分析(1)
(2)
(3)对于反应A(g)+2B(g) C(g)
(4)
一、水溶液中的离子平衡
知能点1 “四大平衡”及粒子浓度的比较
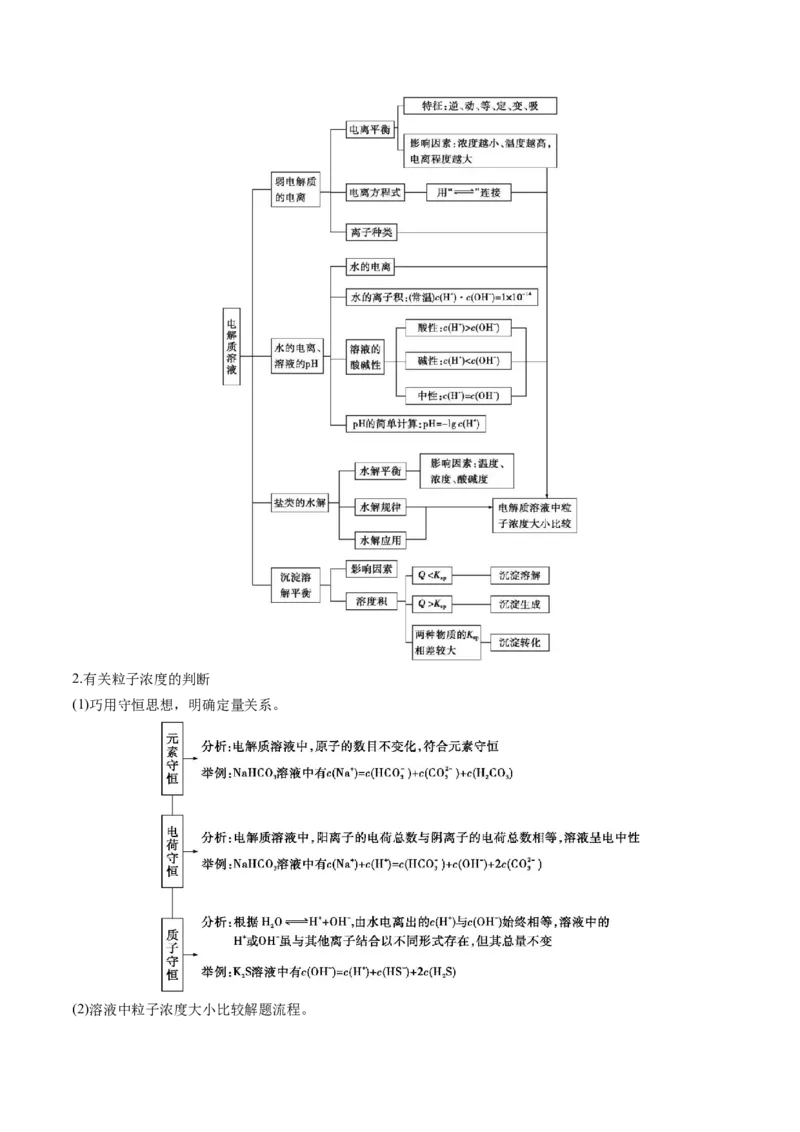
1.四大平衡及其影响因素2.有关粒子浓度的判断
(1)巧用守恒思想,明确定量关系。
(2)溶液中粒子浓度大小比较解题流程。知能点2 K 、K、K、K 、K 之间的关系
w a b sp h
1.平衡常数之间的关系
已知:常温下,HS的电离常数为K 、K ,Cu(OH) 、CuS、Ag S的溶度积常数分别为K 、K ′、K ″。
2 a1 a2 2 2 sp sp sp
(1)水解常数与电离常数、水的离子积之间的关系。
K K
常温下的NaS溶液中,S2-的水解常数K = w ,HS-的水解常数K = w 。
2 h1 K h2 K
a2 a1
(2)水解常数与溶度积、水的离子积之间的关系。
K2
常温下的CuCl 溶液中,Cu2+的水解常数K= w。
2 h
K
sp
(3)平衡常数与电离常数、溶度积之间的关系。
K '
①反应CuS(s)+2Ag+(aq) Cu2+(aq)+Ag S(s)的平衡常数K= sp 。
2 K ″
sp
K '
②反应CuS(s)+2H+(aq) Cu2+(aq)+H S(aq)的平衡常数K= sp 。
2 K ·K
a1 a2
(4)判断溶液的酸碱性。
NaHS溶液呈碱性,离子浓度大小顺序为c(Na+)>c(HS-)>c(OH-)>c(H+)>c(S2-)。
K
上述判断的理由是HS-的水解常数( w )大于其电离常数(K )。
K a2
a1
2.根据图形节点求算弱电解质的电离平衡常数
(1)由图形起点计算平衡常数。
(2)由图形交点计算平衡常数。
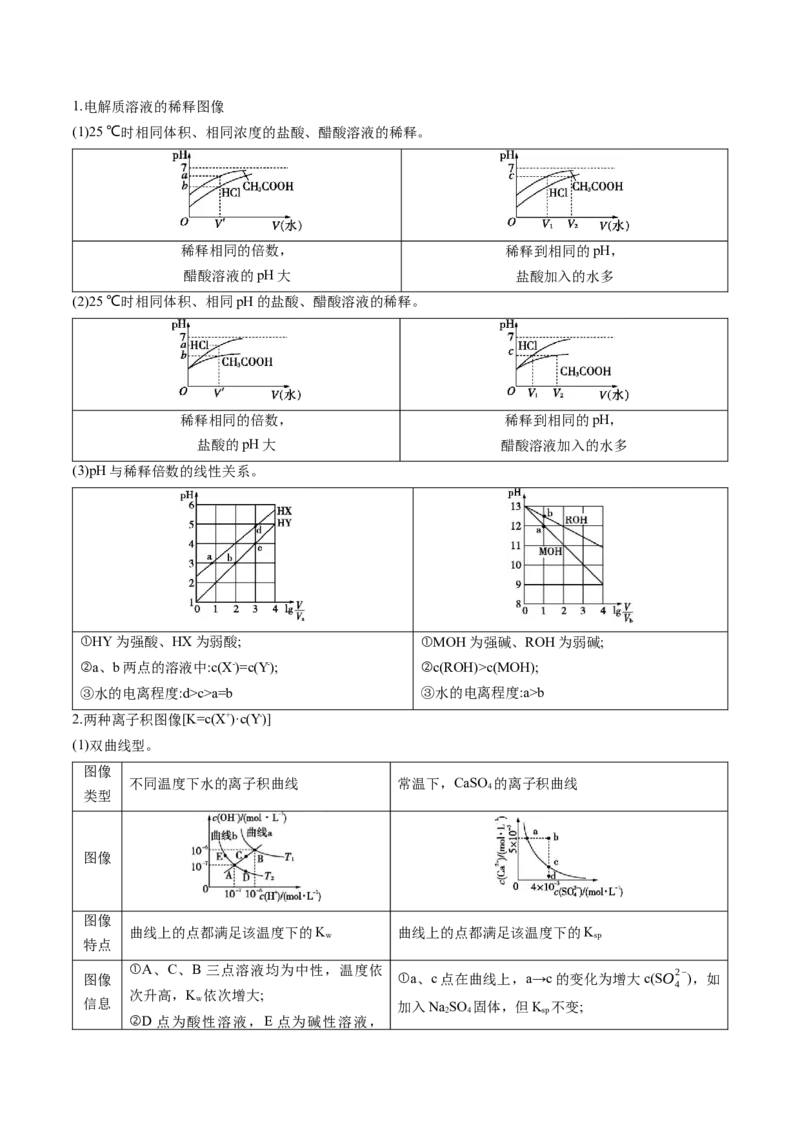
知能点3 电解质溶液图像题的分析1.电解质溶液的稀释图像
(1)25 ℃时相同体积、相同浓度的盐酸、醋酸溶液的稀释。
稀释相同的倍数, 稀释到相同的pH,
醋酸溶液的pH大 盐酸加入的水多
(2)25 ℃时相同体积、相同pH的盐酸、醋酸溶液的稀释。
稀释相同的倍数, 稀释到相同的pH,
盐酸的pH大 醋酸溶液加入的水多
(3)pH与稀释倍数的线性关系。
①HY为强酸、HX为弱酸; ①MOH为强碱、ROH为弱碱;
②a、b两点的溶液中:c(X-)=c(Y-); ②c(ROH)>c(MOH);
③水的电离程度:d>c>a=b ③水的电离程度:a>b
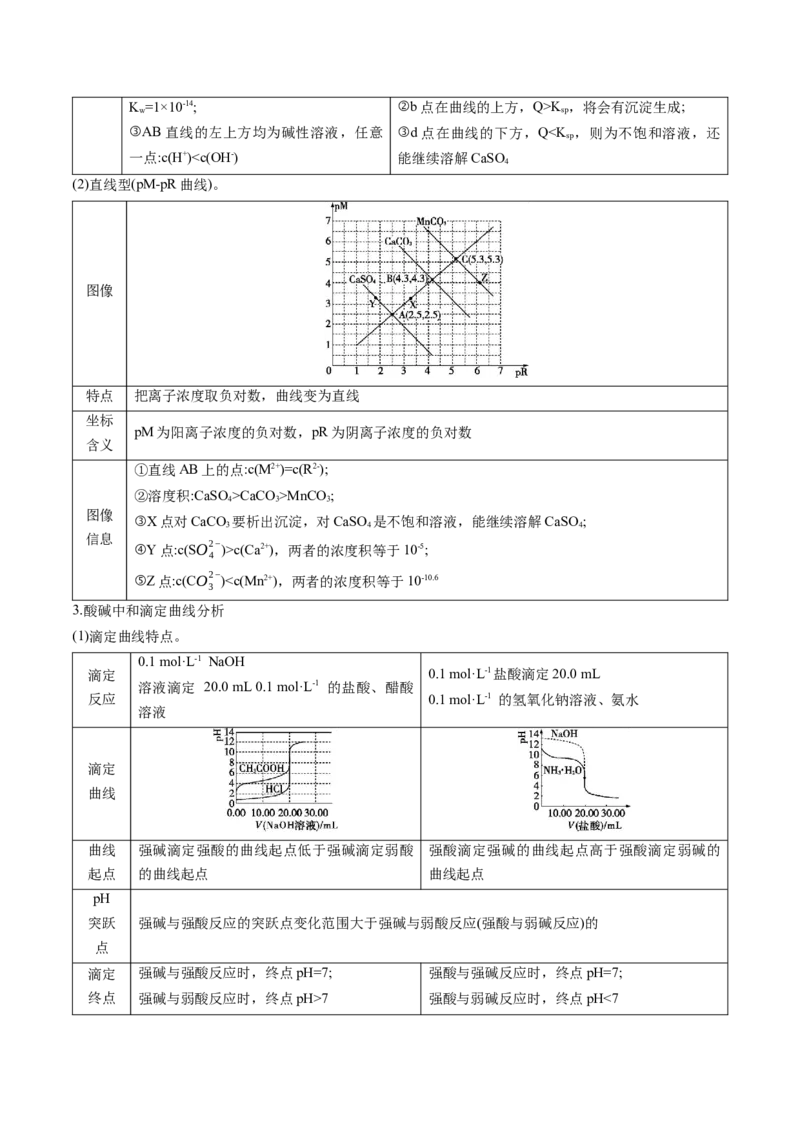
2.两种离子积图像[K=c(X+)·c(Y-)]
(1)双曲线型。
图像
不同温度下水的离子积曲线 常温下,CaSO 的离子积曲线
4
类型
图像
图像
曲线上的点都满足该温度下的K 曲线上的点都满足该温度下的K
w sp
特点
图像
①A、C、B三点溶液均为中性,温度依
①a、c点在曲线上,a→c的变化为增大c(SO2−
),如
4
次升高,K 依次增大;
信息 w 加入NaSO 固体,但K 不变;
2 4 sp
②D 点为酸性溶液,E 点为碱性溶液,K =1×10-14; ②b点在曲线的上方,Q>K ,将会有沉淀生成;
w sp
③AB直线的左上方均为碱性溶液,任意 ③d点在曲线的下方,QCaCO >MnCO;
4 3 3
图像
③X点对CaCO 要析出沉淀,对CaSO 是不饱和溶液,能继续溶解CaSO;
3 4 4
信息
④Y点:c(SO2− )>c(Ca2+),两者的浓度积等于10-5;
4
⑤Z点:c(CO2− )7 强酸与弱碱反应时,终点pH<7的
pH
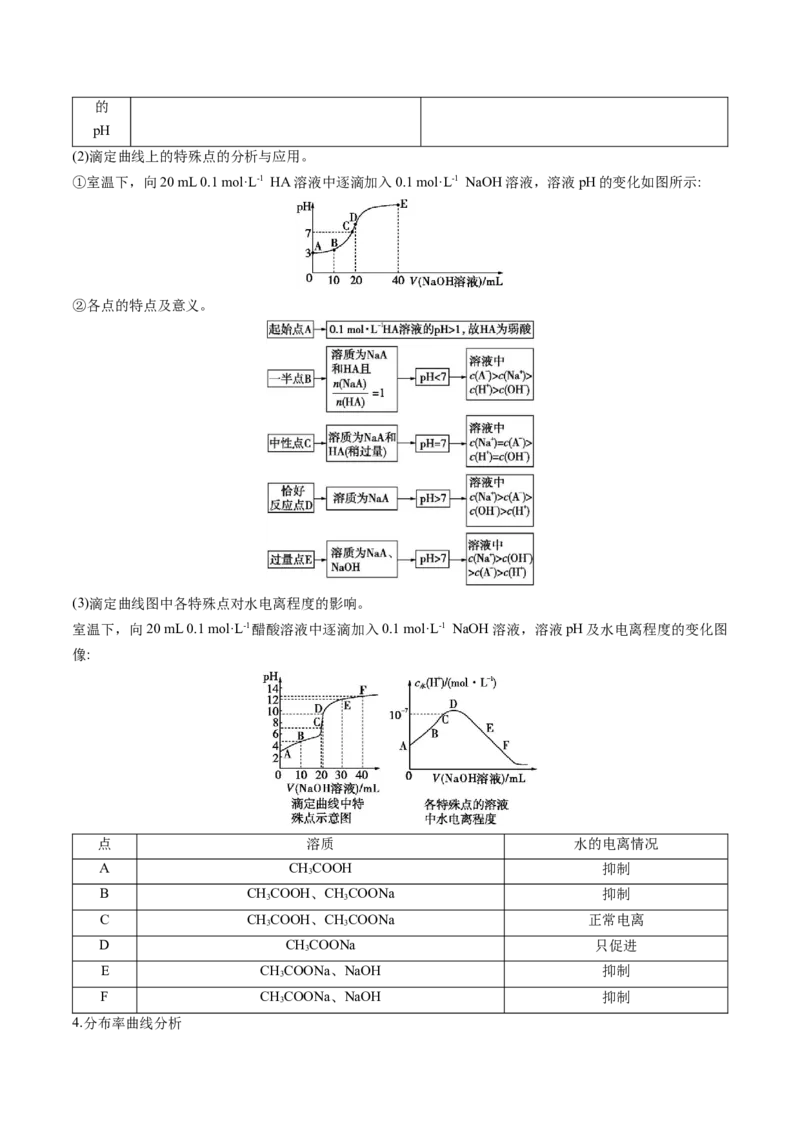
(2)滴定曲线上的特殊点的分析与应用。
①室温下,向20 mL 0.1 mol·L-1 HA溶液中逐滴加入0.1 mol·L-1 NaOH溶液,溶液pH的变化如图所示:
②各点的特点及意义。
(3)滴定曲线图中各特殊点对水电离程度的影响。
室温下,向20 mL 0.1 mol·L-1醋酸溶液中逐滴加入0.1 mol·L-1 NaOH溶液,溶液pH及水电离程度的变化图
像:
点 溶质 水的电离情况
A CHCOOH 抑制
3
B CHCOOH、CHCOONa 抑制
3 3
C CHCOOH、CHCOONa 正常电离
3 3
D CHCOONa 只促进
3
E CHCOONa、NaOH 抑制
3
F CHCOONa、NaOH 抑制
3
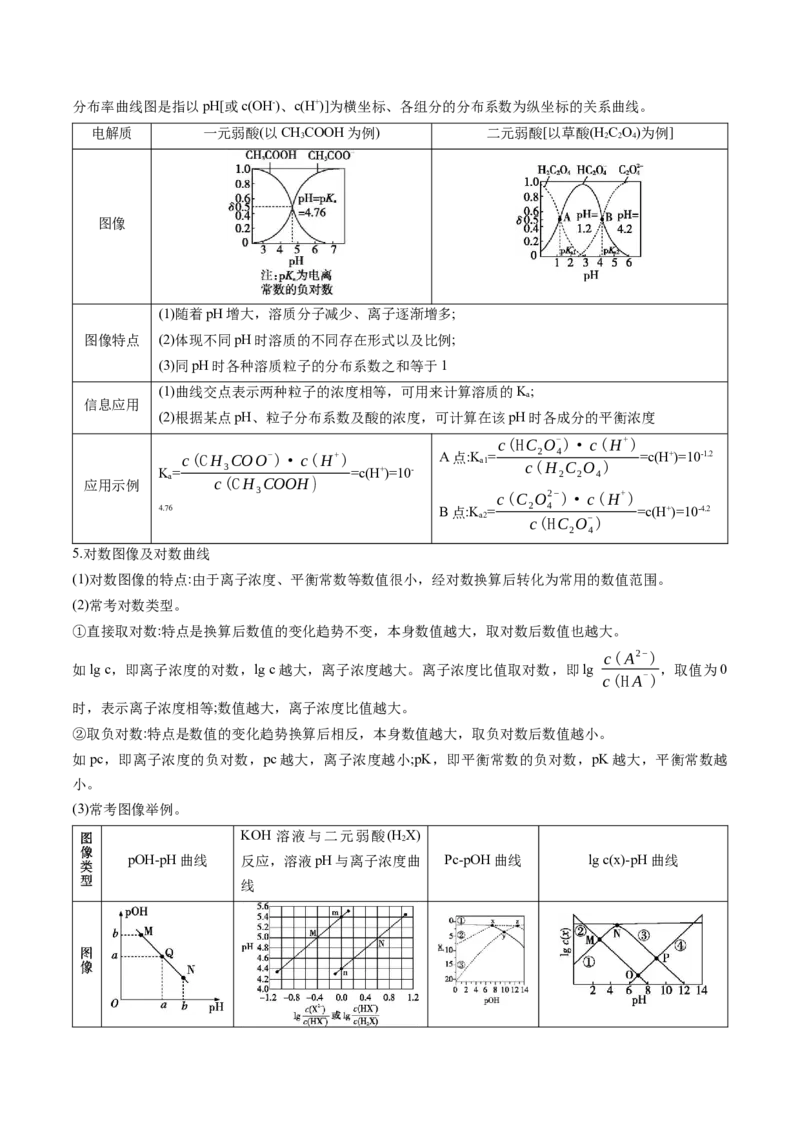
4.分布率曲线分析分布率曲线图是指以pH[或c(OH-)、c(H+)]为横坐标、各组分的分布系数为纵坐标的关系曲线。
电解质 一元弱酸(以CHCOOH为例) 二元弱酸[以草酸(H C O)为例]
3 2 2 4
图像
(1)随着pH增大,溶质分子减少、离子逐渐增多;
图像特点 (2)体现不同pH时溶质的不同存在形式以及比例;
(3)同pH时各种溶质粒子的分布系数之和等于1
(1)曲线交点表示两种粒子的浓度相等,可用来计算溶质的K;
a
信息应用
(2)根据某点pH、粒子分布系数及酸的浓度,可计算在该pH时各成分的平衡浓度
c(HC O-)·c(H+)
应用示例 K a = c(CH c( 3 C C O H O C - O )· OH c( ) H+) =c(H+)=10- A点:K a1 = c( 2 H 4 2 C 2 O 4 ) =c(H+)=10-1.2
3 c(C O2−)·c(H+)
4.76 B点:K = 2 4 =c(H+)=10-4.2
a2 c(HC O-)
2 4
5.对数图像及对数曲线
(1)对数图像的特点:由于离子浓度、平衡常数等数值很小,经对数换算后转化为常用的数值范围。
(2)常考对数类型。
①直接取对数:特点是换算后数值的变化趋势不变,本身数值越大,取对数后数值也越大。
c(A2−)
如lg c,即离子浓度的对数,lg c越大,离子浓度越大。离子浓度比值取对数,即lg ,取值为0
c(HA-)
时,表示离子浓度相等;数值越大,离子浓度比值越大。
②取负对数:特点是数值的变化趋势换算后相反,本身数值越大,取负对数后数值越小。
如pc,即离子浓度的负对数,pc越大,离子浓度越小;pK,即平衡常数的负对数,pK越大,平衡常数越
小。
(3)常考图像举例。
KOH 溶液与二元弱酸(H X)
2
pOH-pH曲线 反应,溶液pH与离子浓度曲 Pc-pOH曲线 lg c(x)-pH曲线
线图 0.1 mol· L-1
表示一元酸与一元
像 HPO 溶液含磷 0.1 mol· L-1 CHCOOH 溶液
3 3 3
碱中和过程中H+与 同pH时,各粒子浓度的大小
特 粒子的 pc-pOH 中各粒子浓度与pH关系
OH-浓度的关系
点 关系
a.三条曲线,三
种粒子,是二
元弱酸;
a.根据各粒子与pH关系可确
① 是
HPO2−
,
3 定:
a.二元弱酸(H 2 X)一级电离程 ② 是 H 2 PO 3 - , ①是lg c(CH 3 COO-),②是lg
a.Q点溶液显中性; 度远大于二级电离程度; ③是H 3 PO 3 ; c(H+),
b.M 点 溶 液 显 酸 b.N代表一级电离的曲线,M b.x 点 c(HPO2− ③是 lg c(CHCOOH),④是
3 3
性,N点溶液显碱 代表二级电离的曲线; )= lg c(OH-);
性,这两点水的电 c. 根 据 n 点 的 坐 标 计 算 c(HPO-
) , 根
b.N 点
2 3
离程度相同 K =10-4.4,根据 m 点的坐标 c(CHCOOH)=c(CH COO-),
a1 据横坐标可计 3 3
计算K =10-5.4 可计算其K;
a2 算K ; a
a2
c.O点c(H+)=c(OH-),
c.z 点
c(HPO-
2 3
溶液显中性
)=c(H PO ),根
3 3
据横坐标可计
算K
a1
考点一 化学反应速率与平衡
1.(2024届广东省省二模)液化石油气的主要成分C H 在光照条件下与Cl 反应,可得到各种氯代丙
3 8 2
烷。已知:
①C H 与Cl 反应的机理为自由基反应,包括以下几步:
3 8 2
Ⅰ.链引发:
Ⅱ.链传递: , ,……
Ⅲ.链终止: , ,……
②丙烷氯代反应中链传递的一步反应能量变化如下。下列说法正确的是
A.将液化石油气灶改用天然气为燃料,若进气口保持不变,则需要调大风门
B.先将Cl 用光照射,然后迅速在黑暗处与C H 混合,可得到氯代丙烷
2 3 8
C.先将Cl 用光照射,然后在黑暗处放置较长时间,再与C H 混合,可得到氯代丙烷
2 3 8
D.断裂—CH 中1 mol C—H比断裂—CH—中1 mol C—H所需能量小
3 2
【答案】B
【解析】A.当将液化石油气灶改用为天然气燃料时,如果进气口保持不变,即燃料气体的流量不变,由
于天然气的的耗氧量低,则可以调节小风门,A错误;
B.在光照条件下,氯气分子会吸收光能并分解成自由基,在黑暗处,已经生成的氯自由基与丙烷反应,
可以生成氯代丙烷,B正确;
C.在黑暗条件下,已经生成的氯自由基会很快失去活性,因为它们无法继续吸收光能来维持链式反应。
因此,即使氯气在光照下已经部分分解,但在黑暗处放置较长时间后,这些自由基的数量会大大减少,甚
至可能几乎不存在,几乎不可能生成氯代丙烷,C错误;
D.键能越大的化学键越稳定,越不容易被断裂。甲基中的C-H键比亚甲基中的C-H键更强,那么断裂甲
基中的C-H键所需的能量应该更大,D错误;
故选B。
2.(2024届广东省深圳一模)常温下,向某溶剂(不参与反应)中加入一定量X、Y和M,所得溶液中
同时存在如下平衡:
(ⅰ)
(ⅱ)
(ⅲ)
X、Y的物质的量浓度 随反应时间 的变化关系如图所示,300 s后反应体系达到平衡状态。
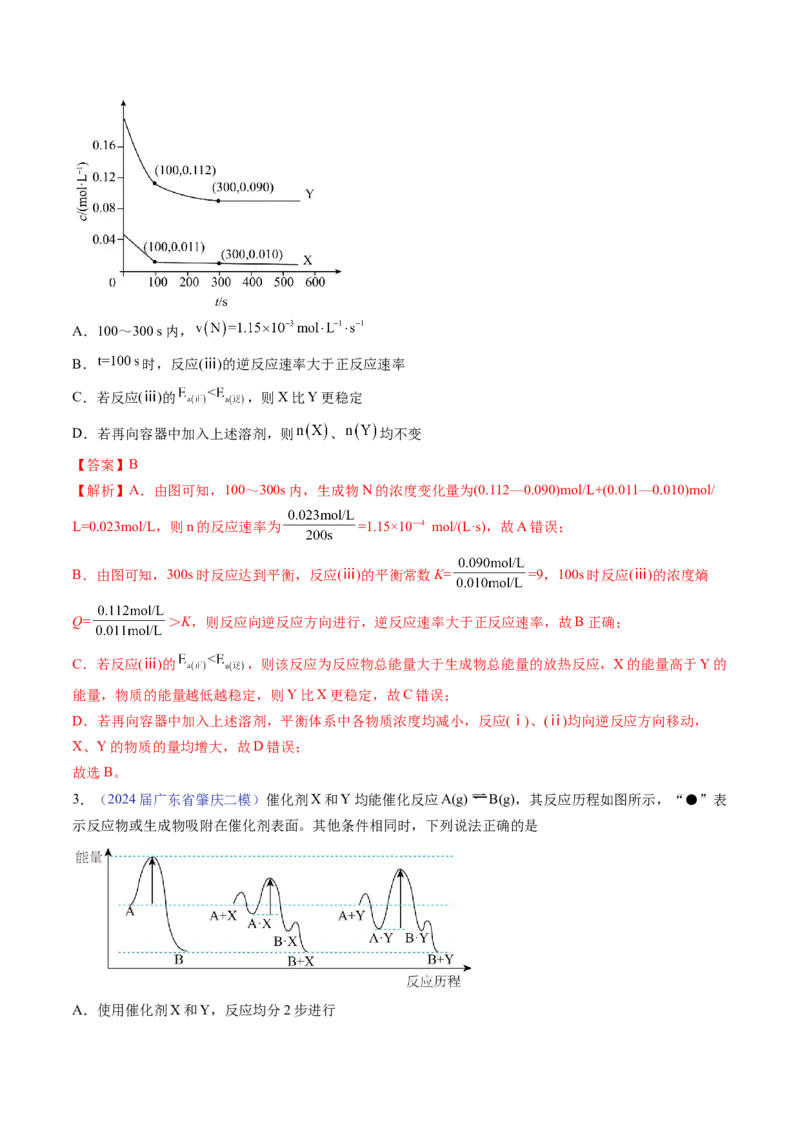
下列说法正确的是A.100~300 s内,
B. 时,反应(ⅲ)的逆反应速率大于正反应速率
C.若反应(ⅲ)的 ,则X比Y更稳定
D.若再向容器中加入上述溶剂,则 、 均不变
【答案】B
【解析】A.由图可知,100~300s内,生成物N的浓度变化量为(0.112—0.090)mol/L+(0.011—0.010)mol/
L=0.023mol/L,则n的反应速率为 =1.15×10—4 mol/(L·s),故A错误;
B.由图可知,300s时反应达到平衡,反应(ⅲ)的平衡常数K= =9,100s时反应(ⅲ)的浓度熵
Q= >K,则反应向逆反应方向进行,逆反应速率大于正反应速率,故B正确;
C.若反应(ⅲ)的 ,则该反应为反应物总能量大于生成物总能量的放热反应,X的能量高于Y的
能量,物质的能量越低越稳定,则Y比X更稳定,故C错误;
D.若再向容器中加入上述溶剂,平衡体系中各物质浓度均减小,反应(ⅰ)、(ⅱ)均向逆反应方向移动,
X、Y的物质的量均增大,故D错误;
故选B。
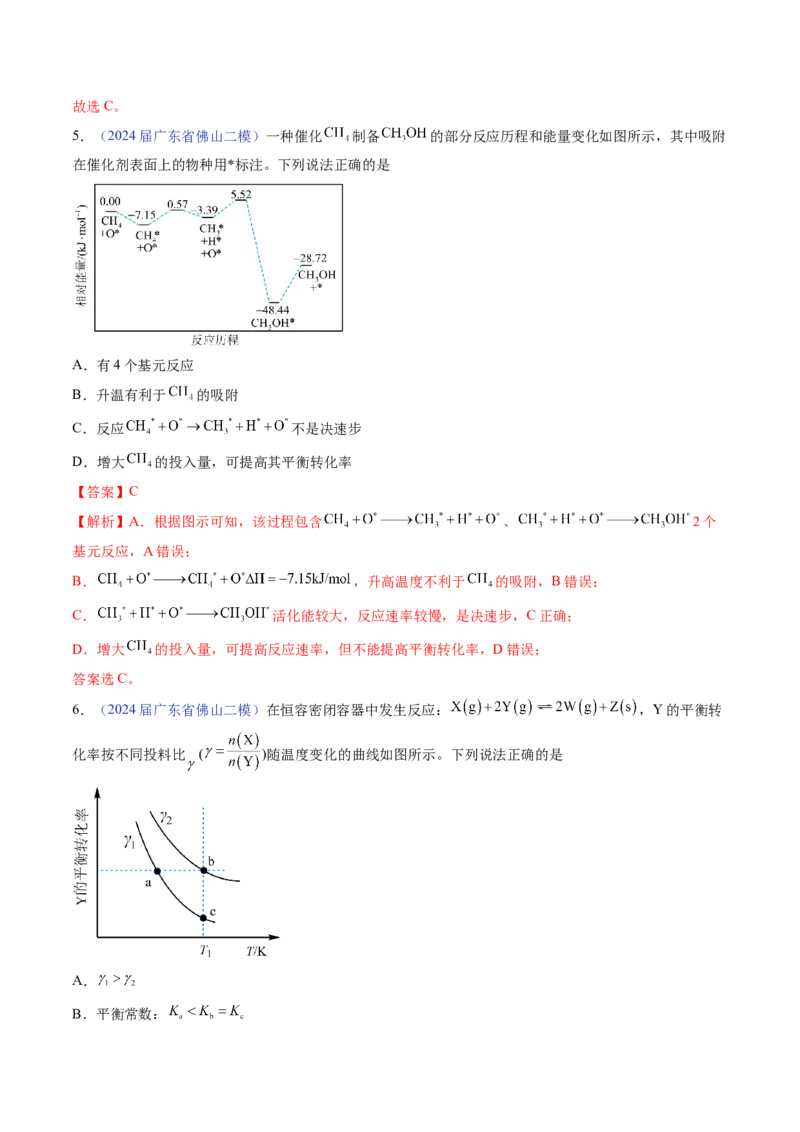
3.(2024届广东省肇庆二模)催化剂X和Y均能催化反应A(g) B(g),其反应历程如图所示,“●”表
示反应物或生成物吸附在催化剂表面。其他条件相同时,下列说法正确的是
A.使用催化剂X和Y,反应均分2步进行B.使用催化剂Y比使用催化剂X,反应更快达到平衡
C.反应达到平衡后,降低温度,B的浓度减小
D.反应过程中A·Y所能达到的最高浓度大于A·X
【答案】D
【解析】A.由图可知两种催化剂均出现3个波峰,所以使用催化剂X和Y,反应历程都分3步进行,A
错误;
B.由图可知,X的最高活化能小于Y的最高活化能,所以使用X时反应速率更快,反应体系更快达到平
衡,B错误;
C.由图可知,该反应是放热反应,所以达平衡时,降低温度平衡向右移动,B的浓度增大,C错误;
D.由图可知,A·X生成B·X的活化能小于A·Y生成B·Y的活化能,则A·Y更难转化为B·Y,故反应过程
中A·Y所能达到的最高浓度大于A·X,D正确;
故选D。
4.(2024届广东省省一模) 下,分别向恒为 的恒温密闭容器甲、恒为 的绝热密闭容器乙中加入
和 ,发生反应 ,两容器中 的转化率随时间的变化如
图所示。下列说法正确的是
A.若 后加入催化剂,则曲线Ⅰ中 的平衡转化率会增大
B.曲线Ⅰ、Ⅱ对应反应的平衡常数:K(Ⅰ))>K(Ⅱ)
C. 点的 大于 点的
D. 内,曲线Ⅱ中 的平均反应速率
【答案】C
【解析】A. 后反应已经达到平衡状态,催化剂不能改变平衡转化率,A项错误;
B.曲线Ⅰ先出现拐点,说明温度更高,反应放热,则曲线Ⅰ是绝热装置乙的曲线,由于反应放热,温度
升高平衡逆向移动,K(Ⅰ)小于K(Ⅱ),B项错误;
C. 两点转化率相同,则两者浓度相同,两点都向正反应方向进行,则 都大于 ,a点温度更高,
则 点的 大于 点的 大于 点的 ,C项正确;
D. 内,曲线Ⅱ的转化率为 , 转化的浓度均为 ,
,D项错误;故选C。
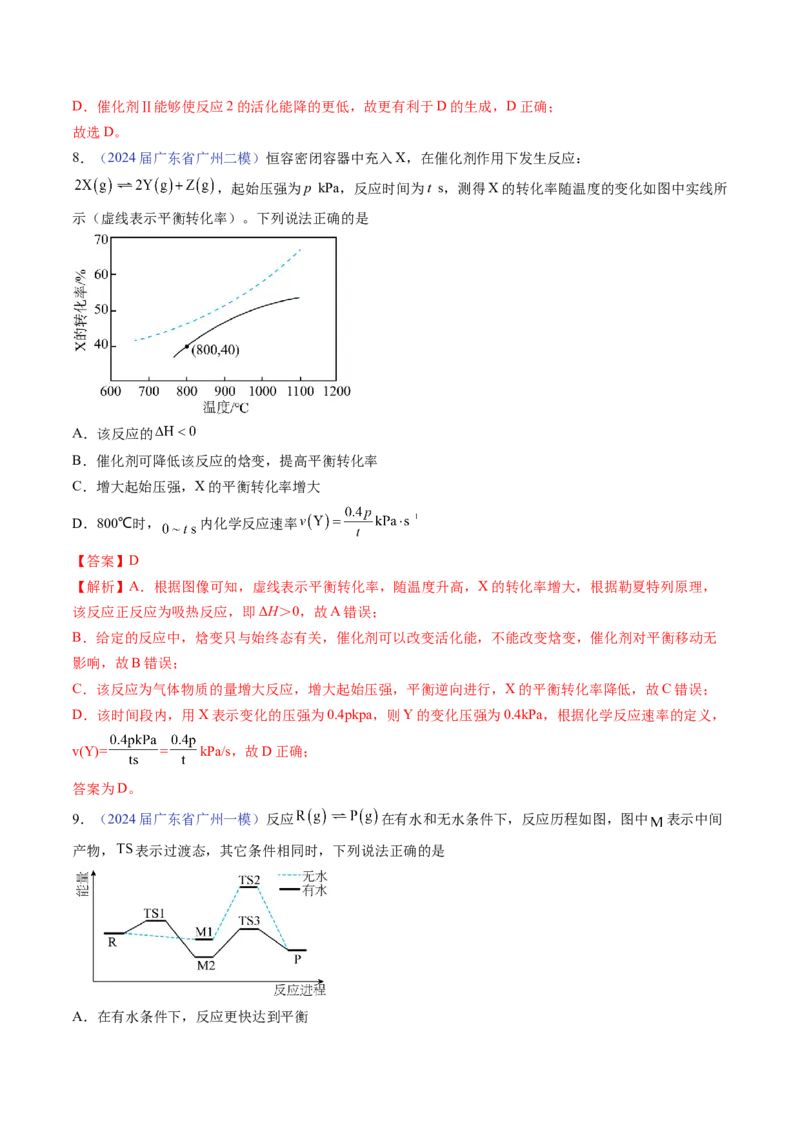
5.(2024届广东省佛山二模)一种催化 制备 的部分反应历程和能量变化如图所示,其中吸附
在催化剂表面上的物种用*标注。下列说法正确的是
A.有4个基元反应
B.升温有利于 的吸附
C.反应 不是决速步
D.增大 的投入量,可提高其平衡转化率
【答案】C
【解析】A.根据图示可知,该过程包含 、 2个
基元反应,A错误;
B. ,升高温度不利于 的吸附,B错误;
C. 活化能较大,反应速率较慢,是决速步,C正确;
D.增大 的投入量,可提高反应速率,但不能提高平衡转化率,D错误;
答案选C。
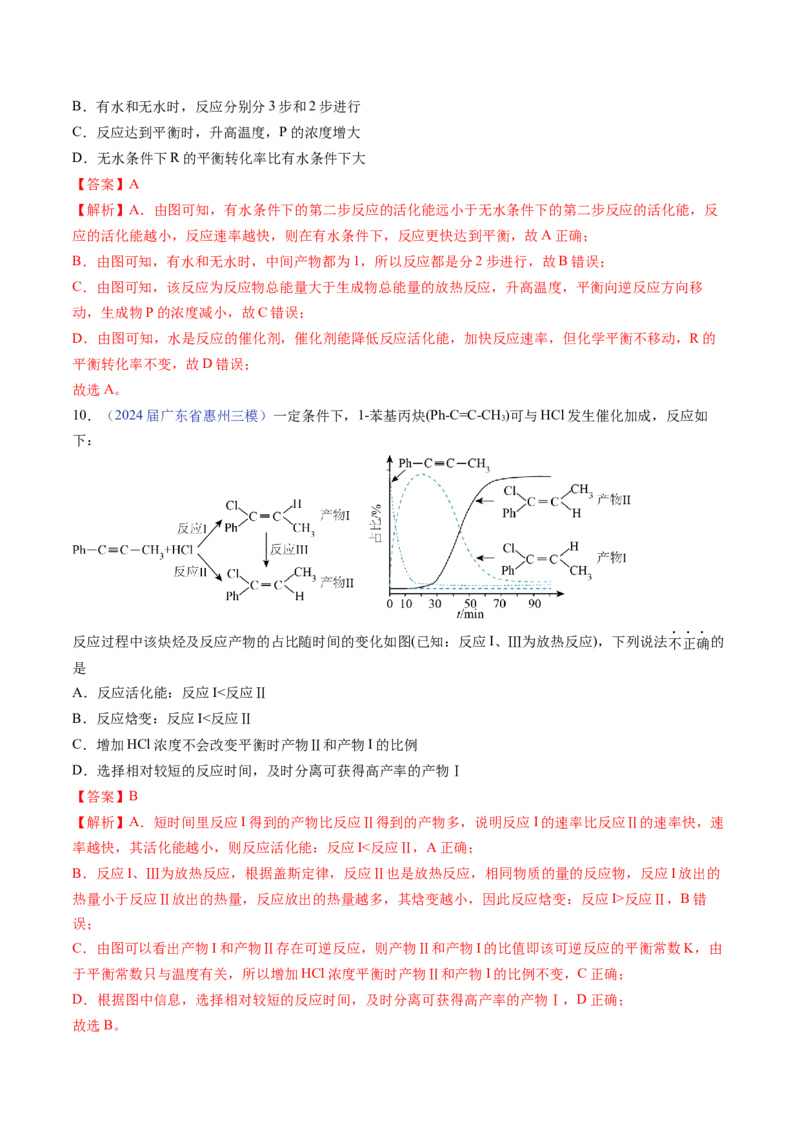
6.(2024届广东省佛山二模)在恒容密闭容器中发生反应: ,Y的平衡转
化率按不同投料比 ( )随温度变化的曲线如图所示。下列说法正确的是
A.
B.平衡常数:C.当容器内气体密度不变时,反应达到平衡
D. 温度下增大压强,c点向a点方向移动
【答案】C
【分析】由题图可知,投料比不变时,随温度的升高Y的平衡转化率减小,平衡逆向移动,所以该反应正
向为放热反应;在相同的温度下,投料比增大,相当于在Y的投料量不变的情况下增大X的投料量,当反
应物不止一种时,其他条件不变,增大其中一种气态反应物的投料量会增大其他反应物的平衡转化率,同
时降低自身平衡转化率,故投料比越大,Y的平衡转化率越大。
【解析】A.由题图可知,温度相同时,γ 对应曲线的Y的转化率大于γ 对应曲线的Y的转化率,故
2 1
γ>γ ,A错误;
2 1
B.该反应正向为放热反应,温度越高,K越小,故K>K =K,B错误;
a b c
C.由于产物之一为固体,容器恒容,若反应未平衡,气体总质量会改变,气体密度会改变,故当容器内
气体密度不变时,反应达到平衡,C正确;
D.正向反应气体体积数减小,温度一定,增大压强,平衡逆向移动,Y的转化率不会升高,D错误;
本题选C。
7.(2024届广东省佛山一模)密闭容器中,发生 和
两个竞争反应,反应历程如图所示.下列说法正确的是
A.增大压强,物质C的浓度不变
B.升高温度,平衡时体系内D的浓度增大
C.反应
D.加入催化剂Ⅱ更有利于D的生成
【答案】D
【解析】
A.反应2为气体体积减小的反应,增大压强会使反应朝正向进行,导致 A和B的浓度减小,从而导致反
应1朝逆向进行,导致C的浓度减小,A错误;
B.根据反应历程可知,反应2为放热反应,反应1为吸热反应,升高温度会使反应2向逆向进行,使反应
1向正向进行,最终会导致D的浓度减小,B错误;
C.根据盖斯定律可得: ,C错误;D.催化剂Ⅱ能够使反应2的活化能降的更低,故更有利于D的生成,D正确;
故选D。
8.(2024届广东省广州二模)恒容密闭容器中充入X,在催化剂作用下发生反应:
,起始压强为p kPa,反应时间为t s,测得X的转化率随温度的变化如图中实线所
示(虚线表示平衡转化率)。下列说法正确的是
A.该反应的
B.催化剂可降低该反应的焓变,提高平衡转化率
C.增大起始压强,X的平衡转化率增大
D.800℃时, 内化学反应速率
【答案】D
【解析】A.根据图像可知,虚线表示平衡转化率,随温度升高,X的转化率增大,根据勒夏特列原理,
该反应正反应为吸热反应,即ΔH>0,故A错误;
B.给定的反应中,焓变只与始终态有关,催化剂可以改变活化能,不能改变焓变,催化剂对平衡移动无
影响,故B错误;
C.该反应为气体物质的量增大反应,增大起始压强,平衡逆向进行,X的平衡转化率降低,故C错误;
D.该时间段内,用X表示变化的压强为0.4pkpa,则Y的变化压强为0.4kPa,根据化学反应速率的定义,
v(Y)= = kPa/s,故D正确;
答案为D。
9.(2024届广东省广州一模)反应 在有水和无水条件下,反应历程如图,图中 表示中间
产物, 表示过渡态,其它条件相同时,下列说法正确的是
A.在有水条件下,反应更快达到平衡B.有水和无水时,反应分别分3步和2步进行
C.反应达到平衡时,升高温度,P的浓度增大
D.无水条件下R的平衡转化率比有水条件下大
【答案】A
【解析】A.由图可知,有水条件下的第二步反应的活化能远小于无水条件下的第二步反应的活化能,反
应的活化能越小,反应速率越快,则在有水条件下,反应更快达到平衡,故A正确;
B.由图可知,有水和无水时,中间产物都为1,所以反应都是分2步进行,故B错误;
C.由图可知,该反应为反应物总能量大于生成物总能量的放热反应,升高温度,平衡向逆反应方向移
动,生成物P的浓度减小,故C错误;
D.由图可知,水是反应的催化剂,催化剂能降低反应活化能,加快反应速率,但化学平衡不移动,R的
平衡转化率不变,故D错误;
故选A。
10.(2024届广东省惠州三模)一定条件下,1-苯基丙炔(Ph-C=C-CH )可与HCl发生催化加成,反应如
3
下:
反应过程中该炔烃及反应产物的占比随时间的变化如图(已知:反应I、Ⅲ为放热反应),下列说法不正确的
是
A.反应活化能:反应I<反应Ⅱ
B.反应焓变:反应I<反应Ⅱ
C.增加HCl浓度不会改变平衡时产物Ⅱ和产物I的比例
D.选择相对较短的反应时间,及时分离可获得高产率的产物Ⅰ
【答案】B
【解析】A.短时间里反应I得到的产物比反应Ⅱ得到的产物多,说明反应I的速率比反应Ⅱ的速率快,速
率越快,其活化能越小,则反应活化能:反应I<反应Ⅱ,A正确;
B.反应I、Ⅲ为放热反应,根据盖斯定律,反应Ⅱ也是放热反应,相同物质的量的反应物,反应I放出的
热量小于反应Ⅱ放出的热量,反应放出的热量越多,其焓变越小,因此反应焓变:反应I>反应Ⅱ,B错
误;
C.由图可以看出产物I和产物Ⅱ存在可逆反应,则产物Ⅱ和产物I的比值即该可逆反应的平衡常数K,由
于平衡常数只与温度有关,所以增加HCl浓度平衡时产物Ⅱ和产物I的比例不变,C正确;
D.根据图中信息,选择相对较短的反应时间,及时分离可获得高产率的产物Ⅰ,D正确;
故选B。11.(2024届广东省江门一模)标准状态下,反应 的历程示意图如下。下列说法
不正确的是
A. B.历程Ⅱ中Cl是催化剂
C.历程Ⅰ的活化能为 D.相同条件下, 的平衡转化率:历程Ⅱ>历程Ⅰ
【答案】D
【解析】A.由图可知,Cl原子是历程Ⅱ的催化剂,催化剂不能改变反应的反应热,则历程Ⅰ、Ⅱ的反应
热相等,即 H= ,故A正确;
B.由图可知△,Cl原子在历程Ⅱ中反应前后均有,因此作为催化剂,故B正确;
C.从反应物的起始到最高点的过渡态为活化能,因此历程Ⅰ的活化能为 ,故C正确;
D.催化剂不能改变反应的始态和终态,不能改变反应物的平衡转化率,即相同条件下O 的平衡转化率:
3
历程Ⅱ=历程Ⅰ,故D错误;
故答案选D。
12.(2024届广东省茂名二模)我国科研人员探究了不同催化剂电化学催化 生产HCOOH的催化性
能,反应机理如图所示。下列说法不正确的是
A.使用三种催化剂,反应历程都分4步进行
B.该反应过程仅涉及 键的断裂与形成
C.相同条件下,HCOOH(l)比 (g)稳定
D.相同条件下,使用催化剂In(101)时,反应过程中*OCHO所能达到的最高浓度更大
【答案】B
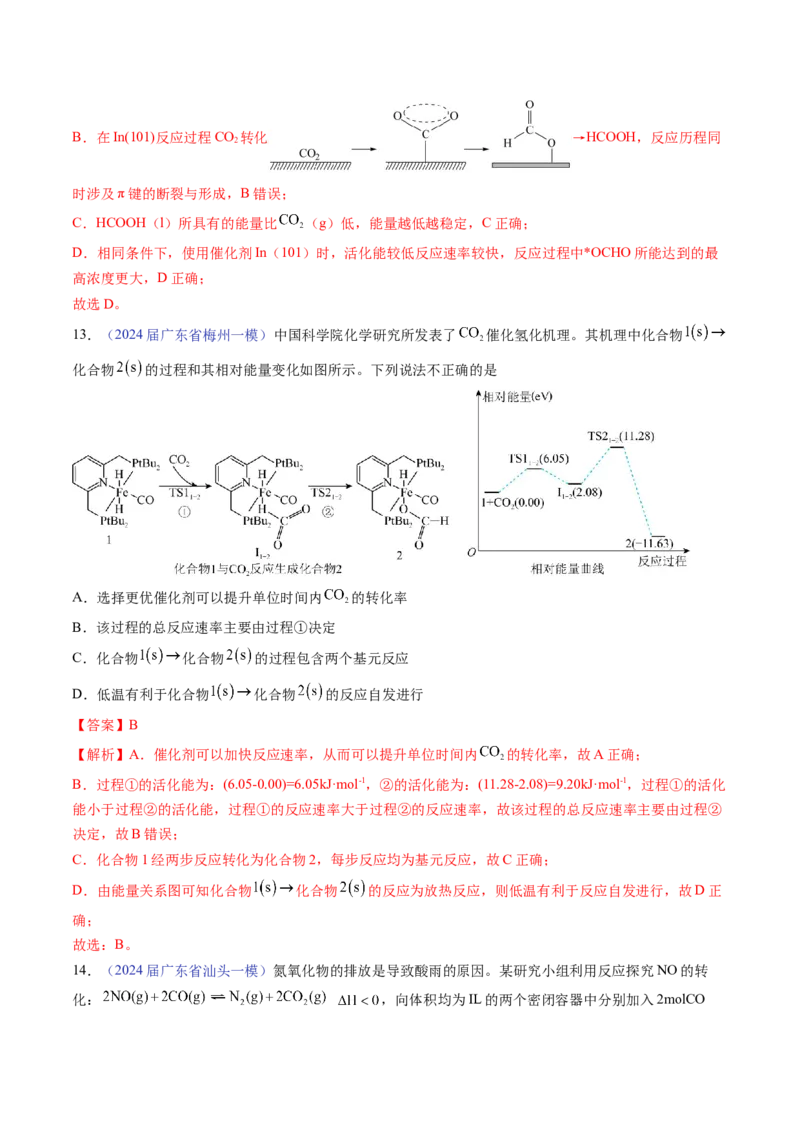
【解析】A.使用三种催化剂,反应历程中4次活化能的改变,反应历程都分4步进行 ,A正确;B.在In(101)反应过程CO 转化 →HCOOH,反应历程同
2
时涉及π键的断裂与形成,B错误;
C.HCOOH(l)所具有的能量比 (g)低,能量越低越稳定,C正确;
D.相同条件下,使用催化剂In(101)时,活化能较低反应速率较快,反应过程中*OCHO所能达到的最
高浓度更大,D正确;
故选D。
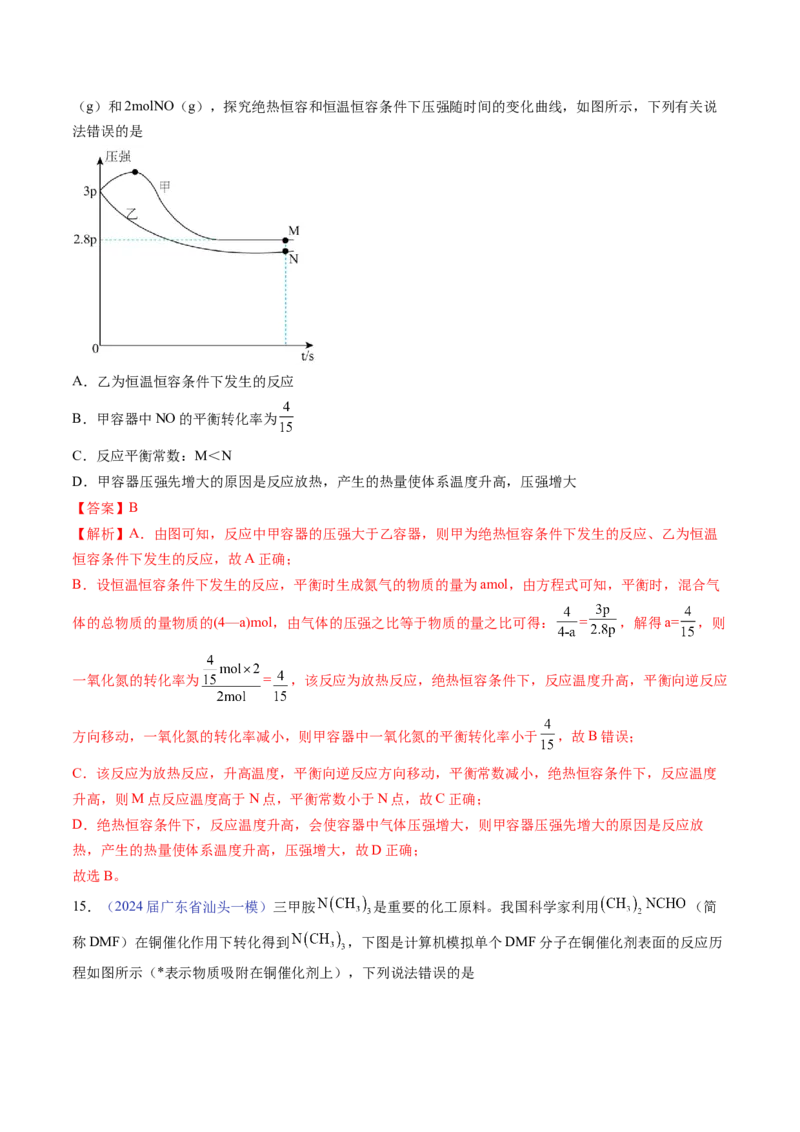
13.(2024届广东省梅州一模)中国科学院化学研究所发表了 催化氢化机理。其机理中化合物
化合物 的过程和其相对能量变化如图所示。下列说法不正确的是
A.选择更优催化剂可以提升单位时间内 的转化率
B.该过程的总反应速率主要由过程①决定
C.化合物 化合物 的过程包含两个基元反应
D.低温有利于化合物 化合物 的反应自发进行
【答案】B
【解析】A.催化剂可以加快反应速率,从而可以提升单位时间内 的转化率,故A正确;
B.过程①的活化能为:(6.05-0.00)=6.05kJ·mol-1,②的活化能为:(11.28-2.08)=9.20kJ·mol-1,过程①的活化
能小于过程②的活化能,过程①的反应速率大于过程②的反应速率,故该过程的总反应速率主要由过程②
决定,故B错误;
C.化合物1经两步反应转化为化合物2,每步反应均为基元反应,故C正确;
D.由能量关系图可知化合物 化合物 的反应为放热反应,则低温有利于反应自发进行,故D正
确;
故选:B。
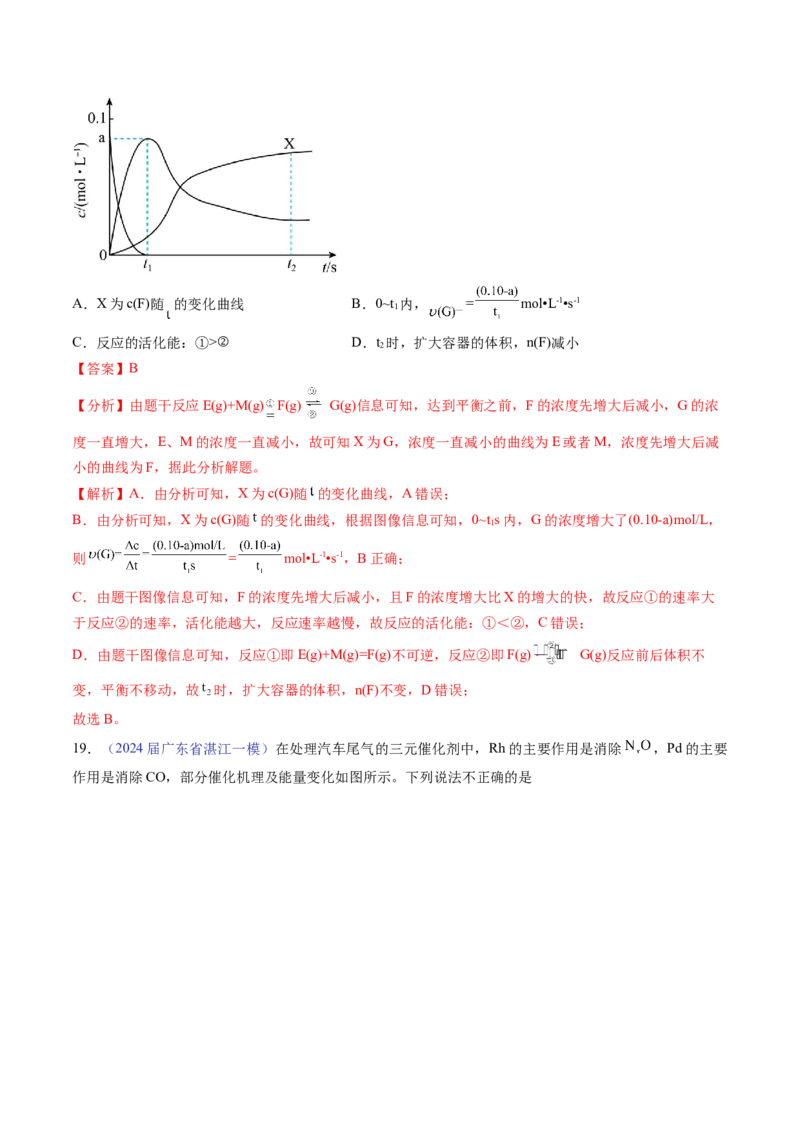
14.(2024届广东省汕头一模)氮氧化物的排放是导致酸雨的原因。某研究小组利用反应探究NO的转
化: ,向体积均为IL的两个密闭容器中分别加入2molCO(g)和2molNO(g),探究绝热恒容和恒温恒容条件下压强随时间的变化曲线,如图所示,下列有关说
法错误的是
A.乙为恒温恒容条件下发生的反应
B.甲容器中NO的平衡转化率为
C.反应平衡常数:M<N
D.甲容器压强先增大的原因是反应放热,产生的热量使体系温度升高,压强增大
【答案】B
【解析】A.由图可知,反应中甲容器的压强大于乙容器,则甲为绝热恒容条件下发生的反应、乙为恒温
恒容条件下发生的反应,故A正确;
B.设恒温恒容条件下发生的反应,平衡时生成氮气的物质的量为amol,由方程式可知,平衡时,混合气
体的总物质的量物质的(4—a)mol,由气体的压强之比等于物质的量之比可得: = ,解得a= ,则
一氧化氮的转化率为 = ,该反应为放热反应,绝热恒容条件下,反应温度升高,平衡向逆反应
方向移动,一氧化氮的转化率减小,则甲容器中一氧化氮的平衡转化率小于 ,故B错误;
C.该反应为放热反应,升高温度,平衡向逆反应方向移动,平衡常数减小,绝热恒容条件下,反应温度
升高,则M点反应温度高于N点,平衡常数小于N点,故C正确;
D.绝热恒容条件下,反应温度升高,会使容器中气体压强增大,则甲容器压强先增大的原因是反应放
热,产生的热量使体系温度升高,压强增大,故D正确;
故选B。
15.(2024届广东省汕头一模)三甲胺 是重要的化工原料。我国科学家利用 (简
称DMF)在铜催化作用下转化得到 ,下图是计算机模拟单个DMF分子在铜催化剂表面的反应历
程如图所示(*表示物质吸附在铜催化剂上),下列说法错误的是A.该反应为放热反应,降温可提高DMF的平衡转化率
B.该历程包含6个基元反应,最大能垒(活化能)为1.19eV
C.设法提高 的速率可以提高总反应速率
D.若1molDMF完全转化为三甲胺,则会吸收1.02eV·N 的能量
A
【答案】D
【解析】A.由图可知,该反应为反应物总能量高于生成物总能量的放热反应,降低温度,平衡向正反应
方向移动,DMF的平衡转化率增大,故A正确;
B.由图可知,该历程包含6个基元反应,最大能垒(活化能)为1.19eV,故B正确;
C.反应的活化能越大,反应速率越慢,总反应的速率取决于慢反应,由图可知,最大能垒(活化能)为
1.19eV,反应的方程式为 ,故C正确;
D.由反应物和生成物的相对能量可知,反应放热为0eV-(-1.02eV)=1.02eV,1molDMF完全转化为三甲
胺,则会释放出1.02eV·N 的能量,故D错误;
A
故选D。
16.(2024届广东省韶关一模)我国科研人员提出了由CO 和CH 转化为高附加值产品CHCOOH的催化
2 4 3
反应历程,该历程示意图如图所示。下列说法不正确的是
A.生成CHCOOH总反应的原子利用率为 100%
3
B.反应过程中有极性共价键的断裂和非极性共价键的形成
C.① ②收能量并形成了C-C键
D.该催化剂可有效降低活化能,提高反应速率
【答案】C
【解析】A.CO 和CH 反应生成CHCOOH的化学方程式为:CO+CH →CHCOOH,该反应的原子利用
2 4 3 2 4 3率为100%,A正确;
B.整个反应中,有极性共价键的断裂和非极性共价键的形成,B正确;
C.①→②的反应中,能量升高,吸收能量,但过渡态并没有真正形成化学键,C错误;
D.该催化剂可有效降低活化能,提高反应速率,D正确;
故选C。
17.(2024届广东省深圳二模)基元反应过渡态理论认为,基元反应在从反应物到产物的变化过程中要经
历一个中间状态,这个状态称为过渡态 。某反应在催化剂作用下的反应进程如图所示,下列说法正确
的是
A.步骤ii→iii为决速步
B.使用催化剂降低了反应的焓变
C.基于上述理论,该反应进程中包含四步基元反应
D.升高温度,反应物分子中活化分子的百分数不变
【答案】A
【解析】A.步骤ii→iii的活化能最大,反应速率最慢,所以步骤ii→iii为决速步,A正确;
B.使用催化剂降低了反应的活化能,不能改变反应的焓变,B错误;
C.基元反应在从反应物到产物的变化过程中要经历一个中间状态,这个状态称为过渡态,该反应进程共
有2个过渡态,所有有2个基元反应,C错误;
D.升高温度,反应物分子中活化分子的百分数增加,D错误;
故选A。
18.(2024届广东省深圳二模)一定温度下,向恒容密闭容器中投入E和M发生如下反应:E(g)+M(g)
F(g) G(g)。已知反应初始c(E)=c (M)=0.10mol/L,部分物质的浓度(c)随时间(t)的变化关系如图所示,
0 0
t 后反应体系达到平衡状态。下列说法正确的是
2A.X为c(F)随 的变化曲线 B.0~t 内, = mol•L-1•s-1
1
C.反应的活化能:①>② D.t 时,扩大容器的体积,n(F)减小
2
【答案】B
【分析】由题干反应E(g)+M(g) F(g) G(g)信息可知,达到平衡之前,F的浓度先增大后减小,G的浓
度一直增大,E、M的浓度一直减小,故可知X为G,浓度一直减小的曲线为E或者M,浓度先增大后减
小的曲线为F,据此分析解题。
【解析】A.由分析可知,X为c(G)随 的变化曲线,A错误;
B.由分析可知,X为c(G)随 的变化曲线,根据图像信息可知,0~ts内,G的浓度增大了(0.10-a)mol/L,
1
则 = mol•L-1•s-1,B正确;
C.由题干图像信息可知,F的浓度先增大后减小,且F的浓度增大比X的增大的快,故反应①的速率大
于反应②的速率,活化能越大,反应速率越慢,故反应的活化能:①<②,C错误;
D.由题干图像信息可知,反应①即E(g)+M(g)=F(g)不可逆,反应②即F(g) G(g)反应前后体积不
变,平衡不移动,故 时,扩大容器的体积,n(F)不变,D错误;
故选B。
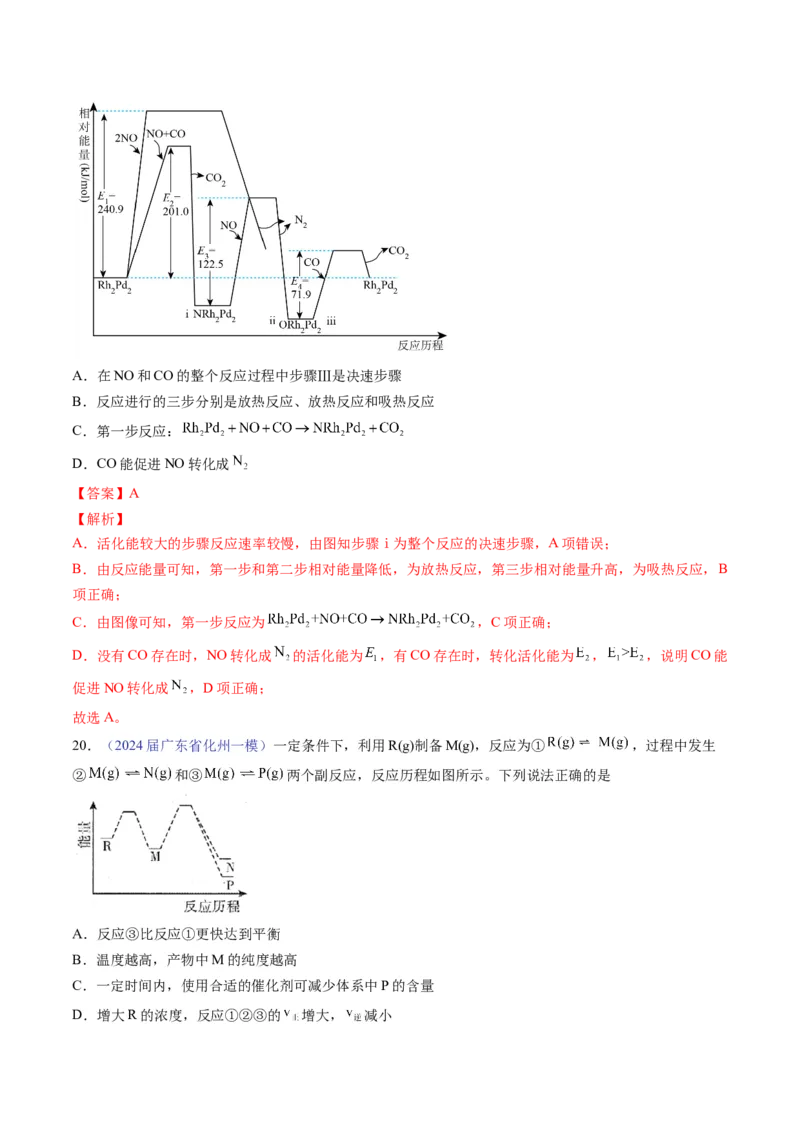
19.(2024届广东省湛江一模)在处理汽车尾气的三元催化剂中,Rh的主要作用是消除 ,Pd的主要
作用是消除CO,部分催化机理及能量变化如图所示。下列说法不正确的是A.在NO和CO的整个反应过程中步骤Ⅲ是决速步骤
B.反应进行的三步分别是放热反应、放热反应和吸热反应
C.第一步反应:
D.CO能促进NO转化成
【答案】A
【解析】
A.活化能较大的步骤反应速率较慢,由图知步骤ⅰ为整个反应的决速步骤,A项错误;
B.由反应能量可知,第一步和第二步相对能量降低,为放热反应,第三步相对能量升高,为吸热反应,B
项正确;
C.由图像可知,第一步反应为 ,C项正确;
D.没有CO存在时,NO转化成 的活化能为 ,有CO存在时,转化活化能为 , ,说明CO能
促进NO转化成 ,D项正确;
故选A。
20.(2024届广东省化州一模)一定条件下,利用R(g)制备M(g),反应为① ,过程中发生
② 和③ 两个副反应,反应历程如图所示。下列说法正确的是
A.反应③比反应①更快达到平衡
B.温度越高,产物中M的纯度越高
C.一定时间内,使用合适的催化剂可减少体系中P的含量
D.增大R的浓度,反应①②③的 增大, 减小【答案】C
【解析】A. 从图中可以看出,反应③的活化能比反应①大,则反应③速率比反应①慢,达到平衡的时间
更长,A不正确;
B.升高温度,反应速率加快,但三个反应都是放热反应,虽然副反应进行的程度减小,但反应①的转化
率也降低,产物中M的纯度并不高,B不正确;
C.一定时间内,使用合适的催化剂,可提高反应①的选择性,降低副反应②、③的选择性,从而减少体
系中P的含量,C正确;
D.增大R的浓度,可增大单位体积内的活化分子数,有效碰撞的次数增多,反应①②③的 增大,
也增大,D不正确;
故选C。
考点二 水溶液中的离子平衡
21.(2024届广东省大湾区一模)常温下,向 次磷酸 (一元酸)中,逐滴加入
溶液,溶液的 与所加 溶液的体积关系如图所示。下列有关叙述正确的是
A.a点溶液中
B.b点溶液中
C. 溶液显酸性
D. 的电离平衡常数约为
【答案】A
【解析】
A.根据电荷守恒,a点溶液中 ,A正确;
B.b点溶液中恰好完全反应,溶质为 , 水解呈碱性, ,B错误;
C. 为一元酸, 溶液为正盐, 水解呈碱性,C错误;
D.由起点, 的电离平衡常数约为 ,D错误;
故选A。
22.(2024届广东省广州市黄浦区二模)水溶液中,过二硫酸盐与碘离子反应的离子方程式为:
,向溶液中加入含 的溶液,反应机理如图所示。下列有关该反应的说法不正
确的是A.反应①的速率比反应②的速率快
B. 是该反应的催化剂,加入 后反应体系更快达到平衡
C.向反应后的溶液小滴加淀粉溶液,溶液变蓝,再适当升温,蓝色变浅
D.反应②的离子方程式为
【答案】A
【解析】A.由图可知,反应①的活化能比反应②的大,因此反应②的速率更快,故A错误;
B.图中产物应为 ,因此 是该反应的催化剂,可加快反应速率,故B正确;
C.由图可知,该反应为放热反应,升高温度,平衡逆向移动c(I)下降,溶液蓝色变浅,故C正确;
2
D.图中产物应为 ,即反应②的离子方程式为 ,故D正确;
故选A。
23.(2024届广东省广州市黄浦区二模)常温下,用 盐酸滴定 弱碱 溶
液,溶液中 、分布系数 随滴加盐酸体积 盐酸 的变化关系如图所示[比如 的分布系数:
],下列说法正确的是
A.曲线①代表 ,曲线②代表
B. 的电离平衡常数是
C. 水溶液中:
D. 水溶液加水稀释, 降低
【答案】B【分析】常温下,用0.1mol/L盐酸滴定25.00mL 0.1mol/L弱碱MOH溶液时,溶液中MOH的浓度减小,
M+浓度增大、溶液pH增大,则曲线①代表δ(M+)、曲线②代表pH的变化。
【解析】A.由分析可知,曲线①代表δ(M+),故A错误;
B.由图可知,a点时溶液中MOH与M+浓度相等,溶液pH为9.55,则MOH的电离平衡常数为
= c(OH-)= ,故B正确;
C.MCl溶液中存在电荷守恒关系 ,故C错误;
D.MCl是强酸弱碱盐,在溶液中水解使溶液呈酸性,加水稀释时,溶液中的氢离子浓度减小,溶液pH增
大,故D错误;
故选B。
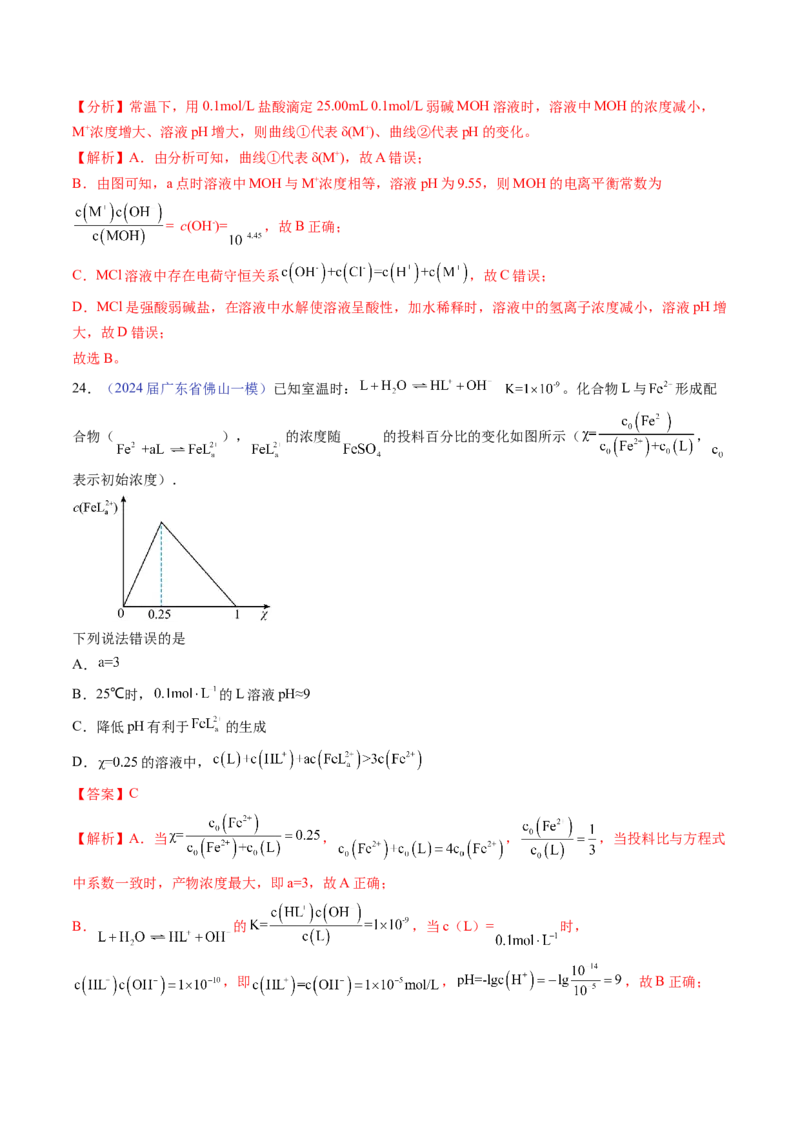
24.(2024届广东省佛山一模)已知室温时: 。化合物L与 形成配
合物( ), 的浓度随 的投料百分比的变化如图所示( ,
表示初始浓度).
下列说法错误的是
A.
B.25℃时, 的L溶液pH≈9
C.降低pH有利于 的生成
D. 的溶液中,
【答案】C
【解析】A.当 , , ,当投料比与方程式
中系数一致时,产物浓度最大,即a=3,故A正确;
B. 的 ,当c(L)= 时,
,即 , ,故B正确;C.降低pH, 平衡正向移动,c(L)减小,使得 平衡逆向移动,不
利于 的生成,故C错误;
D.由A可知,a=3, 的溶液中,由物料守恒可得:
,即 ,故D正确;
故选C。
25.(2024届广东省广州二模)常温下,乳酸(用HL表示)的 ,乳酸和氢氧化钠溶液反应
生成乳酸钠(用NaL表示)。下列说法正确的是
A.NaL水溶液呈中性
B.0.01 HL溶液的pH=2
C.0.01 HL溶液中,
D.0.01 NaL溶液中,
【答案】D
【解析】A.NaL是强碱弱酸盐,水解显碱性,A错误;
B. , ,pH=2.75,B错误;
C.HL微弱电离, ,C错误;
D.根据物料守恒, ,D正确;
故选D。
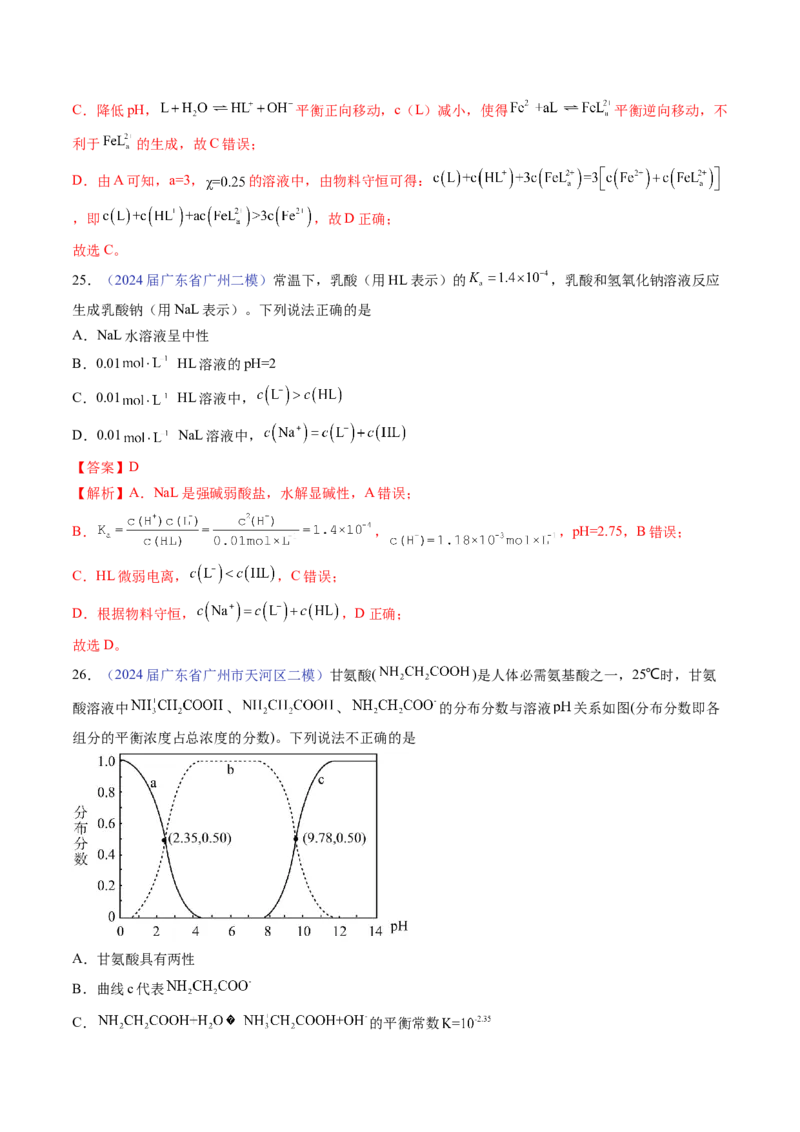
26.(2024届广东省广州市天河区二模)甘氨酸( )是人体必需氨基酸之一,25℃时,甘氨
酸溶液中 、 、 的分布分数与溶液 关系如图(分布分数即各
组分的平衡浓度占总浓度的分数)。下列说法不正确的是
A.甘氨酸具有两性
B.曲线c代表
C. 的平衡常数D. 溶液中
【答案】C
【分析】甘氨酸中含有氨基和羧基,氨基显碱性,羧基显酸性,在酸性条件下,存在的形式为
CHCOOH,随着pH 增大,逐步转化成NH CHCOOH,最终转化成NH CHCOO-,从而确定曲线a 代表
2 2 2 2 2
CHCOOH,曲线b代表为NH CHCOOH,曲线c 代表NH CHCOO-,据此分析。
2 2 2 2 2
【解析】A.甘氨酸含有氨基和羧基,故具有两性,故A正确;
B.分析可知,C为NH CHCOO-,故B正确;
2 2
C.分析a、b交点可知c(NH CHCOOH)=c( CHCOOH),此时pH为2.35,K=c(OH-)= =10-11.65,
2 2 2
故C错误;
D.NH CHCOOK溶液中酸根离子NH CHCOO-会发生水解,故c(K+)>c(NH CHCOO-),此时水解后溶液
2 2 2 2 2 2
显碱性,故c(OH-)>c(H+),则 ,故D正确;
故答案为:C。
27.(2024届广东省梅州二模)用一定浓度 溶液滴定某一元酸 溶液。滴定终点附近溶液 和
导电能力的变化如下图所示。下列说法正确的是
A. 为一元强酸
B.a点对应的溶液中:
C.根据溶液 和导电能力的变化可判断
D.a、b、c三点对应的溶液中b点水的电离程度最大
【答案】D
【解析】A.随着氢氧化钠溶液的加入,溶液的导电能力逐渐增强,说明原 溶液中的酸未完全电离,
即 为一元弱酸,A错误;
B.题干未指明溶液是否处于室温,pH=7不能说明 ,B错误;
C.根据b点溶液导电能力突然增大可知,b点NaOH与HA完全中和,a点溶液显中性,说明HA未完全
中和,则 ,C错误;
D.a点溶液中含有HA和NaA、b点溶液中含有NaA、c点溶液中含有NaA和NaOH,酸或碱抑制水的电
离,能够水解的盐促进水的电离,因此a、b、c三点对应的溶液中水的电离程度b最大,D正确;答案选D。
28.(2024届广东省汕头二模)牙齿表面有一层牙釉质在保护着,存在如下平衡:
,已知的 的
。下列说法错误的是
A.口腔中残留大量的酸性物质会破坏牙釉质
B.牙膏中添加适量的磷酸盐,可以有效保护牙齿
C.若用碳酸氢钠稀溶液进行漱口,会使上述平衡发生移动,此时 变小
D.使用含氟(NaF)牙膏,可实现 与 的转化
【答案】C
【解析】A.牙釉质的主要成分为羟基磷酸钙[Ca (PO )OH],口腔中残留大量的酸性物质,将消耗 ,
5 4 3
导致生成物 浓度减小,使羟基磷酸钙沉淀溶解平衡右移,破坏牙釉质,故A正确;
B.在牙膏中添加适量的磷酸盐,增大了磷酸根离子的浓度,使得反应
化学平衡逆向移动,有利于生成羟基磷灰石,能起
到保护牙齿的作用,故B正确;
C. 只受温度影响,加入碳酸氢钠后,温度不变, 不变,故C错误;
D.发生的反应为: ,由方程式可知,反应的平衡
常数K= = = = ≈2.4×1024,因此使用添加NaF的含
氟牙膏,可实现 与 的转化,故D正确;
故答案选C。
29.(2024届广东省韶关二模)常温下,用 溶液滴定10mL等浓度的HCl溶液和用
的 溶液滴定10mL等浓度的 溶液,滴定过程中溶液的导电能力如图所示。
下列说法不正确的是
A.曲线①表示用 的 溶液滴定10mL等浓度的HCl溶液过程中溶液的导电能力变化
B.等浓度等体积的HCl溶液与 溶液的导电能力相同
C.a点的K 等于b点的K
w w
D.d点和e点溶液中均有:【答案】B
【分析】用0.1000mol/L的NaOH溶液滴定10mL等浓度的HCl溶液过程中,在酸碱恰好完全中和之前,
溶液中离子物质的量几乎不变,但溶液体积增大,离子浓度降低,导电能力降低至最低点,恰好完全反应
后继续滴加氢氧化钠溶液,导电性增强,但用0.1000mol/L的CHCOOH溶液滴定10mL等浓度的NaOH溶
3
液时,酸碱恰好完全反应后,再继续滴加的醋酸为弱酸,相当于稀释了生成的醋酸钠溶液,所以溶液导电
性会减弱,即曲线①代表氢氧化钠滴定盐酸,曲线②代表醋酸滴定氢氧化钠溶液。
【解析】A.据以上分析可知,曲线①表示用0.1000mol/L的NaOH溶液滴定10mL等浓度的HCl溶液过程
中溶液的导电能力变化,故A正确;
B.曲线①代表氢氧化钠滴定盐酸,曲线②代表醋酸滴定氢氧化钠溶液,即a点代表0.1000mol/L的盐酸的
导电能力,b点代表等浓度的氢氧化钠溶液的导电能力,所以等浓度等体积的HCl溶液与NaOH溶液的导
电能力不同,故B错误;
C.K 只与温度有关,所以a点的K 等于b点的K ,故C正确;
w w w
D.d点为醋酸和NaOH恰好完全反应的点,e点溶液中的溶质为醋酸钠和醋酸,其中均有电荷守恒:
,故D正确;
故答案为:B。
30.(2024届广东省湛江二模)常温下,等浓度的氨水和醋酸溶液互相滴定过程中,溶液中pH与pX[
或 ]的关系如图所示。下列说法错误的是
A.常温下,
B.水的电离程度:
C.曲线Ⅱ代表NH •H O溶液滴定CHCOOH溶液
3 2 3
D.g点
【答案】B
【分析】Ⅰ曲线开始显碱性,代表CHCOOH酸溶液滴定NH •H O碱溶液,则Ⅱ曲线代表NH •H O碱溶液
3 3 2 3 2
滴定CHCOOH酸溶液;因为为等浓度NH •H O碱溶液和CHCOOH酸溶液互相滴定,则g点代表两者恰
3 3 2 3
好完全反应,此时溶质为CHCOONH,据此分析作答。
3 4
【解析】A.当pH=4.76,呈酸性,-lg =lg =0,即 =1,K(CHCOOH)= =10-4.76,A正确;
a 3
B.由于CHCOONH 是盐溶液,促进水的电离,所以水的电离程度最大,当碱溶液中c(OH-)与酸溶液中
3 4
c(H+)相等时,都会水的电离抑制程度相同,水的电离程度也相同,所以水的电离程度:e=f<g,B错误;
C.由分析可知,曲线Ⅱ代表NH •H O溶液滴定CHCOOH溶液,C正确;
3 2 3
D.由图可知,g点的溶质是弱酸弱碱盐CHCOONH,pH=7,则g点c(CHCOO- )=c( B+)>
3 4 3
c(CHCOOH)=c(NH •H O),D正确;
3 3 2
故答案为:B。