文档内容
热点 12 “看图说话”描述微观结构变化过程
“看图说话”描述微观结构变化过程是近几年江苏高考的必考内容,属于热点问题,
主要考查用语言描述微观结构变化过程,解题时读懂题干信息,看清图像中微粒变化或者
结构的变化进行正确描述,注意语言精练,表达准确,同时迁移应用正确的化学原理及结
构化学知识,备考时关注核心考点的掌握至关重要。
一、反应机理
(1)反应机理是用来描述某反应物到反应产物所经由的全部基元反应,就是把一个复杂
反应分解成若干个基元反应,以图示的形式来描述某一化学变化所经由的全部反应,然后
按照一定规律组合起来,从而阐述复杂反应的内在联系,以及总反应与基元反应内在联系。
(2)反应机理详细描述了每一步转化的过程,包括过渡态的形成,键的断裂和生成,以
及各步的相对速率大小等。典型的是基元反应碰撞理论和基元反应过渡态理论。
(3)反应机理中包含的基元反应是单分子反应或双分子反应。完整的反应机理需要考虑
到反应物、催化剂、反应的立体化学、产物以及各物质的用量。
(4)认识化学反应机理,任何化合物的每一步反应都应该是在该条件下此类化合物的通
用反应。
2.有效碰撞理论
(1)化学反应发生的条件:在化学反应中,反应物分子不断发生碰撞,大多数碰撞无法
发生反应,只有少数分子的碰撞才能发生化学反应,能发生有效碰撞的分子是活化分子。
普通反应物分子形成活化分子所需要的能量叫活化能。而活化分子的碰撞也不一定都能发
生有效碰撞。发生有效碰撞不仅有能量的因素,还有空间因素,只有同时满足这两者的要
求才能发生有效碰撞。
二、有机反应机理必备知识
1.自由基反应
自由基反应,常指有机分子在反应中共价键发生均裂,产生自由基中间体。有自由基参
加的反应称为自由基反应。
2. 亲电加成反应
(1)鎓离子历程:X2与C=C经 π- 络合物 形成卤鎓离子 ,亲核的X-经反式加成生成产物。
(2)碳正离子 历程:
(3)烯烃的自由基加成 反应机理
(4)烯烃被过氧酸氧化成环氧化合物 的反应机理
(5)1,2-环氧化合物的开环反应
1,2-环氧化合物是不稳定的,在酸或碱的催化作用下都会发生开环反应;碱催化,负离
子进攻空阻较小 的碳。酸催化,负离子进攻正性较大 的碳。
考向 “看图说话”描述微观结构变化过程
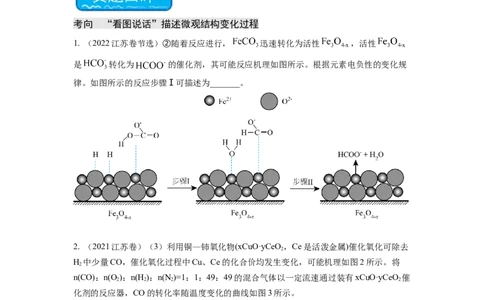
1. (2022江苏卷节选)②随着反应进行, 迅速转化为活性 ,活性
是 转化为 的催化剂,其可能反应机理如图所示。根据元素电负性的变化规
律。如图所示的反应步骤Ⅰ可描述为_______。
2. (2021江苏卷)(3)利用铜—铈氧化物(xCuO·yCeO ,Ce是活泼金属)催化氧化可除去
2
H 中少量CO,催化氧化过程中Cu、Ce的化合价均发生变化,可能机理如图2所示。将
2
n(CO):n(O ):n(H ):n(N )=1:1:49:49的混合气体以一定流速通过装有xCuO·yCeO 催
2 2 2 2
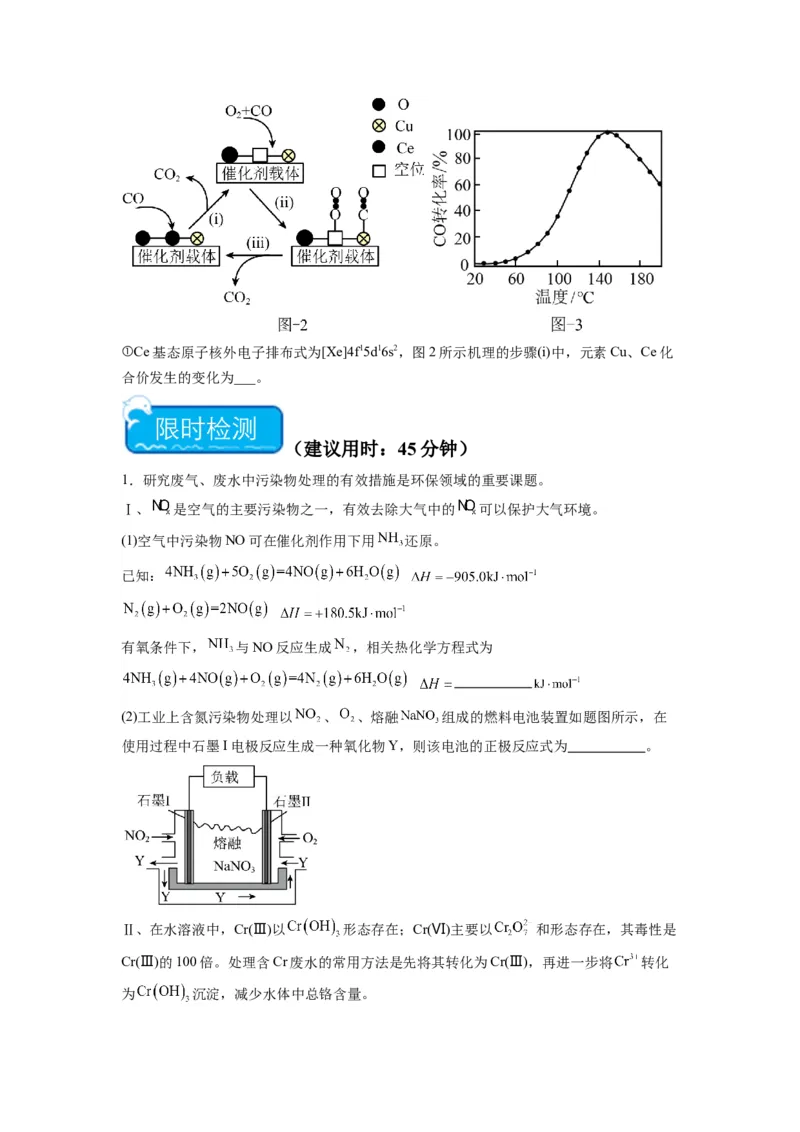
化剂的反应器,CO的转化率随温度变化的曲线如图3所示。①Ce基态原子核外电子排布式为[Xe]4f15d16s2,图2所示机理的步骤(i)中,元素Cu、Ce化
合价发生的变化为___。
(建议用时:45分钟)
1.研究废气、废水中污染物处理的有效措施是环保领域的重要课题。
Ⅰ、 是空气的主要污染物之一,有效去除大气中的 可以保护大气环境。
(1)空气中污染物NO可在催化剂作用下用 还原。
已知:
有氧条件下, 与NO反应生成 ,相关热化学方程式为
(2)工业上含氮污染物处理以 、 、熔融 组成的燃料电池装置如题图所示,在
使用过程中石墨I电极反应生成一种氧化物Y,则该电池的正极反应式为 。
Ⅱ、在水溶液中,Cr(Ⅲ)以 形态存在;Cr(Ⅵ)主要以 和形态存在,其毒性是
Cr(Ⅲ)的100倍。处理含Cr废水的常用方法是先将其转化为Cr(Ⅲ),再进一步将 转化
为 沉淀,减少水体中总铬含量。(3)Cr(Ⅵ)在水溶液中常有 和 两种存在形式,加酸可以使 转化为 ,
该反应的离子方程式为 。
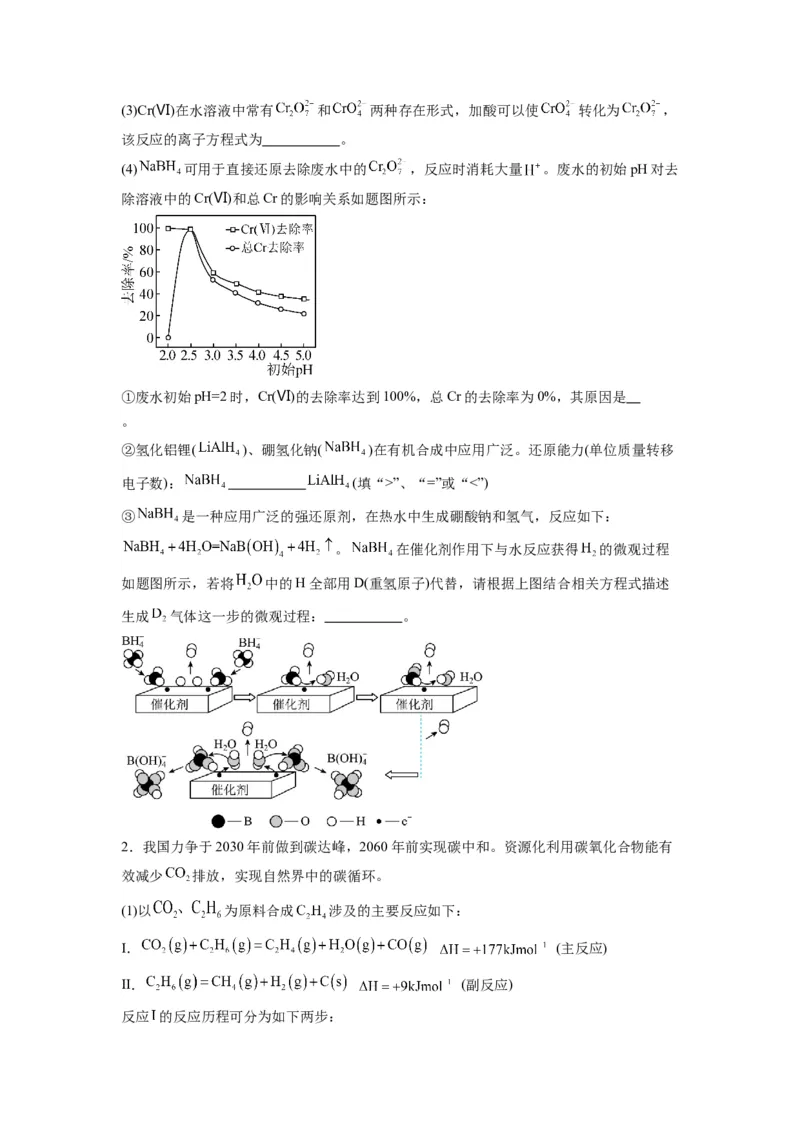
(4) 可用于直接还原去除废水中的 ,反应时消耗大量 。废水的初始pH对去
除溶液中的Cr(Ⅵ)和总Cr的影响关系如题图所示:
①废水初始pH=2时,Cr(Ⅵ)的去除率达到100%,总Cr的去除率为0%,其原因是
。
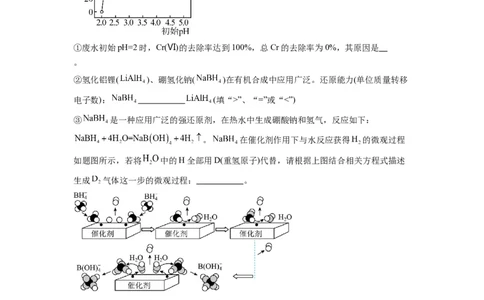
②氢化铝锂( )、硼氢化钠( )在有机合成中应用广泛。还原能力(单位质量转移
电子数): (填“>”、“=”或“<”)
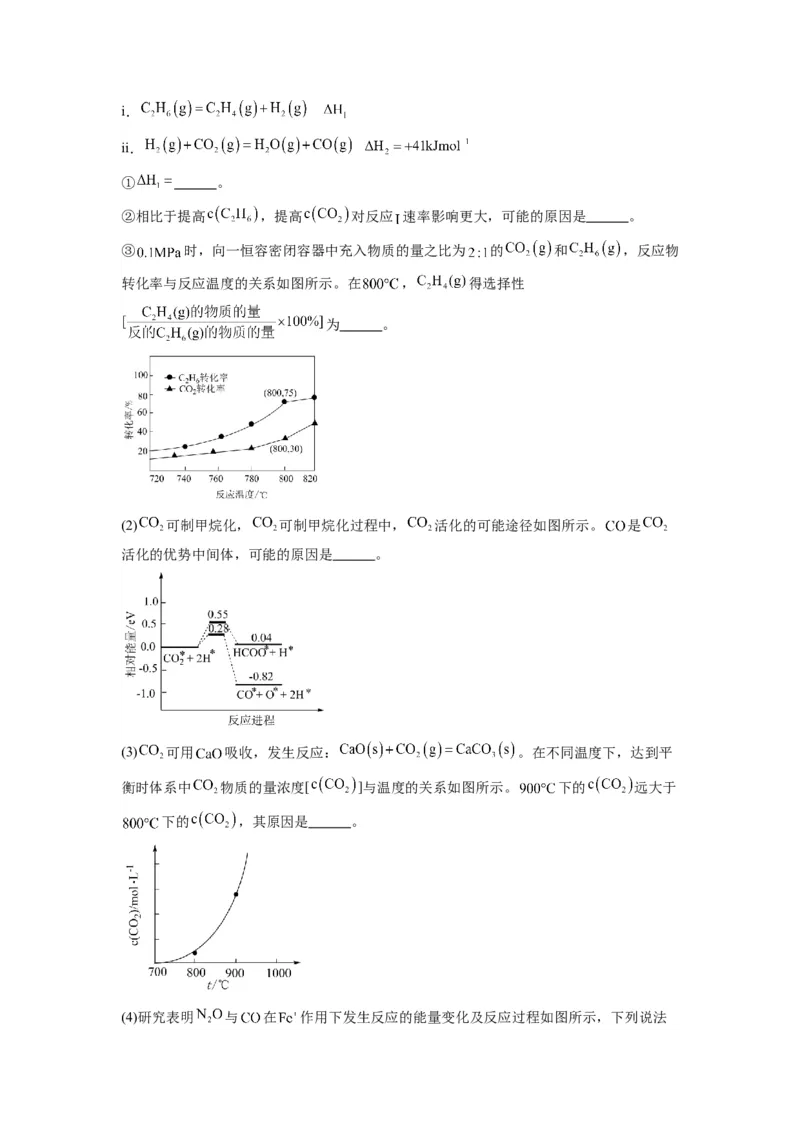
③ 是一种应用广泛的强还原剂,在热水中生成硼酸钠和氢气,反应如下:
。 在催化剂作用下与水反应获得 的微观过程
如题图所示,若将 中的H全部用D(重氢原子)代替,请根据上图结合相关方程式描述
生成 气体这一步的微观过程: 。
2.我国力争于2030年前做到碳达峰,2060年前实现碳中和。资源化利用碳氧化合物能有
效减少 排放,实现自然界中的碳循环。
(1)以 为原料合成 涉及的主要反应如下:
I. (主反应)
II. (副反应)
反应 的反应历程可分为如下两步:i.
ii.
① 。
②相比于提高 ,提高 对反应 速率影响更大,可能的原因是 。
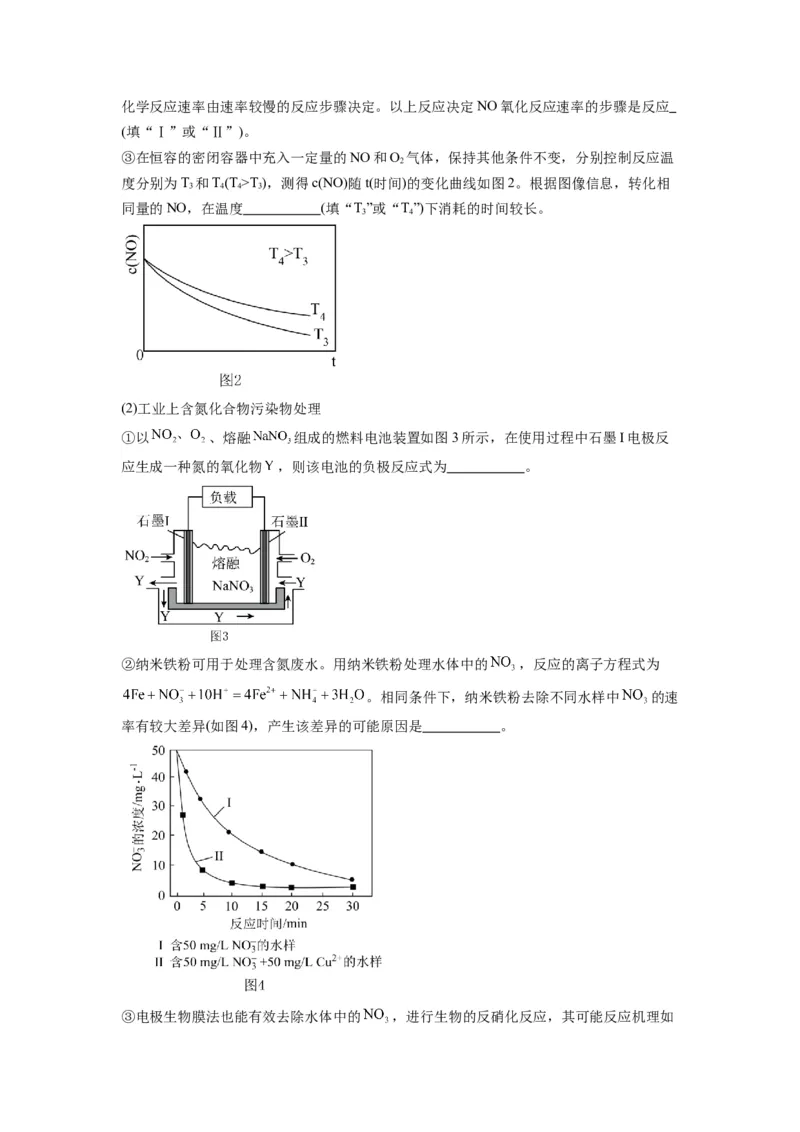
③ 时,向一恒容密闭容器中充入物质的量之比为 的 和 ,反应物
转化率与反应温度的关系如图所示。在 , 得选择性
为 。
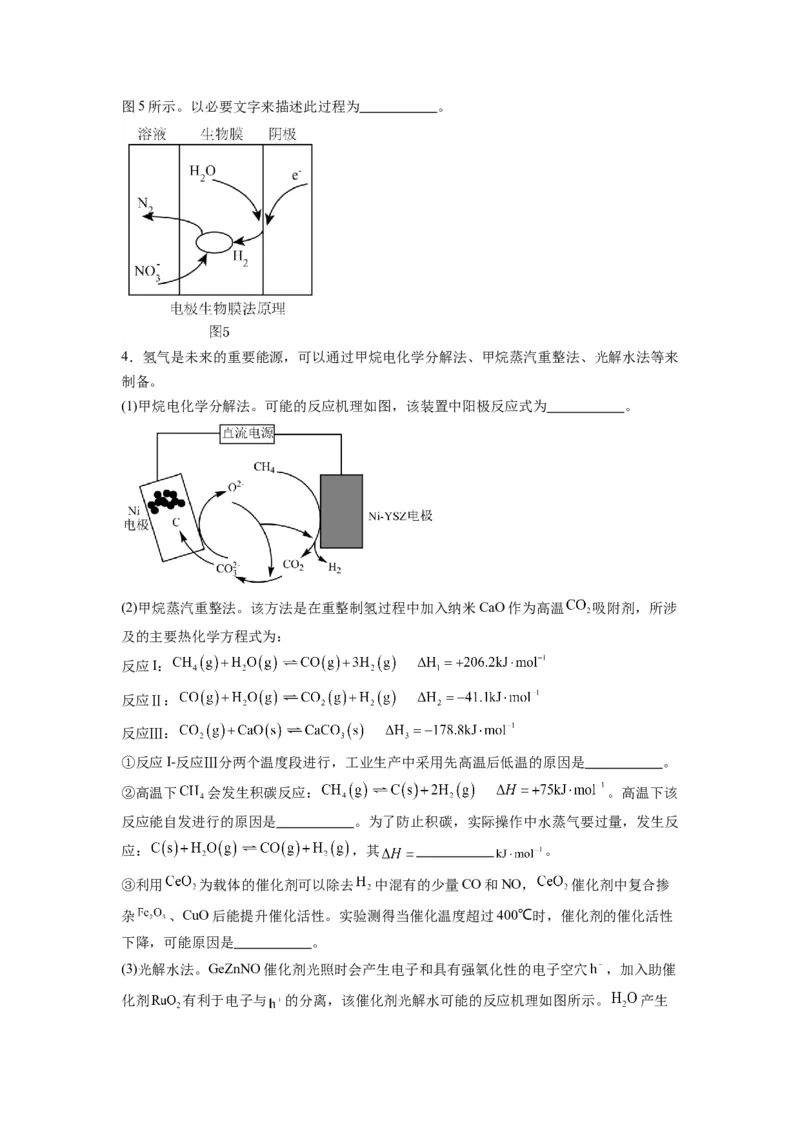
(2) 可制甲烷化, 可制甲烷化过程中, 活化的可能途径如图所示。 是
活化的优势中间体,可能的原因是 。
(3) 可用 吸收,发生反应: 。在不同温度下,达到平
衡时体系中 物质的量浓度[ ]与温度的关系如图所示。 下的 远大于
下的 ,其原因是 。
(4)研究表明 与 在 作用下发生反应的能量变化及反应过程如图所示,下列说法正确的是___________。
A. 是催化剂, 是中间产物
B.增大压强可以提高 与 的反应速率和平衡转化率
C.每当有 生成时,转移 电子
D. 与 转变成 和 的总过程,温度升高,平衡常数K增大
3. 是空气的主要污染物之一,有效去除大气中的 可以保护大气环境。含氮废水氨
氮(以 存在)和硝态氮(以 存在)引起水体富营养化,需经处理后才能排
放。
(1)空气中污染物 可在催化剂作用下用 还原。
①已知: ;
;
有氧条件下, 与 反应生成 ,相关热化学方程式为
; 。
②NO氧化反应:2NO(g)+O(g) 2NO (g)分两步进行,其反应过程能量变化如图1。
2 2
反应Ⅰ.2NO(g) NO(g) ΔH;
2 2 1
反应Ⅱ.NO(g)+O(g)=2NO (g) ΔH
2 2 2 2 2化学反应速率由速率较慢的反应步骤决定。以上反应决定NO氧化反应速率的步骤是反应
(填“Ⅰ”或“Ⅱ”)。
③在恒容的密闭容器中充入一定量的NO和O 气体,保持其他条件不变,分别控制反应温
2
度分别为T 和T(T >T),测得c(NO)随t(时间)的变化曲线如图2。根据图像信息,转化相
3 4 4 3
同量的NO,在温度 (填“T”或“T”)下消耗的时间较长。
3 4
(2)工业上含氮化合物污染物处理
①以 、熔融 组成的燃料电池装置如图3所示,在使用过程中石墨I电极反
应生成一种氮的氧化物 ,则该电池的负极反应式为 。
②纳米铁粉可用于处理含氮废水。用纳米铁粉处理水体中的 ,反应的离子方程式为
。相同条件下,纳米铁粉去除不同水样中 的速
率有较大差异(如图4),产生该差异的可能原因是 。
③电极生物膜法也能有效去除水体中的 ,进行生物的反硝化反应,其可能反应机理如图5所示。以必要文字来描述此过程为 。
4.氢气是未来的重要能源,可以通过甲烷电化学分解法、甲烷蒸汽重整法、光解水法等来
制备。
(1)甲烷电化学分解法。可能的反应机理如图,该装置中阳极反应式为 。
(2)甲烷蒸汽重整法。该方法是在重整制氢过程中加入纳米CaO作为高温 吸附剂,所涉
及的主要热化学方程式为:
反应I:
反应Ⅱ:
反应Ⅲ:
①反应I-反应Ⅲ分两个温度段进行,工业生产中采用先高温后低温的原因是 。
②高温下 会发生积碳反应: 。高温下该
反应能自发进行的原因是 。为了防止积碳,实际操作中水蒸气要过量,发生反
应: ,其 。
③利用 为载体的催化剂可以除去 中混有的少量CO和NO, 催化剂中复合掺
杂 、CuO后能提升催化活性。实验测得当催化温度超过400℃时,催化剂的催化活性
下降,可能原因是 。
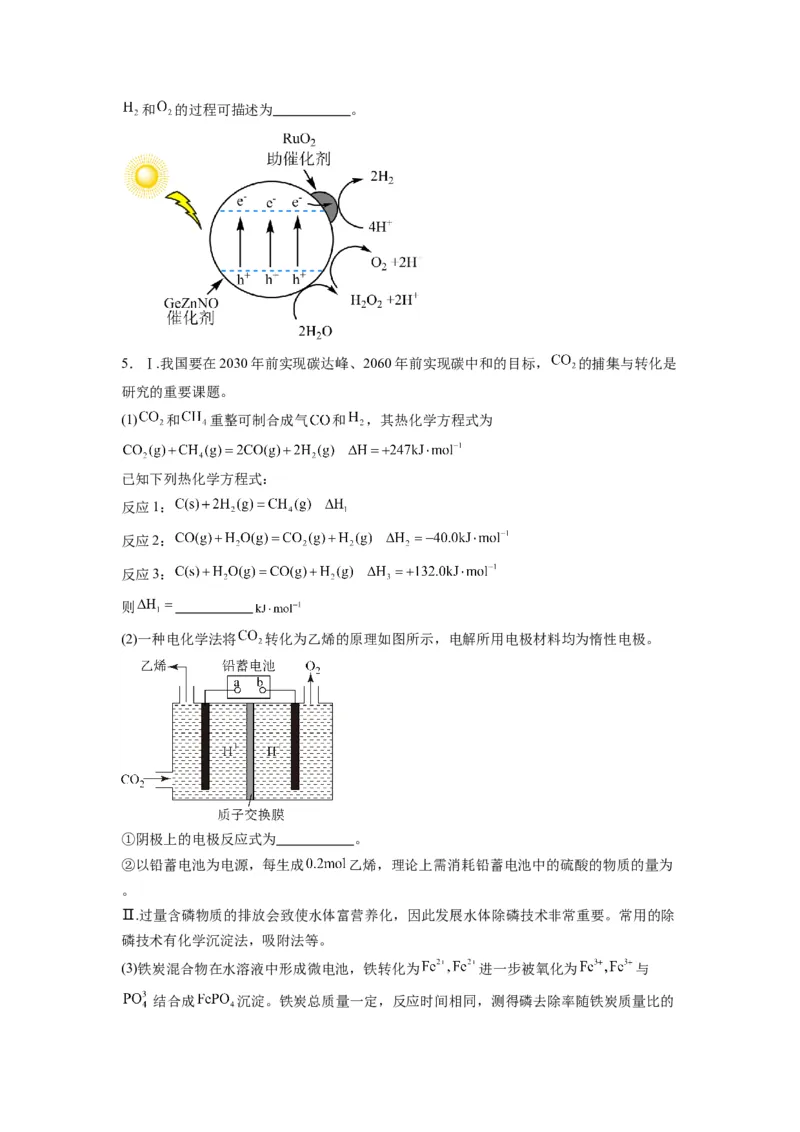
(3)光解水法。GeZnNO催化剂光照时会产生电子和具有强氧化性的电子空穴 ,加入助催
化剂 有利于电子与 的分离,该催化剂光解水可能的反应机理如图所示。 产生和 的过程可描述为 。
5.Ⅰ.我国要在2030年前实现碳达峰、2060年前实现碳中和的目标, 的捕集与转化是
研究的重要课题。
(1) 和 重整可制合成气 和 ,其热化学方程式为
已知下列热化学方程式:
反应1:
反应2:
反应3:
则
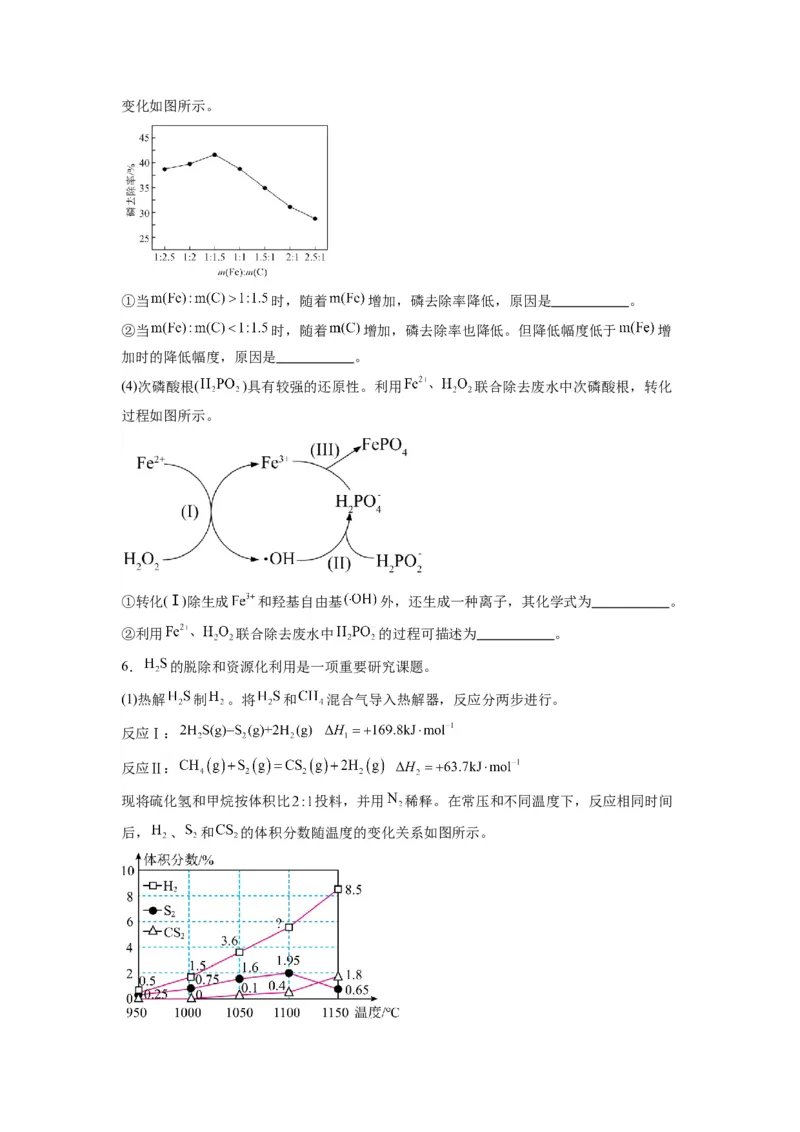
(2)一种电化学法将 转化为乙烯的原理如图所示,电解所用电极材料均为惰性电极。
①阴极上的电极反应式为 。
②以铅蓄电池为电源,每生成 乙烯,理论上需消耗铅蓄电池中的硫酸的物质的量为
。
Ⅱ.过量含磷物质的排放会致使水体富营养化,因此发展水体除磷技术非常重要。常用的除
磷技术有化学沉淀法,吸附法等。
(3)铁炭混合物在水溶液中形成微电池,铁转化为 进一步被氧化为 与
结合成 沉淀。铁炭总质量一定,反应时间相同,测得磷去除率随铁炭质量比的变化如图所示。
①当 时,随着 增加,磷去除率降低,原因是 。
②当 时,随着 增加,磷去除率也降低。但降低幅度低于 增
加时的降低幅度,原因是 。
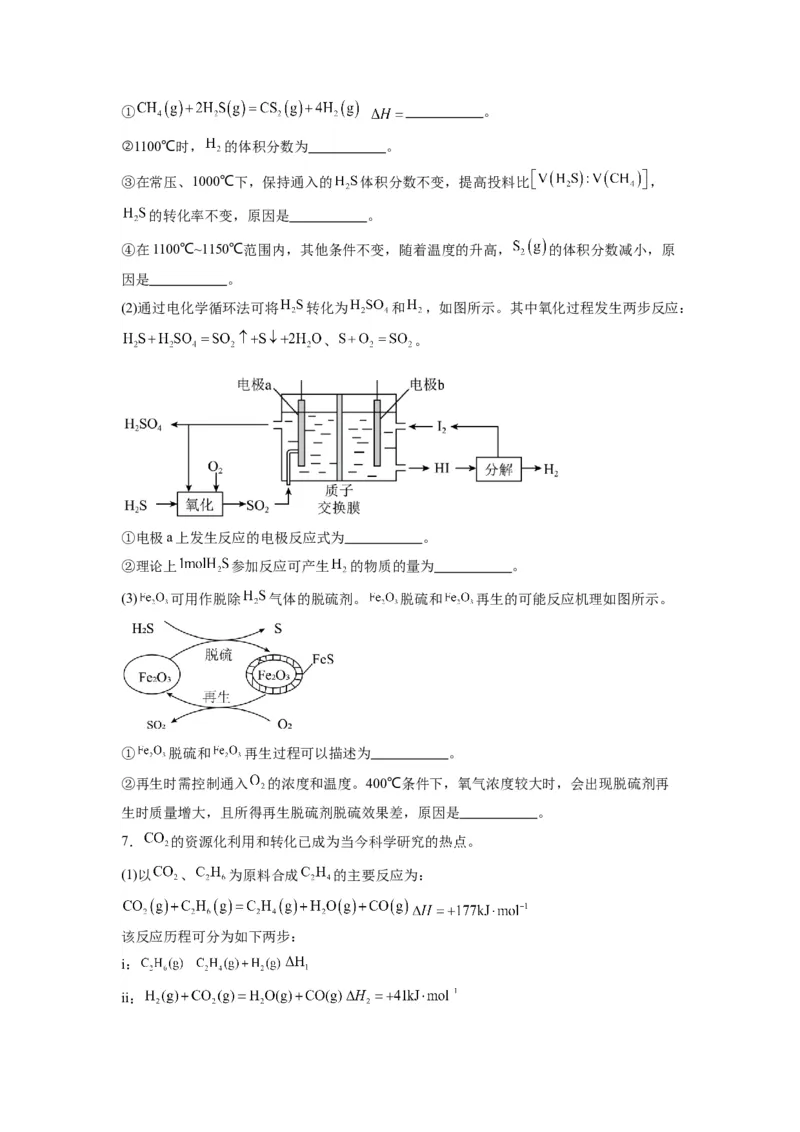
(4)次磷酸根( )具有较强的还原性。利用 联合除去废水中次磷酸根,转化
过程如图所示。
①转化(Ⅰ)除生成 和羟基自由基 外,还生成一种离子,其化学式为 。
②利用 联合除去废水中 的过程可描述为 。
6. 的脱除和资源化利用是一项重要研究课题。
(1)热解 制 。将 和 混合气导入热解器,反应分两步进行。
反应Ⅰ:
反应Ⅱ:
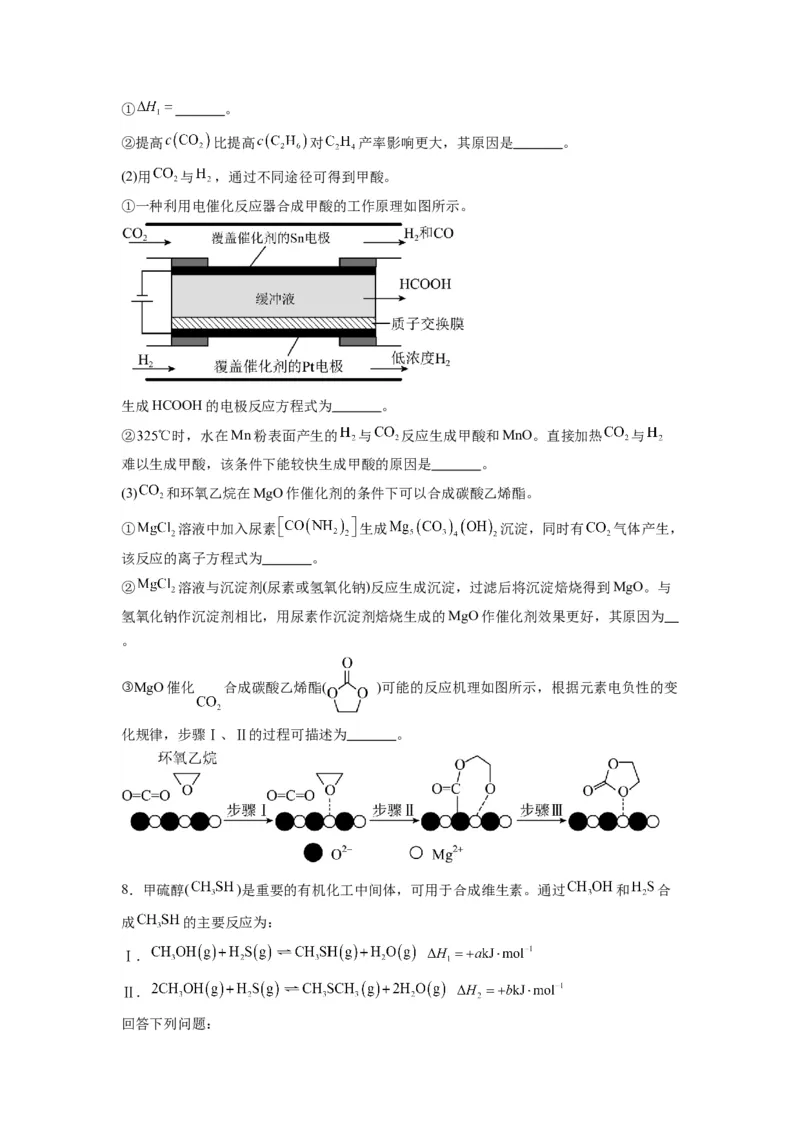
现将硫化氢和甲烷按体积比 投料,并用 稀释。在常压和不同温度下,反应相同时间
后, 、 和 的体积分数随温度的变化关系如图所示。① 。
②1100℃时, 的体积分数为 。
③在常压、1000℃下,保持通入的 体积分数不变,提高投料比 ,
的转化率不变,原因是 。
④在1100℃~1150℃范围内,其他条件不变,随着温度的升高, 的体积分数减小,原
因是 。
(2)通过电化学循环法可将 转化为 和 ,如图所示。其中氧化过程发生两步反应:
、 。
①电极a上发生反应的电极反应式为 。
②理论上 参加反应可产生 的物质的量为 。
(3) 可用作脱除 气体的脱硫剂。 脱硫和 再生的可能反应机理如图所示。
① 脱硫和 再生过程可以描述为 。
②再生时需控制通入 的浓度和温度。400℃条件下,氧气浓度较大时,会出现脱硫剂再
生时质量增大,且所得再生脱硫剂脱硫效果差,原因是 。
7. 的资源化利用和转化已成为当今科学研究的热点。
(1)以 、 为原料合成 的主要反应为:
该反应历程可分为如下两步:
i:
ii:① 。
②提高 比提高 对 产率影响更大,其原因是 。
(2)用 与 ,通过不同途径可得到甲酸。
①一种利用电催化反应器合成甲酸的工作原理如图所示。
生成HCOOH的电极反应方程式为 。
② 时,水在Mn粉表面产生的 与 反应生成甲酸和MnO。直接加热 与
难以生成甲酸,该条件下能较快生成甲酸的原因是 。
(3) 和环氧乙烷在MgO作催化剂的条件下可以合成碳酸乙烯酯。
① 溶液中加入尿素 生成 沉淀,同时有 气体产生,
该反应的离子方程式为 。
② 溶液与沉淀剂(尿素或氢氧化钠)反应生成沉淀,过滤后将沉淀焙烧得到MgO。与
氢氧化钠作沉淀剂相比,用尿素作沉淀剂焙烧生成的MgO作催化剂效果更好,其原因为
。
③MgO催化 合成碳酸乙烯酯( )可能的反应机理如图所示,根据元素电负性的变
化规律,步骤Ⅰ、Ⅱ的过程可描述为 。
8.甲硫醇( )是重要的有机化工中间体,可用于合成维生素。通过 和 合
成 的主要反应为:
Ⅰ.
Ⅱ.
回答下列问题:(1)计算反应 的ΔH= 。
(2) 时,向恒容密闭容器中充入一定量 和 发生反应,下列事实能说明
反应达到平衡状态的是 (填选项字母);若按相同比例再充入一定量 和
, 的平衡转化率将 (填“变大”“变小”或“不变”)。
A.容器内气体密度不再发生变化 B.混合气体的平均相对分子质量不再发生变化
C. 的体积分数不再发生变化 D. 和 的物质的量之比不再变
化
(3) 时,按物质的量之比为1︰2向压强为 的恒压密闭容器中充入 和
发生反应,达到平衡时, 的转化率为80%, 的体积分数为
5%。
①计算 的选择性为 ( 的选择性
)。
②反应Ⅰ的平衡常数 ( 是用分压表示的平衡常数)。
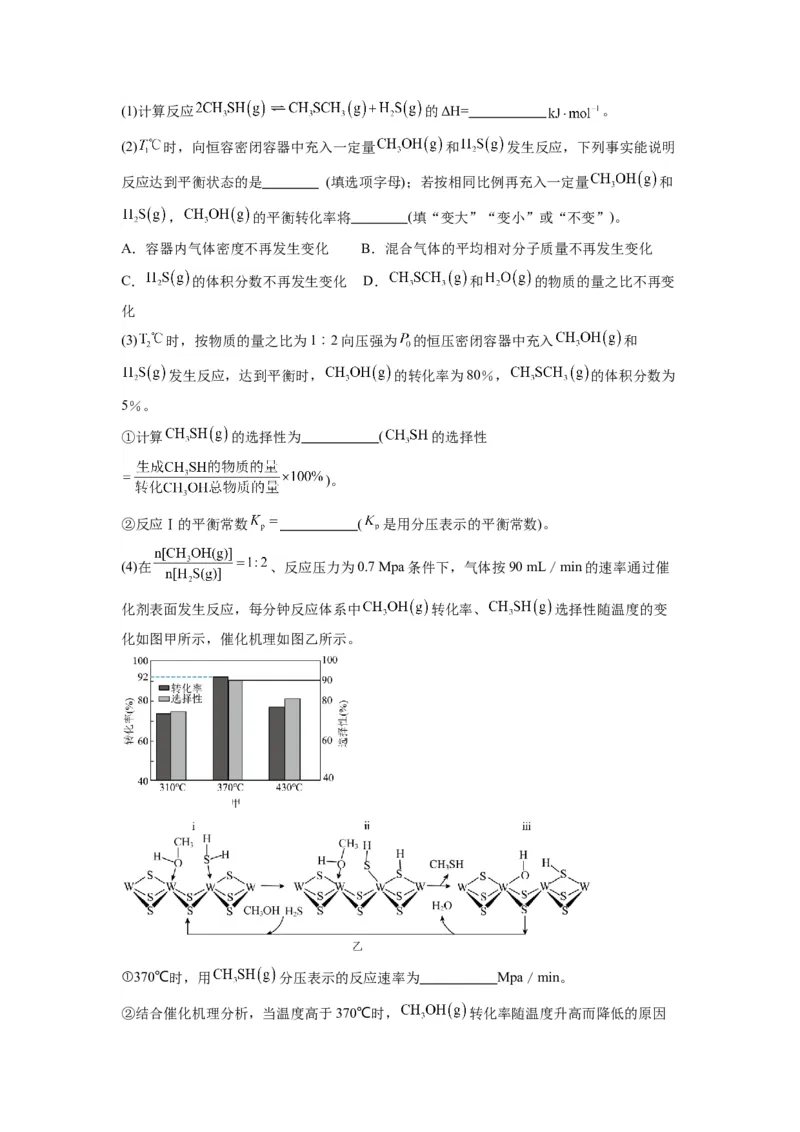
(4)在 、反应压力为0.7 Mpa条件下,气体按90 mL/min的速率通过催
化剂表面发生反应,每分钟反应体系中 转化率、 选择性随温度的变
化如图甲所示,催化机理如图乙所示。
①370℃时,用 分压表示的反应速率为 Mpa/min。
②结合催化机理分析,当温度高于370℃时, 转化率随温度升高而降低的原因可能为 。
③从化学键的角度描述ⅲ→ⅰ脱水的过程: 。