文档内容
第 15 练
水溶液中的离子平衡图像分析
1.pH与稀释倍数的线性关系图像分析(以HX,HY为例子)
【方法技巧】
(1)依据曲线变化,判断HY为强酸、HX为弱酸
(2)a、b两点的溶液中:c(X-)=c(Y-)=c(H+)一c(OH-)
(3)水的电离程度:d>c>a=b
2.酸碱中和滴定曲线上的特殊点分析(常温下,用0.1000 mol·L-1 NaOH溶液滴定
20.00 mL 0.1000 mol·L-1 CHCOOH溶液所得滴定曲线为例子)
3
【方法技巧】解题时巧抓“四点”,突破溶液中的粒子浓度关系:
(1)抓反应“一半”点,判断是什么溶质的等量混合。
(2)抓“恰好”反应点,判断生成什么溶质及溶液的酸碱性。
(3)抓溶液的“中性”点,判断生成什么溶质,哪种物质过量或不足。
(4)抓反应的“过量”点,判断溶液中是什么溶质,哪种物质过量。
“一半”点B点,溶质为CHCOONa、CHCOOH,离子浓度关系:
3 3
c(CHCOO-)>c(Na+)>c(H+)>c(OH-) ;
3
“中性”点C点,溶质为CHCOONa、CHCOOH,离子浓度关系:
3 3
c(CHCOO-)=c(Na+)>c(H+)=c(OH-);
3
“恰好”反应点D点,溶质为CHCOONa,离子浓度关系:
3
c(Na+)>c(CHCOO-)>c(OH-)>c(H+);
3
“过量”点E或F点,溶质为CHCOONa、NaOH,离子浓度关系:
3
c(Na+)>c(OH-)>c(CHCOO-)>c(H+)
33.沉淀溶解平衡图像分析(以氯化银为例)
【方法技巧】沉淀溶解平衡图像题的解题策略
第一步:明确图像中横、纵坐标的含义
横、纵坐标通常是难溶物溶解后电离出的离子浓度。
第二步:理解图像中线上点、线外点的含义
(1)在该沉淀溶解平衡图像上,曲线上任意一点都达到了沉淀溶解平衡状态,此时Q=
K。在温度不变时,无论改变哪种离子的浓度,另一种离子的浓度只能在曲线上变化,不
sp
会出现在曲线以外。
(2)曲线上方区域的点均为过饱和溶液,此时Q>K。
sp
(3)曲线下方区域的点均为不饱和溶液,此时Q<K 。
sp
第三步:抓住K 的特点,结合选项分析判断
sp
(1)溶液在蒸发时,离子浓度的变化分两种情况:
①原溶液不饱和时,离子浓度都增大;
②原溶液饱和时,离子浓度都不变。
(2)溶度积常数只是温度的函数,与溶液中溶质的离子浓度无关,在同一曲线上的点,
溶度积常数相同。
4.其它常考有关对数图像举例分析
(1)pC:类比pH,即为C离子浓度的负对数,规律是pC越大,C离子浓度越小。
(2)pK:平衡常数的负对数,规律是pK越大,平衡常数越小,对于一元弱酸(HX):pK
a
=pH-lg ,lg 越大,HX的电离程度越大。
(3)AG=lg ,氢离子浓度与氢氧根离子浓度比的对数,规律是 AG越大,酸性越强,中
性时AG=0。
6.巧用三大守恒规律解决实际问题(以NaCO 溶液为例子)
2 3
(1)电荷守恒:电解质溶液中所有阳离子的正电荷总数与所有阴离子的负电荷总数相等。
c(Na+)+c(H+)=2c(CO)+c(HCO)+c(OH-)。
(2)物料守恒:电解质溶液中由于电离或水解因素,离子会发生变化,变成其他离子或
分子等,但离子或分子中某些特定元素的原子的总数存在确定的比例关系。
c(Na+)=2【c(CO)+c(HCO)+c(HCO)】
2 3
(3)质子守恒:即HO电离出的氢离子和氢氧根离子总数相等。一般根据电荷守恒式和
2
物料守恒式整理得到。
c(OH-)=c(HCO)+2c(HCO)+c(H+)
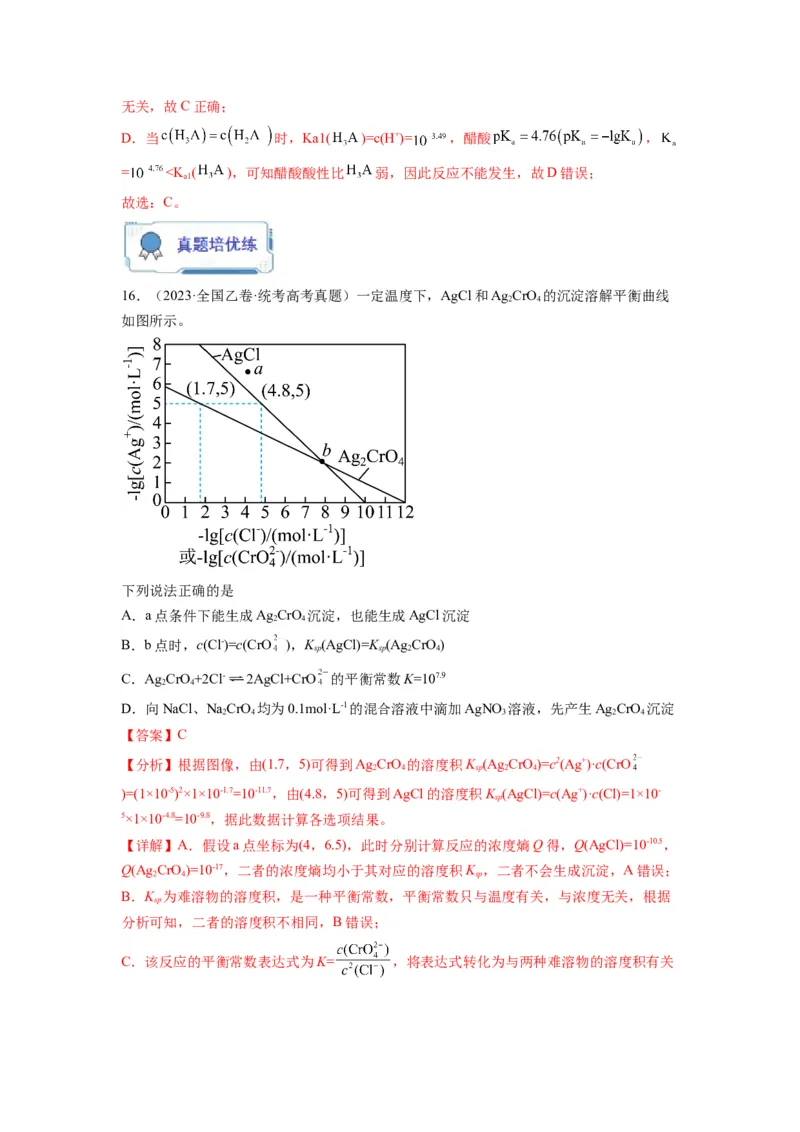
2 31.(2023·浙江·校联考三模)在一定温度下,冰醋酸稀释过程中溶液的导电能力与pH的
变化如图。下列有关说法中正确的是
A.a点 溶液未达到电离平衡状态
B.离子总浓度越大,溶液导电能力越强
C.向a、b两点溶液中分别滴入同一NaOH溶液至中性,溶液中的 相同
D.b点后,溶液中加水稀释,所有离子浓度均减小
【答案】B
【详解】A.加水稀释过程中,a点、b点都达到了电离平衡,故A错误;
B.导电能力与离子浓度和所带电荷数有关,因此离子总浓度越大,溶液导电能力越强,
故B正确;
C.根据电荷守恒 ,溶液呈中性,
,a点醋酸浓度大,向a、b两点溶液中分别滴入同一NaOH溶液至
中性,a点消耗的氢氧化钠溶液比b点消耗的氢氧化钠溶液多,因此溶液中的
是a点大于b点,故C错误;
D.b点后,溶液中加水稀释,醋酸根、氢离子浓度减小,氢氧根浓度增大,故D错误。
综上所述,答案为B。
2.(2023·上海·模拟预测)常温下,往20mL0.1mol•L-1CHCOOH溶液中逐滴滴入
3
0.1mol•L-1NH •H O溶液,溶液的pH与所加NH •H O溶液体积的关系如图所示,下列说法
3 2 3 2
正确的是已知:K(CHCOOH)=K (NH •H O)=2×10-5。
a 3 b 3 2
A.a点溶液中,离子浓度大小关系为c(CHCOO-)>c(H+)>c(OH-)
3
B.b点溶液中,一定存在c(NH )+c(NH•H O)=c(CHCOO-)+c(CH COOH)
3 2 3 3
C.c点溶液中,c(CHCOO-)+c(H+)>c(NH •H O)+c(OH-)+c(NH )
3 3 2
D.a→c的过程中,水的电离程度依次增大
【答案】B
【详解】A.a点溶液中,根据电荷守恒,离子浓度大小关系为c(H+)>c(CHCOO-)>
3
c(OH-),A错误;
B.根据物料守恒,b点溶液中, c(NH )+c(NH•H O)=c(CHCOO-)+c(CH COOH),B正确;
3 2 3 3
C.c点NH •H O过量,根据物料关系,c(NH •H O)+c(NH )> c(CHCOO-)+c(CH COOH)>
3 2 3 2 3 3
c(CHCOO-),又c(OH-)> c(H+),故c(CHCOO-)+c(H+)HY。下列判断正确的是
A.V>V
x Y
B.M点:c(X-)= c(Y-)
C.b表示盐酸滴定NaX溶液的曲线
D.常温下,K (HX) = 9.0×10-12
a
【答案】A
【分析】已知:酸性HX>HY,则NaY溶液水解程度更大,初始碱性更强,故ab分别为
NaX、NaY溶液的滴定曲线;
【详解】A.NaY溶液水解程度更大,初始碱性更强,氢氧根离子浓度更大;加入等量V
M
体积盐酸后,NaX、NaY溶液的pH相等,那么两者消耗氢氧根离子的量相同,则NaY溶
液的体积更小,故V>V ,A正确;
x Y
B.根据物料守恒可知,NaX溶液中 ,NaY溶液中
,且初始钠离子浓度相同,若M点:c(X-)= c(Y-),则,M点pH相同,则 ;已知:
酸性HX>HY,则 ;两者相互矛盾,B错误;
C.由分析可知,b表示盐酸滴定NaY溶液的曲线,C错误;
D. ,由0.1 mol·L-1的NaX溶液的初始pH=11可知,pOH=3,
、 ,则 ,
,D错误;
故选A。
4.(2023·山东烟台·统考二模)已知HX的电离常数 、 。常温
2
下,难溶物BaX在不同浓度盐酸(足量)中恰好不再溶解时,测得混合液中)lgc(Ba2+)与pH的
关系如图所示。下列说法错误的是
A. 约为
B.M点:
C.N点: 约为 mol⋅L
D.直线上任一点均满足:
【答案】B
【详解】A.由BaX+2H+=Ba2++H X结合HX的Ka、Ka 可知c(Ba2+)≈c(HX),HX H+
2 2 1 2 2 2
+HX-,HX- H++X2-故Ka= ,Ka= ,KaKa= =
1 2 1 2
,得到c(X2-)= , =c(Ba2+)c(X2-)= ,由题
干图示信息,当pH=1时,lg(Ba2+)=0即c(H+)=0.1mol/L,
c(Ba2+)=1.0mol/L,故 =c(Ba2+)c(X2-)= = 约为,A正确;
B.由题干信息可知,直线MN的方程式为:lg(Ba2+)=1-pH,故M点为lg(Ba2+)=0.4,
pH=0.6,故c(HX)≈c(Ba2+)=10-0.4mol/L,c(H+)=10-0.6mol/L,此时溶质为BaCl 和HX,故
2 2 2
,B错误;
C.由题干信息可知,直线MN的方程式为:lg(Ba2+)=1-pH,故N点pH=0.8,
lg(Ba2+)=0.2,故c(HX)≈c(Ba2+)=10-0.2mol/L,c(H+)=10-0.8mol/L, = =
2
约为 mol⋅L ,C正确;
D.由BaX+2H+=Ba2++H X、HX H++HX-、HX- H++X2-,根据物料守恒可知,直线上
2 2
任一点均满足: ,D正确;
故答案为:B。
5.(2023·河北·校联考模拟预测)常温下,用0.100 0 NaOH溶液滴定20 mL
0.100 0 溶液,溶液pH与滴入NaOH溶液的体积间的关系如图所示。下列
说法错误的是
A. 为二元弱酸
B.当 时:
C.滴定过程中,随着NaOH溶液的滴入,水的电离程度逐渐增强
D.当 时,
【答案】C
【详解】A.从滴定曲线上可知 的pH大于1小于2,则为二元弱酸,A正确;
B.当 时,溶液显酸性,所以 的电离大于水解,存在
,B正确;
C.40 mL后随着NaOH溶液的滴入,水的电离程度逐渐减小,C错误;
D.当 时根据物料守恒关系可知:。,D正确;
故选C。
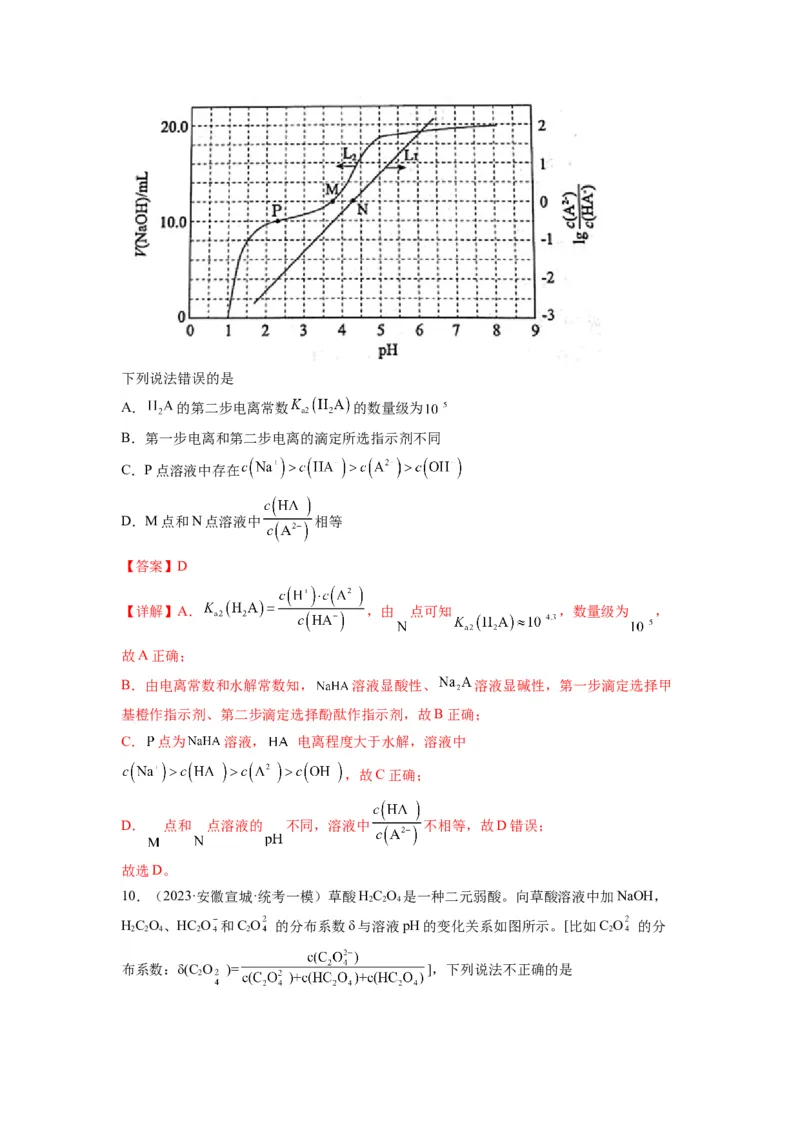
6.(2023·福建·校联考三模)常温下,向20 mL 0.1 mol/L H S溶液中缓慢加入少量溶于水
2
的MSO 粉末(已知MS难溶,忽略溶液体积变化),溶液中 与 变化如图所示。
4
已知: , 。下列说法错误的是
A.a点溶液的pH约为5
B.a、b、c三点溶液中由水电离产生的 最大的是a点
C.b点溶液中,
D.c点溶液中,
【答案】C
【详解】A.设0.1mol/L的HS溶液中c(H+)为x,则c(H+)≈c(HS-)=xmol/L,K (H S)=
2 a1 2
= ≈ =1.0×10-9,x=10-5mol/L,a点溶液的pH约为5,A正确;
B.随着MSO 粉末的加入发生反应MSO +H S=MS↓+HSO ,随反应进行硫酸浓度增大,
4 4 2 2 4
对水电离的抑制程度增大,a、b、c三点中由水电离产生的c(H+)最大的是a点,B正确;
C.K (H S)= =1.0×10-9,K (H S)= =1.0×10-13,K (H S)×K (H S)=
a1 2 a2 2 a1 2 a2 2
× =1.0×10-9×1.0×10-13,得到 =1.0×10-22,b点
c(H+)=0.1mol/L,故有: =1.0×10-20,C错误;
D.物料守恒可知,c点除了溶液中含硫元素外,沉淀MS中也含硫元素,则c(HS)+c(HS-)
2
+c(S2-)<0.1molL-1,D正确;
故答案为:C。
⋅
7.(2023·陕西榆林·统考模拟预测)常温下,用0. 20 mol∙L−1的NaOH溶液滴定10. 00 mL
0.20 mol∙L−1某二元弱酸的酸式盐NaHX溶液,滴定曲线如图所示。下列说法错误的是A.HX的二级电离常数K ≈5×10−10
2 a2
B.水的电离程度:c>b> a
C.b点溶液中:c(Na+ )>c(X2−)
D.c点溶液中:c(Na+ )=c(HX-) +c(HX)
2
【答案】D
【详解】A.HX的二级电离常数K = ,其中c(H+)≈c(X-)=1×10-5mol∙L−1,
2 a2
c(HX-)≈0.02mol∙L−1,因此K ≈ ,A正确;
a2
B.NaHX溶液呈酸性,说明HX-的电离程度大于水解程度,则NaHX抑制水电离,X2-能
水解而促进水电离,b点溶质为等物质的量浓度的NaX、NaHX,比a点抑制水电离程度小,
2
所以水的电离程度: c> b> a,B正确;
C.b点溶液中存在等物质的量浓度的NaHX和NaX,显然c(Na+ )>c(X2−),C正确;
2
D.c点NaHX和NaOH完全反应,为NaX溶液,根据物料守恒,则c(Na+ )=2[c(HX-)
2
+c(H X)+c(X2-)],D错误;
2
答案选D。
8.(2023·河北唐山·统考二模)已知HA、HB均为一元弱酸,且 ,向20
mL 的NaB溶液中逐滴滴加等浓度的HA溶液,溶液中 与 的
变化关系如图所示:下列说法错误的是
A.
B.pH=7时,
C.滴入HA溶液10 mL时,
D.滴入HA溶液20 mL时,
【答案】D
【详解】A.从图中可以看出,当c(HA)=c(HB)时,c(A-)=10c(B-)。K (HA)= ,
a
K (HB)= ,两式相除得 ,将 、
a
c(HA)=c(HB)、c(A-)=10c(B-)带入可得 ,故A正确;
B. = =10>1,所以 ,故B正
确;
C.滴入HA溶液10 mL时,溶液中有电荷守恒:c(Na)+c(H+)=c(OH-)+c(A-)+c(B-),元素质
量守恒:2c(A-)+2c(HA)=c(Na+)=c(HB)+c(B-),整理可得 ,
故C正确;
D.滴入HA溶液20mL时,NaB和HA恰好完全反应生成等物质的量的NaA和HB,NaA
是强电解质,完全电离,Na+浓度最大,A-水解,HB电离,A-的水解常数为
,HB的电离常数为2×10-4,HB的电离程度大于A-的水解程度,
所以溶液中c(A-)>c(HB),故D错误;
故选D。
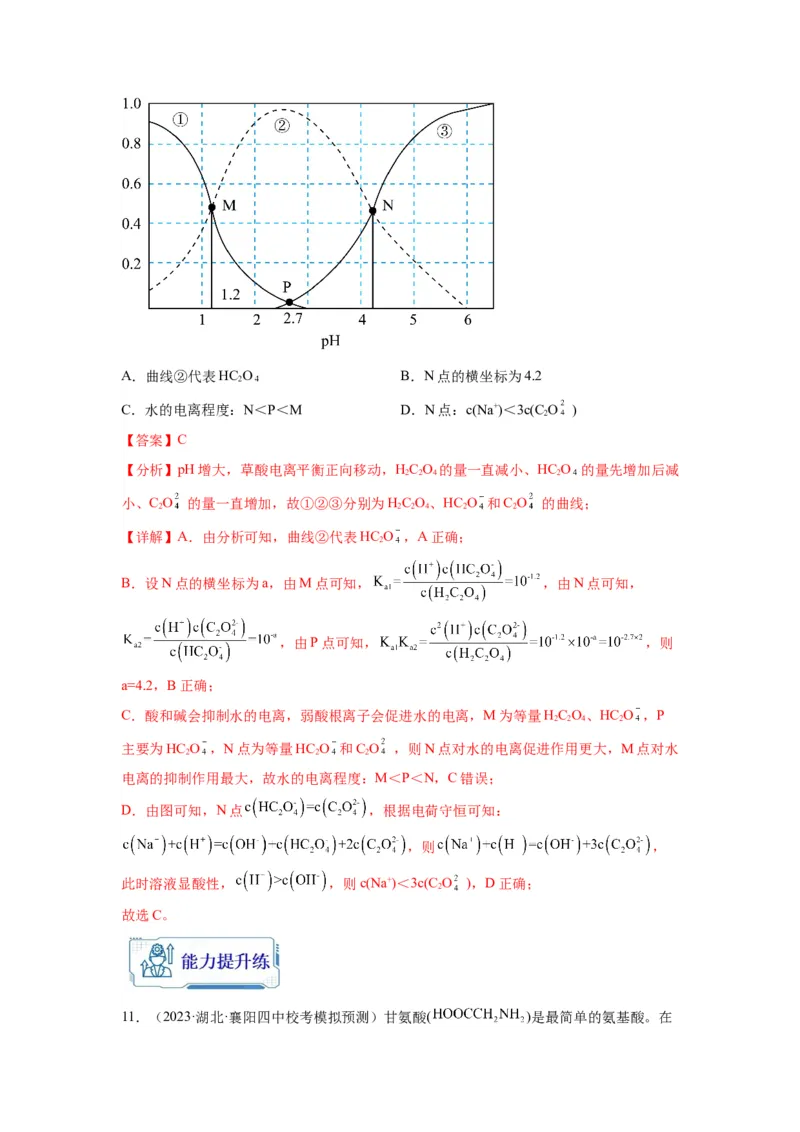
9.(2023·河北张家口·统考三模)25℃时,用 溶液滴定
溶液,加入NaOH溶液的体积、混合溶液中的离子浓度与pH的变
化关系如图所示。下列说法错误的是
A. 的第二步电离常数 的数量级为
B.第一步电离和第二步电离的滴定所选指示剂不同
C.P点溶液中存在
D.M点和N点溶液中 相等
【答案】D
【详解】A. ,由 点可知 ,数量级为 ,
故A正确;
B.由电离常数和水解常数知, 溶液显酸性、 溶液显碱性,第一步滴定选择甲
基橙作指示剂、第二步滴定选择酚酞作指示剂,故B正确;
C. 点为 溶液, 电离程度大于水解,溶液中
,故C正确;
D. 点和 点溶液的 不同,溶液中 不相等,故D错误;
故选D。
10.(2023·安徽宣城·统考一模)草酸HC O 是一种二元弱酸。向草酸溶液中加NaOH,
2 2 4
HC O、HC O 和C O 的分布系数δ与溶液pH的变化关系如图所示。[比如C O 的分
2 2 4 2 2 2
布系数:δ(C O )= ],下列说法不正确的是
2A.曲线②代表HC O B.N点的横坐标为4.2
2
C.水的电离程度:N<P<M D.N点:c(Na+)<3c(C O )
2
【答案】C
【分析】pH增大,草酸电离平衡正向移动,HC O 的量一直减小、HC O 的量先增加后减
2 2 4 2
小、C O 的量一直增加,故①②③分别为HC O、HC O 和C O 的曲线;
2 2 2 4 2 2
【详解】A.由分析可知,曲线②代表HC O ,A正确;
2
B.设N点的横坐标为a,由M点可知, ,由N点可知,
,由P点可知, ,则
a=4.2,B正确;
C.酸和碱会抑制水的电离,弱酸根离子会促进水的电离,M为等量HC O、HC O ,P
2 2 4 2
主要为HC O ,N点为等量HC O 和C O ,则N点对水的电离促进作用更大,M点对水
2 2 2
电离的抑制作用最大,故水的电离程度:M<P<N,C错误;
D.由图可知,N点 ,根据电荷守恒可知:
,则 ,
此时溶液显酸性, ,则c(Na+)<3c(C O ),D正确;
2
故选C。
11.(2023·湖北·襄阳四中校考模拟预测)甘氨酸( )是最简单的氨基酸。在常温下, 、 和 的分布分数[如
与溶液pOH[ ]关系如图。下列说法
正确的是
A.曲线a代表的是
B.甘氨酸的
C.当溶液 时,
D. 的平衡常数
【答案】D
【分析】随着溶液碱性增强, 的量减小, 的量先增加后减
小, 的量增加,故abc分别为 、 、
的曲线;
【详解】A.由分析可知,曲线a代表的是 ,A错误;
B. ,由点(4.22,0.5)可知,
,B错误;
C.由图可知,当溶液 时, ,C错误;
D.由点(11.65,0.5)可知, ,由点(4.22,0.5)
可知, ;
的平衡常数,D正确;
故选D。
12.(2023·浙江·统考模拟预测)亚磷酸(H PO )及其盐在工农业生产中有着重要作用。
3 3
25℃时,已知HPO 溶液中含磷微粒的浓度之和为0.1mol•L-1,溶液中所有含磷微粒的lgc
3 3
-pOH的关系如图所示。已知:pOH表示OH-浓度的负对数[pOH=-lgc(OH-)]。下列说法正
确的是
A.曲线①表示lgc(H PO )随pOH的变化
2
B.pH=4的溶液中:c(HPO )+2c(HPO )=0.1mol•L-1
3 3
C.反应HPO +HPO 2HPO 的平衡常数K=1.0×10-5.3
3 3 2
D.浓度均为0.1mol•L-1的NaHPO 和NaOH的混合液,加水稀释10倍后溶液中
2 3
将增大
【答案】D
【分析】任何pOH下,图中含R物质均有3种,说明HRO 存在二级电离,为二元弱酸;
3 3
随着c(OH-)逐渐增大,pOH减小,根据HRO+OH-= +H O、 +OH-=
3 3 2
+H O,可知c(HRO)逐渐减小,c( )先增大后减小,c( )逐渐增大,故
2 3 3
lgc(H RO)逐渐减小,lgc( )先增大后减小,lgc( )逐渐增大,故曲线①表示c(
3 3
),曲线②表示c( ),曲线③表示c(HRO),据此分析解题。
3 3
【详解】A.由分析可知,曲线②表示c( )随pOH的变化,故A错误;
B.pH=4时,pOH=10,由图可知,此时,lgc(H RO)=lgc( ),即c( )=c(H RO),
3 3 3 3
而c(HRO)+c( )+c( )=0.1 mol•L-1,故2c(HRO)+c( )=0.1 mol•L-1,故B错
3 3 3 3
误;C.根据a点知,c( )=c( )时,pOH=7.3,c(OH-)=10-7.3 mol/L,c(H+)=10-6.7
mol/L,则HRO 的K = =c(H+)=10-6.7,根据c点知,c( )=c(H RO),
3 3 a2 3 3
pOH=12.6,c(OH-)=10-12.6 mol/L,c(H+)=10-1.4 mol/L,则HRO 的K =
3 3 a1
=c(H+)=10-1.4,由HRO +H+减去 +H+,可得HRO+ 2
3 3 3 3
⇌ ⇌ ⇌
,则平衡常数K= =105.3,故C错误;
D.浓度均为0.1mol/L的NaHPO 和NaOH的混合液,加水稀释10倍后溶液碱性减弱,
2 3
c(OH-)减小, 的水解平衡常数不变,根据 可知,该比值增大,
故D正确;
故选:D。
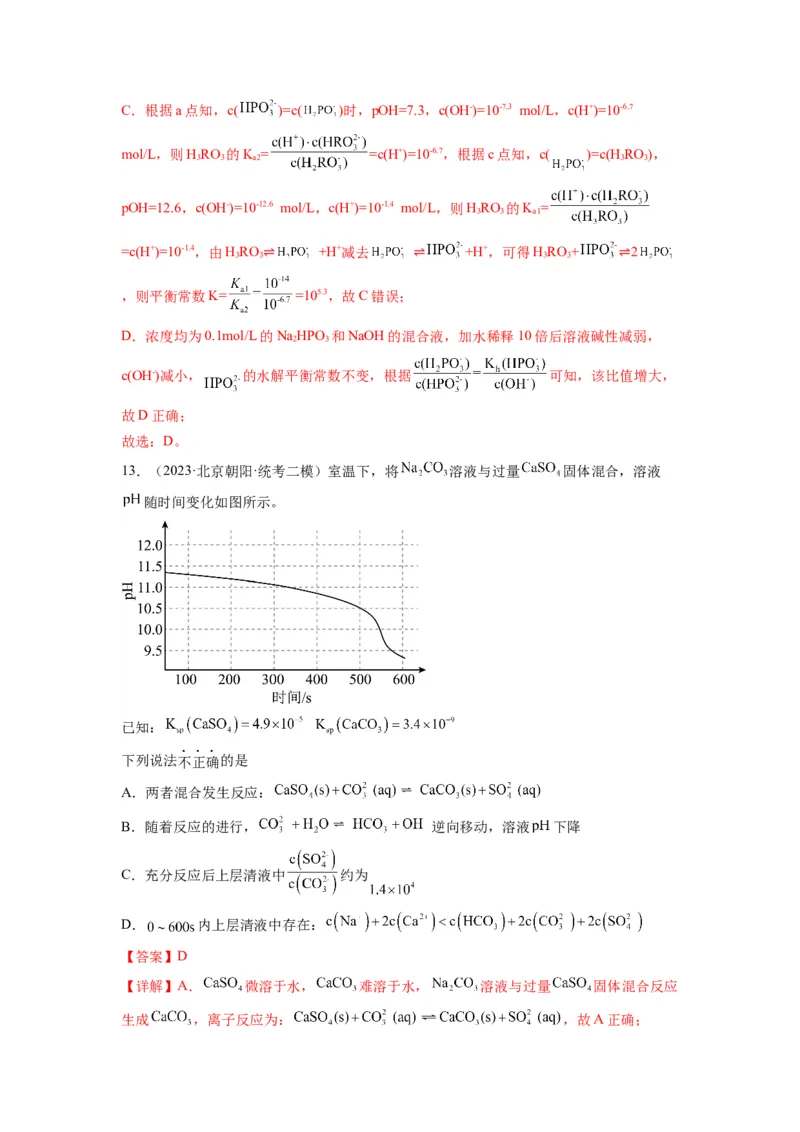
13.(2023·北京朝阳·统考二模)室温下,将 溶液与过量 固体混合,溶液
随时间变化如图所示。
已知:
下列说法不正确的是
A.两者混合发生反应:
B.随着反应的进行, 逆向移动,溶液 下降
C.充分反应后上层清液中 约为
D. 内上层清液中存在:
【答案】D
【详解】A. 微溶于水, 难溶于水, 溶液与过量 固体混合反应
生成 ,离子反应为: ,故A正确;B.随上述反应的进行, 减小,使得 逆向移动,c(
)减小,pH减小,故B正确;
C.充分反应后上层清液为碳酸钙和硫酸钙的饱和溶液,
≈ ,故C正确;
D.根据电荷守恒得: ,
溶液呈碱性, ,则 ,
故D错误;
故选:D。
14.(2023·辽宁·校联考一模)室温下,用 溶液滴定体积均为 未知
浓度的 溶液和 溶液。滴定过程中,溶液的 与相关离子浓度的关系如下图(X代表
A或B),当消耗 溶液时,两溶液 均恰好等于7,下列说法错误的是
A. 的数量级为
B.滴定前浓度:
C.将M、N两点溶液混合,所得溶液中存在
D.水的电离程度:
【答案】B
【详解】A.由图可知 时, 和 的电离平衡常数即等于此时溶液的
,所以 的数量级为 ,A项正确;
B.由A选项可知,酸性:HA>HB;滴定至 时,所用 溶液体积相同,则酸的
酸性越弱,浓度越大,则滴定前浓度: ,B项错误;
C. 时,两溶液中均存在 、 ,将M、N两点溶液混合,
所得溶液中也存在 ,C项正确;D. 越小,水的电离程度越弱,所以水的电离程度: ,D项正确;
答案选B。
15.(2023·辽宁·校联考模拟预测)25℃时,向0.1mol/L的丙三羧酸(用 表示)溶液中
滴加 溶液,如下图所示。
① (分布分数)为某种含A微粒占所有含A微粒的物质的量分数。
②醋酸的
则下列叙述正确的是
A.分别向a、b、c各点代表的溶液中滴加少量酸或碱溶液,溶液的pH变化均较大
B.c点溶液中:
C. 和 的 溶液中 离子的浓度都约为
D.醋酸与少量丙三羧酸钠反应的离子方程式为
【答案】C
【详解】A.a、b、c均存在电离平衡,滴加少量酸或碱溶液引起平衡正向或逆向移动,可
以减弱溶液pH值的变化,因此pH变化不大,故A错误;
B.根据电荷守恒: ,由图可知c
点时 ,则得: ,此时溶液
pH小于7,即 ,则 ,故B错误;
C. ,K = , ,K = ,联
a1 a2
立得:K ·K = ①, 为弱酸,电离程度较低,则平衡时 约等于
a1 a2
起始浓度,多元弱酸电离以第一步电离为主,则氢离子浓度约等于第一步电离出氢离子浓
度,在第一步电离中 ,则 ≈K ②,联立①②得:
a1
≈K ,由b点数据得K = ,则 ≈ ,与 的初始浓度
a2 a2无关,故C正确;
D.当 时,Ka1( )=c(H+)= ,醋酸 ,
= ,则
会同时沉淀,故D错误;
答案选C。
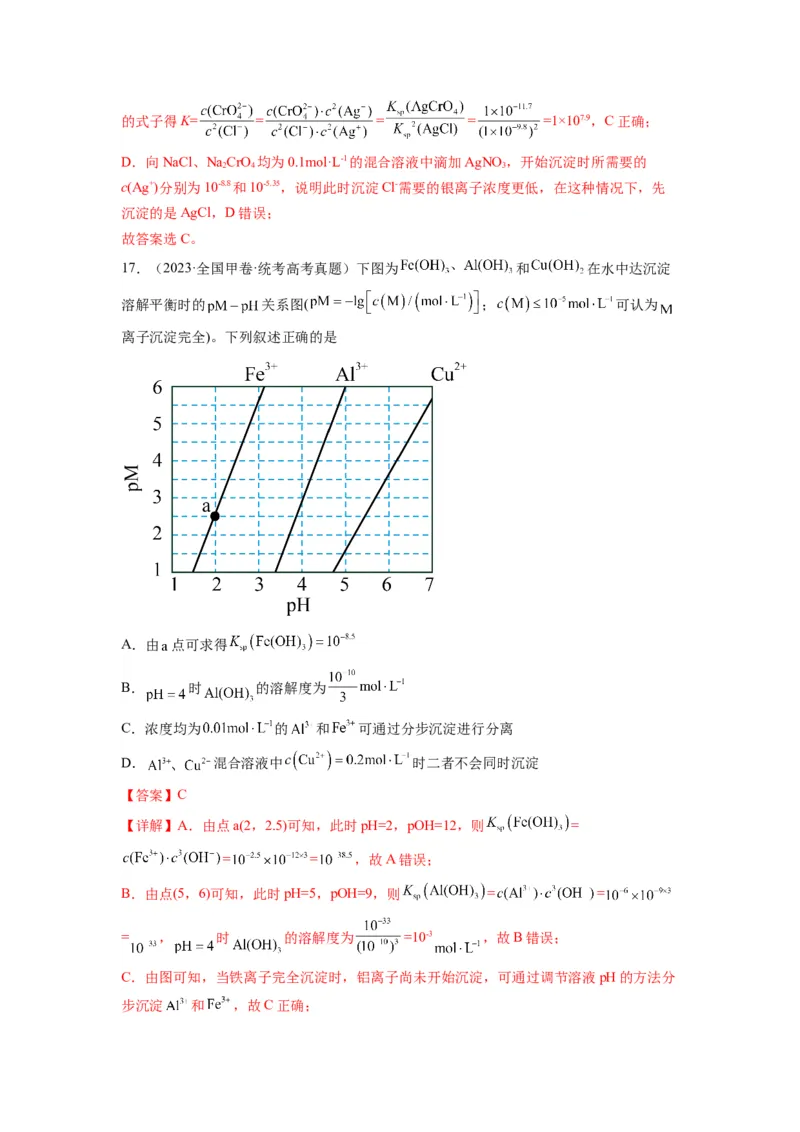
18.(2023·湖南·统考高考真题)常温下,用浓度为 的 标准溶液滴定
浓度均为 的 和 的混合溶液,滴定过程中溶液的 随 (
)的变化曲线如图所示。下列说法错误的是
A. 约为
B.点a:
C.点b:
D.水的电离程度:
【答案】D
【分析】NaOH溶液和HCl、CHCOOH混酸反应时,先与强酸反应,然后再与弱酸反应,
3
由滴定曲线可知,a点时NaOH溶液和HCl恰好完全反应生成NaCl和水,CHCOOH未发
3
生反应,溶质成分为NaCl和CHCOOH;b点时NaOH溶液反应掉一半的CHCOOH,溶
3 3
质成分为NaCl、CHCOOH和 CHCOONa;c点时NaOH溶液与CHCOOH恰好完全反应,
3 3 3
溶质成分为NaCl、CHCOONa;d点时NaOH过量,溶质成分为NaCl、CHCOONa和
3 3
NaOH,据此解答。
【详解】A.由分析可知,a点时溶质成分为NaCl和CHCOOH,
3
c(CHCOOH)=0.0100mol/L,c(H+)=10-3.38mol/L, =
3=10-4.76,故A正确;
B.a点溶液为等浓度的NaCl和CHCOOH混合溶液,存在物料守恒关系
3
c(Na+)=c(Cl-)=c(CH COOH)+c(CH COO-),故B正确;
3 3
C.点b溶液中含有NaCl及等浓度的CHCOOH和 CHCOONa,由于pH<7,溶液显酸性,
3 3
说明CHCOOH的电离程度大于CHCOO-的水解程度,则c(CHCOOH)d,故D错误;
答案选D。
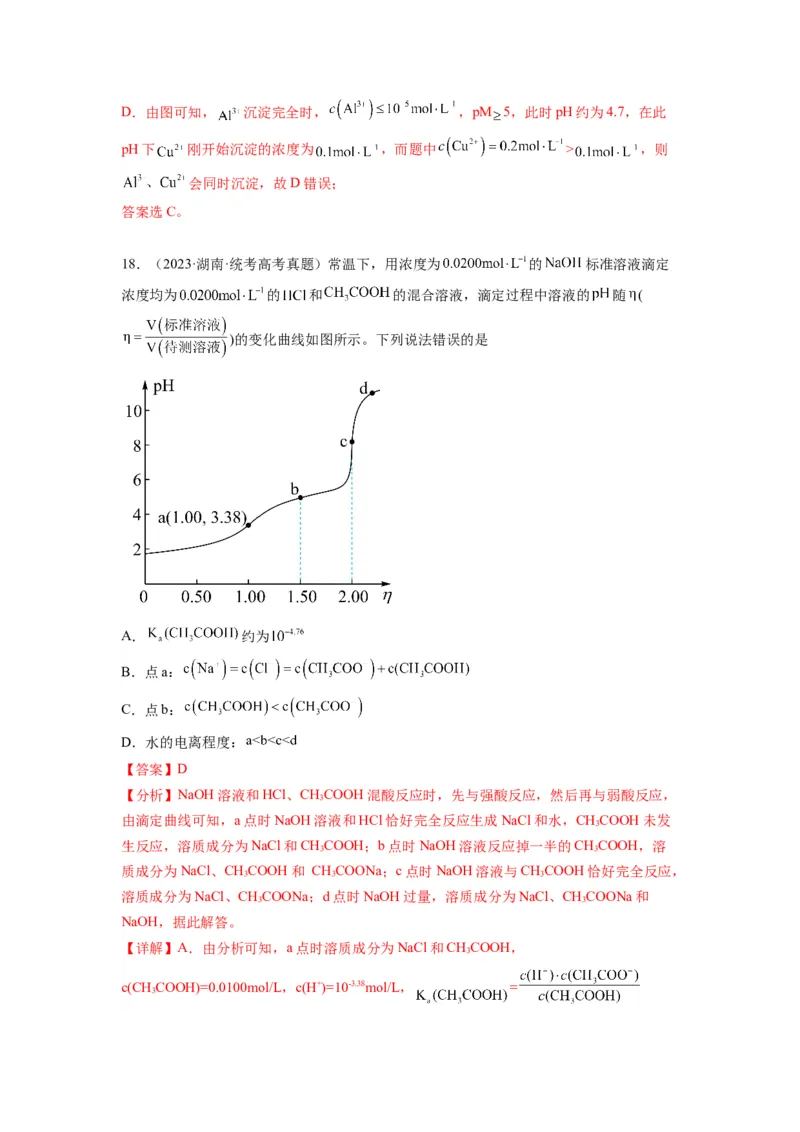
19.(2022·河北·高考真题)某水样中含一定浓度的CO 、HCO 和其他不与酸碱反应的
离子。取10.00mL水样,用0.01000mol•L-1的HCl溶液进行滴定,溶液pH随滴加HCl溶液
体积V(HCl)的变化关系如图(混合后溶液体积变化忽略不计)。
下列说法正确的是
A.该水样中c(CO )=0.01mol•L-1
B.a点处c(H CO)+c(H+)=c(OH—)
2 3
C.当V(HCl)≤20.00mL时,溶液中c(HCO )基本保持不变
D.曲线上任意一点存在c(CO )+c(HCO )+c(H CO)=0.03mol•L-1
2 3
【答案】C
【分析】向碳酸根和碳酸氢根的混合溶液中加入盐酸时,先后发生如下反应CO
+H+=HCO 、HCO +H+= H CO,则滴定时溶液pH会发生两次突跃,第一次突跃时碳酸根
2 3
离子与盐酸恰好反应生成碳酸氢根离子,第二次突跃时碳酸氢根离子与盐酸恰好反应生成
碳酸,由图可知,滴定过程中溶液pH第一次发生突跃时,盐酸溶液的体积为20.00mL,由反应方程式CO +H+=HCO 可知,水样中碳酸根离子的浓度为
=0.02mol/L,溶液pH第二次发生突跃时,盐酸溶液的体积为50.00mL,则水样中碳酸氢根
离子的浓度为 =0.01mol/L。
【详解】A.由分析可知,水样中碳酸根离子的浓度为0.02mol/L,故A错误;
B.由图可知,a点发生的反应为碳酸根离子与氢离子恰好反应生成碳酸氢根离子,可溶性
碳酸氢盐溶液中质子守恒关系为c(H CO)+c(H+)=c(OH—)+ c(CO ),故B错误;
2 3
C.由分析可知,水样中碳酸氢根离子的浓度为0.01mol/L,当盐酸溶液体积
V(HCl)≤20.00mL时,只发生反应CO +H+=HCO ,滴定时溶液中碳酸氢根离子浓度为
=0.01mol/L,则滴定时溶液中碳酸氢根离子
浓度不变,故C正确;
D.由分析可知,水样中碳酸根离子和碳酸氢根离子浓度之和为0.03mol/L,由物料守恒可
知,溶液中c(CO )+c(HCO )+c(H CO)=0.03 mol/L,滴定加入盐酸会使溶液体积增大,则
2 3
溶液中[c(CO )+c(HCO )+c(H CO)]会小于0.03 mol/L,故D错误;
2 3
故选C。
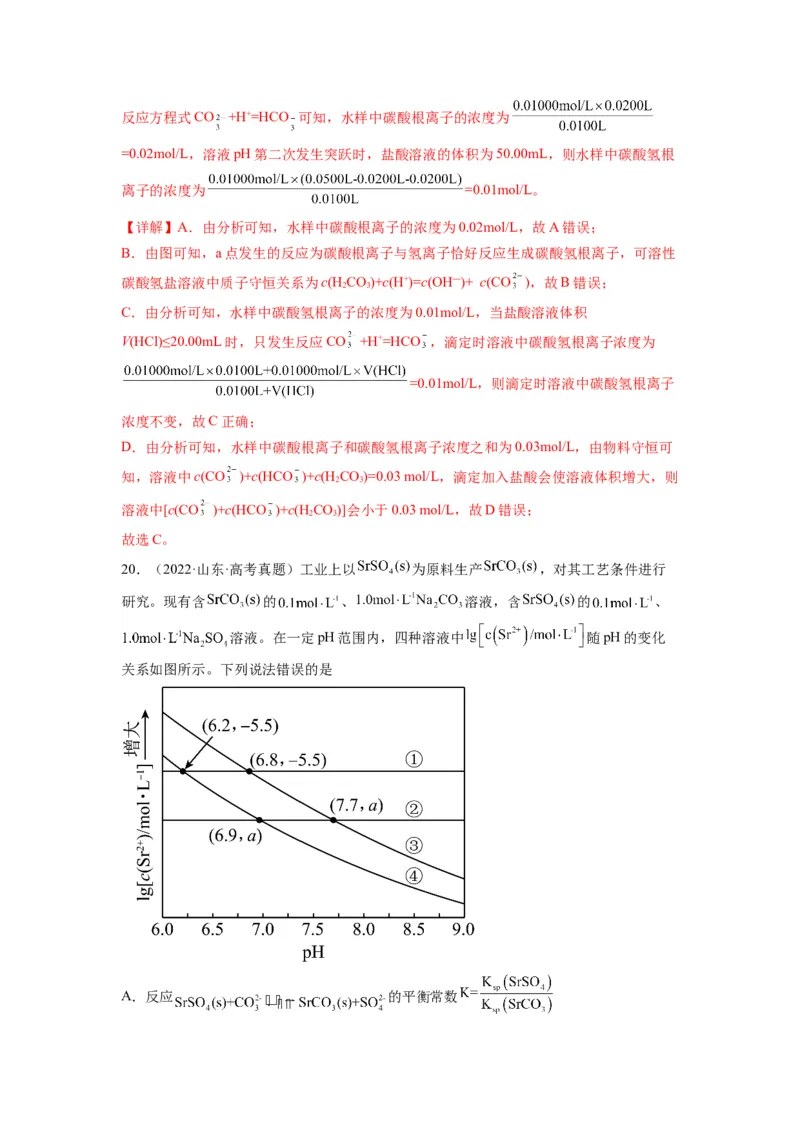
20.(2022·山东·高考真题)工业上以 为原料生产 ,对其工艺条件进行
研究。现有含 的 、 溶液,含 的 、
溶液。在一定pH范围内,四种溶液中 随pH的变化
关系如图所示。下列说法错误的是
A.反应 的平衡常数B.
C.曲线④代表含 的 溶液的变化曲线
D.对含 且 和 初始浓度均为 的混合溶液, 时才
发生沉淀转化
【答案】D
【分析】溶液pH变化,含硫酸锶固体的硫酸钠溶液中锶离子的浓度几乎不变,pH相同时,
溶液中硫酸根离子越大,锶离子浓度越小,所以曲线①代表含硫酸锶固体的0.1mol/L硫酸
钠溶液的变化曲线,曲线②代表含硫酸锶固体的1mol/L硫酸钠溶液的变化曲线;碳酸是弱
酸,溶液pH减小,溶液中碳酸根离子离子浓度越小,锶离子浓度越大,pH相同时,
1mol/L碳酸钠溶液中碳酸根离子浓度大于0.1mol/L碳酸钠溶液,则曲线③表示含碳酸锶固
体的0.1mol/L碳酸钠溶液的变化曲线,曲线④表示含碳酸锶固体的1mol/L碳酸钠溶液的变
化曲线。
【详解】A.反应SrSO (s)+CO SrCO (s)+SO 的平衡常数K= =
4 3
= ,A正确;
B.由分析可知,曲线①代表含硫酸锶固体的0.1mol/L硫酸钠溶液的变化曲线,则硫酸锶
的溶度积K (SrSO )=10—5.5×0.1=10—6.5,温度不变,溶度积不变,则溶液pH为7.7时,锶离
sp 4
子的浓度为 =10—6.5,则a为-6.5,B正确;
C.由分析可知,曲线④表示含碳酸锶固体的1mol/L碳酸钠溶液的变化曲线,C正确;
D.对含SrSO (s)且NaSO 和NaCO 初始浓度均为1.0mol·L-1的混合溶液中锶离子的浓度
4 2 4 2 3
为10-6, 5,根据图示, 锶离子的降低,所以 发生沉淀转化,D错误;
故选D。
21.(2022·湖南·高考真题)室温时,用 的标准 溶液滴定 浓度
相等的 、 和 混合溶液,通过电位滴定法获得 与 的关系曲线如
图所示(忽略沉淀对离子的吸附作用。若溶液中离子浓度小于 时,认为该离
子沉淀完全。 , , )。下列说
法正确的是A.a点:有白色沉淀生成
B.原溶液中 的浓度为
C.当 沉淀完全时,已经有部分 沉淀
D.b点:
【答案】C
【分析】向含浓度相等的 Cl-、 Br-和 I-混合溶液中滴加硝酸银溶液,根据三种沉淀的溶度
积常数,三种离子沉淀的先后顺序为I-、Br-、Cl-,根据滴定图示,当滴入4.50mL硝酸银
溶液时,Cl-恰好沉淀完全,此时共消耗硝酸银的物质的量为4.50mL×10-3L/mL×0.1000mol/
L=4.5×10-4mol,所以Cl-、 Br-和 I-均为1.5×10-4mol。
【详解】A.I-先沉淀,AgI是黄色的,所以a点有黄色沉淀AgI生成,故A错误;
B.原溶液中I-的物质的量为1.5×10-4mol,则I-的浓度为 =0.0100mol⋅L-1,故B
错误;
C.当Br-沉淀完全时(Br-浓度为1.0×10-5mol/L),溶液中的c(Ag+)=
=5.4×10-8mol/L,若Cl-已经开始沉淀,则此时溶液中的c(Cl-)=
=3.3×10-3mol/L,原溶液中的c(Cl-)= c(I-)=0.0100mol⋅L-1,则已经有部分Cl-沉淀,故C正确;
D.b点加入了过量的硝酸银溶液,溶液中的I-、Br-、Cl-全部转化为沉淀,则Ag+浓度最大,
根据溶度积可知,b点各离子浓度为: ,故D错误;
故选C。
22.(2022·浙江·统考高考真题)某同学在两个相同的特制容器中分别加入
20mL0.4mol·L-1NaCO 溶液和40mL0.2mol·L-1NaHCO 溶液,再分别用0.4mol·L-1盐酸滴定,
2 3 3
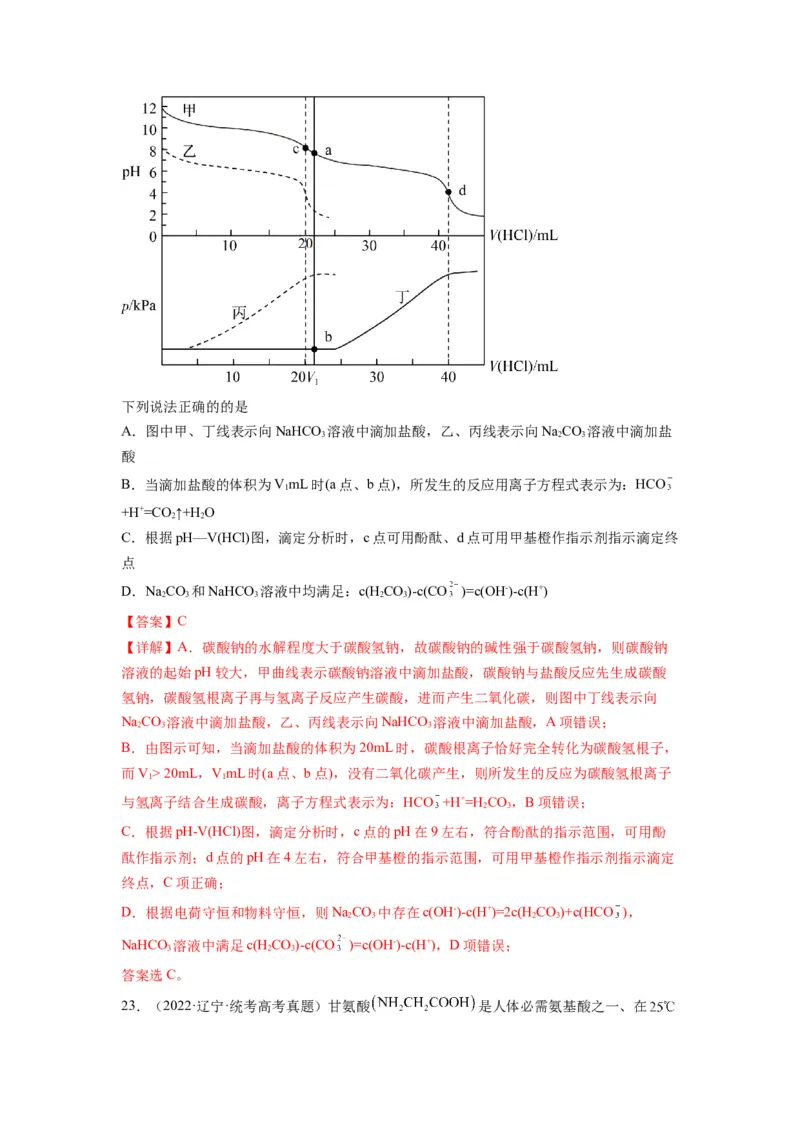
利用pH计和压力传感器检测,得到如图曲线:下列说法正确的的是
A.图中甲、丁线表示向NaHCO 溶液中滴加盐酸,乙、丙线表示向NaCO 溶液中滴加盐
3 2 3
酸
B.当滴加盐酸的体积为VmL时(a点、b点),所发生的反应用离子方程式表示为:HCO
1
+H+=CO ↑+H O
2 2
C.根据pH—V(HCl)图,滴定分析时,c点可用酚酞、d点可用甲基橙作指示剂指示滴定终
点
D.NaCO 和NaHCO 溶液中均满足:c(HCO)-c(CO )=c(OH-)-c(H+)
2 3 3 2 3
【答案】C
【详解】A.碳酸钠的水解程度大于碳酸氢钠,故碳酸钠的碱性强于碳酸氢钠,则碳酸钠
溶液的起始pH较大,甲曲线表示碳酸钠溶液中滴加盐酸,碳酸钠与盐酸反应先生成碳酸
氢钠,碳酸氢根离子再与氢离子反应产生碳酸,进而产生二氧化碳,则图中丁线表示向
NaCO 溶液中滴加盐酸,乙、丙线表示向NaHCO 溶液中滴加盐酸,A项错误;
2 3 3
B.由图示可知,当滴加盐酸的体积为20mL时,碳酸根离子恰好完全转化为碳酸氢根子,
而V> 20mL,VmL时(a点、b点),没有二氧化碳产生,则所发生的反应为碳酸氢根离子
1 1
与氢离子结合生成碳酸,离子方程式表示为:HCO +H+=H CO,B项错误;
2 3
C.根据pH-V(HCl)图,滴定分析时,c点的pH在9左右,符合酚酞的指示范围,可用酚
酞作指示剂;d点的pH在4左右,符合甲基橙的指示范围,可用甲基橙作指示剂指示滴定
终点,C项正确;
D.根据电荷守恒和物料守恒,则NaCO 中存在c(OH-)-c(H+)=2c(H CO)+c(HCO ),
2 3 2 3
NaHCO 溶液中满足c(HCO)-c(CO )=c(OH-)-c(H+),D项错误;
3 2 3
答案选C。
23.(2022·辽宁·统考高考真题)甘氨酸 是人体必需氨基酸之一、在时, 、 和 的分布分数【如
】与溶液 关系如图。下列说法错误的是
A.甘氨酸具有两性
B.曲线c代表
C. 的平衡常数
D.
【答案】D
【详解】A. 中存在 和-COOH,所以溶液既有酸性又有碱性,故A正
确;
B.氨基具有碱性,在酸性较强时会结合氢离子,羧基具有酸性,在碱性较强时与氢氧根
离子反应,故曲线a表示 的分布分数随溶液pH的变化,曲b表示
的分布分数随溶液pH的变化,曲线c表示 的分布分数随溶液
pH的变化,故B正确;
C. 的平衡常数
, 时,根据a,b曲线交点坐标 可知,
时, ,则 ,故C
正确;
D.由C项分析可知, ,根据b,c曲线交点坐标坐标
分析可得电离平衡 的电离常数为K= , ,则
1
,即
,故D错误;
故答案选D。
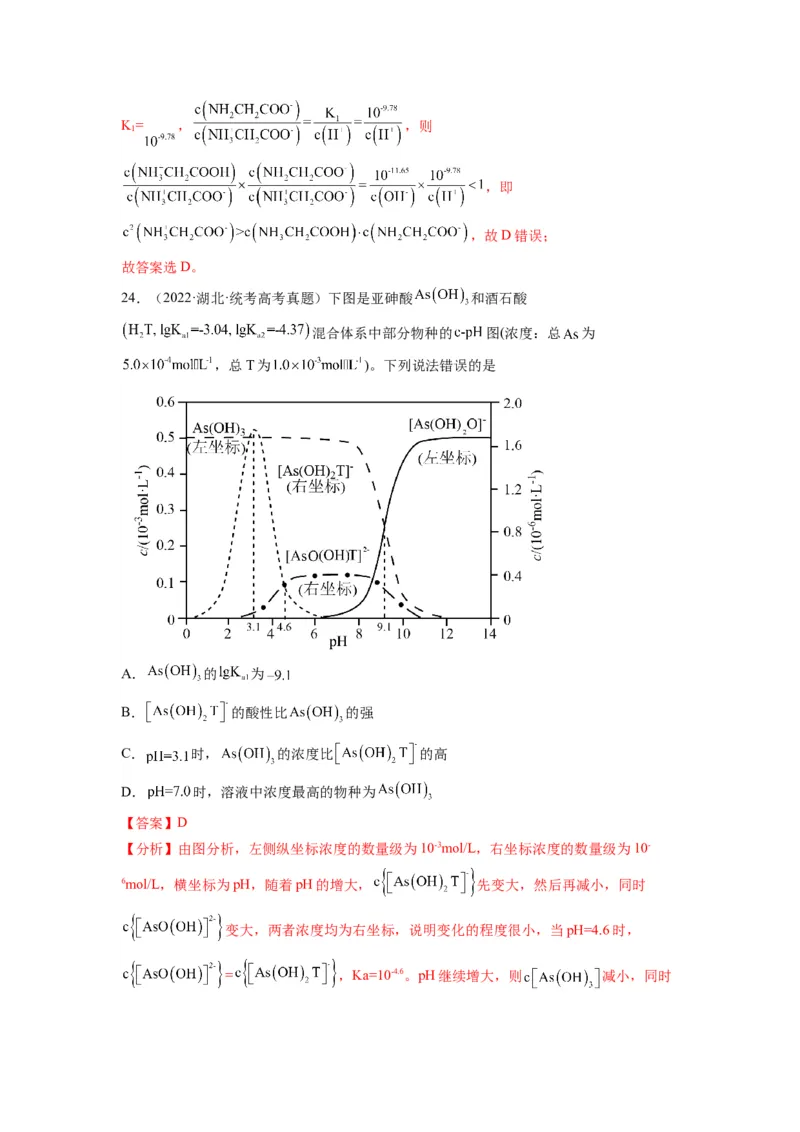
24.(2022·湖北·统考高考真题)下图是亚砷酸 和酒石酸
混合体系中部分物种的 图(浓度:总 为
,总T为 )。下列说法错误的是
A. 的 为
B. 的酸性比 的强
C. 时, 的浓度比 的高
D. 时,溶液中浓度最高的物种为
【答案】D
【分析】由图分析,左侧纵坐标浓度的数量级为10-3mol/L,右坐标浓度的数量级为10-
6mol/L,横坐标为pH,随着pH的增大, 先变大,然后再减小,同时
变大,两者浓度均为右坐标,说明变化的程度很小,当pH=4.6时,
= ,Ka=10-4.6。pH继续增大,则 减小,同时增大,当pH=9.1时, = ,
,二者用左坐标表示,浓度比较大,说明变化的幅度比较大,但混合溶
液中存在着酒石酸,电离常数远大于亚砷酸,且总T浓度也大于总As。
【详解】A. , ,当pH=9.1
时, = , , 为 ,A正确;
B. ,当pH=4.6时,
= ,Ka=10-4.6,而由A选项计算得HAsO 的
3 3
,即Ka > Ka1,所以 的酸性比 的强,B正确;
C.由图可知 的浓度为左坐标,浓度的数量级为10-3mol/L, 的浓度
为右坐标,浓度的数量级为10-6mol/L,所以 时, 的浓度比
的高,C正确;
D.由可知条件,酒石酸 , 的 为 ,即酒
石酸的第一部电离常数远大于亚砷酸的第一步电离常数,所以酒石酸的酸性远强于
,另外总As的浓度也小于总T的浓度,所以当 时,溶液中浓度最高的物
种不是 ,D错误;
故选D。
25.(2022·海南·统考高考真题)某元素M的氢氧化物 在水中的溶解反应为:
、 ,25℃,-lgc
与pH的关系如图所示,c为 或 浓度的值。下列说法错误的是A.曲线①代表 与pH的关系
B. 的 约为
C.向 的溶液中加入NaOH溶液至pH=9.0,体系中元素M主要以
存在
D.向 的溶液中加入等体积0.4mol/L的HCl后,体系中元素M主
要以 存在
【答案】BD
【分析】由题干信息,M(OH) (s) M2+(aq)+2OH-(aq),M(OH) (s)+2OH-(aq) M(OH)
2 2
(aq),随着pH增大,c(OH-)增大,则c(M2+)减小,c[M(OH) ]增大,即-lg c(M2+)增大,-lg
c[M(OH) ]减小,因此曲线①代表-lg c(M2+)与pH的关系,曲线②代表-lg c[M(OH) ]与pH
的关系,据此分析解答。
【详解】A.由分析可知,曲线①代表-lg c(M2+)与pH的关系,A正确;
B.由图象,pH=7.0时,-lg c(M2+)=3.0,则M(OH) 的K =c(M2+)·c2(OH-)=1×10-17,B错误;
2 sp
C.向c(M2+)=0.1mol/L的溶液中加入NaOH溶液至pH=9.0,根据图象,pH=9.0时,
c(M2+)、c[M(OH) ]均极小,则体系中元素M主要以M(OH) (s)存在,C正确;
2
D.根据图象,c[M(OH) ]=0.1mol/L时溶液的pH约为14.5,c(OH-)≈ mol/
L≈3.2mol/L,加入等体积的0.4mol/L的HCl后,发生中和反应,反应后c (OH-)=
mol/L=1.4mol/L,此时体系中元素M仍主要以M(OH) 存在,D错误;
答案选BD。