文档内容
第 20 讲 化学反应速率
目录
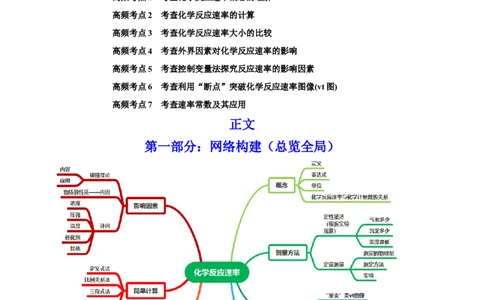
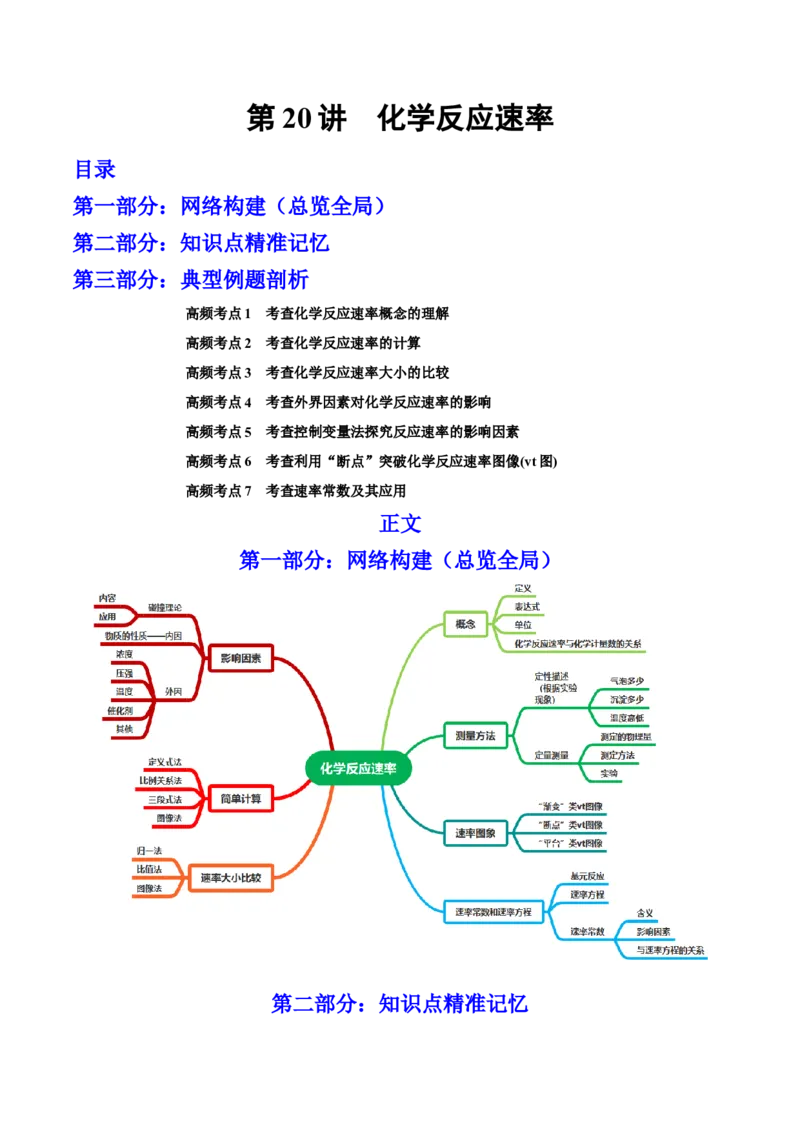
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
第三部分:典型例题剖析
高频考点1 考查化学反应速率概念的理解
高频考点2 考查化学反应速率的计算
高频考点3 考查化学反应速率大小的比较
高频考点4 考查外界因素对化学反应速率的影响
高频考点5 考查控制变量法探究反应速率的影响因素
高频考点6 考查利用“断点”突破化学反应速率图像(vt图)
高频考点7 考查速率常数及其应用
正文
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆知识点一 化学反应速率的概念及计算
1.表示方法
通常用单位时间内反应物浓度的减少或生成物浓度的增加来表示。
2.数学表达式及单位
v=,单位为 mol·L - 1 ·min - 1 或 mol·L - 1 ·s - 1 。
3.化学反应速率与化学计量数的关系
同一反应在同一时间内,用不同物质来表示的反应速率可能不同,但反应速率的数值之比等于这些物质在
化学方程式中的化学计量数之比。
如在反应aA(g)+bB(g) cC(g)+dD(g)中,存在v(A)∶v(B)∶v(C)∶v(D)=a∶b∶c∶d
【特别提醒】(1)一般不用固体或纯液体物质表示化学反应速率。
(2)由v=计算得到的是一段时间内的平均速率,用不同物质表示时,其数值可能不同,但意义相同。
(3)化学反应速率一般指反应的平均速率而不是瞬时速率,且无论用反应物表示还是用生成物表示均取正值。
知识点二 影响化学反应速率的因素
1.内因:反应物本身的性质是主要因素。如相同条件下Mg、Al与稀盐酸反应的速率大小关系为 Mg >
Al。
2.外因
【特别提醒】(1)压强对反应速率的影响是通过改变浓度来实现的,浓度不变,速率不变。
(2)温度改变,化学反应速率一定改变。
(3)不特别指明,催化剂一般是加快化学反应速率。
(4)固体反应物量的增减,不能改变化学反应速率,固体的表面积改变才能改变化学反应速率。
3.理论解释——有效碰撞理论
(1)活化分子、活化能、有效碰撞
①活化分子:能够发生有效碰撞的分子。
②活化能:如图
图中:E 为正反应的活化能,使用催化剂时的活化能为E,反应热为E - E 。(注:E 为逆反应的活化能)
1 3 1 2 2③有效碰撞:活化分子之间能够引发化学反应的碰撞。
(2)活化分子、有效碰撞与反应速率的关系
【特别提醒】(1)由于固体和纯液体的浓度可视为常数,故改变其用量反应速率不变。但当固体颗粒变小时,
其表面积增大将导致反应速率增大。
(2)压强对化学反应速率的影响是通过改变反应物浓度实现的,所以分析压强的改变对反应速率的影响时,
要从反应物浓度是否发生改变的角度来分析。若改变总压强而各物质的浓度不改变,则反应速率不变。
(3)改变温度,使用催化剂,反应速率一定发生变化,其他外界因素的改变,反应速率则不一定发生变化。
(4)其他条件一定,升高温度,不论正反应还是逆反应,不论放热反应还是吸热反应,反应速率都要增大,
只不过正、逆反应速率增加的程度不同。
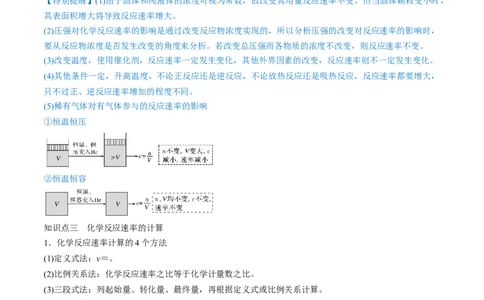
(5)稀有气体对有气体参与的反应速率的影响
①恒温恒压
②恒温恒容
知识点三 化学反应速率的计算
1.化学反应速率计算的4个方法
(1)定义式法:v=。
(2)比例关系法:化学反应速率之比等于化学计量数之比。
(3)三段式法:列起始量、转化量、最终量,再根据定义式或比例关系计算。
(4)依据图像求反应速率的步骤
第一步:找出横、纵坐标对应的物质的量;
第二步:将图中的变化量转化成相应的浓度变化量;
第三步:根据公式v=进行计算。
2.化学反应速率计算的万能方法——三段式法
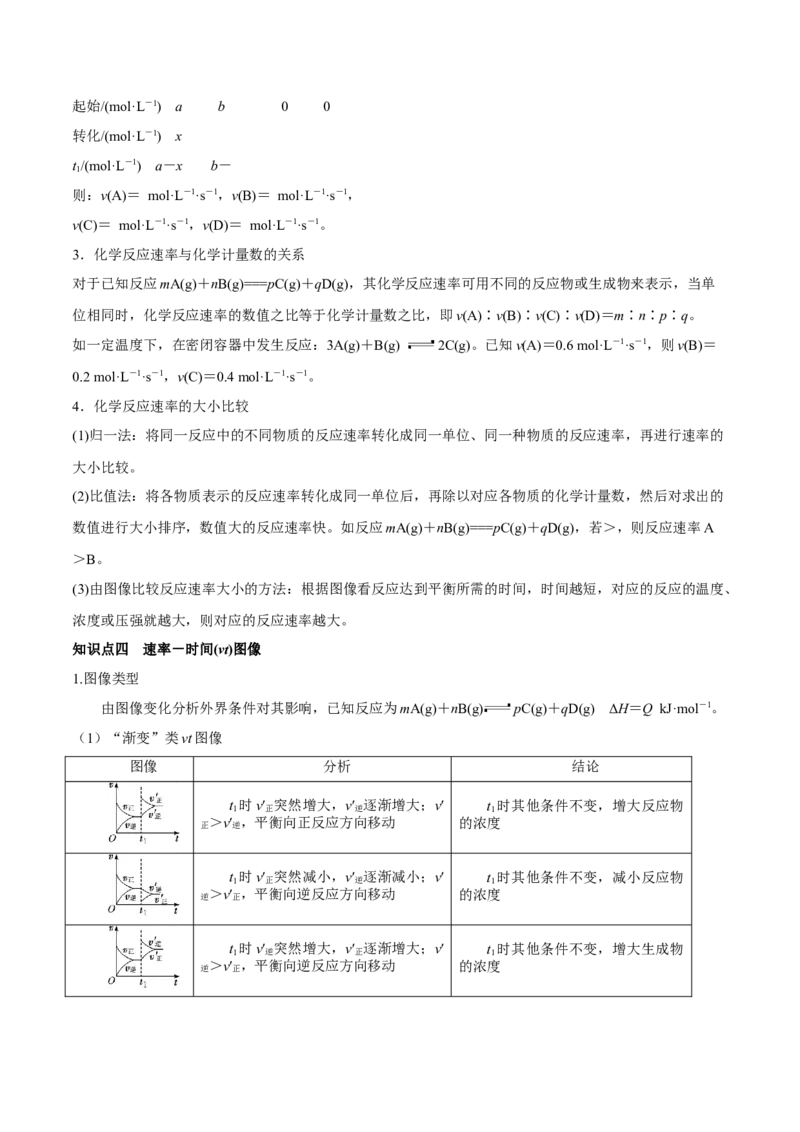
对于反应mA(g)+nB(g) pC(g)+qD(g),起始时A的浓度为a mol·L-1,B的浓度为b mol·L-1,反应
进行至ts时,A消耗了x mol·L-1,则化学反应速率可计算如下:
1
mA(g)+nB(g) pC(g)+qD(g)起始/(mol·L-1) a b 0 0
转化/(mol·L-1) x
t/(mol·L-1) a-x b-
1
则:v(A)= mol·L-1·s-1,v(B)= mol·L-1·s-1,
v(C)= mol·L-1·s-1,v(D)= mol·L-1·s-1。
3.化学反应速率与化学计量数的关系
对于已知反应mA(g)+nB(g)===pC(g)+qD(g),其化学反应速率可用不同的反应物或生成物来表示,当单
位相同时,化学反应速率的数值之比等于化学计量数之比,即v(A)∶v(B)∶v(C)∶v(D)=m∶n∶p∶q。
如一定温度下,在密闭容器中发生反应:3A(g)+B(g) 2C(g)。已知v(A)=0.6 mol·L-1·s-1,则v(B)=
0.2 mol·L-1·s-1,v(C)=0.4 mol·L-1·s-1。
4.化学反应速率的大小比较
(1)归一法:将同一反应中的不同物质的反应速率转化成同一单位、同一种物质的反应速率,再进行速率的
大小比较。
(2)比值法:将各物质表示的反应速率转化成同一单位后,再除以对应各物质的化学计量数,然后对求出的
数值进行大小排序,数值大的反应速率快。如反应mA(g)+nB(g)===pC(g)+qD(g),若>,则反应速率A
>B。
(3)由图像比较反应速率大小的方法:根据图像看反应达到平衡所需的时间,时间越短,对应的反应的温度、
浓度或压强就越大,则对应的反应速率越大。
知识点四 速率-时间(vt)图像
1.图像类型
由图像变化分析外界条件对其影响,已知反应为mA(g)+nB(g ) pC(g)+qD(g) ΔH=Q kJ·mol-1。
(1)“渐变”类vt图像
图像 分析 结论
t 时v′ 突然增大,v′ 逐渐增大;v′ t 时其他条件不变,增大反应物
1 正 逆 1
>v′ ,平衡向正反应方向移动 的浓度
正 逆
t 时v′ 突然减小,v′ 逐渐减小;v′ t 时其他条件不变,减小反应物
1 正 逆 1
>v′ ,平衡向逆反应方向移动 的浓度
逆 正
t 时v′ 突然增大,v′ 逐渐增大;v′ t 时其他条件不变,增大生成物
1 逆 正 1
>v′ ,平衡向逆反应方向移动 的浓度
逆 正t 时v′ 突然减小,v′ 逐渐减小;v′ t 时其他条件不变,减小生成物
1 逆 正 1
>v′ ,平衡向正反应方向移动 的浓度
正 逆
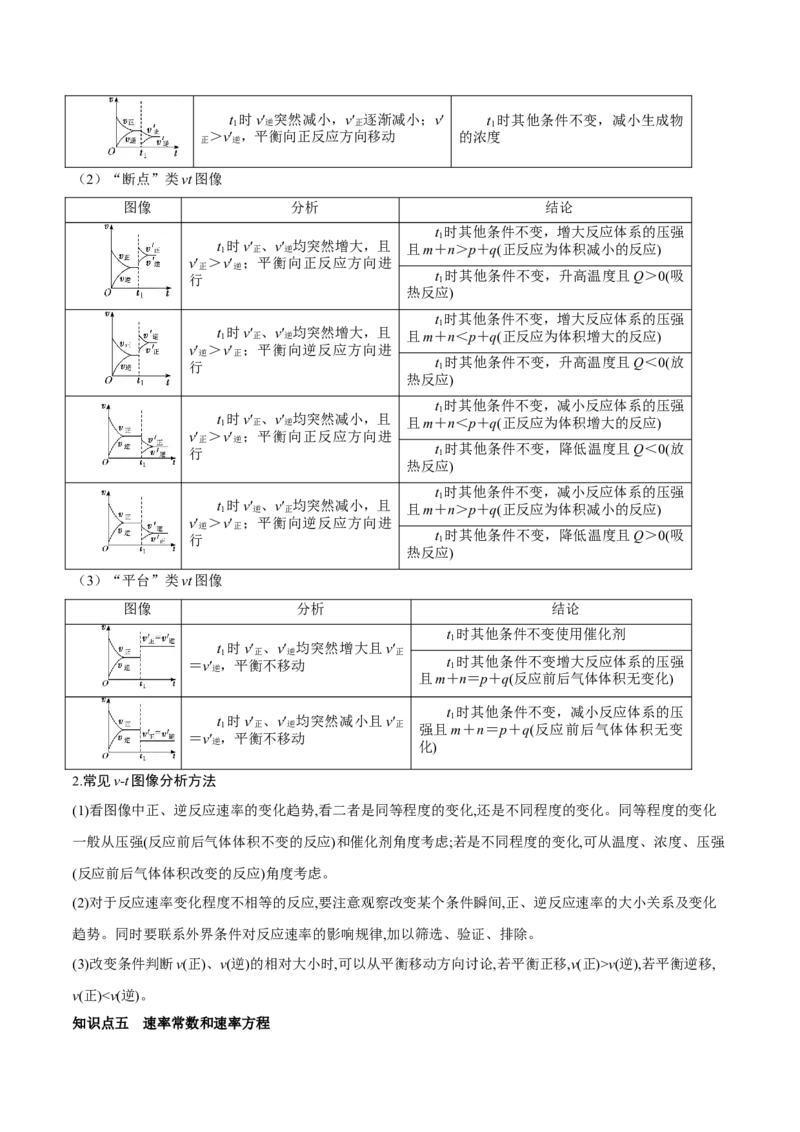
(2)“断点”类vt图像
图像 分析 结论
t 时其他条件不变,增大反应体系的压强
1
t 1 时v′ 正 、v′ 逆 均突然增大,且 且m+n>p+q(正反应为体积减小的反应)
v′ >v′ ;平衡向正反应方向进
正 逆
行 t 1 时其他条件不变,升高温度且Q>0(吸
热反应)
t 时其他条件不变,增大反应体系的压强
1
t 1 时v′ 正 、v′ 逆 均突然增大,且 且m+n<p+q(正反应为体积增大的反应)
v′ >v′ ;平衡向逆反应方向进
逆 正
行 t 1 时其他条件不变,升高温度且Q<0(放
热反应)
t 时其他条件不变,减小反应体系的压强
1
t 1 时v′ 正 、v′ 逆 均突然减小,且 且m+n<p+q(正反应为体积增大的反应)
v′ >v′ ;平衡向正反应方向进
正 逆
行 t 1 时其他条件不变,降低温度且Q<0(放
热反应)
t 时其他条件不变,减小反应体系的压强
1
t 1 时v′ 逆 、v′ 正 均突然减小,且 且m+n>p+q(正反应为体积减小的反应)
v′ >v′ ;平衡向逆反应方向进
逆 正
行 t 1 时其他条件不变,降低温度且Q>0(吸
热反应)
(3)“平台”类vt图像
图像 分析 结论
t 时其他条件不变使用催化剂
1
t 时v′ 、v′ 均突然增大且v′
1 正 逆 正
=v′ 逆 ,平衡不移动 t 1 时其他条件不变增大反应体系的压强
且m+n=p+q(反应前后气体体积无变化)
t 时其他条件不变,减小反应体系的压
t 时v′ 、v′ 均突然减小且v′ 1
1 正 逆 正 强且m+n=p+q(反应前后气体体积无变
=v′ ,平衡不移动
逆 化)
2.常见v-t图像分析方法
(1)看图像中正、逆反应速率的变化趋势,看二者是同等程度的变化,还是不同程度的变化。同等程度的变化
一般从压强(反应前后气体体积不变的反应)和催化剂角度考虑;若是不同程度的变化,可从温度、浓度、压强
(反应前后气体体积改变的反应)角度考虑。
(2)对于反应速率变化程度不相等的反应,要注意观察改变某个条件瞬间,正、逆反应速率的大小关系及变化
趋势。同时要联系外界条件对反应速率的影响规律,加以筛选、验证、排除。
(3)改变条件判断v(正)、v(逆)的相对大小时,可以从平衡移动方向讨论,若平衡正移,v(正)>v(逆),若平衡逆移,
v(正)0
B.反应Ⅰ,在0~20min时的平均反应速率v(H )=0.15mol•L-1•min-1
2
C.反应Ⅰ达到平衡时,加入1molCO 和1molCH OH,此时平衡不移动
2 3
D.起始温度相同的反应Ⅰ、Ⅱ,平衡时平衡常数K也相同
【变式训练2】(依据图像计算)(2020·全国·高三专题练习)一定温度下,把6 mol A和5 mol B通入容
积为4L的恒容密闭容器中发生反应3A(g)+B(g) 2C(g)+2D(g),反应经过5min达到平衡,此时生成2 mol C,正反应速率(v )和逆反应速率(v )随时间(t)的变化如图所示。下列说法正确的是
正 逆
A.t=5min,平衡时3v (A)=2v (D)
2 正 逆
B.0~t,A的平均反应速率为0.15 mol·L-1·min-1
2
C.t~t,各物质的浓度一定相等
2 3
D.B的平衡转化率为25%
【变式训练3】(依据化学方程式计算)(2021·浙江高三二模)利用催化剂将尾气中的NO和CO转变成
CO 和N,是尾气处理的一种方法,方程式为: 。为测定在某种催化剂作用下
2 2
的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
时间(s) 0 1 2 3 4 5
下列说法不正确的是;A.该反应能自发进行,则反应的
B.前2s内的平均反应速率
C.在该温度下,反应的平衡常数K=500
D.在密闭容器中发生上述反应,缩小容积能提高NO转化率
高频考点3 考查化学反应速率大小的比较
例3.(2022·全国·高三专题练习)对于可逆反应A(g)+3B(s) 2C(g)+2D(g),在不同条件下的化学反应速
率如下,其中表示的反应速率最快的是
A.v(A)=0.5mol·L-1·min-1 B.v(B)=1.2mol·L-1·s-1
C.v(D)=0.4mol·L-1·min-1 D.v(C)=0.1mol·L-1·s-1
【规律总结】定量法比较化学反应速率的大小
(1)归一法:按照化学计量数关系换算成同一物质、同一单位表示,再比较数值大小。
(2)比值法:比较化学反应速率与化学计量数的比值。如 aA(g)+bB(g) cC(g),即比较与,若>,则用A表示时的反应速率比用B表示时大。
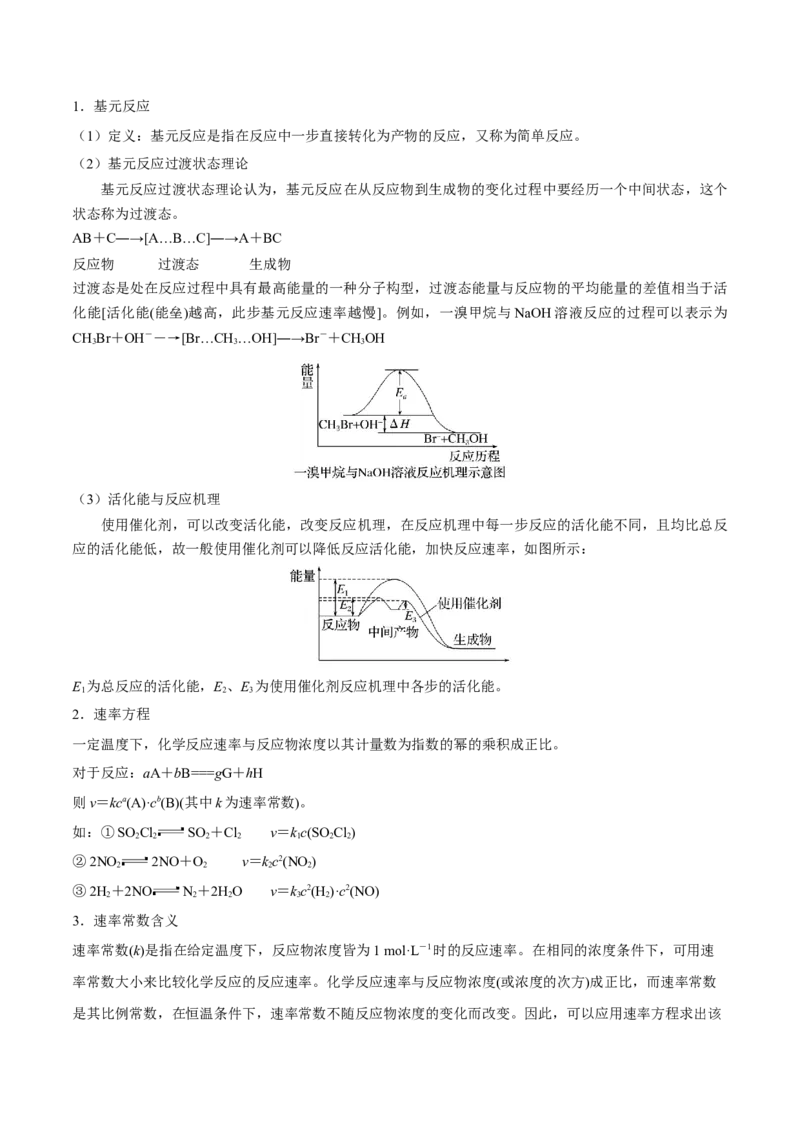
【变式训练】(根据图像判断某点反应速率的大小)(2021·浙江高三) 温度下,向2L真空密闭容器中
加入 固体,发生反应: (未配平),反应过程如图,下列说法正确的是
A.X可能为
B. 用 表示的反应速率为
C.第2min时逆反应速率大于第4min时逆反应速率
D.第4min时,保持温度和容积不变,向容器中再加入 ,混合气体颜色加深
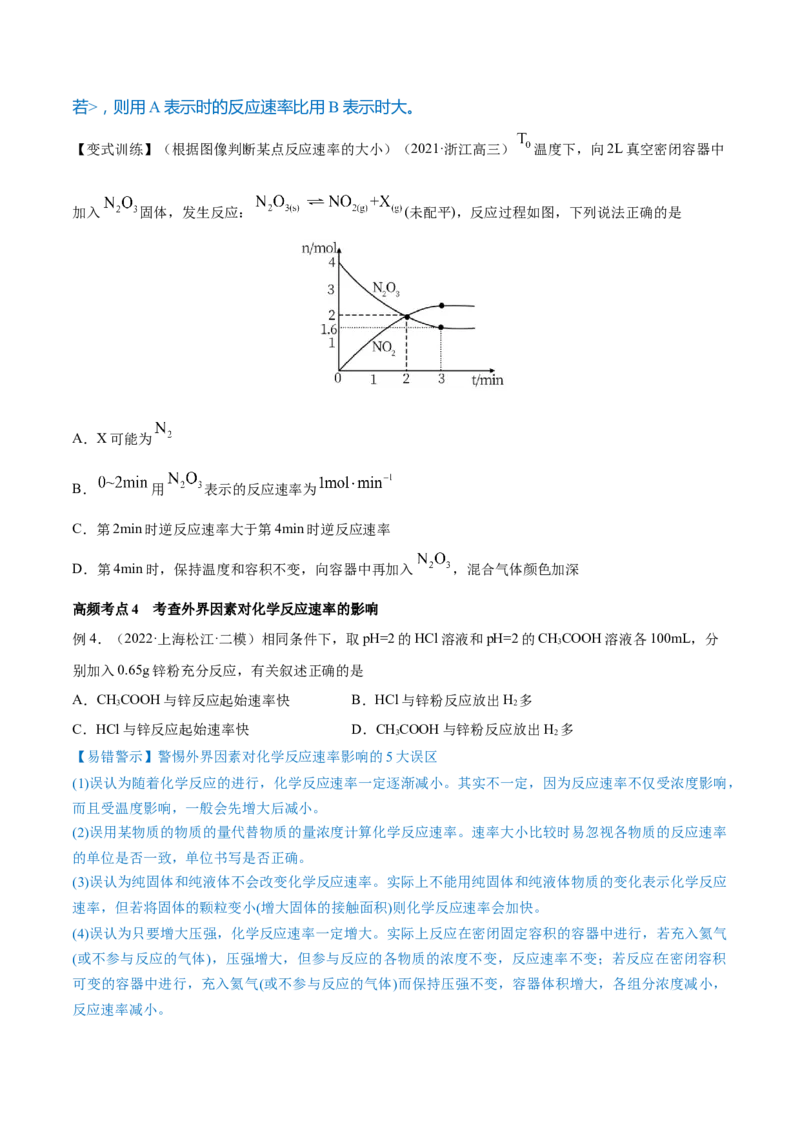
高频考点4 考查外界因素对化学反应速率的影响
例4.(2022·上海松江·二模)相同条件下,取pH=2的HCl溶液和pH=2的CHCOOH溶液各100mL,分
3
别加入0.65g锌粉充分反应,有关叙述正确的是
A.CHCOOH与锌反应起始速率快 B.HCl与锌粉反应放出H 多
3 2
C.HCl与锌反应起始速率快 D.CHCOOH与锌粉反应放出H 多
3 2
【易错警示】警惕外界因素对化学反应速率影响的5大误区
(1)误认为随着化学反应的进行,化学反应速率一定逐渐减小。其实不一定,因为反应速率不仅受浓度影响,
而且受温度影响,一般会先增大后减小。
(2)误用某物质的物质的量代替物质的量浓度计算化学反应速率。速率大小比较时易忽视各物质的反应速率
的单位是否一致,单位书写是否正确。
(3)误认为纯固体和纯液体不会改变化学反应速率。实际上不能用纯固体和纯液体物质的变化表示化学反应
速率,但若将固体的颗粒变小(增大固体的接触面积)则化学反应速率会加快。
(4)误认为只要增大压强,化学反应速率一定增大。实际上反应在密闭固定容积的容器中进行,若充入氦气
(或不参与反应的气体),压强增大,但参与反应的各物质的浓度不变,反应速率不变;若反应在密闭容积
可变的容器中进行,充入氦气(或不参与反应的气体)而保持压强不变,容器体积增大,各组分浓度减小,
反应速率减小。(5)误认为温度、压强等条件的改变对正、逆反应速率影响不一致。如认为升温既然使化学平衡向吸热方向
移动,则对于放热反应,升温时,逆反应速率增大,而正反应速率减小。其实不然,温度升高,正、逆反
应速率都增大,只是吸热反应方向速率增大程度大;同理,降温会使吸热反应方向速率减小程度大,而导
致化学平衡向放热方向移动。
【变式训练】(2021·陕西咸阳市·高三一模)氨的工业合成对工农业生产具有划时代意义。在容积固定的
密闭容器中充入一定量的 和 ,一定条件下发生反应 。下
列有关叙述正确的是
A.相同条件下,
B.温度不变时,向容器中充入氦气,反应速率加快
C.升高温度,正反应速率减小,平衡向逆反应方向移动
D.增大 的浓度,能提高 的转化率
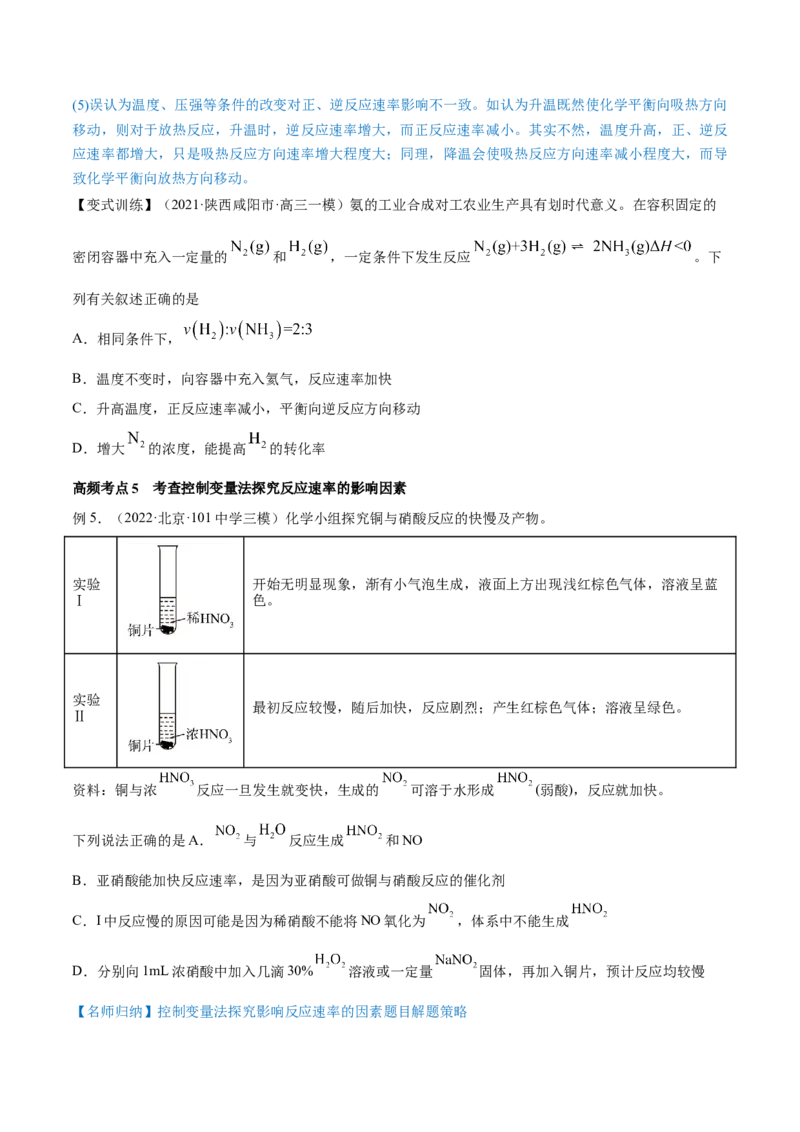
高频考点5 考查控制变量法探究反应速率的影响因素
例5.(2022·北京·101中学三模)化学小组探究铜与硝酸反应的快慢及产物。
实验 开始无明显现象,渐有小气泡生成,液面上方出现浅红棕色气体,溶液呈蓝
Ⅰ 色。
实验
最初反应较慢,随后加快,反应剧烈;产生红棕色气体;溶液呈绿色。
Ⅱ
资料:铜与浓 反应一旦发生就变快,生成的 可溶于水形成 (弱酸),反应就加快。
下列说法正确的是A. 与 反应生成 和NO
B.亚硝酸能加快反应速率,是因为亚硝酸可做铜与硝酸反应的催化剂
C.I中反应慢的原因可能是因为稀硝酸不能将NO氧化为 ,体系中不能生成
D.分别向1mL浓硝酸中加入几滴30% 溶液或一定量 固体,再加入铜片,预计反应均较慢
【名师归纳】控制变量法探究影响反应速率的因素题目解题策略(1)确定变量:理清影响实验探究结果的所有因素。
(2)定多变一:在探究时,先确定其他的因素不变,只变化一种因素,看这种因素与探究的问题存在怎样的
关系;这样确定一种以后,再确定另一种,通过分析每种因素与所探究问题之间的关系,得出所有影响因
素与所探究问题之间的关系。
(3)数据有效:解答时注意选择数据(或设置实验)要有效,且变量统一,否则无法作出正确判断。
【变式训练】(2021·山东滨州市·高三二模)某同学为探究浓度对化学反应速率的影响,设计以下实验。
① ② ③ ④
1mL0.01mol/L酸性高 1mL0.01mol/L酸性 1mL0.01mol/L酸性 1mL0.01mol/L酸性高
试剂a
锰酸钾水溶液 高锰酸钾水溶液 高锰酸钾水溶液 锰酸钾水溶液
1mL以浓盐酸为溶剂
试剂b 2mL0.1mol/LH 2 C 2 O 4 水 2mL0.2mol/LH 2 C 2 O 4 1mL0.2mol/ 配制的0.2mol/L
溶液 水溶液 LHC O 水溶液
2 2 4
HC O 水溶液
2 2 4
褪色时
690s 677s 600s
间
下列说法错误的是
A.对比实验①、②可知,HC O 水溶液浓度增大,反应速率加快
2 2 4
B.对比实验②、③可知,酸性高锰酸钾水溶液浓度增大,反应速率加快
C.为验证H+浓度对反应速率的影响,设计实验④并与③对照
D.实验③的离子方程式为2 +6H++5H C O=2Mn2++10CO ↑+8H O
2 2 4 2 2
高频考点6 考查利用“断点”突破化学反应速率图像(vt图)
例6.(2021·全国·高三专题练习)对于反应2SO (g)+O(g) 2SO (g) ΔH<0已达平衡,如果其他条件
2 2 3
不变时,分别改变下列条件,对化学反应速率和化学平衡产生影响,下列条件与图像不相符的是(0~t:v
1
=v ;t 时改变条件,t 时重新建立平衡)( )
正 逆 1 2
A.增加氧气的浓度 B.增大压强C.升高温度 D.加入催化剂
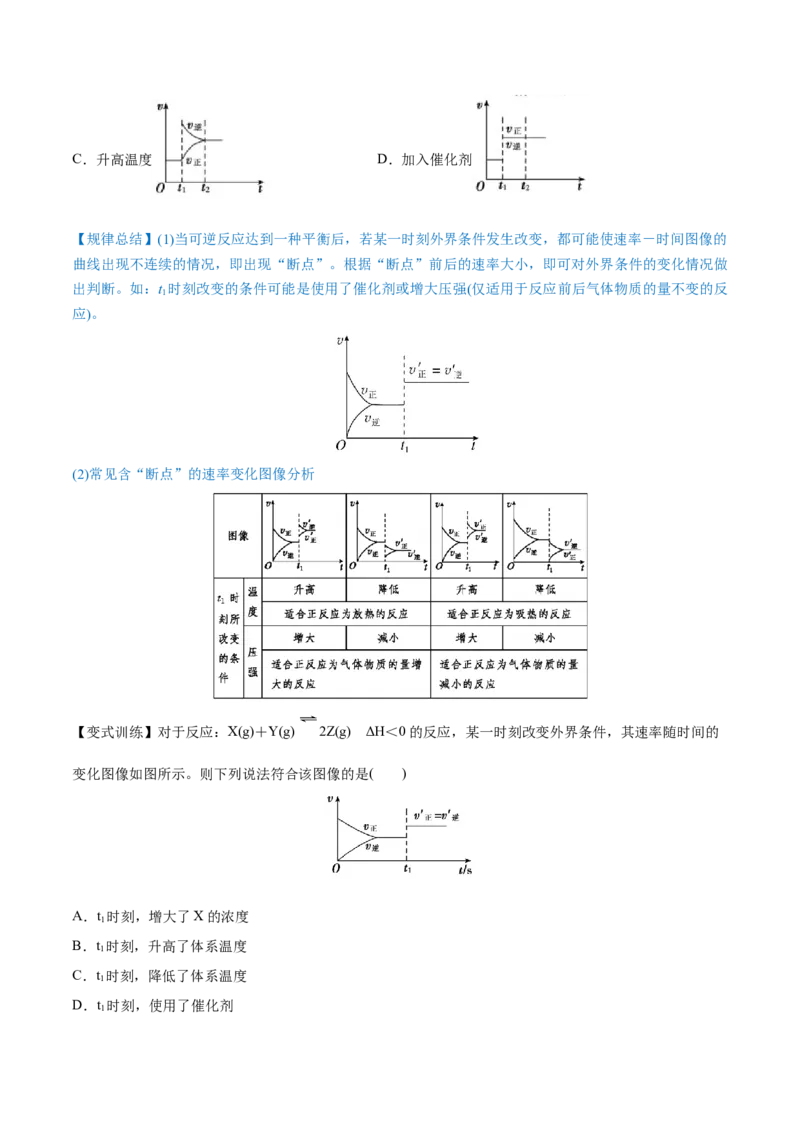
【规律总结】(1)当可逆反应达到一种平衡后,若某一时刻外界条件发生改变,都可能使速率-时间图像的
曲线出现不连续的情况,即出现“断点”。根据“断点”前后的速率大小,即可对外界条件的变化情况做
出判断。如:t 时刻改变的条件可能是使用了催化剂或增大压强(仅适用于反应前后气体物质的量不变的反
1
应)。
(2)常见含“断点”的速率变化图像分析
【变式训练】对于反应:X(g)+Y(g) 2Z(g) ΔH<0的反应,某一时刻改变外界条件,其速率随时间的
变化图像如图所示。则下列说法符合该图像的是( )
A.t 时刻,增大了X的浓度
1
B.t 时刻,升高了体系温度
1
C.t 时刻,降低了体系温度
1
D.t 时刻,使用了催化剂
1高频考点7 考查速率常数及其应用
例7.(2022·全国·高三专题练习)T℃时,H 还原NO以消除氮氧化物污染的反应2NO(g)+2H (g) N(g)
2 2 2
+2H O(g)能自发进行,其正反应速率方程为 =kca(NO)cb(H ),实验得到如下数据:
2 2
组
c(NO)起始/mol·L-1 c(H)起始/mol·L-1 (正反应)起始/mol·L-1·s-1
别 2
I 6.00×10-3 2.00×10-3 2.16×10-3
II 1.20×10-2 2.00×10-3 8.64×10-3
III 6.00×10-3 4.00×10-3 4.32×10-3
下列说法正确的是
A.H 还原NO是熵增的反应 B.正反应一定为吸热反应
2
C.a=2,b=2 D.T℃时,k的数值为3×104
【变式训练】(2021·山东高三)某反应 的速率方程为
,其半衰期(当剩余反应物恰好是起始的一半时所需的时间)为 。改变反应物浓度时,
反应的瞬时速率如表所示:
0.25 0.050 1.4
0.50 0.050 2.8
1.00 0.050 5.6
0.50 0.100 2.8
下列说法正确的是
A.速率方程中的 、
B.该反应的速率常数
C.增大反应物浓度,k增大导致反应的瞬时速率加快D.在过量的B存在时,反应掉87.5%的A所需的时间是375min
高频考点8 考查化学速率的测定
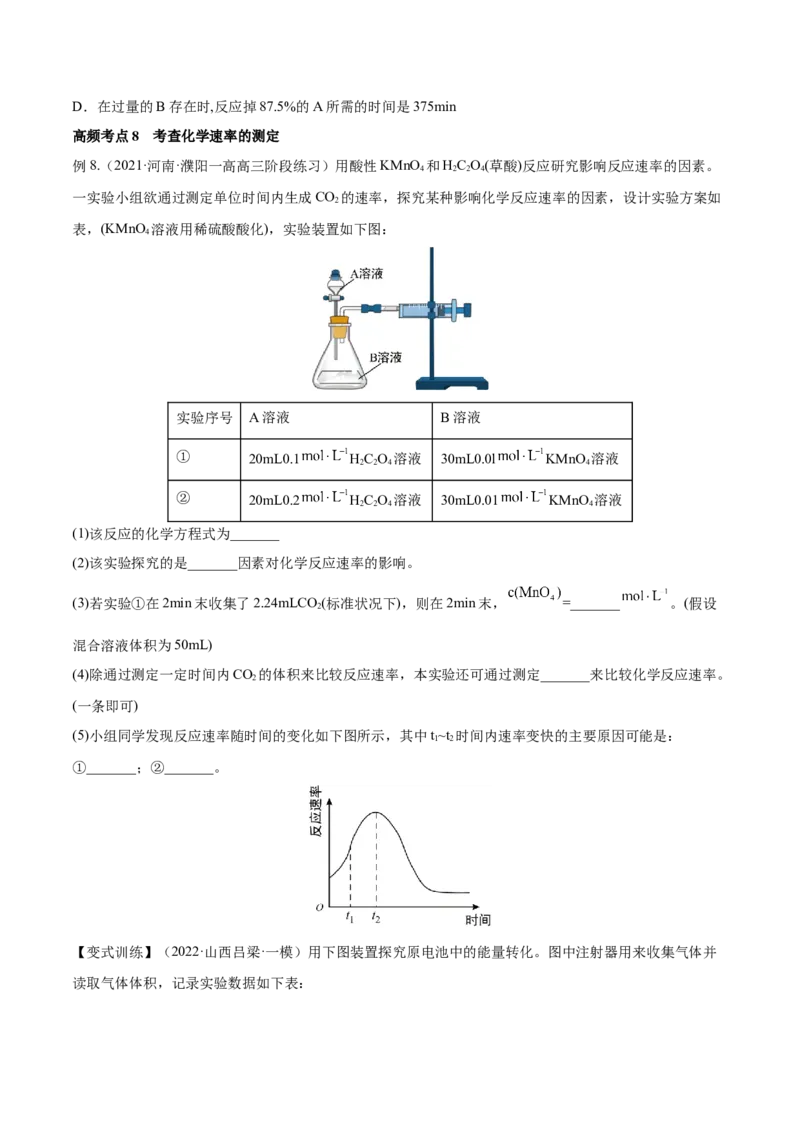
例8.(2021·河南·濮阳一高高三阶段练习)用酸性KMnO 和HC O(草酸)反应研究影响反应速率的因素。
4 2 2 4
一实验小组欲通过测定单位时间内生成CO 的速率,探究某种影响化学反应速率的因素,设计实验方案如
2
表,(KMnO 溶液用稀硫酸酸化),实验装置如下图:
4
实验序号 A溶液 B溶液
① 20mL0.1 HC O 溶液 30mL0.0l KMnO 溶液
2 2 4 4
② 20mL0.2 HC O 溶液 30mL0.01 KMnO 溶液
2 2 4 4
(1)该反应的化学方程式为_______
(2)该实验探究的是_______因素对化学反应速率的影响。
(3)若实验①在2min末收集了2.24mLCO(标准状况下),则在2min末, =_______ 。(假设
2
混合溶液体积为50mL)
(4)除通过测定一定时间内CO 的体积来比较反应速率,本实验还可通过测定_______来比较化学反应速率。
2
(一条即可)
(5)小组同学发现反应速率随时间的变化如下图所示,其中t~t 时间内速率变快的主要原因可能是:
1 2
①_______;②_______。
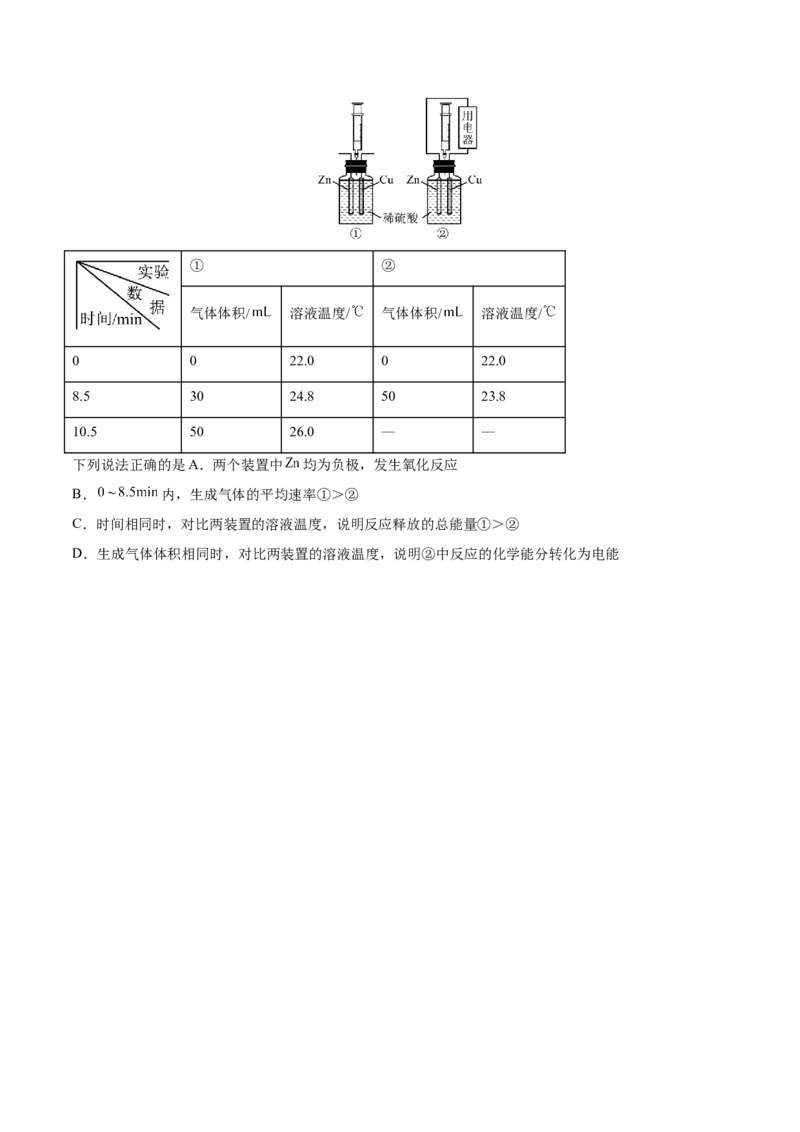
【变式训练】(2022·山西吕梁·一模)用下图装置探究原电池中的能量转化。图中注射器用来收集气体并
读取气体体积,记录实验数据如下表:① ②
气体体积/ 溶液温度/ 气体体积/ 溶液温度/
0 0 22.0 0 22.0
8.5 30 24.8 50 23.8
10.5 50 26.0 — —
下列说法正确的是A.两个装置中 均为负极,发生氧化反应
B. 内,生成气体的平均速率①>②
C.时间相同时,对比两装置的溶液温度,说明反应释放的总能量①>②
D.生成气体体积相同时,对比两装置的溶液温度,说明②中反应的化学能分转化为电能