文档内容
第 20 讲 化学平衡常数及转化率的计算
1.汽车尾气(含烃类、CO、NO与SO 等)是城市主要污染源之一,治理的办法之一是在汽车排气管上装催
2
化转化器,它能使 NO 与 CO 反应生成可参与大气生态循环的无毒气体,其反应原理是 2NO(g)+
2CO(g)===N (g)+2CO(g)。由此可知,下列说法中正确的是( )
2 2
A.该反应是熵增大的反应
B.该反应不能自发进行,因此需要合适的催化剂
C.该反应常温下能自发进行,催化剂条件只是加快反应的速率
D.该反应常温下能自发进行,因为正反应是吸热反应
2.已知反应①:CO(g)+CuO(s)CO (g)+Cu(s)和反应②:H(g)+CuO(s)Cu(s)+HO(g)在相同的某温度
2 2 2
下的平衡常数分别为K 和K ,该温度下反应③:CO(g)+HO(g)CO (g)+H(g)的平衡常数为K。则下列说
1 2 2 2 2
法正确的是( )
A.反应①的平衡常数K =
1
B.反应③的平衡常数K=
C.对于反应③,恒容时,温度升高,H 浓度减小,则该反应的焓变为正值
2
D.对于反应③,恒温恒容时,增大压强,H 浓度一定减小
2
3.反应Fe(s)+CO(g)FeO(s)+CO(g),700 ℃时平衡常数为1.47,900 ℃时平衡常数为2.15。下列说法
2
正确的是( )
A.升高温度,该反应的正反应速率增大,逆反应速率减小
B.该反应的化学平衡常数表达式为K=
C.该反应的正反应是吸热反应
D.增大CO 浓度,平衡常数增大
2
4.下列反应中,一定不能自发进行的是( )
A.2KClO(s)===2KCl(s)+3O(g) ΔH=-78.03 kJ/mol ΔS=+1 110 J/(mol·K)
3 2
B.CO(g)===C(石墨,s)+1/2O (g) ΔH=+110.5 kJ/mol ΔS=-89.36 J/(mol·K)
2
C.4Fe(OH) (s)+2HO(l)+O(g)===4Fe(OH) (s) ΔH=-444.3 kJ/mol ΔS=-280.1 J/(mol·K)
2 2 2 3
D.NH HCO (s)+CHCOOH(aq)===CO (g)+CHCOONH(aq)+HO(l) ΔH=+37.301 kJ/mol ΔS=
4 3 3 2 3 4 2
+184.05 J/(mol·K)
5.已知热化学方程式:aX(g)+3Y(s)bZ(g) ΔH<0。现在容积为2 L的密闭容器中加入0.9 mol X
和1 mol Y,当Y的物质的量减少0.75 mol时,达到平衡状态,此时X、Z的浓度分别是0.2 mol·L-1和0.5mol·L-1,该温度下的平衡常数为( )
A. B. C.35 D.20
6.实现“节能减排”和“低碳经济”的一项重要课题就是如何将CO 转化为可利用的资源。目前工业
2
上有一种方法是用CO 来生产燃料甲醇。一定条件下发生反应:CO(g)+3H(g)CH OH(g)+HO(g),如图
2 2 2 3 2
表示该反应过程中能量(单位为kJ·mol-1)的变化:
下列关于该反应的说法中,正确的是( )
A.ΔH>0,ΔS>0 B.ΔH>0,ΔS<0
C.ΔH<0,ΔS<0 D.ΔH<0,ΔS>0
7.下列反应不可能自发进行的是( )
A.2O(g)===3O (g) ΔH<0
3 2
B.2CO(g)===2C(s)+O(g) ΔH>0
2
C.N(g)+3H(g)===2NH(g) ΔH<0
2 2 3
D.CaCO (s)===CaO(s)+CO(g) ΔH>0
3 2
8.CO 催化加氢制取甲醇的研究,对于环境、能源问题都具有重要的意义。反应如下:
2
反应ⅰ:CO(g)+3H(g)CH OH(g)+HO(g) ΔH=-58 kJ· mol-1
2 2 3 2 1
反应ⅱ:CO(g)+H(g)CO(g)+HO(g) ΔH=+42 kJ· mol-1
2 2 2 2
下列说法不正确的是( )
A.增大氢气浓度能提高二氧化碳的转化率
B.增大压强,有利于向生成甲醇的方向进行,反应ⅰ的平衡常数增大
C.升高温度,生成甲醇的速率加快,反应ⅱ的限度同时增加
D.选用理想的催化剂可以提高甲醇在最终产物中的比率
9.在淀粉KI溶液中存在下列平衡:I(aq)+I-(aq)I(aq)。测得不同温度下该反应的平衡常数K如表所示:
2
t/℃ 5 15 25 35 50
K 1 100 841 689 533 409
下列说法正确的是( )
A.反应I(aq)+I-(aq)I(aq)的ΔH>0
2
B.其他条件不变,升高温度,溶液中c(I)减小
C.该反应的平衡常数表达式为K=D.25 ℃时,向溶液中加入少量KI固体,平衡常数K小于689
10.在一定容积的密闭容器中,进行如下化学反应:CO(g)+H(g)CO(g)+HO(g),其化学平衡常数K
2 2 2
和温度t的关系如表:
t/℃ 700 800 830 1 000 1 200
K 0.6 0.9 1.0 1.7 2.6
回答下列问题:
(1)该反应的化学平衡常数表达式为K=_____________。
(2)该反应的正反应为________反应(填“吸热”或“放热”)。
(3)某温度下,各物质的平衡浓度符合关系式:3c(CO)·c(H )=5c(CO)·c(H O),试判断此时的温度为
2 2 2
________。
(4)若 830 ℃时,向容器中充入 1 mol CO、5 mol H O,反应达到平衡后,其化学平衡常数
2
K________1.0(填“大于”“小于”或“等于”)。
(5)830 ℃时,容器中的反应已达到平衡。在其他条件不变的情况下,扩大容器的容积,平衡________
移动(填“向正反应方向”“向逆反应方向”或“不”)。
(6)若1 200 ℃时,在某时刻反应体系中CO 、H 、CO、HO的浓度分别为2 mol·L-1、2 mol·L-1、4
2 2 2
mol·L-1、4 mol·L-1,则此时上述反应_______________________(填“向正反应方向进行”“向逆反应方向
进行”或“处于平衡状态”)。
1.下列说法不正确的是( )
A.ΔH<0、ΔS>0的反应在任何温度下都能自发进行
B.NH HCO (s)===NH(g)+HO(g)+CO(g) ΔH=+185.57 kJ·mol-1能自发进行,原因是体系有自发
4 3 3 2 2
地向混乱度增加的方向转变的倾向
C.因为焓变和熵变都与反应的自发性有关,因此焓变或熵变均可以单独作为反应自发性的判据
D.在其他外界条件不变的情况下,使用催化剂可以改变化学反应进行的速率
2.某温度下,将2 mol A和3 mol B充入一密闭容器中,发生反应:aA(g)+B(g)C(g)+D(g),5
min后达到平衡,已知该温度下其平衡常数K=1,若温度不变时将容器的容积扩大为原来的10倍,A的转
化率不发生变化,则( )
A.a=3 B.a=2
C.B的转化率为40% D.B的转化率为60%
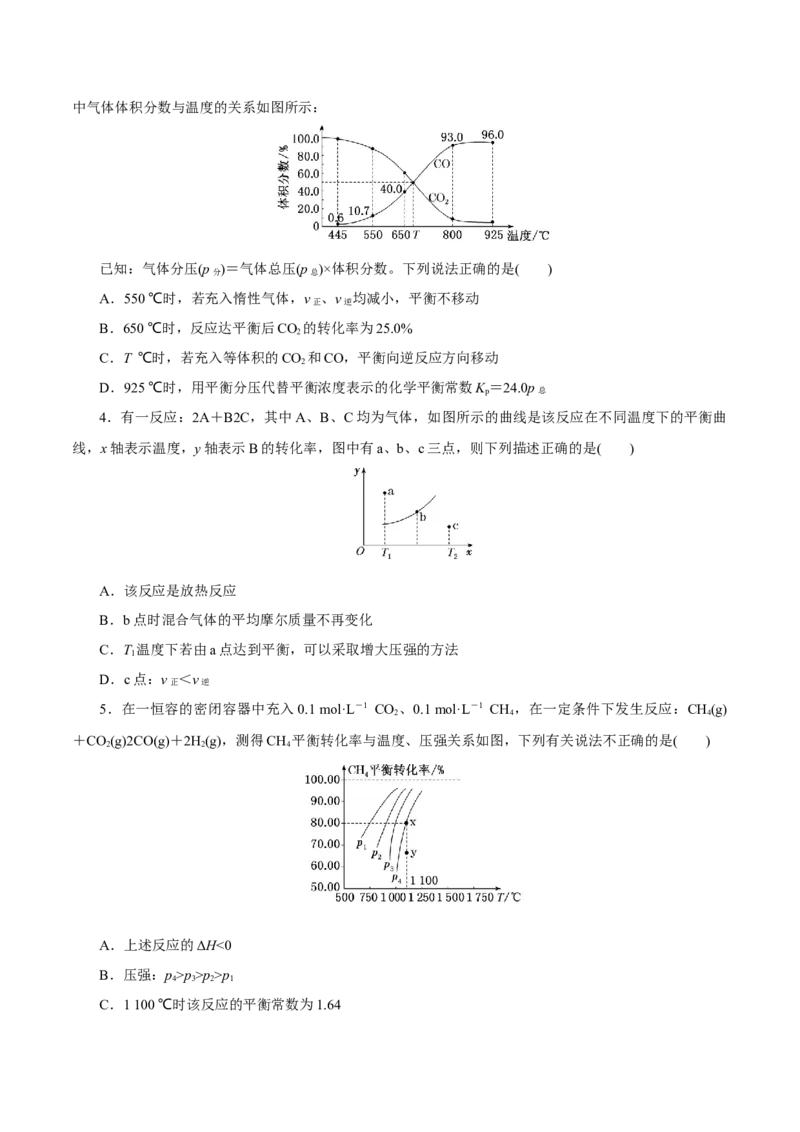
3.一定量的CO 与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO(g)2CO(g)。平衡时,体系
2 2中气体体积分数与温度的关系如图所示:
已知:气体分压(p )=气体总压(p )×体积分数。下列说法正确的是( )
分 总
A.550 ℃时,若充入惰性气体,v 、v 均减小,平衡不移动
正 逆
B.650 ℃时,反应达平衡后CO 的转化率为25.0%
2
C.T ℃时,若充入等体积的CO 和CO,平衡向逆反应方向移动
2
D.925 ℃时,用平衡分压代替平衡浓度表示的化学平衡常数K =24.0p
p 总
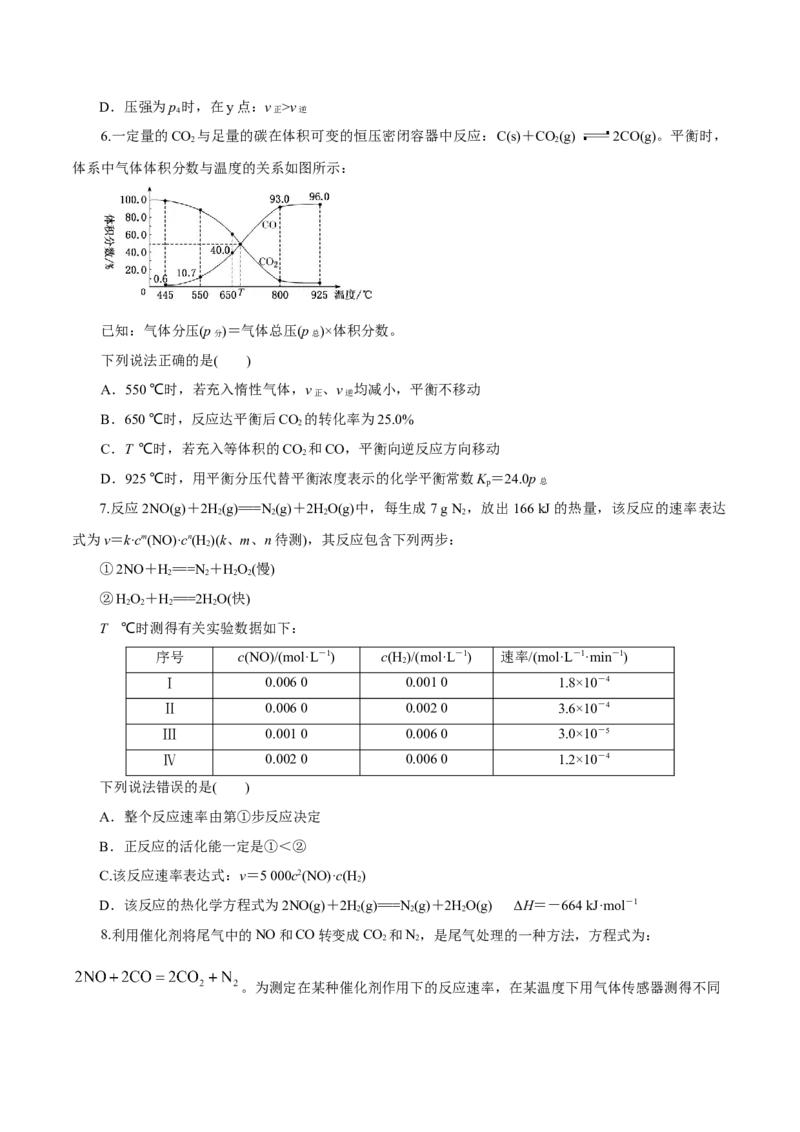
4.有一反应:2A+B2C,其中A、B、C均为气体,如图所示的曲线是该反应在不同温度下的平衡曲
线,x轴表示温度,y轴表示B的转化率,图中有a、b、c三点,则下列描述正确的是( )
A.该反应是放热反应
B.b点时混合气体的平均摩尔质量不再变化
C.T 温度下若由a点达到平衡,可以采取增大压强的方法
1
D.c点:v <v
正 逆
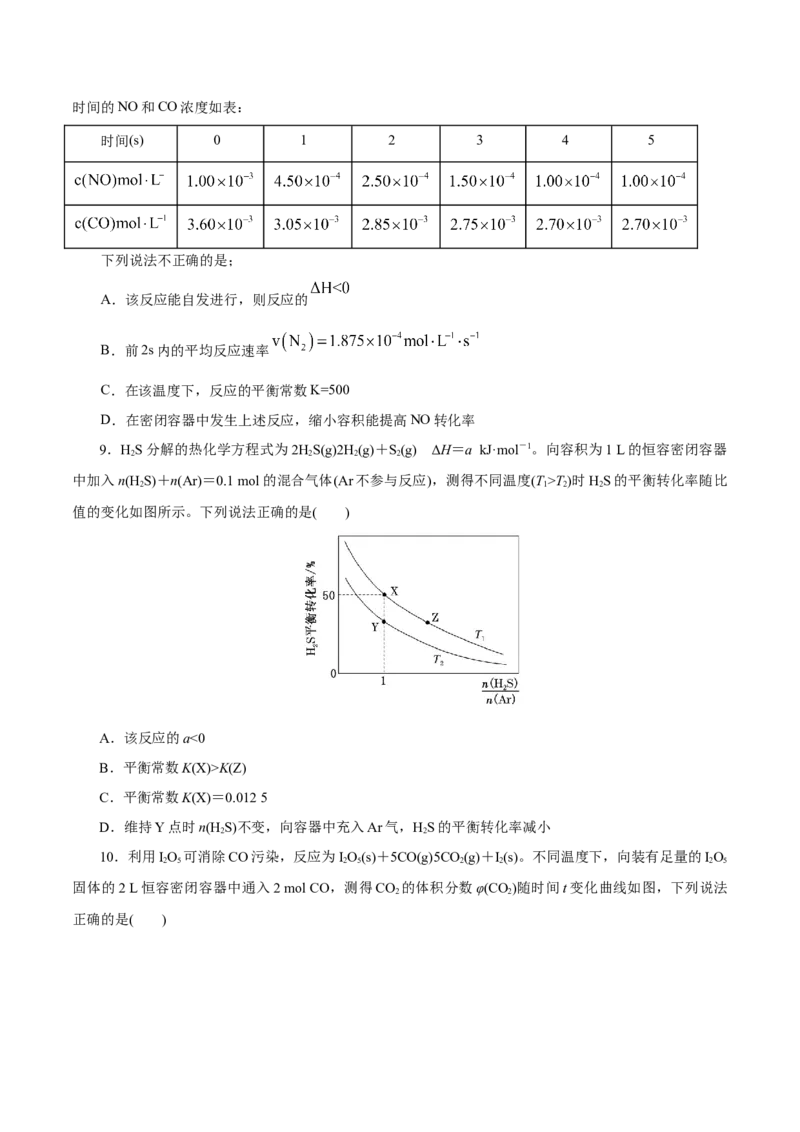
5.在一恒容的密闭容器中充入0.1 mol·L-1 CO 、0.1 mol·L-1 CH ,在一定条件下发生反应:CH(g)
2 4 4
+CO(g)2CO(g)+2H(g),测得CH 平衡转化率与温度、压强关系如图,下列有关说法不正确的是( )
2 2 4
A.上述反应的ΔH<0
B.压强:p>p>p>p
4 3 2 1
C.1 100 ℃时该反应的平衡常数为1.64D.压强为p 时,在y点:v >v
4 正 逆
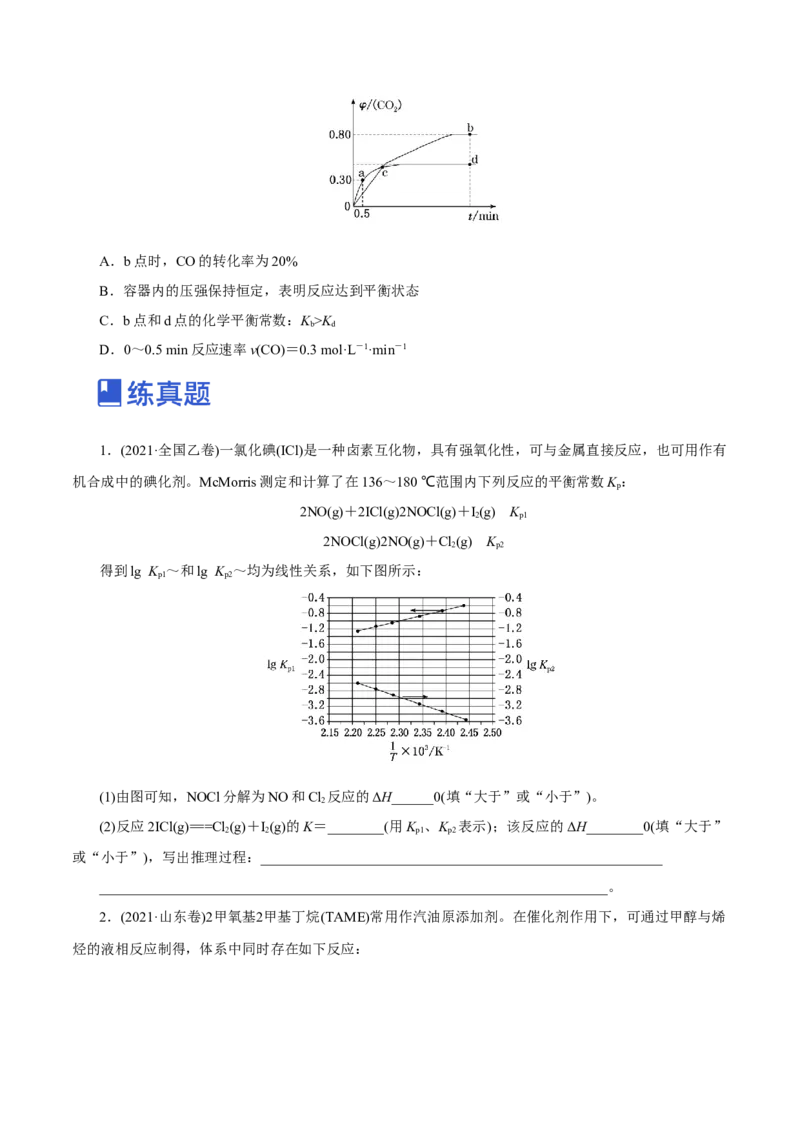
6.一定量的CO 与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO(g) 2CO(g)。平衡时,
2 2
体系中气体体积分数与温度的关系如图所示:
已知:气体分压(p )=气体总压(p )×体积分数。
分 总
下列说法正确的是( )
A.550 ℃时,若充入惰性气体,v 、v 均减小,平衡不移动
正 逆
B.650 ℃时,反应达平衡后CO 的转化率为25.0%
2
C.T ℃时,若充入等体积的CO 和CO,平衡向逆反应方向移动
2
D.925 ℃时,用平衡分压代替平衡浓度表示的化学平衡常数K =24.0p
p 总
7.反应2NO(g)+2H(g)===N (g)+2HO(g)中,每生成7 g N ,放出166 kJ的热量,该反应的速率表达
2 2 2 2
式为v=k·cm(NO)·cn(H )(k、m、n待测),其反应包含下列两步:
2
①2NO+H===N +HO(慢)
2 2 2 2
②HO+H===2H O(快)
2 2 2 2
T ℃时测得有关实验数据如下:
序号 c(NO)/(mol·L-1) c(H )/(mol·L-1) 速率/(mol·L-1·min-1)
2
Ⅰ 0.006 0 0.001 0 1.8×10-4
Ⅱ 0.006 0 0.002 0 3.6×10-4
Ⅲ 0.001 0 0.006 0 3.0×10-5
Ⅳ 0.002 0 0.006 0 1.2×10-4
下列说法错误的是( )
A.整个反应速率由第①步反应决定
B.正反应的活化能一定是①<②
C.该反应速率表达式:v=5 000c2(NO)·c(H )
2
D.该反应的热化学方程式为2NO(g)+2H(g)===N (g)+2HO(g) ΔH=-664 kJ·mol-1
2 2 2
8.利用催化剂将尾气中的NO和CO转变成CO 和N,是尾气处理的一种方法,方程式为:
2 2
。为测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
时间(s) 0 1 2 3 4 5
下列说法不正确的是;
A.该反应能自发进行,则反应的
B.前2s内的平均反应速率
C.在该温度下,反应的平衡常数K=500
D.在密闭容器中发生上述反应,缩小容积能提高NO转化率
9.HS分解的热化学方程式为2HS(g)2H (g)+S(g) ΔH=a kJ·mol-1。向容积为1 L的恒容密闭容器
2 2 2 2
中加入n(H S)+n(Ar)=0.1 mol的混合气体(Ar不参与反应),测得不同温度(T>T)时HS的平衡转化率随比
2 1 2 2
值的变化如图所示。下列说法正确的是( )
A.该反应的a<0
B.平衡常数K(X)>K(Z)
C.平衡常数K(X)=0.012 5
D.维持Y点时n(H S)不变,向容器中充入Ar气,HS的平衡转化率减小
2 2
10.利用IO 可消除CO污染,反应为IO(s)+5CO(g)5CO (g)+I(s)。不同温度下,向装有足量的IO
2 5 2 5 2 2 2 5
固体的2 L恒容密闭容器中通入2 mol CO,测得CO 的体积分数φ(CO)随时间t变化曲线如图,下列说法
2 2
正确的是( )A.b点时,CO的转化率为20%
B.容器内的压强保持恒定,表明反应达到平衡状态
C.b点和d点的化学平衡常数:K >K
b d
D.0~0.5 min反应速率v(CO)=0.3 mol·L-1·min-1
1.(2021·全国乙卷)一氯化碘(ICl)是一种卤素互化物,具有强氧化性,可与金属直接反应,也可用作有
机合成中的碘化剂。McMorris测定和计算了在136~180 ℃范围内下列反应的平衡常数K :
p
2NO(g)+2ICl(g)2NOCl(g)+I(g) K
2 p1
2NOCl(g)2NO(g)+Cl(g) K
2 p2
得到lg K ~和lg K ~均为线性关系,如下图所示:
p1 p2
(1)由图可知,NOCl分解为NO和Cl 反应的ΔH______0(填“大于”或“小于”)。
2
(2)反应2ICl(g)===Cl(g)+I(g)的K=________(用K 、K 表示);该反应的ΔH________0(填“大于”
2 2 p1 p2
或“小于”),写出推理过程:_________________________________________________________
________________________________________________________________________。
2.(2021·山东卷)2甲氧基2甲基丁烷(TAME)常用作汽油原添加剂。在催化剂作用下,可通过甲醇与烯
烃的液相反应制得,体系中同时存在如下反应:回答下列问题:
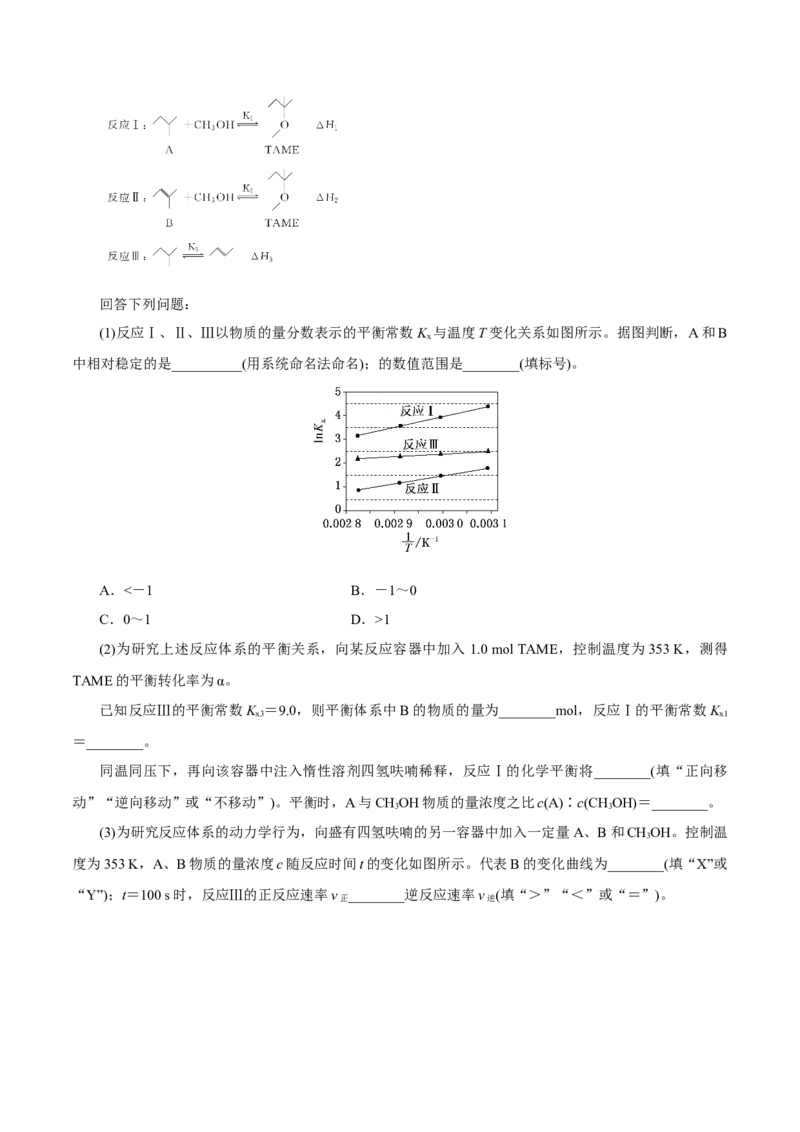
(1)反应Ⅰ、Ⅱ、Ⅲ以物质的量分数表示的平衡常数 K 与温度T变化关系如图所示。据图判断,A和B
x
中相对稳定的是__________(用系统命名法命名);的数值范围是________(填标号)。
A.<-1 B.-1~0
C.0~1 D.>1
(2)为研究上述反应体系的平衡关系,向某反应容器中加入 1.0 mol TAME,控制温度为353 K,测得
TAME的平衡转化率为α。
已知反应Ⅲ的平衡常数K =9.0,则平衡体系中B的物质的量为________mol,反应Ⅰ的平衡常数K
x3 x1
=________。
同温同压下,再向该容器中注入惰性溶剂四氢呋喃稀释,反应Ⅰ的化学平衡将________(填“正向移
动”“逆向移动”或“不移动”)。平衡时,A与CHOH物质的量浓度之比c(A)∶c(CHOH)=________。
3 3
(3)为研究反应体系的动力学行为,向盛有四氢呋喃的另一容器中加入一定量A、B和CHOH。控制温
3
度为353 K,A、B物质的量浓度c随反应时间t的变化如图所示。代表B的变化曲线为________(填“X”或
“Y”);t=100 s时,反应Ⅲ的正反应速率v ________逆反应速率v (填“>”“<”或“=”)。
正 逆3.(2020·浙江卷)5 mL 0.1 mol·L-1 KI溶液与1 mL 0.1 mol·L-1 FeCl 溶液发生反应:2Fe3+(aq)+2I-
3
(aq) 2Fe2+(aq)+I(aq),达到平衡。下列说法不正确的是( )
2
A.加入苯,振荡,平衡正向移动
B.经苯2次萃取分离后,在水溶液中加入KSCN,溶液呈血红色,表明该化学反应存在限度
C.加入FeSO 固体,平衡逆向移动
4
D.该反应的平衡常数K=4.(2021·河北卷)当今,世界多国相继规划了碳达峰、碳中和的时间节点,
因此,研发二氧化碳利用技术、降低空气中二氧化碳含量成为研究热点。
(1)雨水中含有来自大气的CO,溶于水中的CO 进一步和水反应,发生电离:
2 2
①CO(g)CO (aq)
2 2
②CO(aq)+HO(l)H+(aq)+HCO(aq)
2 2
25 ℃时,反应②的平衡常数为K 。
2
溶液中CO 的浓度与其在空气中的分压成正比(分压=总压×物质的量分数),比例系数为y mol·L-
2
1·kPa-1,当大气压强为p kPa,大气中CO(g)的物质的量分数为x时,溶液中H+浓度为________mol·L-
2
1(写出表达式,考虑水的电离,忽略HCO的电离)。
(2)105 ℃时,将足量的某碳酸氢盐(MHCO )固体置于真空恒容容器中,存在如下平衡:
3
2MHCO (s)=====MCO(s)+HO(g)+CO(g)
3 2 3 2 2
上述反应达平衡时体系的总压为46 kPa。
保持温度不变,开始时在体系中先通入一定量的CO(g),再加入足量MHCO (s),欲使平衡时体系中
2 3
水蒸气的分压小于5 kPa,CO(g)的初始压强应大于________kPa。
2
5.(2020·全国Ⅲ卷)二氧化碳催化加氢合成乙烯是综合利用CO 的热点研究领域。回答下列问题:
2
(1)CO 催化加氢生成乙烯和水的反应中,产物的物质的量之比n(C H)∶n(H O)=________。当反应达
2 2 4 2
到平衡时,若增大压强,则n(C H)________(填“变大”“变小”或“不变”)。
2 4
(2)理论计算表明,原料初始组成n(CO)∶n(H )=1∶3,在体系压强为0.1 MPa,反应达到平衡时,四
2 2
种组分的物质的量分数x随温度T的变化如图所示。图中,表示 C H 、CO 变化的曲线分别是________、________。CO 催化加氢合成 C H 反应的
2 4 2 2 2 4
ΔH______0(填“大于”或“小于”)。
(3)根据图中点A(440,0.39),计算该温度时反应的平衡常数K =________(列出计算式。以分压表示,
p
分压=总压×物质的量分数)。
(4)二氧化碳催化加氢合成乙烯反应往往伴随副反应,生成C H 、C H 、C H 等低碳烃。一定温度和压
3 6 3 8 4 8
强条件下,为了提高反应速率和乙烯选择性,应当____________________________。