文档内容
第 31 讲 难溶电解质的溶解平衡与应用
(模拟精练+真题演练)
完卷时间:50分钟
一、选择题(每小题只有一个正确选项,共12×5分)
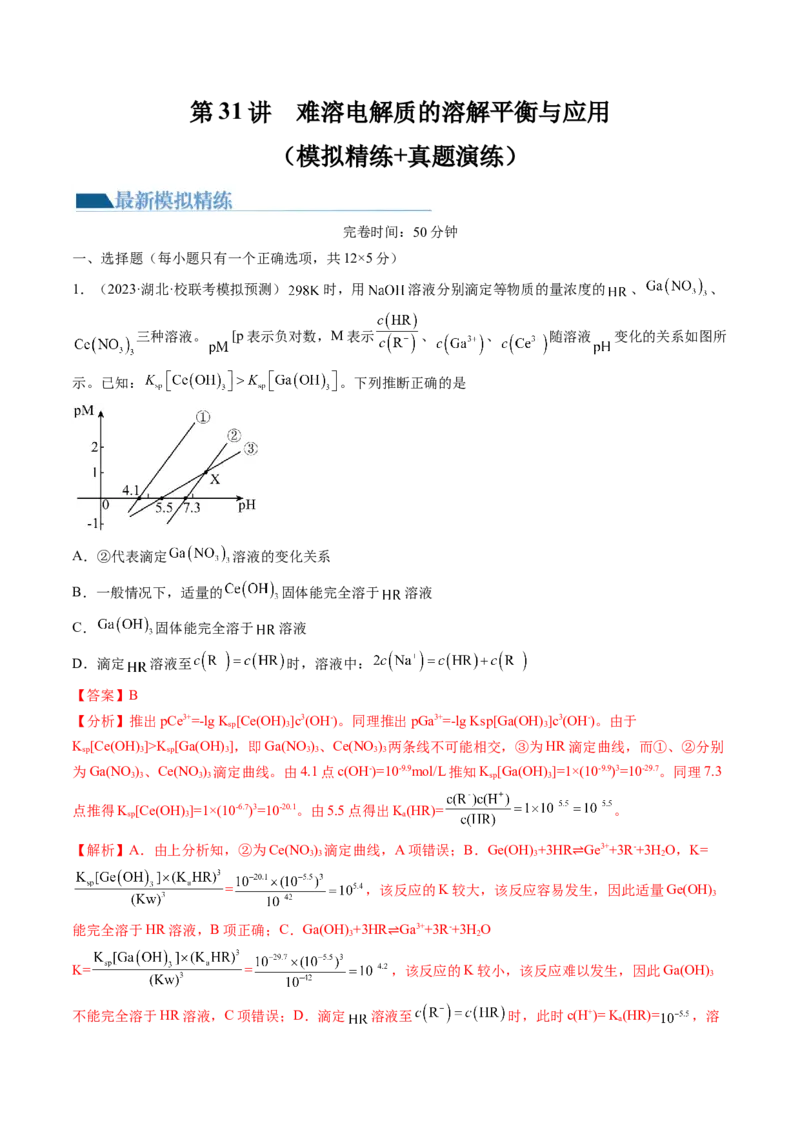
1.(2023·湖北·校联考模拟预测) 时,用 溶液分别滴定等物质的量浓度的 、 、
三种溶液。 [p表示负对数,M表示 、 、 随溶液 变化的关系如图所
示。已知: 。下列推断正确的是
A.②代表滴定 溶液的变化关系
B.一般情况下,适量的 固体能完全溶于 溶液
C. 固体能完全溶于 溶液
D.滴定 溶液至 时,溶液中:
【答案】B
【分析】推出pCe3+=-lg K [Ce(OH) ]c3(OH-)。同理推出pGa3+=-lg Ksp[Ga(OH) ]c3(OH-)。由于
sp 3 3
K [Ce(OH) ]>K [Ga(OH)],即Ga(NO )、Ce(NO ) 两条线不可能相交,③为HR滴定曲线,而①、②分别
sp 3 sp 3 3 3 3 3
为Ga(NO )、Ce(NO ) 滴定曲线。由4.1点c(OH-)=10-9.9mol/L推知K [Ga(OH)]=1×(10-9.9)3=10-29.7。同理7.3
3 3 3 3 sp 3
点推得K [Ce(OH) ]=1×(10-6.7)3=10-20.1。由5.5点得出K(HR)= 。
sp 3 a
【解析】A.由上分析知,②为Ce(NO ) 滴定曲线,A项错误;B.Ge(OH) +3HR Ge3++3R-+3H O,K=
3 3 3 2
⇌
= ,该反应的K较大,该反应容易发生,因此适量Ge(OH)
3
能完全溶于HR溶液,B项正确;C.Ga(OH) +3HR Ga3++3R-+3H O
3 2
⇌
K= = ,该反应的K较小,该反应难以发生,因此Ga(OH)
3
不能完全溶于HR溶液,C项错误;D.滴定 溶液至 时,此时c(H+)= K(HR)= ,溶
a液呈酸性,若溶液中: ,则可得: ,再结合电荷守恒:
,则 ,与溶液环境不符,故D错误;故选:B。
2.(2023·浙江绍兴·统考模拟预测)氢氧化镁是常见难溶物,将过量氢氧化镁粉末置于水中达到溶解平衡:
。已知 , ;通常,
溶液中某离子的浓度小于 时,可以认为该离子已沉淀完全。下列有关说法不正确的是
A.滴入几滴稀硫酸,溶液的pH先下降后上升,最后保持一个稳定值
B. 的饱和溶液中
C.NaOH溶液可使 较彻底地转化为
D.氢氧化镁可处理印染厂的酸性废水,处理后 ,此时溶液呈碱性
【答案】B
【解析】A.滴入几滴稀硫酸后,氢离子和氢氧根离子反应生成水,氢氧根离子浓度降低,pH降低,随后
沉淀溶解平衡正向移动,氢氧根离子浓度增大,pH增大,A正确;B.碳酸镁电离产生镁离子和碳酸根离
子,但是碳酸根离子会水解,故镁离子浓度大于碳酸根离子,B错误;C.通过信息可知,氢氧化镁的溶
度积常数要小的多,故碳酸镁更加容易转化为氢氧化镁,则NaOH溶液可使 较彻底地转化为
,C正确;D.处理后 ,则此时
,氢氧根离子浓度较大,溶液显碱性,D
正确;故选B。
3.(2023·浙江金华·模拟预测)在25℃时,下列几种难溶电解质的溶度积常数(K )如表所示,下列说法不
sp
正确的是
BaSO(白) BaCO (白) AgCl(白) Ag S(黑) Ag CrO(砖红)
4 3 2 2 4
1.1×10-10 2.6×10-9 1.8×10-10 6.3×10-50 2.0×10-7
A.重晶石的主要成分是BaSO 工业上常用饱和碳酸钠溶液反复浸泡重晶石,将难处理的BaSO 转化为更
4 4
易处理的BaCO
3
B.在食盐除杂实验中,利用BaCl 除去溶液中的SO 后,应先过滤,再加入NaCO 除去溶液中的Ba2+和
2 2 3
Ca2+,过滤的目的是防止BaSO 转化为BaCO
4 3
C.在含银工业废水的处理中,相同浓度的NaS溶液比NaCl溶液沉淀效果好,而且NaS溶液可以沉淀多
2 2
种重金属离子
D.将浓度均为0.2mol•L-1的NaCl溶液和NaCrO 溶液等体积混合后,滴加AgNO 溶液,先析出Ag CrO
2 4 3 2 4
沉淀
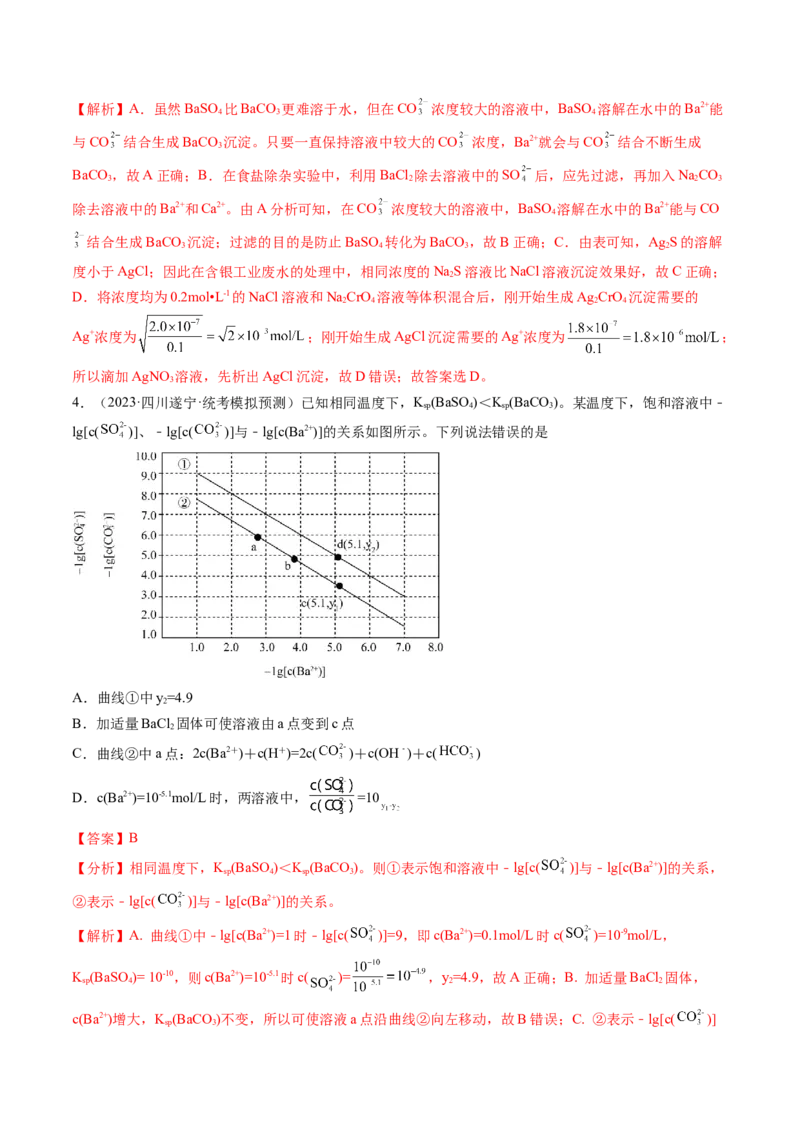
【答案】D【解析】A.虽然BaSO 比BaCO 更难溶于水,但在CO 浓度较大的溶液中,BaSO 溶解在水中的Ba2+能
4 3 4
与CO 结合生成BaCO 沉淀。只要一直保持溶液中较大的CO 浓度,Ba2+就会与CO 结合不断生成
3
BaCO ,故A正确;B.在食盐除杂实验中,利用BaCl 除去溶液中的SO 后,应先过滤,再加入NaCO
3 2 2 3
除去溶液中的Ba2+和Ca2+。由A分析可知,在CO 浓度较大的溶液中,BaSO 溶解在水中的Ba2+能与CO
4
结合生成BaCO 沉淀;过滤的目的是防止BaSO 转化为BaCO ,故B正确;C.由表可知,Ag S的溶解
3 4 3 2
度小于AgCl;因此在含银工业废水的处理中,相同浓度的NaS溶液比NaCl溶液沉淀效果好,故C正确;
2
D.将浓度均为0.2mol•L-1的NaCl溶液和NaCrO 溶液等体积混合后,刚开始生成Ag CrO 沉淀需要的
2 4 2 4
Ag+浓度为 ;刚开始生成AgCl沉淀需要的Ag+浓度为 ;
所以滴加AgNO 溶液,先析出AgCl沉淀,故D错误;故答案选D。
3
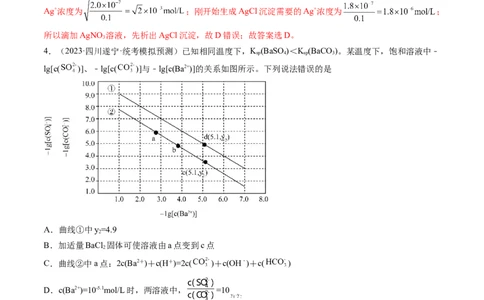
4.(2023·四川遂宁·统考模拟预测)已知相同温度下,K (BaSO)<K (BaCO)。某温度下,饱和溶液中﹣
sp 4 sp 3
lg[c( )]、﹣lg[c( )]与﹣lg[c(Ba2+)]的关系如图所示。下列说法错误的是
A.曲线①中y=4.9
2
B.加适量BaCl 固体可使溶液由a点变到c点
2
C.曲线②中a点:2c(Ba2+)+c(H+)=2c( )+c(OH﹣)+c( )
D.c(Ba2+)=10-5.1mol/L时,两溶液中, =10
【答案】B
【分析】相同温度下,K (BaSO)<K (BaCO)。则①表示饱和溶液中﹣lg[c( )]与﹣lg[c(Ba2+)]的关系,
sp 4 sp 3
②表示﹣lg[c( )]与﹣lg[c(Ba2+)]的关系。
【解析】A. 曲线①中﹣lg[c(Ba2+)=1时﹣lg[c( )]=9,即c(Ba2+)=0.1mol/L时c( )=10-9mol/L,
K (BaSO)= 10-10,则c(Ba2+)=10-5.1时c( )= ,y=4.9,故A正确;B. 加适量BaCl 固体,
sp 4 2 2
c(Ba2+)增大,K (BaCO)不变,所以可使溶液a点沿曲线②向左移动,故B错误;C. ②表示﹣lg[c( )]
sp 3与﹣lg[c(Ba2+)]的关系,根据电荷守恒,曲线②中a点:2c(Ba2+)+c(H+)=2c( )+c(OH﹣)+c( ),
故C正确;D,c(Ba2+)=10-5.1mol/L时,K (BaSO)= 、K (BaCO) = ,两溶液中,
sp 4 sp 3
= =10 ,故D正确;选B。
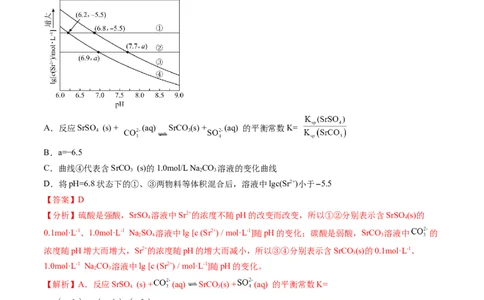
5.(2023·吉林长春·东北师大附中校考模拟预测)工业上以SrSO (s)为原料生产SrCO (s),对其工艺条
4 3
件进行研究。现有分别含SrCO (s)的0.1mol·L-1、1.0mol·L-1 Na CO 溶液,以及分别含SrSO (s)的
3 2 3 4
0.1mol·L-1、1.0mol·L-1 Na SO 溶液。在一定pH范围内(固体足量),四种溶液中lg [c (Sr2+) / mol·L-1]随pH
2 4
的变化关系如图所示。下列说法错误的是
A.反应SrSO (s) + (aq) SrCO (s) + (aq) 的平衡常数K=
4 3
B.a=−6.5
C.曲线④代表含SrCO (s)的1.0mol/L Na CO 溶液的变化曲线
3 2 3
D.将pH=6.8状态下的①、③两物料等体积混合后,溶液中lgc(Sr2+)小于−5.5
【答案】D
【分析】硫酸是强酸,SrSO 溶液中Sr2+的浓度不随pH的改变而改变,所以①②分别表示含SrSO (s)的
4 4
0.1mol·L-1、1.0mol·L-1 Na SO 溶液中lg [c (Sr2+) / mol·L-1]随pH的变化;碳酸是弱酸,SrCO 溶液中 的
2 4 3
浓度随pH增大而增大,Sr2+的浓度随pH的增大而减小,所以③④分别表示含SrCO (s)的0.1mol·L-1、
3
1.0mol·L-1 Na CO 溶液中lg [c (Sr2+) / mol·L-1]随pH的变化。
2 3
【解析】A.反应SrSO (s) + (aq) SrCO (s) + (aq) 的平衡常数K=
4 3
,故A正确;B.K 只与温度有关, 浓度越大,c (Sr2+)越
sp
小,则①表示SrSO (s)在0.1mol·L-1 Na SO 溶液中的lg c(Sr2+),②表示SrSO (s)在1mol·L-1 Na SO 溶液中
4 2 4 4 2 4
的lg c(Sr2+),根据①, = ,则a点c(Sr2+)= ,a=-6.5,故B正确;
C.③④分别表示SrCO (s)的0.1L mol·L-1、1.0 mol·L-1 Na CO 溶液中lg [c (Sr2+) / mol·L-1]随pH的变化,
3 2 3
点(6.2、-5.5)、点(6.2、-5.5),c(Sr2+)相等,所以 相等,碳酸的电离平衡常数不变,pH越大,增大,所以曲线④代表含SrCO (s)的1.0mol/L Na CO 溶液的变化曲线,故C正确;D.将
3 2 3
pH=6.8状态下的①、③两物料等体积混合后,相当于溶液稀释, 、 减小,所以溶液中lg
c(Sr2+)大于−5.5,故D错误;故选D。
6.(2023·江西宜春·江西省宜丰中学校考模拟预测)天然溶洞的形成与岩石中的CaCO 和空气中CO 溶于
3 2
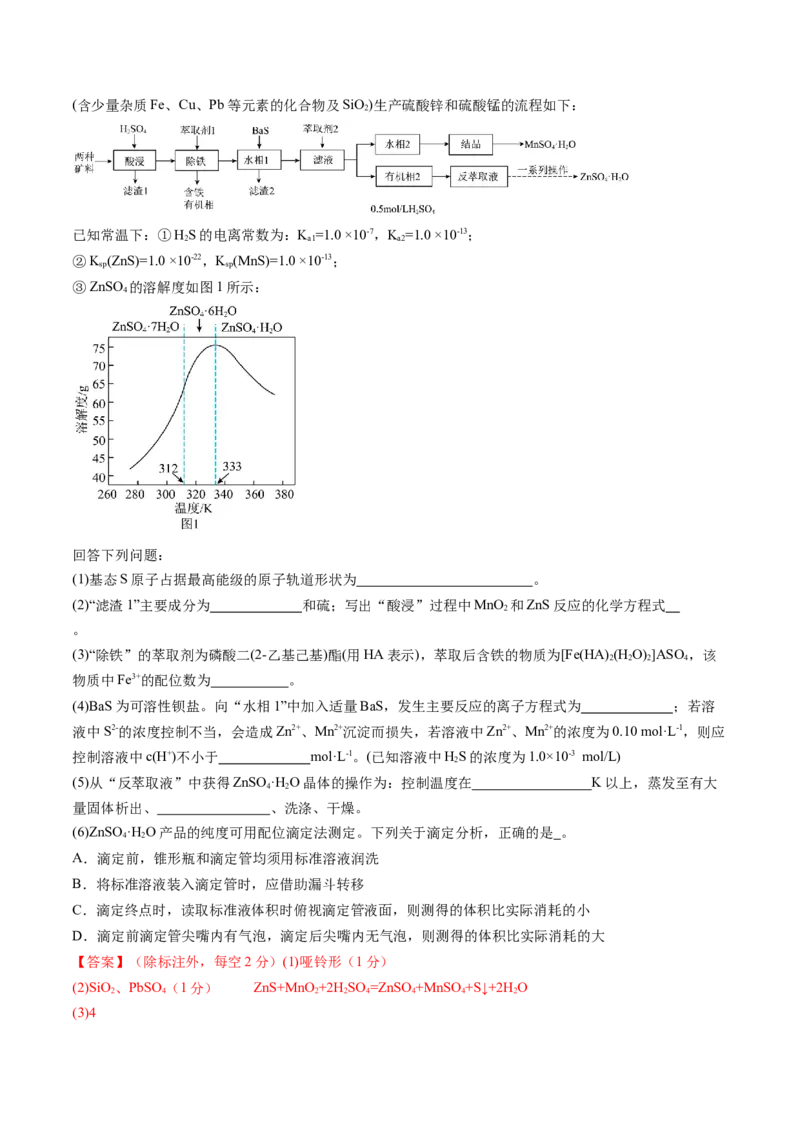
天然水体形成的含碳物种的浓度有密切关系。常温下,某溶洞水体中pM随pH的变化关系如图所示。[已
知: ; ,M为 或 ],下列说法不正确的是
A.曲线②代表 与pH的关系
B. 的数量级为10-4
C.
D.pH由4到8的过程中 增大的比 快
【答案】D
【解析】A.由图中曲线可知,离子浓度越小,pM的值越大,PH越小,碳酸根和碳酸氢根的浓度越大,
曲线②代表 与pH的关系,曲线③代表 ,故A正确;B.点(10.3,1.1)时,
,故B正确;C.(8.6,n),碳酸根浓度等于钙离子浓度,
, mol/L, (8.6,m),即pH=8.6,c(H+)=10-
8.6mol/L,c(OH-)=10-14÷10-8.6=10-5.4mol/L, ,
,c( )=101.7×c( )=101.7×10-4.27=10-2.57, ,故
C正确;D.根据图像斜率,pH由4到8的过程中 增大的比 慢,D错误;故本题选D。
7.(2023·河北衡水·衡水市第二中学校考三模)某污水处理厂用“ 沉淀法”处理含铬废水(主要含
以及少量 、 )的工艺流程如图所示:已知:①金属离子 、 、 沉淀完全时( )pH分别为6.7、5.6、2.8。
② 。
下列说法错误的是
A.“氧化”时生成 的离子方程式为
B.“沉降”过程中加入NaOH溶液,调节溶液pH>6.7
C.加入 生成 ,说明
D.“沉铬”过程中,增大溶液的pH,沉铬率提高
【答案】A
【解析】A.碱性环境中不能生成 ,A错误;B.“沉降”过程中加入NaOH溶液,调节pH使 和
生成沉淀,故需要调节溶液的 ,B正确;C.在滤液中加入 通过沉淀转化生成 ,
说明溶度积 ,C正确;D.在沉铬过程中增大溶液的pH,平衡
正向移动, 浓度增大,沉铬率提高,D正确。 故选A。
8.(2023·浙江金华·统考模拟预测)已知HA是一元弱酸,难溶盐MA的饱和溶液中 随 的变
化而变化,其中 不发生水解。实验中往难溶盐MA的饱和溶液不断通入HCl气体,调节溶液的 ,
结果发现,298K时, 为线性关系,如下图中实线所示。下列叙述不正确的是
A.当 时,
B.溶液 时,
C.MA的溶度积常数D.HA的电离常数
【答案】A
【分析】由图中线性关系可得关系式 ,以下选项可据此回答。
【解析】A.MA溶液中物料守恒c(A-)+c(HA)=c(M+),因为A-水解,此时溶液呈碱性,通入HCl使溶液呈
酸性,仍存在c(A-)+c(HA)=c(M+),所以 ,A错误;B.根据
可计算,当pH=4时c(M+)= ,所以
,B正确;C.由题中信息可知c(H+)=0 mol/L时,为MA的饱和溶液,MA的溶
度积常数 ,C正确;D.当c(A-)=c(HA)时,HA的电离常数
,
当c(A-)=c(HA)时,根据物料守恒: c(A-)+c(HA)=c(M+),则c(M+)=2c(A-),根据
,则 ,代入线性关系式
,可得c(H+)= mol/L,所以 ,
D正确;故答案选A。
9.(2023·全国·统考一模)某温度下,25mL含KX和KY的混合溶液,用0.1000mol•L-1的硝酸银标准溶
液对该混合液进行电位滴定(在滴定过程中,随着滴定剂的不断加入,电极电位E不断发生变化,电极电位
发生突跃时,说明滴定到达终点)、获得电动势(E)和银硝酸银标准溶液体积(V)的电位滴定曲线如图所示。
已知:
I.Ag+与Y-反应过程为:①Ag++2Y- [AgY ]-、②[AgY ]-+Ag+ 2AgY↓。
2 2
II.该温度下,K (AgY)=2×10-16,K (AgX)=2×10-10
sp sp
III.Y-与H+的反应可以忽略。
下列说法不正确的是
A.若HY为弱酸,则从开始到A点,水的电离程度不断减小
B.原混合溶液中c(KX)=0.02000mol•L-1,c(KY)=0.03000mol•L-1
C.若反应①的平衡常数为K,反应②的平衡常数为K,则 =K (AgY)
1 2D.将AgX和AgY的饱和溶液等体积混合,加入足量硝酸银溶液,析出固体AgX多于AgY
【答案】B
【解析】A.对于结构相似的物质,溶度积小的先生成沉淀,根据反应的方程式可知,A点生成[AgY ]-,B
2
点生成AgY,若HY为弱酸,则KY溶液中由于水解促进水的电离,滴加AgNO 溶液时,Y-浓度逐渐减小,
3
水的电离程度逐渐减小,故A正确;B.OA段发生的反应为Ag++2Y- [AgY ]-,AB段发生的反应为
2
[AgY ]-+Ag+ 2AgY↓,所以V=5.0,原溶液中n(Y-)=2 0.1000 mol/L 2.50 10-3 L=5 10-4mol,c(KY)=5
2 1
10-4mol÷0.025 L=0.02000 mol/L,BC段发生的反应为Ag++X-=AgX↓,BC段消耗的标准AgNO3溶液的体
积为12.50mL-5.00ml=7.50 mL,则原溶液中n(X- )=0. 1000 mol/L 7.5 10-3 L=7.5 10-4mol,c(KX)=
=0.03mol/L,故B错误;C.①的平衡常数为K= ,反应②的平衡常数为K=
1 2
,K K= ,Ag++Y-=AgY↓,K (AgY)=c(Ag+)c(Y-)= ,则
1 2 sp
=K (AgY),故C正确;D.因为K (AgY)0,则 即 ,又由
于2c(Mg2+)=c(F-)+c(HF),故溶液中存在c(Cl-)>c(Mg2+)=c(HF)>c(H+),故D错误;故选:C。
二、主观题(共3小题,共40分)
13.(12分)(2023·湖南娄底·统考模拟预测)某小组拟设计实验探究金属氢氧化物在铵盐溶液中溶解度
的影响因素。
已知:①常温下,几种氢氧化物的溶度积数据如下表所示:②可能用到的试剂: 溶液、 溶液、 溶液和
溶液;
③常温下, 的电离常数 , 的电离常数 。
实验一 比较 在不同浓度的 溶液中溶解情况。
操作 试剂X 现象
(Ⅰ) 溶液,
白色浊液逐渐变澄清
10.0mL
(Ⅱ) 溶液,
白色浊液变化不明显
10.0mL
(1)实验结论是 。
(2)针对实验(I),“白色浊液变澄清”的原因,提出如下假设:
假设①: , , 。
假设②: , (补充离子方程式)。
为了验证(2)提出的假设,设计如下实验:
实验二 比较 在不同浓度的 溶液中溶解情况。
操作 试剂X 现象
(Ⅲ)
溶 白色浊液逐渐变澄清
液,10.0mL
(Ⅳ)
溶 白色浊液变化不明显
液,10.0mL
(3)选择 的理由是 。
实验结论是(2)中假设 成立(填“①”或“②”)。
根据上述实验,有同学认为金属氢氧化物都能溶解于 溶液。为了验证他的观点,设计如下实
验:实验三 探究 、、在 溶液中溶解情况。
操作 Y 现象
(Ⅴ) 没有明显现象
(Ⅵ) 浊液变澄清溶液
(Ⅶ) 没有明显现象
已知:(a) 、 、 都易溶于水,实验(Ⅵ)浊液变澄清可能的原因
是 更难电离;
(b)其他条件相同,难溶金属氢氧化物的溶解度越小,在同种铵盐溶液中溶解度越小。
(4)常温下, 、 、 溶解度由大到小排序为 。
(5)通过上述实验,影响 在铵盐溶液中溶解度的因素主要有铵盐浓度、 、 。
【答案】(除标注外,每空2分)(1) 溶解度随着 浓度减小而减小
(2)
(3) 、 的电离常数相等, 溶液显中性,排除了 干扰 ②
(4)
(5)产物电离程度(1分) 本身的溶度积大小(1分)
【解析】(1)对比实验Ⅰ、Ⅱ,NH Cl浓度小的沉淀变化不明显,说明NH Cl浓度小
4 4
Mg(OH) 的溶解度小。答案为Mg(OH) 溶解度随着NH Cl浓度减小而减小;
2 2 4
(2)溶解度增大即溶解平衡正向只要解释到OH-减少平衡正向即可,所以 +OH− NH HO。答案为
3 2
+OH− NH HO; ⇌ ⋅
3 2
(3)假设①⇌解释⋅ NH Cl呈酸性消耗OH-,所以若验证假设Ⅱ需要排除溶液酸碱性的干扰只考虑铵根结合
4
OH-的问题。而CHCOONH 呈中性同时有铵根,满足实验要求。结合实验看,增大CHCOONH 的浓度沉
3 4 3 4
淀澄清溶解,说明假设②成立。答案为CHCOONH;②;
3 4
(4)同类型的物质,溶解度越大,K 越大。对比数据,溶解度的Ni(OH) >Pb(OH) >Sn(OH) 。答案为
sp 2 2 2
Ni(OH) >Pb(OH) >Sn(OH) ;
2 2 2
(5)结合Mg(OH) 和其他三个的实验对比,Mg(OH) 溶度积最大溶解了,可看出在铵盐溶液中溶解度与
2 2
物质本身溶度积有关。而Ni(OH) 、Pb(OH)、Sn(OH) 三者对比,溶解度中间的Pb(OH) 却溶于
2 2 2 2
CHCOONH,主要由于(CHCOO) Pb更难电离,所有与产物电离程度有关。答案为产物电离程度;本身
3 4 3 2
的溶度积大小。
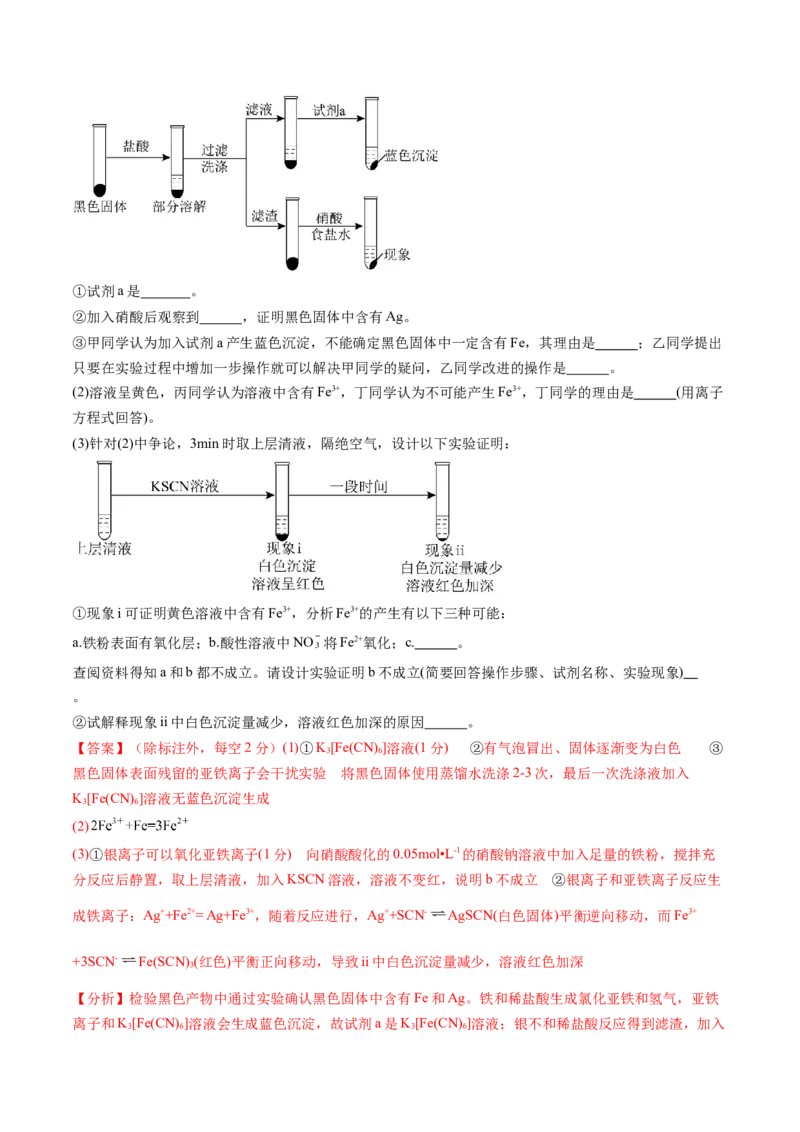
14.(14分)(2023·黑龙江哈尔滨·哈尔滨三中校考模拟预测)利用锌精矿(ZnS)和软锰矿(MnO )两种矿料
2(含少量杂质Fe、Cu、Pb等元素的化合物及SiO)生产硫酸锌和硫酸锰的流程如下:
2
已知常温下:①HS的电离常数为:K =1.0 ×10-7,K =1.0 ×10-13;
2 a1 a2
②K (ZnS)=1.0 ×10-22,K (MnS)=1.0 ×10-13;
sp sp
③ZnSO 的溶解度如图1所示:
4
回答下列问题:
(1)基态S原子占据最高能级的原子轨道形状为 。
(2)“滤渣1”主要成分为 和硫;写出“酸浸”过程中MnO 和ZnS反应的化学方程式
2
。
(3)“除铁”的萃取剂为磷酸二(2-乙基己基)酯(用HA表示),萃取后含铁的物质为[Fe(HA) (H O) ]ASO ,该
2 2 2 4
物质中Fe3+的配位数为 。
(4)BaS为可溶性钡盐。向“水相1”中加入适量BaS,发生主要反应的离子方程式为 ;若溶
液中S2-的浓度控制不当,会造成Zn2+、Mn2+沉淀而损失,若溶液中Zn2+、Mn2+的浓度为0.10 mol·L-1,则应
控制溶液中c(H+)不小于 mol·L-1。(已知溶液中HS的浓度为1.0×10-3 mol/L)
2
(5)从“反萃取液”中获得ZnSO·H O晶体的操作为:控制温度在 K以上,蒸发至有大
4 2
量固体析出、 、洗涤、干燥。
(6)ZnSO ·H O产品的纯度可用配位滴定法测定。下列关于滴定分析,正确的是 。
4 2
A.滴定前,锥形瓶和滴定管均须用标准溶液润洗
B.将标准溶液装入滴定管时,应借助漏斗转移
C.滴定终点时,读取标准液体积时俯视滴定管液面,则测得的体积比实际消耗的小
D.滴定前滴定管尖嘴内有气泡,滴定后尖嘴内无气泡,则测得的体积比实际消耗的大
【答案】(除标注外,每空2分)(1)哑铃形(1分)
(2)SiO、PbSO (1分) ZnS+MnO+2H SO =ZnSO +MnSO +S↓+2H O
2 4 2 2 4 4 4 2
(3)4(4)Cu2++S2- +Ba2++ =CuS↓+BaSO ↓(1分) 0.10
4
(5)333 趁热过滤(1分)
(6)CD
【分析】利用锌精矿(ZnS)和软锰矿(MnO )两种矿料(含少量杂质Fe、Cu、Pb等元素的化合物及SiO)生产
2 2
硫酸锌和硫酸锰的流程中,加硫酸酸浸,锌、铁、铜、锰生成硫酸盐,硫酸铅为沉淀和二氧化硅一起进入
滤渣1,萃取剂1溶解铁离子,加入BaS,除去铜离子和硫酸根离子,萃取剂2萃取硫酸锌,水相为硫酸锰,
进一步得到MnSO ·H O有机相为硫酸锌,进一步反萃取的到ZnSO·H O。
4 2 4 2
【解析】(1)基态S原子占据最高能级的原子轨道为3p,形状为哑铃型。
(2)加硫酸酸浸,锌、铁、铜、锰生成硫酸盐,硫酸铅为沉淀和二氧化硅一起进入滤渣1,故答案为:
SiO、PbSO 。
2 4
“酸浸”过程中MnO 和ZnS反应生成硫单质,化学方程式为:
2
ZnS+MnO+2H SO =ZnSO +MnSO +S↓+2H O。
2 2 4 4 4 2
(3)萃取后含铁的物质为[Fe(HA) (H O) ]ASO ,该物质中Fe3+的配位数为2+2=4。
2 2 2 4
(4)向“水相1”中加入适量BaS,发生主要反应的离子方程式为:Cu2++S2- +Ba2++ =CuS↓+BaSO ↓。
4
若溶液中S2-的浓度控制不当,会造成Zn2+、Mn2+沉淀而损失,若溶液中Zn2+、Mn2+的浓度为0.10 mol·L-1,
则应控制溶液中c(H+)不小于0.10mol·L-1。
,由K (ZnS)=1.0 ×10-22,K (MnS)=1.0 ×10-13且Zn2+、Mn2+的浓度为0.10
sp sp
mol·L-1,可知 ≤1.0 ×10-23,带入 ,可得c(H+)≥0.10mol·L-1。
(5)观察题图可知应该≥333K,并且趁热过滤。
(6)A.滴定前,锥形瓶不须用标准溶液润洗,A错误;B.将标准溶液装入滴定管时,应借助烧杯转移,
B错误;C.滴定终点时,读取标准液体积时俯视滴定管液面,则测得的体积比实际消耗的小,C正确;
D.滴定前滴定管尖嘴内有气泡,滴定后尖嘴内无气泡,则测得的体积比实际消耗的大,D正确;故选
CD。
15.(14分)(2023·山东潍坊·校联考模拟预测)某化学兴趣小组在隔绝空气条件下,向硝酸酸化的
0.05mol•L-1硝酸银溶液(pH≈2)中加入过量铁粉,搅拌后静置,烧杯底部有黑色固体,溶液呈黄色。针对实
验现象该小组同学设计开展了系列实验,具体探究过程如下。
已知:Ag++SCN- AgSCN(白色固体);Fe3++3SCN- Fe(SCN) (红色)
3
回答下列问题:
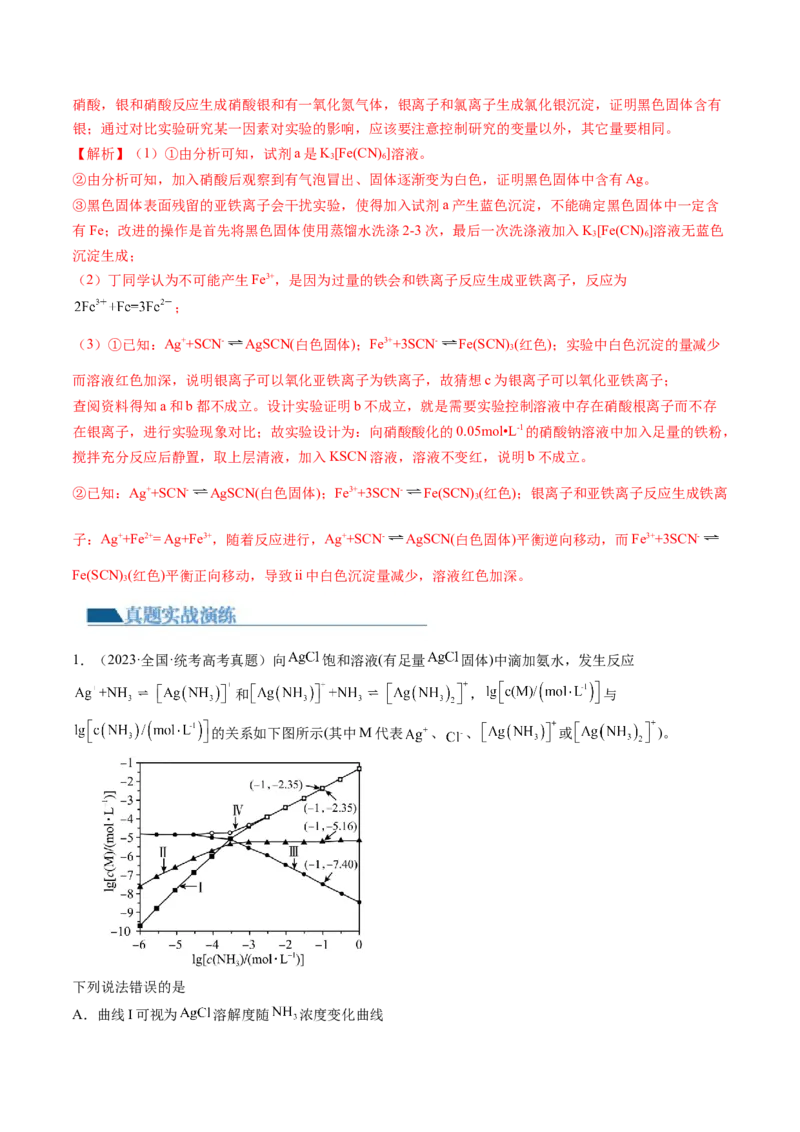
(1)检验黑色产物:取出少量黑色固体,进行如图实验,确认黑色固体中含有Fe和Ag。①试剂a是 。
②加入硝酸后观察到 ,证明黑色固体中含有Ag。
③甲同学认为加入试剂a产生蓝色沉淀,不能确定黑色固体中一定含有Fe,其理由是 ;乙同学提出
只要在实验过程中增加一步操作就可以解决甲同学的疑问,乙同学改进的操作是 。
(2)溶液呈黄色,丙同学认为溶液中含有Fe3+,丁同学认为不可能产生Fe3+,丁同学的理由是 (用离子
方程式回答)。
(3)针对(2)中争论,3min时取上层清液,隔绝空气,设计以下实验证明:
①现象i可证明黄色溶液中含有Fe3+,分析Fe3+的产生有以下三种可能:
a.铁粉表面有氧化层;b.酸性溶液中NO 将Fe2+氧化;c. 。
查阅资料得知a和b都不成立。请设计实验证明b不成立(简要回答操作步骤、试剂名称、实验现象)
。
②试解释现象ii中白色沉淀量减少,溶液红色加深的原因 。
【答案】(除标注外,每空2分)(1)①K[Fe(CN) ]溶液(1分) ②有气泡冒出、固体逐渐变为白色 ③
3 6
黑色固体表面残留的亚铁离子会干扰实验 将黑色固体使用蒸馏水洗涤2-3次,最后一次洗涤液加入
K[Fe(CN) ]溶液无蓝色沉淀生成
3 6
(2)
(3)①银离子可以氧化亚铁离子(1分) 向硝酸酸化的0.05mol•L-1的硝酸钠溶液中加入足量的铁粉,搅拌充
分反应后静置,取上层清液,加入KSCN溶液,溶液不变红,说明b不成立 ②银离子和亚铁离子反应生
成铁离子:Ag++Fe2+= Ag+Fe3+,随着反应进行,Ag++SCN- AgSCN(白色固体)平衡逆向移动,而Fe3+
+3SCN- Fe(SCN) (红色)平衡正向移动,导致ii中白色沉淀量减少,溶液红色加深
3
【分析】检验黑色产物中通过实验确认黑色固体中含有Fe和Ag。铁和稀盐酸生成氯化亚铁和氢气,亚铁
离子和K[Fe(CN) ]溶液会生成蓝色沉淀,故试剂a是K[Fe(CN) ]溶液;银不和稀盐酸反应得到滤渣,加入
3 6 3 6硝酸,银和硝酸反应生成硝酸银和有一氧化氮气体,银离子和氯离子生成氯化银沉淀,证明黑色固体含有
银;通过对比实验研究某一因素对实验的影响,应该要注意控制研究的变量以外,其它量要相同。
【解析】(1)①由分析可知,试剂a是K[Fe(CN) ]溶液。
3 6
②由分析可知,加入硝酸后观察到有气泡冒出、固体逐渐变为白色,证明黑色固体中含有Ag。
③黑色固体表面残留的亚铁离子会干扰实验,使得加入试剂a产生蓝色沉淀,不能确定黑色固体中一定含
有Fe;改进的操作是首先将黑色固体使用蒸馏水洗涤2-3次,最后一次洗涤液加入K[Fe(CN) ]溶液无蓝色
3 6
沉淀生成;
(2)丁同学认为不可能产生Fe3+,是因为过量的铁会和铁离子反应生成亚铁离子,反应为
;
(3)①已知:Ag++SCN- AgSCN(白色固体);Fe3++3SCN- Fe(SCN) (红色);实验中白色沉淀的量减少
3
而溶液红色加深,说明银离子可以氧化亚铁离子为铁离子,故猜想c为银离子可以氧化亚铁离子;
查阅资料得知a和b都不成立。设计实验证明b不成立,就是需要实验控制溶液中存在硝酸根离子而不存
在银离子,进行实验现象对比;故实验设计为:向硝酸酸化的0.05mol•L-1的硝酸钠溶液中加入足量的铁粉,
搅拌充分反应后静置,取上层清液,加入KSCN溶液,溶液不变红,说明b不成立。
②已知:Ag++SCN- AgSCN(白色固体);Fe3++3SCN- Fe(SCN) (红色);银离子和亚铁离子反应生成铁离
3
子:Ag++Fe2+= Ag+Fe3+,随着反应进行,Ag++SCN- AgSCN(白色固体)平衡逆向移动,而Fe3++3SCN-
Fe(SCN) (红色)平衡正向移动,导致ii中白色沉淀量减少,溶液红色加深。
3
1.(2023·全国·统考高考真题)向 饱和溶液(有足量 固体)中滴加氨水,发生反应
和 , 与
的关系如下图所示(其中M代表 、 、 或 )。
下列说法错误的是
A.曲线I可视为 溶解度随 浓度变化曲线B. 的溶度积常数
C.反应 的平衡常数K的值为
D. 时,溶液中
【答案】A
【分析】氯化银饱和溶液中银离子和氯离子的浓度相等,向饱和溶液中滴加氨水,溶液中银离子浓度减小,
氯离子浓度增大、一氨合银离子增大,继续滴加氨水,一氨合银离子增大的幅度小于二氨合银离子,则曲
线I、Ⅱ、Ⅲ、Ⅳ分别表示二氨合银离子、一氨合银离子、银离子、氯离子与氨气浓度对数变化的曲线。
【解析】A.氨的浓度较小时AgCl(s) Ag+(aq)+Cl-(aq),浓度较大时AgCl(s)+2NH
3
(aq)+Cl-(aq),氯化银的溶解度曲线应与氯离子的曲线吻合,应该为曲线Ⅳ,故A错误;B.由图可知,
c(NH )=10-1mol/L时,c(Cl-)=10-2.35mol/L,c(Ag+)=10-7.40mol/L,则氯化银的溶度积为10-2.35×10-7.40=10-9.75,故B
3
正确;C.由图可知,氨分子浓度对数为-1时,溶液中二氨合银离子和一氨合银离子的浓度分别为10-
2.35mol/L和10-5.16mol/L,则 的平衡常数K= =
= ,故C正确;D.由分析可知,曲线I、Ⅱ、Ⅲ、Ⅳ分别表示二氨合银离子、一氨合银离子、
银离子、氯离子与氨气浓度对数变化的曲线,则 时,溶液中
,故D正确;故选A。
2.(2023·北京·统考高考真题)利用平衡移动原理,分析一定温度下 在不同 的 体系中的
可能产物。
已知:i.图1中曲线表示 体系中各含碳粒子的物质的量分数与 的关系。
ii.2中曲线Ⅰ的离子浓度关系符合 ;曲线Ⅱ的离子浓度关系符合
[注:起始 ,不同 下 由图1得到]。下列说法不正确的是
A.由图1,
B.由图2,初始状态 ,无沉淀生成
C.由图2,初始状态 ,平衡后溶液中存在
D.由图1和图2,初始状态 、 ,发生反应:
【答案】C
【解析】A.水溶液中的离子平衡 从图1可以看出 时,碳酸氢根离子与碳酸根离子浓度相同,
A项正确;B.从图2可以看出 、 时,该点位于曲线Ⅰ和曲线Ⅱ的下方,不会产
生碳酸镁沉淀或氢氧化镁沉淀,B项正确;C.从图2可以看出 、 时,该点位于曲
线Ⅱ的上方,会生成碳酸镁沉淀,根据物料守恒,溶液中 ,C
项错误;D. 时,溶液中主要含碳微粒是 , , 时,该点位于曲线Ⅱ的
上方,会生成碳酸镁沉淀,因此反应的离子方程式为 ,D项正确;
故选C。
3.(2023·山东·统考高考真题)在含HgI (g)的溶液中,一定c(I-)范围内,存在平衡关系:
2
; ; ; ;
,平衡常数依次为 。已知 、 , 、
随 的变化关系如图所示,下列说法错误的是A.线 表示 的变化情况
B.随 增大, 先增大后减小
C.
D.溶液中I元素与 元素的物质的量之比始终为
【答案】B
【分析】由题干反应方程式 可知,K= ,则有c(Hg2+)= ,则有
1
lgc(Hg2+)=lgK +lgc(HgI )-2lgc(I-),同理可得:lgc(HgI+)=lgK +lgc(HgI )-lgc(I-), =lgK +lgc(HgI )+
1 2 2 2 3 2
lgc(I-), ==lgK+lgc(HgI )+ 2lgc(I-),且由 可知K= 为一定值,
4 2 0
故可知图示中 曲线1、2、3、4即L分别代表 、
、 、 ,据此分析解题。
【解析】A.由分析可知,线 表示 的变化情况,A正确;B.已知 的化学
平衡常数K= ,温度不变平衡常数不变,故随 增大, 始终保持不变,B错误;
0
C.由分析可知,曲线1方程为:lgc(Hg2+)=lgK +lgc(HgI )-2lgc(I-),曲线2方程为:
1 2
lgc(HgI+)=lgK +lgc(HgI )-lgc(I-)即有①b= lgK+lgc(HgI )-2a,②b= lgK+lgc(HgI )-a,联合①②可知得:
2 2 1 2 2 2
,C正确;D.溶液中的初始溶质为HgI ,根据原子守恒可知,该溶液中I元素与 元
2
素的物质的量之比始终为 ,D正确;故答案为:B。
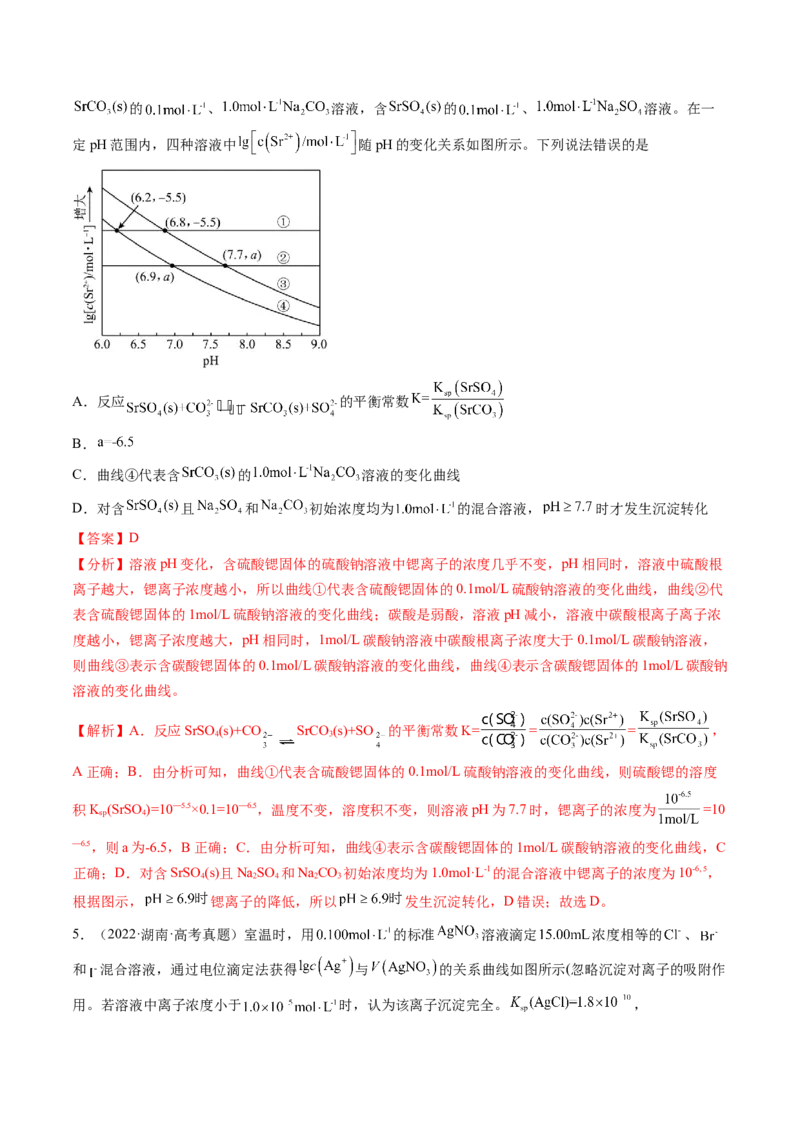
4.(2022·山东·高考真题)工业上以 为原料生产 ,对其工艺条件进行研究。现有含的 、 溶液,含 的 、 溶液。在一
定pH范围内,四种溶液中 随pH的变化关系如图所示。下列说法错误的是
A.反应 的平衡常数
B.
C.曲线④代表含 的 溶液的变化曲线
D.对含 且 和 初始浓度均为 的混合溶液, 时才发生沉淀转化
【答案】D
【分析】溶液pH变化,含硫酸锶固体的硫酸钠溶液中锶离子的浓度几乎不变,pH相同时,溶液中硫酸根
离子越大,锶离子浓度越小,所以曲线①代表含硫酸锶固体的0.1mol/L硫酸钠溶液的变化曲线,曲线②代
表含硫酸锶固体的1mol/L硫酸钠溶液的变化曲线;碳酸是弱酸,溶液pH减小,溶液中碳酸根离子离子浓
度越小,锶离子浓度越大,pH相同时,1mol/L碳酸钠溶液中碳酸根离子浓度大于0.1mol/L碳酸钠溶液,
则曲线③表示含碳酸锶固体的0.1mol/L碳酸钠溶液的变化曲线,曲线④表示含碳酸锶固体的1mol/L碳酸钠
溶液的变化曲线。
【解析】A.反应SrSO (s)+CO SrCO (s)+SO 的平衡常数K= = = ,
4 3
A正确;B.由分析可知,曲线①代表含硫酸锶固体的0.1mol/L硫酸钠溶液的变化曲线,则硫酸锶的溶度
积K (SrSO )=10—5.5×0.1=10—6.5,温度不变,溶度积不变,则溶液pH为7.7时,锶离子的浓度为 =10
sp 4
—6.5,则a为-6.5,B正确;C.由分析可知,曲线④表示含碳酸锶固体的1mol/L碳酸钠溶液的变化曲线,C
正确;D.对含SrSO (s)且NaSO 和NaCO 初始浓度均为1.0mol·L-1的混合溶液中锶离子的浓度为10-6, 5,
4 2 4 2 3
根据图示, 锶离子的降低,所以 发生沉淀转化,D错误;故选D。
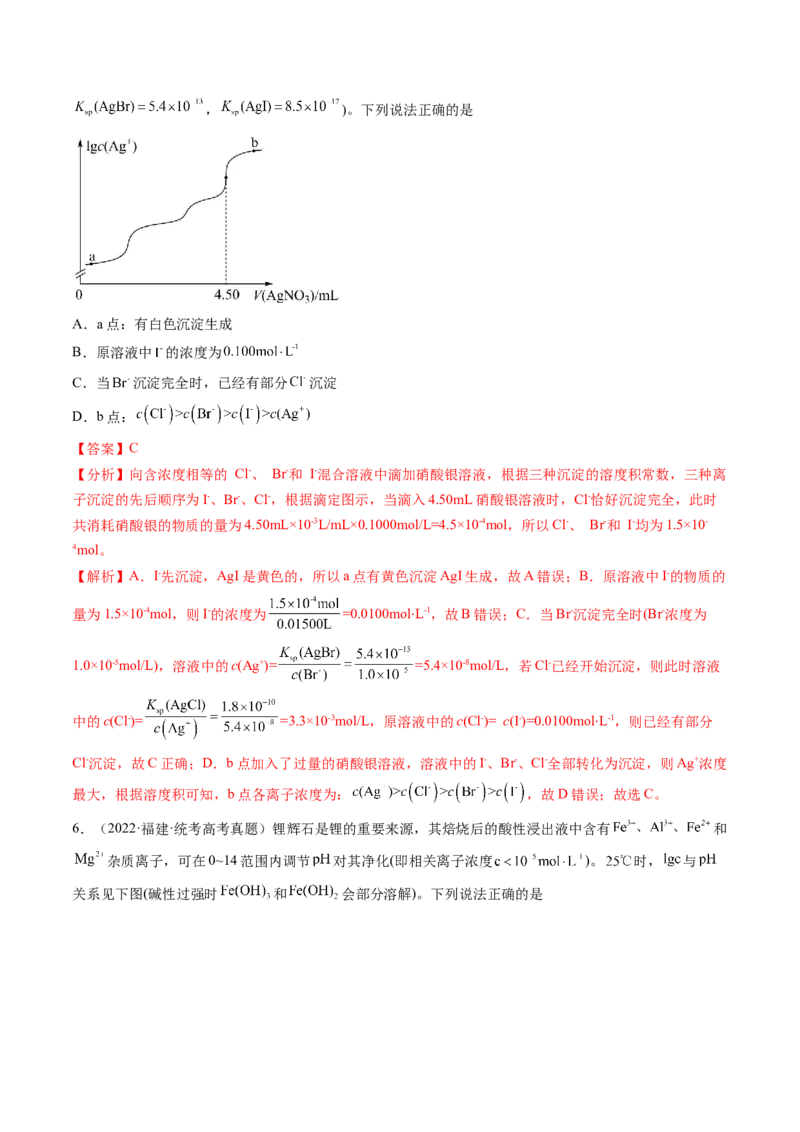
5.(2022·湖南·高考真题)室温时,用 的标准 溶液滴定 浓度相等的 、
和 混合溶液,通过电位滴定法获得 与 的关系曲线如图所示(忽略沉淀对离子的吸附作
用。若溶液中离子浓度小于 时,认为该离子沉淀完全。 ,, )。下列说法正确的是
A.a点:有白色沉淀生成
B.原溶液中 的浓度为
C.当 沉淀完全时,已经有部分 沉淀
D.b点:
【答案】C
【分析】向含浓度相等的 Cl-、 Br-和 I-混合溶液中滴加硝酸银溶液,根据三种沉淀的溶度积常数,三种离
子沉淀的先后顺序为I-、Br-、Cl-,根据滴定图示,当滴入4.50mL硝酸银溶液时,Cl-恰好沉淀完全,此时
共消耗硝酸银的物质的量为4.50mL×10-3L/mL×0.1000mol/L=4.5×10-4mol,所以Cl-、 Br-和 I-均为1.5×10-
4mol。
【解析】A.I-先沉淀,AgI是黄色的,所以a点有黄色沉淀AgI生成,故A错误;B.原溶液中I-的物质的
量为1.5×10-4mol,则I-的浓度为 =0.0100molL-1,故B错误;C.当Br-沉淀完全时(Br-浓度为
⋅
1.0×10-5mol/L),溶液中的c(Ag+)= =5.4×10-8mol/L,若Cl-已经开始沉淀,则此时溶液
中的c(Cl-)= =3.3×10-3mol/L,原溶液中的c(Cl-)= c(I-)=0.0100molL-1,则已经有部分
⋅
Cl-沉淀,故C正确;D.b点加入了过量的硝酸银溶液,溶液中的I-、Br-、Cl-全部转化为沉淀,则Ag+浓度
最大,根据溶度积可知,b点各离子浓度为: ,故D错误;故选C。
6.(2022·福建·统考高考真题)锂辉石是锂的重要来源,其焙烧后的酸性浸出液中含有 和
杂质离子,可在0~14范围内调节 对其净化(即相关离子浓度 )。 时, 与
关系见下图(碱性过强时 和 会部分溶解)。下列说法正确的是A. 可被净化的 区间最大
B.加入适量 ,可进一步提升净化程度
C.净化的先后顺序:
D.
【答案】B
【解析】A.对离子净化时,相关离子浓度c<10-5mol/L,则lgc<-5,由图可知,可作净化的pH区间最大的
是Fe3+,A错误;B.加入适量HO,可将Fe2+氧化为Fe3+,提高净化程度,B正确;C.由图可知,净化
2 2
的先后顺序为 ,C错误;D.对离子净化时,相关离子浓度c<10-5mol/L,
lgc<-5,,由图可知,Fe3+完全沉淀的pH约为2.5,c(H+)=10-2.5mol/L,c(OH-)=10-11.5mol/L,
,Al3+完全沉淀的pH约为4.5,c(H+)=10-4.5mol/L,
c(OH-)=10-9.5mol/L, ,Fe2+完全沉淀的pH约为8.5,
c(H+)=10-8.5mol/L,c(OH-)=10-5.5mol/L, ,则有
,D错误;故选B。