文档内容
第 32 讲 无机化工流程题的解题策略
(模拟精练+真题演练)
完卷时间:50分钟
一、选择题(共12×5分)
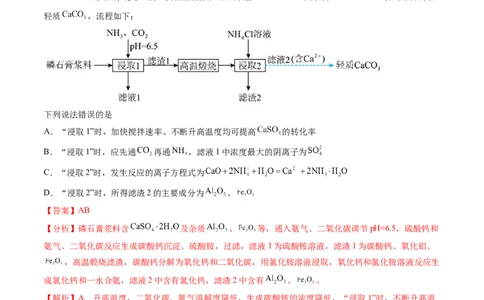
1.(2023·山东聊城·统考一模)实验室模拟以磷石膏(含 及杂质 、 等)为原料制取
轻质 ,流程如下:
下列说法错误的是
A.“浸取1”时,加快搅拌速率、不断升高温度均可提高 的转化率
B.“浸取1”时,应先通 再通 ,滤液1中浓度最大的阴离子为
C.“浸取2”时,发生反应的离子方程式为
D.“浸取2”时,所得滤渣2的主要成分为 、
【答案】AB
【分析】磷石膏浆料含 及杂质 、 等,通入氨气、二氧化碳调节pH=6.5,硫酸钙和
氨气、二氧化碳反应生成碳酸钙沉淀、硫酸铵,过滤,滤液1为硫酸铵溶液,滤渣1为碳酸钙、氧化铝、
,高温煅烧滤渣,碳酸钙分解为氧化钙和二氧化碳,用氯化铵溶液浸取,氧化钙和氯化铵溶液反应生
成氯化钙和一水合氨,滤液2中含有氯化钙,滤渣2中含有 、 。
【解析】A.升高温度,二氧化碳、氨气溶解度降低,生成碳酸铵的浓度降低,“浸取1”时,不断升高温
度,不一定能提高 的转化率,故A错误;B.氨气的溶解度大于二氧化碳,为增大二氧化碳的溶解
度,“浸取1”时,应先通 再通 ,硫酸钙和氨气、二氧化碳反应生成碳酸钙沉淀、硫酸铵,微溶的
硫酸钙转化为更难溶的碳酸钙,滤液1的成分主要是硫酸铵,浓度最大的阴离子为 ,故B错误;
C.“浸取2”时,氧化钙和氯化铵溶液反应生成氯化钙和一水合氨,发生反应的离子方程式为
,故C正确;D.滤渣1为碳酸钙、氧化铝、 ,高温煅烧滤渣,
碳酸钙分解为氧化钙和二氧化碳, “浸取2”时,氧化钙和氯化铵溶液反应生成氯化钙和一水合氨,所得
滤渣2的主要成分为 、 ,故D正确;选AB。2.(2023·山东聊城·统考三模)从废钼催化剂(主要成分为 ,含少量 、 、 )中回收
钼酸铵晶体的工艺流程如图所示:
注:酸浸后钼元素以 形式存在,溶液中某离子浓度 时,认为沉淀完全;常温下
, 。下列说法错误的是
A.焙烧过程中被氧化的元素有Mo、S、Fe
B.滤渣1的主要成分是
C.“调pH”过程中调节溶液的pH略大于2.83,可除去目标杂质离子
D.反萃取发生的离子方程式为
【答案】AC
【分析】已知,酸浸后钼元素以 形式存在;氧气具有氧化性,废钼催化剂在焙烧过程中得到六价钼
的氧化物、氧化铜、氧化亚铁、砷的氧化物和二氧化硫气体,焙烧后固体加入硫酸酸浸,二氧化硅不反应
成为滤渣1,滤液含有钼铜铁砷的盐溶液,加入MoO 调节pH得到滤渣2氢氧化铜、氢氧化铁沉淀,滤液
3
加入萃取剂萃取出钼砷后加入氨水反萃取得到含钼砷的水相,加入氯化镁除去砷,滤液结晶得到
(NH )MoO ;【解析】A.由分析可知,焙烧过程中得到六价钼的氧化物、氧化铜、氧化亚铁、砷的氧化
4 2 4
物和二氧化硫气体,被氧化的元素有Mo、S,铁元素没有被氧化,A错误;B.由分析可知,滤渣1的主
要成分是 ,B正确;C.铁离子完全沉淀时, ,
pOH=11.12,则pH=2.83;同理,铜离子完全沉淀时, ,
pOH=7.3,则pH=6.7,故“调pH”过程中调节溶液的pH略大于6.7,可除去目标杂质离子,C错误;
D.反萃取过程中加入氨水将 转化为 得到(NH )MoO ,发生的离子方程式为
4 2 4
,D正确;故选AC。
3.(2023·江西·江西师大附中校联考模拟预测)近日,天津大学钟澄团队制备锌镍电池的负极材料——
,流程如下,已知:离心分离是借助于离心力,使比重不同的物质进行分离的方法,下列叙
述错误的是A.“反应池1”中发生的离子反应为
B.“反应池1”和“反应池2”可通过搅拌加快反应
C.“加热”时选择蒸发皿盛放ZnO和BiOI固体
D.“操作1”可以为离心分离,用于分离固体和液体混合物
【答案】C
【分析】由题给流程可知,反应池1中碘化钾溶液与硝酸铋溶液反应生成BiOI沉淀,反应池2中加入氧化
锌固体搅拌得到氧化锌和BiOI的悬浊液,过滤得到氧化锌和BiOI固体混合物;在坩埚中高温灼烧得到
。
【解析】A.由分析可知,反应池1中碘化钾溶液与硝酸铋溶液反应生成BiOI沉淀,反应的离子方程式为
,故A正确;B.由分析可知,反应池1中碘化钾溶液与硝酸铋溶液反应生成
BiOI沉淀,反应池2中加入氧化锌固体搅拌得到氧化锌和BiOI的悬浊液,物质在溶液中混合时可通过搅
拌加快反应,故B正确;C.固体灼烧时应在坩埚中进行,不能在蒸发皿中进行,故C错误;D.由分析
可知,操作1为离心分离,目的是过滤得到氧化锌和BiOI固体混合物,故D正确;故选C。
4.(2023·山东菏泽·山东省鄄城县第一中学校考三模)加碘食盐中加入的碘酸钾是一种白色结晶粉末,常
温下很稳定,加热至560℃开始分解。在酸性条件下碘酸钾是一种较强的氧化剂,可与碘化物、亚硫酸盐
等还原性物质反应。工业上生产碘酸钾的流程如下。
已知:20℃ 的溶解度为8.08g,50℃ 的溶解度为10.20g,100℃ 的溶解度为15.30g。
下列说法不正确的是
A.步骤①反应器发生的反应为
B.步骤②中可用氢氧化钠代替KOH
C.步骤②中氢氧化钾的主要作用是将 转化为
D.步骤③的操作为加热浓缩、冷却结晶
【答案】B
【分析】由框图可知:碘酸钾是一种较强的氧化剂,加入氯水增加溶液的酸性,生成 ,在加水和氢
氧化钾调节溶液酸碱性,得到 溶液,在经过蒸发浓缩、冷却结晶即得 晶体。
【解析】A.根据流程可知,步骤①反应器发生的反应为 ,
A正确;B.步骤②中可用氢氧化钠代替KOH,则会导致产品中混入碘酸钠杂质,B错误;C.碘单质与
氯酸钾在水中发生反应产生KH(IO),加入KOH时可以使之转化为KIO ,C正确;D.根据信息可知,
3 2 3.
的溶解度随温度变化较大,故步骤③的操作为加热浓缩、冷却结晶,D正确;故选B。5.(2023·浙江温州·乐清市知临中学校考一模)辉铜矿[ ,含 杂质]合成
目标产物的流程如下。下列说法正确的是
A.步骤Ⅰ在足量 中煅烧产生气体的主要成分:
B.步骤Ⅱ得溶液 中溶质的主要成分: 和
C.步骤Ⅲ的溶液D中存在平衡平衡:
D.为得纯净目标产物,步骤Ⅳ的实验操作步骤依次:加热蒸发、冷却结晶、抽滤洗涤。
【答案】C
【分析】辉铜矿通入氧气进行煅烧,发生反应 ,固体B为CuO和 ,
加入盐酸得到Cu2+、Fe3+、Fe2+的溶液,加入过量氨水,得到氢氧化铁、氢氧化亚铁、Cu[(NH )]Cl 。
3 4 2
【解析】A. 步骤Ⅰ在足量 中煅烧时,发生的化学方程式为: ,产生气体
的主要成分为 ,故A错误;B. 步骤Ⅱ得溶液 中溶质的主要成分: 、 和 ,故B错误;
C. 步骤Ⅲ的溶液D中存在平衡平衡: ,故C正确;D. 从流程
看,溶液D中阴离子主要为氯离子,为得纯净目标产物,溶液D中应引入硫酸根,再向滤液中加入乙醇,
再过滤、洗涤、干燥,故D错误。答案为C。
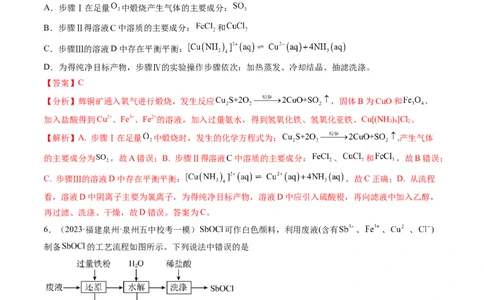
6.(2023·福建泉州·泉州五中校考一模) 可作白色颜料,利用废液(含有 、 、 、 )
制备 的工艺流程如图所示。下列说法中错误的是
A.“还原”流程中,“滤渣”的成分有铜和铁
B.“水解”流程中,加水能够促进 的水解
C.“水解”流程的离子反应是
D.“洗涤”流程加入的稀盐酸能换成 溶液
【答案】D
【分析】废液加入铁粉发生Fe+2Fe3+=3Fe2+和Fe+Cu2+=Fe2++Cu两个反应,滤渣中有生成的铜和过量的铁,
加水稀释可以让Sb3+离子水解生成SbOCl,最后用稀盐酸洗去表面的杂质离子如Fe2+。【解析】A.废液加入铁粉发生Fe+2Fe3+=3Fe2+和Fe+Cu2+=Fe2++Cu两个反应,滤渣中有生成的铜和过量的
铁,故A正确;B.越稀越水解,加水可以降低氢离子浓度,水解正向移动,可以促进水解,故B正确;
C.Sb3+水解生成SbOCl沉淀同时生成氢离子,方程式正确,故C正确;D.“洗涤”流程加入的稀盐酸能
换成 溶液,会引入Na+杂质,故D错误;答案选D。
7.(2023·山东济南·山东省实验中学校考模拟预测)连二亚硫酸钠( )常用于纺织工业、食品漂白
等领域。工业上生产 的流程如图所示。若在实验室模拟该工艺流程,下列说法错误的是
A.将锌粉投入水中形成悬浮液主要是为了加快反应速率
B.向 溶液中加入NaCl固体对 的产率无明显影响
C.洗涤 时用乙醇效果好于蒸馏水
D.该流程中涉及化合反应、分解反应、复分解反应
【答案】B
【分析】由流程图可知,锌粉与二氧化硫反应生成ZnS O,向ZnS O 溶液中加入氢氧化钠溶液,两者反应
2 4 2 4
生成氢氧化锌沉淀和NaSO,过滤后向NaSO 溶液中加入NaCl固体降低NaSO 溶解度,析出
2 2 4 2 2 4 2 2 4
NaSO·2H O晶体,过滤后加热NaSO·2H O晶体脱去结晶水生成NaSO。
2 2 4 2 2 2 4 2 2 2 4
【解析】A.将锌粉投入水中形成悬浮液可增大与二氧化硫的接触面积,加快反应速率,A正确;B.加
NaCl固体和冷却搅拌都有利于溶解平衡逆向移动,可析出更多的NaSO·2H O,若使用NaCl溶液,会降
2 2 4 2
低钠离子浓度使析出的NaSO·2H O减少,NaSO 产率降低,B错误;C.乙醇沸点低易挥发便于干燥,
2 2 4 2 2 2 4
故洗涤 时用乙醇效果好于蒸馏水,C正确;D.锌粉与二氧化硫的反应是化合反应,反应中
元素有化合价变化,也是氧化还原反应,ZnS O 溶液与NaOH溶液的反应是复分解反应,加热
2 4
NaSO·2H O生成NaSO 的反应是分解反应,D正确;故选B。
2 2 4 2 2 2 4
8.(2023·福建泉州·福建省泉州第一中学校考模拟预测)以锆矿石(主要成分为 ,还含有 及钠、
铝、铜的氧化物等杂质)为原料制备工业纯 的工艺流程如图:
下列说法错误的是
A.“高温氯化”结束前通一段时间氧气的目的是除去过量的炭黑B.“溶液1”中含有的溶质主要为NaCl、NaOH、
C.“碱浸”后分离操作要用到的玻璃仪器有烧杯、玻璃棒、漏斗
D.“除杂”的目的是除去铜元素
【答案】B
【分析】“高温氯化”可以把氧化物转化为氯化物,ZrO₂与C和氯气发生反应方程式为ZrO₂+2Cl₂+C
ZrCl+CO ↑,同时生成氯化铜、氯化铝等,加入“过量的NaOH稀溶液”将氯化物转化为沉淀,并将AlCl
4 2 3
转化为 而除去,溶液1成分为NaCl、NaAlO 、Na₂SiO₃,加入NaOH浓溶液得到[Cu(OH) ]2-和
2 4
Zr(OH) 沉淀,焙烧分解可得ZrO₂。
4
【解析】A.C可以和氧气高温反应生产CO₂,结束前通一段时间氧气的目的是除去过量的炭黑,故A正
确;B.根据分析,溶液1成分为NaCl、NaAlO₂、NaOH、Na₂SiO ,故B错误;C.碱浸后分离操作为除
3
去氢氧化铜,为过滤,要用到的玻璃仪器有烧杯、玻璃棒、漏斗,故C正确;D.除杂的目的是分离氢氧
化铜,除去铜元素,故D正确;答案选B。
9.(2023·江苏连云港·连云港高中校考模拟预测)氧化钪( )广泛应用于航天、激光等科学领域。利用
钛白酸性废水(含 、 、 等)制备氧化钪的工艺具有较高的经济价值,其流程如下图所示。
已知: 、 均能与P504(用HR表示)发生络合反应,且机理均为 。下列说
法不正确的是
A.酸洗时, 、 与P504的络合能力:
B.萃取、反萃取后均可使用分液漏斗分离,有机相应从分液漏斗上口倒出
C.“反萃取”时加入NaOH溶液的作用是将 转化为
D.沉钪时能得到 ,则焙烧时的反应方程式:
【答案】C
【解析】A.由向有机相中加入稀硫酸后 先被洗出可知,与P504的络合能力 ,A正确;
B.煤油的密度小于水的密度,“萃取”时,有机相应从分液漏斗上口倒出,B正确;C.“反萃取”时加
入NaOH溶液的作用是利用NaOH与Sc3+反应,使得络合反应不断左移,将Sc3+从络合物当中释放出来,C
错误;D.沉钪时能得到 ,则焙烧时与氧气发生氧化还原反应,根据得失电子守恒,原子守恒得 ,D正确;故选C。
10.(2023·湖南·校联考模拟预测)中国“天向一号”探测器用于火星探测,搭载全球最先进的三结砷化
镓太阳能电池阵为其提供动力,一种从砷化镓废料(主要成分为 ,含 、 、 等杂质)中
回收单质镓和砷的化合物的工艺流程如图所示:
已知:①“碱当”时 中Ga以 的形式进入溶液。
②Ga与Al位于同一主族,性质相似,向 溶液中通入 ,有 沉淀析出。
③离子完全沉淀时的pH: 为8, 为5.6。
下列说法正确的是
A.“碱浸”时, 发生的离子方程式为
B.“滤渣①”的成分为 , ,“滤渣③”的成分为
C.“调pH①”时,为使得杂质离子沉淀完全,可通入过量的
D.“系列操作”为蒸发结晶、过滤、洗涤、干燥
【答案】A
【分析】砷化镓废料粉碎增大碱浸速率,加氢氧化钠和过氧化氢, 和 溶解生成 、 和
, 、 不溶于碱,“滤渣①”为 、 ,滤液通 可以得硅酸,除去硅元素,
滤液再通 可以将 转化为 ,过滤,滤液为 ,经过蒸发浓缩、冷却结晶可以得到
, 沉淀加 溶液生成 溶液,通电电解得到镓单质。
【解析】A.“碱浸”时 中Ga以 的形式进入溶液,As会被 氧化生成 ,根据
得失电子守恒和电荷守恒、原子守恒得出反应的离子方程式为
,故A正确;B.根据分析可知, 、 不溶于
溶液,“滤渣①”的成分为 、 ,向含有 、 和 的溶液中,先通入 先
得硅酸沉淀,除去硅元素,然后再通 可以将 转化为 ,“滤渣③”的成分为 ,
故B错误;C.通入过量的 ,会使 过早沉淀下来,使产率降低,故C错误;D.滤液为
,析出带结晶水的晶体要经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥,可以得到
,故D错误;答案选A。
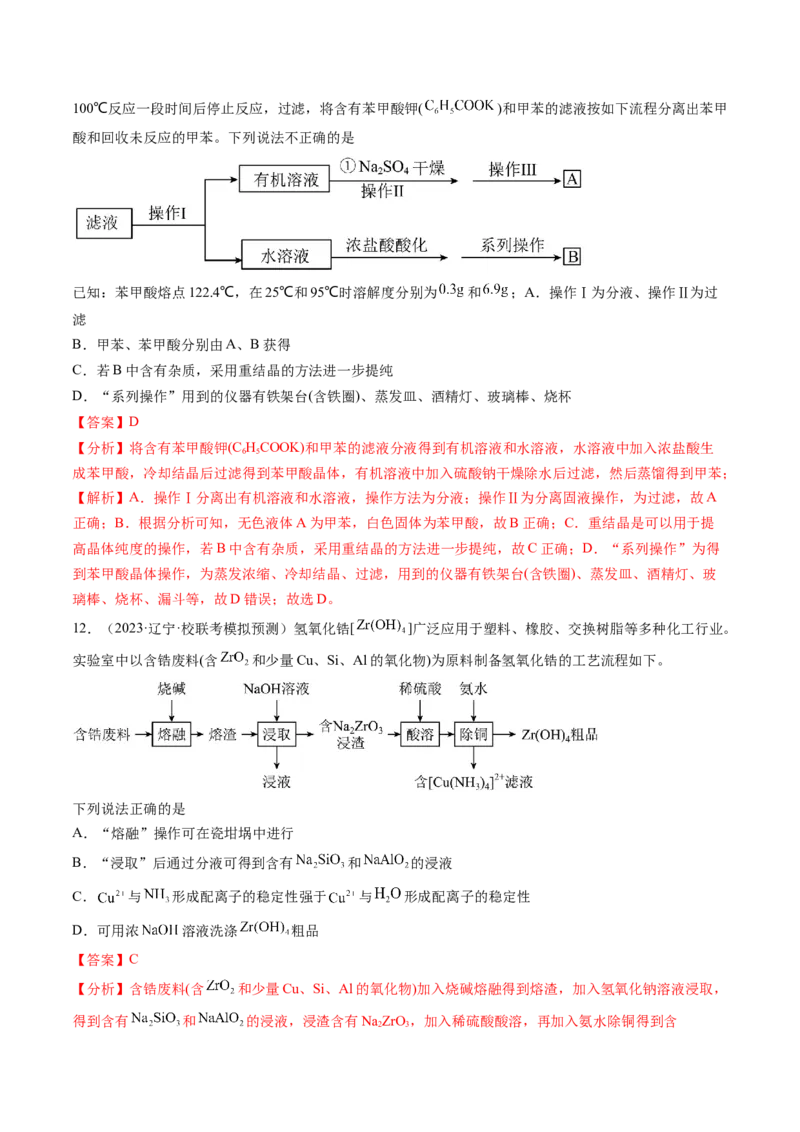
11.(2023·山东聊城·统考三模)用 氧化甲苯制备苯甲酸。实验方法:将甲苯和 溶液在100℃反应一段时间后停止反应,过滤,将含有苯甲酸钾( )和甲苯的滤液按如下流程分离出苯甲
酸和回收未反应的甲苯。下列说法不正确的是
已知:苯甲酸熔点122.4℃,在25℃和95℃时溶解度分别为 和 ;A.操作Ⅰ为分液、操作Ⅱ为过
滤
B.甲苯、苯甲酸分别由A、B获得
C.若B中含有杂质,采用重结晶的方法进一步提纯
D.“系列操作”用到的仪器有铁架台(含铁圈)、蒸发皿、酒精灯、玻璃棒、烧杯
【答案】D
【分析】将含有苯甲酸钾(C HCOOK)和甲苯的滤液分液得到有机溶液和水溶液,水溶液中加入浓盐酸生
6 5
成苯甲酸,冷却结晶后过滤得到苯甲酸晶体,有机溶液中加入硫酸钠干燥除水后过滤,然后蒸馏得到甲苯;
【解析】A.操作Ⅰ分离出有机溶液和水溶液,操作方法为分液;操作Ⅱ为分离固液操作,为过滤,故A
正确;B.根据分析可知,无色液体A为甲苯,白色固体为苯甲酸,故B正确;C.重结晶是可以用于提
高晶体纯度的操作,若B中含有杂质,采用重结晶的方法进一步提纯,故C正确;D.“系列操作”为得
到苯甲酸晶体操作,为蒸发浓缩、冷却结晶、过滤,用到的仪器有铁架台(含铁圈)、蒸发皿、酒精灯、玻
璃棒、烧杯、漏斗等,故D错误;故选D。
12.(2023·辽宁·校联考模拟预测)氢氧化锆[ ]广泛应用于塑料、橡胶、交换树脂等多种化工行业。
实验室中以含锆废料(含 和少量Cu、Si、Al的氧化物)为原料制备氢氧化锆的工艺流程如下。
下列说法正确的是
A.“熔融”操作可在瓷坩埚中进行
B.“浸取”后通过分液可得到含有 和 的浸液
C. 与 形成配离子的稳定性强于 与 形成配离子的稳定性
D.可用浓 溶液洗涤 粗品
【答案】C
【分析】含锆废料(含 和少量Cu、Si、Al的氧化物)加入烧碱熔融得到熔渣,加入氢氧化钠溶液浸取,
得到含有 和 的浸液,浸渣含有NaZrO,加入稀硫酸酸溶,再加入氨水除铜得到含
2 3滤液和 粗品;
【解析】A.瓷坩埚中含二氧化硅,烧碱在高温条件下与二氧化硅反应,会腐蚀瓷坩埚,选项A错误;
B.分离溶液和难溶物需用过滤,选项B错误;C.在水溶液中 稳定存在,则 与 形
成配离子的稳定性强于 与 形成配离子的稳定性,选项C正确;D.由转化关系推知, 为两
性氧化物,则 为两性氢氧化物,能溶于浓 溶液,选项D错误;答案选C。
二、主观题(共3小题,共40分)
13.(12分)(2023·海南·校联考一模)以电镀污泥[含Ni(OH) 、Fe(OH) 、Cr(OH) 和SiO]为原料,利用
2 3 3 2
以下工艺可制备硫酸镍晶体(NiSO ·6H O)并获得副产品黄钠铁矾[NaFe (SO )(OH) ]。
4 2 3 4 2 6
已知:黄钠铁矾沉淀易于过滤,相对于Fe(OH) ,沉淀不易吸附Ni2+。
3
请回答下列问题:
(1)①下列措施不能提高“酸浸”过程浸出率的是 (填字母)。
a.适当升高反应温度 b.增大压强 c.不断搅拌
②滤渣1的主要成分的化学式为 。
(2)“沉铁”时NaCO 加入速度不宜过快,原因是 。
2 3
(3)“沉铬”过程中发生反应的离子方程式为 。
(4)一系列操作的实验步骤依次如下,请补充相关内容:
i.过滤、洗涤;
ii.将沉淀转移至烧杯中,向其中 ;
iii. ,过滤得 晶体。
【答案】(每空2分)(1)b SiO
2
(2)避免溶液的碱性太强,产生Fe(OH) ,Fe(OH) 吸附大量的Ni2+,造成Ni2+的损失
3 3
(3)Cr3++ =CrPO↓
4
(4)加入稀硫酸将固体完全溶解 将滤液蒸发浓缩、冷却结晶
【分析】由题干工艺流程图可知,以电镀污泥[含Ni(OH) 、Fe(OH) 、Cr(OH) 和SiO]为原料,加入稀硫酸
2 3 3 2
进行酸浸后,将Ni(OH) 、Fe(OH) 、Cr(OH) 分别转化为NiSO 、Fe (SO )、Cr (SO ) 溶液,过滤出滤渣1
2 3 3 4 2 4 3 2 4 3
主要成分为SiO,向滤液中加入NaCO 将Fe3+转化为黄钠铁矾沉淀,过滤出黄钠铁矾,继续向滤液中加入
2 2 3
NaPO 进行沉铬即将Cr3+转化为CrPO 沉淀,过滤出滤渣2即CrPO ,在向滤液中加入NaCO 进行沉镍,
3 4 4 4 2 3
然后过滤,洗涤沉淀NiCO,向固体NiCO 中加入稀硫酸将固体完全溶解,过滤洗涤后将滤液蒸发浓缩、
3 3
冷却结晶,过滤洗涤、低温干燥,即可得到硫酸镍晶体(NiSO ·6H O),据此分析解题。
4 2
【解析】(1)①a.适当升高反应温度,反应速率加快,能够提高“酸浸”过程浸出率,a不合题意;b.增大压强,对于溶液的浓度几乎无影响,故不能提高“酸浸”过程浸出率,b符合题意;c.不断搅拌,可
以使反应物充分接触,加快反应速率,故能够提高“酸浸”过程浸出率,c不合题意;故答案为:b;
②由分析可知,滤渣1的主要成分的化学式为SiO,故答案为:SiO;
2 2
(2)已知NaCO 溶液呈碱性,故“沉铁”时若NaCO 加入速度过快,导致溶液的碱性增强,产生
2 3 2 3
Fe(OH) ,Fe(OH) 吸附大量的Ni2+,造成Ni2+的损失,故答案为:避免溶液的碱性太强,产生Fe(OH) ,
3 3 3
Fe(OH) 吸附大量的Ni2+,造成Ni2+的损失;
3
(3)由分析可知,“沉铬”过程中发生反应为Cr (SO )+2Na PO =CrPO+3Na SO ,该反应的离子方程式
2 4 3 3 4 4 2 4
为Cr3++ =CrPO↓,故答案为:Cr3++ =CrPO↓;
4 4
(4)由分析可知,一系列操作的实验步骤依次为:i.在向滤液中加入NaCO 进行沉镍,然后过滤,洗涤
2 3
沉淀NiCO,ii.将沉淀转移至烧杯中,向固体NiCO 中加入稀硫酸将固体完全溶解,iii.过滤洗涤后将滤
3 3
液蒸发浓缩、冷却结晶,过滤洗涤、低温干燥,即可得到硫酸镍晶体(NiSO ·6H O),故答案为:加入稀硫
4 2
酸将固体完全溶解;将滤液蒸发浓缩、冷却结晶。
14.(14分)(2023·福建宁德·统考一模)钴盐在生活和生产中有着重要应用。
(1)在活性炭的催化作用下,通过氧化CoCl ·6H O制得到[Co(NH )]Cl 流程如下:
2 2 3 6 3
①在“氧化”过程,需水浴控温在50~60℃,温度不能过高,原因是: 。“系列操作”是指在高浓度
的盐酸中使[Co(NH )]Cl 结晶析出,过滤,醇洗,干燥。使用乙醇洗涤产品的具体操作是: 。
3 6 3
②结束后废水中的Co2+,人们常用FeS沉淀剂来处理,原理是 (用离子方程式表示)。
(2)草酸钴是制备钴氧化物的重要原料,常用(NH )C O 溶液和CoCl 溶液制取难溶于水的CoC O·2H O晶
4 2 2 4 2 2 4 2
体。
①常温下,(NH )C O 溶液的pH 7(填“>”、“=”或“<”)。(已知:常温下K(NH ·H O)=1.8×10-5,
4 2 2 4 b 3 2
HC O:K =5.6×10-2,K =5.4×10-5)
2 2 4 a1 a2
②制取CoC O·2H O晶体时,还需加入适量氨水,其作用是 。
2 4 2
③在空气中加热10.98g二水合草酸钴(CoC O·2H O),受热过程中在不同温度范围内分别得到一种固体物
2 4 2
质。已知Co的两种常见化合价为+2价和+3价,M(CoC O·2H O)=183g/mol。
2 4 2
温度范围/℃ 150~210 290~320
固体质量/g 8.82 4.82
i.温度在 范围内,固体物质为 (填化学式);
ii.从 加热到 时生成一种钴的氧化物和CO,此过程发生反应的化学方程式是 。
2
【答案】(每空2分)(1)温度过高,HO 大量分解,降低产率 向漏斗中注入乙醇使其浸没沉淀,待乙醇
2 2
自然流下,重复操作2~3次 Co2++FeS=CoS+Fe2+
(2)< 抑制(NH )C O 的水解,提高 的利用率(或“调节溶液pH,提高草酸钴晶体的产率”等)
4 2 2 4
CoC O 3CoC O+2O Co O+6CO
2 4 2 4 2 3 4 2【分析】CoCl ·6H O加氯化铵溶液和活性炭,再加浓氨水,反应生成[Co(NH )]Cl ,在加5%H O 氧化
2 2 3 6 2 2 2
[Co(NH )]Cl 生成[Co(NH )]Cl ,再经浓缩、结晶、过滤、洗涤、干燥等操作得到[Co(NH )]Cl ;
3 6 2 3 6 3 3 6 3
【解析】(1)①氧化过程中使用的氧化剂为HO,不稳定,受热易分解,温度过高,HO 大量分解,降
2 2 2 2
低产率;使用乙醇洗涤产品的具体操作是:向漏斗中注入乙醇使其浸没沉淀,待乙醇自然流下,重复操作
2~3次;
②结束后废水中的Co2+,人们常用FeS沉淀剂来处理,原理是Co2++FeS=CoS+Fe2+;
(2)①K(NH ·H O)9时,会导致 。
(5)“分离钒”步骤中,将溶液pH调到1.8左右得到VO 沉淀,VO 在pH<1时,溶解为VO 或VO3+在碱
2 5 2 5
性条件下,溶解为VO 或VO ,上述性质说明VO 具有 (填标号)。
2 5
A.酸性 B.碱性 C.两性
(6)“还原”步骤中加入焦亚硫酸钠(Na SO)溶液,反应的离子方程式为 。
2 2 5
【答案】(1)Na CrO
2 4
(2)Fe O
2 3
(3)Al(OH)
3
(4)磷酸根会与H+反应使其浓度降低导致MgNH PO 无法完全沉淀,同时可能产生硅酸胶状沉淀不宜处理
4 4
会导镁离子生成氢氧化镁沉淀,不能形成MgSiO 沉淀,导致产品中混有杂质,同时溶液中铵根离子浓度
3
降低导致MgNH PO 无法完全沉淀
4 4(5)C
(6)2Cr O +3S O +10H+=4Cr3++6SO +5H O
2 2 2
【分析】由题给流程可知,铬钒渣在氢氧化钠和空气中煅烧,将钒、铬、铝、硅、磷等元素转化为相应的
最高价含氧酸盐,煅烧渣加入水浸取、过滤得到含有二氧化硅、氧化铁的滤渣和滤液;向滤液中加入稀硫
酸调节溶液pH将Al元素转化为氢氧化铝沉淀,过滤得到强氧化铝滤渣和滤液;向滤液中加入硫酸镁溶液、
硫酸铵溶液将硅元素、磷元素转化为MgSiO 和MgNH PO 沉淀,过滤得到含有MgSiO 、MgNH PO 的滤
3 4 4 3 4 4
渣和滤液;向滤液中加入稀硫酸调节溶液pH将钒元素转化为五氧化二钒,过滤得到五氧化二钒和滤液;
向滤液中焦亚硫酸钠溶液将铬元素转化为三价铬离子,调节溶液pH将铬元素转化为氢氧化铬沉淀,过滤
得到氢氧化铬。
【解析】(1)由分析可知,煅烧过程中,铬元素转化为铬酸钠,故答案为:NaCrO;
2 4
(2)由分析可知,水浸渣中主要有二氧化硅、氧化铁,故答案为:Fe O;
2 3
(3)由分析可知,沉淀步骤调pH到弱碱性的目的是将Al元素转化为氢氧化铝沉淀,故答案为:
Al(OH) ;
3
(4)由分析可知,加入硫酸镁溶液、硫酸铵溶液的目的是将硅元素、磷元素转化为MgSiO 和MgNH PO
3 4 4
沉淀,若溶液pH<9时,磷酸根会与H+反应使其浓度降低导致MgNH PO 无法完全沉淀,同时可能产生硅
4 4
酸胶状沉淀不宜处理;若溶液pH>9时,会导镁离子生成氢氧化镁沉淀,不能形成MgSiO 沉淀,导致产品
3
中混有杂质,同时溶液中铵根离子浓度降低导致MgNH PO 无法完全沉淀,故答案为:磷酸根会与H+反应
4 4
使其浓度降低导致MgNH PO ,同时可能产生硅酸胶状沉淀不宜处理;会导镁离子生成氢氧化镁沉淀,不
4 4
能形成MgSiO 沉淀,导致产品中混有杂质,同时溶液中铵根离子浓度降低导致MgNH PO 无法完全沉淀;
3 4 4
(5)由题给信息可知,五氧化二钒水能与酸溶液反应生成盐和水,也能与碱溶液发生生成盐和水的两性
氧化物,故选C;
(6)由题意可知,还原步骤中加入焦亚硫酸钠溶液的目的是将铬元素转化为铬离子,反应的离子方程式
为2Cr O +3S O +10H+=4Cr3++6SO +5H O,故答案为:2Cr O +3S O +10H+=4Cr3++6SO +5H O。
2 2 2 2 2 2
4.(2023·湖北·统考高考真题) 是生产多晶硅的副产物。利用 对废弃的锂电池正极材料
进行氯化处理以回收Li、Co等金属,工艺路线如下:
回答下列问题:
(1)Co位于元素周期表第 周期,第 族。
(2)烧渣是LiCl、 和 的混合物,“500℃焙烧”后剩余的 应先除去,否则水浸时会产生大量
烟雾,用化学方程式表示其原因 。(3)鉴别洗净的“滤饼3”和固体 常用方法的名称是 。
(4)已知 ,若“沉钴过滤”的pH控制为10.0,则溶液中 浓度为
。“850℃煅烧”时的化学方程式为 。
(5)导致 比 易水解的因素有 (填标号)。
a.Si-Cl键极性更大 b.Si的原子半径更大
c.Si-Cl键键能更大 d.Si有更多的价层轨道
【答案】(1)4 Ⅷ
(2)
(3)焰色反应
(4)
(5)abd
【分析】由流程和题中信息可知, 粗品与 在500℃焙烧时生成氧气和烧渣,烧渣是LiCl、
和 的混合物;烧渣经水浸、过滤后得滤液1和滤饼1,滤饼1的主要成分是 和 ;滤
液1用氢氧化钠溶液沉钴,过滤后得滤饼2(主要成分为 )和滤液2(主要溶质为LiCl);滤饼2
置于空气中在850℃煅烧得到 ;滤液2经碳酸钠溶液沉锂,得到滤液3和滤饼3,滤饼3为 。
【解析】(1)Co是27号元素,其原子有4个电子层,其价电子排布为 ,元素周期表第8、9、10
三个纵行合称第Ⅷ族,因此,其位于元素周期表第4周期、第Ⅷ族。
(2)“500℃焙烧”后剩余的 应先除去,否则水浸时会产生大量烟雾,由此可知,四氯化硅与可水反
应且能生成氯化氢和硅酸,故其原因是: 遇水剧烈水解,生成硅酸和氯化氢,该反应的化学方程式为
。
(3)洗净的“滤饼3”的主要成分为 ,常用焰色反应鉴别 和 , 的焰色反应为
紫红色,而 的焰色反应为黄色。故鉴别“滤饼3”和固体 常用方法的名称是焰色反应。
(4)已知 ,若“沉钴过滤”的pH控制为10.0,则溶液中
, 浓度为 。“850℃煅烧”时,
与 反应生成 和 ,该反应的化学方程式为 。
(5)a.Si-Cl键极性更大,则 Si-Cl键更易断裂,因此, 比 易水解,a有关;b.Si的原子半径
更大,因此, 中的共用电子对更加偏向于 ,从而导致Si-Cl键极性更大,且Si原子更易受到水电离
的 的进攻,因此, 比 易水解,b有关;c.通常键能越大化学键越稳定且不易断裂,因此,Si-Cl键键能更大不能说明Si-Cl更易断裂,故不能说明 比 易水解,c无关;d.Si有更多的价层
轨道,因此更易与水电离的 形成化学键,从而导致 比 易水解,d有关;综上所述,导致
比 易水解的因素有abd。
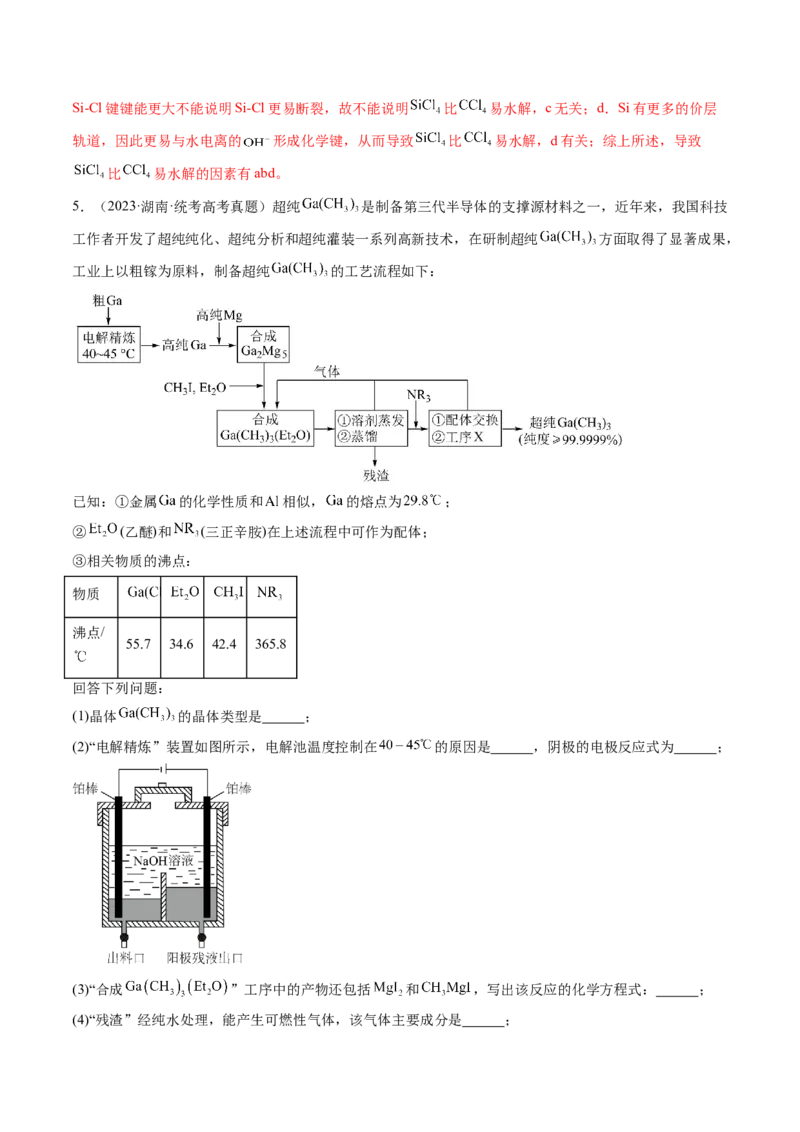
5.(2023·湖南·统考高考真题)超纯 是制备第三代半导体的支撑源材料之一,近年来,我国科技
工作者开发了超纯纯化、超纯分析和超纯灌装一系列高新技术,在研制超纯 方面取得了显著成果,
工业上以粗镓为原料,制备超纯 的工艺流程如下:
已知:①金属 的化学性质和 相似, 的熔点为 ;
② (乙醚)和 (三正辛胺)在上述流程中可作为配体;
③相关物质的沸点:
物质
沸点/
55.7 34.6 42.4 365.8
回答下列问题:
(1)晶体 的晶体类型是 ;
(2)“电解精炼”装置如图所示,电解池温度控制在 的原因是 ,阴极的电极反应式为 ;
(3)“合成 ”工序中的产物还包括 和 ,写出该反应的化学方程式: ;
(4)“残渣”经纯水处理,能产生可燃性气体,该气体主要成分是 ;(5)下列说法错误的是_______;
A.流程中 得到了循环利用
B.流程中,“合成 ”至“工序X”需在无水无氧的条件下进行
C.“工序X”的作用是解配 ,并蒸出
D.用核磁共振氢谱不能区分 和
(6)直接分解 不能制备超纯 ,而本流程采用“配体交换”工艺制备超纯
的理由是 ;
(7)比较分子中的 键角大小: (填“>”“<”或“=”),其原因是
。
【答案】(1)分子晶体
(2)保证Ga为液体,便于纯Ga流出 +3eˉ+2HO=Ga+4OH-(或[Ga(OH)]-+3eˉ=Ga+4OH-)
2 4
(3)8CH I+2EtO+Ga Mg=2 +3 +2 ;
3 2 2 5
(4)CH
4
(5)D
(6)NR 沸点较高,易与Ga(CH ) 分离,EtO的沸点低于Ga(CH ),一起气化,难以得到超纯Ga(CH )
3 3 3 2 3 3 3 3
(7)> Ga(CH ) 中Ga为sp2杂化,所以为平面结构,而Ga(CH )(Et O)中Ga为sp3杂化,所以为四面体结
3 3 3 3 2
构,故夹角较小
【分析】以粗镓为原料,制备超纯 ,粗Ga经过电解精炼得到纯Ga,Ga和Mg反应生产
GaMg,GaMg 和CHI、EtO反应生成 、MgI 和CHMgI,然后经过蒸发溶剂、蒸馏,
2 5 2 5 3 2 2 3
除去残渣MgI 、CHMgI,加入NR 进行配体交换、进一步蒸出得到超纯 ,EtO重复利用。
2 3 3 2
【解析】(1)晶体 的沸点较低,晶体类型是分子晶体;
(2)电解池温度控制在 可以保证Ga为液体,便于纯Ga流出;粗Ga在阳极失去电子,阴极得到
Ga,电极反应式为 +3eˉ+2HO=Ga+4OH-(或[Ga(OH)]-+3eˉ=Ga+4OH-);
2 4
(3)“合成 ”工序中的产物还包括 和 ,该反应的化学方程式
8CHI+2EtO+Ga Mg=2 +3 +2 ;
3 2 2 5
(4)“残渣”含 ,经纯水处理,能产生可燃性气体CH;
4
(5)A.根据分析,流程中 得到了循环利用,A正确;B. 容易和水反应,容易被氧
化,则流程中,“合成 ”至“工序X”需在无水无氧的条件下进行,B正确;C. “配体交换”得到
,“工序X”先解构 后蒸出 ,C正确;D.二者甲基的环境不同,
核磁共振氢谱化学位移不同,用核磁共振氢谱能区分 和 ,D错误;故选D;(6)直接分解时由于EtO的沸点较低,与Ga(CH ) 一起蒸出,不能制备超纯 ,而本流程采用
2 3 3
“配体交换”工艺制备超纯 的理由是,根据题给相关物质沸点可知,NR 沸点远高于Ga(CH ),
3 3 3
与Ga(CH ) 易分离;
3 3
(7)分子中的 键角 > ,其原因是Ga(CH ) 中Ga为sp2杂化,所以为
3 3
平面结构,而Ga(CH )(Et O)中Ga为sp3杂化,所以为四面体结构,故夹角较小。
3 3 2