文档内容
第一章 物质及其变化
测试卷
时间:75分钟 分值:100分
可能用到的相对原子质量:H 1 C 12 O16 Mg 24 Cl 35.5 V 51
一、选择题(每小题只有一个正确选项,共15×3分)
1.(2024·河北·三模)古诗中蕴含着丰富的化学知识,下列诗句同时体现了化学反应中的物质变化和能量
变化的是
A.刘长卿的《酬张夏》中,“水声冰下咽,沙路雪中平”
B.李白的《秋浦歌》中,“炉火照天地,红星乱紫烟”
C.刘禹锡的《浪淘沙》中,“美人首饰侯王印,尽是沙中浪底来”
D.岑参的《白雪歌送武判官归京》中,“忽如一夜春风来,千树万树梨花开”
【答案】B
【解析】A.“水声冰下咽,沙路雪中平”,利用诗和景很自然地引入物质的三态变化的知识,物质并未
变化,A不符合题意;B.“炉火照天地,红星乱紫烟”,描述的是红星四溅,紫烟蒸腾的冶炼场景,是
燃烧反应,包括了物质变化和能量变化,B符合题意;C.“美人首饰侯王印,尽是沙中浪底来”,说明
金在自然界中以游离态存在,不需要冶炼还原,“沙里淘金”就是利用金与沙密度的差异,用水反复淘洗
得到,物质并未变化,属于物理变化,C不符合题意;D.“忽如一夜春风来,千树万树梨花开”,以梨
花喻雪,为水的三态变化,属于物理变化,D不符合题意;故答案选B。
2.(2024·黑龙江牡丹江·模拟预测)空气湿度增大,水汽凝结就易形成雾,灰尘、硫酸、硝酸、有机碳氢
化合物等颗粒物的浓度增大就易形成霾。下列说法不正确的是
A.防雾霾口罩的原理与过滤类似,防雾霾效果好的口罩往往呼吸阻力较大
B.PM2.5是直径小于或等于2.5微米的污染物颗粒,属于胶体粒子的直径范围
C.汽车车灯在雾霾天照出“通路”的现象属于丁达尔效应
D.可通过在燃煤烟囱上加装高压静电装置除去煤灰中的固体颗粒物
【答案】D
【解析】A.防雾霾口罩的原理与过滤、渗析类似,防雾霾效果好的口罩间隙更小,透气性更差,往往呼
吸阻力较大,A正确;B.可通过在燃煤烟囱上加装高压静电装置除去煤灰中的固体颗粒物,利用的是胶
体的电泳,B正确;C.雾霾天,汽车车灯照出“通路”的现象是空气中的气溶胶对光线发生的散射作
用,属于胶体的丁达尔效应,C正确;D.胶粒直径在1~100 nm之间,PM5是直径小于等于2.5微米的污
染物颗粒(1微米=1000纳米),不属于胶体粒子的直径范围,D错误;故选D。
3.(2024·河南南阳·二模)物质的转化是化学学习的重要内容,甲、乙、丙所代表的物质不符合如图所示
转化关系的是A. NaOH B.CuO
C. Fe D. NaCl
【答案】D
【解析】A.硫酸钠与氢氧化钡反应生成硫酸钡沉淀和氢氧化钠,碳酸钠和稀硫酸反应生成硫酸钠,氢氧
化钠和二氧化碳反应生成碳酸钠和水,碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,故A项正确;
B.氧化铜和氢气反应生成氧化铜和水,氧气和铜反应生成氧化铜,电解水可以生成氢气和氧气,氧气和
氢气反应生成水,故B项正确;C.氯化亚铁和锌反应生成铁,硫酸亚铁和氯化钡反应生成氯化亚铁,铁
和稀硫酸反应生成硫酸亚铁,硫酸亚铁和锌反应生成铁,故C项正确;D.碳酸钠和稀盐酸反应生成氯化
钠,硝酸钠无法生成碳酸钠,故D项错误;故本题选D。
4.(2024·江苏苏州·三模)在给定条件下,下列物质转化或方程式正确的是
A.工业制漂白粉:
B.工业制
C.电解饱和食盐水:
D. 碱性溶液与 反应:
【答案】D
【解析】A.二氧化锰和浓硫酸反应不生成氯气,故A项错误;B. ,Fe与HCl反应
生成FeCl ,故B项错误;C.工业上通过电解饱和食盐水生成烧碱,离子方程式为
2
,故C项错误;D.KClO和KOH混合溶液与,反应方程式为
,故D项正确;故本题选D。
5.(2024·江苏宿迁·三模)硫元素约占地球总质量的1.9%,广泛分布并循环于地球内部各圈层。硫有
32S、34S、33S和36S四种同位素。硫元素主要以氢化物、硫化物、含氧酸和含氧酸盐等形式存在。硫的单质
有S、S、S 等多种分子形态;硫的氢化物(H S、HS)均有弱酸性;低价硫易被氧气氧化。硫在生物圈的
2 4 8 2 2 2
演化中扮演了重要角色,在细菌作用下硫元素可发生氧化或还原反应,促进了硫元素在地球各圈层中的循
环。下列化学反应的表示正确的是
A.二硫化氢与足量烧碱溶液反应:HS+2OH-=S +2HO
2 2 2
B.黄铁矿在细菌作用下转化为强酸:2FeS+2HO+7O 2Fe2++4H++4SO
2 2 2C.用NaSO 除去废水中的氯气:SO +4Cl+10OH-=2SO +8Cl-+5HO
2 2 3 2 2 2
D.硫化亚铁除废水中汞离子:S2-+Hg2+=HgS↓
【答案】A
【解析】A.二硫化氢为弱酸,与足量烧碱溶液反应:HS+2OH-= +2HO,A正确;B.Fe2+能被O
2 2 2 2
氧化为Fe3+,离子方程式: ,B错误;C.NaSO 还原性较强,
2 2 3
在溶液中易被氯气氧化成 ,Cl 被还原为Cl-,则根据电子守恒、原子守恒和电荷守恒,离子方程式:
2
SO +4Cl+5HO =2SO +8Cl-+10H+,C错误;D.FeS难溶于水,离子方程式:FeS+Hg2+
2 2 2
=HgS+Fe2+,D错误;故选A。
6.(2024·安徽安庆·模拟预测)黄铜 用 溶液浸泡后生成单质硫,所得CuSO 溶液
4
可用于制取纳米Cu O,Cu O能与酸发生反应。Co3+具有强氧化性,可与浓盐酸反应生成氯气。由
2 2
、 、 和 反应制备的配合物 可应用于 的鉴定。下列化学反应方
程式表示错误的是
A.Cu O与稀硫酸反应:
2
B. 溶液和 反应:
C. 与足量浓盐酸反应:
D.制备 的反应:
【答案】C
【解析】A.Cu O与稀硫酸反应生成铜、硫酸铜和水,反应的离子方程式为:Cu O+2H+=Cu+Cu2++H O,
2 2 2
A正确;B.CuFeS 和Fe (SO ) 溶液反应生成硫酸铜、硫酸亚铁和硫单质,反应的离子方程式为:
2 2 4 3
CuFeS+4Fe3+=Cu2++2S+5Fe2+,B正确;C.已知Co3+具有强氧化性,可与浓盐酸反应生成氯气,Co(OH)
2 3
与足量盐酸反应:2Co(OH) +2Cl-+6H+=2Co2++Cl↑+6H O,C错误;D.CHCOOH不能拆,制备
3 2 2 3
Na[Co(NO )]的反应的离子离子反应为应:12 +2Co2++H O+2CH COOH=2[Co(NO )]3-+2CH COO-
3 2 6 2 2 3 2 6 3
+2H O,D正确;故答案为:C。
2
7.(2024·山西·模拟预测)下列根据实验操作及现象不能达到相应实验目的的是
选项 实验操作及现象 实验目的
向滴有几滴 的 溶液中加入 ,缓缓通入少
A 验证还原性:
量 并振荡、静置,水层显红色,有机层显无色
相同温度下,同时进行 与 和 的反应,观 探究 键的极性对反应速率的
B
察产生 的快慢 影响C 将胆矾晶体投入浓硫酸中,固体由蓝色变为白色 验证浓硫酸具有脱水性
确定
D 分别测定 和 与盐酸反应的反应热
的
【答案】C
【解析】本题以实验操作、现象与实验目的为情境,考查还原性强弱、键的极性比较及反应热的测定等知
识,意在考查探究与创新能力,科学探究与创新意识的核心素养。
A. 中 和 均可与 反应,产生 和 ,其中 遇 显红色, 进入 中使有
机层显橙红色,故根据现象可知, 先与 反应,故还原性: ,A项不符合题意;B. 与
和 的反应中均发生了氢氧键的断裂,氢氧键的极性越强,越容易断裂,反应速率越快,所
以可以通过观察产生 的快慢,探究 键的极性对反应速率的影响,B项不符合题意;C.将胆矾晶
体投入浓硫酸中,固体由蓝色变为白色,体现的是浓硫酸的吸水性,C项符合题意;D.分别测定
和 与盐酸反应的反应热,根据盖斯定律可确定 的 ,D项
不符合题意;故选C。
8.(2024·湖北·模拟预测)稀有气体化合物的合成更新了对“惰性”的认知。已知:
,设 为阿伏加德罗常数的值。下列说法错误的是
A.1 mol 中心原子的孤电子对数目为
B.18 g 中所含质子数目为
C.生成1 mol ,转移电子数目为
D.3.36 L HF(标准状况)所含的分子数为
【答案】D
【解析】A. 最外层有8个电子,提供4个电子分别与4个F形成共用电子,则1 mol 中心原子的
孤电子对数目为 ,A正确;B.18 g 是1mol,1个 中有10个质子,则18 g 中所含质子数
目为 ,B正确;C. ,该反应中 是氧化产物, 是
还原产物, 是氧化产物,生成1 mol 时生成2 mol ,转移电子数目为 ,C正确;
D.标准状况时HF不是气体,则3.36 L HF(标准状况)不是0.15 mol,所含的分子数不是 ,D错误;
故选D。
9.(2024·河北石家庄·三模)亚氯酸钠( )具有强氧化性、受热易分解,可用作漂白剂、食品消
毒剂等,以氯酸钠等为原料制备亚氯酸钠的工艺流程如图所示。已知高浓度的 易爆炸。下列说法错误
的是A.“反应1”中 是还原产物,母液中主要成分是
B.“反应1”需要通入 稀释 ,以防发生爆炸
C.“反应2”中,氧化剂和还原剂的物质的量之比为
D.若还原产物均为 时, 的氧化能力是等质量 的2.5倍
【答案】D
【分析】由题给流程可知,反应1为二氧化硫与稀硫酸、氯酸钠反应生成硫酸钠、二氧化氯和水,反应2
为二氧化氯与过氧化氢、氢氧化钠混合溶液反应生成亚氯酸钠、氧气和水,反应得到的亚氯酸钠在55℃条
件下减压蒸发、冷却结晶、过滤得到亚氯酸钠粗产品。
【解析】A.反应1中二氧化硫与稀硫酸、氯酸钠反应生成硫酸钠、二氧化氯和水,Cl元素化合价由+5价
下降到+4价, 是还原产物,母液中主要成分是 ,A正确;B.已知高浓度的 易爆炸,反
应1”需要通入 稀释 ,以防发生爆炸,B正确;C.“反应2”中发生反应的化学方程式为
,HO 是还原剂,NaClO 是氧化剂,氧化剂与还原剂的物质的
2 2 2
量之比为2∶1,C正确;D.1 molCl 完全反应转化2 mole-,1 mol 完全反应转化5 mole-,所以等物质
2
的量的 氧化能力是 的2.5倍,D错误;故选D。
10.(2024·黑龙江吉林·模拟预测)便携式消毒除菌卡主要活性成分为亚氯酸钠(NaClO);一种制备
2
NaClO 粗产品的工艺流程如图。已知纯ClO 易分解爆炸,一般用空气稀释到10%以下。
2 2
下列说法正确的是
A.溶解过程中可以用盐酸代替稀硫酸
B.流程中HO 做氧化剂
2 2
C.发生器中鼓入空气的主要目的是提供氧化剂
D.吸收塔中温度不宜过高,否则会导致NaClO 产率下降
2
【答案】D
【分析】NaClO 在稀硫酸中溶解,通入SO 在发生器中发生氧化还原反应,生成ClO 和NaSO ,通过鼓
3 2 2 2 4
入空气,防止ClO 浓度过高,还可以将其吹进吸收塔,根据氧化还原反应规律可知,在吸收塔中ClO 与
2 2双氧水、氢氧化钠反应生成NaClO 和氧气,再经过一系列操作得到NaClO 粗产品。
2 2
【解析】A.NaClO 具有强氧化性,可以氧化HCl,则溶解过程中不可以用盐酸代替稀硫酸,A错误;B.
3
ClO 与双氧水、氢氧化钠反应生成NaClO 和氧气,流程中HO 做还原剂,B错误;C.发生器中鼓入空气
2 2 2 2
的主要目的是防止ClO 浓度过高,因为纯ClO 易分解爆炸,C错误;D.HO 不稳定,温度过高,HO 容
2 2 2 2 2 2
易分解,如果吸收塔中温度过高,会导致HO 分解,从而导致NaClO 产率下降,D正确;故选D。
2 2 2
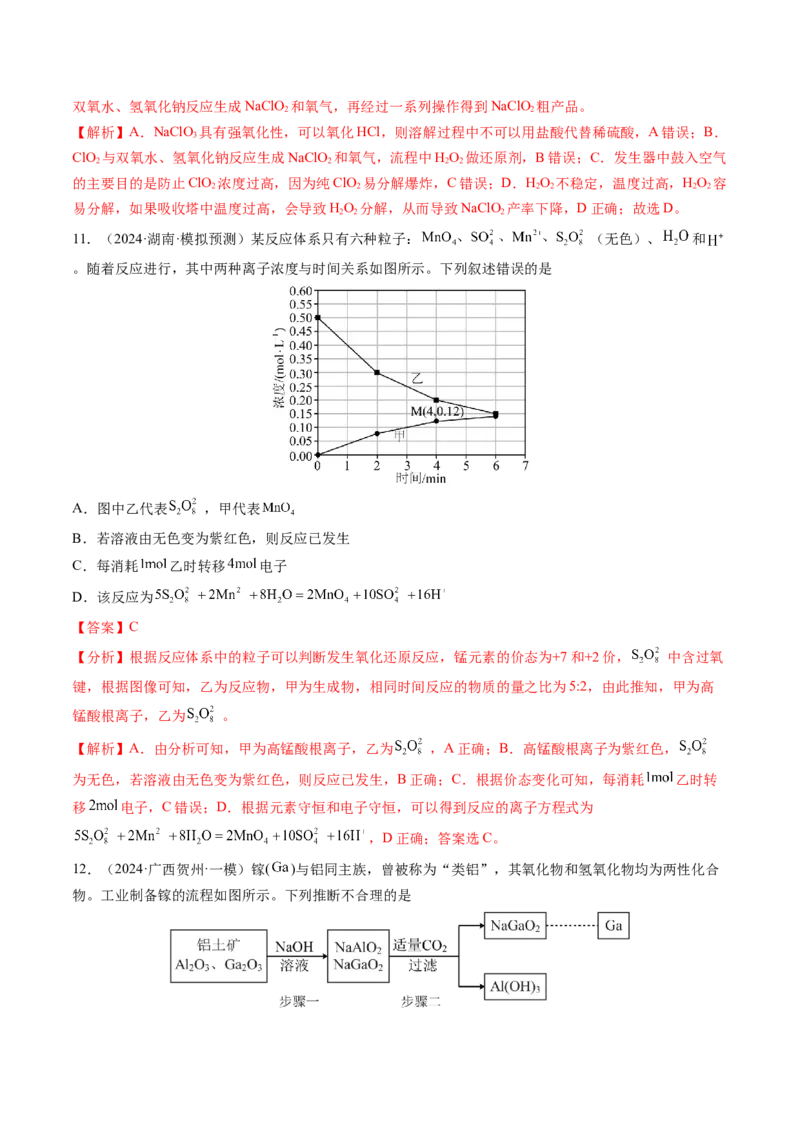
11.(2024·湖南·模拟预测)某反应体系只有六种粒子: (无色)、 和
。随着反应进行,其中两种离子浓度与时间关系如图所示。下列叙述错误的是
A.图中乙代表 ,甲代表
B.若溶液由无色变为紫红色,则反应已发生
C.每消耗 乙时转移 电子
D.该反应为
【答案】C
【分析】根据反应体系中的粒子可以判断发生氧化还原反应,锰元素的价态为+7和+2价, 中含过氧
键,根据图像可知,乙为反应物,甲为生成物,相同时间反应的物质的量之比为5:2,由此推知,甲为高
锰酸根离子,乙为 。
【解析】A.由分析可知,甲为高锰酸根离子,乙为 ,A正确;B.高锰酸根离子为紫红色,
为无色,若溶液由无色变为紫红色,则反应已发生,B正确;C.根据价态变化可知,每消耗 乙时转
移 电子,C错误;D.根据元素守恒和电子守恒,可以得到反应的离子方程式为
,D正确;答案选C。
12.(2024·广西贺州·一模)镓( )与铝同主族,曾被称为“类铝”,其氧化物和氢氧化物均为两性化合
物。工业制备镓的流程如图所示。下列推断不合理的是A.向 溶液中逐滴加入足量稀氨水,先生成沉淀,后沉淀溶解
B.向 和 溶液中通入适量二氧化碳后得到氢氧化铝沉淀,可知酸性:
C.金属镓可以与 溶液反应生成 和
D.步骤二中不能通入过量的 的理由是
【答案】A
【分析】镓(Ga)与铝同主族,曾被称为“类铝”,其氧化物和氢氧化物均为两性化合物。工业制备镓的流
程如图,分析可知氧化铝和氧化镓都可以与氢氧化钠溶液反应生成盐,并且二氧化碳可以制取氢氧化铝,
却无法与偏镓酸钠反应,可实现铝和镓的分离。
【解析】A.镓( )与铝同主族,曾被称为“类铝”,则其氢氧化物不会溶与弱碱氨水,向GaCl 溶液中
3
逐滴加入足量氨水,有Ga(OH) 沉淀生成,沉淀不溶解,A错误;B.适量二氧化碳可以制取氢氧化铝,
3
却无法与Na[Ga(OH) ]反应,说明酸性氢氧化铝比氢氧化镓弱, ,B正确;C.铝能与
4
氢氧化钠反应生成偏铝酸钠和氢气,所以金属镓也可以与NaOH溶液反应生成 和氢气,C
正确;D.碳酸溶液为酸性,所以步骤二中不能通入过量的 是因为 会发生反应生成
Ga(OH) 沉淀, ,D正确;故选A。
3
13.(2024·山东菏泽·模拟预测)乙苯脱氢的反应历程如下图(Ph-为苯基),下列说法正确的是
A.物质Ⅰ为催化剂
B.此反应过程中 是氧化剂
C.只有过程②有电子转移
D.每脱去1mol氢原子,转移2mol电子
【答案】B
【解析】A.乙苯在物质Ⅳ的作用下生成苯乙烯,Ⅳ为催化剂,A错误;B. 在反应中生成 ,作氧
化剂,B正确;C.过程②④都有电子转移,C错误;D.H元素化合价变为为1,每脱去 氢原子,转
移 电子,D错误;答案选B。14.(2024·浙江丽水·二模)已知过氧化铬 的结构式如图所示, 溶于稀硫酸的化学方程式为:
,有关该反应说法不正确的是
A. 在元素周期表中的位置为第四周期第VIB族
B. 既作氧化剂,又作还原剂
C.氧化产物与还原产物的物质的量之比为
D.若有 发生该反应,则反应中共转移 个电子
【答案】C
【解析】A.Cr在元素周期表中位置为第四周期第ⅥB族,故A正确;B. 中Cr元素化合价下降,O
元素化合价上升,HSO 中O元素化合价未发生变化,则 既作氧化剂,又作还原剂,故B正确;C.
2 4
中4个氧原子与铬形成的是Cr-O键,每个氧原子的化合价为-1价,1个氧原子与铬形成的是Cr=O
键,这种氧原子的化合价为-2价,Cr为+6价,Cr元素由+6价下降到+3价,O元素由-1价下降到-2价,有
由-1价上升到0价, 和2个HO是还原产物,O 是氧化产物,氧化产物与还原产物的物质的量
2 2
之比为 ,故C错误;D. 中4个氧原子与铬形成的是Cr-O键,每个氧原子的化合价为-1价,1个
氧原子与铬形成的是Cr=O键,这种氧原子的化合价为-2价,Cr为+6价,Cr元素由+6价下降到+3价,O
元素由-1价下降到-2价,有由-1价上升到0价,若有 发生该反应,生成 molO ,则反应中共转
2
移 个电子,故D正确;故选C。
15.(2024·重庆荣昌·模拟预测)黄铁矿( )在酸性条件下发生催化氧化的反应历程如图所示。下列说
法错误的是
A.反应Ⅰ、Ⅱ、Ⅲ均发生氧化还原反应
B.反应Ⅰ中氧化剂与还原剂的物质的量之比为
C.反应Ⅱ的离子方程式为
D.该过程的总反应为【答案】A
【分析】反应I的离子方程式为4Fe(NO)2++O +4H+=4Fe3++4NO+2HO,反应Ⅲ的离子方程式为Fe2+
2 2
+NO=Fe(NO)2+,反应Ⅱ的离子方程式为FeS+14Fe3++8H O=15Fe2++2 +16H+;
2 2
【解析】A.反应I、Ⅱ是氧化还原反应;反应Ⅲ,无元素化合价变化,为非氧化还原反应,A错误;B.
反应I的离子方程式为4Fe(NO)2++O +4H+=4Fe3++4NO+2HO,氧化剂与还原剂的物质的量之比为 ,B正
2 2
确;C.反应Ⅱ的离子方程式为 ,C正确;D.该过程的总反应为
,D正确;故选A。
二、非选择题(共4小题,共55分)
16.(23-24高三上·北京·开学考试)(16分)零价铁还原性强、活性高,对很多重金属离子及含磷、砷离
子都有较好的去除和富集作用。
Ⅰ.零价铁的制备。
(1)富铁矿石经破碎、筛分到微米级后,在氢气氛围下 高温还原 可以制备微米级零价铁。请写出
磁铁矿与氢气反应制备零价铁的化学方程式 。
(2)采用 还原铁盐,可以制备出纳米级的零价铁。
已知: 的电负性是2.0, 的电负性是2.1
①请写出 的电子式 。
②请写出 与硫酸反应的离子方程式 。
③补充完整下列化学方程式 。
每生成 零价铁 ,转移电子的物质的量是 。
Ⅱ.零价铁的结构和作用机理。
研究发现,纳米级和微米级的零价铁,均具有“核-壳”结构。
已知:①壳层可以导电;
②当 时,铁的氧化物质子化,壳层表面带正电;当 时,铁的氧化物去质子化,壳层表面带负
电;
③磷酸盐溶解度一般较小。
(3)去离子水中加入零价铁, 从6上升到9.5左右。检测壳层物质,发现有 、 、 、
等。导致产生壳层微粒的氧化剂是 、 。
(4)部分金属阳离子去除机理如图所示。纳米零铁去除污水中 、 主要机理不同,请简述两
者的区别并解释原因 。(5)去除含磷( )微粒:
①控制 8,原因是 。
②通过形成 (填化学式)进一步去除 。
(6)综上所述,零价铁去除重金属离子及含磷微粒的主要机理有 。
【答案】(1) (1分)
(2) (1分) (2分)
(2分) (1分)
(3) (1分)
(4)零价铁的还原性大于 ,小于 ,因此, 被铁还原为 而除去,而 无法还原 ,主
要通过吸附作用除去 (2分)
(5) (1分) 时零价铁壳层表面带正电,能更好地吸附带负电的 (2分) 、
沉淀(1分)
(6)还原、吸附、共沉淀(2分)
【解析】(1)磁铁矿与氢气反应生成零价铁和水的反应方程式为 。
(2)① 是离子化合物,故电子式为 。②由于B的电负性是2.0,H的电负性是
2.1,故H是-1价,有强还原性,故与硫酸发生氧化还原反应 。③根据得
失电子守恒,可得 ,反应中Fe和水中的H的化合价共降低24
价, 中H的化合价共升高24价,故每生成 零价铁 ,转移电子的物质的量是12mol。
(3)去离子水中加入零价铁,pH从6上升到9.5左右,说明HO作氧化剂。
2(4)零价铁的还原性大于 ,小于 ,因此, 被铁还原为 而除去,而 无法还原 ,主
要通过吸附作用除去 。
(5)①根据已知,当pH<8时,铁的氧化物质子化,壳层表面带正电,能更好地吸附带负电的 。②
、 都是沉淀,故能进一步去除 。
(6)综上所述,(3)中利用还原法去除重金属离子,(4)中利用吸附法去除金属离子,(5)利用沉淀
法沉淀含磷微粒。
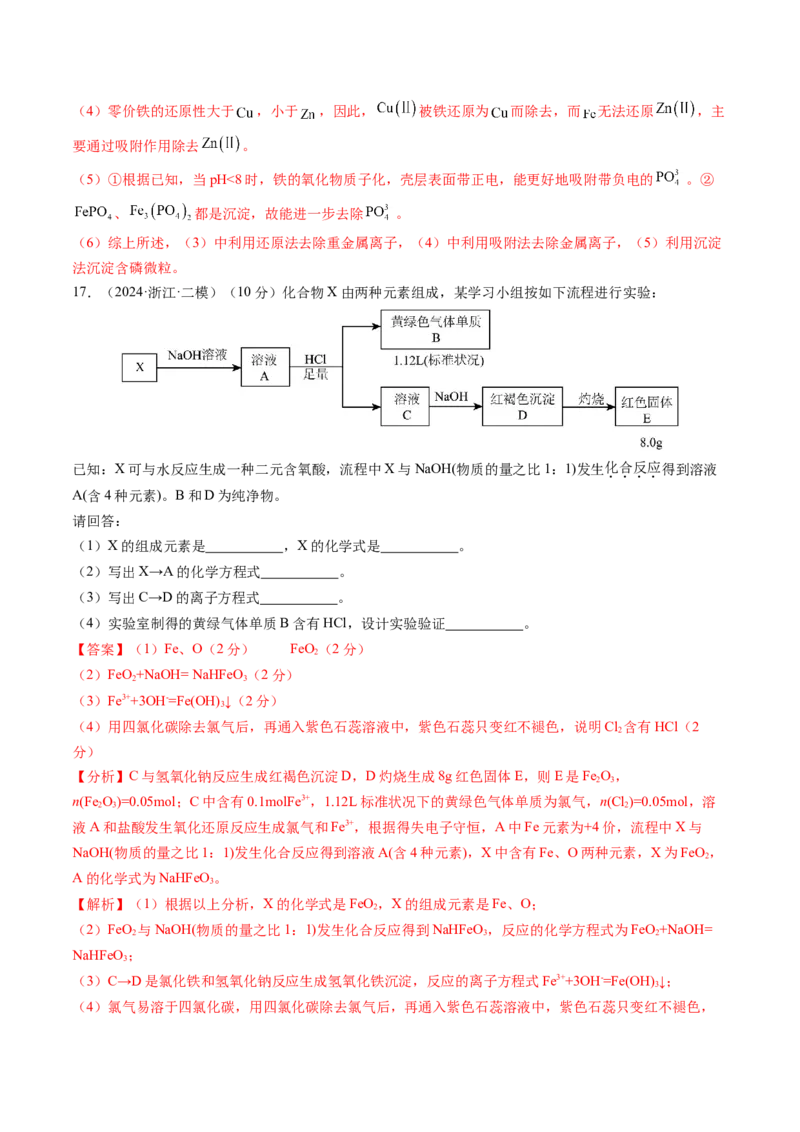
17.(2024·浙江·二模)(10分)化合物X由两种元素组成,某学习小组按如下流程进行实验:
已知:X可与水反应生成一种二元含氧酸,流程中X与NaOH(物质的量之比1:1)发生化合反应得到溶液
A(含4种元素)。B和D为纯净物。
请回答:
(1)X的组成元素是 ,X的化学式是 。
(2)写出X→A的化学方程式 。
(3)写出C→D的离子方程式 。
(4)实验室制得的黄绿气体单质B含有HCl,设计实验验证 。
【答案】(1)Fe、O(2分) FeO(2分)
2
(2)FeO+NaOH= NaHFeO (2分)
2 3
(3)Fe3++3OH-=Fe(OH) ↓(2分)
3
(4)用四氯化碳除去氯气后,再通入紫色石蕊溶液中,紫色石蕊只变红不褪色,说明Cl 含有HCl(2
2
分)
【分析】C与氢氧化钠反应生成红褐色沉淀D,D灼烧生成8g红色固体E,则E是Fe O,
2 3
n(Fe O)=0.05mol;C中含有0.1molFe3+,1.12L标准状况下的黄绿色气体单质为氯气,n(Cl )=0.05mol,溶
2 3 2
液A和盐酸发生氧化还原反应生成氯气和Fe3+,根据得失电子守恒,A中Fe元素为+4价,流程中X与
NaOH(物质的量之比1:1)发生化合反应得到溶液A(含4种元素),X中含有Fe、O两种元素,X为FeO,
2
A的化学式为NaHFeO 。
3
【解析】(1)根据以上分析,X的化学式是FeO,X的组成元素是Fe、O;
2
(2)FeO 与NaOH(物质的量之比1:1)发生化合反应得到NaHFeO ,反应的化学方程式为FeO+NaOH=
2 3 2
NaHFeO ;
3
(3)C→D是氯化铁和氢氧化钠反应生成氢氧化铁沉淀,反应的离子方程式Fe3++3OH-=Fe(OH) ↓;
3
(4)氯气易溶于四氯化碳,用四氯化碳除去氯气后,再通入紫色石蕊溶液中,紫色石蕊只变红不褪色,说明Cl 含有HCl。
2
18.(2024·湖北·一模)(13分)某学习小组为探究Mg与酸、碱、盐溶液的反应。完成如下实验:
编号 操作 现象
Ⅰ 将镁条放入 稀硫酸中 迅速放出大量气体,试管壁发热
Ⅱ 将镁条放入pH为 的 溶液中 无明显现象
将镁条放入pH为 的 溶液
Ⅲ 放出气体,溶液中有白色沉淀生成
中
回答下列问题:
(1)实验前除去镁表面氧化物的方法是 。
(2)实验Ⅰ的离子方程式为 。
(3)经实验分析,实验Ⅲ中产生的气体为 和 混合气体。产生 气体的原因是 。
(4)该组同学们比较实验Ⅱ、Ⅲ后,分析认为:实验Ⅲ能快速反应的原因,与溶液中白色沉淀有关。为
探究其成分,设计了如下实验。
取出镁条,将沉淀过滤、洗涤、低温烘干,得到纯净固体 。将一半固体放入锥形瓶中,按如图连接
好装置。滴加稀硫酸到无气体放出为止,在 处通入足量空气。最后称量 形管增重 。将另一半固
体高温灼烧,最后剩余固体氧化物为 。
①最后通入空气的目的是 。
②固体充分高温灼烧后,需要放在 (填仪器名称)中冷却后才能称量。称量时 (选填“是”
“不是”)采用托盘天平称量。
(5)依据以上分析,实验Ⅲ中发生反应的方程式为 。通过以上实验得出结论: 置换氢气
与 、温度、 与溶液接触面积有关,在 溶液中,生成的沉淀能破坏 表面覆盖的
,从而较快进行。
【答案】(1)用砂纸打磨。(或者:浸入稀硫酸中至表面有均匀气泡,取出,洗净。)(2分)
(2) (2分)
(3) 与水反应放热使 分解放出 (2分)
(4)将系统内生成的 完全排入到U形管中被吸收(2分) 干燥器(1分)不是(1分)
(5) (3分)【解析】(1)实验前除去镁表面氧化物的方法是:用砂纸打磨。(或者:浸入稀硫酸中至表面有均匀气
泡,取出,洗净。);
(2)实验Ⅰ,镁与硫酸反应的离子方程式为
(3)实验Ⅲ中产生的气体为 和 混合气体。产生的 是镁与水反应产生的,产生 气体只能由
分解产生,故原因是 与水反应放热使 分解放出
(4)①最后通入空气的目的是:将系统内生成的 完全排入到U形管中被吸收;
②固体充分高温灼烧后,需要放在干燥器中冷却后才能称量,防止高温下与水反应。托盘天平称量时精确
到小数点后一位,题中是后两位,所以不是采用托盘天平称量。
(5)高温灼烧,最后剩余固体氧化物为MgO,则n(MgO)= ,n(Mg) , 形
管增重 为 的质量,由此可得 的物质的量为 , 的物质的量
为0.01mol,含镁化合物总质量为0.01×58g/mol+0.03×84g/mol=3.1g,则结晶水的物质的量为
,白色沉淀为 ,实验Ⅲ中发生反应的方程式为:
;
19.(2024·山西·模拟预测)(16分)以废钒电池负极电解液(主要化学成分是V3+、V2+、HSO ) 为原料,
2 4
回收其中的钒制备VO 的工艺流程如图所示:
2 5
已知:氯酸浓度较高或受热时易发生分解。
回答下列问题:
(1)在“氧化”中低价态钒都转化为 ,其中V3+转化反应的离子方程式为 ,实际生产中
的氧化剂不选择HClO 的原因是 。
3
(2)“浓缩”至钒溶液质量浓度(折合VO 质量浓度)为27.3 g·L-1'时,则溶液中c( )=
2 5
mol·L-1。(结果保留1位小数)
(3)pH对沉钒率(η)的影响如图所示,则沉钒时控制钒液合适的pH范围是 ,沉淀产物为
2NH VO·H O,则加(NH )SO 沉钒的化学方程式是 。
4 3 8 2 4 2 4(4)“过滤”后对沉淀进行洗涤,采用稀(NH )SO 作洗涤液的目的是 。检验沉淀已洗涤干净
4 2 4
的操作是 。
(5)“煅烧”需要在通风或氧化气氛下进行,其目的是 。
【答案】(1)3V3++ +3H O=3 +Cl-+6H+(2分) HClO 易分解,不及NaClO 稳定;HClO
2 3 3 3
会提高体系酸度,从而增加后续NaOH的用量(2分)
(2)0.3(2分)
(3)2.0~2.5(2分) (NH )SO + 3(VO )SO + 5H O = 2NH VO·H O↓+4HSO (2分)
4 2 4 2 2 4 2 4 3 8 2 2 4
(4)降低2NH VO·H O的溶解度,减少洗涤时的损耗(2分) 取少量最后一次的洗涤液于试管中,
4 3 8 2
加过量Ba(NO ) 溶液,充分反应后静置,向上层清液中继续加AgNO 溶液,不出现浑浊,则证明沉淀已洗
3 2 3
涤干净(2分)
(5)防止NH 将VO 还原,导致产品纯度降低(2分)
3 2 5
【分析】废钒电池负极电解液(主要化学成分是V3+、V2+、HSO ),加入NaClO 氧化,生成 ,再加入
2 4 3
硫酸铵得到沉淀2NH VO·H O,过滤后煅烧得到五氧化二钒。据此作答。
4 3 8 2
【解析】(1)酸性条件下,V3+转化为 的离子方程式为:3V3++ +3H O=3 +Cl-+6H+;由于H
2
氯酸浓度较高或受热时易发生分解,不及NaClO 稳定,不利于储存运输,同时HClO 是酸,会增大溶液
3 3
的酸性,,从而增加后续NaOH的用量,所以实际生产中的氧化剂不选择HClO;
3
(2)“浓缩”至钒溶液质量浓度(折合VO 质量浓度)为27.3 g·L-1时,即c(VO)= 27.3
2 5 2 5
g·L-1÷182g/mol=0.15mol/L,根据钒元素守恒,则溶液中c( )=2c(V O)=0.15mol/L×2=0.3mol/L;
2 5
(3)根据图示, pH范围是2.0-2.5时,沉钒率(η)最高;沉钒时的反应物是(NH )SO 和(VO )SO ,沉淀产
4 2 4 2 2 4
物为2NH VO·H O,则反应的化学方程式为(NH )SO + 3(VO )SO + 5H O = 2NH VO·H O↓+4HSO ;
4 3 8 2 4 2 4 2 2 4 2 4 3 8 2 2 4
(4)用稀(NH )SO 作洗涤液的目的是为了降低2NH VO·H O的溶解度,减少洗涤时的损耗;检验沉淀
4 2 4 4 3 8 2
已洗涤干净即检验是否含有Cl-,操作是取少量最后一次的洗涤液于试管中,加过量Ba(NO ) 溶液,充分反
3 2
应后静置,向上层清液中继续加AgNO 溶液,不出现浑浊,则证明沉淀已洗涤干净;
3
(5)煅烧时受热分解产生NH ,氨气具有较强的还原性,容易将VO 还原,导致产品纯度降低,所以需
3 2 5
要在通风或氧化气氛下进行,目的是防止NH 将VO 还原,导致产品纯度降低。
3 2 5