文档内容
第三章 金属及其化合物
测试卷
时间:90分钟 分值:100分
可能用到的相对原子质量:O 16 Na 23 Fe 56
一、选择题(每小题只有一个正确选项,共16×3分)
1.(2023·湖北武汉·华中师大一附中校考模拟预测)Li和Mg是两种重要的金属元素。下列说法正确的是
A.金属镁一般保存在石蜡油中 B.单质Li和冷水不反应
C.单质Li可与 反应生成 D.Li、Mg的焰色试验现象相同
2.(2023·四川攀枝花·统考三模)恨据下列实验操作和现象得出的结论中,正确的是
选项 实验操作和现象 结论
部分NaSO 被氧
2 3
A 向久置的NaSO 溶液中加入足量BaCl 溶液,出现白色沉淀,再加入足量稀
2 3 2
化
盐酸,部分沉淀溶解
B 取少量可能被氧化的还原铁粉,加稀盐酸溶解,滴入KSCN溶液,溶液不显
还原铁粉未被氧化
红色
C 氯化铁溶液中含有
将可能含有Fe2+的氯化铁溶液滴入酸性KMnO 溶液中,溶液紫红色褪去
4
Fe2+
D 将绕成螺旋状的铜丝灼烧后反复插入盛有乙醇的试管,然后滴加酸性高锰酸 乙醇被氧化成了乙
钾溶液,溶液紫红色褪去 醛
3.(2023·辽宁大连·统考二模)大力推广锂电池新能源汽车对实现“碳达峰”和“碳中和”具有重要意义。
与 都是锂离子电池的电极材料,可利用钛铁矿(主要成分为 ,还有少量 、
等杂质)来制备,工艺流程如下:
下列叙述错误的是
A.酸浸后,得到滤渣的主要成分是
B.在滤液②中主要的金属阳离子有 、
C.制备 时需要加入水,同时加热,促使水解反应趋于完全D.在制备 的过程中会生成 ( 为 价),则 中含有的过氧键的数目为
4.(2023·辽宁大连·统考二模)《新修本草》是我国古代中药学著作之一,其中关于“青矾”的描述为:
“本来绿色,新出窟未见风者,正如琉璃……,烧之赤色……”,则“青矾”的主要成分是
A. B.
C. D.
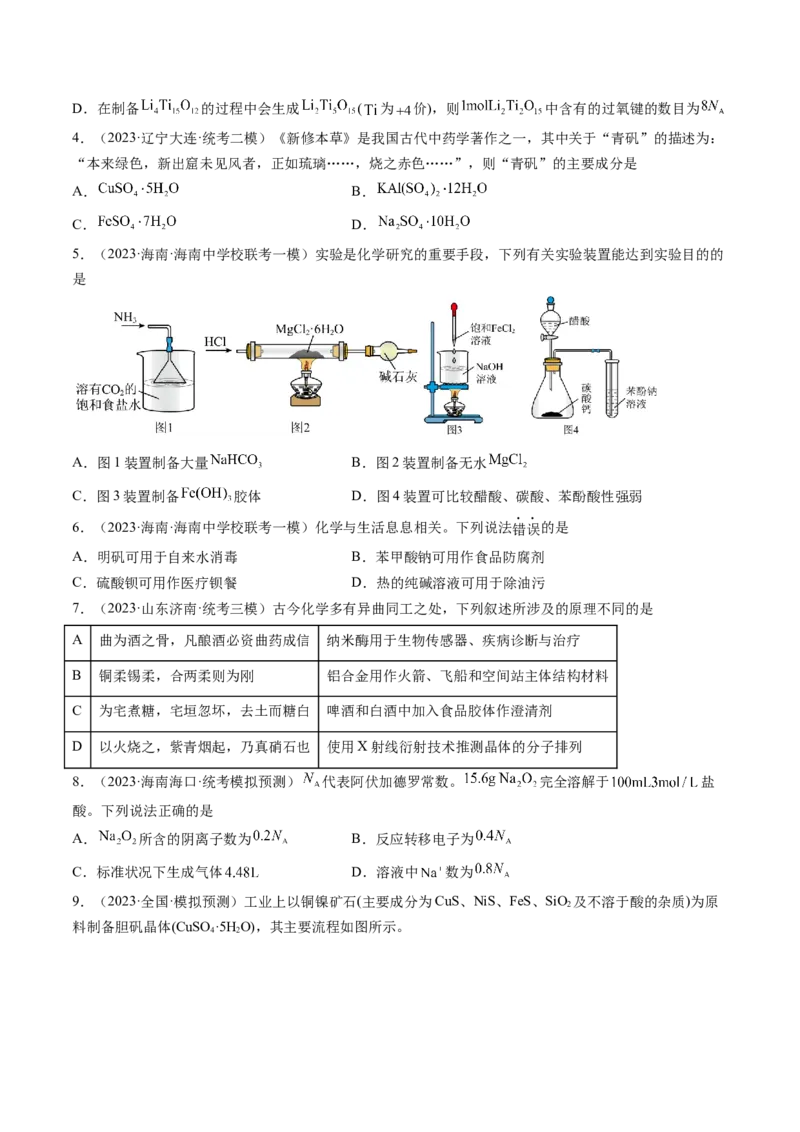
5.(2023·海南·海南中学校联考一模)实验是化学研究的重要手段,下列有关实验装置能达到实验目的的
是
A.图1装置制备大量 B.图2装置制备无水
C.图3装置制备 胶体 D.图4装置可比较醋酸、碳酸、苯酚酸性强弱
6.(2023·海南·海南中学校联考一模)化学与生活息息相关。下列说法错误的是
A.明矾可用于自来水消毒 B.苯甲酸钠可用作食品防腐剂
C.硫酸钡可用作医疗钡餐 D.热的纯碱溶液可用于除油污
7.(2023·山东济南·统考三模)古今化学多有异曲同工之处,下列叙述所涉及的原理不同的是
A 曲为酒之骨,凡酿酒必资曲药成信 纳米酶用于生物传感器、疾病诊断与治疗
B 铜柔锡柔,合两柔则为刚 铝合金用作火箭、飞船和空间站主体结构材料
C 为宅煮糖,宅垣忽坏,去土而糖白 啤酒和白酒中加入食品胶体作澄清剂
D 以火烧之,紫青烟起,乃真硝石也 使用X射线衍射技术推测晶体的分子排列
8.(2023·海南海口·统考模拟预测) 代表阿伏加德罗常数。 完全溶解于 盐
酸。下列说法正确的是
A. 所含的阴离子数为 B.反应转移电子为
C.标准状况下生成气体 D.溶液中 数为
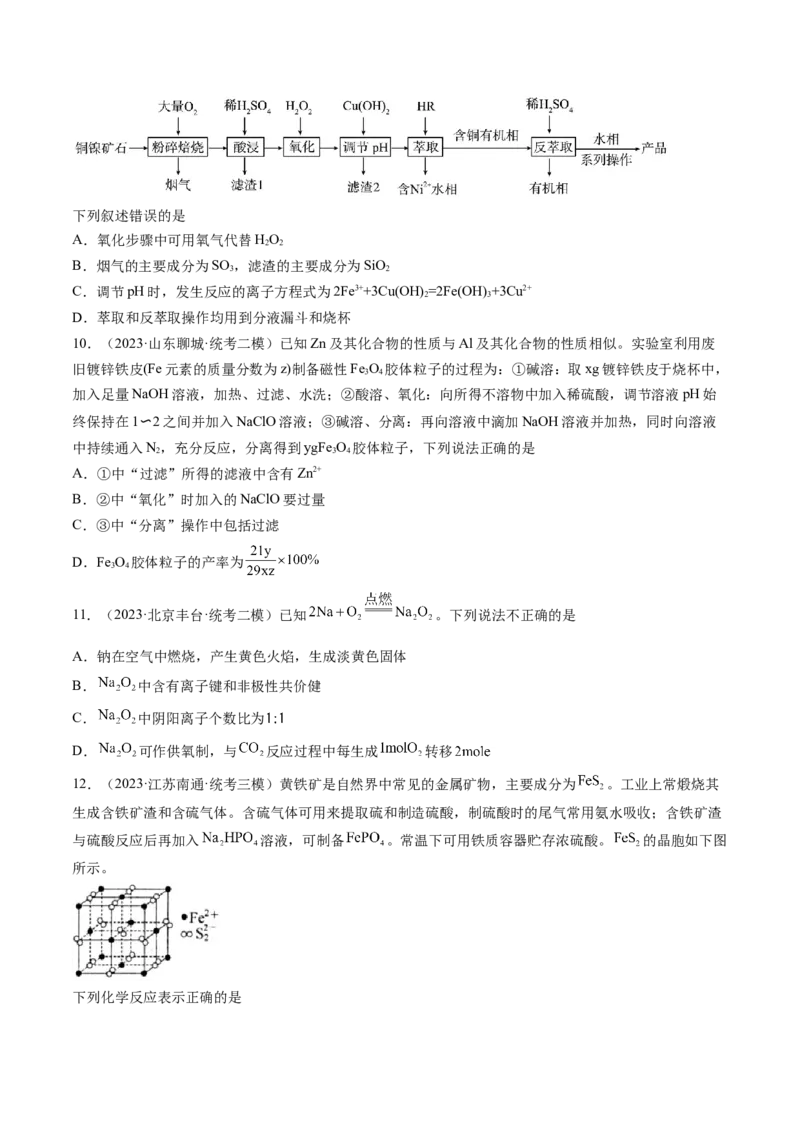
9.(2023·全国·模拟预测)工业上以铜镍矿石(主要成分为CuS、NiS、FeS、SiO 及不溶于酸的杂质)为原
2
料制备胆矾晶体(CuSO ·5H O),其主要流程如图所示。
4 2下列叙述错误的是
A.氧化步骤中可用氧气代替HO
2 2
B.烟气的主要成分为SO ,滤渣的主要成分为SiO
3 2
C.调节pH时,发生反应的离子方程式为2Fe3++3Cu(OH) =2Fe(OH) +3Cu2+
2 3
D.萃取和反萃取操作均用到分液漏斗和烧杯
10.(2023·山东聊城·统考二模)已知Zn及其化合物的性质与Al及其化合物的性质相似。实验室利用废
旧镀锌铁皮(Fe元素的质量分数为z)制备磁性Fe O 胶体粒子的过程为:①碱溶:取xg镀锌铁皮于烧杯中,
3 4
加入足量NaOH溶液,加热、过滤、水洗;②酸溶、氧化:向所得不溶物中加入稀硫酸,调节溶液pH始
终保持在1〜2之间并加入NaClO溶液;③碱溶、分离:再向溶液中滴加NaOH溶液并加热,同时向溶液
中持续通入N,充分反应,分离得到ygFe O 胶体粒子,下列说法正确的是
2 3 4
A.①中“过滤”所得的滤液中含有Zn2+
B.②中“氧化”时加入的NaClO要过量
C.③中“分离”操作中包括过滤
D.Fe O 胶体粒子的产率为
3 4
11.(2023·北京丰台·统考二模)已知 。下列说法不正确的是
A.钠在空气中燃烧,产生黄色火焰,生成淡黄色固体
B. 中含有离子键和非极性共价健
C. 中阴阳离子个数比为
D. 可作供氧制,与 反应过程中每生成 转移
12.(2023·江苏南通·统考三模)黄铁矿是自然界中常见的金属矿物,主要成分为 。工业上常煅烧其
生成含铁矿渣和含硫气体。含硫气体可用来提取硫和制造硫酸,制硫酸时的尾气常用氨水吸收;含铁矿渣
与硫酸反应后再加入 溶液,可制备 。常温下可用铁质容器贮存浓硫酸。 的晶胞如下图
所示。
下列化学反应表示正确的是A.煅烧黄铁矿:
B. 气体与 气体混合:
C.氨水吸收过量 :
D. 溶液与 溶液混合的离子方程式:
13.(2023·海南海口·统考模拟预测)下列实验操作、现象和结论均正确且有对应关系的是
选
实验操作、现象 结论
项
A 将铁片溶于稀硫酸中,滴加铁氰化钾溶液,产生蓝色沉淀 说明铁片表面没有生成
B 在酸性 溶液中滴加葡萄糖溶液,溶液褪色 说明葡萄糖具有还原性
C 在硫酸四氨合铜溶液中加入乙醇,析出蓝色晶体 说明乙醇具有吸水性
D 在2mL0.1 溶液中滴加少量新制的氯水,溶液变黄色 说明还原性:
14.(2023·辽宁鞍山·鞍山一中校考模拟预测)化学与科技、生活密切相关,下列说法错误的是
A.印制货币票面文字、号码等处使用含 的油墨,利用了 的稳定性
B.“奋斗者”号万米深潜载人舱球壳所使用的钛合金属于金属材料
C.卡塔尔世界杯用球“旅程”使用水性涂料代替有机涂料,更加环保
D.电热水器用镁棒防止内胆腐蚀,应用的原理是牺牲阳极的阴极保护法
15.(2023·湖南·校联考模拟预测)从含镍催化剂(含NiO、 、 等物质)中回收金属资源的流程如
下:
下列说法错误的是
A.试剂X可以是NaOH溶液
B.“酸化”反应的离子方程式为
C.该工艺回收的金属资源为 、 、
D.若杂质中含有 ,浓缩结晶所得产品中可能含有
16.(2023·海南海口·统考模拟预测)下列过程对应的离子方程式或化学方程式书写正确的是
A.向稀硝酸中加入少量铜粉:B.锂在氧气中燃烧:
C.向 溶液中滴几滴NaClO溶液:
D.用烧碱溶液除去铁粉中的少量铝粉:
二、主观题(共5小题,共52分)
17.(9分)钠、铝、铁是三种重要的金属。请回答:
(1)钠元素的金属性比铝的_______(填“强”或“弱”)。
(2)将一小块金属钠投入水中,发生反应的离子方程式为_______;
(3)取一定量的FeCl ,分装在两支试管中。请回答:
3
a.若向其中一支试管中滴加KSCN溶液,则溶液变成_______色。
b.向另一支试管中滴加NaOH溶液,反应的离子方程式是_______。
(4)野外焊接钢轨常采用铝热反应,发生的反应为 。
a.该反应所属基本反应类型是_______。
b.该反应中,发生氧化反应的是_______(填化学式包括以下各空),发生还原反应的_______,氧化产物是
_______,还原产物是_______。
a.b.18.(8分)根据化学知识和基本原理回答下列问题。
(1)根据组成和性质分类, 应属于_______氧化物;金属Al溶于氢氧化钠溶液的离子反应方程式为
_______。
(2)15.6g 固体中所含阴离子的数目为_______,标准状况下4.48L 中所含电子数目为_______,
与其含有相同H原子数目的HC1气体的物质的量为_______mol。
(3)将0.4mol HCl气体溶于水配成200mL溶液,则所得盐酸溶液中溶质的物质的量浓度为_______mol/L,
从该溶液中取出25.00mL,加水稀释至500mL,则稀释后盐酸溶液中溶质的物质的量浓度为
_______mol/L。
(4)100mL某 和 的混合溶液中,已知 , ,则该
溶液中所含 的物质的量浓度为_______mol/L。
19.(10分)元素的“价一类”二维图是我们学习元素及其化合物相关知识的重要模型和工具,它指的是
以元素的化合价为纵坐标,以物质的类别为横坐标所绘制的二维平面图像。如图为铁元素的“价一类”二
维图,箭头表示部分物质间的转化关系。请回答以下问题:
(1) 中Fe的化合价为_______。
(2) 是否为碱性氧化物_______(填是或否),理由:_______。
(3)制备氢氧化亚铁时,现象由白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释现象:_______。
(4)已知 在强碱溶液中稳定存在,PH越小稳定性越差;则制备 时需要在_______(填“酸
性”“碱性”或“中性”)环境中进行: 也可以作为净水剂,能与水反应生成具有吸附性的
胶体,写出其中离子方程式:_______。其中检验溶液中 的试剂是_______。
(5)FeO、 是合成氨工业生产中所用的 催化剂的主要成分。某FeO、 混合物中,铁原子、氧
原子的物质的量之比为4∶5,其中FeO、 的物质的量之比为_______。
20.(12分)(2023·上海徐汇·统考二模)金属钠及其化合物在人类生产、生活中起着重要作用。
(1)Na的轨道表示式为_______。
(2)NaCl的熔点为800.8℃。工业上,采用电解熔融的NaCl和 混合盐,制备金属Na,电解的化学方
程式为: ,加入 的目的是_______。
(3)采用空气和Na为原料可直接制备 。空气与熔融的金属Na反应前需依次通过的试剂为_______、
_______(填序号)。
a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d. 溶液
(4) 的电子式为_______。在25℃和101kPa时,Na与 反应生成 放出510.9kJ的热量,写
出该反应的热化学方程式:_______。
(5)向酸性 溶液中加入 粉末,观察到溶液褪色,发生如下反应。
配平上述离子方程式_______。
该反应说明 具有_______(选填“氧化性”“还原性”或“漂白性”)。
(6)在密闭容器中,将 和bmol 固体混合物加热至250℃,充分反应后,若剩余固体为和NaOH、排出气体为 和 时, 的取值范围为_______。
21.(9分)某干燥白色固体可能含有 , 、 中的几种,取一定质量的该固体加蒸馏
水配制 溶液,并向该溶液中滴加 的盐酸,得到 体积(换算成标准状况下)与盐酸体积
的关系如图所示。请回答下列问题:
(1)产生的 的物质的量为_______ ,AB段发生反应的化学方程式为_______。
(2)若白色固体由 和 组成,则x=_______, _______。
(3)若白色固体由 和 组成, ,则 与 溶于水后发生反应的离子方程式为
_______, _______。
(4)若白色固体只由 和 组成,且 , ,则 _______ 。