文档内容
考点 02 离子反应 离子方程式
1.3年真题考点分布
考点分布
年份 卷区
电解质 离子方程式正误判断 溶液的导电性
福建 √
广东 √
2022 江苏 √
湖南 √
浙江 √ √
广东 √
湖北 √
2021
北京 √ √
浙江 √
北京 √
江苏 √
2020
天津 √
浙江 √ √
2.命题规律及备考策略
【命题规律】近3年新高考卷对于离子反应的考查主要有:
(1)电解质的相关概念判断
(2)电离方程式的书写
(3)电解质溶液导电性
(4)离子方程式正误判断
(5)陌生离子方程式书写
【备考策略】熟练掌握各种物质之间的转化关系,明确离子方程式的拆分规则。另外,在学习过程中,要注意
一书写的熟练度,能够达到直接写出离子方程式。
【命题预测】纵观近几年高考会发现本讲内容在高考试题中主要涉及点为离子方程式的书写及判断,在选择题
的个别选项中也会考查电解质的判断及其电离知识,其中离子反应方程式的书写和判断为高考的必考题型,预
计今后还会结合氧化还原反应、化学反应原理在工艺流程、实验题中考查,该类试题具有一定的综合性。
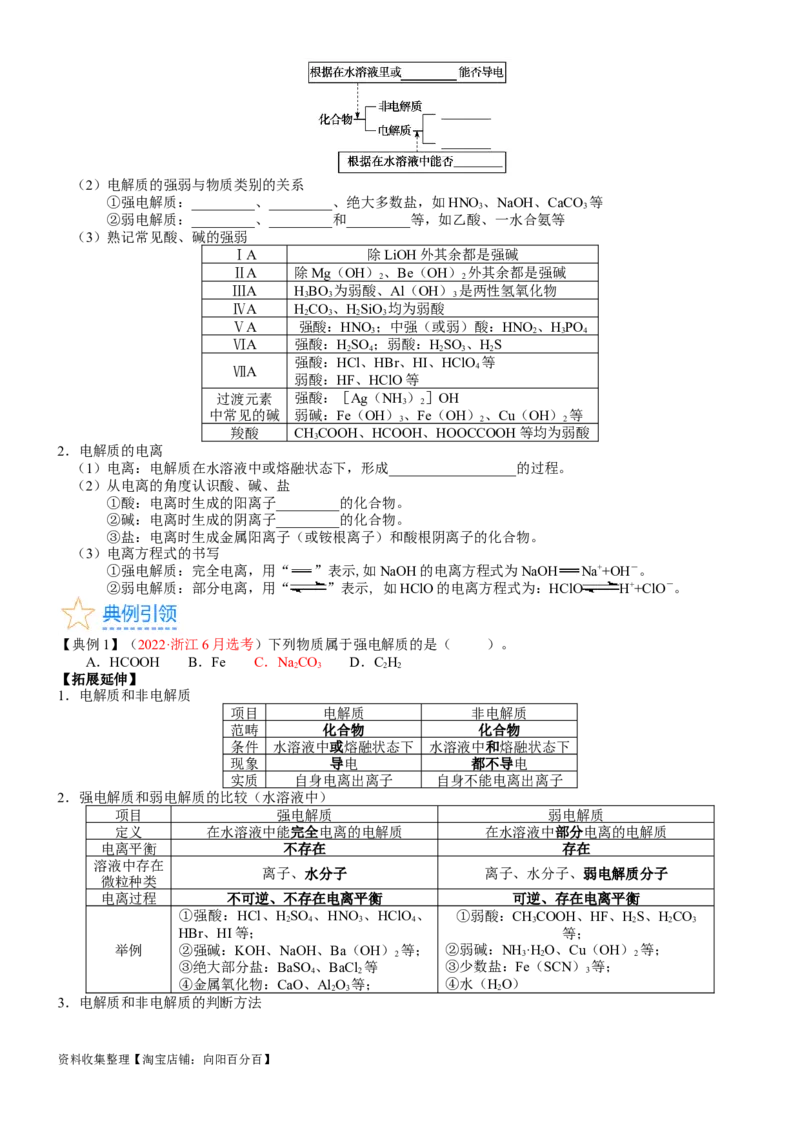
考法 1 电解质及其电离
一、电解质及其电离
1.电解质和非电解质
(1)分类依据
资料收集整理【淘宝店铺:向阳百分百】(2)电解质的强弱与物质类别的关系
①强电解质:_________、_________、绝大多数盐,如HNO、NaOH、CaCO 等
3 3
②弱电解质:_________、_________和_________等,如乙酸、一水合氨等
(3)熟记常见酸、碱的强弱
ⅠA 除LiOH外其余都是强碱
ⅡA 除Mg(OH)、Be(OH) 外其余都是强碱
2 2
ⅢA HBO 为弱酸、Al(OH) 是两性氢氧化物
3 3 3
ⅣA HCO、HSiO 均为弱酸
2 3 2 3
ⅤA 强酸:HNO;中强(或弱)酸:HNO、HPO
3 2 3 4
ⅥA 强酸:HSO ;弱酸:HSO 、HS
2 4 2 3 2
强酸:HCl、HBr、HI、HClO 等
ⅦA 4
弱酸:HF、HClO等
过渡元素 强酸:[Ag(NH )]OH
3 2
中常见的碱 弱碱:Fe(OH)、Fe(OH)、Cu(OH) 等
3 2 2
羧酸 CHCOOH、HCOOH、HOOCCOOH等均为弱酸
3
2.电解质的电离
(1)电离:电解质在水溶液中或熔融状态下,形成__________________的过程。
(2)从电离的角度认识酸、碱、盐
①酸:电离时生成的阳离子_________的化合物。
②碱:电离时生成的阴离子_________的化合物。
③盐:电离时生成金属阳离子(或铵根离子)和酸根阴离子的化合物。
(3)电离方程式的书写
①强电解质:完全电离,用“ ”表示,如NaOH的电离方程式为NaOH Na++OH-。
②弱电解质:部分电离,用“ ”表示, 如HClO的电离方程式为:HClO H++ClO-。
【典例1】(2022·浙江6月选考)下列物质属于强电解质的是( )。
A.HCOOH B.Fe C.NaCO D.C H
2 3 2 2
【拓展延伸】
1.电解质和非电解质
项目 电解质 非电解质
范畴 化合物 化合物
条件 水溶液中或熔融状态下 水溶液中和熔融状态下
现象 导电 都不导电
实质 自身电离出离子 自身不能电离出离子
2.强电解质和弱电解质的比较(水溶液中)
项目 强电解质 弱电解质
定义 在水溶液中能完全电离的电解质 在水溶液中部分电离的电解质
电离平衡 不存在 存在
溶液中存在
离子、水分子 离子、水分子、弱电解质分子
微粒种类
电离过程 不可逆、不存在电离平衡 可逆、存在电离平衡
①强酸:HCl、HSO 、HNO 、HClO 、 ①弱酸:CHCOOH、HF、HS、HCO
2 4 3 4 3 2 2 3
HBr、HI等; 等;
举例 ②强碱:KOH、NaOH、Ba(OH) 等; ②弱碱:NH ·HO、Cu(OH) 等;
2 3 2 2
③绝大部分盐:BaSO、BaCl 等 ③少数盐:Fe(SCN) 等;
4 2 3
④金属氧化物:CaO、Al O 等; ④水(HO)
2 3 2
3.电解质和非电解质的判断方法
资料收集整理【淘宝店铺:向阳百分百】【特别提醒】
(1)电解质不一定能导电,如固态NaCl、液态HCl等;能导电的物质不一定是电解质,如金属单质和电解质
溶液等。
(2)非电解质不导电,但不导电的物质不一定是非电解质,如金刚石、单质硫等一些非金属单质。(3)强电
解质溶液的导电能力不一定强,弱电解质溶液的导电能力不一定弱,如极稀的NaCl溶液的导电能力不如浓氨水
的导电能力强。溶液的导电能力取决于自由移动离子的浓度和离子的电荷数,离子浓度越大,所带电荷数越多,
溶液导电能力越强。
(4)电解质是指自身电离能生成离子的化合物,有些化合物的水溶液能导电,但溶液中的离子不是它自身电离
产生的,不属于电解质,如 CO 、SO 、NH 、SO 等非电解质,它们与水反应生成的产物 HCO 、HSO 、
2 2 3 3 2 3 2 3
NH ·H O、HSO 是电解质。
3 2 2 4
【典例2】(2023·河南商丘高三上学期期中)下列指定化学用语正确的是( )。
A.NaHCO 的电离方程式:NaHCO Na++H++CO 2-
3 3 3
B.HF的电离方程式:HF H++F-
C.NaHSO 在水溶液中的电离方程式:NaHSO Na++H++SO2-
4 4 4
D.HS的电离方程式:HS 2H++S2-
2 2
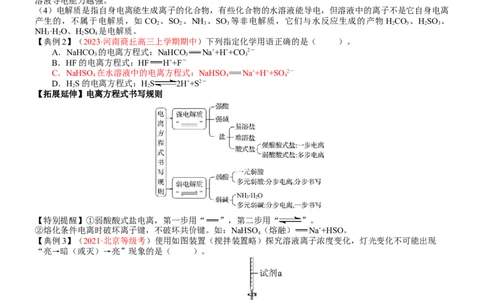
【拓展延伸】电离方程式书写规则
【特别提醒】①弱酸酸式盐电离,第一步用“ ”,第二步用“ ”。
②熔化条件电离时破坏离子键,不破坏共价键。如:NaHSO(熔融) Na++HSO。
4
【典例3】(2021·北京等级考)使用如图装置(搅拌装置略)探究溶液离子浓度变化,灯光变化不可能出现
“亮→暗(或灭)→亮”现象的是( )。
选项 A B C D
试剂
CuSO NH HCO HSO CHCOOH
a 4 4 3 2 4 3
试剂
Ba(OH) Ca(OH) Ba(OH) NH ·HO
b 2 2 2 3 2
【拓展延伸】
1.电解质导电性与导电能力强弱的判断
资料收集整理【淘宝店铺:向阳百分百】2.金属导电与电解质溶液导电的原理比较
(1)金属导电是由于自由电子在电场作用下的定向移动。温度升高,金属阳离子振动幅度增大,自由电子定
向移动阻力增大,金属导电性减弱。
(2)电解质溶液之所以导电,是由于溶液中有自由移动的离子存在。电解质溶液导电能力的大小,和电解质
的强弱没有必然联系,取决于溶液中自由移动离子的浓度和离子的电荷数。但温度升高时,弱电解质电离程度
增大,离子浓度增大,导电性会增强;但强电解质溶液的导电性不变。
1.(2023·梅州模拟)下列说法中正确的是( )。
A.HSO 是电解质,所以HSO 能导电
2 4 2 4
B.电解质与非电解质的本质区别是在一定条件下自身能否电离
C.酸、碱和盐都属于电解质,其他化合物一定都是非电解质
D.NaCl和HCl都是电解质,所以它们熔融状态下都能导电
2.(2023·德阳模拟)下列物质在水溶液中的电离方程式不正确的是( )。
A.Ba(OH) Ba2++2OH-
2
B.KHCO K++H++CO 2-
3 3
C.NaHSO Na++H++SO2-
4 4
D.NaCO 2Na++CO 2-
2 3 3
3.(2023·泉州模拟)用如图装置分别进行导电性实验,使小灯泡明显变暗的实验操作是( )。
A.向CHCOOH溶液中加入适量NaOH固体
3
B.向SO 饱和溶液中滴加适量HO 溶液
2 2 2
C.向AgNO 溶液中加入适量NaCl固体
3
D.向HSO 稀溶液中加入适量Ba(OH) 固体
2 4 2
4.现有9种物质:①铜;②稀硫酸;③HCl;④乙醇;⑤NaCl;⑥HS;⑦CaCO ;⑧蔗糖;⑨Fe(OH)。
2 3 3
(1)属于非电解质的有________(填序号,下同)。
(2)属于电解质,但熔融状态下不能导电的是________________。
(3)既不是电解质,也不是非电解质,但本身能导电的是________________。
(4)属于强电解质的是________。
(5)分别写出③⑥⑨的电离方程式:________________、________________、________________。
考法 2 离子反应、离子方程式的书写
1.离子反应
(1)概念:在溶液中有离子参加或生成的反应。
(2)本质:溶液中某些离子的种类或浓度改变。
(3)类型
①复分解反应型:在溶液中离子间发生互换生成沉淀、气体或难电离物质(水、弱酸、弱碱)。
Ag++Cl- AgCl↓,CO2-+2H+ HO+CO↑,NH ++OH- NH ·HO
3 2 2 4 3 2
②氧化还原反应型:离子或物质间发生电子转移生成新的离子或物质。
Fe+Cu2+ Fe2++Cu,2Fe2++2H++H O 2Fe3++2H O
2 2 2
③盐类的水解反应型:在溶液中盐电离出的离子与水电离出的H+或OH-结合生成弱电解质。
Fe3++3H O Fe(OH)+3H+,SO2-+H O HSO-+OH-
2 3 3 2 3
④络合反应型:离子间通过配位键结合成络合物(或配合物)或络离子。
Fe3++3SCN- Fe(SCN),Cu2++4NH ·HO Cu(NH )2++4HO
3 3 2 3 4 2
⑤电化学反应型:实质为氧化还原反应,但需要添加电解或通电条件。
资料收集整理【淘宝店铺:向阳百分百】2Cl-+2H O 2OH-+Cl↑+H↑,2Cu2++2H O 2Cu+O ↑+4H+
2 2 2 2 2
2.离子方程式
(1)概念:用实际参加反应的离子符号来表示离子反应的式子。
(2)意义:不仅表示一定物质间的某个反应,而且可以表示同一类型的离子反应。
①CaCO +2CH COOH Ca2++2CH COO-+CO ↑+H O表示___________________________
3 3 3 2 2
②CaCO +2H+ Ca2++CO ↑+H O表示_____________________________________________
3 2 2
(3)离子方程式书写步骤以CaCO 与盐酸的反应为例。
3
【典例4】(2023·湖南等级考)下列有关电极方程式或离子方程式错误的是( )。
A.碱性锌锰电池的正极反应:MnO +H O+e- MnO(OH)+OH-
2 2
B.铅酸蓄电池充电时的阳极反应:Pb2++2H O-2e- PbO +4H+
2 2
C.K[Fe(CN)]溶液滴入FeCl 溶液中:K++Fe2++[Fe(CN)]3- KFe[Fe(CN)]↓
3 6 2 6 6
D.TiCl 加入水中:TiCl +(x+2)HO TiO·xHO↓+4H++4Cl-
4 4 2 2 2
【拓展延伸】正确判断离子方程式的关键点
1.审清题意“三注意”
(1)注意反应环境;
(2)注意操作顺序;
(3)注意反应物之间量的关系。
2.化学式拆写“四原则”
(1)易溶强电解质拆,弱电解质、难溶物不拆;
(2)微溶物清拆浊不拆;
(3)单质、氧化物不拆;
(4)浓硫酸不拆,浓盐酸、浓硝酸拆。
3.反应产物“三分析”
(1)分析量不同时的产物;
(2)分析是否漏掉同步反应;
(3)分析变价元素的产物。
4.方程式遵循“三守恒”
(1)原子是否守恒;
(2)电荷是否守恒;
(3)得失电子是否守恒。
【规律方法】一般离子方程式正误判断流程
【典例5】(1)(2023·湖北选择考)铜与过量HO 反应的探究如下:
2 2
实验②中Cu溶解的离子方程式为_____________________________________;产生的气体为_______。比较实验
资料收集整理【淘宝店铺:向阳百分百】①和②,从氧化还原角度说明H+的作用是_____________。
(2)(2023·湖南选择考)雷尼Ni的制备
操作(a)中,反应的离子方程式是________________________________。
【典例6】下列反应的离子方程式不正确的是____________。
A.(2021·全国乙卷)过量铁粉加入稀硝酸中:3Fe2++4H++NO- 3Fe3++2H O+NO↑
3 2
B.(2021·全国乙卷)硫酸铝溶液中滴加少量氢氧化钾溶液:Al3++4OH- AlO-+2H O
2 2
C.(2022·浙江6月选考)NaCO 溶液中通入过量SO:CO2-+2SO+2H O 2HSO -+CO
2 3 2 3 2 2 3 2
D.(2022·全国甲卷)明矾溶液与过量氨水湿合:Al3++4NH+4HO AlO-+4NH+
3 2 2 4
E.(2021·湖北省选择考)向次氯酸钙溶液中通入少量二氧化碳气体:ClO-+CO +H O HClO+HCO -
2 2 3
F.(2020·天津等级考)NaOH溶液与过量HC O 溶液反应:HC O+2OH- C O2-+2H O
2 2 4 2 2 4 2 4 2
G.(2020·天津等级考)C HONa溶液中通入少量CO:2C HO-+CO +H O 2C HOH+CO2-
6 5 2 6 5 2 2 6 5 3
H.(2020·江苏高考)0.1mol·L-1AgNO 溶液中加入过量浓氨水:Ag++NH+H O AgOH↓+NH +
3 3 2 4
I.(2020·全国Ⅲ卷)用NaSO 溶液吸收少量Cl:3SO 2-+Cl+H O 2HSO -+2Cl-+SO 2-
2 3 2 3 2 2 3 4
J.(2020·浙江7月选考)(NH )Fe(SO ) 溶液与少量Ba(OH) 溶液反应:SO 2-+Ba2+ BaSO↓
4 2 4 2 2 4 4
K.(2018·浙江4月学考真题)漂白粉溶液吸收少量二氧化硫气体:SO +H O+ClOˉ SO 2-+Clˉ+2H+
2 2 4
L.(2015·四川高考)CuSO 溶液与过量浓氨水反应的离子方程式:Cu2++2NH·HO=Cu(OH)↓+2NH+
4 3 2 2 4
【拓展延伸】与量有关的离子方程式的几种类型
一、连续型
指反应生成的离子因又能跟剩余(过量)的反应物继续反应而跟用量有关。
1.可溶性多元弱酸(或其酸酐)与碱溶液反应。如CO 通入NaOH溶液中:
2
(1)少量CO:CO+2OH- CO2-+HO
2 2 3 2
(2)过量CO:CO+OH- HCO -
2 2 3
2.多元弱酸(或其酸酐)与更弱酸的盐溶液反应。如CO 通入Na[Al(OH)]溶液中:
2 4
(1)少量CO:2[Al(OH)]-+CO 2Al(OH)↓+CO 2-+H O
2 4 2 3 3 2
(2)过量CO:[Al(OH)]-+CO Al(OH)↓+HCO-
2 4 2 3 3
3.多元弱酸盐与强酸反应。如NaCO 溶液与稀盐酸
2 3
(1)少量盐酸:CO2-+H+ HCO -
3 3
(2)过量盐酸:CO2-+2H+ CO↑+H O
3 2 2
4.铝盐溶液与强碱溶液反应
(1)少量强碱:Al3++3OH- Al(OH)↓
3
(2)过量强碱:Al3++4OH- [Al(OH)]-
4
5.Na[Al(OH)]溶液与强酸溶液反应
4
(1)少量强酸:[Al(OH)]-+H+ Al(OH)↓+H O
4 3 2
(2)过量强酸:[Al(OH)]-+4H+ Al3++4H O
4 2
6.Fe与稀HNO 溶液反应
3
(1)少量铁:Fe+NO-+4H+ Fe3++NO↑+2H O
3 2
(2)过量铁:3Fe+2NO-+8H+ 3Fe2++2NO↑+4H O
3 2
二、先后型
一种反应物的两种或两种以上的组成离子,都能跟另一种反应物的组成离子反应,但因反应次序不同而跟
用量有关。又可称为竞争型。
1.NH HSO 溶液与NaOH溶液的反应
4 4
(1)少量NaOH:H++OH- HO
2
(2)过量NaOH:NH ++H++2OH- NH ·HO+HO
4 3 2 2
2.将Fe(NO ) 溶液与HI混合
3 3
(1)少量HI:8H++2NO-+6I- 4HO+3I +2NO↑
3 2 2
(2)过量HI:Fe3++12H++3NO-+10I- Fe2++5I +6H O+3NO↑
3 2 2
3.向FeBr 溶液通入Cl
2 2
(1)少量Cl:2Fe2++Cl 2Fe3++2Cl-
2 2
(2)过量Cl:2Fe2++4Br-+3Cl 2Fe3++2Br +6Cl-
2 2 2
4.向FeI 溶液通入Cl
2 2
(1)少量Cl:2I-+Cl=I+2Cl-
2 2 2
(2)过量Cl:2Fe2++4I-+3Cl 2Fe3++2I+6Cl-
2 2 2
5.向含有OH-、CO2-、[Al(OH)]-的溶液中,逐滴加入稀盐酸至过量,反应依次是:
3 4
(1)OH-+H+ HO
2
资料收集整理【淘宝店铺:向阳百分百】(2)[Al(OH)]-+H+ Al(OH)↓+H O
4 3 2
(3)CO2-+H+ HCO -、HCO -+H+ CO↑+H O
3 3 3 2 2
(4)Al(OH)+3H+ Al3++3H O
3 2
6.向含有H+、Al3+、NH +的溶液中,逐滴加入NaOH溶液至过量,反应依次为:
4
(1)H++OH- HO
2
(2)Al3++3OH- Al(OH)↓
3
(3)NH ++OH- NH ·HO
4 3 2
(4)Al(OH)+OH- [Al(OH)]-
3 4
三、配比型
当一种反应物中有两种或两种以上组成离子参与反应时,因其组成比例不协调(一般为复盐或酸式盐),
当一种组成离子恰好完全反应时,另一种组成离子不能恰好完全反应(有剩余或不足),因而跟用量有关。
1.Ca(HCO ) 溶液与NaOH溶液反应
3 2
(1)少量NaOH:Ca2++HCO-+OH- CaCO ↓+H O
3 3 2
(2)过量NaOH:Ca2++2HCO-+2OH- CaCO ↓+2H O+CO2-
3 3 2 3
2.NaHCO 溶液与Ca(OH) 溶液反应
3 2
(1)少量NaHCO :HCO -+OH-+Ca2+ CaCO ↓+H O
3 3 3 2
(2)过量NaHCO :Ca2++2OH-+2HCO- CaCO ↓+CO 2-+2H O
3 3 3 3 2
3.Ba(OH) 溶液与NaHSO 溶液反应
2 4
(1)n[Ba(OH)]∶n(NaHSO)=1∶1,Ba2++OH-+H++SO2- BaSO↓+H O,此时溶液呈碱性;
2 4 4 4 2
(2)n[Ba(OH) ]∶n(NaHSO )=1∶2,Ba2++2OH-+2H++SO2- BaSO↓+2H O,此时溶液呈中性,
2 4 4 4 2
若向该溶液中再加入Ba(OH) 溶液,离子方程式为SO 2-+Ba2+ BaSO↓。
2 4 4
4.KAl(SO ) 与Ba(OH) 溶液反应
4 2 2
(1)n[KAl(SO )]∶n[Ba(OH)]=1∶1,3Ba2++3SO2-+2Al3++6OH- 3BaSO↓+2Al(OH)↓
4 2 2 4 4 3
(2)n[KAl(SO )]∶n[Ba(OH)]=1∶2,Al3++2SO2-+2Ba2++4OH- [Al(OH)]-+2BaSO ↓
4 2 2 4 4 4
5.NH Al(SO ) 与Ba(OH) 溶液反应
4 4 2 2
(1)n[NH Al(SO ) ]∶n[Ba(OH) ]=1∶1,3Ba2++3SO2-+2Al3++6OH- 3BaSO↓+2Al(OH)
4 4 2 2 4 4
↓
3
(2)n[NH Al(SO ) ]∶n[Ba(OH) ]=1∶2,NH ++Al3++2SO2-+2Ba2++4OH- NH ·HO+Al
4 4 2 2 4 4 3 2
(OH)↓+2BaSO ↓
3 4
【特别提醒】常见的与量无关的离子反应
(1)向 ONa溶液通入少量或过量CO: O-+CO +H O C HOH+HCO-
2 2 2 6 5 3
(2)向NaClO溶液通入少量或过量CO:ClO-+CO +H O HClO+HCO-
2 2 2 3
(3)向铝盐溶液通入少量或过量NH :Al3++3NH·HO Al(OH)↓+3NH+
3 3 2 3 4
1.(重庆市2022~2023学年高三上学期半期质量监测)下列有关离子方程式正确的是( )。
A.向纯碱溶液中滴加少量稀盐酸:2H++CO2- HO+CO↑
3 2 2
B.Fe(OH) 胶体的制备:Fe3++3H O Fe(OH)(胶体)+3H+
3 2 3
C.向氯化镁溶液中加入过量氨水:Mg2++2OH- Mg(OH)↓
2
D.Al和氢氧化钠溶液反应:Al+2OH- AlO-+H ↑
2 2
2.(2022~2023学年豫北名校11月大联考)下列有关硫及其化合物之间转化反应的离子方程式正确的是(
)。
A.硫单质转化为S2-:2S+4OH- SO 2-+S2-+2HO
3 2
B.SO 2-转化为HSO -:SO2-+SO +H O 2HSO -
3 3 3 2 2 3
C.向NaSO 溶液中滴加稀硝酸:2H++S O2- SO ↑+S↓+H O
2 2 3 2 3 2 2
D.FeS与盐酸反应制备HS:S2-+2H+ HS↑
2 2
3.(2022·福建等级考)实验室需对少量污染物进行处理。以下处理方法和对应的反应方程式均错误的是(
)。
A.用硫磺处理洒落在地上的水银:S+Hg HgS
B.用盐酸处理银镜反应后试管内壁的金属银:2Ag+2H+ 2Ag++H ↑
2
C.用烧碱溶液吸收蔗糖与浓硫酸反应产生的刺激性气体:SO +2OH- SO 2-+H O
3 4 2
D.用烧碱溶液吸收电解饱和食盐水时阳极产生的气体:Cl+2OH- Cl-+ClO-+HO
2 2
【基础过关】
资料收集整理【淘宝店铺:向阳百分百】1.下列俗名所表示的物质或其主要成分属于非电解质的是( )。
A.明矾 B.氯仿 C.生石灰 D.冰醋酸
2.(2023•泉州高三第一学期期中检测)下列化学用语正确的是( )。
A.NaHCO 的电离:NaHCO =Na++H++CO 2-
3 3 3
B.HS-的电离:HS-+H O HO++S2-
2 3
C.NaClO的电离:NaClO Na++ClO-
D.NH Cl水解方程式:NH ++H O=NH •HO+H+
4 4 2 3 2
3.(2022·辽阳高三上学期期中)仅能表示唯一化学反应的离子方程式是( )。
A.Zn+2H+=Zn2++H ↑
2
B.CHCOOH+OH―=CHCOO―+H O
3 3 2
C.Ba2++2OH―+2H++SO2―=BaSO↓+2H O
4 4 2
D.CHCOOH+NH ·HO=CHCOO―+NH++H O
3 3 2 3 4 2
4.(2022年广东肇庆高三3月模拟)下列方程式书写正确的是( )。
A.氯酸钾的电离方程式:KClO =K++Cl-+3O2-
3
B.氯化铁与铜反应的离子方程式:Fe3++Cu2+=Cu+Fe2+
C.金属钠投入硫酸铜溶液中:2Na+Cu2+=Cu+2Na+
D.少量氯水滴入NaI的溶液中:2I-+Cl=I+2Cl-
2 2
5.(2022·哈尔滨高三上学期期末)下列解释事实的离子方程式正确的是( )。
A.铁和稀硝酸反应制得浅绿色溶液:Fe+4H++NO- Fe3++NO↑+2H O
3 2
B.实验室盛碱液的瓶子不用玻璃塞:SiO+2OH- SiO2-+H O
2 3 2
C.碳酸氢镁和足量的氢氧化钙溶液反应:Ca2++OH-+HCO- CaCO ↓+H O
3 3 2
D.向Ca(ClO) 溶液中通入过量CO:2ClO-+H O+CO 2HClO+CO 2-
2 2 2 2 3
6.(2023·河南新郑高三上学期期中)下列反应的现象描述与离子方程式都正确的是( )。
A.锌片插入硝酸银溶液中,有银析出:Zn+Ag+=Zn2++Ag
B.氢氧化钡溶液与稀硫酸反应,有白色沉淀生成:SO 2-+Ba2+=BaSO↓
4 4
C.氢氧化铜加到盐酸中,无明显现象:Cu(OH)+2H+=Cu2++2H O
2 2
D.碳酸钡中加入稀盐酸,固体溶解,生成无色无味气体:BaCO↓+2H+=Ba2++CO ↑+H O
3 2 2
7.(广东省深圳市光明区2023届高三上学期第一次模拟)宏观辨识与微观探析是化学学科核心素养之一。下
列关于含N化合物的物质性质实验对应的反应方程式书写不正确的是( )。
3++4NH·HO AlO-+4NH ++2HO
A.将过量氨气通入氯化铝溶液中:Al 3 2 2 4 2
+3Cl 6NH Cl+N
B.用浓氨水检验氯气管道是否泄漏:8NH3 2 4 2
C.温度升高气体颜色加深:N
2
O
4
(g) 2NO
2
(g)△H>0
D.NaNO 溶液显碱性:NO -+H O HNO +OH-
2 2 2 2
8.(2023·吉林四平高三上学期期中)向0.01mol·L-1Ba(OH) 溶液中滴入几滴酚酞溶液后,匀速逐滴加入
2
0.2mol·L-1HSO 溶液,过程中测得混合溶液的电导率变化如图所示。下列有关说法正确的是( )。
2 4
A.0~80s溶液中仅c(Ba2+)降低
B.该反应的离子方程式为H++OH- HO
2
C.溶液颜色逐渐变浅说明BaSO 是难溶电解质
4
D.由80s时溶液的电导率数值可推出HO不是强电解质
2
9.(陕西省咸阳市2023年高考一模)下列离子方程式正确的是( )。
A.向饱和NaCO 溶液中通入足量CO:2Na++CO2-+H O+CO 2NaHCO ↓
2 3 2 3 2 2 3
B.向稀硝酸中滴加NaSO 溶液:SO2-+2H+ SO ↑+S↓+H O
2 2 3 2 3 2 2
C.向新制氯水中滴加少量的FeBr 溶液:2Fe2++2Br-+2Cl 2Fe3++Br +4Cl-
2 2 2
D.向NH Cl溶液中加入一小粒固体钠:2Na+2HO 2Na++2OH-+H ↑
4 2 2
10.(2023·江西省第-次高三大联考)下图是0.01mol/L甲溶液滴定0.01mol/L乙溶液的导电能力变化曲线,其
中曲线③是盐酸滴定NaAc溶液,其他曲线是醋酸滴定NaOH溶液或者NaOH溶液滴定盐酸。下列判断错误的
是( )。
资料收集整理【淘宝店铺:向阳百分百】A.条件相同时导电能力:盐酸>NaAc
B.曲线①是NaOH溶液滴定盐酸导电能力变化曲线
C.随着甲溶液体积增大,曲线①仍然保持最高导电能力
D.a点是反应终点
11.(2022~2023学年湖南郴州高三化学上学期期中)下列离子方程式错误的是( )。
A.向NaClO溶液中通入少量SO :2ClO-+SO+H O 2HClO+SO2-
2 2 2 3
B.高锰酸钾与浓盐酸反应制氯气:2MnO -+10Cl-+16H+ 2Mn2++5Cl↑+8H O
4 2 2
C.FeBr 通入少量的Cl:2Fe2++Cl 2Fe3++2Cl-
2 2 2
D.向NaSO 的酸性溶液中加入NaS:2S2-+SO2-+6H+ 3S↓+3H O
2 3 2 3 2
12.某固体混合物由KCl、KCO、KSO 和不溶于水的杂质组成。为了提纯KCl,将该混合物进行如下实验,
2 3 2 4
回答相关问题:
(1)试剂I的化学式为_________,①中发生反应的离子方程式为____________。
(2)试剂II的化学式为________,②中加入试剂II的目的是________________。
(3)试剂III的名称是_______,③中发生反应的离子方程式为______________。
(4)某同字根据最终所得KCl晶体和原样品的质里求算出氯化钾样品的纯度,你认为其结果是否可靠?并说明
理由(不考虑实验误差)_____________________。
13.一种用软锰矿(主要成分是MnO 、Al O、SiO)和黄铁矿(主要成分是FeS、SiO)为原料制取MnSO
2 2 3 2 2 2 4
溶液的流程如下:
(1)“浸出”后溶液中含有阳离子H+、Fe2+、Mn2+等,“浸出”过程中MnO 反应的离子方程式为
2
_______________________________________________________。
(2)“氧化”过程中发生反应的离子方程式为___________________________。
【能力提升】
1.(浙江省宁波市五校联盟2022~2023学年高三上学期期中联考)如图为NaCl在水中溶解和电离的示意图,
关于该图的说法中。错误的是( )。
A.在NaCl晶体中,Na+和Cl-的排列整齐有序
资料收集整理【淘宝店铺:向阳百分百】B.Na+、Cl-在水中是以水合离子的形式存在的
C.水合离子中,水分子取向都应该是氧原子朝内
D.上述过程通常可表示为NaCl Na++Cl-
2.(河南省新未来2023届高三上学期9月联考)下列过程中的化学反应,相应的离子方程式正确的是
( )。
Cl 通入石灰乳中制取漂白粉:Cl+2OH- Cl-+ClO-+HO
2 2 2
A.将
FeBr 的溶液中通入1molCl:2Fe2++2Br-+2Cl 2Fe3++Br +4Cl-
2 2 2 2
B.向含有1mol
NaHSO 溶液反应:HSO -+ClO- SO 2-+Cl-+H+
3 3 4
C.NaClO溶液与过量
D.向酸性KMnO 溶液中滴加双氧水:2MnO -+H O+6H+ 2Mn2++4HO+3O↑
4 4 2 2 2 2
3.(2023年3月辽宁锦州高三模拟)下列反应的离子方程式正确的是( )。
A.丙烯醛与足量溴水反应:CH=CHCHO+2Br +H O CHBrCHBrCOOH+2H++2Br-
2 2 2 2
B.H18O中投入NaO 固体:2H18O+2Na O 4Na++4OH-+18O↑
2 2 2 2 2 2 2
C.少量Cl 通入NaSO 溶液中:SO 2-+Cl+H O 2H++2Cl-+SO2-
2 2 3 3 2 2 4
D.用酸性高锰酸钾溶液滴定草酸:2MnO -+16H++5C O2- 2Mn2++10CO ↑+8H O
4 2 4 2 2
4.(宁波市2023学年第一学期选考模拟)下列离子方程式书写正确的是( )。
A.用FeS除去废水中的Hg2+:FeS+Hg2+ HgS+Fe2+
B.用醋酸溶液处理水垢中的氢氧化镁:Mg(OH)+2H+ Mg2++2H O
2 2
C.在NaS溶液中滴加NaClO溶液:S2-+ClO-+2H+ S↓+Cl-+H O
2 2
D.谷氨酸与足量氢氧化钠溶液反应:HOOC-(CH) COOH+OH- HOOC-(CH) COO-
2 2 2 2
+H O
2
5.(2023年宁夏银川高三第二次模拟)下列离子方程式与实验对应不正确的是( )。
选项 实验 离子方程式
向橙色KCr O 溶液中加入NaOH Cr O2-+2OH− 2CrO2-+H O
A 2 2 7 2 7 4 2
溶液,溶液变黄色
向AgCl悬浊液中加NaS溶液,有 2AgCl+S2− Ag S+2Cl−
B 2 2
黑色难溶物生成
向NH HCO 溶液中加入过量Ba NH ++HCO -+Ba2++2OH-
C 4 3 4 3
(OH) 稀溶液,有白色沉淀产生 BaCO ↓+NH·HO+HO
2 3 3 2 2
向KMnO 溶液(墨绿色)中加入 3MnO 2-+4H+ 2MnO -
2 4 4 4
D 适量醋酸,溶液变为紫色且有黑色 +MnO↓+2H O
2 2
沉淀生成
6.(湖南省三湘创新发展联合2022~2023学年高三上学期起点调研)用一定浓度的HSO 溶液分别滴定体积均
2 4
为20.00mL、浓度均为0.100mol/L的Ba(OH)、NaOH和NH ·HO三种溶液,滴定过程中三种溶液的电导率
2 3 2
如图所示。(已知:溶液电导率越大,导电能力越强)下列说法错误的是( )。
A.曲线①②③分别代表Ba(OH)、NaOH和NH ·HO
2 3 2
B.HSO 的浓度为0.100mol/L
2 4
C.a、b、c、d四点中,d点水的电离程度最小
D.d点对应的溶液中粒子浓度大小关系:c(NH +)+c(H+)=c(SO 2-)+c(OH-)
4 4
7.(2023·徐州高三上学期期末)莫尔盐[(NH )Fe(SO )•6H O]溶液经常用于定量滴定实验,下列有关
4 2 4 2 2
说法正确的是( )。
A.配制0.1mol•L-1莫尔盐溶液500mL,需莫尔盐19.6g
B.可与含Fe2+、HClO、H+、Cl-微粒的溶液大量共存
资料收集整理【淘宝店铺:向阳百分百】C.加入过量Ba(OH) 溶液发生反应:2Ba2++2SO2-+Fe2++2OH- 2BaSO↓+Fe(OH)↓
2 4 4 2
D.取样,加入浓NaOH溶液并加热,出现可让湿润的蓝色石蕊试纸变红的气体,证明含NH +
4
8.(新疆师范大学附属中学2023届高三上学期一模仿真训练)一定条件下,在NaS-HSO -HO 溶液体系
2 2 4 2 2
中,检测得到pH时间振荡曲线如下图所示,同时观察到体系由澄清→浑浊→澄清的周期性变化。下列有关反
应的离子方程式正确的是( )。
A.NaS溶液水解:S2-+2HO HS+2OH-
2 2 2
B.NaS溶液与少量HSO 反应:S2-+2H+ HS↑
2 2 4 2
C.体系由澄清变浑浊:HS-+HO+H+ S↓+2HO
2 2 2
D.体系由浑浊又变澄清:S+2HO SO 2-+4H+
2 2 4
9.(2023·菏泽高三4月模拟)下列离子方程式正确的是( )。
A.Fe(OH) 与氢溴酸溶液混合:Fe(OH)+3H+ Fe3++3H O
3 3 2
B.1mol/L的NaAlO 溶液和2.5mol/L的HCl等体积互相均匀混合:2AlO―+5H+ Al(OH)↓+Al3+
2 2 3
+HO
2
C.向硫酸铝铵[NH Al(SO )]溶液中滴加少量Ba(OH) 溶液:NH ++Al3++2SO2-+2Ba2++5OH-
4 4 2 2 4 4
AlO-+2BaSO ↓+ NH ·HO+2H O
2 4 3 2 2
D.向Ca(ClO) 溶液中通入适量SO :Ca2++2ClO-+SO+H O CaSO↓+2HClO
2 2 2 2 3
10.(湘潭市2023届高三第一次模拟)下列离子方程式正确的是( )。
Ba(OH) 溶液,至沉淀质量最大时反应的离子方程式为2Al3++3SO2-+3Ba2+
2 4
A.向明矾溶液中逐滴滴入
+6OH- 3BaSO↓+2Al(OH)↓
4 3
NaOH溶液:Mg2++2HCO-+2OH- MgCO ↓+2HO+CO2-
3 3 2 3
B.向碳酸氢镁溶液中加入过量的
1molFeBr 的溶液中通入标准状况下22.4LCl 时,发生的反应为2Fe2++2Br-+2Cl Br +2Fe3++4Cl-
2 2 2 2
C.向含
NaHSO 溶液中滴入Ba(OH) 溶液至恰好显中性:Ba2++OH-+H++SO2-=BaSO↓+H O
4 2 4 4 2
D.向
11.电解质在人体内的作用是十分广泛和十分重要的,当电解质紊乱时,人体就要出现一系列不适症状,甚至
会危及生命。现有下列几种物质:①铜;②NH ;③HSO ;④Ba(OH) 固体;⑤熔融的NaHSO;⑥稀盐酸。
3 2 4 2 4
(1)将上述各物质按物质的分类方法填写在表格的空白处(填物质编号):
分类标准 能导电的 电解质 非电解质
属于该类的物 _______
________ ________
质 _
(2)上述六种物质中有两种物质之间可发生离子反应:H++OH-=HO,该离子反应对应的化学方程式为
2
_________________________。
(3)⑤在水中的电离方程式为___________________________________________。
(4)将少量④的溶液加入⑤的溶液中,溶液呈中性,反应的离子方程式为_______________________。
12.工业生产无铁硫酸铝,以硫酸浸取铝土矿(主要成分是Al O,还有少量的Fe O、SiO)得含铁(Fe3+)的
2 3 2 3 2
硫酸铝溶液,加热到一定温度,搅拌,加入一定量高锰酸钾溶液和硫酸锰溶液,在溶液中生成活性二氧化锰,
调节溶液的pH,反应一段时间,二氧化锰和Fe(OH) 发生吸附共沉作用,最终得到无铁硫酸铝产品。
3
(1)硫酸浸取铝土矿时主要反应的离子方程式为________________________;
(2)完成高锰酸钾溶液和硫酸锰溶液反应的化学方程式:2KMnO +3MnSO +2H O=
4 4 2
________________________________;
(3)调节pH的作用是________________________________;
(4)操作1的名称为________,实验室进行操作2用到的陶瓷质仪器有________;
(5)下列有关工艺的说法正确的是________(双选,填字母)。
A.可以向溶液中再加入铝土矿粉等调节pH
资料收集整理【淘宝店铺:向阳百分百】