文档内容
考点 03 物离子共存 离子的检验与推断
目录
................................................................................................................................................1
1.高考真题考点分布......................................................................................................................................1
2.命题规律及备考策略..................................................................................................................................1
................................................................................................................................................2
考法01 离子共存的判断..............................................................................................................................2
考法02 离子检验和推断..............................................................................................................................5
................................................................................................................................................7
1.高考真题考点分布
考点内容 考点分布
2018年江苏卷4题,3分;
离子共存的判断 2019年江苏卷4题,3分;
2020年江苏卷4题,3分。
离子检验和推断 2023年江苏卷,11题,3分。
2.命题规律及备考策略
【命题规律】
近几年江苏高考对离子共存的选择考察较少,主要在工业流程中废液成分分析中进行命题;离子检验多出
现在实验方案设计中。
【备考策略】
解答有关离子共存试题的方法步骤
(1)抓住关键词语
解答离子共存类试题要审清题目要求的关键词语,如“一定大量共存”“可能大量共存”或“不能大量共
存”等。(2)理解两大条件
若溶液可能呈强酸性也可能呈强碱性时,“可能大量共存”的含义是在两种条件下只要有一种能大量共存
即符合题目要求。“一定大量共存”的含义是两种条件下离子均能大量共存才符合题目要求。
【命题预测】
预计2025年高考会以新的情境载体考查有关物质的成分、分类、转化、胶体的本质知识,题
目难度一般较小。
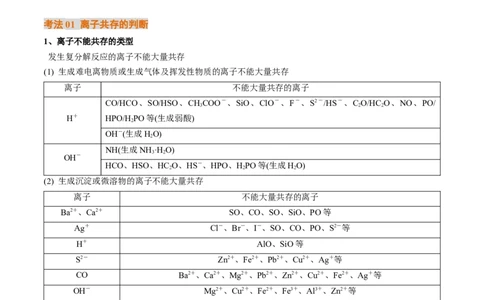
考法01 离子共存的判断
1、离子不能共存的类型
发生复分解反应的离子不能大量共存
(1) 生成难电离物质或生成气体及挥发性物质的离子不能大量共存
离子 不能大量共存的离子
CO/HCO、SO/HSO、CHCOO-、SiO、ClO-、F-、S2-/HS-、C O/HC O、NO、PO/
3 2 2
H+ HPO/H PO等(生成弱酸)
2
OH-(生成HO)
2
NH(生成NH ·H O)
3 2
OH-
HCO、HSO、HC O、HS-、HPO、HPO等(生成HO)
2 2 2
(2) 生成沉淀或微溶物的离子不能大量共存
离子 不能大量共存的离子
Ba2+、Ca2+ SO、CO、SO、SiO、PO等
Ag+ Cl-、Br-、I-、SO、CO、PO、S2-等
H+ AlO、SiO等
S2- Zn2+、Fe2+、Pb2+、Cu2+、Ag+等
CO Ba2+、Ca2+、Mg2+、Pb2+、Zn2+、Cu2+、Fe2+、Ag+等
OH- Mg2+、Cu2+、Fe2+、Fe3+、Al3+、Zn2+等
AlO HCO、HSO等
发生氧化还原反应的离子不能大量共存
(1) 常见的因氧化还原反应而不能大量共存的离子(“√”表示能反应,“×”表示不能反应,“—”表示不讨
论)
S2-(HS-) SO(HSO) I- Fe2+ Br- Cl-
MnO(H+) √ √ √ √ √ √
Cr O(H+) √ √ √ √ √ √
2
ClO- √ √ √ √ √ √(酸性)NO(H+) √ √ √ √ — ×
Fe3+ √ √ √ × × ×
(2) H+与SO不能大量共存:
2
2H++SO===S↓+SO ↑+HO
2 2 2
(3) S2-、SO在酸性条件下不能大量共存:
2S2-+SO+6H+===3S↓+3HO
2
发生相互促进的水解反应的离子不能大量共存
阳离子 阴离子
Al3+ CO、HCO、AlO、S2-、HS-、SiO、ClO-等
Fe3+ CO、HCO、AlO、SiO、ClO-等
NH AlO、SiO等
发生络合反应的离子(或分子)不能大量共存
(1) Fe3+与SCN-、苯酚等。
(2) Ag+、Cu2+、Zn2+等与NH ·H O。
3 2
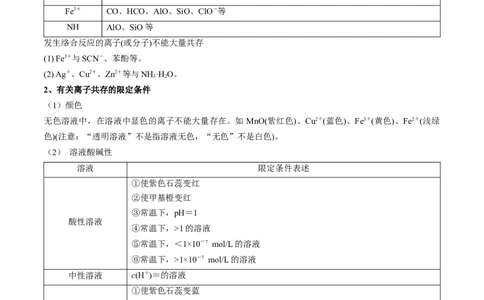
2、有关离子共存的限定条件
(1)颜色
无色溶液中,在溶液中显色的离子不能大量存在。如 MnO(紫红色)、Cu2+(蓝色)、Fe3+(黄色)、Fe2+(浅绿
色)(注意:“透明溶液”不是指溶液无色,“无色”不是白色)。
(2) 溶液酸碱性
溶液 限定条件表述
①使紫色石蕊变红
②使甲基橙变红
③常温下,pH=1
酸性溶液
④常温下,>1的溶液
⑤常温下,<1×10-7 mol/L的溶液
⑥常温下,>1×10-7 mol/L的溶液
中性溶液 c(H+)=的溶液
①使紫色石蕊变蓝
②使酚酞变红
③常温下,pH=13
碱性溶液
④常温下,<1的溶液
⑤常温下,>1×10-7 mol/L的溶液
⑥常温下,<1×10-7 mol/L的溶液
酸性或 ①常温下由水电离出的c(H+)<1×10-7 mol/L 的溶液
碱性溶液 ②与Al反应能放出H 的溶液(酸性溶液中不含有NO)
2
【易错提醒】
纯净物和混合物判断中的特殊情况①只含一种元素的物质不一定是纯净物,也可能是混合物,如O 和O,金刚石和石墨,红磷和白磷。
2 3
判断下列溶液中,离子一定能大量共存打“√”,否则的打“×”
(1)使酚酞溶液变红的溶液:Na+、Cl-、SO、Fe3+
(2)使紫色石蕊溶液变红的溶液:Fe2+、Mg2+、NO、Cl-
(3)常温下,c(H+)=1×10-13 mol·L-1的溶液中:NH、Al3+、SO、NO
(4)碳酸氢钠溶液:K+、SO、Cl-、H+
(5)含大量Fe3+的溶液中:NH、Na+、Cl-、SCN-
(6) (2022·镇江期中)向某溶液X中滴加少量稀盐酸,再滴加几滴Ba(NO ) 溶液,出现白色沉淀,该溶液中含
3 2
有SO
(7) (2019·江苏卷)0.1 mol/L FeCl 溶液中:K+、Mg2+、SO、MnO能大量共存
2
(8) (2018·江苏卷)0.1 mol/L HCl 溶液中:Ba2+、K+、CHCOO-、NO能大量共存
3
(9) (2017·江苏卷)无色透明的溶液中:Fe3+、Mg2+、SCN-、Cl-能大量共存
考向 考查离子共存
【例1】下列离子可以在指定溶液中大量共存的是( )
A.常温下,=1010的溶液:Mg2+、NH、HCO、NO
B.电解饱和食盐水一段时间后的溶液:K+、Na+、CO、SO
C.硫酸酸化的高锰酸钾溶液:Ba2+、NH、I-、Cl-
D.生锈铁钉溶于盐酸后形成的溶液:H+、Ca2+、SCN-、Br-
考法02 离子检验和推断
1、常见离子的检验
离子 试剂 实验操作 现象和结论
用洁净的铂丝蘸取少量待测液,置于 火焰呈黄色,说明溶液中含有
Na+ ——
酒精灯火焰上灼烧,观察火焰颜色 Na+
用洁净的铂丝蘸取待测液,置于酒精
火焰呈紫色,说明溶液中含有
K+ —— 灯火焰上灼烧,透过蓝色钴玻璃观察
K+
火焰颜色
取少量待测液于试管中,加入 NaOH
红色石蕊试纸变蓝,说明该溶
NH NaOH溶液 溶液并加热,把湿润的红色石蕊试纸
液中含有NH
放在试管口
溶液变红,说明原溶液中含有
KSCN溶液 向待测液中滴加KSCN溶液
Fe3+ Fe3+
NaOH溶液 向待测液中滴加NaOH溶液
有红褐色沉淀生成,说明原溶液中含有Fe3+
稀盐酸、 BaC l 溶 先向待测液中加入稀盐酸酸化,无明 有白色沉淀生成,说明原溶液
2
SO
液 显现象,再滴加BaCl 溶液 中含有SO
2
AgNO 溶液、稀硝 先向待测液中加入稀硝酸酸化,再滴 有白色沉淀生成,说明原溶液
3
Cl-
酸 加AgNO 溶液 中含有Cl-
3
2、离子检验中常见干扰离子的排除
待检离子 干扰离子 排除措施
SO 加入过量的Ba(NO ) 溶液
3 2
Cl- CO
加入稀硝酸酸化
OH-
CO
SO SO 加入稀盐酸酸化
Ag+
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)(2022·镇江期中)向某溶液X中滴加少量稀盐酸,再滴加几滴Ba(NO ) 溶液,出现白色沉淀,该溶液
3 2
中含有SO( )
(2)向某溶液中加入BaCl 溶液,有白色沉淀生成,再加入稀盐酸,沉淀不消失,则溶液中一定存在SO(
2
)
(3)向某溶液中加入Ba(NO ) 溶液,产生不溶于稀HNO 的白色沉淀,则溶液中一定存在SO( )
3 2 3
(4)向某溶液中加入Ca(OH) 溶液,有白色沉淀生成,则溶液中一定存在CO( )
2
(5)某溶液的焰色试验呈黄色,则溶液中一定有钠元素,不能确定是否有钾元素( )
(6)无色溶液加入CCl 无现象,滴加氯水后CCl 层呈紫红色,则溶液中一定存在I-( )
4 4
(7)向某溶液中加入稀盐酸,产生能使澄清石灰水变浑浊的气体,溶液中一定存在CO( )
【例1】 (2023·江苏各地模拟重组)室温下进行下列实验,根据实验操作和现象所得到的结论正确的是( )
选项 实验操作和现象 结论
点燃酒精灯,将铂丝在酒精灯上灼烧至火焰无特殊颜
A 不能确定待测液中无K+
色,蘸取待测液灼烧,未观察到紫色火焰
B 向某溶液中加入Ba(OH) 溶液,振荡,产生白色沉淀 该溶液中含有SO
2
向某溶液中滴加几滴新制氯水,振荡,再加入少量KSCN
C 该溶液中一定含有Fe2+
溶液,溶液变为红色
向某溶液中滴加NaOH溶液并将湿润的红色石蕊试纸置
D 原溶液中无NH
于试管口,试纸颜色无明显变化
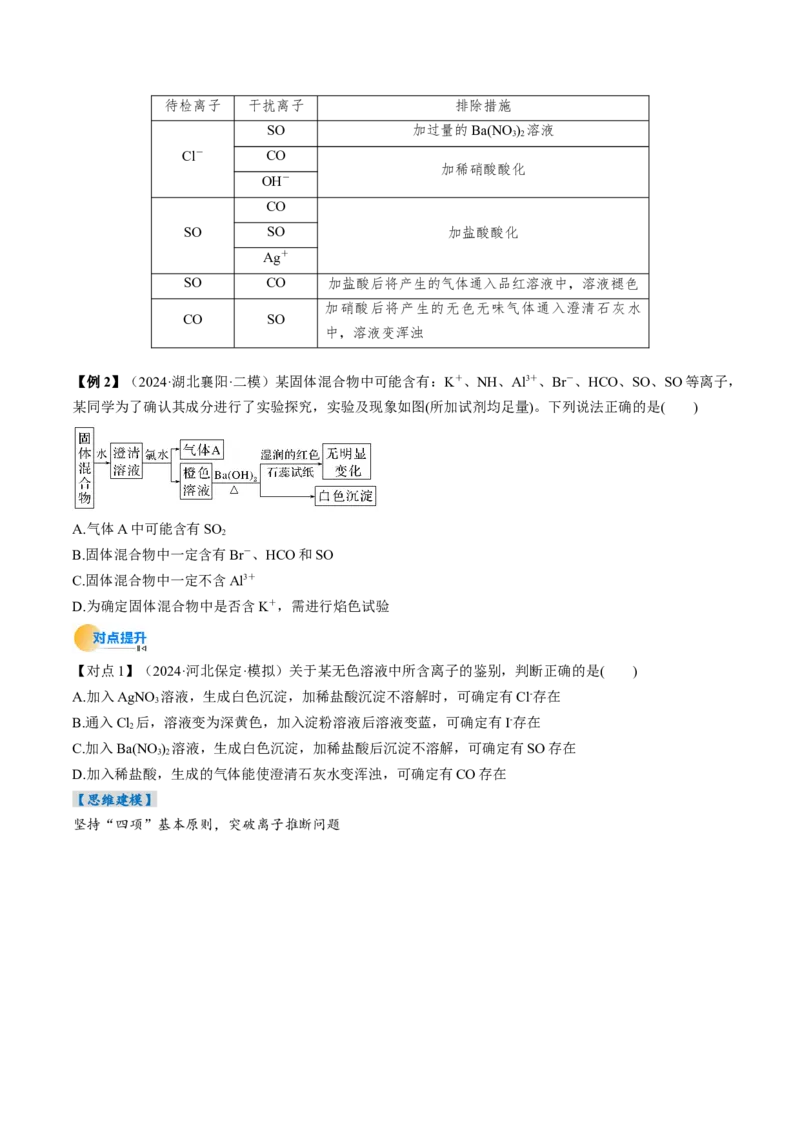
【名师点睛】
离子检验中的常见干扰离子以及排除措施待检离子 干扰离子 排除措施
SO 加过量的Ba(NO ) 溶液
3 2
Cl- CO
加稀硝酸酸化
OH-
CO
SO SO 加盐酸酸化
Ag+
SO CO 加盐酸后将产生的气体通入品红溶液中,溶液褪色
加硝酸后将产生的无色无味气体通入澄清石灰水
CO SO
中,溶液变浑浊
【例2】(2024·湖北襄阳·二模)某固体混合物中可能含有:K+、NH、Al3+、Br-、HCO、SO、SO等离子,
某同学为了确认其成分进行了实验探究,实验及现象如图(所加试剂均足量)。下列说法正确的是( )
A.气体A中可能含有SO
2
B.固体混合物中一定含有Br-、HCO和SO
C.固体混合物中一定不含Al3+
D.为确定固体混合物中是否含K+,需进行焰色试验
【对点1】(2024·河北保定·模拟)关于某无色溶液中所含离子的鉴别,判断正确的是( )
A.加入AgNO 溶液,生成白色沉淀,加稀盐酸沉淀不溶解时,可确定有Cl-存在
3
B.通入Cl 后,溶液变为深黄色,加入淀粉溶液后溶液变蓝,可确定有I-存在
2
C.加入Ba(NO ) 溶液,生成白色沉淀,加稀盐酸后沉淀不溶解,可确定有SO存在
3 2
D.加入稀盐酸,生成的气体能使澄清石灰水变浑浊,可确定有CO存在
【思维建模】
坚持“四项”基本原则,突破离子推断问题题型一 离子共存问题
1.在给定条件下,下列离子组能否大量共存的判断及对应的离子方程式书写不正确的是( )
选项 条件 离子组 离子共存判断及离子方程式
不能大量共存:Al3++3OH-
A 无色透明的溶液 K+、SO、Al3+、OH-
===Al(OH) ↓
3
能大量共存,通CO 时发生的反
2
B 通入少量CO Na+、OH-、K+、NO
2
应为2OH-+CO===CO+HO
2 2
滴加石蕊溶液变
C Fe2+、Na+、Cl-、NO 能大量共存
红的溶液
D 溶液呈蓝色 K+、Na+、Cl-、SO 能大量共存
2.下列各组离子能大量共存的是( )
A.Fe3+、Na+、SCN-、SO
B.K+、Na+、ClO-、I-
C.Al3+、Ca2+、HCO、NO
D.NH、Cu2+、CHCOO-、NO
3
3. (2022·响水中学)常温下,下列各组离子在指定溶液中能大量共存的是
A. 0.1 mol/L 氨水溶液:Na+、K+、OH-、NO
B. 0.1 mol/L 盐酸溶液:Na+、K+、SO、SiO
C. 0.1 mol/L KMnO 溶液:NH、Na+、NO、I-
4
D. 0.1 mol/L AgNO 溶液:NH、Mg2+、Cl-、SO
3题型二 离子检验和推断
3.(2022·陕西安康中学高三检测)通过实验得出的结论正确的是( )
A.将某固体试样完全溶于盐酸,再滴加Ba(NO ) 溶液,出现白色沉淀,则该固体试样中存在SO
3 2
B.将某固体试样完全溶于盐酸,再滴加KSCN溶液,没有出现红色,则该固体试样中不存在Fe3+
C.在某固体试样加水后的溶液中,滴加NaOH溶液,没有产生使湿润红色石蕊试纸变蓝的气体,该固体
试样中仍可能存在NH
D.在某固体试样加水后的上层清液中,滴加盐酸出现白色沉淀,再加 NaOH溶液沉淀溶解,则该固体试
样中存在SiO
4. 下列检验方法或指定反应的离子(或化学)方程式正确的是( )
A. 向NaAlO 溶液中滴入Ca(HCO ) 溶液:
2 3 2
AlO+HCO+HO===Al(OH) ↓+CO
2 3
B. 用溴水检验CH===CHCHO中的碳碳双键:
2
CH===CHCHO+Br ―→CHBr—CHBr—CHO
2 2 2
C. 用NaS溶液吸收少量SO [K (H SO )>K (H S)]:
2 2 a2 2 3 a1 2
S2-+SO +HO===SO+HS↑
2 2 2
D. 向HPO (二元弱酸)溶液中滴加过量烧碱溶液:
3 3
HPO +2OH-===HPO+2HO
3 3 2
5.(2021·湖南,12)对下列粒子组在溶液中能否大量共存的判断和分析均正确的是( )
粒子组 判断和分析
不能大量共存,因发生反应:Al3++
A Na+、Al3+、Cl-、NH ·H O
3 2
4NH ·H O===[Al(OH) ]-+4NH
3 2 4
不能大量共存,因发生反应:2H++
B H+、K+、SO、SO
2
SO===S↓+SO ↑+HO
2 2 2
C Na+、Fe3+、SO、HO 能大量共存,粒子间不反应
2 2
D H+、Na+、Cl-、MnO 能大量共存,粒子间不反应
6.(2022·广东,4)实验室进行粗盐提纯时,需除去Ca2+、Mg2+和SO,所用试剂包括BaCl 以及( )
2
A.NaCO、NaOH、HCl
2 3
B.NaCO、HCl、KOH
2 3
C.KCO、HNO、NaOH
2 3 3
D.NaCO、NaOH、HNO
2 3 3
7.(2021·湖南,12)对下列粒子组在溶液中能否大量共存的判断和分析均正确的是( )
粒子组 判断和分析
A Na+、Al3+、Cl-、NH ·H O 不能大量共存,因发生反应:Al3++
3 24NH ·H O===[Al(OH) ]-+4NH
3 2 4
不能大量共存,因发生反应:2H++
B H+、K+、SO、SO
2
SO===S↓+SO ↑+HO
2 2 2
C Na+、Fe3+、SO、HO 能大量共存,粒子间不反应
2 2
D H+、Na+、Cl-、MnO 能大量共存,粒子间不反应
8. (2023·宿迁实验中学)常温下,下列各组离子在指定溶液中能大量共存的是( )
A. 0.1 mol/L 氨水溶液:Na+、K+、OH-、NO
B. 0.1 mol/L 盐酸溶液:Na+、K+、SO、SiO
C. 0.1 mol/L KMnO 溶液:NH、Na+、NO、I-
4
D. 0.1 mol/L AgNO 溶液:NH、Mg2+、Cl-、SO
3
9. (2023·如皋期初)下列离子在指定条件下能大量共存的是( )
A. 加入过量FeSO 后的溶液中:Cu2+、Mg2+、Br-、SO
4
B. 加入过量明矾[KAl(SO)·12H O]后的溶液中:Ba2+、NH、Cl-、NO
4 2 2
C. 加入过量NaClO后的溶液中:Na+、Fe2+、CHCOO-、Cl-
3
D. 加入过量HI的溶液中:K+、Fe3+、Cl-、SO
10. (2022·泰州中学)一种利用废旧镀锌铁皮制备磁性Fe O 纳米粒子的工艺流程如图。
3 4
下列有关说法不正确的是( )
A. “碱洗”是为了去除废旧镀锌铁皮表面的油污
B. “氧化”时发生反应的离子方程式为2Fe2++ClO-+2H+===2Fe3++Cl-+HO
2
C. “氧化”后的溶液中金属阳离子主要有Fe2+、Fe3+、Na+
D. 用激光笔照射“加热沉铁”后所得分散系,产生丁达尔效应
D. 加入过量HI的溶液中:K+、Fe3+、Cl-、SO
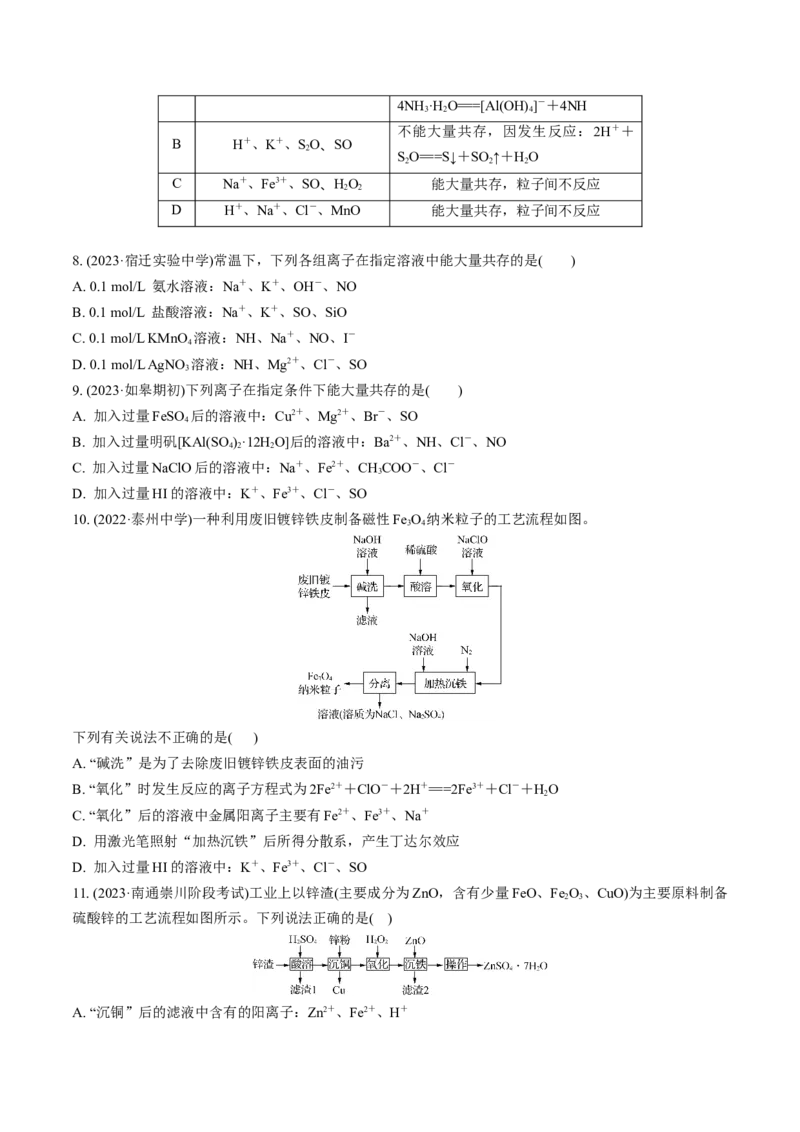
11. (2023·南通崇川阶段考试)工业上以锌渣(主要成分为ZnO,含有少量FeO、Fe O 、CuO)为主要原料制备
2 3
硫酸锌的工艺流程如图所示。下列说法正确的是( )
A. “沉铜”后的滤液中含有的阳离子:Zn2+、Fe2+、H+B. “氧化”时的离子方程式为2HO+2Fe2+===2Fe3++2HO+O↑
2 2 2 2
C. “滤渣2”的主要成分为Fe O
2 3
D. “操作”为蒸发结晶
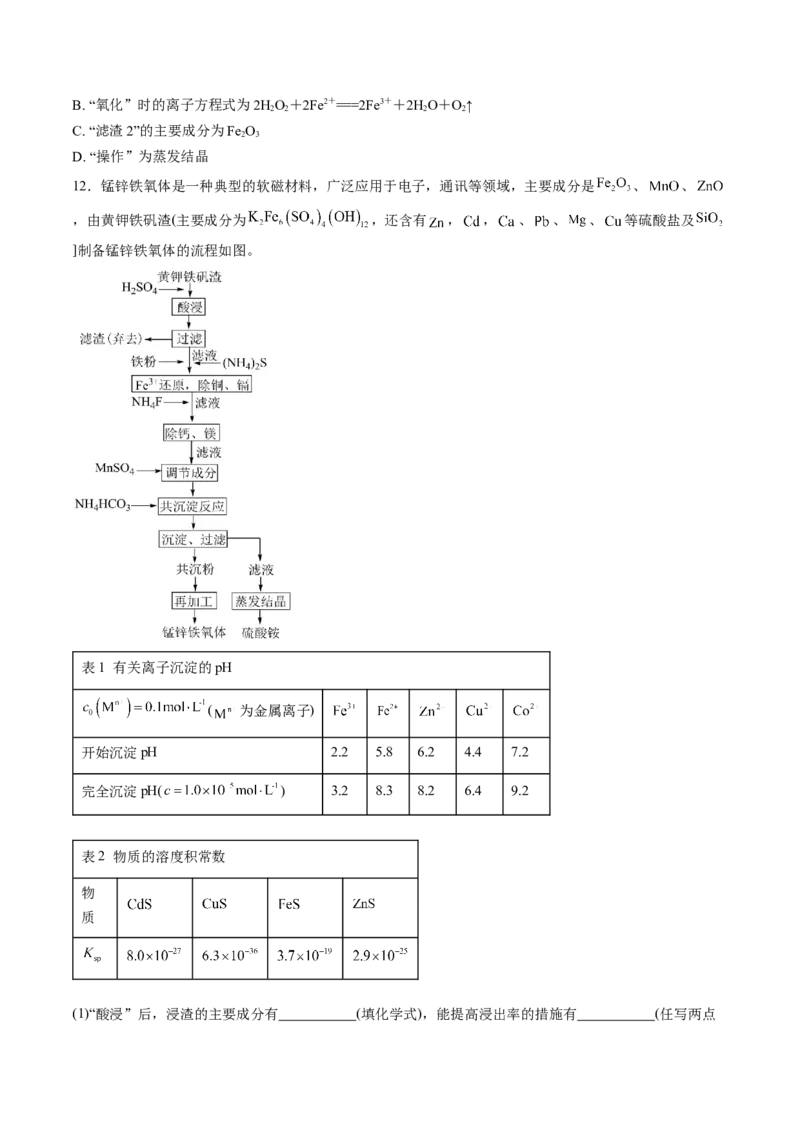
12.锰锌铁氧体是一种典型的软磁材料,广泛应用于电子,通讯等领域,主要成分是 、 、
,由黄钾铁矾渣(主要成分为 ,还含有 , , 、 、 、 等硫酸盐及
]制备锰锌铁氧体的流程如图。
表1 有关离子沉淀的pH
( 为金属离子)
开始沉淀pH 2.2 5.8 6.2 4.4 7.2
完全沉淀pH( ) 3.2 8.3 8.2 6.4 9.2
表2 物质的溶度积常数
物
质
(1)“酸浸”后,浸渣的主要成分有 (填化学式),能提高浸出率的措施有 (任写两点即可)。
(2)加入铁粉时,反应温度对 浓度的影响如图,反应的最佳温度为 。
(3)“除钙、镁”中,溶液的pH不宜太小或太大,生产中pH保持在5左右的原因是 。
(4)“除铜、镉”中,最先沉淀的离子是 (填离子符号),若要将溶液中的铜和镉完全沉淀,溶液
中的 不低于 mol/L。
(5)若锰锌铁氧体中金属元素理论质量配比为 ,若调节成分前溶液
中 , ,则应加入的 质量为 g。
(6)若以 代表溶液成分,则“共沉反应”中,发生反应的离子方程式为 。
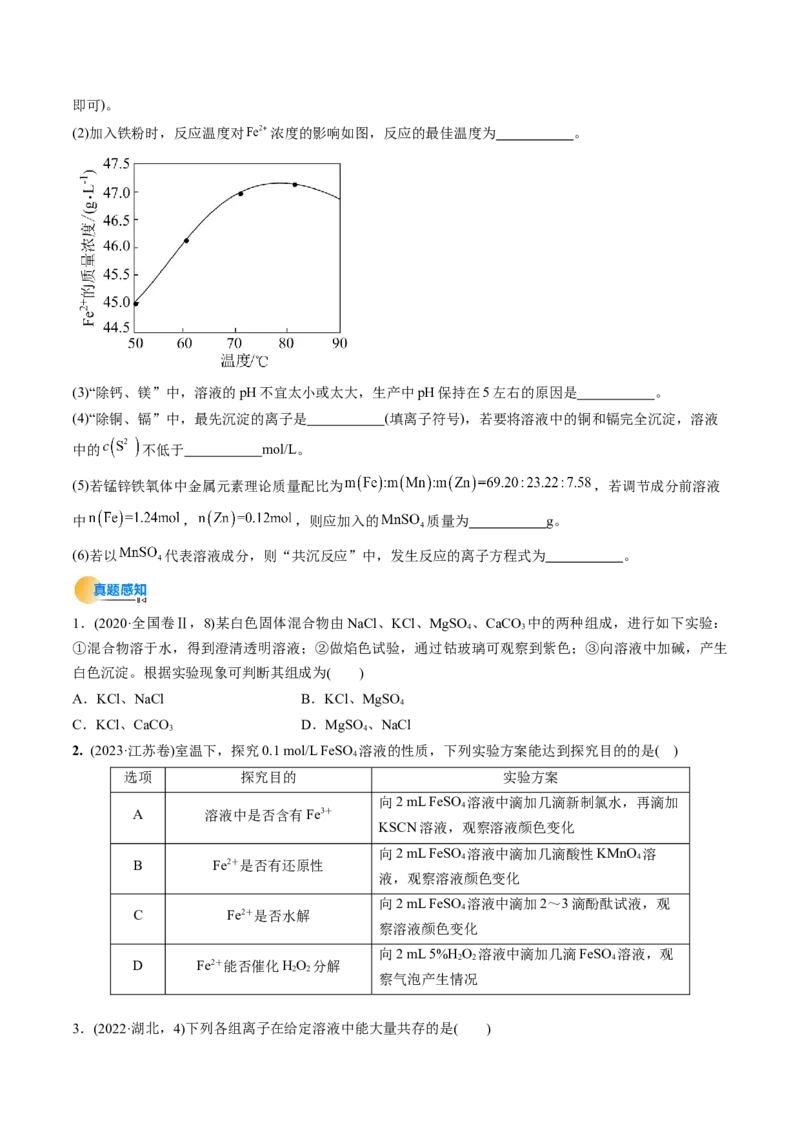
1.(2020·全国卷Ⅱ,8)某白色固体混合物由NaCl、KCl、MgSO 、CaCO 中的两种组成,进行如下实验:
4 3
①混合物溶于水,得到澄清透明溶液;②做焰色试验,通过钴玻璃可观察到紫色;③向溶液中加碱,产生
白色沉淀。根据实验现象可判断其组成为( )
A.KCl、NaCl B.KCl、MgSO
4
C.KCl、CaCO D.MgSO 、NaCl
3 4
2. (2023·江苏卷)室温下,探究0.1 mol/L FeSO 溶液的性质,下列实验方案能达到探究目的的是( )
4
选项 探究目的 实验方案
向2 mL FeSO 溶液中滴加几滴新制氯水,再滴加
4
A 溶液中是否含有Fe3+
KSCN溶液,观察溶液颜色变化
向2 mL FeSO 溶液中滴加几滴酸性KMnO 溶
4 4
B Fe2+是否有还原性
液,观察溶液颜色变化
向2 mL FeSO 溶液中滴加2~3滴酚酞试液,观
4
C Fe2+是否水解
察溶液颜色变化
向2 mL 5%H O 溶液中滴加几滴FeSO 溶液,观
2 2 4
D Fe2+能否催化HO 分解
2 2
察气泡产生情况
3.(2022·湖北,4)下列各组离子在给定溶液中能大量共存的是( )A.在0.1 mol·L-1氨水中:Ag+、Cu2+、NO、SO
B.在0.1 mol·L-1氯化钠溶液中:Fe3+、I-、Ba2+、HCO
C.在0.1 mol·L-1醋酸溶液中:SO、NH、Br-、H+
D.在0.1 mol·L-1硝酸银溶液中:K+、Cl-、Na+、CO
4. (2020·江苏卷)常温下,下列各组离子在指定溶液中能大量共存的是( )
A.0.1 mol/L氨水:Na+、K+、OH-、NO
B.0.1 mol/L盐酸:Na+、K+、SO、SiO
C.0.1 mol/L KMnO 溶液:NH、Na+、NO、I-
4
D.0.1 mol/L AgNO 溶液:NH、Mg2+、Cl-、SO
3
5. (2019·江苏卷)室温下,下列各组离子在指定溶液中能大量共存的是( )
A.0.1 mol/L NaOH溶液:Na+、K+、CO、AlO
B.0.1 mol/L FeCl 溶液:K+、Mg2+、SO、MnO
2
C.0.1 mol/L K CO 溶液:Na+、Ba2+、Cl-、OH-
2 3
D.0.1 mol/L H SO 溶液:K+、NH、NO、HSO
2 4
6. (2018·江苏卷)室温下,下列各组离子在指定溶液中能大量共存的是( )
A.0.1 mol/L KI溶液:Na+、K+、ClO-、OH-
B.0.1 mol/L Fe (SO ) 溶液:Cu2+、NH、NO、SO
2 4 3
C.0.1 mol/L HCl溶液:Ba2+、K+、CHCOO-、NO
3
D.0.1 mol/L NaOH溶液:Mg2+、Na+、SO、HCO