文档内容
考点 21 化学反应的热效应
目录
.............................................................................................................................................1
1.高考真题考点分布...................................................................................................................................1
2.命题规律及备考策略...............................................................................................................................1
.............................................................................................................................................2
考法01 反应热 焓变...............................................................................................................................2
考法02 燃烧热和中和热 能源...............................................................................................................8
考法03 盖斯定律及应用.........................................................................................................................13
...........................................................................................................................................13
1.高考真题考点分布
考点内容 考点分布
能源及其综合利用 2021全国乙卷卷1题,6分;2022广东卷3题,2分;
反应热的计算 2022浙江6月选考18题,2分;2021浙江1月选考20题,2分;
盖斯定律运用 2022浙江1月选考18题,2分;2021浙江6月选考21题,2分;2021北京卷14
题,3分;
2024·甘肃卷10题,3分;2024·广东卷15题,3分;2024·安徽卷10题,3分;
化学反应历程与反 2024·河北卷14题,3分;2024·北京卷13题,3分;2023浙江1月选考14题,3
应机理图像分析 分;2021浙江1月选考24题,2分;2021广东卷14题,4分;2021湖北卷12
题,3分;
能源及其综合利用 2021全国乙卷卷1题,6分;2022广东卷3题,2分;
2.命题规律及备考策略
【命题规律】
高频考点从近几年全国高考试题来看,吸热反应和放热反应判断、热化学方程式正误判断、盖斯定律、燃
烧热和中和热仍是高考命题的热点。
【备考策略】利用盖斯定律计算反应热的“思维步骤”【命题预测】
预计2025年高考会以新的情境载体考查热化学方程式书写及正误判断、盖斯定律的应用,以图象、图表为
背景考查能量变化等知识,题目难度一般适中。
考法01 反应热 焓变
1.化学反应的实质与特征
(1)实质:反应物中 和生成物中 。
(2)特征:既有 变化,又伴有 变化,通常主要表现为 的变化。
2.反应热和焓变
(1)反应热:在等温条件下,化学反应体系向 或从 的热量,称为化学反应的热效应,简称反
应热。
(2)焓变:在等压条件下进行的化学反应,其反应热等于焓变,其符号为 ,单位是 。
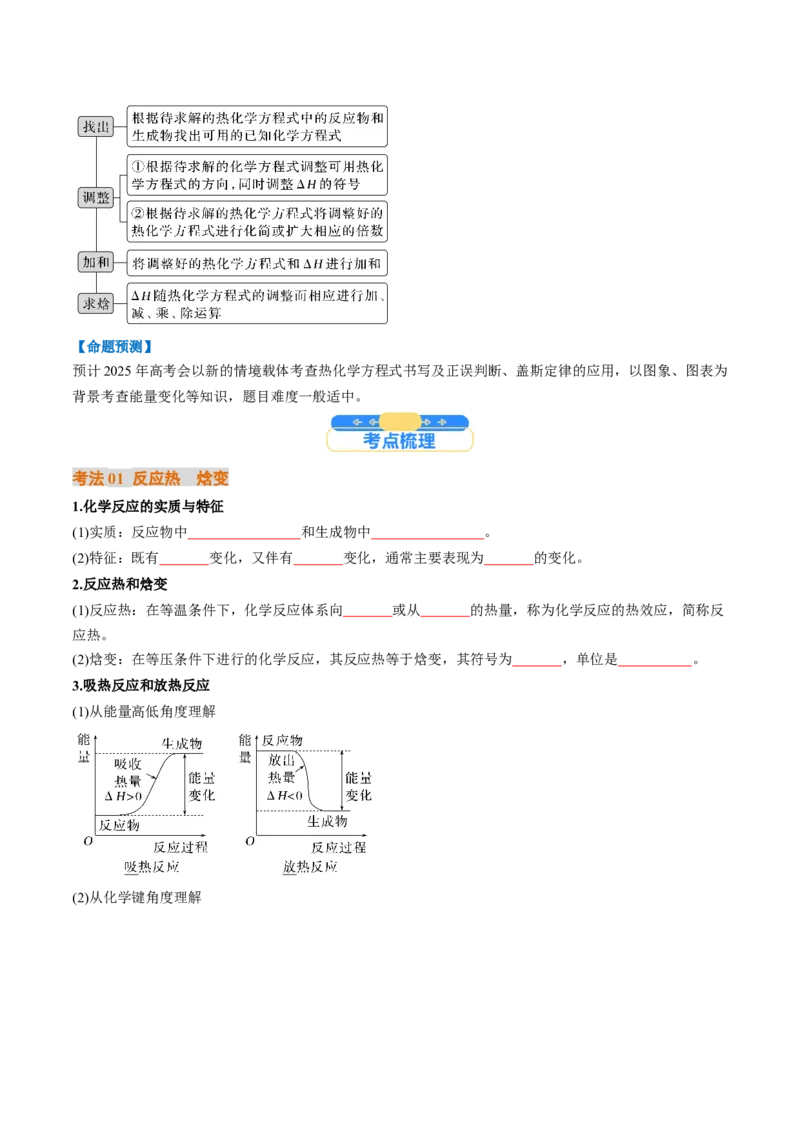
3.吸热反应和放热反应
(1)从能量高低角度理解
(2)从化学键角度理解(3)常见放热反应
①可燃物的燃烧;②酸碱中和反应;③大多数化合反应;④金属跟酸的置换反应;⑤物质的缓慢氧化;⑥
铝热反应。
(4)常见吸热反应
①大多数分解反应;②盐的水解和弱电解质的电离;③Ba(OH) ·8H O 与NH Cl反应;④碳和水蒸气、C
2 2 4
和CO 的反应。
2
4.热化学方程式
(1)概念
表示参与化学反应的物质的 和 的关系的化学方程式。
(2)意义
表明了化学反应中的物质变化和能量变化。例如:2H(g)+O(g)===2H O(l) ΔH=-571.6 kJ·mol-1,表示
2 2 2
25 ℃,101 kPa下, 。
(3)热化学方程式的书写
【易错提醒】
(1)查热化学方程式是否配平。
(2)查各物质的聚集状态是否正确。
(3)查ΔH的“+”“-”符号是否正确。
(4)查反应热的单位是否为kJ·mol-1。
(5)查反应热的数值与化学计量数是否对应。
请判断下列说法的正误(正确的打“√”,错误的打“×”)
1.正误判断(正确打“√”,错误打“×”)。(1)化学变化中的能量变化都是化学能和热能间的相互转化。( )
(2)伴有能量变化的物质变化都是化学变化。( )
(3)需加热才能进行的反应是吸热反应,不需加热就能进行的反应是放热反应。( )
(4)同温同压下,反应H(g)+Cl(g)===2HCl(g)在光照和点燃条件下的ΔH相同。( )
2 2
(5)CO(g)+O(g)===CO (g) ΔH=-Q kJ·mol-1表示标准状况下1 mol CO(g)和 mol O(g)反应生成1 mol
2 2 2
CO(g)时放出Q kJ的热量。( )
2
(6)热化学方程式中的化学计量数与ΔH成正比( )
(7)物质的状态不同ΔH的数值也不同( )
(8)当反应逆向进行时,其反应热与正反应热的反应热数值相等,符号相反( )
(9)2H O(l)===2H (g)+O(g) ΔH>0( )
2 2 2
(10)C(石墨,s)===C(金刚石,s) ΔH>0,说明石墨比金刚石稳定( )
考向01 考查反应过程中物质能量变化图像
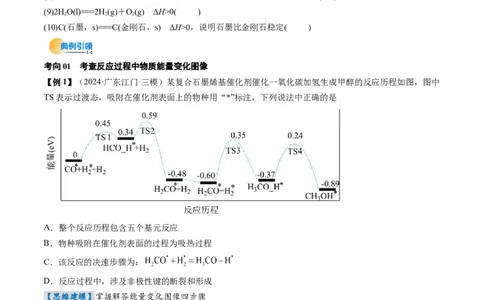
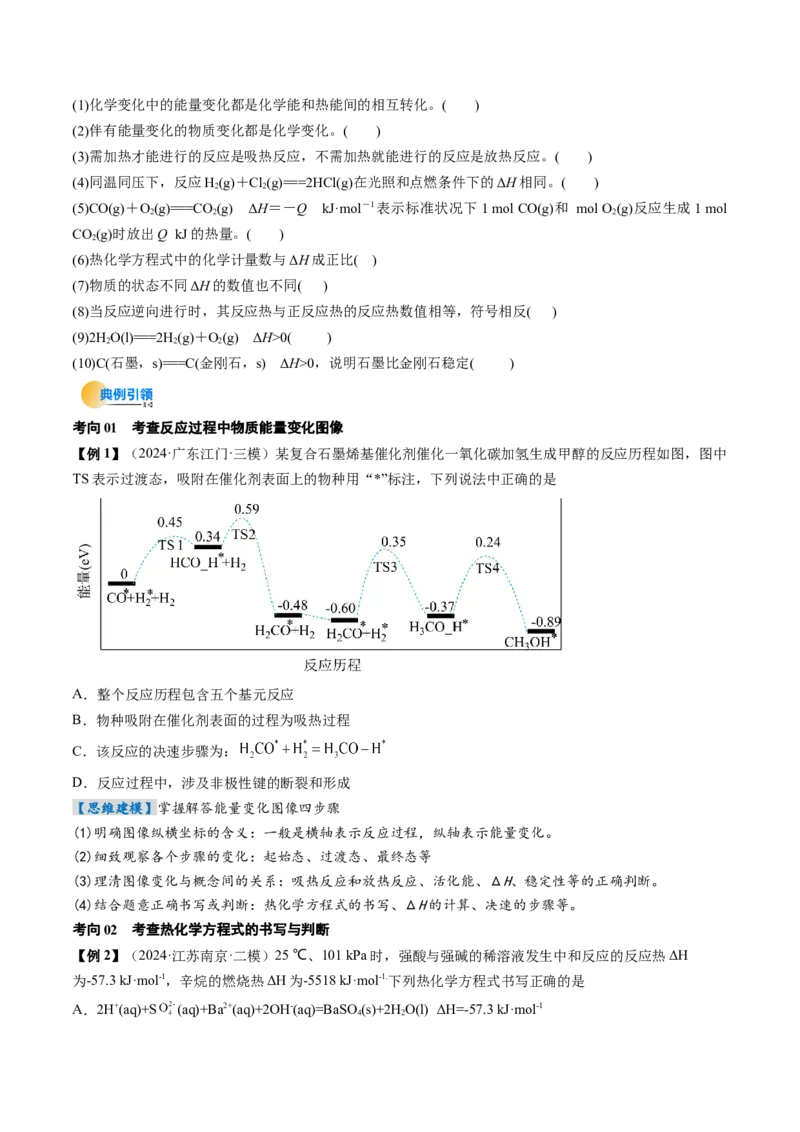
【例1】(2024·广东江门·三模)某复合石墨烯基催化剂催化一氧化碳加氢生成甲醇的反应历程如图,图中
TS表示过渡态,吸附在催化剂表面上的物种用“*”标注,下列说法中正确的是
A.整个反应历程包含五个基元反应
B.物种吸附在催化剂表面的过程为吸热过程
C.该反应的决速步骤为:
D.反应过程中,涉及非极性键的断裂和形成
【思维建模】掌握解答能量变化图像四步骤
(1)明确图像纵横坐标的含义:一般是横轴表示反应过程,纵轴表示能量变化。
(2)细致观察各个步骤的变化:起始态、过渡态、最终态等
(3)理清图像变化与概念间的关系:吸热反应和放热反应、活化能、ΔH、稳定性等的正确判断。
(4)结合题意正确书写或判断:热化学方程式的书写、ΔH的计算、决速的步骤等。
考向02 考查热化学方程式的书写与判断
【例2】(2024·江苏南京·二模)25 ℃、101 kPa时,强酸与强碱的稀溶液发生中和反应的反应热ΔH
为-57.3 kJ·mol-1,辛烷的燃烧热ΔH为-5518 kJ·mol-1.下列热化学方程式书写正确的是
A.2H+(aq)+S (aq)+Ba2+(aq)+2OH-(aq)=BaSO (s)+2HO(l) ΔH=-57.3 kJ·mol-1
4 2B.KOH(aq)+ HSO (aq)= KSO (aq)+H O(l) ΔH=-57.3 kJ·mol-1
2 4 2 4 2
C.C H (l)+ O(g)=8CO (g)+9HO(g) ΔH=-5518 kJ·mol-1
8 18 2 2 2
D.2C H (g)+25O(g)=16CO (g)+18HO(l) ΔH=-5518 kJ·mol-1
8 18 2 2 2
【易错警示】
(1)注明反应的温度和压强(25 ℃、101 kPa下进行的反应可不注明)。
(2)注明反应物和生成物的状态:固态(s)、液态(l)、水溶液(aq)、气态(g)。
(3)热化学方程式中各物质的化学计量数只表示物质的物质的量,而不表示分子个数(或原子个数),因此可
以写成分数。
(4)热化学方程式中不用“↑”和“↓”。
(5)由于ΔH与反应物的物质的量有关,所以热化学方程式中物质的化学计量数必须与 ΔH相对应,如果化
学计量数加倍,则ΔH也要加倍。当反应向逆反应方向进行时,其反应热与正反应的反应热数值相等,符
号相反。
考向03 考查化学反应的焓变与键能的计算
【例2】(2024·山东·模拟预测)硅和碳是重要的非金属元素,有关化学键键能如下表所示:
化学键
键能 356 413 336 226 318 452
下列说法正确的是
A.热稳定性: B.金刚石的熔点低于晶体硅
C.由表可知化学键键能与键长成反比 D.硅烷在种类和数量上都不如烷烃多
【对点1】(2024·黑龙江·三模)无催化剂作用下,以乙二醛和 为原料制取乙醛酸、甲酸、乙二酸的可
能反应历程如图所示,其中 表示过渡态, 表示中间体,下列说法错误的是
A.反应很短一段时间内, 多于B.乙二醛制乙醛酸的最大能垒为
C.选择合适的催化剂可提高乙二酸的选择性
D.乙二醛氧化生成甲酸、乙醛酸或乙二酸均为放热反应
【对点2】(2024高三下·浙江·竞赛)已知A、B两种气体在一定条件下可发生反应:2A+B=C+3D+4E。
现将mg相对分子质量为M的A气体与适量的B气体充入一密闭容器中,恰好完全反应且有少量液滴生
成。在相同温度下测得反应前后容器内的压强为6.06×106Pa和1.01×107Pa,且测得反应共放出热量QkJ。
则该反应的热化学方程式为:
A.2A(g)+B(g)=C(g)+3D(g)+4E(g) △H=- kJ/mol
B.2A(g)+B(g)=C(l)+3D(g)+4E(g) △H=- kJ/mol
C.2A(g)+B(g)=C(g)+3D(g)+4E(l) △H=- kJ/mol
D.2A(g)+B(g)=C(g)+3D(l)+4E(g) △H=- kJ/mol
【对点3】(2024·重庆·模拟预测)下表为某些化学键的键能
化学键
键能(kJ/mol) 154 500 942 a
已知火箭燃料肼(N H)有关化学反应的能量变化为:
2 4
且NH(g)+O(g)=N(g)+2HO(g) ΔH=-534kJ·mol−1,则下列说法正确的是
2 4 2 2 2
A.表中的a=391
B.相同条件下O 比N 稳定
2 2
C.NH(g)+O(g)=N(g)+2HO(l) ΔH>-534kJ·mol−1
2 4 2 2 2
D.图中的ΔH=-2218kJ·mol−1
3
考法02 燃烧热和中和热 能源
1.标准燃烧热
(1)概念:在101 kPa时,1 mol纯物质 生成 时的反应热。标准燃烧热的单位一般用kJ·mol-1表示。
标准燃烧热的限定词有恒压(101 kPa时)、可燃物的物质的量(1 mol)、完全燃烧、稳定的氧化物等,其中的
“完全燃烧”,是指物质中下列元素完全转变成对应的氧化物:C→CO(g),H→H O(l),S→SO (g)等。
2 2 2
(2)表示的意义:例如:C的标准燃烧热为393.5 kJ·mol-1,表示在101 kPa时,1 mol C完全燃烧生成CO 气
2
体时放出393.5 kJ的热量。
(3)书写热化学方程式:标准燃烧热是以1 mol物质 所放出的热量来定义的,因此在书写它的热
化学方程式时,应以燃烧 为标准来配平其余物质的化学计量数。例如:C H (l)+
8 18
O(g)===8CO (g)+9HO(l) ΔH=-5 518 kJ·mol-1,即C H 的标准燃烧热ΔH为-5 518 kJ·mol-1。
2 2 2 8 18
(4)标准燃烧热的计算:可燃物完全燃烧放出的热量的计算方法为Q =n(可燃物)×|ΔH|。式中:Q 为可燃
放 放
物燃烧反应放出的热量;n为可燃物的物质的量;ΔH为可燃物的标准燃烧热。
2.中和热及其测定(以稀盐酸与稀NaOH溶液反应为例)
(1)概念:在稀溶液中, 发生中和反应生成1mol HO时的反应热。
2
(2)注意几个限定词:①稀溶液;②产物是1 mol液态HO;③用热化学方程式可表示为 OH-(aq)+H+
2
(aq)===H O(l) ΔH=-57.3 kJ·mol-1。
2
(3)测定原理
通过量热计测得体系在反应前后的温度变化,再利用有关物质的比热容计算反应热。
(4)实验步骤及装置
实验装置 实验步骤
①测量反应物的温度
②测量反应后体系温度(记录反应后体系的 温度)
③重复步骤①、②两次
④数据处理:取 测量所得温度进行计算,测得的数值取平均值,生成1
mol HO时放出的热量为 kJ
2
大量实验测得:在25 ℃和101 kPa下,强酸的稀溶液与强碱的稀溶液发生中和反应生成1 mol H O时,
2
放出 kJ的热量。
【易错提醒】
①为保证酸完全中和,采取的措施是 。
②因为弱酸或弱碱存在电离平衡,电离过程需要吸热,实验中若使用弱酸或弱碱则测得的反应热数值 。
3.能源
(1)能源分类(2)解决能源问题的措施
①提高能源的 :A.改善开采、运输、加工等各个环节;B.科学控制燃烧反应,使燃料充分燃
烧。
②开发 :开发资源丰富、可以再生、没有污染或污染很小的新能源。
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)煤油是可再生能源。( )
(2)H 燃烧过程中热能转化为化学能。( )
2
(3)化石燃料和植物燃料燃烧时放出的能量均来源于太阳能。( )
(4)开发利用各种新能源,减少对化石燃料的依赖,可以降低空气中PM2.5的含量。( )
(5)根据2H(g)+O(g)===2H O(l) ΔH=-571.6 kJ·mol-1可知,氢气的燃烧热为571.6 kJ·mol-1。( )
2 2 2
(6)已知H+(aq)+OH-(aq)===H O(l) ΔH=-57.3 kJ·mol-1,则HSO 和Ba(OH) 反应的ΔH=2×(-57.3
2 2 4 2
kJ·mol-1)。( )
(7)煤、石油、天然气等燃料的最初来源都可追溯到太阳能( )
(8)化石燃料和植物燃料燃烧时放出的能量均来源于太阳能( )
(9)农村用沼气池产生的沼气作燃料属于生物质能的利用( )
(10)随着科技的发展,氢气将成为主要能源之一( )
考向01 考查燃烧热和中和热(中和反应反应热)的理解
【例1】(2024·河北唐山·一模)21.下列说法正确的是( )
A.葡萄糖的燃烧热是2 800 kJ·mol-1,则C H O(s)+3O(g)===3CO (g)+3HO(l) ΔH=-1 400 kJ·mol-
6 12 6 2 2 2
1
B.在一定条件下将1 mol SO 和0.5 mol O 置于密闭容器中充分反应,放出热量79.2 kJ,则反应的热化学方
2 2
程式为2SO (g)+O(g)2SO (g) ΔH=-158.4 kJ·mol-1
2 2 3
C.已知稀溶液中,H+(aq)+OH-(aq)===H O(l) ΔH=-57.3 kJ·mol-1,则稀氨水与稀盐酸溶液反应生成1
2
mol水时放出57.3 kJ的热量
D.已知HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则稀硫酸与氢氧化钠固体反应生成1 mol水时放
出的热量为57.3 kJ
【思维建模】燃烧热和中和热的比较
燃烧热 中和热
能量变化 放热
相同点
ΔH及其单位 ΔH<0,单位均为kJ·mol-1
反应物的量 1 mol 不一定为1 mol
不同点
生成物的量 不确定 生成水的量为1 mol101 kPa时,1 mol纯物质完全燃烧生成 在稀溶液里,酸与碱发生中和反应
反应热的含义
稳定的氧化物时所放出的热量 生成1 mol水时所放出的热量
燃烧热ΔH=-a kJ· 强酸与强碱反应的中和热ΔH=-
表示方法
mol-1(a>0) 57.3 kJ·mol-1
考向02 考查中和反应反应热的测定
【例2】(2024·山东威海·期中)某同学设计如图所示实验,探究反应中的能量变化。下列判断正确的是
A.实验(a)、(b)、(c)所涉及的反应都是放热反应
B.将实验(a)中的铝片更换为等质量的铝粉后释放出的热量有所增加
C.实验(c)中将玻璃搅拌器改为铁质搅拌棒对实验结果没有影响
D.实验(c)中若用NaOH固体测定,则测定数值偏高
【对点1】(2024·河南安阳·期末)已知:298K时,相关物质的相对能量如图所示。下列说法错误的是。
A.CO燃烧的热化学方程式为2CO(g)+O(g) 2CO(g) H=-566kJmol-1
2 2
B.H 的燃烧热为 H=-242kJmol-1 ∆ ∙
2
C.C H 比C H 稳定
2 6 2 4 ∆ ∙
D.CO(g)+HO(g) CO(g)+H(g)是放热反应
2 2 2
【对点2】中和热测定实验中,用50mL0.50mol/L盐酸和50mL0.55mol/LNaOH进行实验,下列说法错误的是( )
A.改用60mL0.50mol/L盐酸跟50mL0.55mol/LNaOH溶液反应,求得中和热数值和原来相同
B.测了酸后的温度计应用水清洗再去测碱的温度,否则中和热数值偏小
C.酸碱混合时,量筒中NaOH溶液应慢慢倒入小烧杯中以免溶液溅出,再用环形玻璃搅拌棒搅拌
D.装置中的大小烧杯之间填满碎泡沫塑料的作用是保温隔热、减少热量损失
考法03 盖斯定律及应用
1.盖斯定律
(1)内容:对于一个化学反应,无论是一步完成还是分几步完成,其反应热是 的。即:化学反应的反应
热只与反应体系的 和 有关,而与反应的 无关。
(2)意义:间接计算某些反应的反应热。
2.反应热的计算
(1)利用 进行有关计算
根据已知的热化学方程式和已知的反应物或生成物的物质的量或反应吸收或放出的热量,可以把反应热当
作“产物”,计算反应放出或吸收的热量。
(2)根据 数据,计算反应放出的热量
计算公式:Q=×n(可燃物的物质的量)
(3)根据旧键 和 形成过程中的能量差计算焓变
若反应物旧化学键断裂吸收能量E,生成物新化学键形成放出能量E,则反应的ΔH=E-E。
1 2 1 2
(4)利用盖斯定律计算反应热
热化学方程式 焓变之间的关系
aA===B ΔH
1
ΔH=
1
A=== B ΔH
2
aA===B ΔH
1
ΔH=
1
B===aA ΔH
2
ΔH=
3.反应热大小的比较
(1)根据 关系比较反应焓变的大小
①H(g)+O(g)===H O(g) ΔH
2 2 2 1
②2H (g)+O(g)===2H O(g) ΔH
2 2 2 2
反应②中H 的量更多,因此放热更多,故ΔH ΔH。
2 1 2(2)根据 比较反应焓变的大小
③C(s)+O(g)===CO(g) ΔH
2 3
④C(s)+O(g)===CO (g) ΔH
2 2 4
反应④中,C完全燃烧,放热更多,故ΔH ΔH。
3 4
(3)根据 比较反应焓变的大小
⑤S(g)+O(g)===SO(g) ΔH
2 2 5
⑥S(s)+O(g)===SO(g) ΔH
2 2 6
由⑤-⑥可得S(g)===S(s) ΔH=ΔH-ΔH 0,故ΔH ΔH。
5 6 5 6
(4)根据 比较反应焓变的大小
⑦2Al(s)+O(g)===AlO(s) ΔH
2 2 3 7
⑧2Fe(s)+O(g)===Fe O(s) ΔH
2 2 3 8
由⑦-⑧可得2Al(s)+Fe O(s)===2Fe(s)+Al O(s) ΔH
2 3 2 3
已知铝热反应为 ,ΔH=ΔH-ΔH 0,故ΔH ΔH。
7 8 7 8
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)可以直接测量任意一反应的反应热( )
(2)盖斯定律遵守能量守恒定律( )
(3)利用盖斯定律可间接计算通过实验难测定的反应的反应热( )
(4)利用盖斯定律可以计算有副反应发生的反应的反应热( )
(5)不管化学反应是一步完成或分几步完成,其反应热是相同的( )
(6)化学反应的反应热只与反应体系的始态和终态有关,而与反应途径无关( )
(7)可以用已经精确测定的反应热效应来计算难于测量或不能测量的反应的热效应( )
考向01 考查盖斯定律
【例1】(2024·北京东城·一模)碱金属单质M和 反应的能量变化如下图所示。下列说法正确的是
A.CsCl晶体是共价晶体
B.C.若M分别为Na和K,则 :NaE(物质R,l)>E(物质R,s)。
(3)同一化学反应,反应物的用量越多,|ΔH|越大。对于可逆反应,因反应不能进行完全,实际反应过程
中放出或吸收的热量要小于理论数值。
(4)等量的可燃物完全燃烧所放出的热量比不完全燃烧所放出的热量多,则完全燃烧的ΔH较小。
【对点1】(2024·辽宁大连·期中)已知ROH(R=Na、K)固体溶于水放热,有关过程能量变化如图
A.反应①:ΔH<0,ΔS<0
1
B.ΔH(NaOH<ΔH(KOH)
4 4
C.ΔH>ΔH
3 2
D.ΔH=ΔH +ΔH +ΔH +ΔH
4 1 2 5 6
【对点2】(2024·北京海淀·模拟)下列各组热化学方程式中,Q<Q 的是
1 2
A.CH(g)+2O(g)=CO (g)+2HO(g) ΔH=-Q kJ·mol-1
4 2 2 2 1
CH(g)+ O(g)=CO(g)+2HO(g) ΔH=-Q kJ·mol-1
4 2 2 2B.S(g)+O(g)=SO(g) ΔH=-Q kJ·mol-1
2 2 1
S(s)+O(g)=SO(g) ΔH=-Q kJ·mol-1
2 2 2
C.H(g)+Br (g)=2HBr(g) ΔH=-Q kJ·mol-1
2 2 1
H(g)+Cl(g)=2HCl(g) ΔH=-Q kJ·mol-1
2 2 2
D.HCl(aq)+NaOH(aq)=NaCl(aq)+HO(l) ΔH=-Q kJ·mol-1
2 1
CHCOOH(aq)+NaOH(aq)=CH COONa(aq)+HO(l) ΔH=-Q kJ·mol-1
3 3 2 2
1.(2024·浙江宁波·期末)已知1mol下列物质分解为气态原子消耗能量与热化学方程式信息如下表:
物质 NO CO N
2
能量/(kJ/mol) 632 1076 946
热化学方程
2NO(g)+2CO(g)=N (g)+2CO (g) ∆H=-742kJ/mol
2 2
式
则CO 的碳氧双键能为
2
A.-1606kJ/mol B.1606kJ/mol C.803kJ/mol D.-803kJ/mol
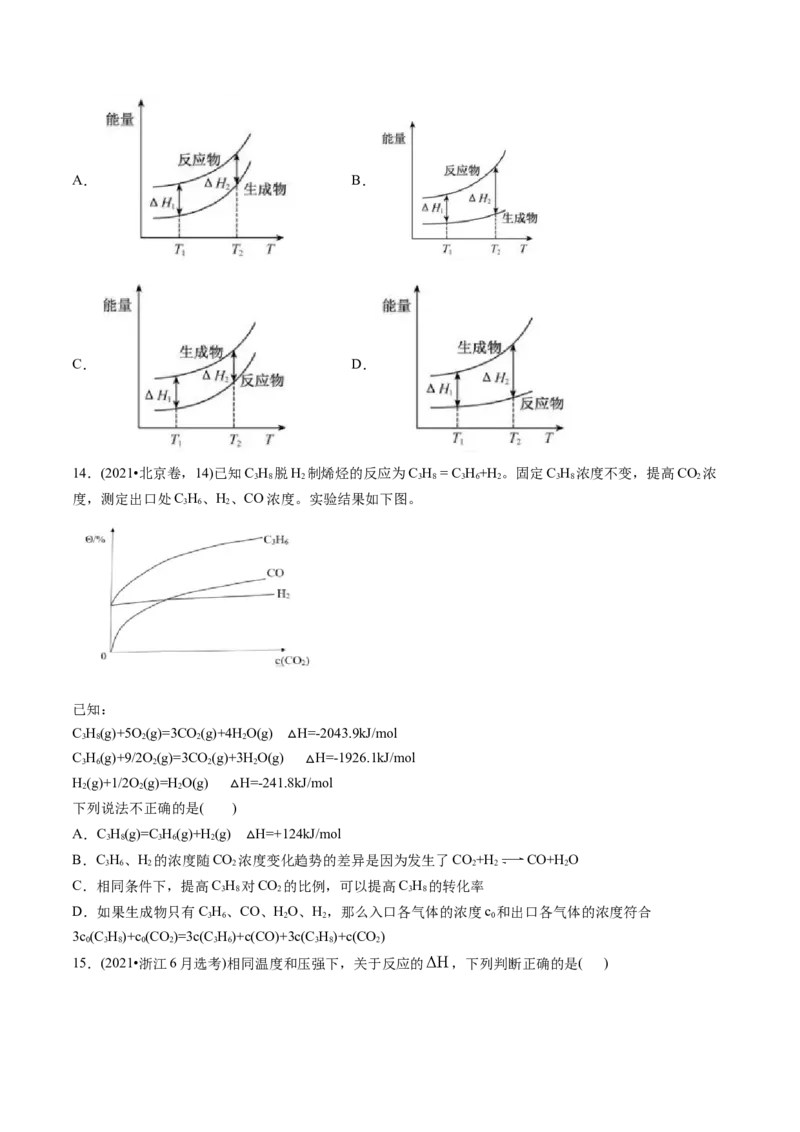
2.(2024·河北保定·期末)相同温度和压强下,关于反应的 ,下列判断正确的是
A. B.
C. D.
3.(2024·湖北·三模)如表所示为部分化学键的键能数据,由键能数据大小,不能解释下列事实的是
化学键
键能 413 348 745 326 318 226 452 347
A.硬度:金刚石 碳化硅
B.熔、沸点:金刚石>CO
2
C.SiH 的稳定性小于CH,更易生成氧化物
4 4
D.硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都远不如烷烃多4.(2024·重庆·三模)甲酸常用于橡胶、医药等工业。在一定条件下可分解生成 和 ,在无、有催
化剂条件下的能量与反应历程的关系如下图所示,下列说法正确的是
A.
B.可以通过 和 计算 的总键能
C.途径二中 参与反应,是该反应过程的中间产物
D.途径二中反应的快慢由生成 的速率决定
5.(2024·山东聊城·二模)苯基甲基乙炔 可用于制备帕瑞昔布钠。一定条件下,苯基甲基乙炔可与
发生催化加成,反应过程如下:
已知: ,下列说法正确的是
A. 中最多4个碳原子共线
B.反应Ⅰ的活化能大于反应Ⅱ
C.产物Ⅱ比产物Ⅰ稳定,两者互为立体异构体
D.其他条件不变,升高温度可增大平衡时产物Ⅱ和产物Ⅰ的浓度比
6.(2024·湖北·模拟预测)苯与Br₂发生取代反应原理为
,其能量与反应进程如下图所示。已知:当碳原子上连有推电子基团时,有利于碳正离子的稳定。
下列说法正确的是
A.第 步涉及非极性键的断裂 B.该反应的决速步骤为第 步
C.反应热 D. 比苯更难发生卤代反应
7.(2024·湖南长沙·一模)苯基甲基乙炔( )可用作医药中间体,制备帕瑞昔布钠。一定条
件下,苯基甲基乙炔可与HCl发生催化加成,反应过程如下:
已知: ,下列说法正确的是
A. 中最多4个碳原子共线
B.
C.产物Ⅱ比产物I稳定,两者互为立体异构体
D.反应I的活化能大于反应Ⅱ
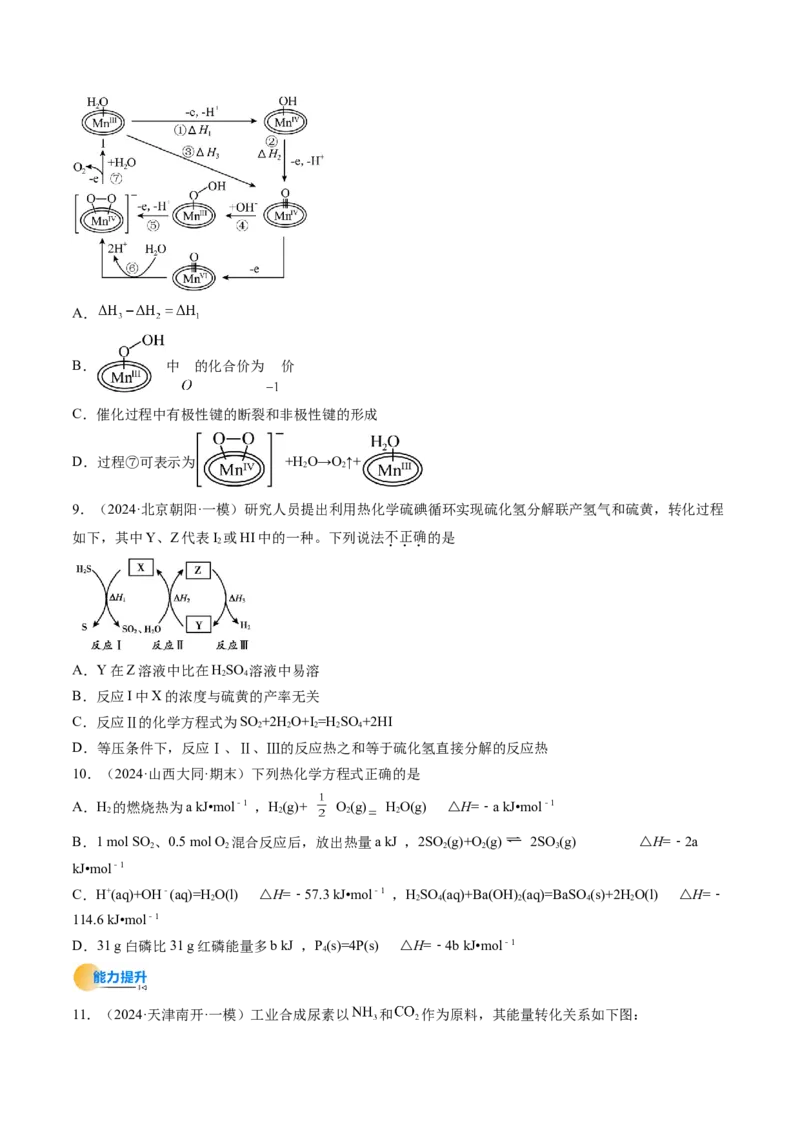
8.(2024·吉林长春·模拟预测)科学家成功捕获并表征到水氧化催化过程中的锰端基氧和锰过氧化物中间
体,明确了水氧化过程中水亲核进攻锰端基氧的氧氧成键机理,如图所示。下列说法错误的是A.
B. 中 的化合价为 价
C.催化过程中有极性键的断裂和非极性键的形成
D.过程⑦可表示为 +H O→O↑+
2 2
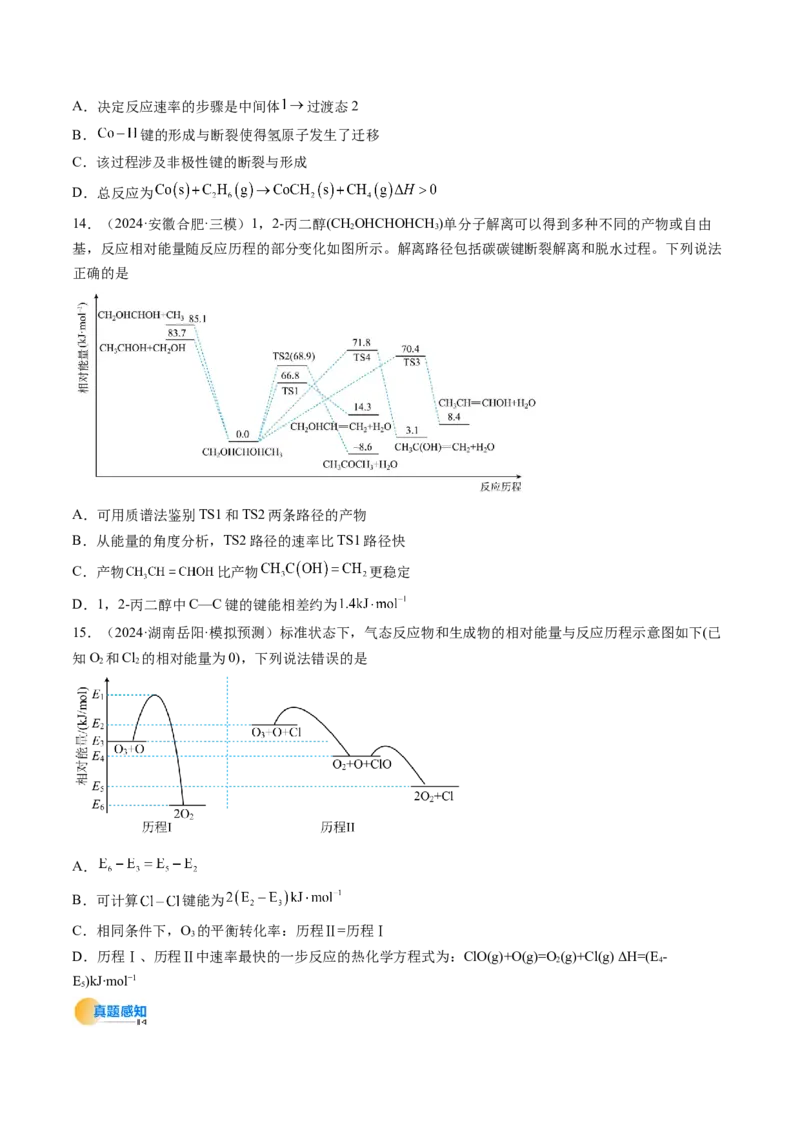
9.(2024·北京朝阳·一模)研究人员提出利用热化学硫碘循环实现硫化氢分解联产氢气和硫黄,转化过程
如下,其中Y、Z代表I 或HI中的一种。下列说法不正确的是
2
A.Y在Z溶液中比在HSO 溶液中易溶
2 4
B.反应I中X的浓度与硫黄的产率无关
C.反应Ⅱ的化学方程式为SO +2H O+I =H SO +2HI
2 2 2 2 4
D.等压条件下,反应Ⅰ、Ⅱ、Ⅲ的反应热之和等于硫化氢直接分解的反应热
10.(2024·山西大同·期末)下列热化学方程式正确的是
A.H 的燃烧热为a kJ•mol﹣1 ,H(g)+ O(g) HO(g) △H=﹣a kJ•mol﹣1
2 2 2 2
B.1 mol SO 、0.5 mol O 混合反应后,放出热量a kJ ,2SO (g)+O(g) 2SO (g) △H=﹣2a
2 2 2 2 3
kJ•mol﹣1
C.H+(aq)+OH﹣(aq)=H O(l) △H=﹣57.3 kJ•mol﹣1 ,HSO (aq)+Ba(OH)(aq)=BaSO (s)+2HO(l) △H=﹣
2 2 4 2 4 2
114.6 kJ•mol﹣1
D.31 g白磷比31 g红磷能量多b kJ ,P(s)=4P(s) △H=﹣4b kJ•mol﹣1
4
11.(2024·天津南开·一模)工业合成尿素以 和 作为原料,其能量转化关系如下图:已知 。下列有关说法正确的是
A.
B.
C.
D.过程③反应速率慢,使用合适的催化剂可减小 而加快反应
12.(2024·湖北武汉·模拟预测)物质的燃烧推动了文明的进步和科技的发展,部分物质的燃烧热数据如
下表:
物质
下列热化学方程式正确的是
A.
B.
C.
D.
13.(2024·北京顺义·二模)我国科研人员研究发现 原子活化乙烷的反应机理,一种机理如图所示。
下列说法不正确的是A.决定反应速率的步骤是中间体 过渡态2
B. 键的形成与断裂使得氢原子发生了迁移
C.该过程涉及非极性键的断裂与形成
D.总反应为
14.(2024·安徽合肥·三模)1,2-丙二醇(CHOHCHOHCH )单分子解离可以得到多种不同的产物或自由
2 3
基,反应相对能量随反应历程的部分变化如图所示。解离路径包括碳碳键断裂解离和脱水过程。下列说法
正确的是
A.可用质谱法鉴别TS1和TS2两条路径的产物
B.从能量的角度分析,TS2路径的速率比TS1路径快
C.产物 比产物 更稳定
D.1,2-丙二醇中C—C键的键能相差约为
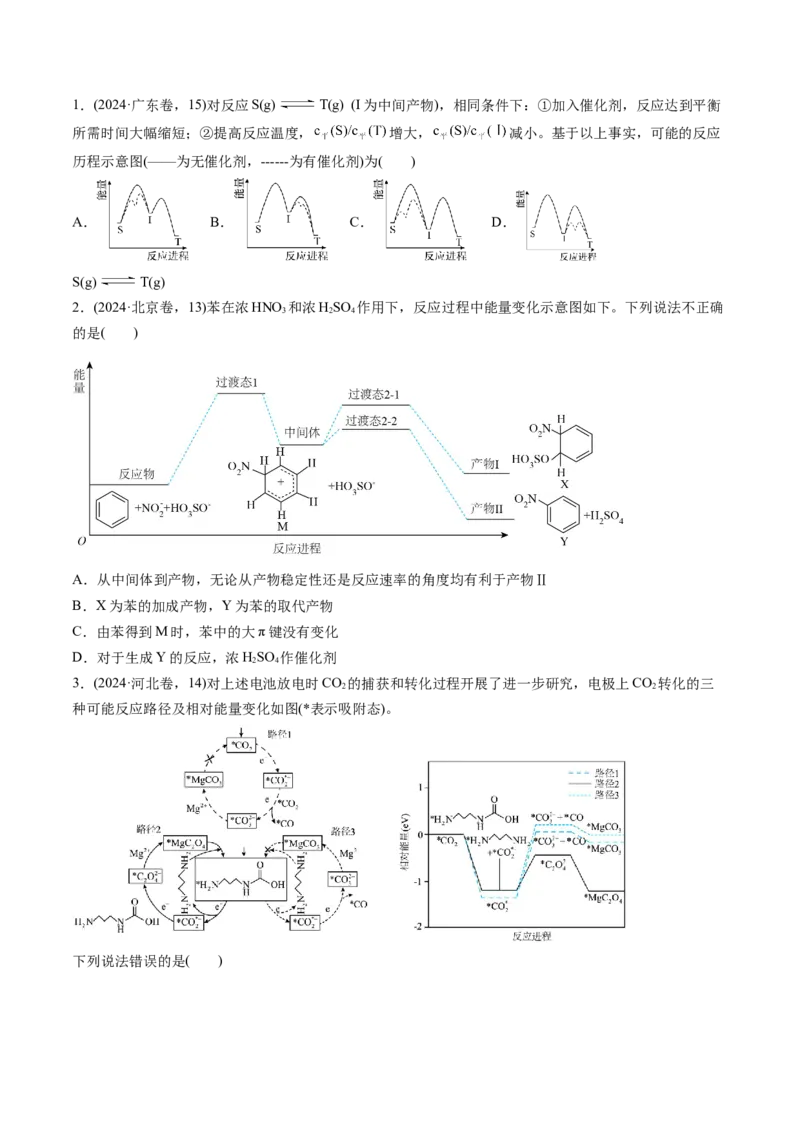
15.(2024·湖南岳阳·模拟预测)标准状态下,气态反应物和生成物的相对能量与反应历程示意图如下(已
知O 和Cl 的相对能量为0),下列说法错误的是
2 2
A.
B.可计算 键能为
C.相同条件下,O 的平衡转化率:历程Ⅱ=历程Ⅰ
3
D.历程Ⅰ、历程Ⅱ中速率最快的一步反应的热化学方程式为:ClO(g)+O(g)=O (g)+Cl(g) ΔH=(E -
2 4
E)kJ∙mol−1
51.(2024·广东卷,15)对反应S(g) T(g) (I为中间产物),相同条件下:①加入催化剂,反应达到平衡
所需时间大幅缩短;②提高反应温度, 增大, 减小。基于以上事实,可能的反应
历程示意图(——为无催化剂,------为有催化剂)为( )
A. B. C. D.
S(g) T(g)
2.(2024·北京卷,13)苯在浓HNO 和浓HSO 作用下,反应过程中能量变化示意图如下。下列说法不正确
3 2 4
的是( )
A.从中间体到产物,无论从产物稳定性还是反应速率的角度均有利于产物Ⅱ
B.X为苯的加成产物,Y为苯的取代产物
C.由苯得到M时,苯中的大π键没有变化
D.对于生成Y的反应,浓HSO 作催化剂
2 4
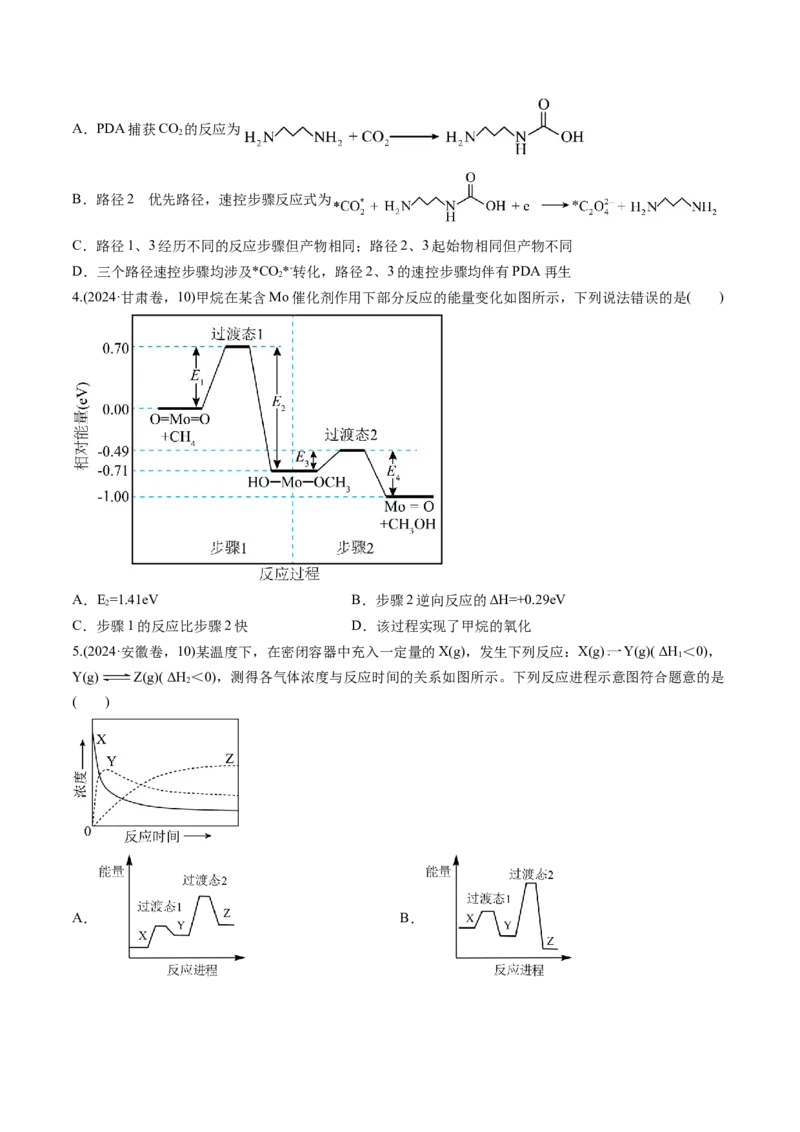
3.(2024·河北卷,14)对上述电池放电时CO 的捕获和转化过程开展了进一步研究,电极上CO 转化的三
2 2
种可能反应路径及相对能量变化如图(*表示吸附态)。
下列说法错误的是( )A.PDA捕获CO 的反应为
2
B.路径2 优先路径,速控步骤反应式为
是
C.路径1、3经历不同的反应步骤但产物相同;路径2、3起始物相同但产物不同
D.三个路径速控步骤均涉及*CO*-转化,路径2、3的速控步骤均伴有PDA再生
2
4.(2024·甘肃卷,10)甲烷在某含Mo催化剂作用下部分反应的能量变化如图所示,下列说法错误的是( )
A.E=1.41eV B.步骤2逆向反应的ΔH=+0.29eV
2
C.步骤1的反应比步骤2快 D.该过程实现了甲烷的氧化
5.(2024·安徽卷,10)某温度下,在密闭容器中充入一定量的X(g),发生下列反应:X(g) Y(g)( ΔH <0),
1
Y(g) Z(g)( ΔH <0),测得各气体浓度与反应时间的关系如图所示。下列反应进程示意图符合题意的是
2
( )
A. B.C. D.
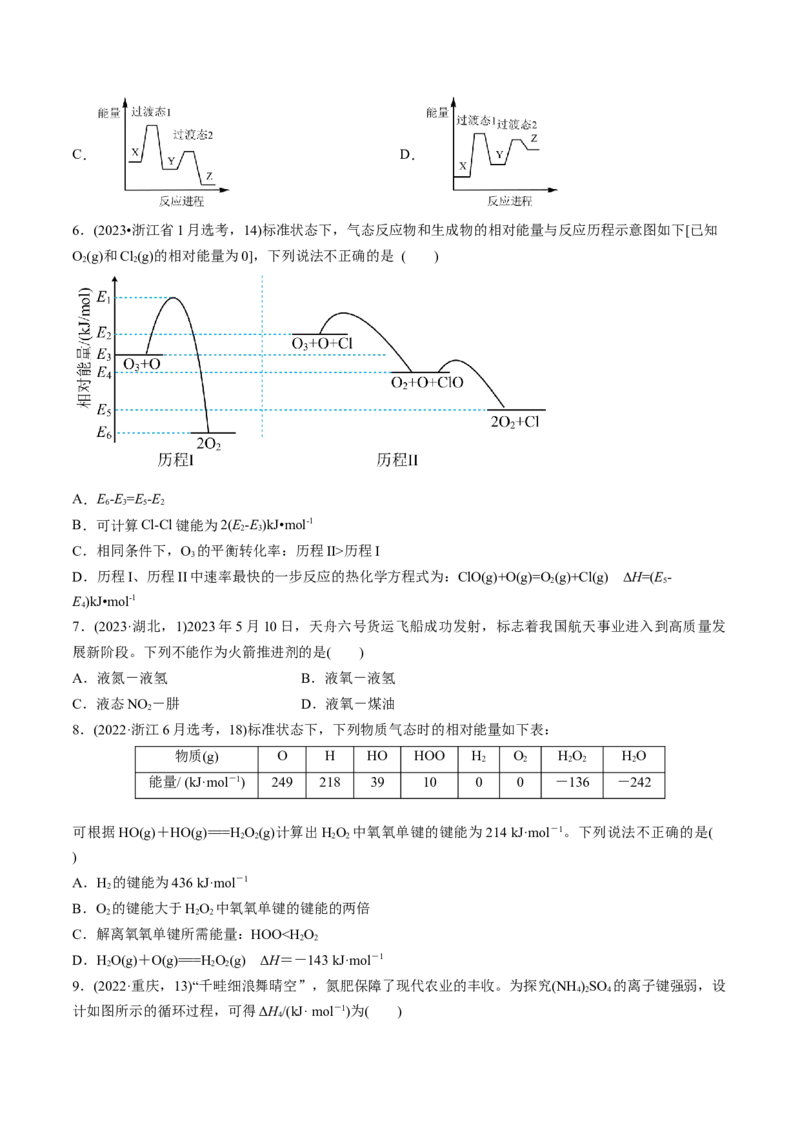
6.(2023•浙江省1月选考,14)标准状态下,气态反应物和生成物的相对能量与反应历程示意图如下[已知
O(g)和Cl(g)的相对能量为0],下列说法不正确的是 ( )
2 2
A.E-E=E-E
6 3 5 2
B.可计算Cl-Cl键能为2(E-E)kJ•mol-1
2 3
C.相同条件下,O 的平衡转化率:历程II>历程I
3
D.历程I、历程II中速率最快的一步反应的热化学方程式为:ClO(g)+O(g)=O (g)+Cl(g) ∆H=(E-
2 5
E)kJ•mol-1
4
7.(2023·湖北,1)2023年5月10日,天舟六号货运飞船成功发射,标志着我国航天事业进入到高质量发
展新阶段。下列不能作为火箭推进剂的是( )
A.液氮-液氢 B.液氧-液氢
C.液态NO -肼 D.液氧-煤油
2
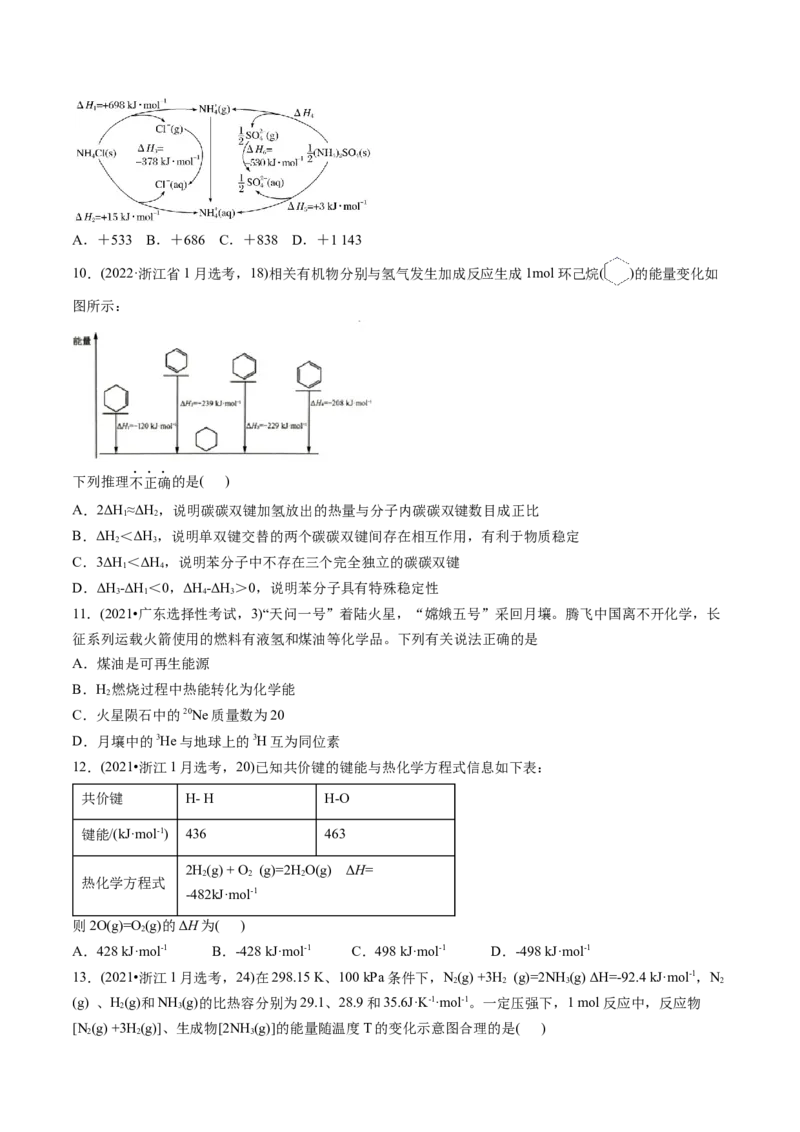
8.(2022·浙江6月选考,18)标准状态下,下列物质气态时的相对能量如下表:
物质(g) O H HO HOO H O HO HO
2 2 2 2 2
能量/ (kJ·mol-1) 249 218 39 10 0 0 -136 -242
可根据HO(g)+HO(g)===H O(g)计算出HO 中氧氧单键的键能为214 kJ·mol-1。下列说法不正确的是(
2 2 2 2
)
A.H 的键能为436 kJ·mol-1
2
B.O 的键能大于HO 中氧氧单键的键能的两倍
2 2 2
C.解离氧氧单键所需能量:HOO