文档内容
解密 10 金属及其化合物
一、单选题
1.(2022·全国·高三专题练习)“矾”是一类金属硫酸盐的结晶水合物,在生活和生产中
有着重要应用,下列有关“矾”的说法正确的是
A.蓝矾(CuSO ·5H O)是一种纯净物,可用于检验酒精中是否含有水
4 2
B.明矾[KAl(SO)·12H O]常用于净水,其水溶液显中性
4 2 2
C.铁铵矾[NH Fe(SO )·12H O]是一种媒染剂,其中Fe的化合价为+3价
4 4 2 2
D.皓矾(ZnSO·7H O)常用作医学收敛剂,铁单质与其溶液反应能置换出Zn
4 2
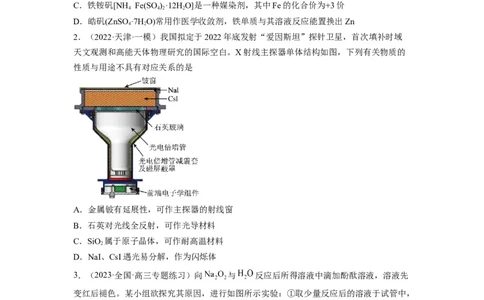
2.(2022·天津·一模)我国拟定于2022年底发射“爱因斯坦”探针卫星,首次填补时域
天文观测和高能天体物理研究的国际空白。X射线主探器单体结构如图,下列有关物质的
性质与用途不具有对应关系的是
A.金属铍有延展性,可作主探器的射线窗
B.石英对光线全反射,可作光导材料
C.SiO 属于原子晶体,可作耐高温材料
2
D.NaI、CsI遇光易分解,作为闪烁体
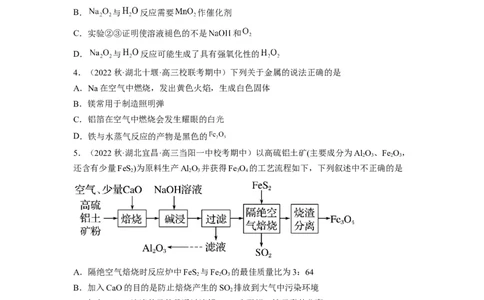
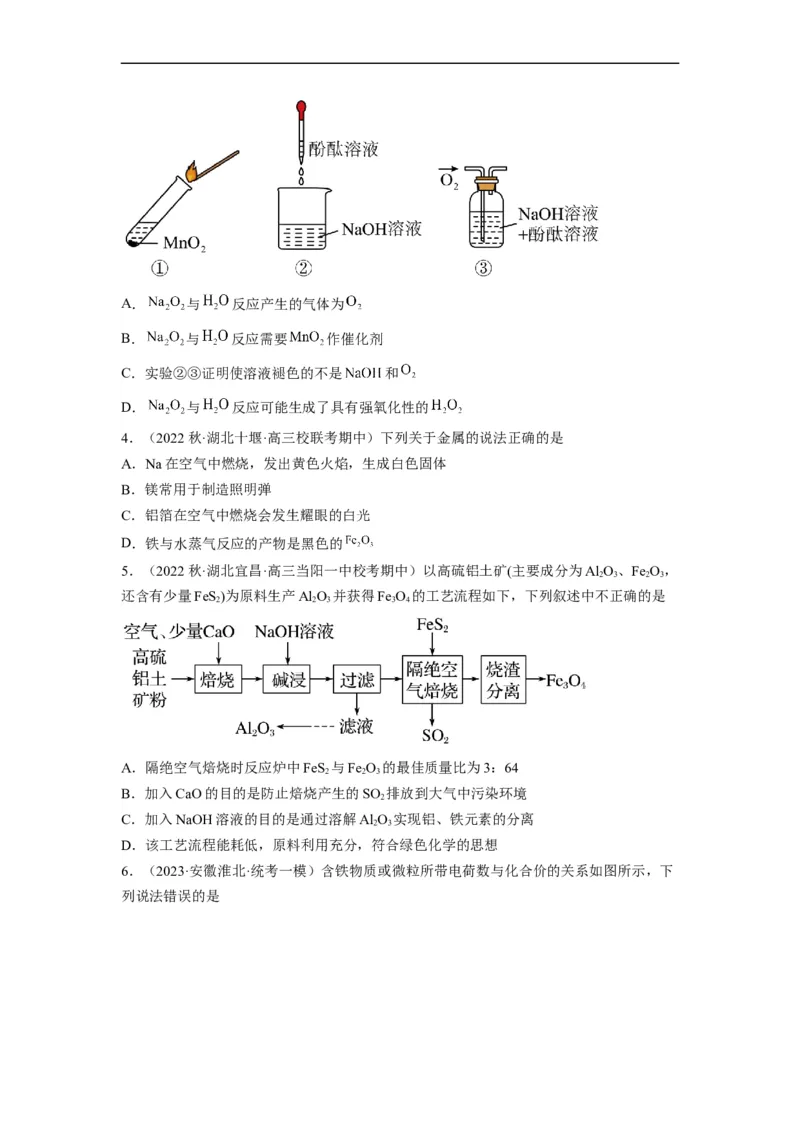
3.(2023·全国·高三专题练习)向 与 反应后所得溶液中滴加酚酞溶液,溶液先
变红后褪色。某小组欲探究其原因,进行如图所示实验:①取少量反应后的溶液于试管中,
加入 后迅速产生大量气体且该气体能使带火星的木条复燃;实验②③中溶液红色均
不褪去。下列分析错误的是A. 与 反应产生的气体为
B. 与 反应需要 作催化剂
C.实验②③证明使溶液褪色的不是 和
D. 与 反应可能生成了具有强氧化性的
4.(2022秋·湖北十堰·高三校联考期中)下列关于金属的说法正确的是
A.Na在空气中燃烧,发出黄色火焰,生成白色固体
B.镁常用于制造照明弹
C.铝箔在空气中燃烧会发生耀眼的白光
D.铁与水蒸气反应的产物是黑色的
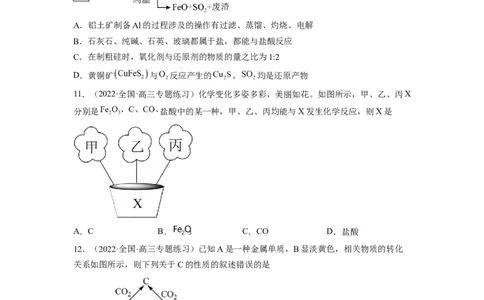
5.(2022秋·湖北宜昌·高三当阳一中校考期中)以高硫铝土矿(主要成分为Al O、Fe O,
2 3 2 3
还含有少量FeS)为原料生产Al O 并获得Fe O 的工艺流程如下,下列叙述中不正确的是
2 2 3 3 4
A.隔绝空气焙烧时反应炉中FeS 与Fe O 的最佳质量比为3:64
2 2 3
B.加入CaO的目的是防止焙烧产生的SO 排放到大气中污染环境
2
C.加入NaOH溶液的目的是通过溶解Al O 实现铝、铁元素的分离
2 3
D.该工艺流程能耗低,原料利用充分,符合绿色化学的思想
6.(2023·安徽淮北·统考一模)含铁物质或微粒所带电荷数与化合价的关系如图所示,下
列说法错误的是A.M可能是
B.R为铁单质,常温下遇浓硫酸发生钝化
C.N可用 溶液检验
D. 与强氧化剂在碱性条件下反应可以生成
7.(2022秋·湖北宜昌·高三当阳一中校考期中)碱式氯化铜[Cu Cl(OH)·nH O]是一种
x y z 2
农药。制备时先将铜粉加入稀盐酸中,并持续通空气反应生成CuCl ,继而制得碱式氯化
2
铜。Fe3+对该反应有催化作用,其催化原理如图所示。下列叙述中正确的是
A.图中M、N分别为Fe2+、Fe3+
B.碱式氯化铜在空气中不稳定,易被氧化变质
C.制备1 molCuCl ,理论上消耗标准状况下22.4 LO
2 2
D.制备CuCl 涉及氧化还原反应,由CuCl 制备碱式氯化铜不涉及氧化还原反应
2 2
8.(2021秋·黑龙江哈尔滨·高三校考阶段练习)我国古代地理名著《水经注》中有如下记
载:“屈茨二百里有山,夜则火光,昼则旦烟,人取此山石炭冶此山铁,恒充三十六国
用”,下列有关理解正确的是
A.“石炭”是焦炭 B.“山铁”是单质铁
C.“石炭”能用于还原铁矿石 D.“石炭”夜晚燃烧时不冒烟
9.(2022春·江苏扬州·高三统考阶段练习)按照绿色化学的思想,最理想的“原子经济性
反应”就是反应物的原子全部转化为期望的最终产物。下列工业生产涉及的反应中最符合
“原子经济性反应”的是
A.钠与氧气反应制取过氧化钠
B.氯气与石灰乳反应制取次氯酸钙
C.一氧化碳还原氧化铁冶炼铁
D.二氧化硅与焦炭反应制取粗硅
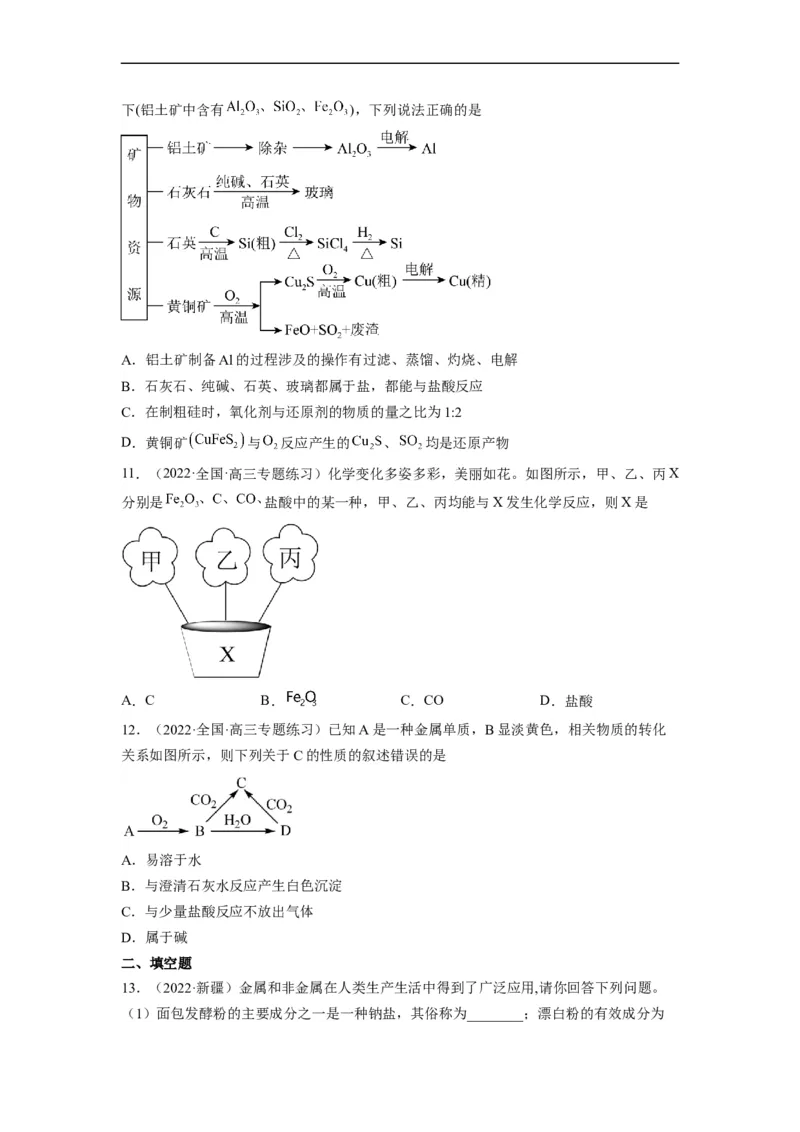
10.(2022·全国·高三专题练习)工业上利用无机矿物资源生产部分材料的流程示意图如下(铝土矿中含有 ),下列说法正确的是
A.铝土矿制备Al的过程涉及的操作有过滤、蒸馏、灼烧、电解
B.石灰石、纯碱、石英、玻璃都属于盐,都能与盐酸反应
C.在制粗硅时,氧化剂与还原剂的物质的量之比为1:2
D.黄铜矿 与 反应产生的 、 均是还原产物
11.(2022·全国·高三专题练习)化学变化多姿多彩,美丽如花。如图所示,甲、乙、丙X
分别是 盐酸中的某一种,甲、乙、丙均能与X发生化学反应,则X是
A.C B. C.CO D.盐酸
12.(2022·全国·高三专题练习)已知A是一种金属单质,B显淡黄色,相关物质的转化
关系如图所示,则下列关于C的性质的叙述错误的是
A.易溶于水
B.与澄清石灰水反应产生白色沉淀
C.与少量盐酸反应不放出气体
D.属于碱
二、填空题
13.(2022·新疆)金属和非金属在人类生产生活中得到了广泛应用,请你回答下列问题。
(1)面包发酵粉的主要成分之一是一种钠盐,其俗称为________;漂白粉的有效成分为__________(写化学式);FeCl 常用作净水剂,其原理为_________(用离子方程式表
3
示)。
(2)沾有水的铁制器皿在高温火焰上会发黑,该反应的化学方程式是_________。
(3)人体血红蛋白中含有Fe2+,若误食亚硝酸盐,会导致Fe2+转化Fe3+而中毒,服用维生
素C可以解毒.对上述的分析正确的是( )
A.亚硝酸盐是还原剂 B.维生素C是氧化剂
C.维生素C被氧化 D.亚硝酸盐发生氧化反应
(4)某CuSO 、HSO 的混合溶液100mL,已知溶液中阳离子的浓度相等(不考虑水解),
4 2 4
且SO 2-的物质的量浓度为6mol/L,则此溶液中阳离子的浓度为___________mol/L,若向此
4
溶液中加入金属Zn,则最多溶解Zn的质量为____________g。
14.(2022秋·湖南株洲·高三校考阶段练习)以软锰矿(主要含有MnO 及少量Fe、Al、
2
Si、Ca、Mg等的氧化物)为原料制备KMnO 的工艺流程如图所示:
4
回答下列问题:
(1)“浸取”时MnO 转化为Mn2+,反应的离子方程式为____。
2
(2)“除Fe、Al、Si”时,需将Fe2+氧化为Fe3+,最适宜的氧化剂为____(填标号)。
a.H O b.HNO c.Cl
2 2 3 2
(3)“除Ca、Mg时,所得溶液中 =____[K (MgF )=5×10-11,K (CaF )=5×10-9]。
sp 2 sp 2
(4)“沉锰”时不宜在较高温度下进行的原因是____。
(5)“焙烧”时,由MnCO 生成MnO 的化学方程式为____。
3 2
(6)“加热氧化”时,MnO 发生反应生成KMnO ,该反应的化学方程式为____;提高“水
2 4
浸”速率可以采取的措施为____(写两条);“系列操作”包括____,过滤、洗涤、干燥。
一、单选题
1.(2022·全国·高三专题练习)下列说法错误的是
A.铁、锰、铬以及他们的合金称为黑色金属材料
B.用铬酸做氧化剂可以使铝表面的氧化膜产生美丽的颜色
C.可溶性铜盐有毒,但在生命体中,铜是一种不可缺少的微量元素
D.钠与水反应、镁与沸水反应、红色的铁与高温水蒸气反应均生成碱和氢气
2.(2023·广东江门·校联考模拟预测)氢化钠是一种重要的储氢试剂、缩合剂、还原剂、
烷基化试剂,在有机合成中具有重要作用,某学习小组利用如图装置制备少量氢化钠,下列说法错误的是
A.装置丙中将Na分散到NaCl晶体中可以增大接触面积,使反应更充分
B.装置乙和装置丁内盛放的试剂可以分别为无水氯化钙和碱石灰
C.实验过程中应先打开K,一段时间后,尾端验纯后再点燃酒精灯
1
D.m gH 储存到NaH中,与足量水反应也释放m gH ,遵从质量守恒定律
2 2
3.(2022·浙江·模拟预测)下列说法不正确的是
A.碳酸钠可与盐酸反应,可用于治疗胃酸过多
B.Mg燃烧可发出耀眼白光,可用作信号弹
C.二氧化硅导光性良好,可用作光导纤维
D. 在水中可形成胶体,可用作净水剂
4.(2023春·青海西宁·高三统考开学考试)铝土矿中主要含有Al O,还有少量Fe O,
2 3 2 3
SiO 杂质,从铝土矿中冶炼金属铝方法如图所示(步骤①、②、③中每步反应结束后经过过
2
滤才进行下一步反应)。下列有关说法不正确的是
A.电解熔融氧化铝制取金属铝时加入冰晶石的作用是降低氧化铝熔融所需的温度
B.步骤②的作用是除去母液1中的Fe3+的H+
C.步骤③生成沉淀的离子反应方程式为AlO +CO +2H O=HCO +Al(OH) ↓
2 2 3
D.将步骤①和步骤②顺序颠倒,再通入足量CO 也能得到氢氧化铝沉淀
2
5.(2023·全国·高三专题练习)某酸性废水中含有Fe2+、Fe3+、Al3+、Mg2+、Na+、K+、
中的若干种,取废水样品分别进行如图所示①~④四个实验,下列推断正确的是
A.废水含有Na+,不含K+
B.废水不含
C.废水不含Fe3+,可能含Fe2+
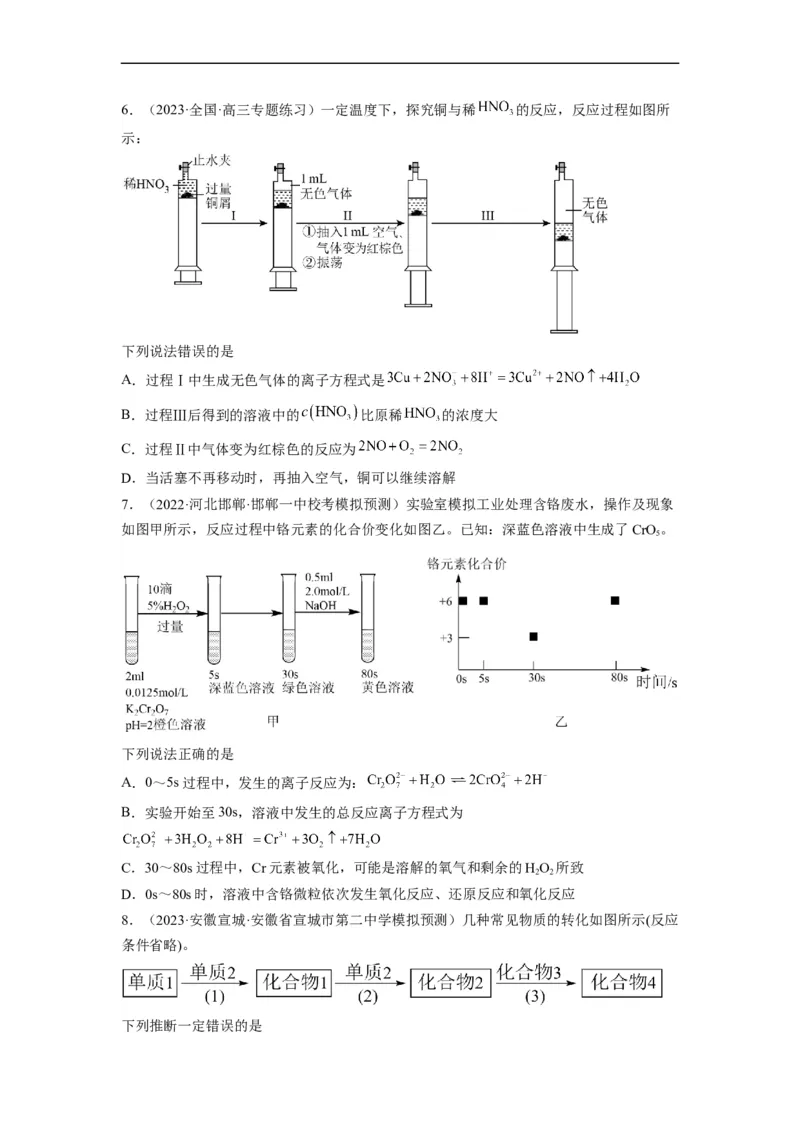
D.废水一定含有Na+、Al3+、6.(2023·全国·高三专题练习)一定温度下,探究铜与稀 的反应,反应过程如图所
示:
下列说法错误的是
A.过程Ⅰ中生成无色气体的离子方程式是
B.过程Ⅲ后得到的溶液中的 比原稀 的浓度大
C.过程Ⅱ中气体变为红棕色的反应为
D.当活塞不再移动时,再抽入空气,铜可以继续溶解
7.(2022·河北邯郸·邯郸一中校考模拟预测)实验室模拟工业处理含铬废水,操作及现象
如图甲所示,反应过程中铬元素的化合价变化如图乙。已知:深蓝色溶液中生成了CrO。
5
下列说法正确的是
A.0~5s过程中,发生的离子反应为:
B.实验开始至30s,溶液中发生的总反应离子方程式为
C.30~80s过程中,Cr元素被氧化,可能是溶解的氧气和剩余的HO 所致
2 2
D.0s~80s时,溶液中含铬微粒依次发生氧化反应、还原反应和氧化反应
8.(2023·安徽宣城·安徽省宣城市第二中学模拟预测)几种常见物质的转化如图所示(反应
条件省略)。
下列推断一定错误的是A.若化合物2是淡黄色固体,化合物3为液态氧化物,则化合物4为碱
B.若单质1为黑色粉末,化合物2能使澄清石灰水变浑浊,则化合物1易溶于水
C.反应(1)和(2)是氧化还原反应,反应(3)可能是非氧化还原反应
D.若化合物1、2、3、4与单质2都含有某种元素,则该元素可能是铁
9.(2023·广东深圳·统考一模)劳动创造幸福。下列劳动项目与所述的化学知识没有关联
的是
选
劳动项目 化学知识
项
A 分析员用X射线衍射仪区分普通玻璃和水晶 普通玻璃属于非晶体,水晶属于晶体
B 面点师制作糕点时添加小苏打作膨松剂 可与碱反应
C 实验员用加热法分离 和NaCl 易升华
D 维修工用NaOH和铝粉疏通厨卫管道 Al与NaOH溶液反应产生
A.A B.B C.C D.D
10.(2023·安徽·统考一模)在实验室中进行下列实验,下列操作能实现实验目的的是
选
实验目的 操作
项
将含有苯甲酸的苯酚加入饱和 ,溶液中,
A 除去苯酚中混有的少量苯甲酸
过滤
检验溶解铁锈所得的溶液中是 取少量溶液,向其中滴加氯水后,再加入 溶
B
否含有 液,观察溶液是否变红
将混合气通过盛有溴的四氯化碳溶液,观察溶液是
C 检验乙烷中是否含有乙烯
否褪色
检验 中是否混有
D 取少量固体,滴加稀盐酸,观察是否有气体生成
A.A B.B C.C D.D
11.(2023·北京西城·高三北京师大附中校考阶段练习)表示下列反应的方程式正确的是
A.铁粉与水蒸气共热,生成可燃性气体:B.过量的铁粉和氯气反应:
C.向 浊液中加入 溶液,生成红褐色沉淀:
D.向 溶液中滴加 溶液,溶液由浅绿色变为黄色:
12.(2023春·广东广州·高三广州市第二中学校联考开学考试)中科院化学所研制的晶体
材料-纳米四氧化三铁,在核磁共振造影及医药上有广泛用途,其生产过程的部分流程如
下所示。
FeCl ·6H O 纳米Fe O
3 2 3 4
下列有关叙述不合理的是
A.在反应①中环丙胺的作用可能是促进氯化铁水解
B.反应②发生的化学方程式为6FeOOH + CO=2Fe O + 3H O + CO
3 4 2 2
C.可用稀硫酸和K[Fe(CN) ]鉴别Fe O 和FeO
3 6 3 4
D.将制得的Fe O 均匀分散在水中可能产生丁达尔效应
3 4
二、填空题
13.(2021秋·江苏淮安·高三校考阶段练习)“纳米零价铁—HO”体系可将烟气中难溶的
2 2
NO氧化为可溶的 。
(1)制备纳米零价铁:将FeSO 溶液与碱性NaBH4溶液混合可生成纳米零价铁、H 和
4 2
NaBO 等,该反应的离子方程式为_______(NaBH 、NaBO 中B元素均为+3价)。
2 4 2
(2)NO的氧化:在一定温度下,将HO 溶液和HCl溶液雾化后与烟气按一定比例混合,以
2 2
一定流速通过装有纳米零价铁的反应装置,可将烟气中的NO氧化。
①Fe2+催化HO 分解产生HO·,HO·将NO氧化为 的机理如图1所示,Y的化学式为
2 2
_______。
②NO与HO 反应生成HNO 的化学方程式为_______。
2 2 3
③NO脱除率随温度的变化如图2所示。温度高于120℃时,NO脱除率随温度升高呈现下
降趋势的主要原因是_______。
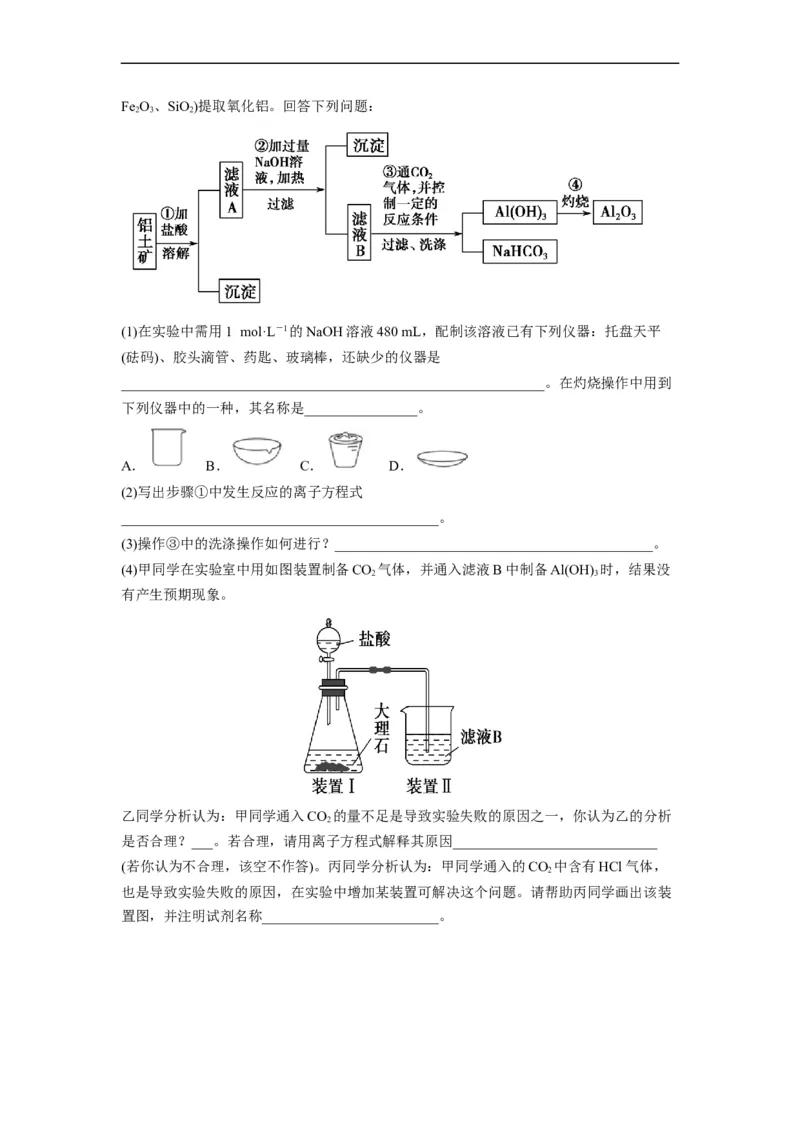
14.(2022·全国·模拟预测)某探究小组在实验室中用铝土矿(主要成分为Al O,还含有
2 3Fe O、SiO)提取氧化铝。回答下列问题:
2 3 2
(1)在实验中需用1 mol·L-1的NaOH溶液480 mL,配制该溶液已有下列仪器:托盘天平
(砝码)、胶头滴管、药匙、玻璃棒,还缺少的仪器是
____________________________________________________________。在灼烧操作中用到
下列仪器中的一种,其名称是________________。
A. B. C. D.
(2)写出步骤①中发生反应的离子方程式
_____________________________________________。
(3)操作③中的洗涤操作如何进行?_____________________________________________。
(4)甲同学在实验室中用如图装置制备CO 气体,并通入滤液B中制备Al(OH) 时,结果没
2 3
有产生预期现象。
乙同学分析认为:甲同学通入CO 的量不足是导致实验失败的原因之一,你认为乙的分析
2
是否合理?___。若合理,请用离子方程式解释其原因_____________________________
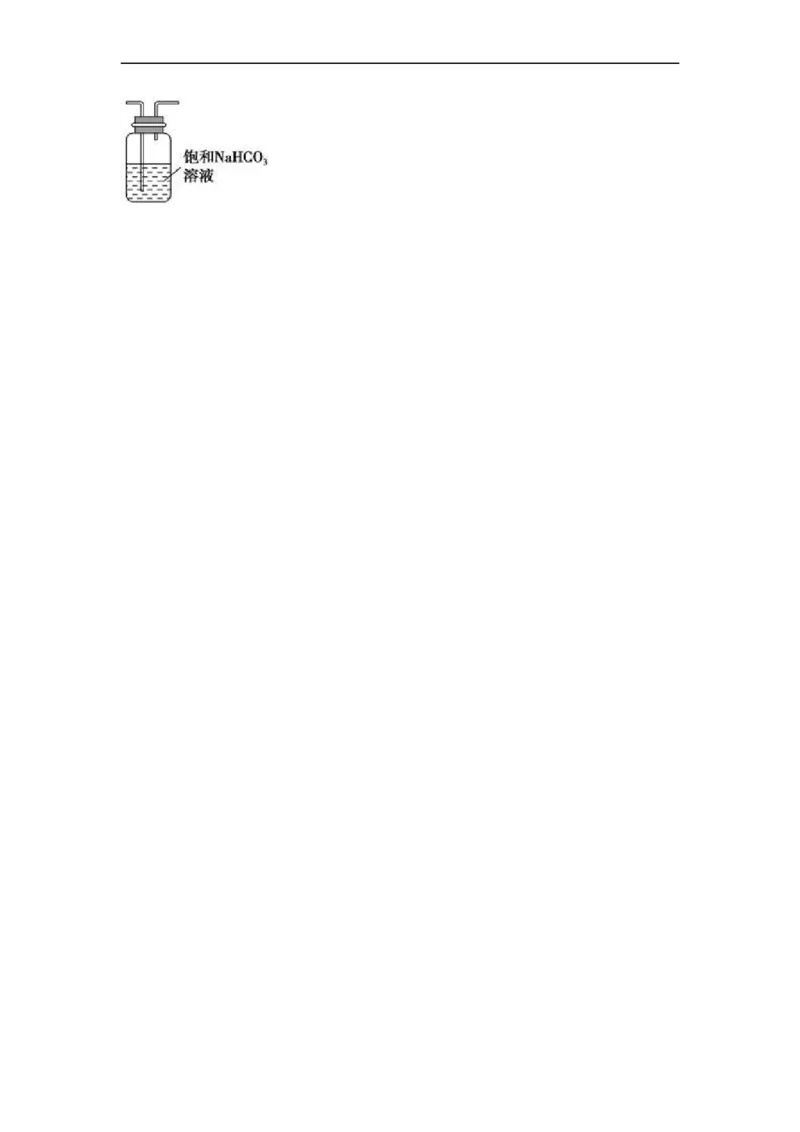
(若你认为不合理,该空不作答)。丙同学分析认为:甲同学通入的CO 中含有HCl气体,
2
也是导致实验失败的原因,在实验中增加某装置可解决这个问题。请帮助丙同学画出该装
置图,并注明试剂名称_________________________。