文档内容
解密 12 实验化学
一、选择题
1.(2021届浙江省山水联盟高三12月联考)下列说法不正确的是( )
A.当溶液发生过饱和现象时,振荡容器可促使晶体析出
B.硝酸钾溶液含有少量氯化钠,可用蒸发浓缩、冷却结晶来提纯硝酸钾
C.抽滤洗涤沉淀时,关小水龙头,使洗涤剂缓慢通过沉淀物
D.纸层析实验中,滤纸作为固定相,展开剂作为流动相
2.(2021届浙江省十校联盟高三联考)下列说法不正确的是( )
A.结晶时溶液浓度越大,溶质的溶解度越小,析出的晶粒就越大
B.蒸馏时忘加沸石,需先停止加热,冷却至室温后补加沸石
C.可用紫外可见分光光度法测定废液中苯酚的含量
D.可用溴的四氯化碳溶液检验丙烯醛(CH= CHCHO)中的碳碳双键
2
3.(2021届浙江省三校高三第一次联考)下列有关实验说法不正确的是( )
A.在4 mL 0.1 mol·L-1的KCr O 溶液中滴加数滴1 mol·L-1的NaOH溶液,溶液颜色从橙色变成黄色
2 2 7
B.酸式滴定管在润洗时,可在滴定管中加入少量待装液,润洗后将溶液从滴定管的上口倒入废液缸
中重复2~3次,润洗完毕
C.“阿司匹林的合成”实验中抽滤制得乙酰水杨酸粗产品时需用滤液淋洗锥形瓶,直至所有晶体被
收集到布氏漏斗中
D.牙膏中的甘油可用新制的碱性氢氧化铜检验,现象是溶液变绛蓝色
4.(2021届浙江省浙南名校联盟高三联考)下列有关实验的说法正确的是( )
A.在“研究NaSO 与酸反应速率的影响因素”实验中,可通过观察产生气泡的快慢来比较不同条件
2 2 3
下该反应的速率大小
B.为了精确测定盐酸与氢氧化钠溶液反应的反应热,当两者混合后,立即读取温度计的读数,防止
热量散失
C.向1mL0.5mol/LAlCl 溶液中先滴加2mL饱和NaF溶液,立即产生大量白色沉淀
3
D.用纸层析法可以分离少量Fe3+与Cu2+
5.(2021届浙江省长兴、余杭、缙云三校高三12月模拟考试)下列有关实验说法不正确的是( )
A.当锌完全溶解后,铁与酸反应产生氢气的速率会显著减慢,此现象可作为判断镀锌铁皮中锌镀层是
否完全被反应掉的依据
B.向少量的火柴头浸泡液中滴加AgNO、稀HNO 和NaNO ,检验火柴头中的氯元素
3 3 2C.制备摩尔盐时,最后在蒸发皿中蒸发浓缩溶液,加热至液体表面出现晶膜为止,不能将溶液全部蒸
干
D.检验氯乙烷中的氯元素时,将氯乙烷和NaOH溶液混合加热后,用稀硫酸进行酸化
6.(2021届浙江省长兴、余杭、缙云三校高三12月模拟考试)下列说法正确的是( )
A.纸上层析属于色谱分析法,其原理跟“毛细现象”相关,通常以滤纸作为惰性支持物,吸附水作为
固定相
B.将两块未擦去氧化膜的铝片分别投入1mol/L CuSO 溶液、1mol/L CuCl 溶液中,铝片表面都观察不
4 2
到明显的反应现象
C.将20g硝酸钠和17g氯化钾放100mL烧杯中,加35mL水,并加热、搅拌,使溶液浓缩至约为原来
的一半时,趁热过滤即可得到硝酸钾晶体
D.用移液管取液后,将移液管垂直伸入容器底部,松开食指使溶液全部流出,数秒后取出移液管
7.(2021届浙江省重点中学高三11月选考模拟)下列说法错误的是( )
A.若不慎吸入较多溴蒸气导致中毒,应立刻进行人工呼吸后送至医院就诊
B.可以用稀硫酸酸化的KI-淀粉溶液鉴别亚硝酸钠和食盐
C.用纸层析法分离Fe3+和Cu2+时,由于 Fe3+亲脂性更强,因此Fe3+在滤纸上流动得快些
D.制摩尔盐时可用酒精洗涤产品,制阿司匹林时可用冷水洗涤产品,制硝酸钾晶体时可用硝酸钾饱和
溶液洗涤产品
8.(2021届浙江省温州市高三选考三模)下列有关实验操作的说法,不正确的是( )
A.减压过滤中的转移,先开大水龙头,再用倾析法转移溶液至布氏漏斗中,待溶液快流尽时再转移
沉淀
B.酸式滴定管的润洗,从滴定管上口加入3~ 5mL所要盛装液体,倾斜着转动滴定管,然后轻轻转动
活塞,将液体从滴定管下部放入预置的烧杯中
C.振荡分液漏斗中的混合溶液,用一只手压住分液漏斗的玻璃塞,另一只 手握住旋塞,将分液漏斗
倒转过来,用力振荡
D.焰色反应检验Na+,取一根铂丝,放在酒精灯火焰上灼烧至无色,然后蘸取少量试液,置于火焰上
灼烧,观察火焰颜色
9.(2021届浙江富阳、浦江、新昌三校高三第三次联考)下列有关实验说法不正确的是( )
A.用容量瓶配制溶液,定容时若加水超过刻度线,需重新配置
B.海带灼烧成灰烬后,加水煮沸2~3min并过滤,滤液中可以加入适量的HO 来氧化I-
2 2
C.火柴头的浸泡液中滴加AgNO 溶液,稀HNO 和NaNO 溶液,可检验火柴头是否含有氯元素
3 3 2
D.在淀粉溶液中加入硫酸并加热数分钟,冷却后依次加入新制Cu(OH) 悬浊液和碘水检验淀粉是否已
2发生水解和是否完全水解。
10.(2021届浙江省嘉兴市高三12月教学测试)下列有关实验说法不正确的是( )
A.配制一定物质的量浓度的NaOH溶液时,NaOH固体溶解后未恢复到室温就定容,所配制的溶液浓
度将偏小
B.向试管中注入5 mL 1-溴丙烷和10 mL 20%的氢氧化钾水溶液,加热,充分反应后再加入硝酸酸化,
滴加硝酸银溶液,可以看到淡黄色沉淀
C.在纸层析分离Fe3+和Cu2+的实验中,亲脂性强的成分在流动相中分配得多一些,随流动相移动的速
度就快一些
D.用移液管量取一定体积液体时,应将移液管垂直放入稍倾斜的容器中,并使管尖与容器内壁接触
11.(2021届浙江省金丽衢十二校高三联考)下列有关实验说法中,不正确的是( )
A.利用纸层析法分离Fe3+、Cu2+时,氨熏显色后上方出现红棕色斑点,下方出现深蓝色斑点
B.可用AgNO 溶液和稀HNO 区分NaCl、NaNO 和NaNO
3 3 2 3
C.在“镀锌铁皮的镀层厚度的测定”实验中,将镀锌铁皮放人稀硫酸,待产生气泡的速率显著减小
时,可以判断锌镀层已反应完全
D.溶质的溶解度小,溶液的浓度高,可析出较大晶粒
12.下列说法正确的是( )
A.在“镀锌铁皮锌镀层厚度的测定”实验中,将镀锌铁皮放入稀硫酸,待产生氢气的速率突然减小,
可以判断锌镀层已反应完全
B.在“火柴头中氯元素的检验”实验中,摘下几根未燃过的火柴头,将其浸于水中,稍后取少量溶
液于试管中,滴加硝酸银溶液和稀硝酸后,即可判断氯元素的存在
C.在“硫酸亚铁铵的制备”实验中,为了得到硫酸亚铁铵晶体,应小火加热蒸发皿,直到有大量晶
体析出时停止加热
D.受强酸或强碱腐蚀致伤时,应先用大量水冲洗,再用 2%醋酸溶液或饱和硼酸溶液洗,最后用水冲
洗,并视情况作进一步处理
13.下列说法不正确的是( )
A.胶状沉淀或颗粒太小的沉淀不宜用减压过滤,溶液有强酸性、强碱性或强氧化性时,应用玻璃纤
维代替滤纸或用玻璃砂漏斗代替布氏漏斗
B.移液管吸取溶液后,应将其垂直放入稍倾斜的容器中,并使管尖与容器内壁接触,松开食指使溶
液全部流出,数秒后,取出移液管
C.红外光谱仪、质谱仪、核磁共振仪可用于测定有机物结构,同位素示踪法可用于研究化学反应历
程
D.为检验火柴头中是否存在氯元素,将火柴头浸于水中,片刻后取少量溶液于试管中,加AgNO 溶
3
液、稀硝酸溶液。若出现白色沉淀,说明含氯元素
14.(2021届浙江省温州市高三适应性测试)下列有关实验的说法,正确的是( )A.溶液中滴加BaCl 溶液出现白色沉淀,再加入足量稀盐酸沉淀不溶解,说明含SO 2-
2 4
B.为了使阿司匹林晶体能从过饱和溶液中析出,可用玻璃棒摩擦与溶液接触处的容器壁
C.用容量瓶配制溶液,定容时仰视刻度,所配溶液浓度偏大
D.有机溶剂乙醇、丙酮、四氯化碳等极易被引燃,使用时需远离火源
15.(2021届浙江省杭州高级中学高三模拟)下列有关实验说法正确的是( )
A.容量瓶和滴定管上都标有使用温度,使用时滴定管水洗后还需润洗,但容量瓶水洗后不用润洗
B.测溶液pH: 用干燥洁净的玻璃棒蘸取NaClO溶液,滴到放在表面皿上的pH 试纸中部, 变色后
与标准比色卡比对
C.抽滤过程中洗涤沉淀时, 应关小水龙头, 加洗涤剂浸没沉淀,用玻璃棒在过滤器上搅拌以使沉
淀跟洗涤剂充分接触,以便洗得更干净
D.实验过程中的有毒药品不得进入口内或者接触伤口,剩余的废液不得再回收使用,应倒入下水道
16.(2021届浙江省Z20名校联盟高三联考)下列说法正确的是( )
A.火柴头上的物质一般是KClO、MnO 等氧化剂和S 等易燃物,而火柴盒侧面涂有白磷、Sb S 等
3 2 3 3
B.稀释 CoCl •6H O的乙醇溶液,颜色由粉红色变成蓝色
2 2
C.NaSO 与HSO 反应速率可以通过观察出现浑浊的快慢来比较反应速率大小, 而很难用气泡产生
2 2 3 2 4
的快慢来比较反应速率大小
D.NaCl 固体与 NaNO 固体可以用 AgNO 溶液来鉴别
2 3
二、非选择题
17.(2021届浙江富阳、浦江、新昌三校高三第三次联考)K [Fe(C O)]·3H O[三草酸合铁(Ⅲ)酸钾晶体]
3 2 4 3 2
易溶于水,难溶于乙醇,可作为有机反应的催化剂。实验室可用铁屑为原料制备,相关反应的化学方程式
为:
Fe(s)+HSO =FeSO+H↑
2 4 4 2
FeSO +HC O+2HO=FeC O·2H O↓+HSO
4 2 2 4 2 2 4 2 2 4
2FeC O·2H O+HO+HC O+3KC O=2K [Fe(C O)]+6HO
2 4 2 2 2 2 2 4 2 2 4 3 2 4 3 2
2MnO -+5C O2-+16H+=2Mn2++10CO↑+8HO
4 2 4 2 2
回答下列问题:
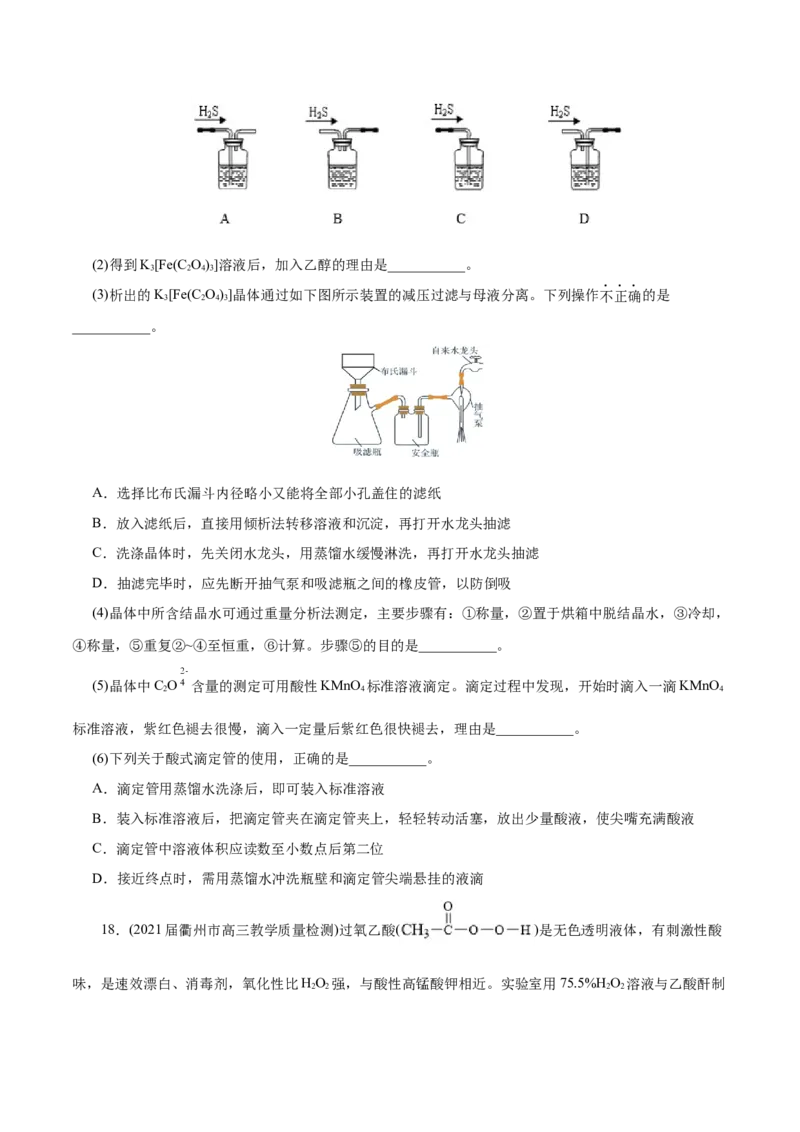
(1)铁屑中常含硫元素,因而在制备FeSO 时会产生有毒的HS气体,该气体可用氢氧化钠溶液吸收。下
4 2
列吸收装置正确的是___________。(2)得到K[Fe(C O)]溶液后,加入乙醇的理由是___________。
3 2 4 3
(3)析出的K[Fe(C O)]晶体通过如下图所示装置的减压过滤与母液分离。下列操作不正确的是
3 2 4 3
___________。
A.选择比布氏漏斗内径略小又能将全部小孔盖住的滤纸
B.放入滤纸后,直接用倾析法转移溶液和沉淀,再打开水龙头抽滤
C.洗涤晶体时,先关闭水龙头,用蒸馏水缓慢淋洗,再打开水龙头抽滤
D.抽滤完毕时,应先断开抽气泵和吸滤瓶之间的橡皮管,以防倒吸
(4)晶体中所含结晶水可通过重量分析法测定,主要步骤有:①称量,②置于烘箱中脱结晶水,③冷却,
④称量,⑤重复②~④至恒重,⑥计算。步骤⑤的目的是___________。
(5)晶体中C O 含量的测定可用酸性KMnO 标准溶液滴定。滴定过程中发现,开始时滴入一滴KMnO
2 4 4
标准溶液,紫红色褪去很慢,滴入一定量后紫红色很快褪去,理由是___________。
(6)下列关于酸式滴定管的使用,正确的是___________。
A.滴定管用蒸馏水洗涤后,即可装入标准溶液
B.装入标准溶液后,把滴定管夹在滴定管夹上,轻轻转动活塞,放出少量酸液,使尖嘴充满酸液
C.滴定管中溶液体积应读数至小数点后第二位
D.接近终点时,需用蒸馏水冲洗瓶壁和滴定管尖端悬挂的液滴
18.(2021届衢州市高三教学质量检测)过氧乙酸( )是无色透明液体,有刺激性酸
味,是速效漂白、消毒剂,氧化性比HO 强,与酸性高锰酸钾相近。实验室用75.5%H O 溶液与乙酸酐制
2 2 2 2备高浓度过氧乙酸。反应方程式为:(CHCO) O+HO CHCOOOH+CH COOH。实验分成
3 2 2 2 3 3
过氧化氢和过氧乙酸生成两个步骤。
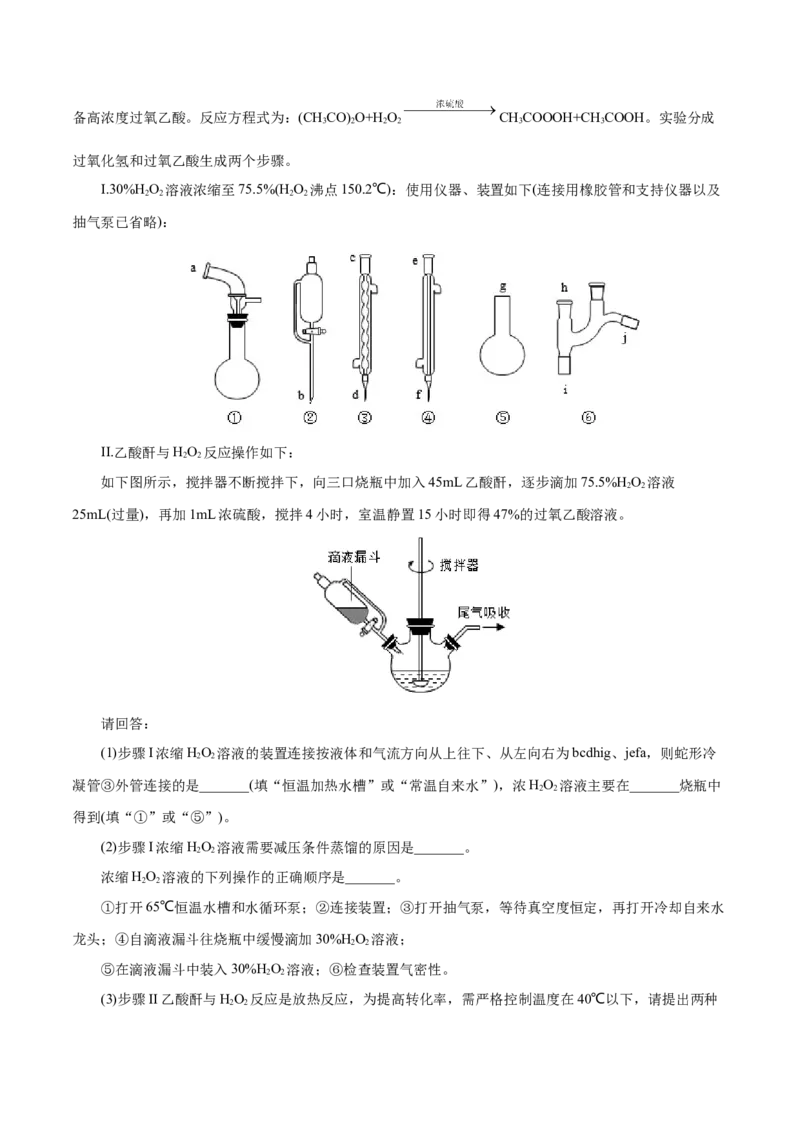
I.30%H O 溶液浓缩至75.5%(H O 沸点150.2℃):使用仪器、装置如下(连接用橡胶管和支持仪器以及
2 2 2 2
抽气泵已省略):
II.乙酸酐与HO 反应操作如下:
2 2
如下图所示,搅拌器不断搅拌下,向三口烧瓶中加入45mL乙酸酐,逐步滴加75.5%H O 溶液
2 2
25mL(过量),再加1mL浓硫酸,搅拌4小时,室温静置15小时即得47%的过氧乙酸溶液。
请回答:
(1)步骤I浓缩HO 溶液的装置连接按液体和气流方向从上往下、从左向右为bcdhig、jefa,则蛇形冷
2 2
凝管③外管连接的是_______(填“恒温加热水槽”或“常温自来水”),浓HO 溶液主要在_______烧瓶中
2 2
得到(填“①”或“⑤”)。
(2)步骤I浓缩HO 溶液需要减压条件蒸馏的原因是_______。
2 2
浓缩HO 溶液的下列操作的正确顺序是_______。
2 2
①打开65℃恒温水槽和水循环泵;②连接装置;③打开抽气泵,等待真空度恒定,再打开冷却自来水
龙头;④自滴液漏斗往烧瓶中缓慢滴加30%H O 溶液;
2 2
⑤在滴液漏斗中装入30%H O 溶液;⑥检查装置气密性。
2 2
(3)步骤II乙酸酐与HO 反应是放热反应,为提高转化率,需严格控制温度在40℃以下,请提出两种
2 2控制温度的措施:①_______,②_______。
(4)步骤II乙酸酐与HO 反应尾气可以用_______吸收。
2 2
(5)氧化还原滴定:加过量的还原剂KI反应生成I,以淀粉为指示剂滴定I 的量,来测定氧化剂含量的
2 2
方法。下列方法中可以测定产品中过氧乙酸含量的是_______。
A.酸碱中和滴定法 B.与Zn、Fe反应测H 法
2
C.氧化还原滴定法 D.加MnO 测O 法
2 2
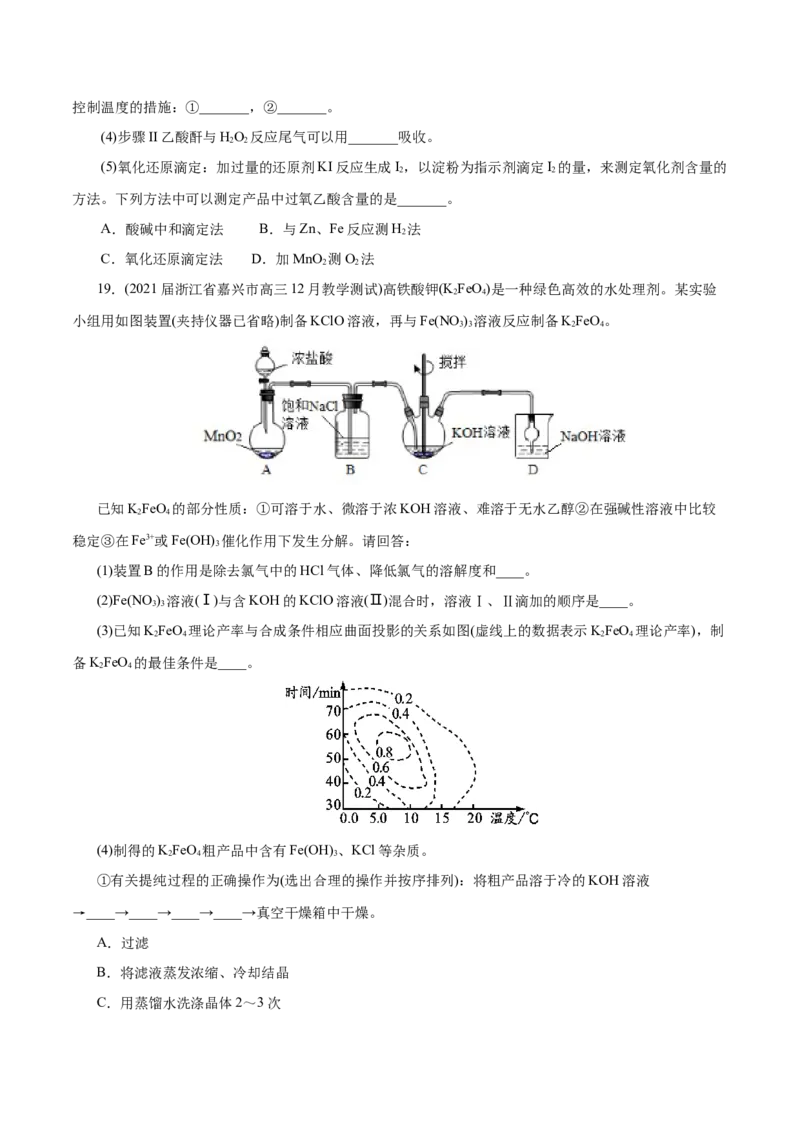
19.(2021届浙江省嘉兴市高三12月教学测试)高铁酸钾(K FeO)是一种绿色高效的水处理剂。某实验
2 4
小组用如图装置(夹持仪器已省略)制备KClO溶液,再与Fe(NO ) 溶液反应制备KFeO。
3 3 2 4
已知KFeO 的部分性质:①可溶于水、微溶于浓KOH溶液、难溶于无水乙醇②在强碱性溶液中比较
2 4
稳定③在Fe3+或Fe(OH) 催化作用下发生分解。请回答:
3
(1)装置B的作用是除去氯气中的HCl气体、降低氯气的溶解度和____。
(2)Fe(NO ) 溶液(Ⅰ)与含KOH的KClO溶液(Ⅱ)混合时,溶液Ⅰ、Ⅱ滴加的顺序是____。
3 3
(3)已知KFeO 理论产率与合成条件相应曲面投影的关系如图(虚线上的数据表示KFeO 理论产率),制
2 4 2 4
备KFeO 的最佳条件是____。
2 4
(4)制得的KFeO 粗产品中含有Fe(OH) 、KCl等杂质。
2 4 3
①有关提纯过程的正确操作为(选出合理的操作并按序排列):将粗产品溶于冷的KOH溶液
→____→____→____→____→真空干燥箱中干燥。
A.过滤
B.将滤液蒸发浓缩、冷却结晶
C.用蒸馏水洗涤晶体2~3次D.往滤液中加入冷的饱和KOH溶液,静置
E.用适量乙醇洗涤晶体2~3次
②过滤时应选用的漏斗是____。
③洗涤时选择相应操作的原因是____。
20.(2021届浙江省精诚联盟高三适应性联考)无水碱式氯化铜[Cu (OH) Cl]为绿色或墨绿色结晶性粉末,
2 3
难溶于水,溶于稀酸和氨水,在空气中十分稳定。
Ⅰ模拟制备碱式氯化铜晶体
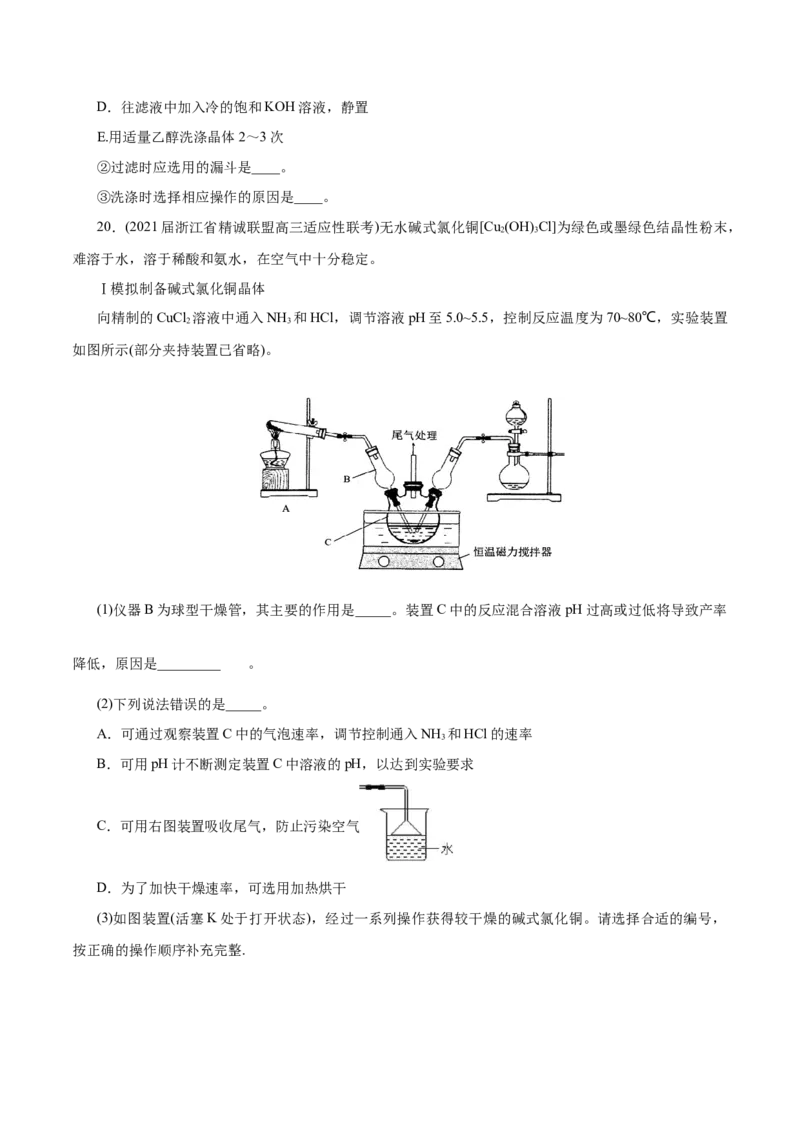
向精制的CuCl 溶液中通入NH 和HCl,调节溶液pH至5.0~5.5,控制反应温度为70~80℃,实验装置
2 3
如图所示(部分夹持装置已省略)。
(1)仪器B为球型干燥管,其主要的作用是_____。装置C中的反应混合溶液pH过高或过低将导致产率
降低,原因是_________ 。
(2)下列说法错误的是_____。
A.可通过观察装置C中的气泡速率,调节控制通入NH 和HCl的速率
3
B.可用pH计不断测定装置C中溶液的pH,以达到实验要求
C.可用右图装置吸收尾气,防止污染空气
D.为了加快干燥速率,可选用加热烘干
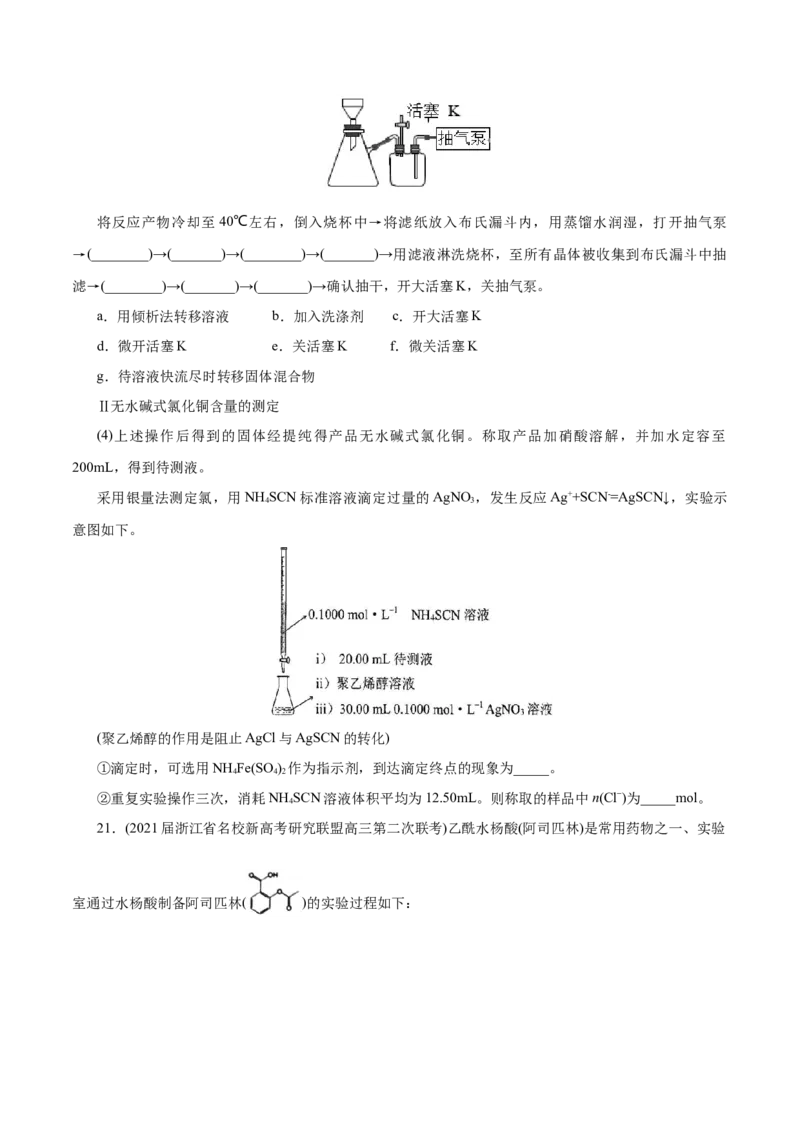
(3)如图装置(活塞K处于打开状态),经过一系列操作获得较干燥的碱式氯化铜。请选择合适的编号,
按正确的操作顺序补充完整.将反应产物冷却至40℃左右,倒入烧杯中→将滤纸放入布氏漏斗内,用蒸馏水润湿,打开抽气泵
→(________)→(_______)→(________)→(_______)→用滤液淋洗烧杯,至所有晶体被收集到布氏漏斗中抽
滤→(________)→(_______)→(_______)→确认抽干,开大活塞K,关抽气泵。
a.用倾析法转移溶液 b.加入洗涤剂 c.开大活塞K
d.微开活塞K e.关活塞K f.微关活塞K
g.待溶液快流尽时转移固体混合物
Ⅱ无水碱式氯化铜含量的测定
(4)上述操作后得到的固体经提纯得产品无水碱式氯化铜。称取产品加硝酸溶解,并加水定容至
200mL,得到待测液。
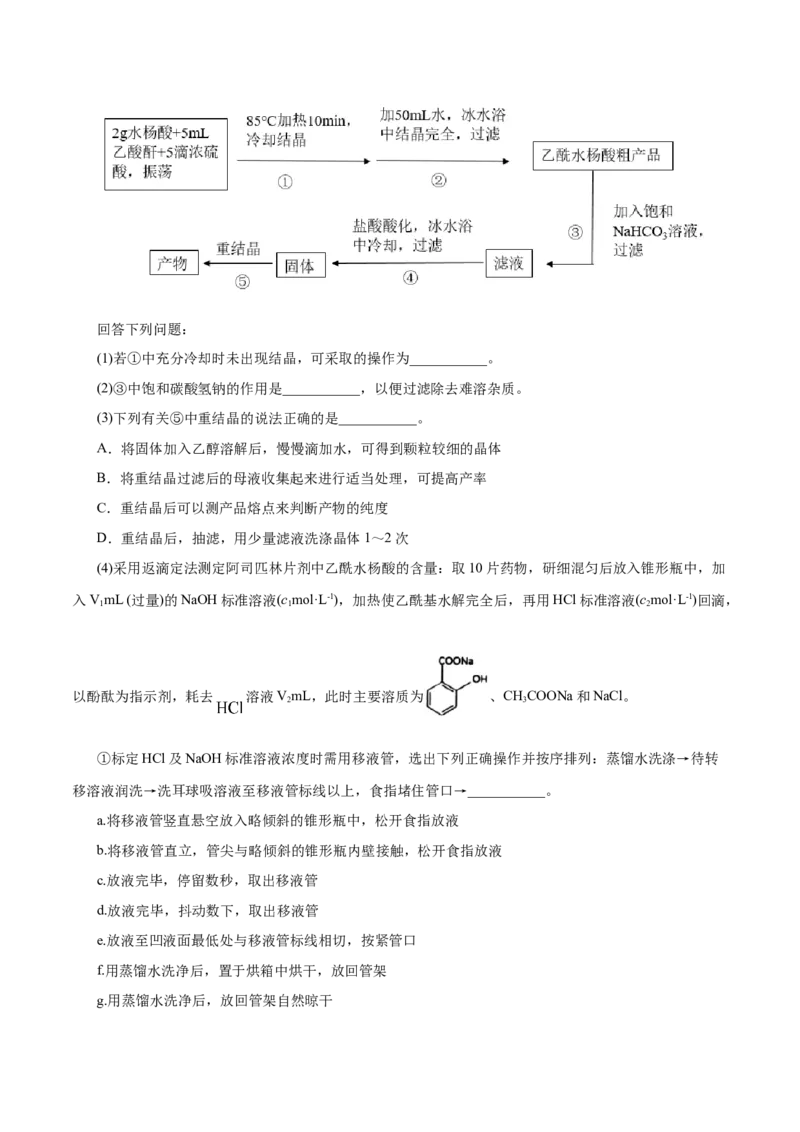
采用银量法测定氯,用NH SCN标准溶液滴定过量的AgNO ,发生反应Ag++SCN-=AgSCN↓,实验示
4 3
意图如下。
(聚乙烯醇的作用是阻止AgCl与AgSCN的转化)
①滴定时,可选用NH Fe(SO ) 作为指示剂,到达滴定终点的现象为_____。
4 4 2
②重复实验操作三次,消耗NH SCN溶液体积平均为12.50mL。则称取的样品中n(Cl−)为_____mol。
4
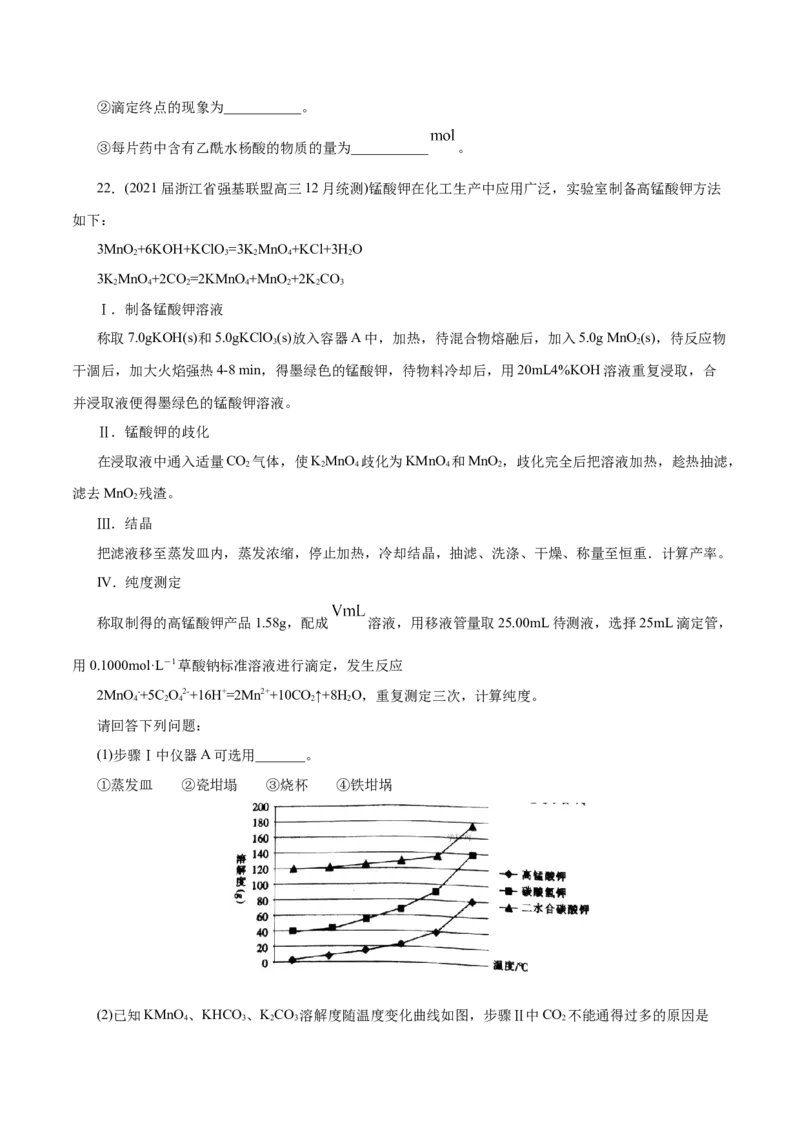
21.(2021届浙江省名校新高考研究联盟高三第二次联考)乙酰水杨酸(阿司匹林)是常用药物之一、实验
室通过水杨酸制备阿司匹林( )的实验过程如下:回答下列问题:
(1)若①中充分冷却时未出现结晶,可采取的操作为___________。
(2)③中饱和碳酸氢钠的作用是___________,以便过滤除去难溶杂质。
(3)下列有关⑤中重结晶的说法正确的是___________。
A.将固体加入乙醇溶解后,慢慢滴加水,可得到颗粒较细的晶体
B.将重结晶过滤后的母液收集起来进行适当处理,可提高产率
C.重结晶后可以测产品熔点来判断产物的纯度
D.重结晶后,抽滤,用少量滤液洗涤晶体1~2次
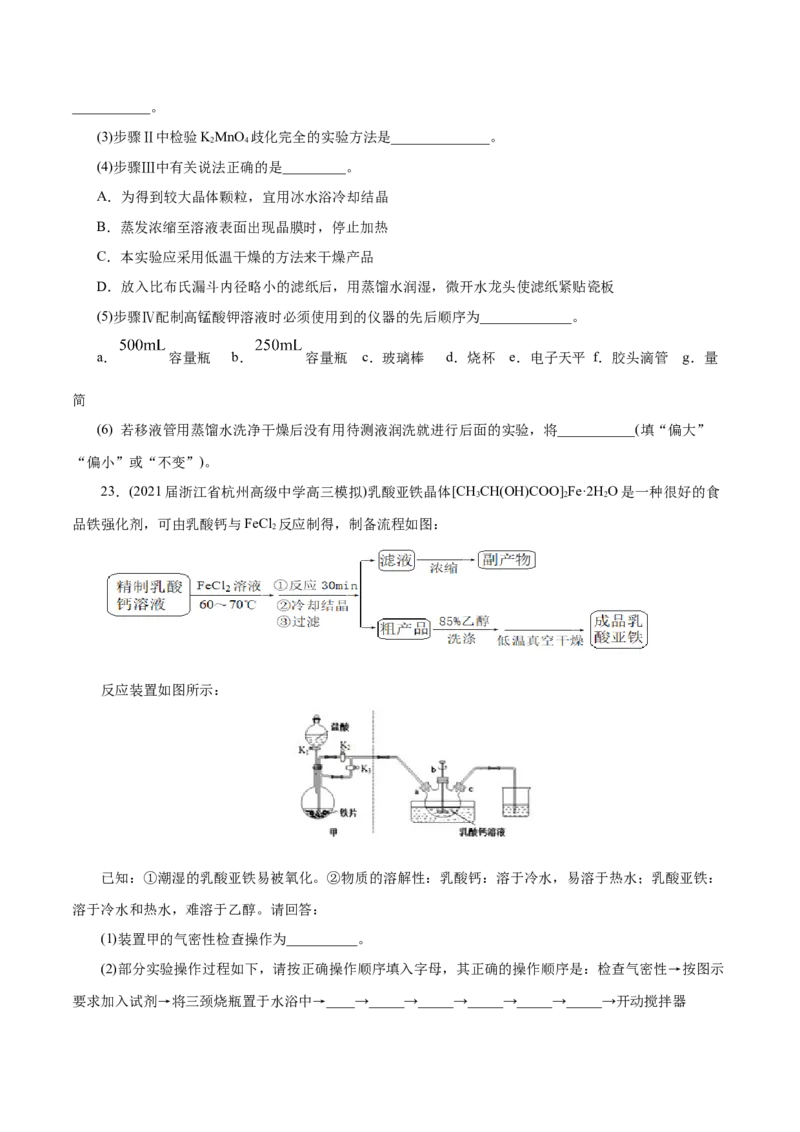
(4)采用返滴定法测定阿司匹林片剂中乙酰水杨酸的含量:取10片药物,研细混匀后放入锥形瓶中,加
入VmL (过量)的NaOH标准溶液(cmol·L-1),加热使乙酰基水解完全后,再用HCl标准溶液(cmol·L-1)回滴,
1 1 2
以酚酞为指示剂,耗去 溶液VmL,此时主要溶质为 、CHCOONa和NaCl。
2 3
①标定HCl及NaOH标准溶液浓度时需用移液管,选出下列正确操作并按序排列:蒸馏水洗涤→待转
移溶液润洗→洗耳球吸溶液至移液管标线以上,食指堵住管口→___________。
a.将移液管竖直悬空放入略倾斜的锥形瓶中,松开食指放液
b.将移液管直立,管尖与略倾斜的锥形瓶内壁接触,松开食指放液
c.放液完毕,停留数秒,取出移液管
d.放液完毕,抖动数下,取出移液管
e.放液至凹液面最低处与移液管标线相切,按紧管口
f.用蒸馏水洗净后,置于烘箱中烘干,放回管架
g.用蒸馏水洗净后,放回管架自然晾干②滴定终点的现象为___________。
③每片药中含有乙酰水杨酸的物质的量为___________ 。
22.(2021届浙江省强基联盟高三12月统测)锰酸钾在化工生产中应用广泛,实验室制备高锰酸钾方法
如下:
3MnO +6KOH+KClO =3K MnO +KCl+3H O
2 3 2 4 2
3KMnO +2CO =2KMnO +MnO+2K CO
2 4 2 4 2 2 3
Ⅰ.制备锰酸钾溶液
称取7.0gKOH(s)和5.0gKClO (s)放入容器A中,加热,待混合物熔融后,加入5.0g MnO (s),待反应物
3 2
干涸后,加大火焰强热4-8 min,得墨绿色的锰酸钾,待物料冷却后,用20mL4%KOH溶液重复浸取,合
并浸取液便得墨绿色的锰酸钾溶液。
Ⅱ.锰酸钾的歧化
在浸取液中通入适量CO 气体,使KMnO 歧化为KMnO 和MnO ,歧化完全后把溶液加热,趁热抽滤,
2 2 4 4 2
滤去MnO 残渣。
2
Ⅲ.结晶
把滤液移至蒸发皿内,蒸发浓缩,停止加热,冷却结晶,抽滤、洗涤、干燥、称量至恒重.计算产率。
IV.纯度测定
称取制得的高锰酸钾产品1.58g,配成 溶液,用移液管量取25.00mL待测液,选择25mL滴定管,
用0.1000mol·L-1草酸钠标准溶液进行滴定,发生反应
2MnO -+5C O2-+16H+=2Mn2++10CO ↑+8H O,重复测定三次,计算纯度。
4 2 4 2 2
请回答下列问题:
(1)步骤Ⅰ中仪器A可选用_______。
①蒸发皿 ②瓷坩塌 ③烧杯 ④铁坩埚
(2)已知KMnO 、KHCO 、KCO 溶解度随温度变化曲线如图,步骤Ⅱ中CO 不能通得过多的原因是
4 3 2 3 2___________。
(3)步骤Ⅱ中检验KMnO 歧化完全的实验方法是______________。
2 4
(4)步骤Ⅲ中有关说法正确的是_________。
A.为得到较大晶体颗粒,宜用冰水浴冷却结晶
B.蒸发浓缩至溶液表面出现晶膜时,停止加热
C.本实验应采用低温干燥的方法来干燥产品
D.放入比布氏漏斗内径略小的滤纸后,用蒸馏水润湿,微开水龙头使滤纸紧贴瓷板
(5)步骤Ⅳ配制高锰酸钾溶液时必须使用到的仪器的先后顺序为_____________。
a. 容量瓶 b. 容量瓶 c.玻璃棒 d.烧杯 e.电子天平 f.胶头滴管 g.量
简
(6) 若移液管用蒸馏水洗净干燥后没有用待测液润洗就进行后面的实验,将___________(填“偏大”
“偏小”或“不变”)。
23.(2021届浙江省杭州高级中学高三模拟)乳酸亚铁晶体[CHCH(OH)COO] Fe·2H O是一种很好的食
3 2 2
品铁强化剂,可由乳酸钙与FeCl 反应制得,制备流程如图:
2
反应装置如图所示:
已知:①潮湿的乳酸亚铁易被氧化。②物质的溶解性:乳酸钙:溶于冷水,易溶于热水;乳酸亚铁:
溶于冷水和热水,难溶于乙醇。请回答:
(1)装置甲的气密性检查操作为__________。
(2)部分实验操作过程如下,请按正确操作顺序填入字母,其正确的操作顺序是:检查气密性→按图示
要求加入试剂→将三颈烧瓶置于水浴中→____→_____→_____→_____→_____→_____→开动搅拌器→……
a.关闭K; b.盖上分液漏斗上口玻璃塞; c.关闭K,打开K; d.关闭K,打开K;
1 3 2 2 3
e.打开分液漏斗上口玻璃塞; f打开K
1
(3)该装置制备乳酸亚铁的优点是__________副产物为__________
(4)下列说法正确的是__________
A.装置甲中的主要仪器是球形分液漏斗和蒸馏烧瓶
B.本实验采用较大铁片而不是铁粉的主要原因是控制反应速率,防止进入三颈烧瓶的氯化亚铁过多,
反应过于剧烈
C.乳酸亚铁悬浊液应从b口倒出进行抽滤,并用滤液洗涤三颈烧瓶,将洗涤液倒入布氏漏斗再次抽
滤
D.粗产品的洗涤液,经蒸馏后所得的残留液,与滤液混合可提高副产物的产量
(5)有同学提出可直接用KMnO 滴定法测定样品中的Fe2+量进而计算纯度,但实验后发现结果总是大于
4
100%,其主要原因可能是_________
24.(2021届浙江省十校联盟高三联考)连二亚硫酸钠(Na SO)俗称保险粉,可以用作染色工艺的还原
2 2 4
剂,纸浆、肥皂等的漂白剂。NaSO 易溶于水,难溶于甲醇,在碱性介质中较稳定,在潮湿空气中易被氧
2 2 4
化生成两种常见的酸式盐。锌粉法制备NaSO 的工艺流程如图所示:
2 2 4
回答下列问题:
(1)若用NaSO 固体和某酸反应制备SO 气体,你认为下列最适宣选用的酸是_______。
2 3 2
A.浓盐酸 B.质量分数为70%的HSO
2 4
C.稀硝酸 D.质量分数为10%的稀硫酸
(2)在步骤Ⅲ中加入固体NaCl的作用是________________________;
(3)保险粉在潮湿空气中被氧化的化学方程式_________________________。
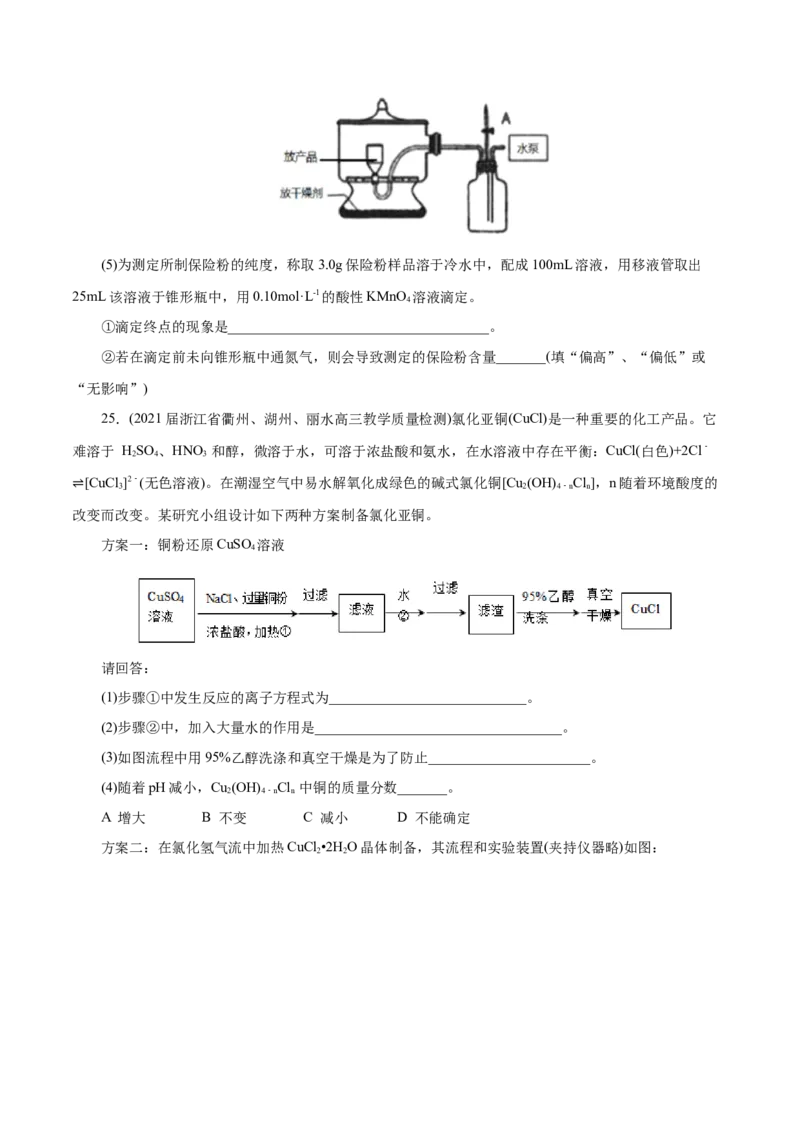
(4)后续处理得到保险粉产品的过程中
①洗涤步骤可能需要用到以下操作:a.加入水至浸没沉淀物;b.加入甲醇至浸没沉淀物; c.洗涤剂缓
慢通过沉淀物;d.洗涤剂快速通过;e.关小水龙头;f.开大水龙头;g.重复2-3次。请选出正确的操作并排
序____→____→____→g→____
②干燥步骤如图所示,选用此装置的目的是______________________________。(5)为测定所制保险粉的纯度,称取3.0g保险粉样品溶于冷水中,配成100mL溶液,用移液管取出
25mL该溶液于锥形瓶中,用0.10mol·L-1的酸性KMnO 溶液滴定。
4
①滴定终点的现象是_____________________________________。
②若在滴定前未向锥形瓶中通氮气,则会导致测定的保险粉含量_______(填“偏高”、“偏低”或
“无影响”)
25.(2021届浙江省衢州、湖州、丽水高三教学质量检测)氯化亚铜(CuCl)是一种重要的化工产品。它
难溶于 HSO 、HNO 和醇,微溶于水,可溶于浓盐酸和氨水,在水溶液中存在平衡:CuCl(白色)+2Cl﹣
2 4 3
[CuCl ]2﹣(无色溶液)。在潮湿空气中易水解氧化成绿色的碱式氯化铜[Cu (OH) Cl],n随着环境酸度的
3 2 4﹣n n
⇌改变而改变。某研究小组设计如下两种方案制备氯化亚铜。
方案一:铜粉还原CuSO 溶液
4
请回答:
(1)步骤①中发生反应的离子方程式为____________________________。
(2)步骤②中,加入大量水的作用是___________________________________。
(3)如图流程中用95%乙醇洗涤和真空干燥是为了防止_______________________。
(4)随着pH减小,Cu (OH) Cl 中铜的质量分数_______。
2 4﹣n n
A 增大 B 不变 C 减小 D 不能确定
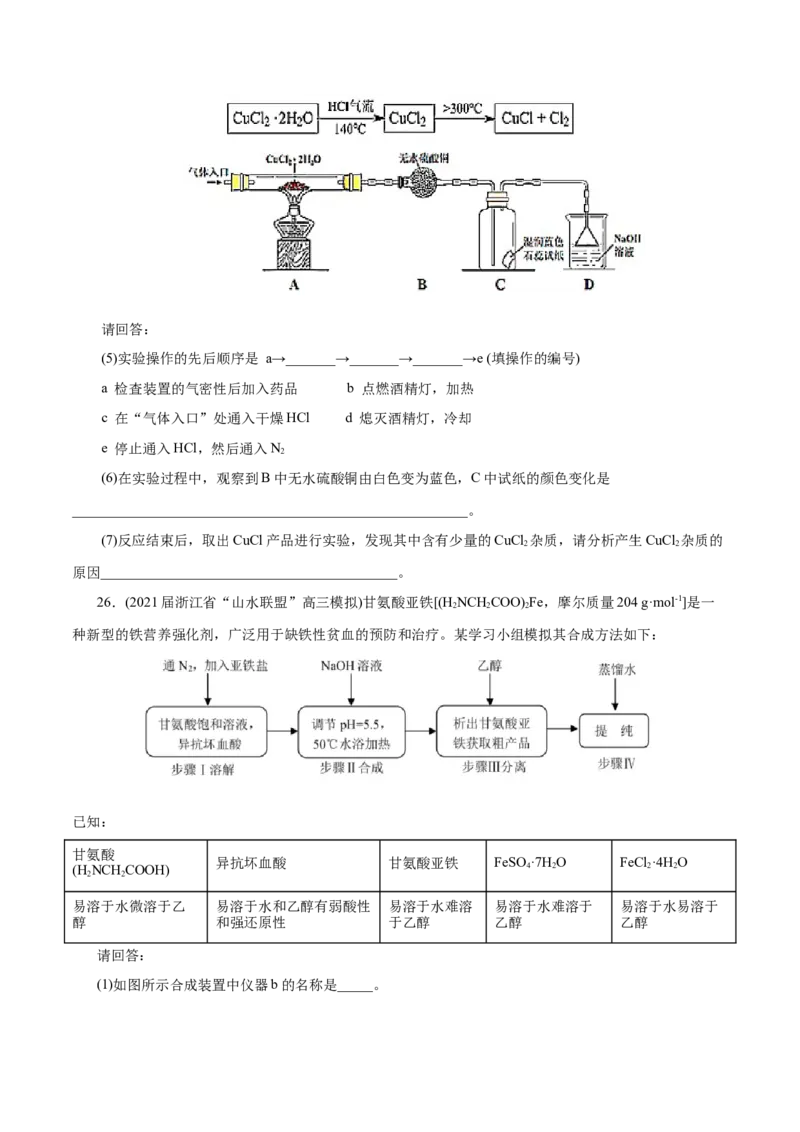
方案二:在氯化氢气流中加热CuCl •2H O晶体制备,其流程和实验装置(夹持仪器略)如图:
2 2请回答:
(5)实验操作的先后顺序是 a→_______→_______→_______→e (填操作的编号)
a 检査装置的气密性后加入药品 b 点燃酒精灯,加热
c 在“气体入口”处通入干燥HCl d 熄灭酒精灯,冷却
e 停止通入HCl,然后通入N
2
(6)在实验过程中,观察到B中无水硫酸铜由白色变为蓝色,C中试纸的颜色变化是
________________________________________________________。
(7)反应结束后,取出CuCl产品进行实验,发现其中含有少量的CuCl 杂质,请分析产生CuCl 杂质的
2 2
原因__________________________________________。
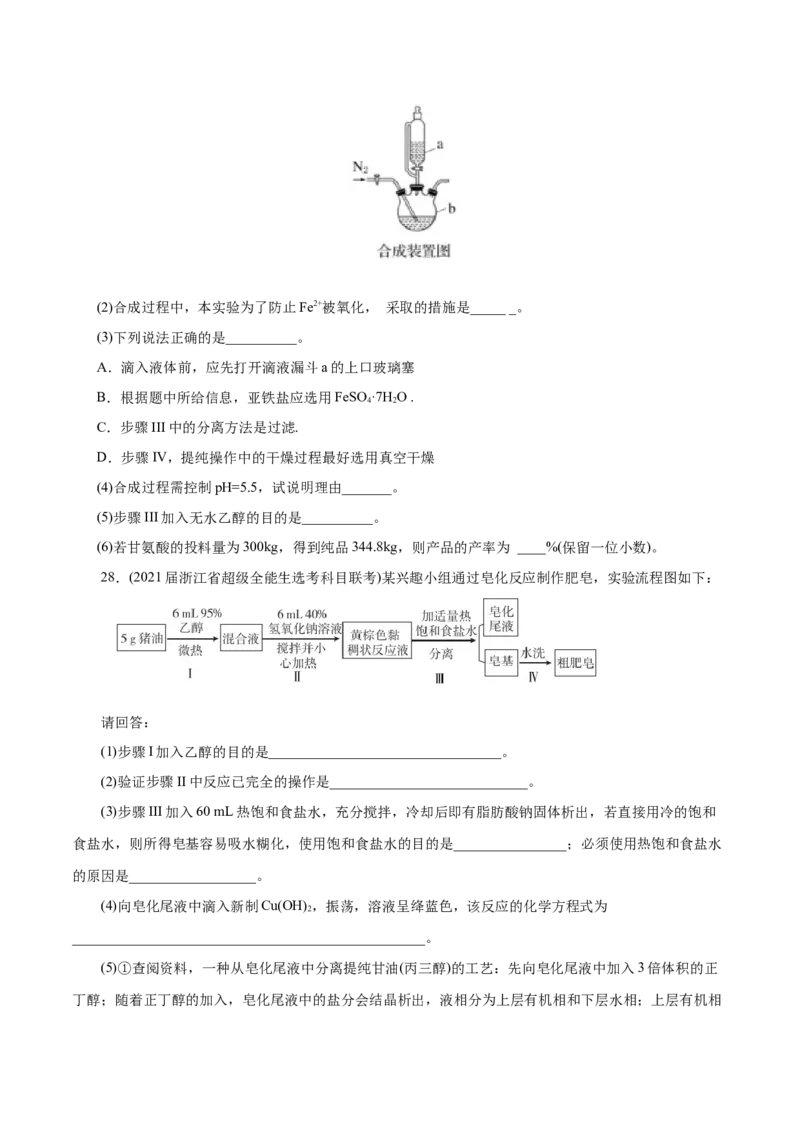
26.(2021届浙江省“山水联盟”高三模拟)甘氨酸亚铁[(H NCH COO) Fe,摩尔质量204 g·mol-1]是一
2 2 2
种新型的铁营养强化剂,广泛用于缺铁性贫血的预防和治疗。某学习小组模拟其合成方法如下:
已知:
甘氨酸
异抗坏血酸 甘氨酸亚铁 FeSO ·7H O FeCl ·4H O
(H NCH COOH) 4 2 2 2
2 2
易溶于水微溶于乙 易溶于水和乙醇有弱酸性 易溶于水难溶 易溶于水难溶于 易溶于水易溶于
醇 和强还原性 于乙醇 乙醇 乙醇
请回答:
(1)如图所示合成装置中仪器b的名称是_____。(2)合成过程中,本实验为了防止Fe2+被氧化, 采取的措施是_____ _。
(3)下列说法正确的是__________。
A.滴入液体前,应先打开滴液漏斗a的上口玻璃塞
B.根据题中所给信息,亚铁盐应选用FeSO ·7H O .
4 2
C.步骤III中的分离方法是过滤.
D.步骤IV,提纯操作中的干燥过程最好选用真空干燥
(4)合成过程需控制pH=5.5,试说明理由_______。
(5)步骤III加入无水乙醇的目的是__________。
(6)若甘氨酸的投料量为300kg,得到纯品344.8kg,则产品的产率为 ____%(保留一位小数)。
28.(2021届浙江省超级全能生选考科目联考)某兴趣小组通过皂化反应制作肥皂,实验流程图如下:
请回答:
(1)步骤I加入乙醇的目的是_________________________________。
(2)验证步骤II中反应已完全的操作是____________________________。
(3)步骤III加入60 mL热饱和食盐水,充分搅拌,冷却后即有脂肪酸钠固体析出,若直接用冷的饱和
食盐水,则所得皂基容易吸水糊化,使用饱和食盐水的目的是________________;必须使用热饱和食盐水
的原因是__________________。
(4)向皂化尾液中滴入新制Cu(OH) ,振荡,溶液呈绛蓝色,该反应的化学方程式为
2
__________________________________________________。
(5)①查阅资料,一种从皂化尾液中分离提纯甘油(丙三醇)的工艺:先向皂化尾液中加入3倍体积的正
丁醇;随着正丁醇的加入,皂化尾液中的盐分会结晶析出,液相分为上层有机相和下层水相;上层有机相经过精馏(一种蒸馏方法),回收正丁醇,同时除去水,并得到高纯度甘油;下层水相过滤,滤液回流至萃
取塔内再处理,结晶的氯化钠洗涤回收。
下列说法正确的是__________。
A.正丁醇与水可以任意比例互溶 B.氯化钠在正丁醇中溶解度小
C.分层后甘油全在有机相,水相中没有残留 D.正丁醇的沸点低于甘油
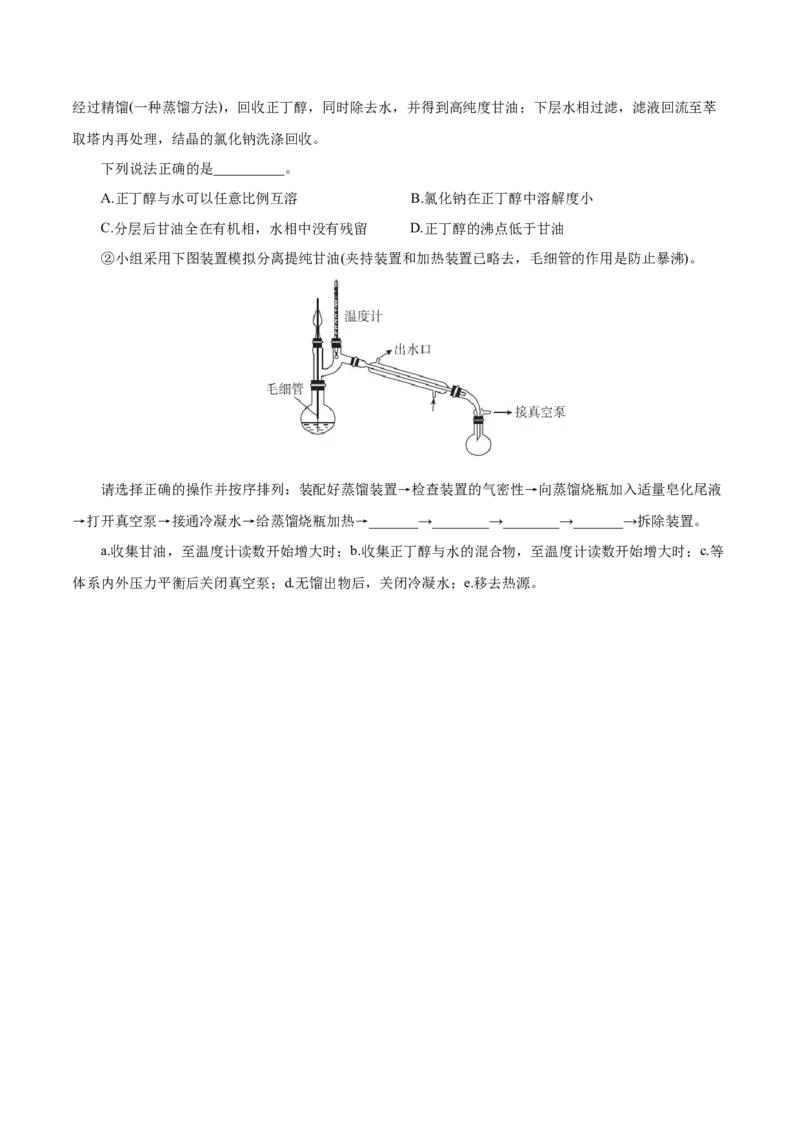
②小组采用下图装置模拟分离提纯甘油(夹持装置和加热装置已略去,毛细管的作用是防止暴沸)。
请选择正确的操作并按序排列:装配好蒸馏装置→检查装置的气密性→向蒸馏烧瓶加入适量皂化尾液
→打开真空泵→接通冷凝水→给蒸馏烧瓶加热→_______→________→________→_______→拆除装置。
a.收集甘油,至温度计读数开始增大时;b.收集正丁醇与水的混合物,至温度计读数开始增大时;c.等
体系内外压力平衡后关闭真空泵;d.无馏出物后,关闭冷凝水;e.移去热源。