文档内容
西安市铁一中学 2022-2023 学年上学期期末
高三化学
注意事项:
1.答题时,务必将自己的姓名、班级、准考证号填写在答题卡规定的位置上。
2.答选择题时,用2B铅笔将答题卡上对应的答案标号涂黑。如需改动,用橡皮擦
干净后,再选涂其他答案标号。
3.答非选择题时,必须使用0.5毫米黑色黑色签字笔把答案写在答题卡规定的位
置上。答案如需改正,请先划掉原来的答案,再写上新答案,不准使用涂改液、
胶带纸、修正带。
4.考试结束后,只将答题卡交回。
一、选择题:(本题共 23小题,每题2分,共46分.在每小题给出的四个
选项中,只有一项是符合题目要求的).
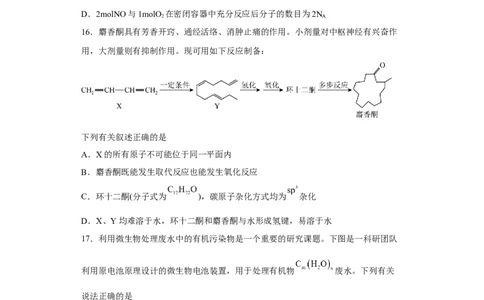
1.下列有关物质性质的叙述正确的是
A.常温下,过量Fe与浓HNO 反应生成Fe(NO )
3 3 2
B.晶体硅的硬度大,可用于制作光电板
C.BaSO 在医疗上可用作“钡餐”
4
D.溴化银具有感光性,可用于人工降雨
2.下列分子中所有原子都满足最外层为8电子结构的是
① ② ③ ④ ⑤ ⑥ ⑦ ⑧ ⑨ ⑩
A.②④⑦⑧⑩ B.②③④⑦⑨⑩ C.①③④⑦⑩ D.③④⑤⑦⑨⑩
3.有下列几种有机物.
(1)CHCOOCH (2)CH=CHCHCl
3 3 2 2
(3)CH=CH—CHO
2
其中既能发生水解反应,又能发生加聚反应的是
A.(1)与(4) B.(2)与(3) C.(2)与(4) D.(1)、(3)和(4)
4.用如图表示的一些物质或概念间的从属关系中不正确的是:
X Y Z例 氧化物 化合物 纯净物
A 苯的同系物 芳香烃 芳香族化合物
B 胶体 分散系 混合物
C 电解质 离子化合物 化合物
D 碱性氧化物 金属氧化物 氧化物
A.A B.B C.C D.D
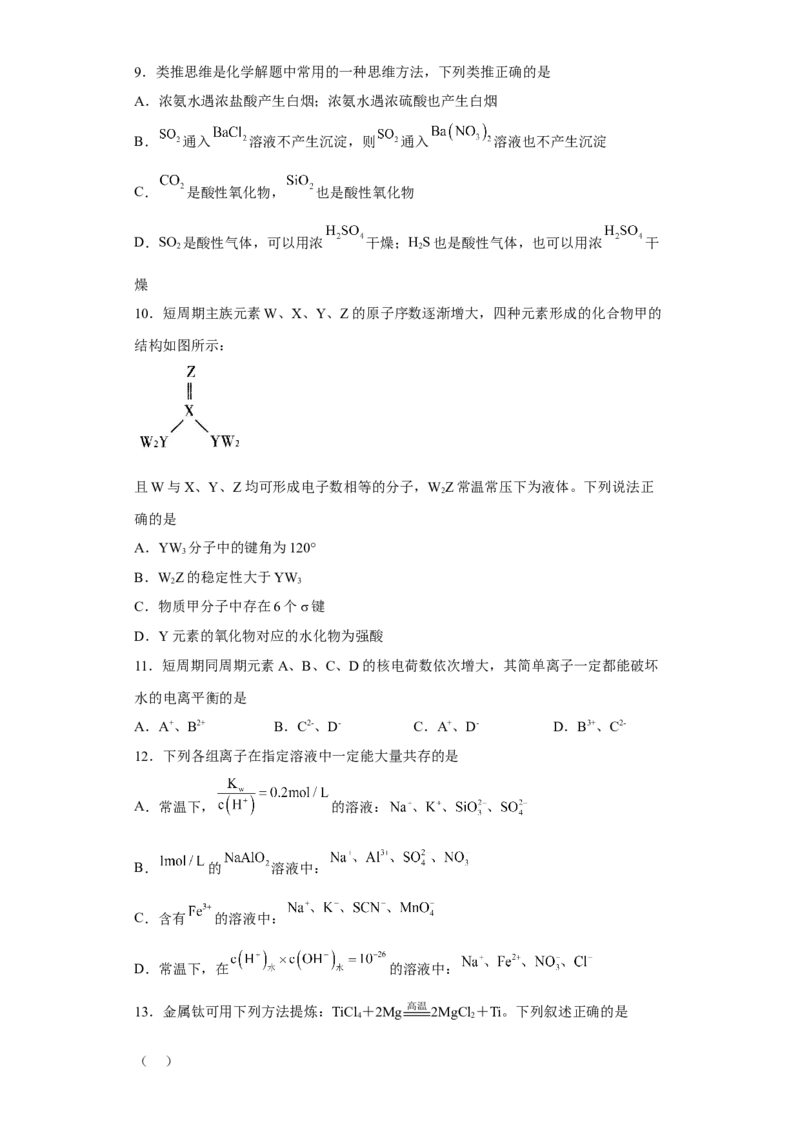
5.室温下,大小相同的A、B两集气瓶中,分别装有0.01mol氨气和0.01mol氯化氢,
抽去如图所示装置中的玻璃片,使两种气体充分反应。下列说法正确的是
A.抽去玻璃片后,集气瓶内出现白烟
B.气体反应物的总体积为0.448L
C.抽去玻璃片前,A、B中气体密度比为36.5:17
D.该反应发生过程中,同时有极性共价键和非极性共价键的断裂和生成
6.下列氯化物中,既能由金属和氯气直接化合制得,又能由金属和盐酸反应制得的是
( )
①CuCl ②FeCl ③MgCl ④ZnCl
2 2 2 2
A.③④ B.②③ C.②③④ D.①②③④
7.下列操作不能区别浓硫酸与稀硫酸的是
A.分别加入铁 B.分别加入蔗糖
C.分别加入氨气 D.分别加入铜片、加热
8.在某无色透明的酸性溶液中,能大量共存的离子组是
A.Na+、K+、SO 、OH-
B.Cu2+、K+、Cl-、NO
C.Cl-、K+、Na+、NO
D.Ag+、K+、SO 、Cl-9.类推思维是化学解题中常用的一种思维方法,下列类推正确的是
A.浓氨水遇浓盐酸产生白烟;浓氨水遇浓硫酸也产生白烟
B. 通入 溶液不产生沉淀,则 通入 溶液也不产生沉淀
C. 是酸性氧化物, 也是酸性氧化物
D.SO 是酸性气体,可以用浓 干燥;HS也是酸性气体,也可以用浓 干
2 2
燥
10.短周期主族元素W、X、Y、Z的原子序数逐渐增大,四种元素形成的化合物甲的
结构如图所示:
且W与X、Y、Z均可形成电子数相等的分子,WZ常温常压下为液体。下列说法正
2
确的是
A.YW 分子中的键角为120°
3
B.WZ的稳定性大于YW
2 3
C.物质甲分子中存在6个σ键
D.Y元素的氧化物对应的水化物为强酸
11.短周期同周期元素A、B、C、D的核电荷数依次增大,其简单离子一定都能破坏
水的电离平衡的是
A.A+、B2+ B.C2-、D- C.A+、D- D.B3+、C2-
12.下列各组离子在指定溶液中一定能大量共存的是
A.常温下, 的溶液:
B. 的 溶液中:
C.含有 的溶液中:
D.常温下,在 的溶液中:
13.金属钛可用下列方法提炼:TiCl +2Mg 2MgCl +Ti。下列叙述正确的是
4 2
( )A.该反应属于复分解反应 B.该反应中镁元素被氧化
C.该反应中Ti是还原剂 D.该反应中TiCl 发生了氧化反应
4
14.NaOH溶于水时,扩散过程吸收了a kJ的热量,水合过程放出了b kJ的热量。下
列判断正确的是
A.a>b B.a=b C.aHA>HB
C.当通入0.1molHCl气体时,c(B-)>c(A-)
D.当混合溶液呈中性时,c(Na+)=c(Cl-)+c(A-)+c(B-)
二、填空题:54分
24.右图中电极a、b为Fe物件和Ag片,电极c、d都是石墨电极。通电一段时间后,
在c、d两极上共收集到336ml(标准状况)气体。回答:
(1)直流电源中,M为_________________极。
(2)欲在Fe物件上镀上一薄层Ag,①Fe物件应为_________极,(填a或b)
②Fe物件增重_________g。
(3)X溶液为____________,其浓度____________,(填“增大”“减小”或“不变”)
(4)若NaOH溶液的质量分数由5.00%变为5.02%,列式计算原NaOH溶液的质量。
25.氯乙烯是制备塑料的重要中间体,可通过乙炔选择性催化制备。已知:
I.
II.
(1) 正反应的活化能为25.8KJ/mol,则其逆反应
的活化能为_______。
(2)在体积可变的密闭容器中以物质的量之比为1:1充入C H(g)和HCl(g),分别在不
2 2
同压强下发生反应,实验测得乙炔的平衡转化率与温度的关系如图所示。P、P、P 由
1 2 3
大到小的顺序为_______,判断的理由是_______。
(3)一定温度下,向盛放催化剂的恒容密闭容器中以物质的量之比为1:1充入C H(g)
2 2
和HCl(g),假设只发生反应I和II。实验测得反应前容器内压强为pPa,5min达到平
0
衡时C HCl(g)、HCl(g)的分压分别为pPa、pPa。
2 4 2 1 2
①0~5min内,反应I和反应II中HCl的总的消耗速率v(HCl)=_______ 。
②反应II的平衡常数K=_______(用含P、P、P 的代数式表示)。
p 0 1 2
(4)电化学腐蚀法可有效将废水中的三氯乙烯转化为乙烯。利用活性纳米Fe电化学腐蚀
处理酸性三氯乙烯(C HCl )废水的过程如图。定义单位时间内纳米Fe释放的总电子的
2 3
物质的量为n,其中用于有效腐蚀的电子的物质的量为n。
t e①上述电化学腐蚀过程①的电极反应为_______。
②在处理过程中,当消耗amol纳米Fe时,产生bL的乙烯气体(标准状况),则该电化
学腐蚀过程的电流效率η=_______(用含a、b的代数式表示)。[已知: ]
四、工业流程题
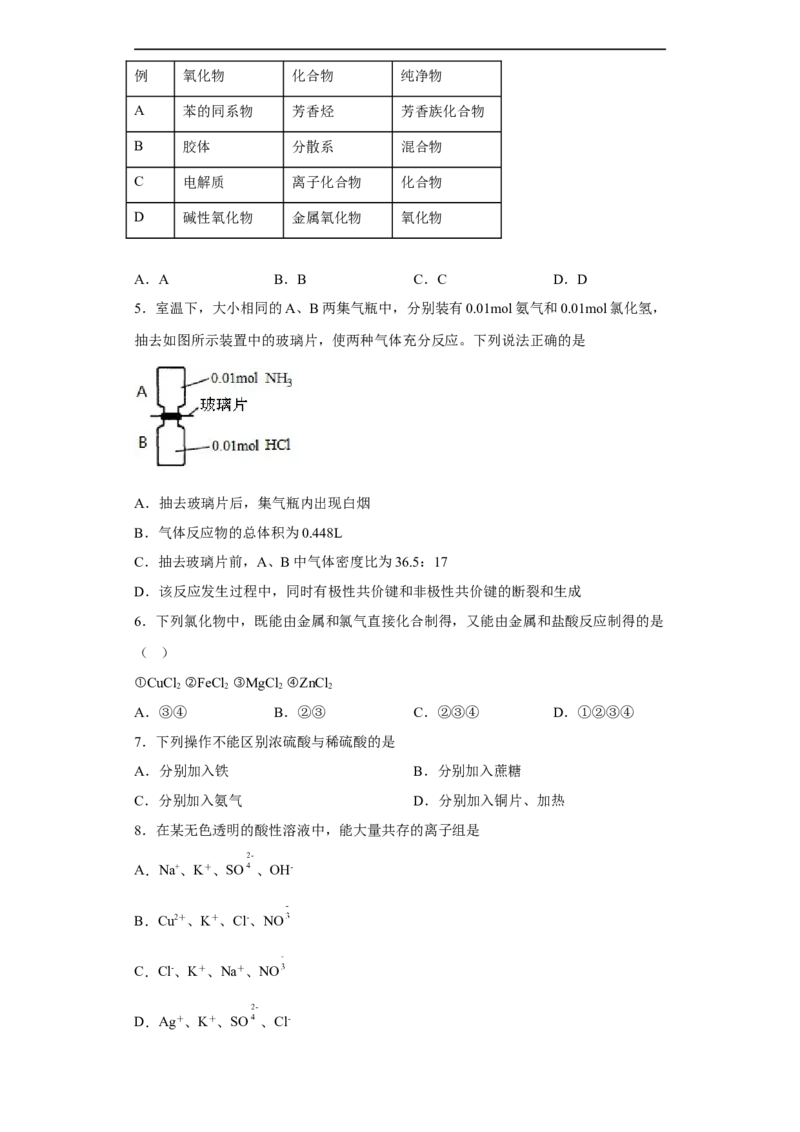
26.聚合硫酸铁(PFS)是一种高效的无机高分子絮凝剂。某工厂利用经浮选的硫铁矿烧
渣(有效成分为Fe2O3 和Fe3O4)制备PFS,其工艺流程如下图所示。
(1)还原焙烧过程中,CO还原Fe3O4生成FeO的热化学方程式为
________________________。
已知: Fe3O4(s)+C(s)= 3FeO(s)+CO(g) ΔH1=+191.9kJ·mol-1
C(s)+O2(g)=CO2(g) ΔH2=-393.5kJ·mol-1
C(s)+CO2(g)=2CO(g) ΔH3=+172.5kJ·mol-1
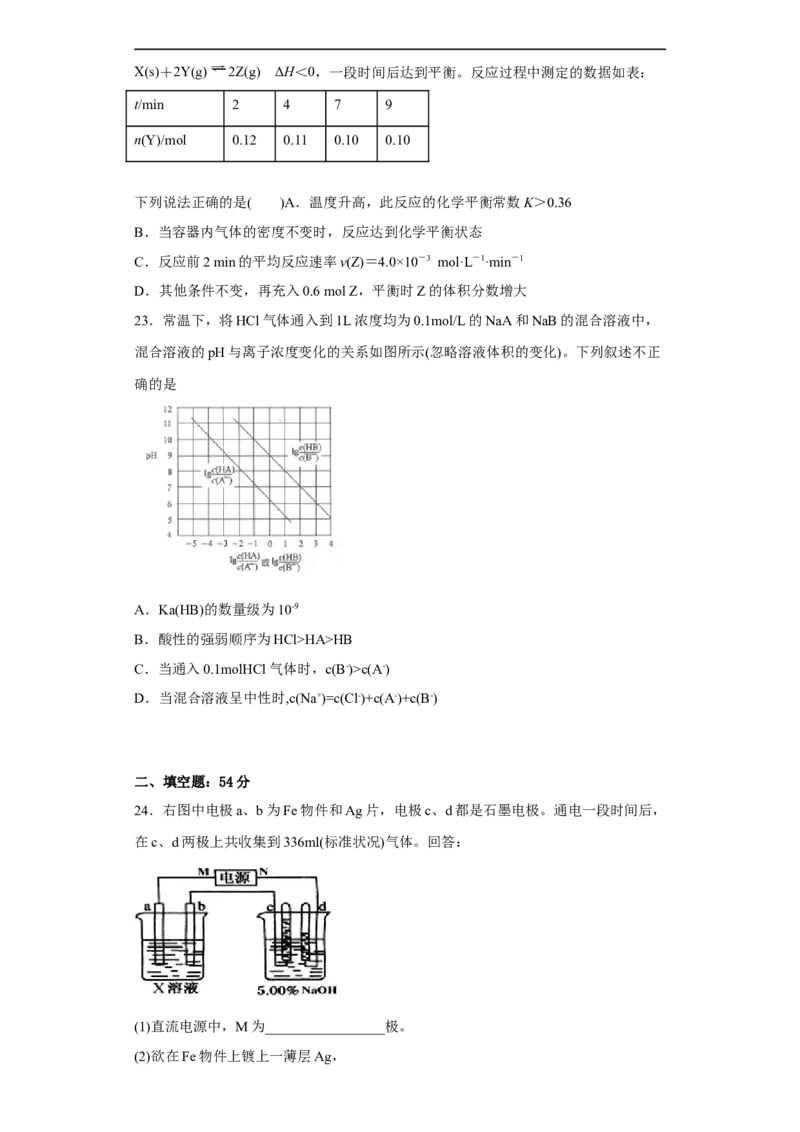
(2)CO是还原焙烧过程的主要还原剂。下图中,曲线表示4个化学反应a、b、c、d
达到平衡时气相组成和温度的关系,I、Ⅱ、Ⅲ、Ⅳ分别是Fe2O3、Fe3O4、FeO、Fe
稳定存在的区域。a属于_________(填“吸热反应”或“放热反应”);570℃时,d
反应的平衡常数K= ____________。(3)工业上,还原焙烧的温度一般控制在800℃左右,温度不宜过高的理由是
___________________。
(4)若“酸浸”时间过长,浸出液中Fe2+含量反而降低,主要原因是
___________________________。
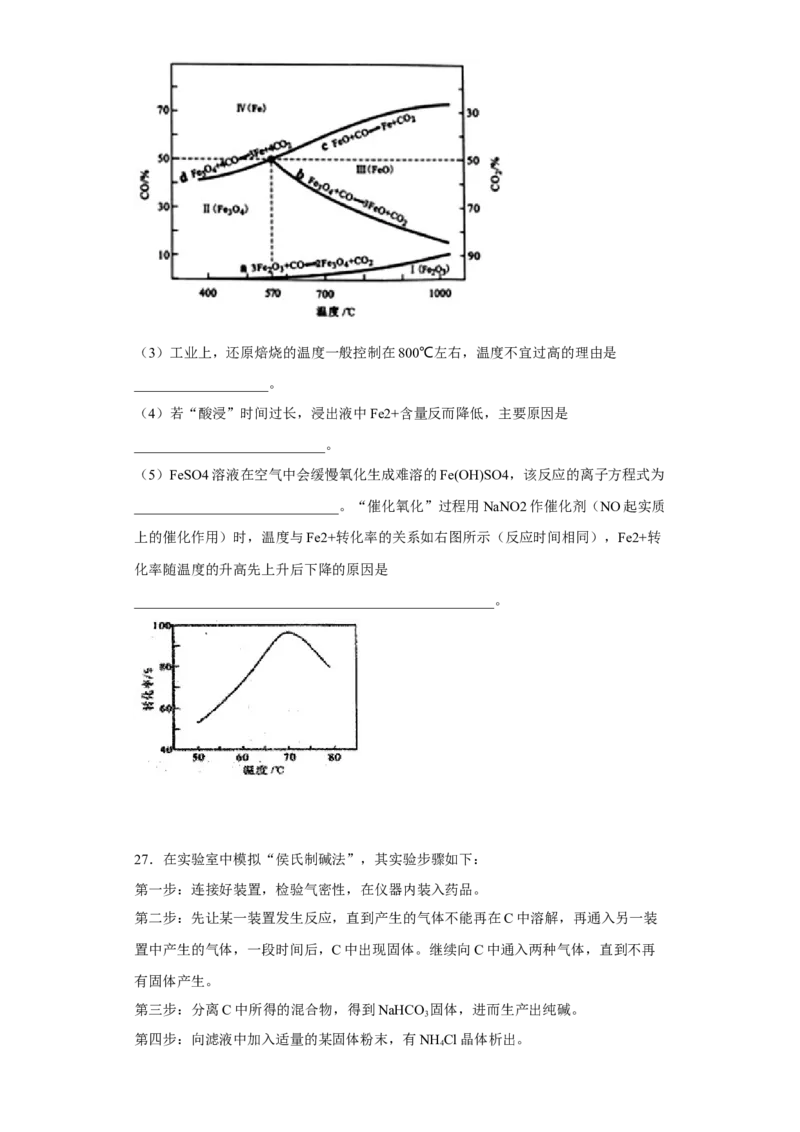
(5)FeSO4溶液在空气中会缓慢氧化生成难溶的Fe(OH)SO4,该反应的离子方程式为
_____________________________。“催化氧化”过程用NaNO2作催化剂(NO起实质
上的催化作用)时,温度与Fe2+转化率的关系如右图所示(反应时间相同),Fe2+转
化率随温度的升高先上升后下降的原因是
___________________________________________________。
27.在实验室中模拟“侯氏制碱法”,其实验步骤如下:
第一步:连接好装置,检验气密性,在仪器内装入药品。
第二步:先让某一装置发生反应,直到产生的气体不能再在C中溶解,再通入另一装
置中产生的气体,一段时间后,C中出现固体。继续向C中通入两种气体,直到不再
有固体产生。
第三步:分离C中所得的混合物,得到NaHCO 固体,进而生产出纯碱。
3
第四步:向滤液中加入适量的某固体粉末,有NH Cl晶体析出。
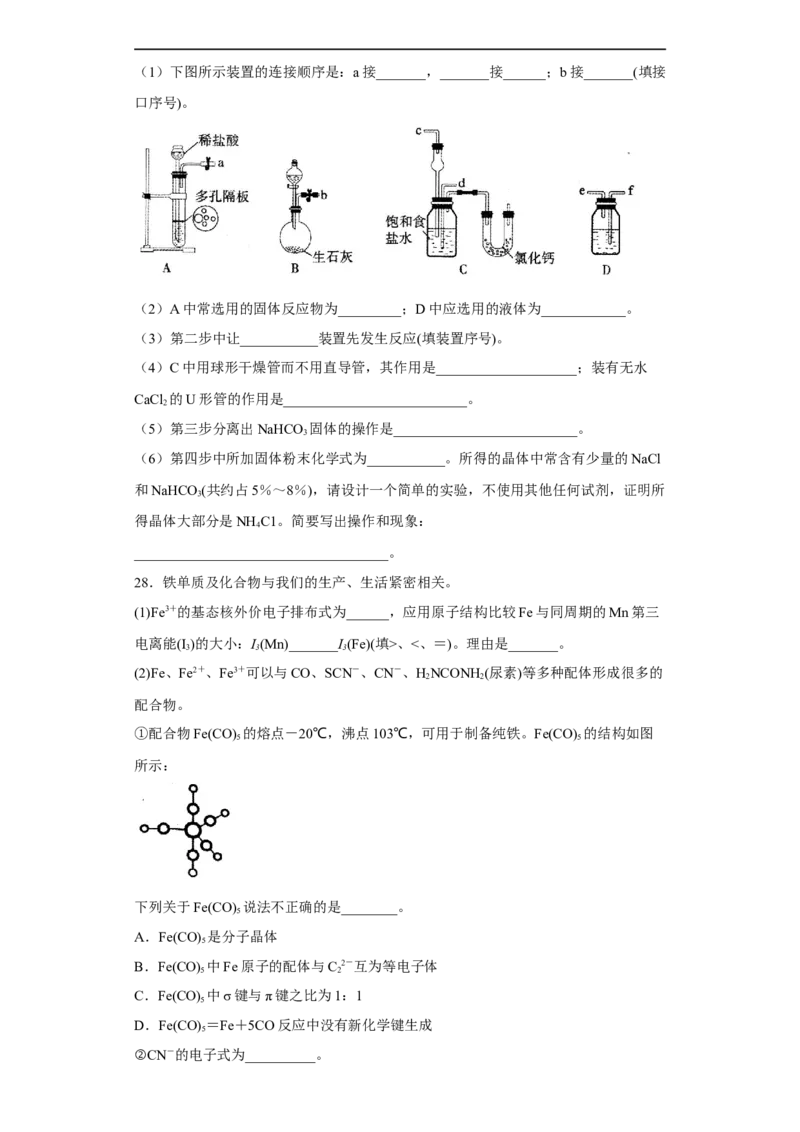
4(1)下图所示装置的连接顺序是:a接_______,_______接______;b接_______(填接
口序号)。
(2)A中常选用的固体反应物为_________;D中应选用的液体为____________。
(3)第二步中让___________装置先发生反应(填装置序号)。
(4)C中用球形干燥管而不用直导管,其作用是____________________;装有无水
CaCl 的U形管的作用是__________________________。
2
(5)第三步分离出NaHCO 固体的操作是__________________________。
3
(6)第四步中所加固体粉末化学式为___________。所得的晶体中常含有少量的NaCl
和NaHCO (共约占5%~8%),请设计一个简单的实验,不使用其他任何试剂,证明所
3
得晶体大部分是NH C1。简要写出操作和现象:
4
____________________________________。
28.铁单质及化合物与我们的生产、生活紧密相关。
(1)Fe3+的基态核外价电子排布式为______,应用原子结构比较Fe与同周期的Mn第三
电离能(I)的大小:I(Mn)_______I(Fe)(填>、<、=)。理由是_______。
3 3 3
(2)Fe、Fe2+、Fe3+可以与CO、SCN-、CN-、HNCONH(尿素)等多种配体形成很多的
2 2
配合物。
①配合物Fe(CO) 的熔点-20℃,沸点103℃,可用于制备纯铁。Fe(CO) 的结构如图
5 5
所示:
下列关于Fe(CO) 说法不正确的是________。
5
A.Fe(CO) 是分子晶体
5
B.Fe(CO) 中Fe原子的配体与C 2-互为等电子体
5 2
C.Fe(CO) 中σ键与π键之比为1:1
5
D.Fe(CO) =Fe+5CO反应中没有新化学键生成
5
②CN-的电子式为__________。③HNCONH(尿素)中N、C原子的杂化方式分别为__________、__________,
2 2
组成尿素的4种元素的第一电离能由大到小的顺序为__________,1 mol H NCONH(尿
2 2
素)分子中含有σ键的数目为__________。
(3)NaCl和MgO都属于离子化合物,NaCl的熔点为801.3C,MgO的熔点高达
2800℃。造成两种晶体熔点差距的主要原因是________。
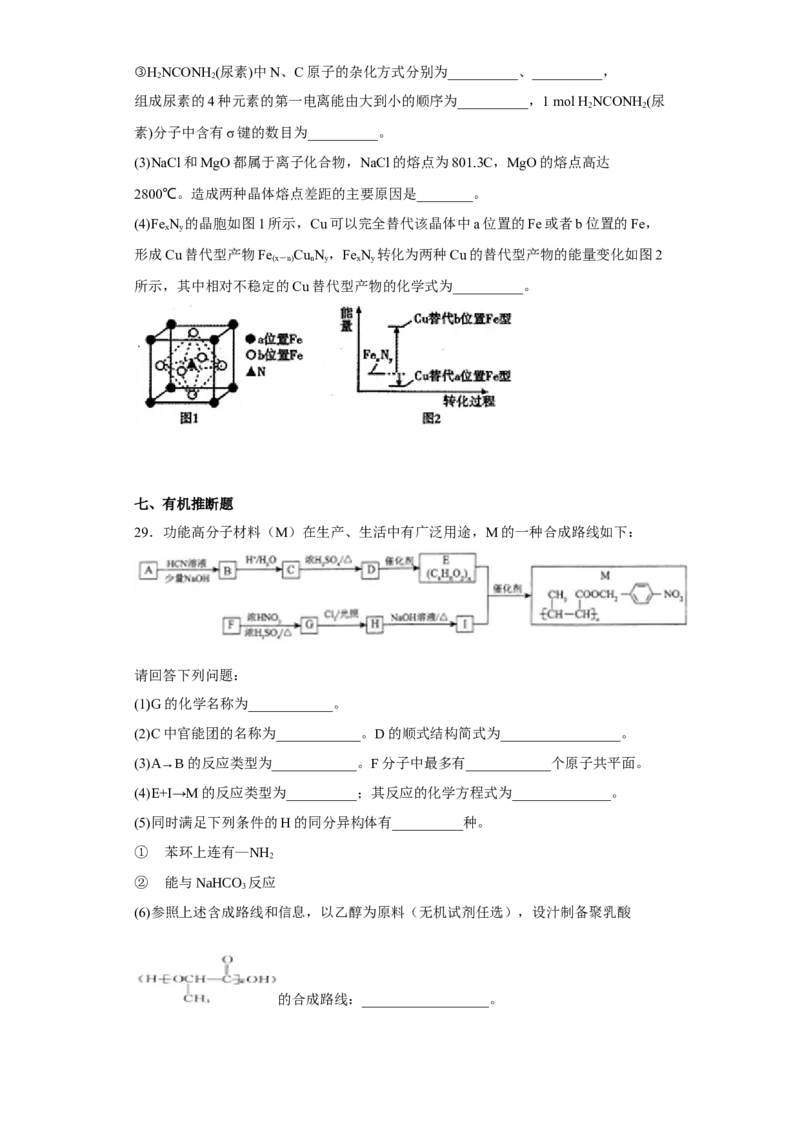
(4)Fe N 的晶胞如图1所示,Cu可以完全替代该晶体中a位置的Fe或者b位置的Fe,
x y
形成Cu替代型产物Fe Cu N,Fe N 转化为两种Cu的替代型产物的能量变化如图2
(x-n) n y x y
所示,其中相对不稳定的Cu替代型产物的化学式为__________。
七、有机推断题
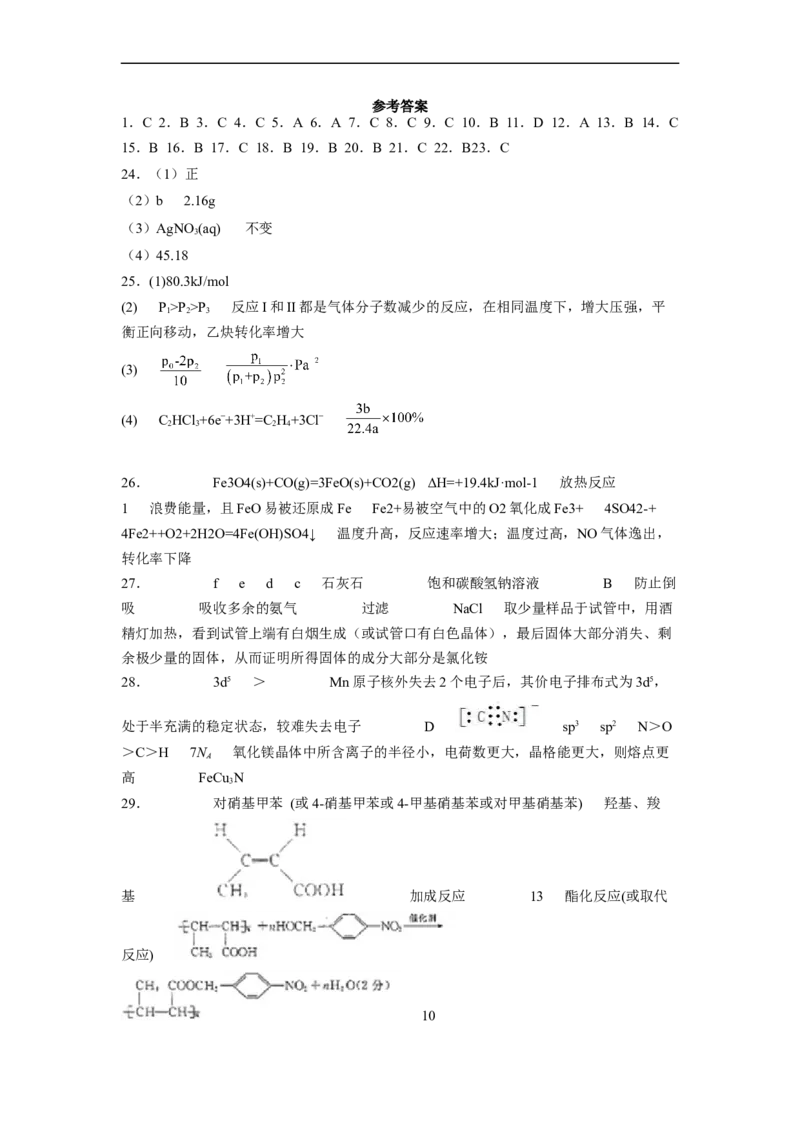
29.功能高分子材料(M)在生产、生活中有广泛用途,M的一种合成路线如下:
请回答下列问题:
(1)G的化学名称为____________。
(2)C中官能团的名称为____________。D的顺式结构简式为_________________。
(3)A→B的反应类型为____________。F分子中最多有____________个原子共平面。
(4)E+I→M的反应类型为__________;其反应的化学方程式为______________。
(5)同时满足下列条件的H的同分异构体有__________种。
① 苯环上连有—NH
2
② 能与NaHCO 反应
3
(6)参照上述含成路线和信息,以乙醇为原料(无机试剂任选),设汁制备聚乳酸
的合成路线:__________________。参考答案
1.C 2.B 3.C 4.C 5.A 6.A 7.C 8.C 9.C 10.B 11.D 12.A 13.B 14.C
15.B 16.B 17.C 18.B 19.B 20.B 21.C 22.B23.C
24.(1)正
(2)b 2.16g
(3)AgNO(aq) 不变
3
(4)45.18
25.(1)80.3kJ/mol
(2) P>P >P 反应I和II都是气体分子数减少的反应,在相同温度下,增大压强,平
1 2 3
衡正向移动,乙炔转化率增大
(3)
(4) C HCl +6e−+3H+=C H+3Cl−
2 3 2 4
26. Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ΔH=+19.4kJ·mol-1 放热反应
1 浪费能量,且FeO易被还原成Fe Fe2+易被空气中的O2氧化成Fe3+ 4SO42-+
4Fe2++O2+2H2O=4Fe(OH)SO4↓ 温度升高,反应速率增大;温度过高,NO气体逸出,
转化率下降
27. f e d c 石灰石 饱和碳酸氢钠溶液 B 防止倒
吸 吸收多余的氨气 过滤 NaCl 取少量样品于试管中,用酒
精灯加热,看到试管上端有白烟生成(或试管口有白色晶体),最后固体大部分消失、剩
余极少量的固体,从而证明所得固体的成分大部分是氯化铵
28. 3d5 > Mn原子核外失去2个电子后,其价电子排布式为3d5,
处于半充满的稳定状态,较难失去电子 D sp3 sp2 N>O
>C>H 7N 氧化镁晶体中所含离子的半径小,电荷数更大,晶格能更大,则熔点更
A
高 FeCu N
3
29. 对硝基甲苯 (或4-硝基甲苯或4-甲基硝基苯或对甲基硝基苯) 羟基、羧
基 加成反应 13 酯化反应(或取代
反应)
10